Method Article
心臓標的ペプチドの導入効率のインビボイメージング
要約
我々は、例として、例として、パラフィン埋め込み、切除、および共焦点蛍光顕微鏡を用いたex vivoイメージングシステムを利用した細胞透過ペプチドによる伝達の程度を評価するためのプロトコルを説明する。我々のプロトコルでは、単一の動物を使用して、同じ器官の両方のタイプのイメージング評価を取得し、それによって研究に必要な動物の数を半分に減らすことができる。
要約
細胞透過ペプチドとも呼ばれるタンパク質伝達ドメインの最初の記述以来、25年以上前に、診断および治療材料を提供するための新しいベクターとして、これらのペプチド、特に細胞特異的なペプチドの開発に強い関心がありました。ファージディスプレイを含む私たちの過去の研究は、静脈注射後わずか15分で見られるピーク取り込みで生体内で正常な心臓組織をトランスデューシングする能力のために、心臓ターゲティングペプチド(CTP)と命名した新しい、非自然発生する12アミノ酸長ペプチドを同定しました。我々は、フルオロフォアシアニン5.5で標識されたCTPを注入し、様々な期間循環させ、複数の臓器を安楽死させ、固定し、切除し、蛍光顕微鏡イメージングを行うことによって、詳細な生体分布試験を行った。本稿では、これらのプロセスと、in vivoイメージングシステムを用いた採取された臓器のex vivoイメージングについて詳しく説明する。CTPを例にしたバイオディストリビューション研究と同様に、トランスダクションを行うための詳細な方法論や実践を提供しています。
概要
細胞原形質膜は、細胞の完全性と生存に不可欠な半透過性バリアであり、細胞内への物質の移動を制御することによって細胞内部を調節するのに役立ちます。生存のために不可欠ですが、それはまた、細胞に貨物の配達に障壁を提示します。1988年、ヒト免疫不全ウイルスの転写(Tat)タンパク質のトランスアクチベーターは、培養細胞に入り、ウイルス遺伝子発現11,22を促進することが示され、この伝達を担うドメインはアルギニンおよびリジンが豊富な13アミノ酸領域に限定された3番目のヘリックス3の細胞貫通ペプチド(CPPs)と命名された。続いて、Tatペプチドが機能性β-ガラクトシダーゼを複数の細胞タイプ4に運ぶ能力を示す研究が行われた。最初の説明以来、細胞貫通ペプチドの数は劇的に増加しています。これらの伝達ドメインは、天然または合成短いペプチド、典型的には6〜20アミノ酸長であり、細胞膜を横切って機能性貨物を運ぶことができる。これらのカルゴは、他の小ペプチド、全長タンパク質、核酸、ナノ粒子、ウイルス粒子、蛍光分子、および放射性同位体5から及ぶ。記載された最初のCpPは細胞特異的ではなく、Tatは複数の細胞タイプによって取り込まれ、血液脳関門4を横断することさえ、その治療可能性を制限した。細胞特異的なCpPsを同定するために、研究者は、大規模な市販ファージライブラリ6を利用したファージディスプレイを実施している。インビニトロおよびインビボファージディスプレイ方法論を用いた当社独自の研究は、心臓標的ペプチド(CTP)7というCPPの同定につながり7、12アミノ酸、非天然のペプチド(NH2-APWHLSSQYSRT-COOH)を同定し、末梢静脈注射後15分でピーク取り込みを行う心臓を標的とする8.2細胞膜マーカーであるラミニンの活性とラミニンの排除を用いて、細胞膜マーカーであるアクチンとの免疫蛍光共局在化を用いて、CTPが静脈注射後にマウス心筋細胞に内在化することを示した7。さらに、細胞内エステラーゼによってしか切断できないエステルリンケージを介して、C末末に6カルボキシフルオレセインとN末流でロダミンで標識された二重標識CTPを有するヒト誘導多能性幹細胞由来の拍動筋細胞をインキュベートした。ロダミンの拍動心筋細胞への急速な蓄積は、共焦点顕微鏡8で15分以内に観察された。
この記事では、生体分布を追跡し、CTPを使用してCCPの組織固有の内部化を確認するために使用できる2つの無料の方法論を例に挙げます。これらの方法論では、CTPを合成し、N末語でシアニン5.5(CY5.5)で蛍光標識し、より大きなペプチド安定性を求めてC末語でアミドキャップを行った。使用される2つの方法論は、生体内蛍光光学イメージングシステムと組織切片の蛍光顕微鏡です。いずれの方法も、蛍光標識されたCpPの生体分布、取り込み、除去の研究に非常に役立ちます。単光子放出断層撮影(SPECT)や陽電子放出断層撮影(PET)など、これらの方法を用いて生体分布を評価する利点は、蛍光標識と比較して、CCPの時間のかかる放射標識が必要な点で、すべてのペプチド合成施設において比較的容易かつ日常的に使用できる点である。in vivoイメージングを使用すると、生体システムのコンテキストでバイオディストリビューションデータが迅速に生成され、断面化は形態学的詳細の保存を通じて細胞内のペプチド取り込みと局在化に関するより深い情報を提供します。このプロトコルは、心臓、肺、肝臓、腎臓、脳、脾臓、胃、大腸、小腸、骨格筋、骨、精巣/卵巣、および目などの臓器および組織の多種多様に適用することができます。
プロトコル
ピッツバーグ大学の制度的動物管理および使用委員会は、これらの動物実験のいずれかを行う前に、この出版物に指定されたすべての動物プロトコルを承認しました。
注:このプロトコルは、パラフィンに臓器を埋め込み、切除し、蛍光顕微鏡を行うことによって、エキビボ光蛍光イメージングを利用したex vivo生体分布研究を行う方法を詳述しています。CTPは一例として用いられているが、この方法は蛍光標識CPPに適用することができる。
1. インビボイメージング
- 固相合成技術99,10を用いて、安定性を高めるためCy5.5およびC末方アミドで標識されたN末語を有するL-アミノ酸を用いたペプチド合成施設からCTPを合成する。
注: 合成された全ての CpP は、11を使用する前に高速液体クロマトグラフィー (HPLC) および/またはマトリックスアシストレーザ脱離/イオン化 (MALDI) を使用して特徴付ける必要があります。 - ジメチルスルホキシド(DMSO)で1mMまたは10mMストックのCTPを、アリコート、-80°C、光保護で保存します。
注:ペプチドは凍結乾燥粉末として送達されます。凍結乾燥粉末は、-20°C、光保護、および吸湿条件下で長期(6ヶ月〜2年)保存することができます。DMSOで引用して保存する場合、フリーズ解凍サイクルは避けるべきです。 - ケタミン/キシラジン溶液の組織重量2μL/g(100mg/kgケタミンおよび20mg/kgキシラジン)を筋肉内(後ろ脚)または腹腔内投与(左下四肢)で6週齢のCD1雌マウスの体重を量り、麻酔する。
注: ケタミン/キシラジン溶液は、使用の日に新鮮にする必要があります..未使用のケタミン/キシラジンは、ケタミンが制御物質であるため、ログに記録されたボリュームと対に対して適切に処分する必要があります。十分なレベルの麻酔は、つま先ピンチへの応答の欠如によって評価されるように、5-7分で達成されます。 - Cy5.5-CTPの10mg/kg用量を計算し、リン酸緩衝生理食塩水(PBS)で200μL以下に希釈し、インスリン注射器を使用してレトロ軌道または尾静脈注射を通して注入する(図1A)。
- ペプチドを15分から6時間の範囲で、事前に指定された時間循環させる。
- 施設動物の世話と使用委員会で指定された高CO2吸入方法を使用してマウスを安楽死させ、はさみを使用して胸腔を開く(図1B)。
- 右心房の側面に小さなニックを配置し、マウスの器官を固定し、赤血球を洗い流す二重目的のために26G針を使用して10%緩衝ホルマリンリンの3mLを注入するために使用する(図1C)。
- 心臓、肺、肝臓、腎臓、脾臓、大腸、小腸、膀胱、卵巣/精巣、および脳を切除し、12ウェルプレートの個々のウェルに入れ、ex vivo光学画像撮影を行う(図1D)。
- イメージ取得ソフトウェアを起動し、[初期化]ボタンをクリックして、システムのイメージングサンプルを準備します。イメージングウィザードを開き、蛍光を選択してからフィルタペアを選択し、染料リストからCy5.5染料を選択して、580 nm励起フィルタと620 nm発光フィルタを適用します。露出パラメータの手動設定を選択してから、ステージ位置をBに設定し、露出時間を1秒に設定し、F/ストップを8に設定し、ビンを小さく設定します。
注: 励起エミッション フィルタは、使用するラベルによって異なります。使用されるラベルの励起および放出は、ソフトウェアに手動で入力して、励起フィルタと放出フィルタを割り当てることができます。飽和を避けるために、カウントが 600 から 60,000 の間であることを確認します。使用しているシステムによっては、自動取得の最適化が可能な場合があります。システムが、取得した画像を異なる設定で比較する補正を持っている場合は、自動設定を使用することができます。報酬がない場合、設定を決定し、保存し、サンプル間で一貫して使用する必要があります。 - システムが完全に初期化されたら、目的の器官を12ウェルプレートに配置し、それを光学イメージングチャンバーの内部に配置し、サンプルが画像に必要に応じて配置されていることを確認します。[取得]を選択し、画像の保存場所を選択します。マウスに関する情報は、画像ラベルの編集ポップアップウィンドウに書き込むことができます。
- イメージング後、チャンバーからサンプルを取り出し、室温での光保護(RT)を有するシンチレーションバイアル中の組織の体積の少なくとも20倍の体積に10%緩衝されたホルマリンリン酸を貯蔵する。
- 単位をラディアント効率に設定し、4x3 ROI を選択し、各ウェルを ROI の 1 つの正方形に均等に収まるように調整し、続いてクリックメジャーをクリックして、画像を定量化します。グリッド ROI 測定タブを開き、エクスポートを選択して、測定値を .cvs ファイルとして保存します。
2. ヒストロジー
注: 異なる臓器を得るためにステップ1.1-1.8に従ってください。あるいは、画像化された同じ器官をすぐにホルマリンに入れ、以下に詳述する断面化に使用することができる。
- 各臓器を10%緩衝されたホルマリンリンに10%ずつ保管してから、組織学用に処理する前に最低48時間保管します。
- 臓器が48時間後に十分に固定されている場合、臓器を組織処理に移し、カセットを埋め込み、組織処理機に入れる(図1E)。
- 処理機を70%エタノールで30分間脱水し、その後に80%エタノールを30分間、エタノールを30分間95%、エタノール95%で30分間、100%エタノールで15分間、100%エタノールを20分間、最後に100%エタノールを20分間設定します。
- キシレン2xで組織をクリアし、各キシレン処理に30分ずつします。
- クリアした組織を、各処理で30分間60°Cで4倍のパラフィンワックス4倍に浸潤する。
- 金属モールドを使用したパラフィンの埋め込み。溶融パラフィン(65°Cに保つ)で金型を充填し、冷たいプレートに移します。金型の底部のパラフィンが固まり始めると、臓器をパラフィンに入れる(図1F)。
- 標識されたカセットをモールドの上にバッキングとして置き、溶融パラフィンをオーバーフィルします。固体になるまで冷却します。次いで、ブロックを-20°Cの冷凍庫に一晩保管し、ワックスをさらに収縮させて金型から容易に取り外します。
注:ブロックは、ライト保護付きのRTで保存できるようになりました。 - 蒸留水で38°Cの水浴を準備します。6°の刃の角度および10 μmのセクションの厚さとのミクロトームを設定します。
- ミクロトームに組織ブロックを取り付け、組織を含む切片が得られるまで切断を開始します。その後、ブロックを水の中に5分間下に置くか、組織が水分を吸収するまで(例えば、組織の薄い白い輪郭がブロック[図1G]に現れる場合)
注: ブレードは、セクションの品質を確保するために頻繁に交換する必要があります。 - 組織を平らな氷のブロックに10分間置き、ステップ2.9と同じ方向にミクロトームに戻します。セクションを取り始め、切り捨てられたセクションがそれぞれ6-10セクションの長いリボンを形成できるようにします。滑り台を覆うのに十分な長さの良質リボンが作られるまで、最適以下のパラフィンリボンを捨てます。切断速度、組織保湿、水浴温度を調整して、組織切片のせん断やしわを避け、切削加工を最適化します。
注:組織が抜け落ちた穴、組織の裂け目、または組織のきついしわや折り目がある部分は廃棄する必要があります。 - 慎重に鈍いエッジ鉗子と選択の品質のリボンを選び、38 °C水浴の表面に浮かぶ。セクションが滑らかになるまで表面に座らせ、パラフィンが崩壊してセクションを引き裂くのを防ぐために長く放置しないように注意してください。
- 平らな部分をきれいなガラススライドの表面に浮かべる。スライドを65°Cのオーブンに30分間入れ、ワックスを溶かします。
注: これらのスライドは、光保護機能付きの RT に保存できます。 - 各処理に対して、キシレン3x、10分でスライドをデパラフィン化します。
- 組織を5分間100%エタノールで再水和し、続いて5分間95%エタノール、5分間エタノール70%、5分間50%エタノール、そして最後に5分間のトリス緩衝生理食塩水(TBS)を1xにして(図1H)。スライドを一晩乾燥させます。
注: これらのスライドは、ライトプロテクトである限り、RT で長期間保存できます。 - 4′,6-ジミジノ-2-フェニリンドール(DAPI)を含む実装媒体の125 μLを使用してカバースリップでスライドを取り付けます, 核蛍光プローブ (図 1I).ドライスライドはRTで一晩、光保護されています。
注:乾燥スライドは、光保護、4°Cで長期保存することができます。 - 蛍光顕微鏡を用いた画像スライド。
注: 飽和画像は定量的に有用ではないため、避けてください。露出とゲインの設定を調整すると、飽和を避けることができます。比較するサンプル間で同じ設定を使用するように注意してください。露出時間を制限することによって組織の漂白を避ける.
結果
このプロトコルを用いて、3匹のマウスを10mg/kgのCy5.5-CTPをレトロ軌道注入で治療した(図1A)。ペプチドを15分間循環させた後、マウスをCO2チャンバーを使用して安楽死させ、胸部を中立のステロトミー切開を通して開き、右心房をニックし、マウス灌流を10%リン酸緩衝ホルマリンの3mLを用いて固定した(図1B,C)。固定後、心臓、肺、肝臓、腎臓、脾臓、および脳を解剖し、12ウェルプレートに配置して、ex vivo光学蛍光イメージングを行う(図1DDおよび図2A)。注射を行っていない3つのコントロールマウスも、透過、解剖、画像化された(図1B-Dおよび図2B)。各器官のセットについて取得した蛍光データは、放射効率に変換されるカウント、イメージングソフトウェアの相対的な蛍光単位に起因して比較することができる。このデータを定量化して、問題の各臓器の定性的画像と定量データの両方を、生体分布研究の異なる時間ポイントにわたって生成することができます(図 2C)。異なる励起波長に応答して異なる器官の自己蛍光を図3A−Eで示す。高められた緑色蛍光タンパク質(EGFP)のような短い励起波長は、特に肝臓および脳において、遠赤色(Cy5.5)または近赤外(Cy7)励起波長よりも高い自己蛍光と関連している(図3)。画像化された器官は、最低48時間RTで10%リン酸緩衝ホルマリンに固定され、続いて組織処理および埋め込みカセットへの移入が行われた(図1E)。組織加工機で処理・パラフィンを行い、パラフィンを充填した型に配置し、-20°Cの段階で凍結し、−20°Cで一晩保存した(図1F)。サンプルを切り離し(図1G)、溶液交換で処理して組織を水分補給する(図1H)。次いで、準備したスライドをDAPI蛍光実装媒体と取り付けた(図1I)。一度乾燥すると、通常は一晩、スライドを蛍光顕微鏡を用いて画像化した。マウスからの各器官の代表的な画像を図4Aに示します。異なる器官からの画像は、マウス間の比較を可能にし、定量化を可能にするために同一の設定を使用して取得した(図4B)。
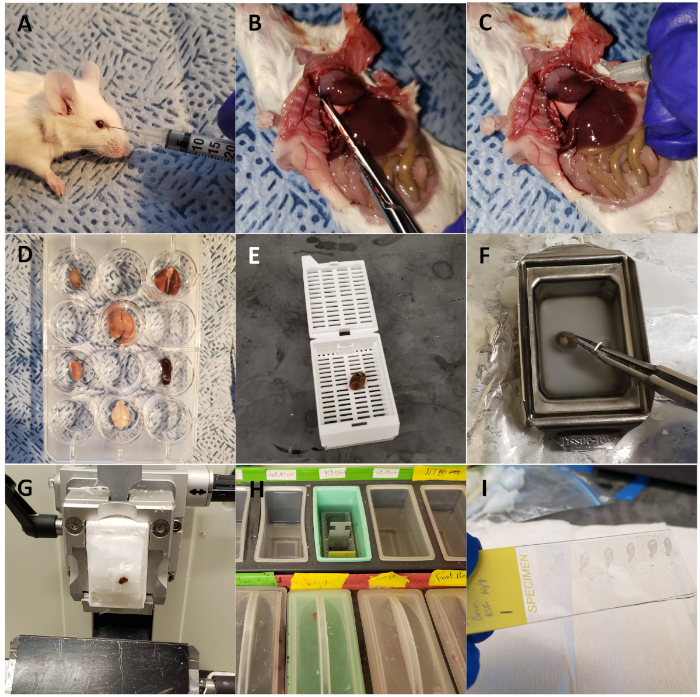
図1:エキビボ蛍光イメージングおよび切除用のマウス器官の採取(A)野生型マウスをCTP-Cy5.5でレトロ軌道に注入した。(B)マウスは、胸部を開いた状態で解剖し、右心房を切り取り、灌流固定を行う。(C)心臓は、動物の灌流固定のために10%緩衝型ホルマリンリン酸の3mLを注入した。(D) 目的の臓器を収穫し、蛍光光学イメージングのための12ウェルプレートに配置する。(E) 心臓をカセットに装填し、組織プロセッサを使用して処理する。(F)パラフィンに埋め込まれた心臓。(G) 心臓はミクロトームに切り離された。(H) 一連のソリューション交換を通じて脱パラフィン化されたスライド。(I) DAPI を使用してカバースリップでマウントされたセクション。この図の大きなバージョンを表示するには、ここをクリックしてください。
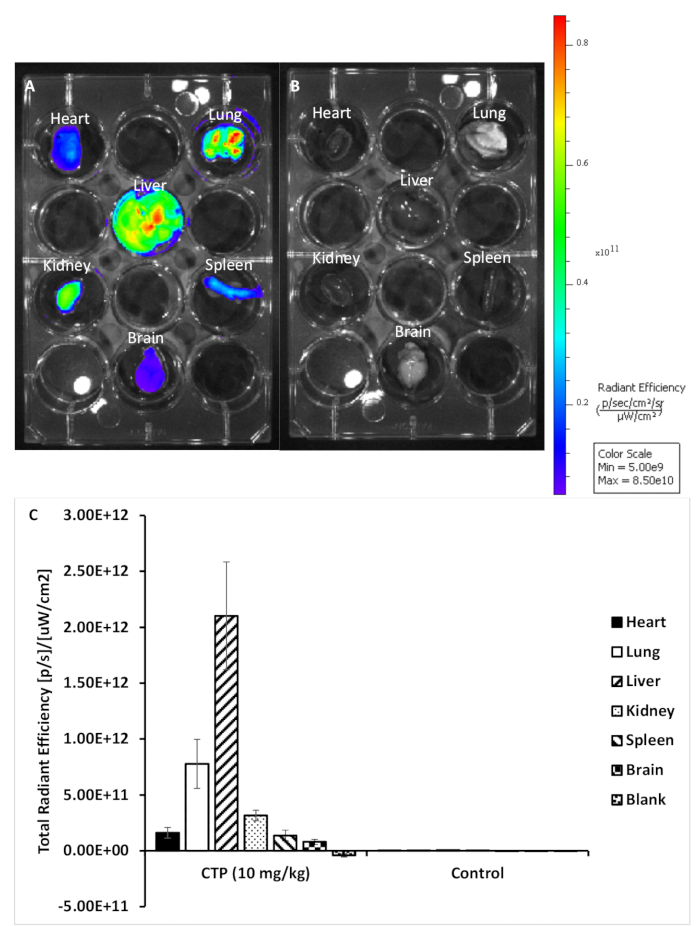
図2:治療および制御器官からの代表的な画像。(A) マウスから 10 mg/kg CTP-Cy5.5 で治療された器官。(B) 未治療のコントロールマウスからの臓器。(C)各器官の蛍光の定量化。この図の大きなバージョンを表示するには、ここをクリックしてください。
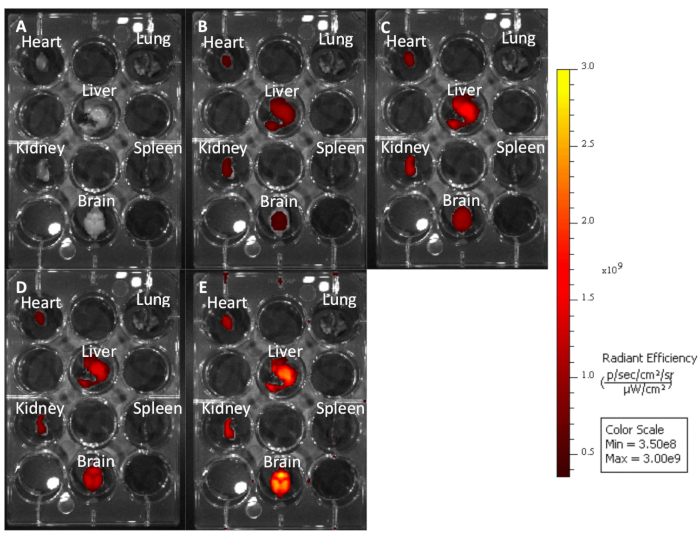
図3:異なる励起発光波長で画像化された未処理のマウス器官は、長い波長が自家蛍光を少なくする方法を示す。(A) Cy7: 740-790.(B) Cy5.5: 660-710.(C) Cy5: 620-670.(D) Cy3: 520-570.(E) EGFP: 480-520.この図の大きなバージョンを表示するには、ここをクリックしてください。
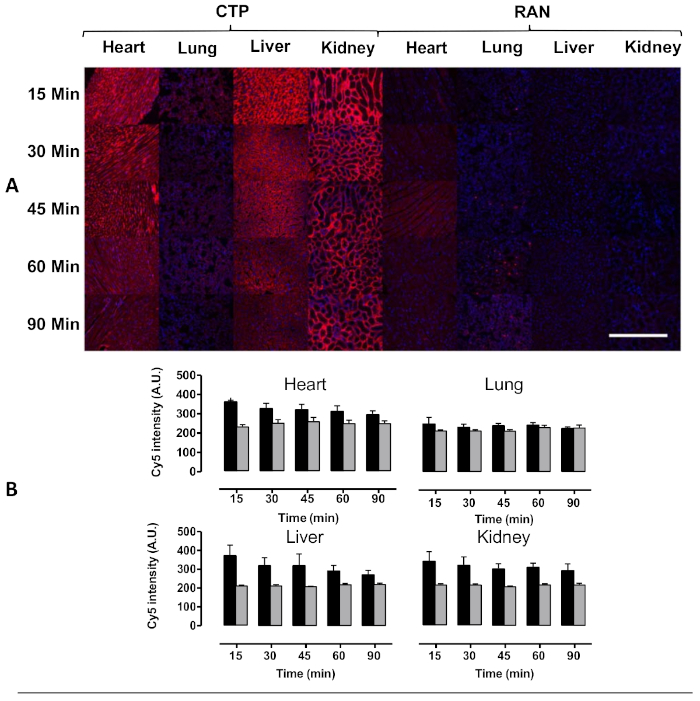
図4:マウスに静脈注射後の心臓、肺、肝臓、腎臓の導入。野生型マウスは、10mg/kgのCy5.5-CTP、またはランダムペプチド(RAN-Cy5.5)を注射し、指示された時点で安楽死させた。(A)心臓組織のピーク伝達は15分で見られ、時間の経過とともに蛍光が安定して減少した。いくつかの毛細血管取り込みは、肝臓だけでなく、腎臓糸球体毛細血管で堅牢な伝達を有する肺で注目された, 後者は排泄の腎機構を暗示.(B)蛍光強度の定量化は、RAN-Cy5.5に対するCTP-Cy5.5の心臓取り込み有意増加を示す。スケールバー= 500 μmこの図はZahidら8から変更されています。この図の大きなバージョンを表示するには、ここをクリックしてください。
ディスカッション
動物モデルは、新しいCCPの同定、生体分布研究、伝達のメカニズム、最終的にこれらの新しいCpPsをベクターとして使用して配達された貨物の有効性をテストすることまで、プロセスのあらゆる段階で前臨床薬の開発に不可欠です。生体分布の評価には、例えば、構造学、核医学イメージング(SPECTおよびPET)、生体内光学イメージング12など多くの一般的に使用される方法がある。核イメージング法は、小型動物SPECTおよびPETシステムの利用が限られているため、また、放射線化学者の専門知識を必要とする放射性標識薬物コンジュゲートを製造する能力のために面倒な場合があります。一方、蛍光標識は非常に簡単で、作業にコスト効率が良い場合があります。本稿で説明するプロトコルにより、複数の方法を用いたバイオ分布の迅速な分析が可能となる。Ex vivo全体臓器蛍光光学イメージングは、異なる組織および治療群間の蛍光の即時比較を可能にし、半定量的な方法で目的の器官の取り込みとピーク取り込みまでの時間を同定することができる。定量的組織組織組織学は、組織の治療、断面、画像化、分析のためにより広範な処理を必要としますが、顕微鏡レベルでより多くのデータを提供し、現在の標準的な技術です。異なる器官および励起波長の各技術で見られる自己蛍光は大きく異なるため、2つの技術間で直接定量的な比較は不可能であることに注意する価値があります。
このプロトコルの重要な部分は、実験のために候補CpPにラベルを付けるために適切な蛍光素を選択することです。潜在的な問題の1つはスペクトルの重複であり、複数のフルオロフォアが必要な場合に問題になる可能性があります。DAPI蛍光実装メディアとCy5.5には、スペクトルが重なっていません。しかし、複数のフルオロフォアが必要な特定の用途では、スペクトルオーバーラップのリスクを慎重に検討する必要があります。使用するシステムによっては、フルオロフォアの選択が制限される場合があります。したがって、システムの機能に関する知識が重要です。蛍光光学系は、短波長13の組織吸収が高いため、遠赤色または近赤外蛍光性蛍光性を用いて最もよく利用される。強化された緑色蛍光タンパク質の範囲の蛍光体は、その励起波長、特に脳および肝臓組織において見られる重要な臓器自己蛍光があるため、大きな制限を有する。実験の条件に応じて、いくつかの蛍光体は避けるのが最善です。一部の水溶性有機フルオロフォアは、脂質二重層と強い相互作用を有し、偽陽性を引き起こす可能性がある。したがって、対象となる組織に対して、フルオロフォアが強い親和性を有するかどうかを判断する措置を講じるのは、14.もう一つの考慮すべき要因は、結果に影響を与える重要なパラメータとなり得る蛍光呼び出しの適切な方法を選択することです。CCPは、ペプチドのN末語とCy5.5-NHSなどの色素のカルボキシル基との共有結合を介して、N末またはC末で蛍光的に標識することができる。ほとんどのCpPsの伝達メカニズムは詳細には理解されず、一方の端での結合は他方よりも取り込みメカニズムに影響を与える可能性があるため、注意が必要です。CpPsを標識するもう一つの可能性は、蛍光標識ストレプトアビジンへの結合のためのN末語をビオチン化することによってである。この戦略を用い、異なる蛍光ストレプトアビジンコンジュゲートを利用できる利便性があります。しかし,この戦略の可能な制限は、ビオチンストレプトアビジン複合体が大規模な構築物であり、転写を妨げる可能性があることである。
蛍光光学イメージングシステムは、異なる臓器や治療間で蛍光の比較を効率的に生成するための効果的な戦略ですが、組織中の絶対濃度の定量的尺度を生成することができません。これは、組織内の光散乱効果によるもので、組織のサイズと密度の自然発生する多様性によってさらに複合化され、血管の違い、蛍光散乱の変化が生じる。組織の自己蛍光は、コラーゲンなどの自然発生生化学的源、または食物13中のクロロフィルのような食物源に起因する要因にもなる。
組織学は、生体分布を測定する最も一般的に使用される方法であり、時間の経過とともに異なる組織間の取り込みの取り込み量を正確に測定し、比較するために使用される可能性があります。すべての組織が同じ厚さ15に切断されるため、この方法を使用して光散乱の問題が回避されます。この方法の主な利点は、免疫検査のための追加の蛍光標識の切除後を含む能力である。別の蛍光体を添加するとイメージングがより困難になる可能性がありますが、蛍光標識の使用は、リソソームやミトコンドリアのような特定の細胞内コンパートメントへのCPPの局在化に役立ちます。抗体は、共焦点顕微鏡実験で使用して、被写体CPP候補が目的の構造と共局化しているかどうかを判断し、CPPが送達物質としての可能性を示すことができるかどうかを判断することができます。この方法の1つの制限は、臓器サンプルからのスライドの調製は時間がかかり、労働集約的であり、人為的ミス12、15,15を起こしやすいということです。スライドをイメージングする場合は、フォトブリーチを避けるために、長すぎる間同じ場所をイメージしないように注意してください。蛍光色素の感度によっては、光の漂白が避けられない。このプロトコルの各段階で、サンプルを周囲光から保護し、適切に保存する16.将来のイメージングのために、光保護された4°Cにスライドを保存することをお勧めします。
特殊な機器を必要とし、より複雑なCPP標識を必要とする可能性がありますが、同等の結果を生み出すことができる候補CPPのバイオディストリビューションを測定するために利用可能な様々な方法があります。本稿で説明するプロトコルは、2つの互換性のある方法を用いて、生体システムの文脈で生体分布データを効率的に生成する一方で、同じサンプルから細胞内のペプチドの内在化に関するより深い情報を取得することができ、研究に必要な動物の数を半分に減らします。これらの方法は、上記のデータを生成するために使用され、両方の方法が同じ動物で順次利用できることを実証し、それぞれによって生成されたデータの品質を示した。我々の結果はまた、定量的な方法で2つの技術間の結果を直接相関させることができないことも強調している。
開示事項
M.Z.およびポール・D・ロビンズ(ミネソタ大学ミネソタ大学、ミネソタ大学、MN、米国)は、心臓ベクターとしての心臓標的ペプチドの使用に関する特許を取得しています(心臓特異的タンパク質標的ドメイン、米国特許シリアル番号9,249,184)。M.Z.はまた、最高科学責任者を務め、スタートアップのVivascセラピューティクス社の取締役会に加え、実質的な将来の株式を保有しています。
謝辞
M.Z.とK.S.F.は、米国心臓協会科学者育成賞17SDG33411180、ピットイノベーションチャレンジ(PInCh®®の下で授与された助成金によって、ピッツバーグ大学臨床トランスレーショナルサイエンス研究所を通じて支援されています。
資料
| Name | Company | Catalog Number | Comments |
| 10% Buffered Formalin Phosphate | ThermoFisher | SF100-4 | |
| 10x Tris Buffered Saline (TBS) | ThermoFisher | BP2471-1 | |
| 12-well Cell Culture Plate | ThermoFisher | 353043 | |
| 1x TBS Solution | 10x TBS is diluted 1:10 with deionized water. This solution can be stored at room temperature. | ||
| 20 mL Scintillation Vials | Wheaton | 334173 | |
| 26G Needles | Becton Dickinson | 305110 | |
| 28G 0.5ml Insulin syringes | Becton Dickinson | 329461 | |
| 3mL Syringe | Becton Dickinson | 309657 | |
| CD1 Mice | Charles River | 022 | 6 to 12 week old albino, female mice |
| Cover Glass | ThermoFisher | 12-544-14 | |
| Cy5.5-CTP-amide | Prepared by peptide synthesis, conjugated with Cy5.5 fluorophore, and purified using HPLC. Lyophilized powder is reconstituted in DMSO at 10mM concentration. After reconstituting, store at -80 °C. | ||
| Dapi Fluoromount G | SouthernBiotech | 0100-20 | |
| Dumont #5 Forceps | Fine Science Tools | 99150-20 | |
| Ethanol | |||
| Extra Fine Bonn Scissors | Fine Science Tools | 14084-08 | |
| Ketamine HCl 100mg/mL | KetaVed | NDC 50989-161-06 | |
| Ketamine/Xylazine Solution | Ketamine HCl is mixed with Xylazine 1:1 to produce a stock solution containing 50mg/mL ketamine and 10mg/mL Xylazine. This solution is made fresh before each use. | ||
| Leica RM2235 Rotary Microtome | Leica | RM2235 | |
| Microscope Slides | ThermoFisher | B9992000TN | |
| Paraplast X-TRA | Sigma | P3808-1KG | |
| Perkin Elmer Lumina S5 IVIS | Perkin Elmer | CLS148588 | |
| Sparkle Optical Lens Cleaner | ThermoFisher | NC0090079 | |
| Tissue-Tek Processing/Embedding Cassettes | ThermoFisher | NC9499605 | |
| Tissue-Tek VIP Processing machine | Tissue-Tek | VIP 5A-F1 | |
| Xylazine 20 mg/mL | AnaSed | NDC 59399-110-20 | |
| Xylenes | ThermoFisher | X5-4 |
参考文献
- Green, M., Loewenstein, P. M. Autonomous functional domains of chemically synthesized human immunodeficiency virus tat trans-activator protein. Cell. 55 (6), 1179-1188 (1988).
- Frankel, A. D., Pabo, C. O. Cellular uptake of the tat protein from human immunodeficiency virus. Cell. 55 (6), 1189-1193 (1988).
- Derossi, D., Joliot, A. H., Chassaing, G., Prochiantz, A. The third helix of the Antennapedia homeodomain translocates through biological membranes. Journal of Biological Chemistry. 269 (14), 10444-10450 (1994).
- Schwarze, S. R., Ho, A., Vocero-Akbani, A., Dowdy, S. F. In vivo protein transduction: delivery of a biologically active protein into the mouse. Science. 285 (5433), 1569-1572 (1999).
- Zahid, M., Robbins, P. D. Cell-type specific penetrating peptides: therapeutic promises and challenges. Molecules. 20 (7), 13055-13070 (2015).
- Zahid, M., Robbins, P. D. Identification and characterization of tissue-specific protein transduction domains using peptide phage display. Methods in Molecular Biology. 683, 277-289 (2011).
- Zahid, M., et al. Identification of a cardiac specific protein transduction domain by in vivo biopanning using a M13 phage peptide display library in mice. PLoS One. 5 (8), e12252 (2010).
- Zahid, M., et al. Cardiac Targeting Peptide, a Novel Cardiac Vector: Studies in Bio-Distribution, Imaging Application, and Mechanism of Transduction. Biomolecules. 8 (4), E147 (2018).
- Amblard, M., Fehrentz, J. A., Martinez, J., Subra, G. Methods and protocols of modern solid phase Peptide synthesis. Molecular Biotechnology. 33 (3), 239-254 (2006).
- Katritzky, A. R., Yoshioka, M., Narindoshvili, T., Chung, A., Johnson, J. V. Fluorescent labeling of peptides on solid phase. Organic and Biomolecular Chemistry. 6 (24), 4582-4586 (2008).
- Prabhala, B. K., Mirza, O., Hojrup, P., Hansen, P. R. Characterization of Synthetic Peptides by Mass Spectrometry. Methods in Molecular Biology. 1348, 77-82 (2015).
- Arms, L., et al. Advantages and Limitations of Current Techniques for Analyzing the Biodistribution of Nanoparticles. Frontiers in Pharmacology. 9, 802 (2018).
- Leblond, F., Davis, S. C., Valdes, P. A., Pogue, B. W. Pre-clinical whole-body fluorescence imaging: Review of instruments, methods and applications. Journal of Photochemistry and Photobiology. 98 (1), 77-94 (2010).
- Hughes, L. D., Rawle, R. J., Boxer, S. G. Choose your label wisely: water-soluble fluorophores often interact with lipid bilayers. PLoS One. 9 (2), e87649 (2014).
- McGowan, J. W., Bidwell, G. L. The Use of Ex Vivo Whole-organ Imaging and Quantitative Tissue Histology to Determine the Bio-distribution of Fluorescently Labeled Molecules. Journal of Visualized Experiments. (118), e54987 (2016).
- Waters, J. C. Accuracy and precision in quantitative fluorescence microscopy. Journal of Cell Biology. 185 (7), 1135-1148 (2009).
転載および許可
このJoVE論文のテキスト又は図を再利用するための許可を申請します
許可を申請さらに記事を探す
This article has been published
Video Coming Soon
Copyright © 2023 MyJoVE Corporation. All rights reserved