このコンテンツを視聴するには、JoVE 購読が必要です。 サインイン又は無料トライアルを申し込む。
Method Article
キラルレニウムポリヒドリド錯体における配位球転位特性評価のための動的NMRスペクトルの線形状解析
要約
さまざまな温度範囲で収集されたNMRスペクトルの線形状分析は、キラルな8配位のレニウム(V)ポリヒドリド錯体であるReH5(PPh3)2(sec-ブチルアミン)の内部配位球原子の再配列のガイドとして機能します。線形状解析は、これらの原子再配列の活性化パラメータΔH‡、ΔS‡、およびΔG‡を決定するためにも使用されます。
要約
動的溶液核磁気共鳴(NMR)分光法は、遷移金属ポリヒドリド錯体の配位球内の原子の動的再配列を特徴付ける典型的な方法です。ダイナミックNMRスペクトルのライン形状フィッティングは、ダイナミック転位プロセスの活性化パラメータの推定につながる可能性があります。金属結合リン原子の動的31P-{1H} NMR分光法とヒドリド配位子の動的1H-{31P} NMR分光法を組み合わせることで、リン原子の再配列と併せて発生するヒドリド配位子の再配列を特定できます。このような結合対の再配列を示す分子の場合、動的NMR分光法を使用して、リガンド再配列の理論モデルをテストできます。動的1H-{31P} NMR分光法とラインシェイプフィッティングは、不定水などの溶媒分子とのプロトン交換を介して、特定の水素化物配位子を金属の内部配位球を超えて移動させる交換プロセスの存在を特定することもできます。複数の動的転位プロセスを例示する新しい化合物ReH5(PPh3)2(sec-ブチルアミン)の調製を、錯体の動的NMRスペクトルのライン形状フィッティングとともに提示します。ライン形状の継ぎ手結果をアイリング方程式で解析して、特定された動的プロセスの活性化パラメータを推定できます。
概要
NMR分光法は、分子内または分子間で発生する動的プロセスを特徴付けるために一般的に使用されます。多くの単純な分子内転位の場合、ΔG‡ の推定は、遅い交換限界での2つの共振間の周波数差Δνを測定し、それらの同じ共鳴の合体温度を決定するのと同じくらい簡単です(図1)1。関係は、
ΔG‡ = 4.575 x 10-3 kcal/mol x T c [9.972 + log (Tc/Δν)]
ここでTcは 、動的試料の緩慢な交換形態を表す一対の共鳴に対する合体温度であり、そのような動的転位に対する活性化の自由エネルギーを解くために使用することができる。より複雑な動的システムでは、活性化パラメータを推定するために、動的NMRスペクトルのライン形状フィッティング、または2次元交換分光法(2D-EXSY)や2次元回転フレームオーバーハウザー効果分光法(2D-ROESY)などの別のNMR技術が必要です。
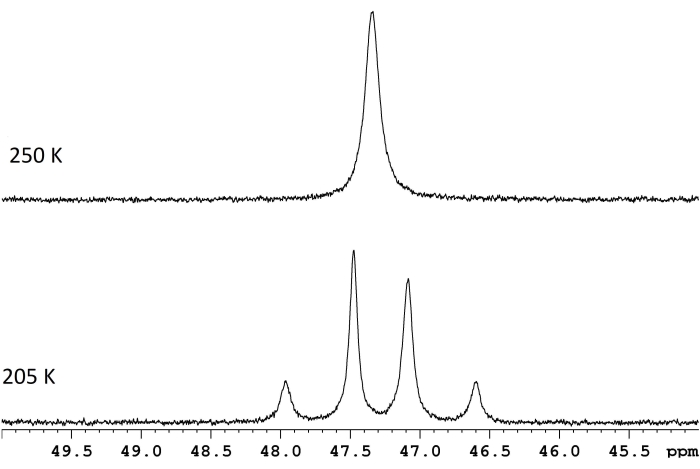
図1:ReH5(PPh3)2(sec-ブチルアミン)のd8-トルエン溶液の2つの温度でのNMRスペクトル。2つの緩慢交換ダブレット(下段トレース、117.8 Hz)と合体温度250 K(上トレース)の周波数差は、11.8 kcal/molのエネルギー障壁(ΔG‡)に相当します。 この図の拡大版を表示するには、ここをクリックしてください。
ダイナミックNMRスペクトルのラインシェイプフィッティングは、活性化エネルギーが約5〜25 kcal/mol 2,3,4,5の物質のダイナミック転位を記述する活性化パラメータの推定に長い間使用されてきた一般的な手法です。水とアミン分子6の間のプロトン交換に対するエネルギー障壁の決定、ジメチルホルムアミド7のC-N結合を中心とした回転に対するエネルギー障壁、または有機部分の一般的なサイズ8は、動的NMRスペクトルのライン形状フィッティングによって評価された多くの特性のほんの一例です。この原稿は、錯体ReH5(PPh3)2(sec-ブチルアミン)で発生する分子間および分子内の動的プロセスを特徴付けるために、ラインシェイプフィッティングの使用を示しています。このおよび類似のライン形状フィッティングNMR実験の目標は、1)NMRで観察可能な分子内動的原子交換プロセスが存在する場合は、そのすべてを特徴付ける、2)NMRで観察可能な分子内動的原子交換プロセスが存在する場合は同定および特徴付け、3)この例では水素原子とリン原子の両方について発生する相関分子内原子交換を同定し、4)ここに提示した例については、 錯体ReH5(PPh3)2(sec-ブチルアミン)で発生する動的プロセスについて、2つの公開モデルを比較します。
8配位レニウム(V)ポリヒドリド系は、配位子が複数の動的プロセスに関与し、リン原子がヒドリド配位子交換プロセスの第2の側面である単一の動的プロセスに参加できる複雑な動的システムです9,10,11,12,13,14,15,16,17,18 ,19,20,21,22,23,24,25,26,
27,28,29。8配位の擬十二面体レニウム(V)ポリヒドリド錯体は分子幾何学(図2)を採用しており、これは配位子の対交台形のペアとして説明できます17,26。台形の長辺の頂点は一般にBサイトとしてラベル付けされており、レニウムポリヒドリド錯体では、通常、3級ホスフィンやアミン配位子などの中性2電子供与体配位子が占める部位です。台形の短辺の頂点は、一般にAサイトとしてラベル付けされ、通常はアニオン性の2電子供与体であるヒドリド配位子によって占められています。レニウム(V)ポリヒドリド錯体の室温NMRスペクトルは、室温溶液中で起こるいくつかの動的プロセスのために、典型的には一見単純である。
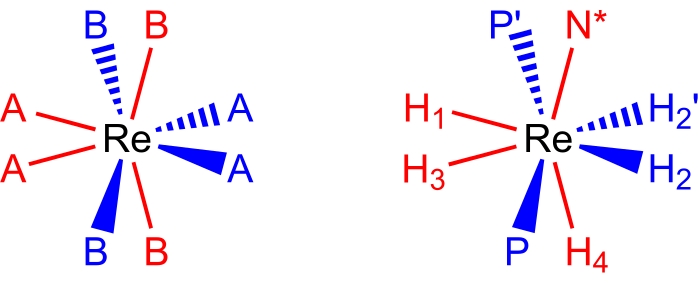
図2:同じ視点(右)からの十二面体配位集合(左)と錯体ReH5(PPh3)2(sec-ブチルアミン)。赤色のサイトは垂直台形を形成する配位サイトを表し、青色のサイトは水平台形を形成する配位サイトを表します。この図の拡大版を表示するには、ここをクリックしてください。
ReH5(PPh3)2(アミン)の形態の錯体は、動的プロセスに関して最も徹底的に研究されているレニウムポリヒドリド錯体のクラスである9,10,12,13,16,30,31。ReH5(PPh3)2(アミン)錯体については、3つの動的過程(図3)が同定されている:1)唯一のBサイト水素化物配位子と水分子からのプロトンとの間のプロトン交換(不定または意図的)9,13、2)一対のAサイト水素化物配位子と隣接するBサイト水素化物配位子9との回転木戸交換、11,13,30,31、および3)Aサイト水素化物配位子のペアワイズ交換およびBサイト原子のレニウム中心の反対側へのペアワイズ移動として現れる立体反転(または擬回転)4,5,6,8,26,27 .レニウムの反対側へのBサイト原子の移動は、動的NMR分光法によって次のように観察できます。 1)室温でN=ピリジンの非当量の3および5個のプロトンを当量にするプロセス10、30、31、 2)N=非対称に置換された芳香族アミン配位子のEおよびZ異性体を室温で高速交換させるプロセス9、 10、13、30、31、または3)アミン配位子9、30、31上に位置するキラル中心に関して、リン原子のジアステレオトピック対の立体的視点の高速交換を引き起こすプロセス。これまで報告されていないキラル錯体ReH5(PPh3)2(sec-ブチルアミン)は、レニウムポリヒドリド錯体の動的転位を同定および特徴付けるために使用できる方法を一般的に説明する機会を提供します。
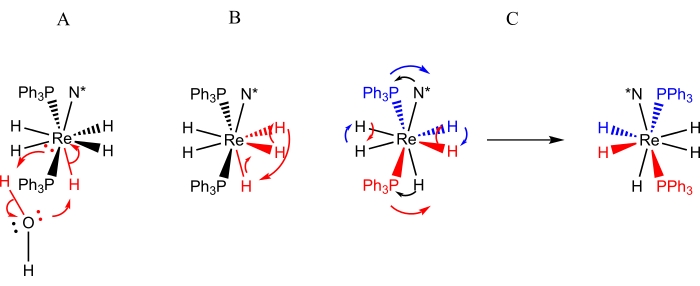
図3:ReH5(PPh3)2(sec-ブチルアミン)溶液のNMR分光法によって観察された動的プロセスの表現。 表現Aは、不定水の単一のプロトンと固有のBサイト水素化物配位子との交換を示しています。表現Bは、3つの隣接する水素化物配位子の改札口交換を示しており、そのうち2つはAサイトに存在し、3つ目は固有のBサイト水素化物配位子です。表現Cは、Aサイトの水素化物配位子のペアワイズ交換と、キラルアミン配位子(N*)に対するリン原子の立体反転の両方を示しています。なお、Aサイトと水素化物配位子の対交換は、Aサイト水素化物配位子をレニウム中心の反対側にシフトさせる必要がない。 この図の拡大版を表示するには、ここをクリックしてください。
レニウムポリヒドリド錯体などの化学系では、動的NMRスペクトルのライン形状フィッティングが、プロセスを特徴付けるために最もよく使用されるNMR技術です9、11、13、16、21、29。2次元EXSY 9,32または2D-ROESY11は、動的プロセスを定量的に特徴付けるためにも使用できる代替の動的NMR技術です。2次元EXSYスペクトルは、通常、低速交換温度領域で測定されます。2次元ROESYスペクトルは、通常、高速交換温度領域で測定されます。両方の2次元技術は、データ取得のために分光計においてかなりの時間を必要とし得るが、その技術のうちの各々は、ライン形状フィッティング解析に必要な1次元データセットよりもはるかに大きなデータセットを所与の温度で取得する。ジメチルホルムアミドの2つのメチル基の動的交換など、よく理解されている単純な動的プロセスは、3つのNMR技術のいずれかによって容易に特徴付けることができます。ReH5(PPh3)2(sec-ブチルアミン)のように、個々のヒドリド配位子が複数の動的プロセスに関与するより複雑な系や、ヒドリド配位子と不定水の間でプロトンを交換する場合と交換しない場合がある新規遷移金属ポリヒドリド錯体など、必ずしもよく理解されていない系は、2次元NMR法よりもライン形状フィッティングNMR法の方が定量的に特徴付けられやすい。 2次元NMR法とは異なり、ラインシェイプフィッティング法は、テストされたモデルと実験データとの間の一致の解釈可能な視覚化と、ヒドリド配位子をレニウムの内部配位圏を超えて移動させる交換の視覚的な証拠を提供します。遅い交換スペクトルのピーク高さとピーク形状に基づいて、ReH5(PPh3)2(sec-ブチルアミン)などの複雑な動的システムでさえ、交換モデルの初期セットを簡単にテストできます。さらに、分子変換に関する複数の理論モデルが報告されている場合、動的NMRスペクトルのライン形状フィッティングにより、各モデルと観測スペクトルを視覚的に比較することができます。
上記の3つのNMR技術を超えて、D2OまたはHDを含む同位体置換NMR実験は、複雑なレニウムポリヒドリド系の原子の分子間交換を定性的に実証するために使用されてきましたが、定量的特性評価には使用されていません9、33、34、35。理論計算は、複雑な動的システムの動的プロセスを特徴付けるための追加の方法を提示します30,31,36。理論計算は、線形状適合解析では区別できない可能性を区別できるという点で、線形状適合よりも優れています。例えば、理論計算は、特定のレニウム(V)錯体上の3つの隣接する水素化物配位子を含む交換を、固有の水素化物配位子および2つの化学的に等価な水素化物配位子のうちの1つを含む各対ワイズ交換との交互の対交換ではなく、3つの水素化物配位子すべてのターンスタイル交換として記述するために使用されてきた30、31。理論計算の結果は、通常、計算結果の妥当性をチェックするために、上記の3つのNMR手法のいずれかから実験的に観察された定量的特性と比較されます。
ダイナミックNMRスペクトルのライン形状フィッティングは、NMR測定中にNMR活性核が異なる化学環境間を移動するときに生じるNMRスペクトルの外観の変化を利用します。低速交換NMRスペクトル(交換核の各セットに対して独立したローレンツ共鳴を有するスペクトル)は、交換する原子核に対する共鳴間の周波数差が原子核の交換速度と比較して大きい温度で生じる37。高速交換NMRスペクトル(核を交換するための単一のローレンツ共鳴を有するスペクトル)は、原子核の交換速度が低速交換共鳴間の周波数差よりもはるかに大きい温度で起こる37。中間交換レートは、低速交換温度領域と高速交換温度領域37との間の温度に対して生じる。ラーム周波数、交換核の化学シフト、交換核の結合定数(もしあれば)、および各核タイプの相対集団の基本パラメータがわかっている場合、核間の推定交換の速度定数は、シミュレートされたスペクトルをいくつかの中間温度で観測されたスペクトルと比較することによって決定できます。複数の温度でのシミュレーションにうまく適合すると、温度と速度定数のデータが得られ、アイリング方程式とともに使用して、推定交換の活性化パラメータを推定できます。この方法の結果は、正確で再現性があることがわかっています。
プロトコル
1. サンプル調製
- ReH7(PPh3)235の調製
- 0.15 gの水素化ホウ素ナトリウムと0.41 gのReOCl 3(PPh 3)2を、ゴム製セプタムとガスポートを備えた2つ口または3つ口の100 mL丸底フラスコ、またはゴム製セプタムを取り付けた100 mLケルダールフラスコ(サイドアームガスポート付き)に入れます(補足図1)。
- 反応容器にスピンバーを追加します。
- ヒュームフード内で、ゴム製圧力チューブを使用して、反応容器のガスポートを真空および窒素ガス用のデュアルガラスマニホールドの活栓の1つに接続します。ガラス真空マニホールドをゴム圧力チューブ付きの真空ポンプに接続し、ガラス窒素マニホールドを調整された窒素ガスボンベに接続します。
- 窒素ガスマニホールドからの出口ガスを、ベントガスを2cmの鉱油カラムまたは2cmの水銀カラムに通すために使用できる活栓に接続します。
- 窒素ボンベの蛇口を開き、流れるガスの圧力を34ポンド/平方インチに調整します。水銀バブラーを通る窒素ガスの流れをベントします。
- ガラスマニホールドの活栓を調整して容器を真空マニホールドに接続することにより、反応容器内のガスを排気します。ガラスマニホールド活栓をガスマニホールドと反応容器に接続するように変えて、反応容器に窒素ガスを充填する。
- 手順1.1.5と1.1.6をさらに2回繰り返して、反応容器内の空気を窒素ガスで完全に置き換えます。フラスコとその内容物を氷浴で冷やす。
- シリンジ を介して 、8 mLの脱酸素水と8 mLの脱酸素テトラヒドロフランを反応容器内の固体に加えます。ガスベント活栓を切り替えて、ガスが鉱油バブラーを通過するようにします。懸濁液を氷浴中で15分間穏やかに撹拌する。最初の15分間の攪拌後に反応容器を氷浴から取り出す。
- 混合物をさらに45分間攪拌し続けるのを待ちます。反応が終了したときの指標として反応混合物の色に注意してください。黄褐色からオレンジ色の反応混合物の色(補足図1)は、反応が終点に達したことを示します。
- 反応混合物のオレンジ色から黄褐色になったら、30 mLの媒体焼結ガラス漏斗を通して混合物をろ過します。回収した固体を水、メタノール、エチルエーテルの15 mLずつで3回洗浄します。真空下で固体を乾燥させ、吸着した溶媒を除去します。
注:反応は通常、0.20gから0.25gの生成物を生成します。
- ReH5(PPh3)2(sec-ブチルアミン)の調製
- 0.070 gのReH7(PPh3)2 を計量し、スピンバーを含む50 mLのシングルネック丸底フラスコに移します。ガスポートを備えたコンデンサーにフラスコを取り付けます。ステップ1.1.3〜1.1.7のポンプアンドフィル法を使用して反応容器を脱酸素します。
- 容量8mLの脱酸素テトラヒドロフランをシリンジ を介して 反応容器に加え、丸底フラスコとコンデンサーの間の接合部を割る。同様の方法で、0.2 mLの 量のsec-ブチルアミンを追加します。ガスベント活栓を切り替えて、ガスベントが鉱油バブラーに通じるようにします。
- 反応混合物を65°Cで還流するまで加熱し、40に設定された可変AC変圧器に接続された加熱マントルを0〜140のスケールで40分間加熱します。フラスコの取り扱いが便利になる温度まで反応混合物を冷却する。
- 反応混合物を125 mL三角フラスコ内の25 mLのメタノールに注ぎます。混合物を5分間激しく攪拌する。5 mLの水を加えて、綿状の黄色の沈殿物の形成を誘発します。
- 焼結ガラス漏斗中で真空濾過することにより黄色沈殿物を集める。固体を15mLのメタノールで洗浄する。真空下で固体を乾燥させます。このプロセスの後、典型的な製品収量は0.035gです。
2. NMRスペクトルの取得と解析
- ダイナミックNMRスペクトルの測定
- 約0.8 mLのd 8-トルエン中に約8 mgの錯体ReH5(PPh3)2(sec-ブチルアミン)を加えてNMRサンプルを調製します。サンプルを機器に挿入します。
- [ ファイル ] タブをクリックし、表示される選択肢から [新規 ] を選択して、NMR 実験の作成に使用するダイアログ ボックスを開きます。
- 次の手順を実行して 、1H 実験を作成します。
- 新しい実験のフォルダー名を割り当てるには、一意のファイル名で [名前] 入力ボックスに入力します。[EXPNO] ボックスで、1 H 実験に 1などの実験番号を割り当てます。
- [PROCNO] ボックスで実験のプロセス番号 1 を割り当てます。DIR のドロップダウンリストを使用して、フォルダをディレクトリに割り当てます。機器がロックオンする溶媒をドロップダウンの[溶媒の選択]から特定します。
- 1H 実験のパラメーターを含むディレクトリを、実験ディレクトリのドロップダウン リストから選択します。ドロップダウンの [実験] リストの選択肢から Proton 実験を選択し、(オプション) [タイトルの入力] ボックスにデータのタイトルを追加します。
- コマンド ラインに Eda コマンドを入力し、必要に応じてパラメーターを調整して、以下の「ディスカッション」セクションの 2 番目の段落で説明する実験の説明を満たします。
- [ウィンドウ] タブをクリックし、リストから [新しいウィンドウ] を選択し、手順 2.1.3.1 から 2.1.3.8 を繰り返して、EXPNO 値 2 を使用して 1 H-{31P} 実験を準備し、以前に作成した 1H 実験と区別します。
- [ウィンドウ] タブをクリックし、リストから [新しいウィンドウ] を選択し、手順 2.1.3.1-2.1.3.8 を繰り返して、EXPNO 値 3 を使用して 31 P-{1 H} 実験を準備し、以前に作成した 1 H および 1 H-{31P} 実験と区別します (詳細なパラメーター情報については、補足表 1を参照してください)。
- コマンドラインに Lock コマンドを入力し、リストからd8-トルエンを選択します。[ OK ] をクリックして、溶媒の選択を受け入れます。可変核Xバンドプローブのため、必要に応じてコマンドラインに Atma コマンドを入力し、機器の 1Hおよび 31Pのラーム周波数での反射エネルギーを最小限に抑えます。
- コマンドラインに Ro コマンドを入力し、ボックスに値20を入力して、[ 回転の開始 ]ボタンをクリックします。コマンド ラインに Shim コマンドを入力します。シムルーチンのリストから Topshim などの適切なオートシムルーチンを選択し、「 開始 」ボタンをクリックします。
- コマンド ラインに Rga コマンドを入力します。 「自動受信機調整 」を選択し、「 OK」をクリックします。次に、コマンドラインの Go コマンドを使用して、各スペクトルに対して64スキャンを使用して、室温でサンプルの3つのスペクトルを測定します。
- 実験のデータをスペクトルに変換するには、コマンド ラインに入力する Efp コマンドを使用します。
- 次のコマンドを使用して、スペクトルの位相を調整します。
- [フェーズ]タブをクリックしてから、[フェーズの調整]タブをクリックします。フェーズツールバーの0ボタンの上にカーソルを置き、マウスの左ボタンを押したままにすると、0ボタンが緑色に変わります。
- マウスの左ボタンを押したまま、ベースラインがスペクトル全体で平らになり、すべての共鳴が吸光度(ピークがベースラインより上に上がる)として表示されるまで、マウスを前後に回転させます。
- 0 ボタンのみでベースラインを平坦にできない場合は、スペクトル ウィンドウ全体でベースラインが平坦になるまで、手順 2.1.10.1 および 2.1.10.2 の説明に従って 1 ボタンと 0 ボタンを調整します。
- フェーズ調整をデータとともに保存するには、フェーズツールバーの[ 保存して戻る ]ボタンをクリックします。
- 必要に応じて、スペクトルの信号対雑音比に基づいて各測定のスキャン回数を調整しますが、信号対雑音比は通常、信号が個々の共振に合体しないため、低温で減少します(図4)。
- ベンダーの指示に従って、温度制御用の分光計を準備します。冷却ガスの流量を200 L/h、プローブの目標温度を290 Kと入力します。分光器を目標温度で2分間安定させます。必要に応じて、冷却ガスの流量を210または220 L / hに上げて、温度を安定させます。
- ステップ 2.1.7 のように、サンプルを 290 K でシムします。ファイル名の末尾に温度を追加して、以前に測定した各スペクトルのファイル名を変更し(手順2.1.2および2.1.3.1)、290 Kで3つのスペクトルのセットを取得します。
- 次の温度で安定させるために必要に応じて、冷却ガスの流量を30 L / h≥増やし、目標温度を10 K下げます。 分光器を次の温度で2分間安定させてから、ステップ2.1.7のようにサンプルをシムします。3つのスペクトルのセットを測定します。
- 必要に応じて手順2.1.13と2.1.14を繰り返して、目的の最低温度までスペクトルを取得します。
注:サンプルの動的プロセスの活性化パラメータを決定するのに適したデータの完全なセットには、通常、200 Kの温度で十分です。 - サンプルを10 K刻みで室温に戻します。プローブのガラスライナーの損傷を防ぐために、サンプルを再度温める前に、各温度で2分間温度を安定させます。
- 測定スペクトルの線形状解析
- NMRプログラム内で、ウィンドウの左上にあるコマンドバーをクリックし、ドロップダウンメニューから[ 開く ]を選択します。[ 標準形式で保存されたNMRデータを開く]を選択します。[ OK ]をクリックして、プログラムのファイルエクスプローラーウィンドウを開きます。
- 線の形状継ぎ手によって解析するデータのフォルダーに移動します。解析するスペクトルに対応するファイル番号を選択し、[ 表示 ]ボタンをクリックします。スペクトル(以前に処理されている場合)または自由誘導減衰(FID)曲線がNMRソフトウェアに表示されます。
- 必要に応じて、コマンド ラインに Efp コマンド (指数乗算、フーリエ変換、位相補正) を入力して、FID を処理します。スペクトルの位相を調整します(ステップ2.1.10)。
- スペクトルのベースラインを調整します。スペクトル全体で平坦でない場合は、次のように0強度の線で水平にします。
- [ プロセス ] タブをクリックし、[ ベースライン] タブをクリックします。 カーソルを [A ] ボタンの上に置きます。マウスの左ボタンを押し、マウスを前後に回して、スペクトルの左(下フィールド)の端で赤い調整線を水平にします。
- それでもベースラインが赤い調整線と同じ高さでない場合は、赤い調整線がスペクトルのベースラインに収まるまで、残りの文字ボタンでこのプロセスを繰り返します。 保存して戻る ボタンを使用して、赤で調整されたベースラインが実際のベースラインと一致したときに調整を保存します。
- NMRソフトウェア内の [解析 ]タブを選択します。解析オプション内で、[ 線の形状 ]を選択してから、[ ダイナミックNMRモデルをフィット ]を選択します。
- スペクトルが線形状継ぎ手モジュールウィンドウに表示されます。スペクトルの上にあるツールバーを使用して、スペクトルの表示方法を調整します。スペクトルの左側のウィンドウは、スペクトルの線形状のフィットを処理します。
- スムーズズームツールを使用してスペクトル表示を調整し、フィットするスペクトルの部分がスペクトルウィンドウに表示されるようにします。スペクトルを左右にシフトツールバーボタンを使用して、スペクトルの一部を表示ウィンドウの中央に配置します。
- 線形状継ぎ手ウィンドウの「 スペクトル」(Spectrum ) タブを選択して、線形状継ぎ手のケミカルシフトウィンドウにアクセスします。
- [ 範囲の編集 ]ボタンをクリックします。線形状継ぎ手の上下の化学シフトを入力し、[ OK ]ボタンをクリックしてこれらの制限を受け入れます。
- 線形状継ぎ手ウィンドウの 「スピンシステム」(Spin System ) タブをクリックして、線形状継ぎ手のモデルを開始します。 [追加 ]ボタンをクリックして、モデルスピンシステムの構築を可能にします。
- LB(線幅の広がり)の選択を解除し、マウスと線の形状継ぎ手ツールバーのLBボタンを使用して、手動で線幅の広い値を入力します。
- 最初の核をモデルに追加するには、[ 核 ]タブをクリックし、次に[ 追加 ]ボタンをクリックします。Nucleus 1 に一連のデフォルト値が表示されます。Nu (iso) ボックスに化学シフトの値を入力するか、線の形状継ぎ手ツールバーの化学シフトツールを使用して、Nucleus 1 の 化学シフト を調整します。
注:選択ボックスがチェックされたフォームのままの場合、この核の化学シフトは、最適な適合を達成するために変化します。チェックされていない変数は、ラインフィッティングプロセスで変更されません。 - 核 1 の [擬似 スピン] ボックスを使用して、各スピン 1/2 原子核が 0.5 に相当する原子核の数を入力します。すべての等価原子核を説明するために、スピンの合計を 擬似スピン ボックスに入力します。
- [ In Molecule ] ボックスを使用して、動的プロセスに参加するために複数の分子を必要とするモデルに対応します。異なる分子から生じる共鳴を、異なる分子の1、2などの指定を使用して別々の分子に割り当てます。単一の分子から生じる共鳴の場合、すべての 分子内 値に1を割り当てます。
- 2番目以降のすべての核をモデルに追加するには、[ 核 ]タブをクリックし、次に [追加 ]ボタンをクリックします。適切な JN ボックス(Nは追加される原子核が結合される核、N = 1、2、...)に結合を入力するか、線の形状継ぎ手ツールバーの スカラー 結合ボタンを調整して、原子核間のスピン-スピン結合を含めます。
- 原子交換を記述するプロセスを開始するには、[ 反応 ]タブをクリックします。交換のレート定数をライン形状継ぎ手で変更する場合は、 チェックボックス をクリックします。交換する原子核の数(核 1 や原子核 2 などの識別タブに対する数)を、モデル内の最初の交換の 交換 ボックスに入力します。
- [取引所]ボックスの下のボックスにテストする 取引所 を説明してください。 下のボックスで Nucleus タブ間の交換を定義します。2つの原子核交換は、原子核1から原子核2、原子核2から原子核1として入力されます。核が原子核1から移動した場合、別の原子核を原子核1に移動させる必要があるという点で、交換が周期的であることを確認してください。
- 速度定数のチェックボックスがオンの場合でも、kの値を反復調整するために、ラインシェイプ継ぎ手ツールバーの[ 速度交換 ]ボタンを使用してkの初期値を変更します。
- モデルに交換を追加するには、[ 反応 ]タブをクリックし、[ 追加 ]ボタンをクリックします。必要に応じて、モデルに交換を追加します。ラインシェイプフィッティングツールバーのツールを使用して、スペクトル強度などの開始変数を、スペクトルが適合するように調整します。
- 線形状フィットツールバーのスペクトル フィットを開始 ボタンをクリックして、反復ラインシェイプフィットを開始します。スペクトルとモデル間の最適なオーバーラップに変化が見つからなくなるまで、または1000回の反復収束計算に達するまで、反復フィットを続けます。フィットが1000回の反復で停止する場合は、「 スペクトルフィットを開始」 ボタンを使用してさらに反復を続行します。モデルスペクトルは、比較のために実際のスペクトルとともに表示されます。
- 適切なタブから最適な値を記録します。線形状フィットウィンドウの スペクトル タブをクリックしてから、 保存 ボタンをクリックして、最適なスペクトルを保存します。
注意: 最適なスペクトルは、データの収集に使用したのと同じフォルダーに保存されます。ベストフィットスペクトルは、保存時に入力される異なる処理番号で保存することで、元のデータと区別されます。 - ライン形状継ぎ手に使用するモデルを保存するには、「 メイン」(Main ) タブをクリックし、「保存」(Save) ボタンをクリックします。モデルの名前を入力します。
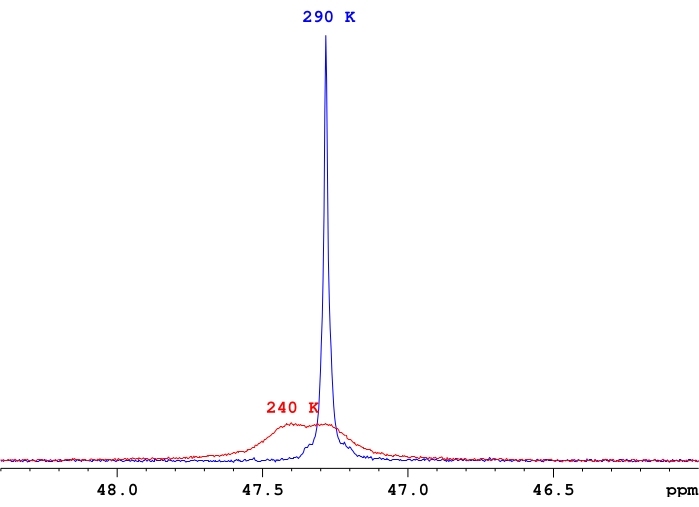
図4:d8-トルエン中のReH5(PPh3)2(sec-ブチルアミン)の単一サンプルに対する31P-{1H}シグナル強度の比較。 高速交換単一リン共鳴と、それらの共鳴の合体温度付近のリン共鳴のペアとの間の信号強度の違いの代表的なデモンストレーション。この図の拡大版を表示するには、ここをクリックしてください。
3. アイリングプロットからの活性化パラメータの決定 1
- モデル化された1つの動的プロセスの線形状フィットから、独立変数を1/T、従属変数をln(k/T)として入力したスプレッドシートにデータを入力します。
- データの散布図をスプレッドシートに挿入します。データに傾向線を追加します。トレンドラインの傾きと切片を使用して、ΔH‡とΔS‡を解きます。傾向線の傾きは-ΔH‡/Rで、傾向線の切片はΔS‡/R + 23.76です。
- 関係式を使用して、特定の温度でΔG‡ を解く
ΔG‡(T) = ΔH‡ - TΔS‡.
注:合体する共鳴を持つ2つの原子核の単純な交換の場合、合体温度で計算されたΔG‡と、共振と合体温度のゆっくりとした交換周波数差から生じるΔG‡の値を比較することにより、ΔH‡とΔS‡の値のチェックを行うことができます。
結果
この原稿に記載されている両方のレニウムポリヒドリド生成物の特性評価は、1 H-{31 P}および31P-{1H} NMR分光法によって最もよく達成されます。室温d6-ベンゼン溶液中では、ReH7(PPh3)2の水素化物配位子共鳴は、1 H NMR分光法により、2JPH = 18 Hzでδ = -4.2 ppmの二項三重項として現れます(補足図2)。?...
ディスカッション
ReH7(PPh3)2の調製には、生産される材料の量と純度に影響を与える可能性のある4つの項目があります。第一に、反応の最初の15分間の氷浴の使用は、水素化ホウ素ナトリウムと水の間で起こる反応から熱を除去するために重要である。初期温度が高くなると、熱分解生成物Re2H8(PPh3)4が形成されるため、ReH7(PPh3)2生?...
開示事項
著者は開示する利益相反を持っていません。
謝辞
著者らは、この研究の財政的支援について、モンマス大学の化学物理学部と創造性と研究助成プログラム(Naik、Moehring)に感謝しています。
資料
| Name | Company | Catalog Number | Comments |
| Bruker Avance II 400 MHz NMR spectrometer | Bruker Biospin | The instrument includes a two channel probe (1H and X) with the X channel tunable from 162 MHz to 10 Mhz. The instrument is also VT capable with a dewar and heat exchanger for VT work. | |
| d8-toluene | MilliporeSigma | 434388 | |
| Powerstat variable transformer | Powerstat | ||
| sec-butyl amine | MilliporeSigma | B89000 | |
| Sodium borohydride | MilliporeSigma | 452882 | |
| Tetrahydrofuran | MilliporeSigma | 186562 | |
| Thermowell C3AM 100 mL | Thermowell | ||
| Topspin 3.0 or 4.1.4 with dNMR | Bruker Biospin | Data was acquired with Topspin version 3.0 and data handling was performed on a second computer that was running Topspin version 4.1.4.. | |
| Trichlorooxobis(triphenylphosphine) rhenium(V) | MilliporeSigma | 370193 | |
| Vacuubrand PC3000 vacuum pump with a CVC 3000 controller | Vacuubrand |
参考文献
- Zimmer, K. D., Shoemaker, R., Ruminski, R. R. Synthesis and characterization of a fluxional Re(I) carbonyl complex fac-[Re(CO)3(dpop')Cl] with the nominally tri-dentate ligand dipyrido(2,3-α:3',2'-j)phenazine (dpop). Inorganica Chimica Acta. 359 (5), 1478-1484 (2006).
- McGlinchey, M. J. Symmetry breaking in NMR spectroscopy: the elucidation of hidden molecular rearrangement processes. Symmetry. 6 (3), 622-654 (2014).
- Casarini, D., Luazzi, L., Mazzanti, A. Recent advances in stereodynamics and conformational analysis by dynamic NMR and theoretical calculations. European Journal of Organic Chemistry. 2010 (11), 2035 (2010).
- Palmer, A. G., Williams, J., McDermott, A. Nuclear magnetic resonance studies of biopolymer dynamics. Journal of Physical Chemistry. 100 (31), 13293-13310 (1996).
- Kern, D., Kern, G., Scherer, G., Fischer, G., Drakenberg, T. Kinetic analysis of cyclophilin-catalyzed prolyl cis/trans isomerization by dynamic NMR spectroscopy. Biochemistry. 34 (41), 13594-13602 (1995).
- Menger, F. M., Lynn, J. L. Fast proton transfer at a micelle surface. Journal of the American Chemical Society. 97 (4), 948-949 (1975).
- Pines, A., Rabinovitz, M. A nuclear magnetic resonance total line-shape treatment of internal rotation in dimethylformamide. Tetrahedron Letters. 9 (31), 3529-3532 (1968).
- Mancinelli, M., Bencivenni, G., Pecorari, D., Mazzanti, A. Stereochemistry and recent applications of axially chiral organic molecules. European Journal of Organic Chemistry. 2020 (27), 4070-4086 (2020).
- Streisel, D. J., et al. Fluxionality, substitution, and hydrogen exchange at eight-coordinate rhenium(V) polyhydride centers. Inorganica Chimica Acta. 496 (1), 119028 (2019).
- Jimenez, Y., Strepka, A. M., Borgohain, M. D., Hinojosa, P. A., Moehring, G. A. Ortho-metalation, rotational isomerization, and hydride-hydride coupling at rhenium(V) polyhydride complexes stabilized by aromatic amine ligands. Inorganica Chimica Acta. 362 (9), 3259-3266 (2009).
- Lee, J. C., Yao, W., Crabtree, R. H., Ruegger, H. Fluxionality in [ReH5(PPh3)2(pyridine)]. Inorganic Chemistry. 35 (3), 695-699 (1996).
- Patel, B. P., Kavallieratos, K., Crabtree, R. H. Effects of dihydrogen bonding on fluxionality in ReH5(PPh3)2L. Journal of Organometallic Chemistry. 528 (1), 205-207 (1997).
- Geetha, B., et al. Chiral amine ligands at rhenium(V) pentahydride complexes allow for characterization of an energetically accessible and reversible steric inversion of diastereotopic phosphorus atoms. Inorganica Chimica Acta. 531 (1), 120741 (2022).
- Paulo, A., Ascenso, J., Domingos, A., Galvao, A., Santos, I. Rhenium-(III) and -(V) hydride complexes with modified poly(pyrazolyl)borates. Journal of the Chemical Society, Dalton Transactions. 1999 (8), 1293-1300 (1999).
- Bianchini, C., et al. Synthesis and characterization of rhenium polyhydrides stabilized by the tripodal ligand MeC(CH2PPh2)3. Journal of Organometallic Chemistry. 451 (1), 97-106 (1993).
- Scorzelli, A. G., Macalush, B. E., Naik, D. V., Moehring, G. A. Comparative study of fluxional processes at two different classes of eight-coordinate rhenium(V) polyhydride complexes. Inorganica Chimica Acta. 516 (1), 120120 (2021).
- Luo, X. -. L., Crabtree, R. H. Synthesis and spectroscopic characterization of rhenium complexes ReH5(triphos)] and [ReH6(triphos)]+ [triphos = PPh(CH2CH2PPh2)2]. Journal of the Chemical Society. 1991 (5), 587-590 (1991).
- Kim, Y., Deng, H., Gallucci, J. C., Wojcicki, A. Rhenium polyhydride complexes containing PhP(CH2CH2CH2PCy2)2 (Cyttp): protonation, insertion, and ligand substitution reactions of ReH5(Cyttp) and structural characterization of ReH5(Cyttp) and [ReH4(η2-H2)(Cyttp)]SbF6. Inorganic Chemistry. 35 (24), 7166-7173 (1996).
- Bolano, S., et al. Synthesis, characterization, protonation studies and X-ray crystal structure of ReH5(PPh3)2(PTA) (PTA = 1,3,5-triaza-7-phosphaadamantane). Journal of Organometallic Chemistry. 691 (4), 629-637 (2006).
- Ginsberg, A. P., Abrahams, S. C., Jamieson, P. B. Nonrigid stereochemistry in eight-coordinate pentahydridorhenium complexes. Journal of the American Chemical Society. 95 (14), 4751-4752 (1973).
- Bolano, S., Bravo, J., Garcia-Fontan, S. Mono- and dinuclear rhenium polyhydride complexes bearing the chelating ligand 1,2-bis(dicyclohexylphosphinanyloxy)ethane. European Journal of Inorganic Chemistry. 2004 (24), 4812-4819 (2004).
- Leeaphon, M., Rohl, K., Thomas, R. J., Fanwick, P. E., Walton, R. A. Reactions of the polyhydride complex ReH7(PPh3)2 with quinoline, 2-hydroxyquinoline, and 2-mercaptoquinoline. The preparation and characterization of hydrido complexes of rhenium(V) and chloro complexes of rhenium(III). Inorganic Chemistry. 32 (24), 5562-5568 (1993).
- Mejia, E., Togni, A. Rhenium complexes containing the chiral tridentate ferrocenyl ligand pigiphos. Organometallics. 30 (17), 4765-4770 (2011).
- Moehring, G. A., Walton, R. A. Reactions of heptahydrobis(triphenylphosphine)rhenium with bidentate aromatic heterocycles. Inorganic Chemistry. 26 (17), 2910-2912 (1987).
- Kosanovich, A. J., Reibenspies, J. H., Ozerov, A. V. Complexes of high-valent rhenium supported by the PCP pincer. Organometallics. 35 (4), 513-519 (2016).
- Emge, T. J., Koetzle, T. F., Bruno, J. W., Caulton, K. G. Pentahydridorhenium: crystal and molecular structure of ReH5(PMePh2)3. Inorganic Chemistry. 23 (24), 4012-4017 (1984).
- Costello, M. T., Fanwick, P. E., Green, M. A., Walton, R. A. Reactions of Heptahydridobis(triphenylphosphine)rhenium with 1-(diphenylphosphino)-2-(diphenylarsino)ethane (arphos) and 1,2-bis(diphenylarsino)ethane (dpae). Structural characterization of ReH5(PPh3)2(arphos-As) and ReH5(PPh3)2(dpae-As). Inorganic Chemistry. 30 (4), 861-864 (1991).
- Alvarez, D., Lundquist, E. G., Ziller, J. W., Evans, W. J., Caulton, K. G. Synthesis, structure and applications of transition-metal polyhydride anions. Journal of the American Chemical Society. 111 (22), 8392-8398 (1989).
- Albinati, A., et al. Synthesis, characterization, and interconversion of the rhenium polyhydrides ReH3(η4-NP3)] and [ReH4(η4-NP3)]+ {NP3 = tris[2-(diphenylphosphanyl)ethyl]amine}. European Journal of Inorganic Chemistry. 2002 (6), 1530-1539 (2002).
- Bosque, R., et al. Site preference energetics, fluxionality, and intramolecular M−H···H−N hydrogen bonding in a dodecahedral transition metal polyhydride. Inorganic Chemistry. 36 (24), 5505-5511 (1997).
- Tao, Y., Sou, W., Luo, G. -. G., Kraka, E. Describing polytopal rearrangement processes of octacoordinate structures. I. renewed insights into fluxionality of the rhenium polyhydride complex ReH5(PPh3)2(Pyridine). Inorganic Chemistry. 60 (4), 2492-2502 (2021).
- Beringhelli, T., D'Alfonso, G., Minoja, A. P. Rhenium-platinum mixed metal clusters. Characterization in solution and dynamic behavior of the isomers of [Re3Pt(µ-H3)(CO)14]. An example of a labile metal fragment that undergoes intermolecular exchange. Organometallics. 13 (2), 663-668 (1994).
- Grieco, G., Blacque, O. Solution and solid-state structure of the first NHC-substituted rhenium heptahydrides. European Journal of Inorganic Chemistry. 2019 (34), 3810-3819 (2019).
- Wazio, J. A., Jimenez, V., Soparawalla, S., John, S., Moehring, G. A. Hydrogen exchange of rhenium(VII) heptahydridobis(triphenylphosphine) with water, aniline, methanol, and itself. Inorganica Chimica Acta. 362 (1), 159-165 (2009).
- Chatt, J., Coffey, R. S. Hydrido-complexes of rhenium-containing tertiary phosphines. Journal of the Chemical Society, A. 1969, 1963-1972 (1969).
- Tao, Y., Wang, X., Zou, W., Luo, G. -. G., Kraka, E. Unusual intramolecular motion of ReH92- in K2ReH9 crystal: circle dance and three-arm turnstile mechanisms revealed by computational study. Inorganic Chemistry. 61 (2), 1041-1050 (2022).
- Berger, X., Braun, S. . 200 and More NMR Experiments a Practical Course. , (2004).
- He, G., Chen, J., Sung, H. H. -. Y., Williams, I. D., Jia, G. Substituent effect on reactions of ReH5(PMe2Ph)3 with propargyl alcohols. Inorganica Chimica Acta. 518 (1), 120239 (2021).
- Donnelly, L. J., Parsons, S., Morrison, C. A., Thomas, S. P., Love, J. B. Synthesis and structures of anionic rhenium polyhydride complexes of boron-hydride ligands and their application in catalysis. Chemical Science. 11 (9), 9994-9999 (2020).
- Donnelly, L. J., et al. C-H borylation catalysis of heteroaromatics by a rhenium boryl polyhydride. ACS Catalysis. 11 (12), 7394-7400 (2021).
- Jin, H., et al. CO-enabled rhenium hydride catalyst for directed C(sp2)-H bond alkylation with olefins. Organic Chemistry Frontiers. 2 (4), 378-382 (2015).
- Takaya, H., Ito, M., Murahashi, S. -. I. Rhenium-catalyzed addition of carbonyl compounds to the carbon−nitrogen triple bonds of nitriles: α-C−H activation of carbonyl compounds. Journal of the American Chemical Society. 131 (31), 10824-10825 (2009).
- Carr, S. W., Fowles, E. H., Fontaine, X. L. R., Shaw, B. L. Multihydride complexes of rhenium, osmium or iridium containing monodentate ditertiary phosphine ligands: selective hydrogen-deuterium exchanges of the rhenium multihydrides. Journal of the Chemical Society, Dalton Transactions. 1990 (2), 573-579 (1990).
- Jin, H., et al. Rhenium-catalyzed acceptorless dehydrogenative coupling via dual activation of alcohols and carbonyl compounds. ACS Catalysis. 3 (10), 2195-2198 (2013).
- Loza, M. L., de Gala, S., Crabtree, R. H. Steric crowding in a rhenium polyhydride induced by a chelating disilyl ligand: synthesis, characterization, and reactivity of ReH5(disil)(PPh3)2 (disil = 1,2-Bis(dimethylsilyl)benzene and 1,2-Bis(dimethylsilyl)ethane). Inorganic Chemistry. 33 (22), 5073-5078 (1994).
- Lin, Y., Zhu, X., Xiang, M. Transition metal polyhydrides-catalyzed addition of activated nitriles to aldehydes and ketones via Knoevenagel condensation. Journal of Organometallic Chemistry. 448 (1-2), 215-218 (1993).
- Abdukader, A., Jin, H., Cheng, Y., Zhu, C. Rhenium-catalyzed amination of alcohols by hydrogen transfer process. Tetrahedron Letters. 55 (30), 4172-4174 (2014).
- Lin, Y., Zhou, Y. Selective transfer hydrogenation catalyzed by transition metal polyhydrides. Fenzi Cuihua. 5 (2), 119-124 (1991).
- Green, M. A., Huffman, J. C., Caulton, K. G., Rybak, W. K., Ziolkowski, J. J. Ligand scavenging and catalytic utilization of the phototransient ReH5(PMe2Ph)2. Journal of Organometallic Chemistry. 218 (2), 39-43 (1981).
- Komiya, S., Chigira, T., Suzuki, T., Hirano, M. Polymerization of alkyl methacrylate catalyzed by hydridorhenium complexes. Chemistry Letters. 4 (4), 347-348 (1999).
- Michos, D., Luo, X. L., Faller, J. W., Crabtree, R. H. Tungsten(VI) hexahydride complexes supported by chelating triphosphine ligands: protonation to give η2-dihydrogen complexes and catalytic dehydrogenation of cyclooctane to cyclooctene. Inorganic Chemistry. 32 (8), 1370-1375 (1993).
転載および許可
このJoVE論文のテキスト又は図を再利用するための許可を申請します
許可を申請さらに記事を探す
This article has been published
Video Coming Soon
Copyright © 2023 MyJoVE Corporation. All rights reserved