É necessária uma assinatura da JoVE para visualizar este conteúdo. Faça login ou comece sua avaliação gratuita.
Method Article
Imagem Química Hiperespectral Não Linear Multimodal Usando Microscopia de Geração de Soma e Frequência Vibracional de Varredura de Linha
Neste Artigo
Resumo
Uma estrutura de imagem hiperespectral rápida e multimodal foi desenvolvida para obter imagens de geração de soma e frequência vibracional de banda larga (VSFG), juntamente com modalidades de imagem de segunda geração harmônica (SHG) de campo claro. Devido à frequência do infravermelho ser ressonante com vibrações moleculares, o conhecimento microscópico estrutural e morfológico mesoscópico é revelado de amostras permitidas por simetria.
Resumo
A geração de soma de frequência vibracional (VSFG), um sinal óptico não-linear de segunda ordem, tem sido tradicionalmente usada para estudar moléculas em interfaces como uma técnica de espectroscopia com uma resolução espacial de ~100 μm. No entanto, a espectroscopia não é sensível à heterogeneidade de uma amostra. Para estudar amostras mesoscopicamente heterogêneas, nós, juntamente com outros, empurramos o limite de resolução da espectroscopia VSFG para o nível de ~1 μm e construímos o microscópio VSFG. Esta técnica de imagem não só pode resolver morfologias de amostras através de imagens, mas também gravar um espectro VSFG de banda larga em cada pixel das imagens. Por ser uma técnica óptica não linear de segunda ordem, sua regra de seleção permite a visualização de estruturas automontadas não centrossimétricas ou quirais comumente encontradas em biologia, ciência dos materiais, bioengenharia, entre outras. Neste artigo, o público será guiado por um projeto de transmissão invertida que permite a obtenção de imagens de amostras não fixas. Este trabalho também mostra que a microscopia VSFG pode resolver informações geométricas químico-específicas de folhas auto-montadas individuais combinando-as com um solver de função de rede neural. Por fim, as imagens obtidas sob configurações de campo brilhante, SHG e VSFG de várias amostras discutem brevemente as informações únicas reveladas pelas imagens VSFG.
Introdução
A geração de soma de frequência vibracional (VSFG), uma técnica óptica não linear de segunda ordem1,2, tem sido usada extensivamente como uma ferramenta de espectroscopia para perfilar quimicamente amostras permitidas por simetria 3,4,5,6,7,8,9,10,11,12,13, 14,15,16,17,18,19,20,21,22. Tradicionalmente, os VSFG têm sido aplicados a sistemas interfaciais 8,9,10,11 (isto é, gás-líquido, líquido-líquido, gás-sólido, sólido-líquido), que não possuem simetria de inversão - um requisito para a atividade do VSFG. Esta aplicação do VSFG tem fornecido uma riqueza de detalhes moleculares de interfaces enterradas 12,13, configurações de moléculas de água em interfaces 14,15,16,17,18 e espécies químicas em interfaces 19,20,21,22.
Embora o VSFG tenha sido poderoso na determinação de espécies moleculares e configurações em interfaces, seu potencial na medição de estruturas moleculares de materiais sem centros de inversão não foi realizado. Isso ocorre em parte porque os materiais podem ser heterogêneos em seu ambiente químico, composições e arranjo geométrico, e um espectrômetro VSFG tradicional tem uma grande área de iluminação da ordem de 100 μm2. Assim, a espectroscopia VSFG tradicional relata informações médias da amostra sobre uma área de iluminação típica de 100 μm2. Essa média de conjunto pode levar a cancelamentos de sinal entre domínios bem ordenados com orientações opostas e descaracterização de heterogeneidades locais 15,20,23,24.
Com os avanços em alta abertura numérica (NA), objetivas de microscópio baseadas em reflexo (geometrias de Schwarzschild e Cassegrain), que são quase livres de aberrações cromáticas, o tamanho do foco dos dois feixes em experimentos VSFG pode ser reduzido de 100 μm 2 para 1-2 μm2 e, em alguns casos, submícron25. Incluindo esse avanço tecnológico, nosso grupo e outros desenvolveram o VSFG em uma plataforma de microscopia 20,23,26,27,28,29,30,31,32,33,34,35,36. Recentemente, implementamos um layout óptico invertido e um esquema de detecção de banda larga37, que permite uma coleção perfeita de imagens multimodais (VSFG, segunda geração harmônica (SHG) e óptica de campo brilhante). A imagem multimodalidade permite a inspeção rápida de amostras usando imagens ópticas, correlacionando vários tipos de imagens e localizando as posições do sinal nas imagens da amostra. Com a óptica de iluminação acromática e a escolha da fonte de iluminação a laser pulsada, esta plataforma óptica permite a integração perfeita futura de técnicas adicionais, como microscopia de fluorescência38 e microscopia Raman, entre outras.
Nesse novo arranjo, amostras como organizações hierárquicas e uma classe de automontagens moleculares (AMEs) têm sido estudadas. Esses materiais incluem colágeno e biomiméticos, onde tanto a composição química quanto a organização geométrica são importantes para a função final do material. Por ser um sinal óptico não-linear de segunda ordem, o VSFG é especificamente sensível a arranjos intermoleculares39,40, como distância intermolecular ou ângulos de torção, tornando-se uma ferramenta ideal para revelar tanto composições químicas quanto arranjos moleculares. Este trabalho descreve as modalidades VSFG, SHG e campo claro do instrumento central que consiste em um laser de estado sólido de cavidade dopada com itérbio que bombeia um amplificador paramétrico óptico (OPA), um microscópio invertido multimodal construído em casa e analisador de frequência monocromador acoplado a um detector bidimensional charged coupled device (CCD)27. Um passo a passo de construção e procedimentos de alinhamento, e uma lista completa de peças da configuração, são fornecidos. Uma análise aprofundada de uma MSA, cuja subunidade molecular fundamental é composta por uma molécula de sulfato de sódio-dodecil (SDS), um surfactante comum, e duas moléculas de β-ciclodextrina (β-CD), conhecidas como SDS@2 β-CD aqui, também são fornecidas como um exemplo para mostrar como o VSFG pode revelar detalhes geométricos específicos de moléculas de matéria organizada. Também foi demonstrado que detalhes geométricos químicos específicos da MSA podem ser determinados com uma abordagem de solucionador de funções de redes neurais.
Protocolo
1. Microscópio VSFG de varredura de linha hiperespectral
- Sistema laser
- Use um sistema de laser pulsado (ver Tabela de Materiais) centrado em 1025 nm ± 5 nm. O laser é regulado em 40 W, 200 kHz (200 μJ/pulso) com uma largura de pulso de ~290 fs.
NOTA: A taxa de repetição exata pode variar, e um laser de alta taxa de repetição geralmente funciona melhor para este microscópio VSFG. - Guie a saída do laser de semente em um amplificador paramétrico óptico comercial (OPA) para gerar um feixe de infravermelho médio (MIR) (veja Tabela de Materiais). Sintonize o MIR com a frequência de interesses (Figura 1A).
NOTA: No presente estudo, a MIR está centrada em 3450 nm ± 85 nm (~2900 ± 72 cm-1) com duração de pulso de ~290 fs e energia de pulso de ~6 μJ, que engloba parte da região -CHx grupo funcional.
- Use um sistema de laser pulsado (ver Tabela de Materiais) centrado em 1025 nm ± 5 nm. O laser é regulado em 40 W, 200 kHz (200 μJ/pulso) com uma largura de pulso de ~290 fs.
- Feixe de conversão ascendente
- Passe o feixe residual de 1025 nm do OPA através de um etalon de Fabry-Perot (ver Tabela de Materiais) para produzir um feixe de conversão ascendente espectralmente estreito com um FWHM de ~4,75 cm-1.
- Filtre espacialmente o feixe estreito de 1025 nm com um orifício de safira de 8 μm.
NOTA: O feixe de 1025 nm pode ser visualizado usando uma placa NIR. - Controle a polarização do pulso de 1025 nm com uma placa de onda λ/2 (ver Tabela de Materiais).
- Feixe MIR
- Guiar o feixe MIR através de um estágio de atraso para controle fino da sobreposição temporal.
- Controle a polarização do MIR com uma placa de onda λ/2.
- Microscópio VSFG
- Sobrepõem-se espacialmente os feixes de conversão ascendente e MIR em um espelho dicroico personalizado (DM, Figura 1B) que é transmissivo para MIR e reflexivo para NIR (veja Tabela de Materiais). Use duas íris para guiar o alinhamento: uma logo após o DM e outra na extremidade oposta. Use um medidor de energia após a íris para determinar se o MIR está centralizado e use uma placa NIR para localizar as posições NIR.
NOTA: Após a sobreposição, o feixe NIR pode ser usado para guiar ambos os feixes. - Direcione os feixes sobrepostos para um microscópio invertido com um scanner de feixe ressonante de eixo único integrado de 325 Hz (montado em um scanner integrado de duas posições (I2PS), Figura 1B) (consulte a Tabela de Materiais).
NOTA: O scanner ressonante projeta uma linha dos dois feixes sobrepostos na abertura traseira da objetiva do condensador. Ele é montado em um controle deslizante que permite a reconfiguração perfeita entre as modalidades VSFG/SHG e brightfield. - Focalize os dois feixes espacialmente sobrepostos na amostra com uma objetiva de Schwarzschild puramente reflexiva (SO, Figura 1B,D) (ver Tabela de Materiais).
- Coletar o sinal VSFG gerado pela amostra com uma objetiva refrativa corrigida infinitamente (RO, Figura 1B,D) (ver Tabela de Materiais).
- Guie o sinal VSFG de saída colimada através de um polarizador linear e, em seguida, através de um sistema de lentes de tubo telecêntrico composto por duas lentes focais f = 60 mm (TL1 e TL2, Figura 1B,C) (ver Tabela de Materiais).
NOTA: A imagem ampliada das lentes do tubo é formada na fenda de entrada do monocromador (MC, Figura 1B,C), e os dados resolvidos espacialmente/frequência são detectados em um detector CCD bidimensional (CCD, Figura 1B).
- Sobrepõem-se espacialmente os feixes de conversão ascendente e MIR em um espelho dicroico personalizado (DM, Figura 1B) que é transmissivo para MIR e reflexivo para NIR (veja Tabela de Materiais). Use duas íris para guiar o alinhamento: uma logo após o DM e outra na extremidade oposta. Use um medidor de energia após a íris para determinar se o MIR está centralizado e use uma placa NIR para localizar as posições NIR.
- Modo SHG
- Para mudar para imagens SHG, bloqueie o feixe IR e gire a grade do espectrógrafo para 501,5 nm para obter imagens do sinal SHG.
- Modo Brightfield
- Para alternar para imagens ópticas de campo brilhante, ligue a fonte de luz branca (consulte Tabela de materiais). Mova o controle deslizante integrado (I2PS, Figura 1B) para coletar imagens de campo brilhante na direção de contrapropagação, com a objetiva de imagem (RO) atuando como condensador e a objetiva do condensador (SO) atuando como a objetiva de imagem.
- Forme uma imagem da saída colimada da objetiva refrativa no plano do sensor de uma câmera de campo brilhante RGB usando um sistema de lente de tubo disponível comercialmente (consulte Tabela de Materiais).

Figura 1: Microscópio VSFG hiperespectral multimodal. (A) Vista superior da configuração principal. Um laser de bomba de 1025 nm foi enviado a uma OPA para gerar um pulso de infravermelho médio ajustável. O resíduo de 1025 nm foi frequentemente estreitado por um etalon (E) e espacialmente filtrado em um feixe gaussiano por um filtro espacial (SFG). Os feixes de IV médio e 1025 nm são sobrepostos espacialmente em um espelho dicroico (DM) personalizado e guiados através do microscópio invertido (região in box em A). (B) Os dois feixes são enviados para um scanner de feixe ressonante de 325 Hz montado em um controle deslizante integrado de 2 posições (I2PS), permitindo a comutação perfeita entre as modalidades óptica de campo brilhante e não linear. A plataforma do microscópio é equipada com uma objetiva de Schwarzschild (SO) de Schwarzschild corrigida infinitamente baseada em reflexiva atuando como um condensador e uma objetiva de imagem (RO) corrigida ao infinito baseada em refração montada em um estágio do eixo z de nanoposicionamento vertical (VNP). O SO focaliza a linha de feixes de entrada que o scanner de feixe ressonante reflete na amostra, enquanto o RO coleta a seção de sinais da linha VSFG. É importante controlar finamente a posição do eixo z da OR com precisão de 1 μm para garantir que a amostra esteja na melhor condição focal para imagens de alta qualidade. A linha colimada do sinal VSFG é então direcionada para um sistema de lentes tubulares composto por 2 lentes tub (TL1 e TL2), formando uma imagem ampliada na fenda de entrada do monocromador (MC). A linha de espectros resolvida em frequência é então hiperespectralmente imageada em um dispositivo acoplado à carga (CCD). Após a coleta de cada linha hiperespectral, a amostra é escaneada no eixo perpendicular ao eixo de varredura do scanner de feixe ressonante usando o NP. Para coletar imagens de campo brilhante da amostra, o I2PS é movido para a posição de campo brilhante e um espelho interceptando a fonte de luz branca (WLS) é instalado. A luz é então focalizada pelo RO e fotografada pelo SO. Uma imagem é então formada no plano do sensor da câmera de campo brilhante (BC) na parte superior do microscópio invertido. (C) Visão detalhada do caminho óptico através da área da lente do tubo para o MC e CCD. (D) Vista detalhada da área amostral entre as OS e RO. Clique aqui para ver uma versão maior desta figura.
2. Alinhamento do microscópio hiperespectral e calibração espacial vertical do eixo CCD
- Otimize aproximadamente a posição do plano da amostra (nano posicionador eixo z) usando uma amostra padrão de ZnO (1 μm de espessura) padrão de pulverização revestida 15 mm x 15 mm x 0,170 mm ± lamínula de cobertura de 0,005 mm e colocando-a em foco de campo brilhante usando a modalidade de imagem de campo brilhante.
NOTA: A posição z da RO, bem como o alinhamento da luz branca, pode precisar ser ajustada conforme necessário. Uma imagem representativa do ZnO no padrão de vidro usado para calibração do alinhamento é mostrada na Figura 2. - Mova o I2PS de volta para o braço de iluminação não linear e otimize a altura da amostra para a intensidade máxima de VSFG não ressonante gerada pelas regiões de ZnO observadas na câmera CCD.
NOTA: A posição z da RO deve ser ajustada para a intensidade máxima. Pode-se ter que iterar os passos 2.1 e 2.2 algumas vezes antes que a altura ideal da amostra e as OR sejam atingidas. - Ligue o scanner de feixe ressonante e colete uma linha das imagens.
- Colete imagens de intensidade não ressonante escaneando a amostra perpendicularmente à direção do scanner de feixe. Faça cortes verticais dos dados da imagem e estabeleça a relação pixel:mícron. (consulte a Figura 3 e sua legenda).
NOTA: A derivada dessas seções de linha é analisada para produzir a relação pixel:mícron do eixo CCD vertical que será usada para imagens futuras.

Figura 2: Qualidade de imagem representativa para alinhamento rugoso da modalidade de imagem de campo claro de um padrão ZnO. Clique aqui para ver uma versão maior desta figura.
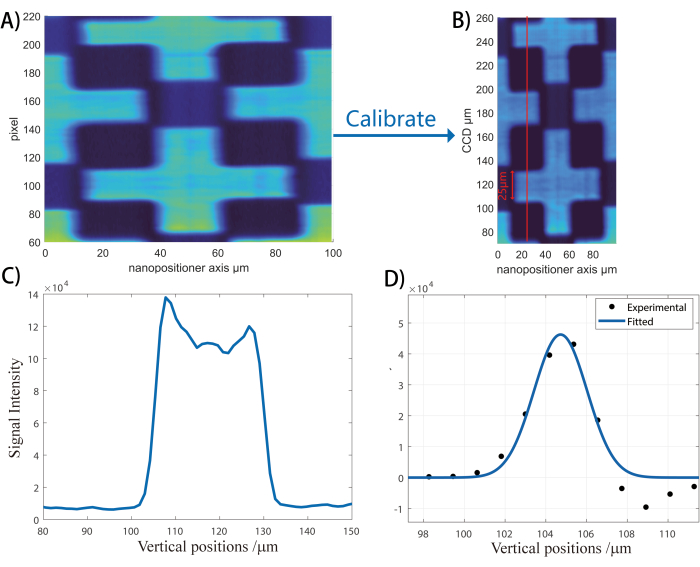
Figura 3: Fluxo de trabalho de calibração do eixo vertical. Esta figura ilustra como converter os pixels CCD em dimensões espaciais verticais na unidade de μm. (A) Uma imagem é coletada e reconstruída da lamínula de cobertura padronizada de ZnO. Em seguida, a distância de pixel de uma para as outras bordas do padrão (pequena barra vertical em A). Como a cruz do padrão ZnO é projetada para ter uma largura de 25 μm, pode-se usar a razão entre largura física e largura de pixel aqui para calcular a razão de dimensão física/pixel. Uma imagem representativa calibrada no eixo vertical é mostrada em (B). (C) Por último, toma-se uma fatia vertical como indicado pela linha vermelha. (D) A derivada do corte vertical é tomada para obter a resolução espacial. A derivada do corte vertical é utilizada para obter a resolução espacial. Clique aqui para ver uma versão maior desta figura.
3. Coleta de dados hiperespectrais
- Coletar os espectros de uma linha vertical dos sinais VSFG no CCD, cujos espectros estão dispersos ao longo do eixo horizontal e as posições espaciais são registradas no eixo vertical do CCD.
Observação : isso resulta em um conjunto de dados bidimensional para uma seção de linha única. - Depois que a seção de linha da amostra for obtida com imagens hiperespectralmente, digitalize a amostra no eixo perpendicular ao eixo de varredura de linha usando o nanoposicionador tridimensional (NP, Figura 1).
NOTA: O posicionador nano 3D é importante para alta precisão e reprodutibilidade na localização de regiões de amostra (plano x-y), bem como trazer a amostra em foco (eixo z). - Itere entre as etapas 3.1 e 3.2 para coletar uma imagem hiperespectral VSFG.
4. Análise hiperespectral dos dados
- Desmisture espectralmente os dados usando o fluxo de trabalho da biblioteca de imagens hiperespectrais da caixa de ferramentas de imagem do MatLab41.
NOTA: A desmistura espectral correlaciona localizações espaciais a espectros únicos. O código Matlab para análise de dados hiperespectrais é fornecido no Arquivo Suplementar 1.- Crie um hipercubo de 4 dimensões (x = espacial, y = espacial, z = intensidade dependente da frequência, ω = frequência) usando a função de hipercubo na biblioteca de imagens hiperespectrais da caixa de ferramentas de processamento de imagens do Matlab41.
- Identifique o número de espectros únicos com a função countEndmembersHFC com um valor de probabilidade de alarme falso (PFA) de 10-7.
- Identifique espectros únicos usando a função de desmistura espectral nfindr .
- Finalmente, usando a função sid , associe cada pixel a um dos espectros exclusivos identificados na etapa anterior.
NOTA: Métodos adicionais de desmistura e correspondência espectral podem ser feitos com funções/algoritmos alternativos oferecidos na MatLab Hyperspectral Imaging Library41.
- Ajuste os dados de soma de cada folha isolada à função Voigt42 (Arquivo Suplementar 1).
NOTA: A função lorentziana representa o limite de linha homogênea pura, enquanto a função gaussiana se origina de limites não homogêneos. Na realidade, os sistemas poderiam estar em uma combinação de limites homogêneos e não homogêneos, o que requer uma função Voigt - uma prática comum para espectroscopia de fase condensada, incluindo VSFG.
5. Análise geométrica da amostra
- Determinar a geometria das amostras de acordo com o procedimento mencionado nos pontos 5.2-5.3. Neste estudo, SDS@2 β-CD é usado como exemplo. Derivar os elementos tensores permitidos por simetria de χ(2) com base na simetria C7 da subunidade molecular da amostra de mesofolhas de SDS@2 β-CD.
NOTA: A simetria permitida χ(2) depende da simetria. Para calcular a suscetibilidade não linear permitida de qualquer simetria, consulte a referência43. - Aplique a rotação de Euler27 para relacionar as medidas do quadro de laboratório com o quadro molecular.
NOTA: No caso do SDS@2 β-CD, sua simetria C7 leva a oito equações independentes relacionando 8 saídas (quadro de laboratório χ(2)) a 8 entradas (6 hiperpolarizabilidade independente β(2), e dois ângulos: Θ, o ângulo de inclinação em relação ao plano da amostra de todas as folhas e, φ, a rotação no plano da folha (Figura 4)). Duas folhas são usadas para extrair os alinhamentos moleculares comuns das duas folhas. As relações entre φ1 e φ2 (ângulo de rotação no plano das duas folhas) podem ser extraídas das imagens de campo brilhante. No exemplo atual, φ2 = φ1 + 60°. Supõe-se que todas as unidades moleculares estejam no mesmo ângulo, então Θ1 = Θ2. Isso resulta em 11 incógnitas (9 independentes, incluindo 6 hiperpolarizabilidade independente β(2), Θ 1 e φ1, e a razão de cobertura relativa entre as folhas N e os dois ângulos dependentes, que são φ 2, e Θ 2) para 16 conhecidos (8 polarizações de quadro de laboratório por folha e duas folhas). - Relacione o quadro de laboratório χ(2) e a hiperpolarizabilidade do quadro molecular β(2) resolvidos pela polarização com um solucionador de função de rede neural.
NOTA: Um resumo detalhado dessa abordagem pode ser encontrado na referência27.- Crie um modelo de rede neural em camadas no Python44usando Keras composto por uma estrutura de nó 200-100-50 e uma função de ativação de tangente hiperbólica.
- Crie uma matriz de 100000 x 11 gerada aleatoriamente de valores de β(2), Θ 1, Θ 2, φ1, φ 2 e N. Calcule o quadro de laboratório correspondente 16 χ(2), usando a equação determinada em 5.2 por rotações de Euler.
- Use os valores χ(2) calculados (um total de 100.000 por 16 valores) como entrada, e aprenda a prever 11 valores (β(2), Θ 1, Θ 2, φ1, φ 2 e N) quando fornecidos 16 valores χ(2).
- Uma vez treinado, use outro conjunto de 1000 entradas com as entradas e saídas para testar o modelo treinado. A saída prevista e a saída verdadeira devem mostrar uma relação linear com uma inclinação de 1.
- Por fim, forneça o χ(2) medido experimentalmente a partir de duas folhas (cada folha tem 8 χ(2 ) medido) e use o modelo treinado para prever o ângulo de inclinação Θ, juntamente com outras propriedades.
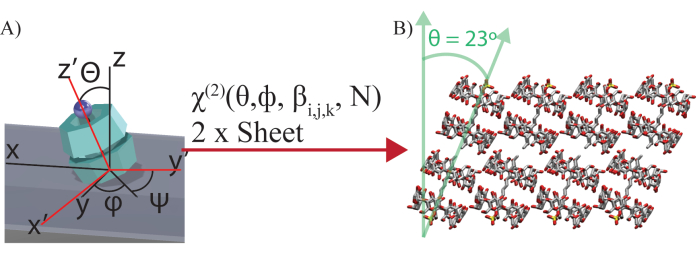
Figura 4: Ilustração da transformação de Euler. (A) Ilustração da transformação de Euler entre as coordenadas de laboratório (XYZ) suscetibilidade de segunda ordem χ(2) e as coordenadas moleculares (xyz) hiperpolarizabilidade βijk. A rotação de Euler z-y'-z'' é realizada nas coordenadas moleculares, com φ como o ângulo de rotação no plano, θ como o ângulo de inclinação e ψ como o ângulo de torção. ψ é integrado para ângulos de torção arbitrários em torno do eixo molecular. φ não é integrado porque todas as moléculas giram para um ângulo específico em relação à estrutura do laboratório para formar as folhas auto-montadas. N é a cobertura superficial relativa das duas folhas. (B) Visualização das subunidades inclinadas formando uma folha determinada pelos resultados da rede neural. Esse valor foi modificado de Wagner et al.27. Clique aqui para ver uma versão maior desta figura.
Resultados
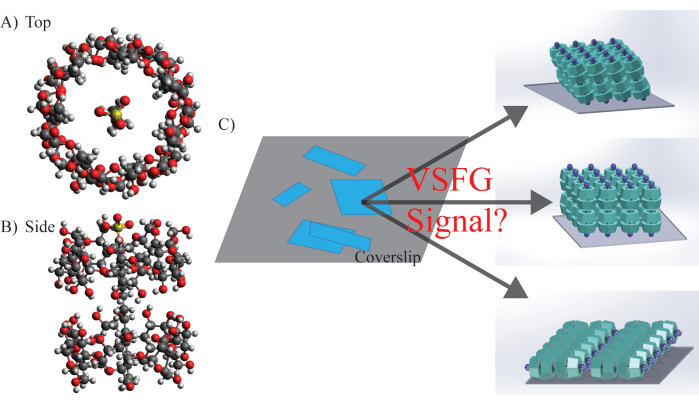
Figura 5: Estrutura molecular, morfologia e orientação potencial do SDS@β-CD. (A) Vista superior e (B) Estrutura química lateral do SDS@β-CD. (C) Distribuição representativa e heterogênea das folhas de mesoescala no plano amostral. A subunidade molecular poderia ter diferentes orientações ...
Discussão
As etapas mais críticas são de 1,42 a 1,44. É fundamental alinhar bem a lente objetiva para uma resolução espacial óptica. Também é importante coletar o sinal emitido, relé e projetar o feixe de varredura como uma linha nas fendas de entrada. Alinhamentos adequados garantiriam a melhor resolução e relação sinal-ruído. Para uma amostra típica, como folhas de SDS@2 β-CD de 100 μm por 100 μm, uma imagem de boa resolução (~1 μm de resolução) com uma alta relação sinal-ruído levaria 20 minutos. Isso ...
Divulgações
Os autores não têm nada a revelar.
Agradecimentos
O desenvolvimento do instrumento é apoiado pelo Grant NSF CHE-1828666. ZW, JCW e WX são apoiados pelo National Institutes of Health, National Institute of General Medical Sciences, Grant 1R35GM138092-01. A BY é apoiada pela Youth Innovation Promotion Association, Academia Chinesa de Ciências (CAS, 2021183).
Materiais
| Name | Company | Catalog Number | Comments |
| 1x Camera Por | Thorlabs | WFA4100 | connect a camera to a microscope or optical system |
| 25.0 mm Right-Angle Prism Mirror, Protected Gold | Thorlabs | MRA25-M01 | reflect light and produce retroreflection, redirecting light back along its original path |
| 3” Universal Post Holder-5 Pack | Thorlabs | UPH3-P5 | hold and support posts of various sizes and configurations |
| 30 mm to 60 mm Cage Plate, 4 mm Thick | Thorlabs | LCP4S | convert between a 30 mm cage system and a 60 mm cage system |
| 500 mm Tall Cerna Body with Epi Arm | Thorlabs | CEA1500 | provide the function of enabling top illumination techniques in microscopy |
| 60 mm Cage Mounted Ø50.0 mm Iris | Thorlabs | LCP50S | control the amount of light passing through an optical system |
| 60 mm Cage Mounting Bracket | Thorlabs | LCP01B | mount and position a 60 mm cage system in optical setups |
| Air spaced Etalon | SLS Optics Ltd. | Customized | generate narrow-band 1030 nm light |
| Cage Plate Mounting Bracket | Thorlabs | KCB2 | hold and adjust mirrors at a precise angle |
| CCD | Andor Technologies | Newton | 2D CCD for frequency and spatial resolution |
| Collinear Optical Parametric Amplifier | Light Conversion | Orpheus-One-HP | Tunable MID light generator |
| Copper Chloride | Thermo Fischer Scientific | A16064.30 | Self-assembly component |
| Customized Dichroic Mirror | Newport | Customized | selectively reflects or transmits light based on its wavelength or polarization |
| Ext to M32 Int Adapter | Thorlabs | SM1A34 | provide compatibility and facilitating the connection between components with different thread types |
| Infinity Corrected Refractive Objective | Zeiss | 420150-9900-000 | Refractive Objective |
| Infinity Corrected Schwarzschild Objective | Pike Technologies Inc. | 891-0007 | Reflective objective |
| Laser | Carbide, Light-Conversion | C18212 | Laser source |
| M32x0.75 External to Internal RMS | Thorlabs | M32RMSS | adapt or convert the threading size or type of microscope objectives |
| M32x0.75 External to M27x0.75 Internal Engraving | Thorlabs | M32M27S | adapt or convert the threading size or type of microscope objectives |
| Manual Mid-Height Condenser Focus Module | Thorlabs | ZFM1030 | adjust the focus of an optical element |
| Monochromator | Andor Technologies | Shamrock 500i | Provides frequency resolution for each line scan |
| Motorized module with 1" Travel for Edge-Mounted Arms | Thorlabs | ZFM2020 | control the vertical positon of the imaging objective |
| Nanopositioner | Mad City Labs Inc. | MMP3 | 3D sample stage |
| Resonant Scanner | EOPC | SC-25 | 325Hz resonant beam scanner |
| RGB Color CCD Camera | Thorlabs | DCU224C | Brightfield camera, discontinued but other cameras will work just as well |
| RGB tube lens | Thorlabs | ITL200 | white light collection |
| Right Angle Kinematic Breadboard | Thorlabs | OPX2400 | incorporate a sliding mechanism with two fixed positions |
| Right Angle Kinematic Mirror Mount, 30 mm | Thorlabs | KCB1 | hold and adjust mirrors at a precise angle |
| Right Angle Kinematic Mirror Mount, 60 mm | Thorlabs | KCB2 | hold and adjust mirrors at a precise angle |
| SM2, 60 mm Cage Arm for Cerna Focusing Stage | Thorlabs | CSA2100 | securely mount and position condensers |
| Snap on Cage Cover for 60 mm Cage, 24 in Long, | Thorlabs | C60L24 | enclose and protect the components inside the cage |
| Sodium dodecyl sulfate | Thermo Fischer Scientific | J63394.AK | Self-assembly component |
| Three-Chnnale Controller and Knob Box for 1" Cerna Travel Stages | Thorlabs | MCM3001 | control ZFM2020 |
| Tube lens | Thorlabs | LA1380-AB - N-BK7 | SFG signal collection |
| Visible LED Set | Thorlabs | WFA1010 | provide illumination in imaging setup |
| Whitelight Source | Thorlabs | WFA1010 | Whitelight illumination source for brightfield imaging |
| WPH05M-1030 - Ø1/2" Zero-Order Half-Wave Plate, Ø1" Mount, 1030 nm | Thorlabs | WPH05M-1030 | alter the polarization state of light passing through it |
| WPLQ05M-3500 - Ø1/2" Mounted Low-Order Quarter-Wave Plate, 3.5 µm | Thorlabs | WPLQ05M-3500 | alter the polarization state of light passing through it |
| X axis Long Travel Steel Extended Contact Slide Stages | Optosigma | TSD-65122CUU | positioning stages that offer extended travel in the horizontal (X) direction |
| XT95 4in Rail Carrier | Thorlabs | XT95RC4 | mount and position optical components |
| X-Y Axis Translation Stage w/ 360 deg. Rotation | Thorlabs | XYR1 | precise movement and positioning of objects in two dimensions, along with the ability to rotate the platform |
| XY(1/2") Linear Translator with Central SM1 Thru Hole | Thorlabs | XYT1 | provide precise movement and positioning in two dimensions |
| Yb doped Solid State Laser | Light Conversion | CB3-40W | Seed laser |
| β-Cyclodextrin | Thermo Fischer Scientific | J63161.22 | Self-assembly component |
Referências
- Zhu, X. D., Suhr, H., Shen, Y. R. Surface vibrational spectroscopy by infrared-visible sum frequency generation. Physical Review B. 35 (6), 3047-3050 (1987).
- Shen, Y. R. Surface properties probed by second-harmonic and sum-frequency generation. Nature. 337 (6207), 519-525 (1987).
- Li, Y., Shrestha, M., Luo, M., Sit, I., Song, M., Grassian, V. H., Xiong, W. Salting up of proteins at the air/water interface. Langmuir. 35 (43), 13815-13820 (2019).
- Wang, C., Li, Y., Xiong, W. Extracting molecular responses from ultrafast charge dynamics at material interfaces. Journal of Materials Chemistry C. 8 (35), 12062-12067 (2020).
- Nihonyanagi, S., Mondal, J. A., Yamaguchi, S., Tahara, T. Structure and dynamics of interfacial water studied by heterodyne-detected vibrational sum-frequency generation. Annual Review of Physical Chemistry. 64 (1), 579-603 (2013).
- Nihonyanagi, S., Yamaguchi, S., Tahara, T. Ultrafast dynamics at water interfaces studied by vibrational sum frequency generation spectroscopy. Chemical Reviews. 117 (16), 10665-10693 (2017).
- Singh, P. C., Nihonyanagi, S., Yamaguchi, S., Tahara, T. Ultrafast vibrational dynamics of water at a charged interface revealed by two-dimensional heterodyne-detected vibrational sum frequency generation. The Journal of Chemical Physics. 137 (9), 094706 (2012).
- Jubb, A. M., Hua, W., Allen, H. C. Environmental chemistry at vapor/water interfaces: insights from vibrational sum frequency generation spectroscopy. Annual Review of Physical Chemistry. 63 (1), 107-130 (2012).
- Ishiyama, T., Sato, Y., Morita, A. Interfacial structures and vibrational spectra at liquid/liquid boundaries: molecular dynamics study of water/carbon tetrachloride and water/1,2-dichloroethane interfaces. The Journal of Physical Chemistry C. 116 (40), 21439-21446 (2012).
- Sapi, A., Liu, F., Cai, X., Thompson, C. M., Wang, H., An, K., Krier, J. M., Somorjai, G. A. Comparing the catalytic oxidation of ethanol at the solid-gas and solid-liquid interfaces over size-controlled pt nanoparticles: striking differences in kinetics and mechanism. Nano Letters. 14 (11), 6727-6730 (2014).
- Chen, X., Wang, J., Sniadecki, J. J., Even, M. A., Chen, Z. Probing α-helical and β-sheet structures of peptides at solid/liquid interfaces with SFG. Langmuir. 21 (7), 2662-2664 (2015).
- Dramstad, T. A., Wu, Z., Gretz, G. M., Massari, A. M. Thin films and bulk phases conucleate at the interfaces of pentacene thin films. The Journal of Physical Chemistry C. 125 (30), 16803-16809 (2021).
- Xiang, B., Li, Y., Pham, C. H., Paesani, F., Xiong, W. Ultrafast direct electron transfer at organic semiconductor and metal interfaces. Science Advances. 3 (11), e1701508 (2017).
- Livingstone, R. A., Nagata, Y., Bonn, M., Backus, E. H. G. Two types of water at the water-surfactant interface revealed by time-resolved vibrational spectroscopy. Journal of the American Chemical Society. 137 (47), 14912-14919 (2015).
- Wagner, J. C., Hunter, K. M., Paesani, F., Xiong, W. Water capture mechanisms at zeolitic imidazolate framework interfaces. Journal of the American Chemical Society. 143 (50), 21189-21194 (2021).
- Montenegro, A., Dutta, C., Mammetkuliev, M., Shi, H., Hou, B., Bhattacharyya, D., Zhao, B., Cronin, S. B., Benderskii, A. V. Asymmetric response of interfacial water to applied electric fields. Nature. 594 (7861), 62-65 (2021).
- Nihonyanagi, S., Ishiyama, T., Lee, T., Yamaguchi, S., Bonn, M., Morita, A., Tahara, T. Unified molecular view of the air/water interface based on experimental and theoretical χ(2) spectra of an isotopically diluted water surface. Journal of the American Chemical Society. 133 (42), 16875-16880 (2011).
- Shen, Y. R., Ostroverkhov, V. Sum-frequency vibrational spectroscopy on water interfaces: polar orientation of water molecules at interfaces. Chemical Reviews. 106 (4), 1140-1154 (2006).
- Hosseinpour, S., Roeters, S. J., Bonn, M., Peukert, W., Woutersen, S., Weidner, T. Structure and dynamics of interfacial peptides and proteins from vibrational sum-frequency generation spectroscopy. Chemical Reviews. 120 (7), 3420-3465 (2020).
- Wang, H., Xiong, W. Vibrational sum-frequency generation hyperspectral microscopy for molecular self-assembled systems. Annual Review of Physical Chemistry. 72 (1), 279-306 (2021).
- Wang, H. -. F., Velarde, L., Gan, W., Fu, L. Quantitative sum-frequency generation vibrational spectroscopy of molecular surfaces and interfaces: lineshape, polarization, and orientation. Annual Review of Physical Chemistry. 66 (1), 189-216 (2015).
- Inoue, K., Ahmed, M., Nihonyanagi, S., Tahara, T. Reorientation-induced relaxation of free oh at the air/water interface revealed by ultrafast heterodyne-detected nonlinear spectroscopy. Nature Communications. 11 (1), 5344 (2020).
- Wang, H., Gao, T., Xiong, W. Self-phase-stabilized heterodyne vibrational sum frequency generation microscopy. ACS Photonics. 4 (7), 1839-1845 (2017).
- Wang, H., Xiong, W. Revealing the molecular physics of lattice self-assembly by vibrational hyperspectral imaging. Langmuir. 38 (10), 3017-3031 (2022).
- Raghunathan, V., Han, Y., Korth, O., Ge, N. -. H., Potma, E. O. Rapid vibrational imaging with sum frequency generation microscopy. Optics Letters. 36 (19), 3891 (2011).
- Wang, H., Wagner, J. C., Chen, W., Wang, C., Xiong, W. Spatially dependent h-bond dynamics at interfaces of water/biomimetic self-assembled lattice materials. Proceedings of the National Academy of Sciences. 117 (38), 23385-23392 (2020).
- Wagner, J. C., Wu, Z., Wang, H., Xiong, W. Imaging orientation of a single molecular hierarchical self-assembled sheet: the combined power of a vibrational sum frequency generation microscopy and neural network. The Journal of Physical Chemistry B. 126 (37), 7192-7201 (2022).
- Han, Y., Hsu, J., Ge, N. -. H., Potma, E. O. Polarization-sensitive sum-frequency generation microscopy of collagen fibers. The Journal of Physical Chemistry B. 119 (8), 3356-3365 (2015).
- Chung, C. -. Y., Potma, E. O. Biomolecular imaging with coherent nonlinear vibrational microscopy. Annual Review of Physical Chemistry. 64 (1), 77-99 (2013).
- Potma, E. O. Advances in vibrationally resonant sum-frequency generation microscopy. Optics in the Life Sciences Congress. , (2017).
- Han, Y., Raghunathan, V., Feng, R. R., Maekawa, H., Chung, C. -. Y. Y., Feng, Y., Potma, E. O., Ge, N. -. H. H. Mapping molecular orientation with phase sensitive vibrationally resonant sum-frequency generation microscopy. The Journal of Physical Chemistry B. 117 (20), 6149-6156 (2013).
- Hsu, J., Haninnen, A., Ge, N. -. H., Potma, E. O. Molecular imaging with sum-frequency generation microscopy. Optics in the Life Sciences. , (2015).
- Hanninen, A., Shu, M. W., Potma, E. O. Hyperspectral imaging with laser-scanning sum-frequency generation microscopy. Biomedical Optics Express. 8 (9), 4230 (2017).
- Wang, H., Chen, W., Wagner, J. C., Xiong, W. Local ordering of lattice self-assembled SDS@2β-CD materials and adsorbed water revealed by vibrational sum frequency generation microscope. The Journal of Physical Chemistry B. 123 (29), 6212-6221 (2019).
- Cimatu, K., Baldelli, S. Chemical imaging of corrosion: sum frequency generation imaging microscopy of cyanide on gold at the solid−liquid interface. Journal of the American Chemical Society. 130 (25), 8030-8037 (2008).
- Shah, S. A., Baldelli, S. Chemical imaging of surfaces with sum frequency generation vibrational spectroscopy. Accounts of Chemical Research. 53 (6), 1139-1150 (2020).
- Wagner, J. a. c. k. s. o. n. . C., Zishan, W. u., Xiong, W. Multimodal nonlinear vibrational hyperspectral imaging. ChemRxiv. , (2023).
- Yan, C., Wagner, J., Wang, C., Ren, J., Lee, C., Wan, Y., Wang, S., Xiong, W. Multi-dimensional widefield infrared-encoded spontaneous emission microscopy: distinguishing chromophores by ultrashort infrared pulses. ChemRxiv. , (2023).
- Lin, Y., Fromel, M., Guo, Y., Guest, R., Choi, J., Li, Y., Kaya, H., Pester, C. W., Kim, S. H. Elucidating interfacial chain conformation of superhydrophilic polymer brushes by vibrational sum frequency generation spectroscopy. Langmuir. 38 (48), 14704-14711 (2022).
- Choi, J., Lee, J., Makarem, M., Huang, S., Kim, S. H. Numerical simulation of vibrational sum frequency generation intensity for non-centrosymmetric domains interspersed in an amorphous matrix: a case study for cellulose in plant cell wall. The Journal of Physical Chemistry B. 126 (35), 6629-6641 (2022).
- Matlab Image Processing Toolbox Hyperspectral Imaging Library. . , .
- Armstrong, B. H. Spectrum line profiles: the Voigt function. Journal of Quantitative Spectroscopy and Radiative Transfer. 7 (1), 61-88 (1967).
- Wu, Z., Xiong, W. Neumann's principle based eigenvector approach for deriving non-vanishing tensor elements for nonlinear optics. The Journal of Chemical Physics. 157 (13), 134702 (2022).
- Chollet, F. Keras Neural Network Library. https://github.com/fchollet/keras accessed Apr 12. , (2021).
- Vicidomini, G., Bianchini, P., Diaspro, A. STED super-resolved microscopy. Nature Methods. 15 (3), 173-182 (2018).
- Xiong, W., Laaser, J. E., Mehlenbacher, R. D., Zanni, M. T. Adding a dimension to the infrared spectra of interfaces using heterodyne detected 2D sum-frequency generation (HD 2D SFG) spectroscopy. Proceedings of the National Academy of Sciences. 108 (52), 20902-20907 (2011).
- Lukas, M., Backus, E. H. G., Bonn, M., Grechko, M. Passively stabilized phase-resolved collinear sfg spectroscopy using a displaced sagnac interferometer. The Journal of Physical Chemistry A. 126 (6), 951-956 (2022).
- Ji, N., Ostroverkhov, V., Chen, C., Shen, Y. Phase-sensitive sum-frequency vibrational spectroscopy and its application to studies of interfacial alkyl chains. Journal of the American Chemical Society. 129 (33), 10056-10057 (2007).
Reimpressões e Permissões
Solicitar permissão para reutilizar o texto ou figuras deste artigo JoVE
Solicitar PermissãoThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Todos os direitos reservados