このコンテンツを視聴するには、JoVE 購読が必要です。 サインイン又は無料トライアルを申し込む。
Method Article
マウス骨格筋の未分画バルク培養によるニッチおよび幹細胞の静止を再現
* これらの著者は同等に貢献しました
要約
骨格筋は、常在幹細胞を含む複数の細胞タイプで構成されており、それぞれが筋肉の恒常性と再生に特別な貢献をしています。ここでは、生理学的、in vivo、および環境的特性の多くを保持するex vivo環境での筋幹細胞および筋細胞ニッチの2D培養について説明します。
要約
骨格筋は体の中で最大の組織であり、運動から体温調節まで、複数の機能を果たします。その機能と損傷からの回復は、多数の細胞タイプと、コア筋細胞(筋繊維、筋幹細胞)とそのニッチの間の分子シグナルに依存しています。ほとんどの実験環境では、この複雑な生理学的微小環境は維持されず、筋幹細胞にとって重要な細胞状態である休止状態のex vivo 研究も許可されていません。ここでは、ニッチの細胞成分を持つ筋幹細胞の ex vivo 培養のためのプロトコルが概説されています。筋肉の機械的および酵素的分解を通じて、細胞タイプの混合物が得られ、それは2D培養に入れられます。免疫染色は、1週間以内に、筋線維、そして重要なことに、静止筋幹細胞の特徴を示すPax7陽性細胞とともに、複数のニッチ細胞が培養中に存在することを示しています。これらの独特な特性はこのプロトコルに基本的で、translational質問に演説するのに使用することができる静止そっくりの幹細胞の細胞拡大そして生成のための強力な用具をする。
概要
運動、呼吸、代謝、姿勢、体温の維持はすべて骨格筋に依存しており、骨格筋の機能不全は衰弱性の病状(ミオパチー、筋ジストロフィーなど)を引き起こす可能性があります。1.骨格筋は、その本質的な機能と豊富さから、正常な筋肉機能をサポートし、治療標的として役立つ重要な側面を理解しようと努力する世界中の研究機関の注目を集めています。さらに、骨格筋は、主にその常在幹細胞2により、健康な筋肉が完全な損傷や変性の後に完全に自己修復できるため、再生と幹細胞機能を研究するために広く使用されているモデルです。これらはサテライト細胞とも呼ばれ、筋線維3の周辺の基底層の下に局在している。
成人の骨格筋の中核となる細胞は、筋線維(長い合胞体多核細胞)とサテライト細胞(筋原性を有する幹細胞で、損傷によって活性化されるまで静止している)です。後者の細胞は筋肉再生の中心細胞であり、このプロセスはそれらがない場合には起こり得ません4,5,6,7。その身近な微小環境には、複数の細胞タイプとそれらにシグナルを送る分子因子があります。このニッチは、発達を通じて成人期8まで徐々に確立されます。成体筋には、複数の細胞タイプ(内皮細胞、周皮細胞、マクロファージ、線維脂肪形成前駆細胞-FAP、制御性T細胞など)が含まれています。9,10および細胞外マトリックス成分(ラミニン、コラーゲン、フィブロネクチン、フィブリリン、ペリオスチンなど)11は、健康、病気、および再生の文脈で互いに、および衛星細胞と相互作用します。
この複雑なニッチを実験環境で維持することは、基本的ではあるが困難である。同様に難しいのは、サテライトセル9にとって重要なセル状態である静止状態を維持または回復させることである。これらの課題に部分的に取り組むためにいくつかの方法が導入されており、それぞれに長所と短所があります(説明のセクションで詳しく説明します)。ここでは、これら2つの障壁を部分的に克服できる方法を紹介します。筋肉は最初に採取され、次に機械的および酵素的に分解されてから、不均一な細胞混合物が培養されます。培養の過程で、ニッチの多くの細胞タイプが検出され、静止状態に戻ったサテライト細胞が観察されます。プロトコルの最後のステップとして、広く受け入れられているマーカーを使用して各細胞タイプの検出を可能にする免疫蛍光法のステップが提示されます。
プロトコル
すべての実験は、Institut Mondor de Recherche Biomédicale(INSERM U955)のフランスおよびEUの動物規制、特に指令2010/63/UEに準拠しています。動物は、認証番号A94、028、379およびD94-028-028の動物施設で管理され、充実した環境で飼育されました。それらは許可された研究者と動物の世話人によってのみ取り扱われ、動物飼育施設の職員によって目視検査が行われ、生涯にわたって不快感の兆候がないか確認されました。彼らは解剖前に子宮頸部脱臼によって安楽死させられた。動物の生涯の間に介入処置は行われなかった。したがって、倫理委員会とフランス高等教育研究イノベーション省から手続きの承認を得る必要はありませんでした。実際、指令2010/63/UEによると、安楽死と死後解剖には倫理的クリアランスは必要ありません。本稿で発表した結果は、野生型C57BL/6NRj系統( 材料表参照)とトランスジェニック Tg:Pax7-nGFP 系統12(我々のチームで作製)によるものです。プロトコルは、8〜12週齢の雄および雌のマウスに適用されました。
1. 試薬および装置調製、前消化
- 解剖器具(直線および湾曲したハサミ、鉗子、 材料表を参照)に70%エタノールをスプレーし、紙で乾かします。コルク板にアルミホイルを塗り、10cmのシャーレ(1匹につき1枚)を近くに置いておく。紙と70%エタノールを手の届くところに用意してください。
注意: 解剖の最後に、解剖ツールを水ですすぎ、70%エタノールをスプレーし、紙で乾かします。 - 回転式ウォーターバスを 37 °C に設定し、DMEM と 1% ペニシリン-ストレプトマイシン、0.5 U/mL コラゲナーゼ、3 U/mL ディスパーゼ( 材料表を参照)、0.2% BSA を 50 mL チューブに混ぜて消化ミックス(20 mL/動物)を調製します。
- 消化ミックスを細胞培養フード内の0.22 μmフィルターに通します。
注意: 消化ミックスは毎回新鮮に準備することをお勧めします。
2. 試薬と機器の準備:消化後
- 消化後、ミックスは凍結または培養できます。凍結には、10% DMSO:90% ウシ胎児血清 (FBS) とクライオチューブのセット (クライオチューブ 2 mL あたり 1 mL の細胞懸濁液) を用意します。培養には、培地(DMEMに1%ペニシリン-ストレプトマイシン、4 ng/mLのbFGF、および20%FBSを添加)と8ウェルプレートのセットを準備します。セルをめっきする前に、プレートをコーティングする必要があります(詳細はステップ7.1で説明します)。
- 染色には、リン酸緩衝生理食塩水(PBS)(8ウェルプレートの0.15 mL/ウェル)およびブロッキング溶液(PBS中の5%IgGフリーウシ血清アルブミン[BSA]、8ウェルプレートの0.15 mL/ウェル)に4%パラホルムアルデヒド(PFA)を調製します。
注意:PFAパウダーを吸い込まないでください。化学フードの下で準備して取り扱ってください。
3.解剖
- 安楽死させた動物に70%エタノールをスプレーします。腹部の高さに大きなハサミで横切り(体の左側から右側)を行い、腰の周りを切ります。後肢の皮膚を引き剥がして筋肉を露出させます(図1A)。
- アルミホイルで覆われたコルクプレートに動物を置き、反対側の前肢と後肢を固定します。すべての後肢の筋肉(前部と後部)を氷の上に置かれた10cmのシャーレにすばやく取り出します(図1B、C)。大腿四頭筋と後頭筋の周りの領域から脂肪組織を取り除くように特別な注意を払ってください。筋膜、神経、腱も、解剖に費やす全体的な時間を損なわなければ、この時点で切除することができます。
注:両方の後肢の最適な解剖時間は約15〜20分です。解剖時間は30分を超えないことをお勧めします。 - 時々DMEMを筋肉に滴下して湿らせますが、切り刻みが難しくなるため、多すぎないようにします。もう一方の後肢についても繰り返します。1匹の動物のすべての筋肉がシャーレに入ったら(図1D)、はさみで7〜10分間細かく刻み、滑らかな均質体を得ます(図1E)。
注:このプロトコルでは、L-グルタミン、ピルビン酸、および4.5 g / L D-グルコースを添加したDMEMが使用されます。
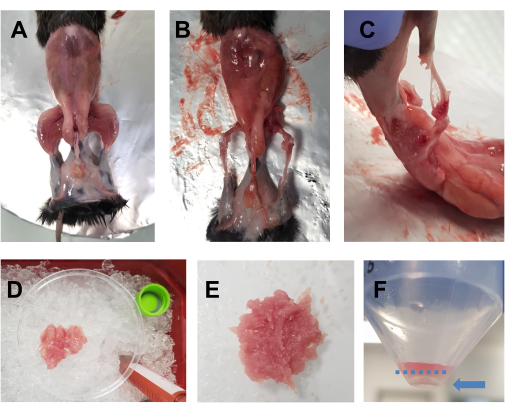
図1:培養前の筋肉の準備。(A)ステップ3.1で説明したように、皮膚を切除して後肢の筋肉を露出させます。(B、C)すべての後肢の筋肉は、ステップ3.2で説明したように、骨の周り(B)と骨の間(C)に採取されます。(D)採取した筋肉を、ステップ3.3で説明したように、DMEM滴で氷上の10cmのシャーレに入れ、湿らせておきます。(E)筋肉をハサミで細かく刻み、この画像に描かれている粘稠度のある滑らかなペーストが得られます。(f)最終遠心分離後のペレットの画像。青い矢印は、青い破線の下で、チューブに接しているペレットを強調表示します。 この図の拡大版をご覧になるには、ここをクリックしてください。
4.消化
注:消化の最後に、セクション5には、4°Cの遠心分離機、氷の入ったバケツ、3つのセルストレーナー(100 um、70 um、40 um)、および3つの50 mLチューブ(動物あたり)が必要です。
- ステップ1.2の説明に従って、分解ミックスを調製し、ろ過します。ミックスを氷の上に置いてください。
- すべての筋肉をみじん切りにしたら、ホモジネートを20 mLの消化ミックスが入った50 mLチューブに入れます。蓋の端をフレキシブルフィルムで包んで漏れを防ぎ、チューブを低速から中速(50rpm)で37°Cの振とう水浴に入れます。
- 37°Cで1時間後、蓋を開け、10 mLのピペットで7回静かにピペッティングして混合し、均一な混合液を得ます。蓋の周りに新しいフィルムを貼り、振とう水浴に戻します。1時間後、チューブを取り外し、浴槽を止めます。
注:培養の場合は、このインキュベーション時間を使用して、セクション5に進む前に、ステップ7.1の説明に従ってプレートをコーティングします。
5. 濾過
- 消化チューブに最大50 mLの冷たいDMEM(1%ペニシリン-ストレプトマイシンを添加)を充填します。チューブを3回ひっくり返して混ぜます。次のステップのために、DMEMをアイスペールに入れておきます。
- 新しい 50 mL チューブに 100 μm のセルストレーナーを置きます。消化した混合物をセルストレーナーに通し、新しいチューブに通します。600 x g で4°Cで5分間遠心分離します。 上澄み液を廃液容器に注ぎます。
- ペレットを1 mLのコールドDMEM(1%ペニシリン-ストレプトマイシンを添加)に再懸濁します。チューブに最大 50 mL の同じ DMEM を充填します。注:遠心分離をスキップすると、次のペレットの識別と維持が難しくなります。
- 新しい 50 mL チューブに 70 μm のセルストレーナーを置きます。遠心分離/再懸濁した混合物をセルストレーナーに通し、新しいチューブに通します。4°Cで5分間、80 x g で遠心分離します。
メモ: この手順は必須ではありませんが、細胞の破片を取り除くために推奨されます。 - 新しい 50 mL チューブに 40 μm セルストレーナーを置きます。上清をセルストレーナーに通して新しいチューブに通します。600 x g で4°Cで5分間遠心分離し、上清を廃液容器に注ぎ、培養フード下のFBSにペレットを再懸濁します。このステップでは、ペレットは非常に小さいです(図1F)。
注:40 μmのストレーナーでろ過すると、培養物の後の染色で非特異的なシグナルが得られる破片が除去されます。
6.(オプション)凍結
注: セクション 6 はオプションです。プロトコルはろ過の後で停止することができますが、これは細胞の生存および培養の成功を減らすことができます。
- DMSO を添加して 10% DMSO:90% FBS 比が得られるようにし、クライオチューブ (クライオチューブ 2 mL あたり 1 mL の再懸濁ペレット) に移します。
- クライオチューブを-80°Cのポリスチレンボックスに入れて一晩置きます。翌日-150°Cに移し、長期保存します。
注:-80°Cでの短期保存も可能です。 - 培養を開始するときは、細胞懸濁液が融解するまで、クライオチューブを37°Cのウォーターバスで素早く解凍します。培養フードの下で4 mLのDMEMと混合します。600 x g で 4 °C で 5 分間スピンします。 上清をピペットで取り出し、ステップ7.2の説明に従って続行します。
7. 培養
注:凍結または新鮮な細胞懸濁液は、3〜4枚の8ウェルプレートの24〜32ウェルを満たすことが期待できます。
- 8ウェルプレートをコーティング溶液でコーティングし、4°Cまたは氷上で解凍します(ストックコーティング溶液は通常-20°Cに保たれます)。1つのウェルに0.4 mLのコーティング溶液を加え、ウェルからウェルへとピペットで移動させます。コーティング液をすべてのウェルに移した後、将来の培養のために再回収して再凍結することができます。セルをプレーティングする前に、コーティングされたプレートを37°Cで30分間保持します。
- 4 ng/mL bFGF( 資料表を参照)を添加したDMEM(1%ペニシリン-ストレプトマイシンを添加)をFBS細胞懸濁液に添加し、20%FBS:80%DMEM比を得ます。
注:bFGFの添加は、初代筋芽細胞培養およびバルク培養におけるサテライト様細胞産生において有益ですが、~7日間のバルク培養でbFGFを省略しても細胞収量が著しく損なわれないため、その添加は任意です。 - ウェルあたり0.4 mLの懸濁液(ステップ7.2から)をコーティングされた8ウェルプレートにプレートします。
注:凍結および生鮮調製の場合、動物あたり30 cm2 の培養を計算します。 - 培養物を37°Cで5%CO2 で最大10日間インキュベートし、培養物が黄色がかった色に変化し始めたら毎日培地を交換します(通常は5〜7日)。
注:細胞周期13のS期の細胞を定量するには、固定の2時間前に10μMのEdUを添加します。最初のS相を捕捉するには、プレーティングから10 μM EdUを添加し、40時間の培養で固定します。
8.固定
注意: セクション8〜10は、特に明記されていない限り、室温で実施する必要があります。
- 培地をピペットで取り出し、細胞を4% PFA(0.15 mL/ウェル)で固定します。
注意:化学フードの下にPFAを追加します。
注:すべてのウェルが同時に固定されている場合は、室温で PFA と 10 分間インキュベートします。ウェルが異なる時点で固定されている場合は、固定するウェルにPFAを添加し、プレートをインキュベーター内で37°Cで5分間保持します。 - PFA をピペットで取り出し、PBS を 10 秒間添加します(0.15 mL/ウェル)。PBSをピペットで取り出し、新鮮なPBSを5分間加えます(0.15 mL/ウェル)。
注:すべてのウェルが同時に固定されている場合は、室温でPBSとインキュベートします。ウェルが異なる時点で固定されている場合は、固定ウェルにPBSを添加し、プレートをインキュベーター内で37°Cで5分間保持します。次に、0.4 mLのPBSを添加し、プレートをインキュベーターで最大1週間保持します。
9. 透過処理とブロッキング
- 染色の準備ができたら、PBSをピペットで取り出し、0.5% TritonX 100 in PBS(0.15 mL/ウェル)で8分間透過処理します。TritonX 100 をピペットで取り出し、PBS で 10 秒間すすぎ(0.15 mL/ウェル)、PBS をピペットで取り出し、PBS で 5 分間(0.15 mL/ウェル)洗浄します。
- PBS中の5%IgGフリーBSAで30〜60分間(0.15 mL/ウェル)ブロックします。
10. 染色
- BSAをピペットで取り出し、PBS(0.15 mL/ウェル)で希釈した一次抗体混合物( 希釈倍率:抗CD31 1:100、抗FOSB 1:200、抗GFP 1:1,000、抗KI67 1:1,000、抗MyHC 1:400、抗MYOD 1:200、抗MYOG 1:150、抗PAX7 1:100、抗PDGFRa 1:50)を加え、4°Cで一晩インキュベーションします。
注:抗体のインキュベーション後、抗体混合物を回収し、アジ化ナトリウムを添加し、将来の再利用のために4°Cまたは-20°C(抗体メーカーの指示に従う)で保管します。 - 抗体ミックスをピペットで取り出し、PBSで10秒間(0.15 mL/ウェル)すすぎ、PBSをピペットで取り出し、PBSで5分間(0.15 mL/ウェル)洗浄します。
- 洗浄PBSをピペットで取り出し、二次抗体ミックス(ヤギ抗マウスAlexa Fluor 488、ヤギ抗ウサギAlexa Fluor 555、ヤギ抗ラットAlexa Fluor 647、ヤギ抗マウスAlexa Fluor 555、ヤギ抗ニワトリAlexa Fluor 488、すべて1:500-1,000の希釈で使用)およびPBS(0.15 mL/ウェル)で希釈した核マーカー(DAPIなど)を添加します( 資料表参照)。 光から保護して室温で1時間インキュベートします。
- 二次抗体混合物をピペットで取り出し、PBSで10秒間すすぎ(0.15 mL/ウェル)、PBSをピペットで取り出し、PBSで5分間(0.15 mL/ウェル)洗浄し、PBSをピペットで取り出し、マウントします。
注意: 取り外し可能なセパレーター付きの8ウェルプレートを使用する場合は、取り付ける前にセパレーターをはがしてください。
結果
このプロトコルは内生ニッチから衛星細胞そしてほとんどのセルを維持している間筋肉細胞培養を可能にする。図 2 はプロトコルの主なステップをまとめたもので、図 1 は解剖と消化の重要な部分を示しています。後肢の筋肉組織の解剖が推奨されます(図1A-C)、この筋肉群はよく研究されており、発...
ディスカッション
成人の骨格筋の機能は、精巧に調整された一連の細胞間相互作用と分子シグナルによって支えられています。ここでは、生理学的微小環境によく似た ex vivo 環境でこれらのパラメータの研究を可能にする方法を提示する。
いくつかのグループは、筋原性細胞を培養するためのin vitro法を報告しています。これらの方法は、サテライト細胞を単離して、その筋...
開示事項
著者は利益相反がないことを宣言します。
謝辞
図 2 では、Servier Medical Art (https://smart.servier.com/) のテンプレートを使用しました。FRラボは、Association Française contre les Myopathies - AFM via TRANSLAMUSCLE(助成金19507および22946)、Fondation pour la Recherche Médicale - FRM(EQU202003010217、ENV202004011730、ECO201806006793)、Agence Nationale pour la Recherche - ANR(ANR-21-CE13-0006-02、ANR-19-CE13-0010、ANR-10-LABX-73)、およびLa Ligue Contre le Cancer(IP/SC-17130)の支援を受けています。上記の資金提供者は、この研究のデザイン、収集、分析、解釈、報告、またはこの原稿の執筆に何の役割も果たしていませんでした。
資料
| Name | Company | Catalog Number | Comments |
| anti-CD31 | BD | 550274 | dilution 1:100 |
| anti-FOSB | Santa Cruz | sc-7203 | dilution 1:200 |
| anti-GFP | Abcam | ab13970 | dilution 1:1000 |
| anti-Ki67 | Abcam | ab16667 | dilution 1:1000 |
| anti-MyHC | DSHB | MF20-c | dilution 1:400 |
| anti-MYOD | Active Motif | 39991 | dilution 1:200 |
| anti-MYOG | Santa Cruz | sc-576 | dilution 1:150 |
| anti-Pax7 | Santa Cruz | sc-81648 | dilution 1:100 |
| anti-PDGFRα | Invitrogen | PA5-16571 | dilution 1:50 |
| b-FGF | Peprotech | 450-33 | concentration 4 ng/mL |
| bovine serum albumin (BSA) – used for digestion | Sigma Aldrich | A7906-1006 | concentration 0.2% |
| BSA IgG-free, protease-free – used for staining | Jackson ImmunoResearch | 001-000-162 | concentration 5% |
| cell strainer 40 um | Dominique Dutscher | 352340 | |
| cell strainer 70 um | Dominique Dutscher | 352350 | |
| cell strainer 100 um | Dominique Dutscher | 352360 | |
| Collagenase | Roche | 10103586001 | concentration 0.5 U/mL |
| Dimethyl sulfoxide (DMSO) | Euromedex | UD8050-05-A | |
| Dispase | Roche | 4942078001 | concentration 3 U/mL |
| Dissection forceps size 5 | Fine Science Tools | 91150-20 | |
| Dissection forceps size 55 | Fine Science Tools | 11295-51 | |
| Dissection scissors (big, straight) | Fine Science Tools | 9146-11 | ideal for chopping |
| Dissection scissors (small, curved) | Fine Science Tools | 15017-10 | |
| Dissection scissors (small, straight) | Fine Science Tools | 14084-08 | |
| Dulbecco's Modified Eagle's Medium (DMEM) | ThermoFisher | 41966-029 | |
| EdU Click-iT kit | ThermoFisher | C10340 | |
| Fetal bovine serum – option 1 | Eurobio | CVF00-01 | |
| Fetal bovine serum – option 2 | Gibco | 10270-106 | |
| Matrigel | Corning Life Sciences | 354234 | coating solution |
| Parafilm | Dominique Dutscher | 090261 | flexible film |
| Penicillin streptomycin | Gibco | 15140-122 | |
| Paraformaldehyde – option 1 | PanReac AppliChem ITW Reagents | 211511.1209 | concentration 4% |
| Paraformaldeyde – option 2 | ThermoFisher | 28908 | concentration 4% |
| Shaking water bath | ThermoFisher | TSSWB27 | |
| TritonX100 | Sigma Aldrich | T8532-500 ML | concentration 0.5% |
| Wild-type mice | Janvier | C57BL/6NRj |
参考文献
- Frontera, W. R., Ochala, J. Skeletal muscle: A brief review of structure and function. Calcified Tissue International. 96 (3), 183-195 (2015).
- Forcina, L., Cosentino, M., Musarò, A. Mechanisms regulating muscle regeneration: Insights into the interrelated and time-dependent phases of tissue healing. Cells. 9 (5), 1297 (2020).
- Mauro, A. Satellite cell of skeletal muscle fibers. Journal of Biophysical and Biochemical Cytology. 9 (2), 493-495 (1961).
- Lepper, C., Partridge, T. A., Fan, C. -. M. An absolute requirement for Pax7-positive satellite cells in acute injury-induced skeletal muscle regeneration. Development. 138 (17), 3639-3646 (2011).
- McCarthy, J. J., et al. Effective fiber hypertrophy in satellite cell-depleted skeletal muscle. Development. 138 (17), 3657-3666 (2011).
- Murphy, M. M., Lawson, J. A., Mathew, S. J., Hutcheson, D. A., Kardon, G. Satellite cells, connective tissue fibroblasts and their interactions are crucial for muscle regeneration. Development. 138 (17), 3625-3637 (2011).
- Sambasivan, R., et al. Pax7-expressing satellite cells are indispensable for adult skeletal muscle regeneration. Development. 138 (17), 3647-3656 (2011).
- Hicks, M. R., Pyle, A. D. The emergence of the stem cell niche. Trends in Cell Biology. 33 (22), 112-123 (2022).
- Relaix, F., et al. Perspectives on skeletal muscle stem cells. Nature Communications. 12 (1), 692 (2021).
- Gama, J. F. G., et al. Role of regulatory T cells in skeletal muscle regeneration: A systematic review. Biomolecules. 12 (6), 817 (2022).
- Loreti, M., Sacco, A. The jam session between muscle stem cells and the extracellular matrix in the tissue microenvironment. NPJ Regenerative Medicine. 7 (1), 16 (2022).
- Sambasivan, R., et al. Distinct regulatory cascades govern extraocular and pharyngeal arch muscle progenitor cell fates. Developmental Cell. 16 (6), 810-821 (2009).
- Pereira, P. D., et al. Quantification of cell cycle kinetics by EdU (5-ethynyl-2'-deoxyuridine)-coupled-fluorescence-intensity analysis. Oncotarget. 8 (25), 40514-40532 (2017).
- Bismuth, K., Relaix, F. Genetic regulation of skeletal muscle development. Experimental Cell Research. 316 (18), 3081-3086 (2010).
- Yin, H., Price, F., Rudnicki, M. A. Satellite cells and the muscle stem cell niche. Physiological Reviews. 93 (1), 23-67 (2013).
- Lertkiatmongkol, P., Liao, D., Mei, H., Hu, Y., Newman, P. J. Endothelial functions of platelet/endothelial cell adhesion molecule-1 (CD31). Current Opinion in Hematology. 23 (3), 253-259 (2016).
- Scholzen, T., Gerdes, J. The Ki-67 protein: From the known and the unknown. Journal of Cellular Physiology. 182 (3), 311-322 (2000).
- Abou-Khalil, R., Le Grand, F., Chazaud, B. Human and murine skeletal muscle reserve cells. Stem Cell Niche. 1035, 165-177 (2013).
- Pasut, A., Oleynik, P., Rudnicki, M. A. Isolation of muscle stem cells by fluorescence activated cell sorting cytometry. Methods in Molecular Biology. 798, 53-64 (2011).
- Liu, L., Cheung, T. H., Charville, G. W., Rando, T. A. Isolation of skeletal muscle stem cells by fluorescence-activated cell sorting. Nature Protocols. 10 (10), 1612-1624 (2015).
- Montarras, D., et al. Direct isolation of satellite cells for skeletal muscle regeneration. Science. 309 (5743), 2064-2067 (2005).
- Qu, Y., Edwards, K., Barrow, J. Isolation, culture, and use of primary murine myoblasts in small-molecule screens. STAR Protocols. 4 (2), 102149 (2023).
- Danoviz, M. E., Yablonka-Reuveni, Z. Skeletal muscle satellite cells: Background and methods for isolation and analysis in a primary culture system. Methods in Molecular Biology. 798, 21-52 (2011).
- Saclier, M., Theret, M., Mounier, R., Chazaud, B. Effects of macrophage conditioned-medium on murine and human muscle cells: analysis of proliferation, differentiation, and fusion. Methods in Molecular Biology. 1556, 317-327 (2017).
- Giordani, L., et al. High-dimensional single-cell cartography reveals novel skeletal muscle-resident cell populations. Molecular Cell. 74 (3), 609-621 (2019).
- Tabula Muris Consortium et al. Single-cell transcriptomics of 20 mouse organs creates a Tabula Muris. Nature. 562 (7727), 367-372 (2018).
- Brunetti, J., Koenig, S., Monnier, A., Frieden, M. Nanopattern surface improves cultured human myotube maturation. Skeletal Muscle. 11 (1), 12 (2021).
- Denes, L. T., et al. Culturing C2C12 myotubes on micromolded gelatin hydrogels accelerates myotube maturation. Skeletal Muscle. 9 (1), 17 (2019).
- LaFramboise, W. A., et al. Effect of muscle origin and phenotype on satellite cell muscle-specific gene expression. Journal of Molecular and Cellular Cardiology. 35 (10), 1307-1318 (2003).
- Azhar, M., Wardhani, B. W. K., Renesteen, E. The regenerative potential of Pax3/Pax7 on skeletal muscle injury. Journal of Generic Engineering and Biotechnology. 20 (1), 143 (2022).
- Hardy, D., et al. Comparative study of injury models for studying muscle regeneration in mice. PLoS One. 11 (1), e0147198 (2016).
転載および許可
このJoVE論文のテキスト又は図を再利用するための許可を申請します
許可を申請さらに記事を探す
This article has been published
Video Coming Soon
Copyright © 2023 MyJoVE Corporation. All rights reserved