Method Article
Tip 1 Diyabet, Çölyak Hastalıkları ve COVID-19 için Yüksek Verimli Çok Katlı Tarama
Bu Makalede
Özet
Tip 1 diyabet, çölyak hastalığı ve koronavirüs hastalığı 2019 için acil tarama ihtiyacı doğrultusunda, dört adacık otoantikorlarını, doku transglutaminaz otoantikorlarını ve şiddetli akut solunum sendromu koronavirüs 2'nin reseptör bağlanma alanına karşı antikorları aynı anda tespit etmek için yüksek verimli bir 6-Plex elektrokemilüminesans testi geliştirdik.
Özet
Devam eden bir klinik çalışma olan Çocuklar için Otoimmünite Taraması (ASK), Amerika Birleşik Devletleri'nde tip 1 diyabet (T1D) ve çölyak hastalığı için genel popülasyondaki ilk tarama çalışmasıdır. Koronavirüs hastalığı 2019 (COVID-19) pandemisi ile birlikte, genel popülasyonda COVID-19'un epidemiyolojisine ve COVID-19 enfeksiyonu ile T1D gelişimi arasındaki ilişki hakkında bilgiye acilen ihtiyaç duyulmaktadır. Radyo bağlama testinin (RBA) şu anda standart tarama yöntemi iki büyük zorluğu karşılamıştır: tek bir tahlil formatı ile düşük verimlilik ve taramada üretilen düşük afiniteli antikorların büyük bir kısmı ile düşük hastalık özgüllüğü. Daha önce kurduğumuz multipleks elektrokemilüminesans (ECL) testinin platformuyla, dört adacık otoantikorunun (IAbs) tümünü tek bir kuyucukta insülin, glutamik asit dekarboksilaz (GAD65), insülinoma antijeni 2 (IA-2) ve T1D için Çinko taşıyıcı 8 (ZnT8), çölyak hastalığı için transglutaminaz otoantikorları (TGA) ve şiddetli akut solunum sendromu koronavirüs 2 (SARS-CoV-2) reseptör bağlayıcı etki alanı (RBD) antikorlarına birleştiren yeni bir 6-Plex ECL testi geliştirilmiştir. COVID-19. Tahlil, 325 pozitif örnek ve 555 tüm antikor-negatif örnek dahil olmak üzere ASK çalışmasından 880 örnek kullanılarak kör olarak doğrulandı ve standart RBA'lar ve tek bir ECL testi ile karşılaştırıldı. Yüksek verimlilik, düşük maliyet ve düşük serum hacminin avantajları ile bu tahlil, ASK çalışması için birincil tarama aracı olarak kabul edilmiştir.
Giriş
Dünya çapında yapılan büyük epidemiyolojik çalışmalar, tip 1 diyabet (T1D) insidansının yılda %3-5 oranında hızla arttığını ve T1D prevalansının son 20 yılda, özellikle küçük çocuklarda iki katına çıktığını göstermektedir 1,2. Adacık otoantikorları (IAbs) genellikle klinik semptomlardan yıllar önce ortaya çıkar ve şu anda T1D3 için en güvenilir prediktif ve tanısal biyobelirteçlerdir. T1D otoantikorlarının taranması, klinik T1D'ye ilerleme riski taşıyan kişileri belirleyebilir, halkı eğitebilir, ketoasidozun hayatı tehdit eden komplikasyonunu büyük ölçüde azaltabilir ve önleme tedavileri için klinik çalışmalara fayda sağlayabilir. T1D için dünya çapında önleme çabaları devam etmektedir ve klinik T1D'ye ilerlemeyi geciktirmek için IAbs pozitif olan denekler arasında çoklu girişimsel çalışmalar yürütülmektedir ve Barbara Davis Diyabet Merkezi, 2016 yılında T1D ve çölyak hastalığı için genel popülasyonda taramanın ilk ABD klinik denemesini başlattı, Çocuklar için Otoimmünite Taraması (ASK)4 . Çölyak hastalığı (ÇH), immün ve genetik faktörlere bağlı kronik intestinal inflamatuar bir hastalıktır. T1D'li çocuklarda ÇH prevalansı %24,5'e kadar çıkabilir5. CD'li bireylerin yarısından fazlasında prezentasyon6'da tipik semptomlar olmayabilir, bu nedenle çölyak hastalığı için serolojik tarama oldukça gereklidir.
Koronavirüs hastalığı 2019 (COVID-19) pandemisinin başlamasından bu yana, dünya çapında 200 milyondan fazla vaka bildirilmiştir ve çocuklar laboratuvar tarafından doğrulanmış vakaların% 16'sını oluşturmaktadır7. Birçok çalışma, mevcut T1D'nin COVID-19 enfeksiyonu8'in ciddiyeti ve ölümü üzerindeki etkisini gösterirken, COVID-19 enfeksiyonunun T1D gelişimi üzerindeki etkisi açık değildir. Şiddetli akut solunum sendromu koronavirüs 2 (SARS-COV-2) antikorlarının belirlenmesi ve COVID-19 enfeksiyonu ile T1D otoimmünitesinin tetiklenmesi veya T1D progresyonunun hızlandırılması arasındaki ilişkinin incelenmesi ile genel popülasyonda COVID-19 enfeksiyonunun toplam oranının araştırılması acilen gerekli ve çok önemlidir, devam eden ASK çalışması ise bunun için mükemmel bir platformdur. Tek tahlil formatı ve büyük oranda düşük afiniteli antikor pozitifliğinin üretilmesi nedeniyle, standart radyo-bağlayıcı tahlil (RBA) düşük verimlilik ve düşük hastalık özgüllüğü9 darboğazını karşılamıştır. Bu yazıda, bir multipleks ECL test platformumuz üzerine inşa edilmiş, altı otoantikor testini tek bir kuyuda birleştiren, dört ana IAb'nin insülin (IAA), glutamik asit dekarboksilaz-65 (GADA), insülinoma antijen-2 (IA-2A) ve Çinko transport-8 (ZnT8A), çölyak hastalığı için transglutaminaza (TGA) otoantikorları da dahil olmak üzere tek bir kuyucukta birleştiren yeni bir 6-Plexed elektrokemilüminesans (ECL) testi sunuyoruz. ve SARS-CoV-2 reseptör bağlayıcı etki alanı (RBD) antikorları (COVID-19A). Bu, dört büyük IAbs'den oluşan eksiksiz bir paneli işe alan ve bunu TGA ve COVID-19A ile birleştiren ilk multipleks tahlildir. ASK çalışmasında standart RBA'nın yerini alan birincil tarama aracı olarak doğrulanmış ve resmi olarak kabul edilmiştir.
Protokol
Araştırma protokolü Colorado Çoklu Kurumsal İnceleme Kurulu tarafından onaylandı.
1. Tampon Hazırlama
- Etiketleme tamponunu hazırlayın (2x PBS, pH 7,9): 400 mL damıtılmış suya 100 mL 10x PBS ekleyin ve NaOH kullanarak pH'ı 7,9'a ayarlayın.
- 3 mM biyotin ve Ru Sulfo-NHS yapın: 588 μL etiketleme tamponunda 1 mg biyotin çözün ve 50 μL etiketleme tamponunda 150 nmol Ru Sulfo-NHS çözün.
- Antijen tamponunu hazırlayın (%1 BSA): 5 g sığır serum albümini (BSA) 500 mL 1x PBS'de çözün.
- Kaplama tamponunu hazırlayın (% 3 Bloker A): 15 g Bloker A'yı 500 mL 1x PBS'de çözün.
- İlk yıkama tamponunu hazırlayın (%0,05 Ara 20, PBST): 5.000 mL 1x PBS'de 2,5 mL Ara 20'yi karıştırın.
- İkinci yıkama tamponunu hazırlayın (0,4 M NaCl): 0,4 M NaCl çözeltisini yapmak için 575 mL damıtılmış suda 50 mL 5 M NaCl karıştırın.
NOT: Etkili etiketleme için, her zaman taze hazırlanmış biyotin ve Ru Sulfo-NHS çözeltilerini kullanın ve daha önce yapılmış olanları saklamayın.
2. Biotin ve Ru Sulfo-NHS ile ayrı ayrı antijen protein etiketlemesi
NOT: Daha yüksek etiketleme verimliliği için daha yüksek konsantrasyonda antijen proteini ≥0.5 mg/mL önerilir.
- Proinsülin, GAD-65, IA-2, ZnT8, TG ve SARS-CoV-2'nin spike proteininin reseptör bağlama alanı (RBD) dahil olmak üzere altı hedefli antijen protein çözeltisi hazırlayın. Her antijen proteininin benlerini moleküler ağırlığına göre hesaplayın ve uygun molar biyotin veya Ru Sulfo-NHS oranlarını yapın. Antijenin biyotin veya Ru Sulfo-NHS toplamına oranı, proinsülin proteini gibi küçük moleküler antijenler (moleküler ağırlık ≤10 kd) için 1: 5 olacaktır. ZnT8 gibi orta moleküler antijenler (moleküler ağırlık 10-50 kd) için oran 1:10'a ayarlanacaktır. GAD gibi büyük moleküler ağırlıklı antijenler (moleküler ağırlık >50 kd) için molar oran 1:20 olacaktır.
- Antijen proteinini iki eşit parçaya bölün ve adım 2.1'de hesaplanan molar oranı kullanarak ayrı ayrı biyotin ve Ru Sulfo-NHS ile karıştırın. Karışımı oda sıcaklığında (RT) 1,5 saat boyunca inkübe ederek ışıktan kaçının.
NOT: Antijen proteininin tamponundaki Tris veya glisin gibi tüm indirgeyici kimyasalların, 2x PBS (pH 7.9) tamponu ile astarlanmış bir boyutlandırma spin sütunu ile uzaklaştırılması gerekir. - Döndürme sütunlarını 2x PBS ile astarlayın (sıkma sütununun boyutu, 2 mL veya 5 mL, etiketleme antijen proteininin hacmine bağlıdır): Döndürme sütununa 1 ml 2x PBS tamponu ekleyin, 2 dakika boyunca 1.000 x g'de santrifüj edin ve adımı 2 kat daha tekrarlayın.
- Antijen protein-biyotin veya -Ru Sulfo-NHS karışımının, saflaştırmak ve etiketleme reaksiyonunu durdurmak için astarlanmış spin kolonundan 1x'ten (kolonu 2 dakika boyunca 1.000 x g'de santrifüj edin) geçmesine izin verin.
- Spin kolonlarından salınan etiketli antijen proteininin son hacmini ölçün, biyotin veya Ru Sulfo-NHS etiketli antijen proteininin konsantrasyonlarını hesaplayın. Etiketli antijen proteininin (50 μL / tüp) daha küçük alikotlarını yapın ve uzun süreli kullanım için -80 ° C'de saklayın.
NOT: Her spin kolonundan sonra proteinin kapsamı yaklaşık% 90 -% 95 tutma oranı olacaktır.
3. 6-Plex ECL testi (dama tahtası testi) için biyotin ve Ru Sulfo-NHS etiketli antijenler için en iyi konsantrasyonu ve oranları tanımlayın
NOT: Her antijen için dama tahtası testi, çoğullanmış teste entegre edilmeden önce gereklidir.
- Her antijen için dama tahtası testini ayrı ayrı uygulayın.
NOT: Adım 3.2.-3.7. TGA'yı kısa bir örnek olarak kullanacaktır. TGA dama tahtası tahlil süreci, tahlil işlemini simüle etmektir, ancak sadece bir tür antijen ile. - Biyotinile tTG ve Ru Sulfo-NHS etiketli tTG'nin seri seyreltmesini yapın. İlk karışım çözeltisinin önerilen çalışma konsantrasyonları, hem biyotinile edilmiş hem de Ru Sulfo-NHS etiketli tTG için 240 ng / mL'den başlar. Hem orijinal biyotinile edilmiş hem de Ru Sulfo-NHS etiketli tTG konsantrasyonlarının 1.0 μg / μL olduğunu varsayalım. Orijinal Ru Sulfo-NHS etiketli tTG'nin 10x seyreltilmesini ve% 5 BSA ile orijinal biyotinile tTG'nin 5x seyreltilmesini sağlayın.
- 4 μL biyotinile tTG proteinini 156 μL% 5 BSA (antijen tamponu) ve streptavidin konjuge bağlayıcının 240 μL'si ile bir tüpte karıştırın ve çözeltiyi RT'de 30 dakika inkübe edin. Ardından, 160 μL durdurma çözeltisi ekleyin ve RT'de 30 dakika daha inkübe edin. Karışımın 400 μL'sini alın ve 2 mL durdurma çözeltisi ile karıştırın. Biyotinile tTG'nin karışımdaki konsantrasyonu 240 ng/mL'dir.
- Biotin etiketli ZnT8 antijeni için seri seyreltme yapmak için, beş yeni tüp daha hazırlayın, adım 3.3'te karışımdan 1 mL aliquot alın. ve yeni bir tüpte 1 mL durdurma çözeltisi ile karıştırın ve karışımı 120 ng / mL'lik bir konsantrasyonla alın. Bu adımı tekrarlayın, seri 1: 1 seyreltmeler yapın ve biyotin etiketli tTG'yi 60 ng / mL, 30 ng / mL, 15 ng / mL ve 7.5 ng / mL'de alın.
- 1.6 mL durdurma çözeltisi ile 4 μL Ru Sulfo-NHS etiketli tTG ekleyin ve 240 ng / mL'lik bir konsantrasyonda Ru Sulfo-NHS etiketli tTG karışımı elde edin. Aynı 3.4. adımlarıyla, seri 1: 1 seyreltmeler yapın ve Ru Sulfo-NHS etiketli ZnT8 antijenini 60 ng / mL, 30 ng / mL, 15 ng / mL, 7.5 ng / mL ve 3.75 ng / mL'de alın. Son konsantrasyon 0 ng / mL'dir, sadece durdurma çözeltisi vardır ve Ru Sulfo-NHS etiketli antijen yoktur.
- tTG pozitif kontrol ve negatif kontrol serum örnekleri (tek bir ECL tTG testi ile önceden onaylanmış ve standartlaştırılmış) ve 96 delikli bir PCR plakası hazırlayın. Aliquot pozitif ve negatif kontrol serum örnekleri sırasıyla plakanın sol yarısına ve sağ yarısına, her bir kuyucukta 7 μL ile. Plakaya kuyucuk başına 33 μL ile 1x PBS ekleyin.
- PCR plakasının sol yarısında, her bir kuyucuğa, seri seyreltilmiş biyotin etiketli tTG-bağlayıcı çözeltisinin 24 μL'sini, en yüksekten en düşüğe doğru bir konsantrasyona sahip bir sütun ekleyin. Aynı şekilde, her bir kuyucuğa, bir konsantrasyonda bir sıra olan seri seyreltilmiş Ru Sulfo-NHS etiketli tTG antijeninin 16 μL'sini ekleyin ve ardından iyice karıştırın. PCR plakasının sağ yarısındaki adımı tekrarlayın.
- Adım 5.3.-9.1'de açıklanan tahlil adımlarının geri kalanına devam edin. ham sayım verileri elde edilene kadar.
- Pozitif kontrol sinyallerinin karşılık gelen negatif kontrol sinyallerine oranlarını hesaplayın. Negatif kontrol örneği için daha yüksek oran değerleri ve daha düşük arka plana sahip biyotin etiketli antijen ve Ru Sulfo-NHS etiketli antijen için en iyi konsantrasyonu belirleyin. Biotin ve Ru Sulfo-NHS etiketli antijen proteininin optimal çalışma konsantrasyonları aşağıda gösterilmiştir: GAD65 için 16.0 ng/mL ve 8.0 ng/mL, SARS-CoV-2 RBD için 18.8 ng/mL ve 9.4 ng/mL, IA-2 için 42.0 ng/mL ve 42.0 ng/mL, tTG için 60.0 ng/mL ve 60.0 ng/mL, ZnT8 için 4.2 ng/mL ve 4.2 ng/mL, ve proinsülin için 31.3 ng / mL ve 31.3 ng / mL.
4. Bağlayıcı bağlantılı antijen çözeltisi oluşturun
- Biotin ve Ru Sulfo-NHS etiketli antijenleri% 5 BSA ile adım 3.9'a göre optimum çalışma konsantrasyonlarına seyreltin.
- Önceden seçilmiş bağlayıcıları her bir biyotinile antijen proteinine bağlayın. Bir 96 kuyucuklu plaka testi için, 4 μL biyotinile GAD65, SARS-CoV-2 RBD, IA-2, tTG, ZnT8 ve proinsülin antijen proteinini% 1 BSA'nın 156 μL'sini içeren ayrı bir tüpe ekleyin ve karşılık gelen streptavidin-konjuge bağlayıcıların 240 μL'si ile karıştırın 1, 2, 3, 8, 9 ve 10 (Şekil 1). RT'de 30 dakika boyunca karışımı inkübe edin.
- Her tüpte 160 μL durdurma çözeltisi Aliquot ve karışımı RT'de 30 dakika boyunca inkübe edin. Her tüpten 400 μL karışım çözeltisini çıkarın ve bunları birleştirin.
- Yukarıdaki karışıma GAD65, SARS-CoV-2 RBD, IA-2, tTG, ZnT8 ve proinsülin antijeni etiketli 4 μL Ru Sulfo-NHS ekleyin ve ardından 1.6 mL durdurma çözeltisi ve 3.2 mL 1x PBS ekleyin ve karıştırın. Şimdi antijen çözeltisi tahlilde kullanıma hazırdır.
5. Serum örneklerini etiketli antijenle inkübe edin
- 96 delikli bir PCR plakası için kuyucuk başına 7 μL serum ve sızdırmazlık filmi ile örtün. Serumları 56 °C'de bir PCR makinesinde 30 dakika boyunca önceden ısıtın. Plakayı 1 dakika boyunca 100 x g'de kısaca santrifüj edin.
- Kuyucuk başına 63 μL antijen çözeltisi (adım 4.4'te hazırlanan) ekleyin ve serumlarla karıştırın. Işıktan kaçınmak için PCR plakasını sızdırmazlık folyosu ile örtün.
- Plakayı RT'de 450 rpm'de bir çalkalayıcı üzerinde 2 saat boyunca çalkalayın ve ardından plakayı 18-24 saat boyunca 4 ° C'de inkübe edin.
6. 6-Plex plakayı hazırlayın
- 4 °C buzdolabından 6-Plex plaka alın ve plakanın RT'ye gelmesine izin verin. 6-Plex plakanın her bir kuyucuğuna 150 μL% 3 Bloker A ekleyin.
- Plakayı tekrar 4 ° C buzdolabına koyun, plakayı ışıktan kaçınarak folyo ile örtün ve gece boyunca inkübe edin.
NOT: 1. Gündeki tahlil adımları bölüm 4.-6'yı içerir.
7. Serum/antijen inkübatörlerini 6-Plex plakaya aktarın
- Ertesi gün, inkübasyon 6-Plex plakasını buzdolabından alın ve tüm tamponu plakadan dışarı atın. Kuruması için tabağı kağıt havluların üzerine oturtun.
- 6-Plex plakayı her seferinde kuyucuk başına 150 μL yıkama tamponu ile 3x yıkayın. Tabağı kağıt havlular üzerinde kurutun ve aliquot serum/antijen, gece boyunca inkübe edilen PCR plakasının her bir kuyucuğundan 6-Plex plakanın iki kuyucuğuna inkübe edilir (kopyalar için kuyucuk başına 30 μL).
- Plakayı folyo ile örtün, ardından plakayı bir plaka çalkalayıcıya koyun ve RT'de 1 saat boyunca 450 rpm hızla çalkalayın.
8. 6-Plex plakayı yıkayın ve okuma tamponu ekleyin
- Çözeltiyi 6-Plex plakaya dökün ve plakayı her seferinde kuyucuk başına 150 μL 0,4 M NaCl yıkama tamponu ile 3x yıkayın.
- Üçüncü yıkama tamamlandıktan sonra, plakayı kağıt havluya karşı kurutun ve her bir oyuğa 150 μL okuma tamponu ekleyin.
NOT: Kuyudaki hava kabarcıkları, plaka okuyucu makinenin doğruluğunu etkiler ve ne pahasına olursa olsun kaçınılmalıdır.
9. Plakayı okuyun ve verileri analiz edin
- Bir elektrokemilüminesans analizöründeki plakayı sayın. Okuma sonuçları, saniye başına sayım (CPS) cinsinden değerlerle sunulacaktır. Okuma makinesinden elde edilen ham CPS'yi, her bir spesifik antikorun iç standart pozitif ve negatif kontrollerinin CPS'sine karşı kullanarak her bir numunenin göreceli antikor indeksini hesaplayın (İndeks değeri = [CPS (örnek) - CPS (negatif standart)] / [CPS (pozitif standart) - CPS (negatif standart)]).
- ASK çalışmasından alınan 555 negatif kontrol örneğinin 99.5. ila 99.8. persentillerinde (diyabet öyküsü veya aile öyküsü veya başka herhangi bir otoimmün hastalık öyküsü olmayan tüm antikorlar negatif örnekleri) belirlenen kesme değerlerini kullanarak negatif veya pozitif antikor sonuçlarını belirleyin.
NOT: 2. Gündeki tahlil adımları 7-9. bölümleri içerir.
Sonuçlar
Tablo 1, Tablo 2 ve Tablo 3 temsili sonuçları göstermektedir. Okuma makinesinden elde edilen ham CPS Tablo 1'de gösterilmiştir. Tablo 2'de, ham CPS altı bağlayıcı ve karşılık gelen antikorlar tarafından düzenlenmiş ve sıralanmıştır. Tablo 3, tahlil protokolünde açıklandığı gibi CPS ile hesaplanan indeks değerlerini göstermektedir. Kötü kopyaların neden olduğu yanlış nihai dizin sonuçlarını önlemek için tüm ham sayım değerleri kontrol edilmelidir. Tablo 1'de, Tablo 3'teki son dizin hesaplamasında hataya neden olan hatalı yineleme örnekleri verilmiştir.
Bu tahlil, 325 IAbs pozitif numune ve 555 tüm Abs negatif numune ile ASK çalışmasından seçilen 880 örnek kullanılarak kör bir şekilde doğrulanmıştır. 880 numune için 6-Plex ECL testinden elde edilen otoantikorların seviyeleri, karşılık gelen tek ECL tahlillerinin seviyeleri (Şekil 2) ve karşılık gelen tek standart RBA (Şekil 3) ile noktadan noktaya karşılaştırıldı. Her bir antikor için kesik, duyarlılık ve özgüllük Tablo 4'te listelenmiştir. Bu ECL-COVID-19A testinin duyarlılığı ve özgüllüğü sırasıyla %100 ve %99,9,10 olarak tanımlanmıştır.
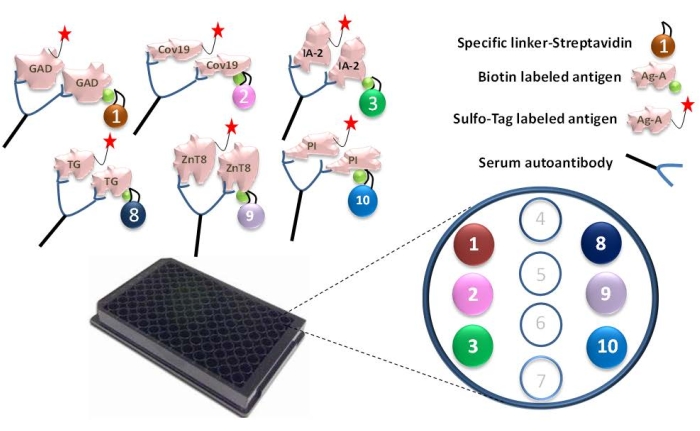
Resim 1: 6-Plex ECL testinin çizimi. Serum otoantikorları, Ru Sulfo-NHS etiketli antijenin, spesifik bir bağlayıcı ile birleştirilen ve bir antijen-antikor-antijen-bağlayıcı kompleksi oluşturan biyotinile antijene bağlanmasını sağlar. Kompleksler, her bir özel bağlayıcı aracılığıyla 6-Plex plakadaki belirli noktalara yakalanır. Her antijen için spesifik bağlayıcı numaraları atandı: GAD-linker-1, Covid-19-linker-2, IA-2-linker-3, tTG-linker-8, ZnT8-linker-9 ve Proinslulin-linker-10. Bu rakam He ve ark.11'in izniyle değiştirilmiştir. Bu şeklin daha büyük bir versiyonunu görüntülemek için lütfen buraya tıklayın.
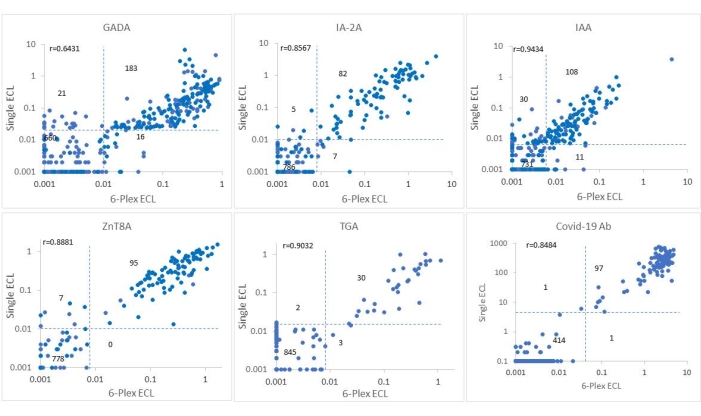
Şekil 2: ASK çalışmasından alınan 880 örnekte altı antikor seviyesinin tek ECL testi ile 6-Plex ECL testi arasında karşılaştırılması. Panellerde sırasıyla GADA, IAA, IA-2A, ZnT8A, TGA ve COVID-19A için antikor düzeylerinin karşılaştırmaları gösterilmektedir (COVID-19A indeksi (100 x hesaplanan indeks değeri) olarak sunulmuştur). Noktalı çizgiler, her antikor testi için tahlil kesiklerini temsil eder. Bu rakam He ve ark.11'in izniyle değiştirilmiştir. Bu şeklin daha büyük bir versiyonunu görüntülemek için lütfen buraya tıklayın.
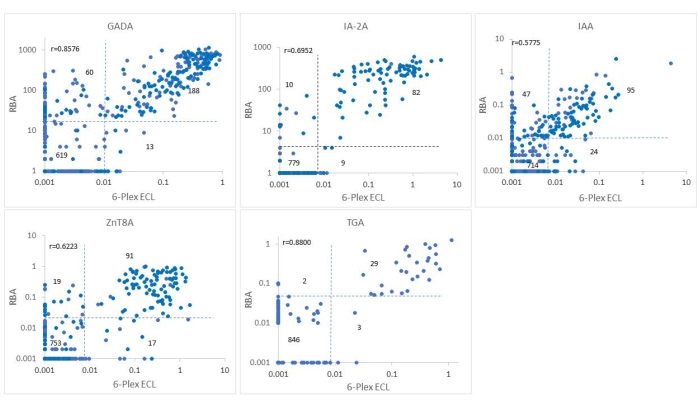
Şekil 3: RBA ve 6-Plex ECL testi arasındaki ASK çalışmasından 880 örnekte beş antikor seviyesinin karşılaştırılması. Paneller sırasıyla GADA, IAA, IA-2A, ZnT8A ve TGA için antikor seviyelerinin karşılaştırmalarını göstermektedir. Noktalı çizgiler, her antikor testi için tahlil kesiklerini temsil eder. Bu rakam He ve ark.11'in izniyle değiştirilmiştir. Bu şeklin daha büyük bir versiyonunu görüntülemek için lütfen buraya tıklayın.
Tablo 1: Ham CPS sayıları (plakanın sol yarısı). Ham CPS, bir tahlil plakasının sol yarısından elde edilen sayımlardır. Her örnek çift olarak gerçekleştirilir. Aynı sütundaki her CPS sayımı (A1, A2, A3, vb.) aynı kuyucuktaki 10 noktadan okuma verilerini temsil eder (karşılık gelen bağlayıcı sayıları işaretlenir). Hatalı yineleme örnekleri, satır D-linker 3 sütun 5 ve sütun 6'da görüldüğü gibi gri renkle vurgulanır. Bu tabloyu indirmek için lütfen tıklayınız.
Tablo 2: Altı bağlayıcı ile sıralanmış Tablo 1 verilerinin düzenlenmesi. Tablo 1'deki CPS değerleri, CPS'nin yinelenen okumaları için ortalama değerler hesaplanarak ve 4-7 bağlayıcıları için kullanılmayan değerler silinerek yeniden düzenlenmiştir. Her otoantikor testinin dahili standart yüksek pozitif, düşük pozitif ve negatif kontrollerinin değerleri koyu kalın olarak işaretlenmiştir. PC, pozitif kontrol. NC, negatif kontrol. Bu tabloyu indirmek için lütfen tıklayınız.
Tablo 3: Dizin değerlerinin sonuçları. Altı antikorun tümü için her numunenin indeks değerleri, karşılık gelen pozitif ve negatif kontrollere karşı hesaplandı. Kesme değerinden daha büyük bir endeks değeri, koyu kalın olarak işaretlenmiş pozitif olarak tanımlanmıştır. Tablo 1'deki hatalı yinelenen CPS değerleri, satır D-bağlayıcı 3-sütun 5 ve 6, örnek 11'in (gri renkle vurgulanmış) pozitif bir IA-2A dizin değerine yol açtı ve bu muhtemelen yanlış pozitif bir sonuçtu. Bu tabloyu indirmek için lütfen tıklayınız.
Tablo 4: 325 IAbs pozitif numune ve 555 tüm antikorlar negatif numune dahil olmak üzere 880 ASK numunesi arasında GADA, IA-2A, ZnT8A, IAA ve TGA için tahlil kesme, duyarlılık ve özgüllük. GADA, IA-2A, ZnT8A, IAA ve TGA testinin optimal kesme indeksi değeri, 555 normal kontrol örneğinin en az 99. yüzdelik dilimine ayarlanmıştır. Bu tabloyu indirmek için lütfen tıklayınız.
Tartışmalar
T1D'ye müdahale, T1D için devam eden ulusal ve uluslararası büyük ölçekli tarama programları ve klinik T1D 12,13'e ilerlemeyi iptal etmek veya yavaşlatmak için aşama 1 T1D'de uygulanan patlayan klinik çalışmalarlaT1D öncesi döneme girmiştir. Tek bir IAb tahlil formatına sahip mevcut standart RBA'yı kullanarak dört IAb'nin ölçülmesi, bir kitle tarama programı için zahmetli ve verimsizdir. Yüksek verimli çoklanmış IAbs testi, çoklanmış ECL testi, 3 Ekranlı ICA ELISA ve aglütinasyon-PCR (ADAP) ile antikor tespiti için acil talep ile şu anda rekabetçi teknolojiler olarak ortaya çıkmıştır. Almanya'daki küçük çocuk popülasyonunda T1D taramasının Fr1da çalışmasında, ana test14 olarak 3 IAb'yi (GADA, IA-2A ve ZnT8A) birleştiren 3 Ekranlı ICA ELISA kullanılmıştır. 3 Ekranlı ICA ELISA'nın önemli bir sınırlaması, çoğunlukla T1D'li küçük çocuklarda yüksek prevalansı olan ilk IAb olan IAA'nın olmamasıdır. Ayrıca, tahlil üç IAbs'den hangisinin pozitif bir sinyalden pozitif olduğunu ayırt edemez ve her pozitif numunenin onay için üç tek tahlille tekrarlanması gerekir. ADAP15, GADA, IA-2A ve IAA'yı birleştirir ve IASP çalıştayında yüksek tahlil duyarlılığı ve özgüllüğü göstermiştir, ancak IASP çalıştayının belirleyemediği T1D çalışmaları için popülasyon tabanlı taramada ne kadar öngörücü olduğuna dair verilerden yoksundur. Bu çalışmadaki multipleks ECL testi, TrailNet 9,16, DAISY 17,18,19 ve ASK 4,20,21 gibi çoklu klinik çalışmalarda mevcut standart RBA'ya karşı doğrulanmış tek bir ECL testinin platformu üzerine inşa edilmiştir. okumak. Mevcut tahlil, ASK çalışmasının katılımcılarından 880 serum örneği kullanılarak hem RBA hem de tek ECL testine karşı doğrulanmıştır. Şekil 2 ve Şekil 3'te gösterildiği gibi, 6-Plex ve tek ECL arasındaki veya 6-Plex ve RBA arasındaki antikor seviyeleri, antikorların pozitifliği için çoğunlukla birbirleriyle uyumluydu. RBA ve 6-Plex ile test edilen IAbs'lerin tesadüf oranları %91.7-97.8, tek ECL ve 6-Plex ile test edilen IAbs'lerin tesadüf oranları ise %95.3-%99.2 idi. ECL testi ve RBA arasındaki uyumsuzluk esas olarak tek IAb'li olanlardan kaynaklanıyordu. 6-Plex ve tek ECL (r = 0.6431-0.9434, tüm p < 0.0001) ve 6-Plex ve RBA (r = 0.5775-0.8576, tüm p < 0.0001) ile test edilen IAbs seviyeleri de iyi korelasyona sahipti. 6-Plex testi ile test edilen TGA, hem RBA (% 99.4) hem de tek ECL testinin (% 99.4) sonuçları ile yüksek oranda korelasyon göstermiştir. Ek olarak, 6-Plex tarafından test edilen COVID-19A, tek ECL testinin sonuçlarıyla %99,8 uyumluluğa ulaşmıştır.
Sonuç olarak, 6-Plex ECL testi, devam eden ASK çalışması için birincil tarama yöntemi olarak resmen kabul edilmiş ve standart RBA22'nin yerini almıştır. Bu test, standart RBA ile karşılaştırıldığında daha yüksek verim, daha düşük maliyet ve daha az serum hacmi ile mükemmel hassasiyetini ve özgüllüğünü göstermiştir.
T1D tarama çalışmasında, IAb pozitifliklerinin büyük bir bölümünü kaplayan RBA tarafından tespit edilen tek IAb'nin, düşük hastalık riski ile düşük afiniteye sahip olduğu ve genel olarak düşük prediktif değer 19,21,23,24,25,26 ile sonuçlandığı belgelenmiştir. Bu kadar düşük risk tahmini, takip ziyaretlerinin büyük ekstra maliyetlerine neden olmuş ve T1D önleyici çalışmalar için zorluklara neden olmuştur. Kurulan ECL tahlil platformu, RBA tarafından üretilen düşük afiniteli IAb'lerden yüksek afiniteli IAb'leri ayırt etmek ve özellikle tek IAb pozitifliği 16,17,18,21 ile dört IAb'nin tümü için öngörücü değerleri önemli ölçüde artırmak için birden fazla klinik çalışmada gösterilmiştir. . Multipleks ECL testi teknolojisi, yüksek afiniteli Abs'nin tespitinin bu belirgin avantajı ile tek ECL testinin platformu üzerine inşa edilmiştir. Bu çalışmada, 6-Plex ECL testi, duyarlılık ve özgüllük açısından karşılık gelen tek ECL testleri ile benzerliğini göstermiştir.
Birden fazla Plex plaka kullanan multipleks ECL testinin bazı sınırlamaları ve teknik kaygıları daha önceki yayınlarda zaten ele alınmıştır27,28. Bir kuyucukta altı etiketli antijen ile, farklı antijenler arasında bazı etkiler olabilir ve aynı kuyucukta çoklama için her bir antikor testi eklenirken tahlil arka planı artabilir. Tahlil koşullarını ayarlamak için, özellikle de her bir antijen için dama tahtası testine dayanan her etiketli antijen proteininin nihai konsantrasyonlarını ayarlamak için, her bir antikor testinin duyarlılığını ve özgüllüğünü korumak için büyük miktarda tahlil optimizasyonu çalışması gereklidir. Önceki çalışmalarda belirtildiği gibi27,28, az sayıda örnek (<%1), altta yatan açık bir neden olmaksızın çoklu Plex plakasında yanlış pozitifliğe neden olur. Tüm olumlu sonuçlar tekrarlanmalı ve rutin laboratuvar kalite güvencesi olarak tek bir ECL testi ile doğrulanmalıdır; genellikle, yanlış pozitifler kaldırılacaktır. Önceki 7-Plex ECL testi27,28'de gözlenen "prozon etkisinin" neden olduğu yanlış negatif sonuçlar bu çalışmada gözlenmemiştir. Burada açıklanan tahlilde, serum örneklerinin asit tedavisinin adımını önceki protokolden çıkardık; Bunun yerine, serum örneklerini 56 ° C'de 30 dakika boyunca önceden ısıttık (adım 5.1.). Plaka yıkamanın ikinci gününde, plakayı daha sıkı bir şekilde yıkamak için normal yıkama tamponu yerine 0,4 M NaCl (adım 8,1.) içeren bir yıkama tamponu kullandık. Bu değişiklikler, multipleks ECL testini daha basit hale getirdi ve tahlil hassasiyetini kaybetmeden arka planı alçalttı.
Sonuç olarak, bu tahlil aynı anda dört IAb, TGA ve COVID-19A'yı tespit etmek için olağanüstü bir performansa sahiptir. Çoklama özelliğinin yanı sıra yüksek verim, düşük maliyet ve küçük serum hacmi gereksinimi, T1D ve eşlik eden hastalıklar için büyük ölçekli taramayı genel popülasyonda çok daha uygulanabilir hale getirir. T1D veya herhangi bir otoimmün hastalığı olan hastalar diğer otoimmün hastalıklar için çok daha yüksek bir riske sahiptir. Multipleks ECL testi, T1D ve çoklu otoimmün hastalıkları aynı anda taramak için mükemmel bir platform sağlar.
Açıklamalar
Yazarların açıklayacak hiçbir şeyleri yoktur.
Teşekkürler
Çalışma JDRF hibe 2-SRA-2019-695-S-B, 2-SRA-2020-965-S-B, 1-SRA-2017-564-M_N, NIH hibe DK32083 ve Diyabet Araştırma Merkezi (DRC) hibe P30 DK116073 tarafından desteklenmiştir.
Malzemeler
| Name | Company | Catalog Number | Comments |
| 5 mM NaCl | ThermoFisher | 1070832 | |
| 96-well Plate Shaker | VWR | 12620-926 | |
| 96-well round bottom plate | Fisher | 8408220 | |
| Biotin | ThermoFisher | PI21329 | |
| Blocker A | MSD | R93AA | |
| Bottle-Top 500 ml-Filter Units | Fisher | 0974064A | |
| Bovine Serum Albumin | Sigma | A-7906 | |
| GAD65 protein | Diamyd Medical | 10-65702-01 | |
| IA-2 protein (aa 605-979) | Creative BioMart | 283309 | |
| MESO QuickPlex SQ120 | MSD | R31QQ-3 | Electrochemiluminescence analyzer |
| PBS 10x | ThermoFisher | 70011044 | |
| PBS 1x | ThermoFisher | 10010023 | |
| Proinsulin protein | AmideBio | 20160118B3 | |
| Read buffer B | MSD | Y0800019 | |
| SARS-CoV-2 RBD protein | Creative Biomart | Spike-190V | |
| Stop Solution | MSD | Y0090019 | |
| Sulfo-TAG | MSD | R91AO-1 | |
| tTG protein | Diarect AG | 15201 | |
| Tween 20 | Sigma | P-1379 | |
| U-Plex 6-Assay SECTOR plate | MSD | Z00U0142E | 6-plex plate |
| U-PLEX Linker 1 | MSD | L0010022 | |
| U-PLEX Linker 10 | MSD | L0100020 | |
| U-PLEX Linker 2 | MSD | L0020015 | |
| U-PLEX Linker 3 | MSD | L0030018 | |
| U-PLEX Linker 8 | MSD | L0080018 | |
| U-PLEX Linker 9 | MSD | L0090014 | |
| ZeBa Column | ThermoFisher | 89892 | Spin columns |
| ZnT8 protein | Research Laboratory | n/a |
Referanslar
- Group, T. S. The Environmental Determinants of Diabetes in the Young (TEDDY) Study. Annals of the New York Academy of Sciences. 1150, 1-13 (2008).
- Vehik, K., et al. Increasing incidence of type 1 diabetes in 0- to 17-year-old Colorado youth. Diabetes Care. 30 (3), 503-509 (2007).
- Insel, R. A., et al. Staging presymptomatic type 1 diabetes: a scientific statement of JDRF, the Endocrine Society, and the American Diabetes Association. Diabetes Care. 38 (10), 1964-1974 (2015).
- Stahl, M. G., et al. Mass screening for celiac disease: The autoimmunity screening for kids study. The American Journal of Gastroenterology. 116 (1), 180-187 (2021).
- Al-Hussaini, A., Sulaiman, N., Al-Zahrani, M., Alenizi, A., El Haj, I. High prevalence of celiac disease among Saudi children with type 1 diabetes: A prospective cross-sectional study. BMC Gastroenterology. 12, 180 (2012).
- Agardh, D., et al. Clinical features of celiac disease: A prospective birth cohort. Pediatrics. 135 (4), 627-634 (2015).
- COVID-19: Clinical manifestations and diagnosis in children. UpToDate Available from: https://www.uptodate.com/contents/covid-19-clinical-manifestations-and-diagnosis-in-children/print (2021)
- Barron, E., et al. Associations of type 1 and type 2 diabetes with COVID-19-related mortality in England: a whole-population study. The Lancet Diabetes & Endocrinology. 8 (10), 813-822 (2020).
- Miao, D., et al. Electrochemiluminescence assays for insulin and glutamic acid decarboxylase autoantibodies improve prediction of type 1 diabetes risk. Diabetes Technology & Therapeutics. 17 (2), 119-127 (2015).
- Jia, X., et al. Prevalence of SARS-CoV-2 antibodies in children and adults with Type 1 diabetes. Diabetes Technology & Therapeutics. 23 (7), 517-521 (2021).
- He, L., et al. High-throughput multiplex electrochemiluminescence assay applicable to general population screening for type 1 diabetes and celiac disease. Diabetes Technology & Therapeutics. , (2022).
- McQueen, R. B., et al. Cost and cost-effectiveness of large-scale screening for type 1 diabetes in Colorado. Diabetes Care. 43 (7), 1496-1503 (2020).
- Insel, R. A., Dunne, J. L., Ziegler, A. G. General population screening for type 1 diabetes: has its time come. Current Opinion in Endocrinology & Diabetes and Obesity. 22 (4), 270-276 (2015).
- Ziegler, A. G., et al. 3 Screen ELISA for high-throughput detection of beta cell autoantibodies in capillary blood. Diabetes Technology & Therapeutics. 18 (11), 687-693 (2016).
- Cortez, F. J., et al. Sensitive detection of multiple islet autoantibodies in type 1 diabetes using small sample volumes by agglutination-PCR. PLoS One. 15 (11), 0242049 (2020).
- Steck, A. K., et al. ECL-IAA and ECL-GADA can identify high-risk single autoantibody-positive relatives in the TrialNet pathway to prevention study. Diabetes Technology & Therapeutics. 18 (7), 410-414 (2016).
- Yu, L., et al. Proinsulin/Insulin autoantibodies measured with electrochemiluminescent assay are the earliest indicator of prediabetic islet autoimmunity. Diabetes Care. 36 (8), 2266-2270 (2013).
- Miao, D., et al. GAD65 autoantibodies detected by electrochemiluminescence assay identify high risk for type 1 diabetes. Diabetes. 62 (12), 4174-4178 (2013).
- Yu, L., et al. Distinguishing persistent insulin autoantibodies with differential risk: Nonradioactive bivalent proinsulin/insulin autoantibody assay. Diabetes. 61 (1), 179-186 (2012).
- Zhao, Z., et al. Higher sensitivity and earlier identification of celiac disease autoimmunity by a nonradioactive assay for transglutaminase autoantibodies. Journal of Immunology Research. 2016, 2904563 (2016).
- Jia, X., et al. High-affinity ZnT8 autoantibodies by electrochemiluminescence assay improve risk prediction for type 1 diabetes. The Journal of Clinical Endocrinology and Metabolism. 106 (12), 3455-3463 (2021).
- He, L., et al. A complete-panel islet autoantibody multiplex ECL assay. Diabetes. 70, 158 (2021).
- Achenbach, P., et al. Mature high-affinity immune responses to (pro)insulin anticipate the autoimmune cascade that leads to type 1 diabetes. Journal of Clinical Investigation. 114 (4), 589-597 (2004).
- Schlosser, M., et al. In insulin-autoantibody-positive children from the general population, antibody affinity identifies those at high and low risk. Diabetologia. 48 (9), 1830-1832 (2005).
- Mayr, A., et al. GAD autoantibody affinity and epitope specificity identify distinct immunization profiles in children at risk for type 1 diabetes. Diabetes. 56 (6), 1527-1533 (2007).
- Siljander, H., et al. Role of insulin autoantibody affinity as a predictive marker for type 1 diabetes in young children with HLA-conferred disease susceptibility. Diabetes/Metabolism Research and Reviews. 25 (7), 615-622 (2009).
- Gu, Y., et al. High-throughput multiplexed autoantibody detection to screen type 1 diabetes and multiple autoimmune diseases simultaneously. Ebiomedicine. 47, 365-372 (2019).
- Jia, X., He, L., Gu, Y., High, H., Yu, L. A high-throughput electrochemiluminescence 7-plex assay simultaneously screening for type 1 diabetes and multiple autoimmune diseases. Journal of Visualized Experiments. (159), e61160 (2020).
Yeniden Basımlar ve İzinler
Bu JoVE makalesinin metnini veya resimlerini yeniden kullanma izni talebi
Izin talebiThis article has been published
Video Coming Soon
JoVE Hakkında
Telif Hakkı © 2020 MyJove Corporation. Tüm hakları saklıdır