Method Article
SARS-CoV-2 Varyantlarının Hızlı Miktar Tayini ve Nötralize Edici Antikorlar için Ha-CoV-2 Psödovirüsünün Uygulanması
Bu Makalede
Özet
Bu protokol, SARS-CoV-2 varyantlarının enfektivitesinin ve nötralize edici antikorlara duyarlılıklarının hızlı bir şekilde ölçülmesi için bir platform olarak yeni bir hibrit alfavirüs-SARS-CoV-2 psödovirüsünün (Ha-CoV-2) uygulanmasını açıklar.
Özet
Koronavirüs hastalığı 2019 pandemisi (COVID-19), ortaya çıkan SARS-CoV-2 varyantlarının bulaşıcılığını ve aşı kaynaklı nötralize edici antikorların viral varyantlara karşı etkinliğini doğru bir şekilde ölçmek için hızlı tahlillere duyulan ihtiyacı vurguladı. Bu tahliller, pandemi sürveyansı ve aşıların ve varyanta özgü güçlendiricilerin doğrulanması için gereklidir. Bu makale, SARS-CoV-2 varyant enfektivitesinin ve viral varyantlara karşı aşı kaynaklı nötralize edici antikorların hızlı bir şekilde ölçülmesi için yeni bir hibrit alfavirüs-SARS-CoV-2 psödovirüsünün (Ha-CoV-2) uygulanmasını göstermektedir. Ha-CoV-2, viral yapısal proteinlerden (S, M, N ve E) ve bir alfavirüs olan Semliki Orman Virüsünden (SFV) türetilen hızlı eksprese eden bir RNA genomundan oluşan SARS-CoV-2 virüsü benzeri bir parçacıktır. Ha-CoV-2 ayrıca viral enfektivitenin hızlı bir şekilde ölçülmesine izin veren hem yeşil floresan proteini (GFP) hem de lusiferaz raportör genlerini içerir. Örnek olarak, SARS-CoV-2 Delta (B.1.617.2) ve Omicron (B.1.1.529) varyantlarının bulaşıcılığı ölçülür ve nötralize edici bir antikora (27VB) duyarlılıkları da ölçülür. Bu örnekler, SARS-CoV-2 varyantlarının hızlı bir şekilde ölçülmesi ve nötralize edici antikorlara duyarlılıkları için sağlam bir platform olarak Ha-CoV-2'nin büyük potansiyelini göstermektedir.
Giriş
Mayıs 2023 itibariyle, şu anda 766 milyondan fazla COVID-19 vakası olmuştur1. Dünya çapındaki aşılama kampanyalarına rağmen, SARS-CoV-2, büyük ölçüde Delta (B.1.617.2) ve Omicron (B.1.1.529) gibi yeni enfeksiyon dalgalarına neden olan yeni varyantların ortaya çıkması nedeniyle sürekli olarak dolaşır ve insanları enfekte eder 2,3,4. SARS-CoV-2'nin sürekli geliştiği göz önüne alındığında, ortaya çıkan varyantların bulaşıcılığını ve bu varyantlara karşı aşı kaynaklı nötralize edici antikorların etkinliğini doğru bir şekilde ölçebilen hızlı tahliller geliştirmek önemlidir. Bu tahliller, pandemik sürveyans ve aşıların ve varyanta özgü güçlendiricilerin etkinliğini belirlemek için gereklidir.
SARS-CoV-2'nin son derece bulaşıcı doğası nedeniyle, Hastalık Kontrol ve Önleme Merkezi (CDC), SARS-CoV-2 ve varyantlarının incelenmesinin biyogüvenlik seviyesi (BSL) 3 tesislerinde 5,6 yürütülmesini şart koşmaktadır. Bu BSL-3 gereksinimi, yaygın araştırma ve klinik laboratuvarlarda viral varyantların bulaşıcılığını ve bunların nötralize edici antikorlarını ölçmek için canlı virüslerin kullanımını sınırlar. Ek olarak, replikasyona yetkin canlı virüsler kullanan plak veya sitopatik etkiye dayalı testler gibi geleneksel SARS-CoV-2 nötralizasyon testleri zaman alıcıdır ve uzun kuluçka süreleri gerektirir7. Nötralize edici antikorların etkinliğini ölçmek için birkaç spike (S) proteini psödotipli SARS-CoV-2 psödovirüsügeliştirilmiştir 8,9,10,11,12. SARS-CoV-2'de S proteini, viral giriş13'e aracılık eden ana proteindir ve SARS-CoV-2 aşılarında kullanılan ana antijendir 9,10,14,15,16. Veziküler stomatit virüsü (VSV-G) veya lentivirüs gibi S proteini psödotipli viryonlar, nötralize edici antikorların 17,18,19 miktar tayini için kullanılmıştır. Bununla birlikte, lentivirüs bazlı psödovirüs, raportör sinyallerini ölçmek için normalde 2 ila 3 günlük enfeksiyon gerektirir. VSV tabanlı psödovirüs sistemleri genellikle yüksek oranda yanlış pozitif sonuçlara neden olabilen ve tipik olarak 24 saat enfeksiyon gerektiren kalıntı VSV virüsleri içerir20.
Yeni bir SARS-CoV-2 psödovirüs sistemi, hibrit alfavirüs-SARS-CoV-2 psödovirüsü (Ha-CoV-2), yakın zamanda Hetrick ve ark.12 tarafından geliştirilmiştir. Ha-CoV-2, yaygın BSL-2 laboratuvarlarında virüs enfektivitesinin ve nötralize edici antikorlara karşı virüs duyarlılığının hızlı bir şekilde ölçülmesi için yeni bir araç sağlar. Yapısal olarak Ha-CoV-2, S proteini (S), zar (M), nükleokapsid (N) ve zarf (E) dahil olmak üzere SARS-CoV-2 yapısal proteinlerinden oluşan SARS-CoV-2 virion partikülüne benzer ve diğer virüslerden yapısal protein yoktur. Ek olarak, Ha-CoV-2 partikülü, hücrelerde hızlı raportör ekspresyonu için bir alfavirüsten hızlı eksprese eden bir RNA genomu içerir. Ha-CoV-2'nin aşılanmış ve iyileşen bireylerin serumlarındaki antikorların nötralize edici aktivitesini hızlı bir şekilde ölçtüğü gösterilmiştir12. Hetrick ve arkadaşları tarafından gösterildiği gibi, bir zaman seyri tahlilinde lentivirüs bazlı SARS-CoV-2 psödovirüsü ile karşılaştırıldığında, Ha-CoV-2, Luc muhabirini enfeksiyondan 2-4 saat sonra eksprese ederken, lentivirüs-psödovirüs Luc'u 24 saat sonraeksprese etti 12. Ek olarak, nötralize edici antikorların miktarını belirlemek için Ha-CoV-2 varyantlarının potansiyel uygulaması, standart bir monoklonal nötralize edici antikor olan 27BV kullanılarak daha da gösterilmiştir ( Bkz. Ek Şekil 1)12. Bu çalışma, Delta (B.1.617.2) ve Omicron (B.1.1.529) varyantlarını örnek olarak kullanarak, SARS-CoV-2 varyantlarının bulaşıcılığının hızlı bir şekilde ölçülmesi için Ha-CoV-2 platformunun kullanımını detaylandırmaktadır. Ek olarak, nötralize edici antikorların miktarını belirlemek için Ha-CoV-2 varyantlarının potansiyel uygulaması, standart bir monoklonal nötralize edici antikor olan 27BV12 kullanılarak daha da gösterilmiştir.
Protokol
1. Virüs ve viral parçacık montajı
- Vektörler: SARS-CoV-2 M, E veya N'nin yanı sıra SARS-CoV-2 S (Vahşi tip, Wt), Delta (B.1.617.2) ve Omicron (B.1.1.529) için ticari olarak ekspresyon vektörleri satın alın.
NOT: Ekspresyon vektörlerinin protein dizileri Ek Dosya 1'de verilmiştir. Bu ifade vektörlerinin satıcısı Malzeme Tablosu altında da bulunabilir. - Hücreler ve hücre kültürü: Dulbecco'nun %10 ısıyla inaktive edilmiş fetal sığır serumu (FBS), 50 birim / mL penisilin ve 50 μg / mL streptomisin içeren modifiye Eagle ortamında (DMEM) HEK293T hücreleri koruyun.
NOT: Tüm hücre kültürü çalışmalarının laminer hava akımı biyogüvenlik kabininde yapılması gerekir. Polietilenimin (PEI) transfeksiyonu tipik olarak 5-6 saat inkübasyon gerektirir. Başlangıç zamanları önceden dikkatlice düşünülmelidir. - Virüs montajı ve PEI bazlı kotransfeksiyon: Ha-CoV-2 partiküllerini HEK293T hücrelerin birlikte transfeksiyonu ile birleştirin. Kotransfeksiyondan bir gün önce 10 mL tam DMEM ortamında 10 cm'lik bir hücre kültürü Petri kabında (tabak başına4-5 x 10 6 hücre) tohum hücreleri. Bu çalışma için, sırasıyla Ha-CoV-2 vahşi tip, Delta ve Omicron'un montajı için hücreleri tohumlamak için üç Petri kabı kullanılmıştır.
- Petri kaplarını gece boyunca 37 °C'de bir CO2 inkübatöründe inkübe edin. Hücrelerin %80 oranında birleştiğinden emin olmak için ertesi sabah bulaşıkları kontrol edin. Ortamın tamamını çıkarın ve 9 mL DMEM serumsuz besiyeri ile değiştirin.
- Her yemek için, SARS-CoV-2 yapısal protein ekspresyon vektörlerinin (N, E, M) her birinden 2,5 μg, 10 μg pAlphaPro-Luc-GFP-PreΨ (HaCoV2 Genomu) ve 2,5 μg S protein ekspresyon vektörü, Delta veya Omicron S varyantları ve 45 μL PEI bazlı transfeksiyon reaktifi içeren bir kotransfeksiyon karışımı hazırlayın. Kotransfeksiyon karışımının 13 dakika inkübe ederek kompleksler oluşturmasına izin verin (30 dakikadan fazla inkübe etmeyin).
- İnkübasyondan sonra, kotransfeksiyon karışımını her bir Petri kabına yavaşça, damla damla ekleyin. Bulaşıkları 37 °C'de 6 saat boyunca bir CO2 inkübatörüne yerleştirin. 6 saat sonra serumsuz DMEM'i çıkarın ve tam DMEM ortamı ile değiştirin. Kotransfeksiyondan 48-60 saat sonra virüsü hasat edin.
- Virüs toplama ve depolama: Kotransfeksiyondan 48 saat sonra parçacıkları hasat edin. Tek tabakanın yüzeyine tekrar tekrar pipetleyerek hücreleri ayırın ve her bir tabaktan hücreleri toplayın, 15 mL'lik santrifüj tüplerine koyun ve 5 dakika boyunca 400 x g'da santrifüjleyin. Süpernatanı toplayın ve 0.22 μM'lik bir filtreden geçirin. Ha-CoV-2 psödovirüsünü -80 °C'de saklayın.
2. Viral enfektivite testi
- Hücreler ve hücre kültürü: Dulbecco'nun %10 ısıyla etkisiz hale getirilmiş FBS, 50 birim / mL penisilin ve 50 μg / mL streptomisin içeren modifiye Eagle ortamında (DMEM) HEK293T (ACE2 / TMPRSS2) hücrelerini koruyun.
- Tohumlama HEK293T (ACE2 / TMPRSS2) hücreleri: Viral enfektivite testinden bir gün önce, 50 μL tam DMEM ortamında 96 oyuklu bir plakada tohum HEK293T (ACE2 / TMPRSS2) hücreleri. Her 96 oyuklu plaka için, her oyuğa 2,5 x 104 hücre tohumlayın ve bir plaka için toplam 2,5 x 106 hücre gerekir. 96 oyuklu plakayı gece boyunca 37 °C'de bir CO2 inkübatöre yerleştirin.
- HEK293T enfeksiyonu (ACE2 / TMPRSS2): HEK293T (ACE2 / TMPRSS2) hücrelerini enfekte etmek için Ha-CoV-2 varyant partiküllerini kullanın. Enfeksiyon sabahı, önceden tohumlanmış 96 oyuklu plakadan 50 μL DMEM çıkarın. Ortamı 37 °C'de 18 saat boyunca 50 μL Ha-CoV-2 Wild tipi, Delta veya Omicron ile değiştirin.
NOT: Enfeksiyon 18 saatlik inkübasyona ulaşana ve plaka Luciferaz Testi ile analiz edilmeye hazır olana kadar protokol burada durdurulabilir. Enfeksiyonun başarısı, enfekte hücrelerde eksprese edilen Luciferase raportör geninden kaynaklanan Luciferaz testi ile belirlenir, bu nedenle ne kadar çok sinyal üretilirse, Ha-CoV-2 varyantının enfeksiyonu o kadar başarılı olur. - Lusiferaz deneyi: 18 saatlik inkübasyondan sonra, her bir oyuğa doğrudan 7.5 μL hücre lizis tamponu ekleyin ve 2 dakika boyunca orbital çalkalayarak karıştırın. Lizis içindeki hücreler, oda sıcaklığında en az 5 dakika bekletilir.
- D-lusiferin çözeltisini Firefly lusiferaz test çözeltisi ile 1:50 oranında karıştırarak Firefly lusiferaz test çözeltisini hazırlayın. 96 oyuklu bir plaka için, 3 mL lusiferaz substrat çözeltisini 60 μL D-lusiferin çözeltisi ile 2940 μL Firefly lusiferaz tampon çözeltisi ile birleştirin.
- Hücre lizatlarına 25 μL Firefly lusiferaz tahlil çözeltisi ekleyin ve plakayı 1 dakika boyunca yörüngesel çalkalayarak karıştırın. Ticari bir lusiferaz mikroplaka okuyucu kullanarak lusiferaz aktivitesini analiz edin.
3. Ha-CoV-2 ve kantitatif ters transkriptaz PCR'nin (RT-qPCR) RNA ekstraksiyonu
- Viral RNA ekstraksiyonu: Üreticinin talimatlarını izleyerek ticari bir viral RNA ekstraksiyon kiti kullanarak Ha-CoV-2 Wild tipi ve Ha-CoV-2 Delta ve Omicron varyant parçacıklarından viral RNA'yı çıkarın. Ekstrakte edilen viral RNA'yı -80 °C'de saklayın veya RT-qPCR için hemen kullanın.
- RT-qPCR: Tek adımlı bir ana karışım kullanarak viral RNA üzerinde RT-qPCR gerçekleştirin. Reaksiyonu ticari bir PCR makinesinde gerçekleştirin. Amplifikasyon hedefinin Ha-CoV-2'nin genomik RNA'sı olduğunu lütfen unutmayın. Standart bir eğri oluşturmak ve her varyantın RNA kopya sayısını hesaplamak için standart olarak Ha-CoV-2 vektör DNA'sını kullanın.
4. Nötralize edici antikor testi
- Tohumlama HEK293T (ACE2 / TMPRSS2) hücreleri: Testten bir gün önce, 50 μL tam DMEM ortamında 96 oyuklu bir plakada HEK293T (ACE2 / TMPRSS2) hücrelerini tohumlayın. HEK293T (ACE2 / TMPRSS2) hücreleri ticari olarak satın alınır.
- Hücreleri saymak için, HEK293T (ACE2 / TMPRSS2) hücreleri içeren bir T75 şişesinden 20 μL hücre elde edin ve 20 μL tripan mavisi çözeltisi ile karıştırın. Bu karışımdan 20 μL'yi hücre sayma odasına ekleyin ve mL'deki hücre sayısını sayın. Enfeksiyon için 96 oyuklu bir plakayı tohumlamak için, oyuk başına 2,5 x 104 hücre kullanın ve toplamda 2,5 x 106 hücreye ihtiyaç duyulacaktır. 96 oyuklu plakayı gece boyunca 37 °C'de bir CO2 inkübatöre yerleştirin.
- Nötralize edici antikor testi: Steril bir polipropilen 96 oyuklu plakada, standart 27BV nötralize edici antikor ve Ha-CoV-2 karışımını hazırlayın. Plakaya 8 μL 27BV (45 mg / mL) ekleyin ve 6 μL serumsuz DMEM ile antikorun seri dilüsyonlarını gerçekleştirin.
NOT: Kuyu transferleri arasında pipet uçlarını değiştirdiğinizden ve doğru sonuçlar elde etmek için antikor ile serumsuz ortamın iyice karıştırıldığından emin olun. - Seri olarak seyreltilmiş antikora 54 μL Ha-CoV-2 partikülü ekleyin ve virüs ile antikoru karıştırın. Ha-CoV-2 partiküllerini seri olarak seyreltilmiş 27BV ile 37 °C'de %5 CO2'de 1 saat önceden inkübe edin. 1 saatlik inkübasyondan sonra, bir gün önce tohumlanan HEK293T (ACE2 / TMPRSS2) hücrelerini (oyuk başına 2.5 x 104 hücre) içeren 96 oyuklu plakaya 50 μL antikor ve Ha-CoV-2 karışımı uygulayın.
- Kontroller için, yalnızca HEK293T (ACE2 / TMPRSS2) hücrelerini içeren en az üç kuyu bırakın. Lusiferaz tahlil okumalarının arka plan sinyali için enfekte olmayan kuyucuklar olarak hizmet etmek üzere bu kuyucuklara 50 μL tam ortam ekleyin.
NOT: Enfeksiyon 37 ° C'de 18 saatlik inkübasyona ulaşana kadar protokol burada durdurulabilir ve daha sonra plaka lusiferaz testi ile analiz edilmeye hazır hale gelir. - Lusiferaz deneyi: 18 saatlik inkübasyondan sonra, her bir oyuğa doğrudan 7.5 μL lizis tamponu ekleyin ve 2 dakika boyunca yörüngesel çalkalayarak karıştırın. Lizis içindeki hücreler, oda sıcaklığında en az 5 dakika bekletilir.
- D-lusiferin çözeltisini Firefly lusiferaz test çözeltisi ile 1:50 oranında karıştırarak Firefly lusiferaz test çözeltisini hazırlayın. 96 oyuklu bir plakanın tamamı için, 3 mL lusiferaz substrat çözeltisini 60 μL D-lusiferin çözeltisi ile 2940 μL ateşböceği lusiferaz tampon çözeltisi ile birleştirin.
- Hücre lizatlarına 25 μL Firefly lusiferaz tahlil çözeltisi ekleyin ve plakayı 1 dakika boyunca yörüngesel çalkalayarak karıştırın. Ticari bir lusiferaz mikroplaka okuyucu kullanarak lusiferaz aktivitesini analiz edin.
5. Niceleme ve istatistiksel analiz
- Veri toplama: Enfeksiyon ve lusiferaz testlerini belirtildiği gibi üç kopya halinde gerçekleştirin (Şekil 1). Lusiferaz tahlil okumaları ile lusiferaz ekspresyonunu ölçün. Ortalama, üç lusiferaz tahlil okumasının ortalama değeridir. Enfekte olmayan kuyulardan alınan arka plan sinyal okumaları bu ortalama değerden çıkarılır. Standart sapma (SD), lusiferaz tahlil okumalarının ortalama değerinden belirlenir.
- Veri analizi: Ticari grafik yazılımı kullanarak antikor nötralizasyon aktivitesini çizin ve ID50 (%50 inhibisyon dozu) değerlerini hesaplayın. ID50 değeri, HEK293T (ACE2 / TMPRSS2) hücrelerinin enfeksiyonunda (lusiferaz test okumalarına dayanarak) %50'lik bir azalmanın elde edildiği antikor inhibitör dilüsyonları olarak tanımlanır.
Sonuçlar
Ha-CoV-2 parçacıkları, HEK293T hücrelerde Ha-CoV-2 RNA genomunu ve SARS-CoV-2'nin yapısal proteinlerini (M, N, E ve S) eksprese eden beş farklı DNA vektörü kullanılarak birleştirildi. S protein vektörü, S varyantına bağlı olarak değişir. Orijinal Ha-CoV-2 Wuhan suşundan (Wild tipi, Wt) elde edilen S proteini pozitif kontrol olarak kullanıldı ve diğer iki varyantın her birinden S proteini ile birlikte birleştirildi: Delta (B.1.617.2) veya Omicron (B.1.1.529). Tüm varyantlarda aynı M, N, E kullanılmıştır. Ha-CoV-2 (Wt) ve varyant partiküller, kotransfeksiyondan 48 saat sonra toplandı ve daha sonra HEK293T (ACE2 / TMPRSS2) hücrelerini enfekte etmek için kullanıldı. Enfektivite, enfeksiyondan 18 saat sonra lusiferaz ekspresyonu ile ölçüldü. Bu sistemde, lusiferaz sinyalinin daha yüksek ekspresyon seviyeleri, Ha-CoV-2 tarafından daha yüksek hücre enfeksiyonunu yansıtır. Lusiferaz sinyali, her varyant için RT-qPCR ile genomik RNA kopyaları ile normalize edildi. Şekil 1'de gösterildiği gibi, Ha-CoV-2 Omicron varyantı, orijinal Ha-CoV-2'den (Wt) 4 ila 10 kat daha yüksek sinyal üretti ve bu da daha yüksek bir bulaşıcılık olduğunu düşündürdü.
Ayrıca, 27BV'nin HaCoV-2(Wt), Delta ve Omicron varyantlarını nötralize etme kapasitesi ölçüldü. 27BV, SARS-COV-2 S1 proteininin RBD alanına karşı geliştirilmiş bir tavşan monoklonal antikorudur. Nötralizasyon deneyleri için, Ha-CoV-2 ile önceden inkübe edilmiş 96 oyuklu bir plakada 27BV'lik seri dilüsyonlar gerçekleştirildi ve daha sonra HEK293T (ACE2 / TMPRSS2) hedef hücrelerine eklendi. Sonuçlar, 27BV'nin test edilen tüm varyantlara karşı nötralize edici aktiviteye sahip olduğunu göstermiştir (Şekil 2). İlginç bir şekilde, Omicron için 27VB'nin ID50'si, Ha-CoV-2(WT) ve Ha-CoV-2(Delta; Şekil 2). Bu sonuçlar, Ha-COV-2 platformunun, ortaya çıkan varyantlarda aşı kaynaklı nötralize edici antikorların miktarını belirlemek için hızlı bir yöntem olarak kullanılabileceğini göstermektedir.
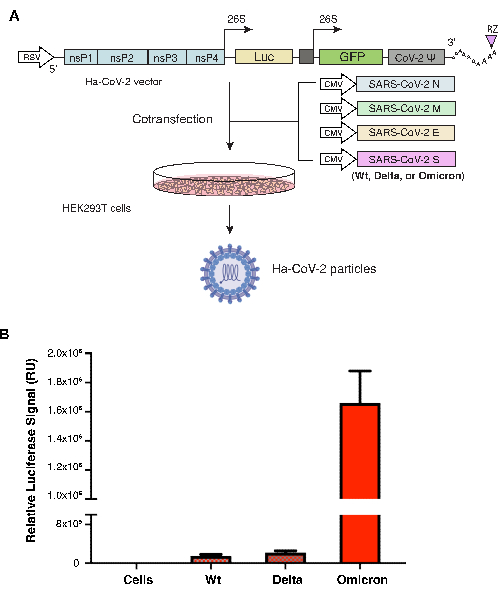
Şekil 1. Ha-CoV-2 varyantlarının montajı ve miktarının belirlenmesi. (A) Ha-CoV-2 ve varyant parçacıkların montajının gösterimi. Ha-CoV-2 raportör genomunu ve yapısal proteinleri (M, S, N ve E) eksprese eden vektörler HEK293T hücrelerde birlikte transfekte edilir. Parçacıklar, kotransfeksiyondan 48 saat sonra toplandı (virion partikülünün görüntülenmesi ve Biorender.com ile HEK293T hücreleri oluşturuldu). (B) Ha-CoV-2 varyantlarının enfektivitesinin ölçülmesi. İki varyantın (Delta ve Omicron) nispi enfektivitesi, bireysel Ha-CoV-2 (Luc) varyantlarının genomik RNA kopyaları kullanılarak ölçülür ve normalleştirilir. Vahşi tip, karşılaştırma için bir kontrol olarak kullanılan Ha-COV-2'dir (Wt). Enfeksiyon ve lusiferaz testleri 3x. RU, bağıl birim. Ortalama ve standart sapma (SD) gösterilir. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.
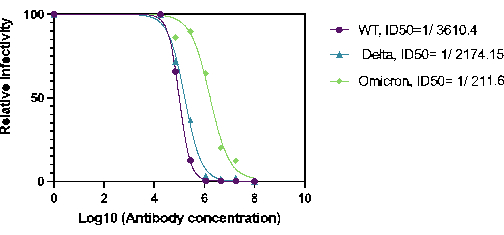
Şekil 2. Ha-CoV-2 (Luc) varyantlarına karşı 27BV nötralizasyon aktivitesinin ölçülmesi 27BV'nin nötralizasyon aktivitesi, HEK293T (ACE2 / TMPRSS2) hücrelerinin enfeksiyonundan 18 saat sonra analiz edildi. ID50 , 27BV konsantrasyonuna karşı nispi enfeksiyon oranı (lusiferaz aktivitesi) kullanılarak hesaplandı. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.
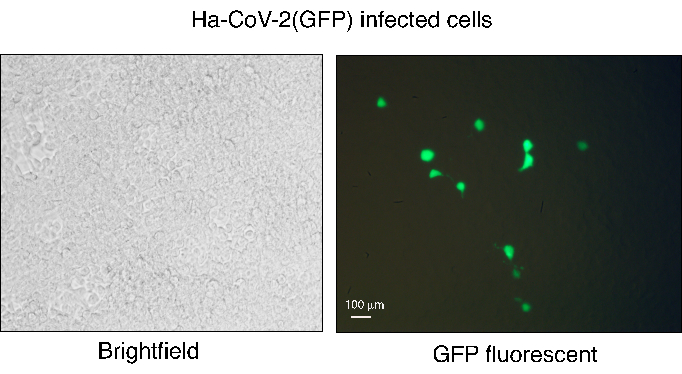
Şekil 3. HEK293T(ACE2/TMPRSS2)'nin Ha-CoV-2(GFP) ile enfeksiyonu. Ha-CoV-2 (GFP) partikülleri birleştirildi ve daha sonra HEK293T (ACE2 / TMPRSS2) hücrelerini enfekte etmek için kullanıldı. GFP ekspresyonu, floresan mikroskobu kullanılarak enfeksiyondan 48 saat sonra gözlendi. Enfekte hücrelerin beyaz alanı solda gösterilir ve GFP görüntüleme sağda gösterilir. Beyaz çubuk 100 μm'yi temsil eder. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.
Ek Şekil 1. Grafik Özet. Ha-CoV-2 psödovirüs yapısı ve uygulaması. Biorender.com ile oluşturulan görüntü. Bu Dosyayı indirmek için lütfen buraya tıklayın.
Ek Dosya 1. Protein Dizileri. SARS-CoV-2 S, M, N ve E proteinlerinin dizilerinin listesi. S protein dizileri ayrıca SARS-CoV-2 varyantları Omicron (B.1.1.529) ve Delta'yı (B.1.617.2) içerir. Bu Dosyayı indirmek için lütfen buraya tıklayın.
Tartışmalar
Ha-CoV-2 platformu, viral varyantları ölçmek ve antikorları nötralize etmek için hızlı, sağlam ve basit bir iş akışı sağlar. Ancak, dikkat edilmesi gereken birkaç kritik adım vardır. Ha-CoV-2 psödovirüsünün üretimi, yüksek canlılığa sahip HEK293T hücreleri kullanılarak gerçekleştirilmelidir. Kotransfeksiyon verimliliği, Ha-CoV-2 genomundan GFP raportör geni kullanılarak transfeksiyondan 24 saat sonra izlenebilir. Ha-CoV-2 genomu iki raportör (GFP ve Luc) içerebilir ve GFP, kotransfeksiyon sırasında ve hedef hücrelerin Ha-CoV-2 enfeksiyonunu takiben eksprese edilebilir12. Enfeksiyondan kaynaklanan GFP+ hücreleri normalde düşük bir yüzdededir (%1 ila %5), ancak enfekte olmuş her hücre güçlü GFP sinyalleri ifade eder (Şekil 3). Bu düşük GFP yüzdesi, enfekte olmuş hücrelerin tüm popülasyonunu ölçen Luc raportörü ile karşılaştırıldığında, antikor nötralizasyonunu ölçmek için GFP'nin sağlam bir okuma olarak kullanımını sınırlayabilir.
Nötralizasyon testini gerçekleştirirken, iyi transferler arasında pipet uçlarını değiştirmek ve doğru sonuçlar elde etmek için antikor ve serumsuz ortamın iyice karıştırıldığından emin olmak önemlidir. Ek olarak, lusiferaz test protokolünü yürütürken, hücrelerin tam olarak parçalanmasını ve lusiferaz enziminin salınmasını sağlamak için hücrelerin en az 3 dakika boyunca tamamen parçalanması gerekir. Bu, tahlilin doğruluğunu sağlayacaktır. Ek olarak, Ateşböceği lusiferaz tahlil çözeltisi optik beyaz duvarlı 96 kuyucuklu plakalara eklendikten sonra, ilk ışık emisyonu yüksek olduğundan ancak ATP tükendikçe zamanla azaldığından plaka 10 dakika içinde analiz edilmelidir21.
Daha fazla SARS-CoV-2 varyantı gelişmeye devam ettikçe, varyant bulaşıcılığını ve aşı kaynaklı nötralize edici antikorlara varyant duyarlılığını hızla taramak için Ha-CoV-2 gibi platformlara artan bir ihtiyaç vardır. Ha-CoV-2 platformu, mevcut psödovirüs tabanlı nötralizasyon testlerine kıyasla daha yüksek hız, daha yüksek sinyal-gürültü oranı ve basit bir protokol sunar 8,9,10,11. Ha-CoV-2 platformu ayrıca BSL-2 laboratuvarlarında kullanılabilmesi ve BSL-3 tesislerinin kullanılmasını gerektirmemesi avantajını da sunmaktadır. Bu, SARS-CoV-2'nin ortak araştırma ve klinik laboratuvarlarda sürdürülmesine izin verir. Ayrıca, Ha-CoV-2 platformu diğer sistemlere kıyasla hızlı sonuçlar üretir. Örneğin, bulaşıcı SARS-CoV-2 virüsüne karşı nötralize edici antikorların incelenmesi genellikle plak azaltma nötralizasyon testini (PRINT)22 kullanır. PRINT güvenilir sonuçlar vermesine rağmen, plak oluşturan birimlerin (PFU'lar) manuel sayımı yavaştır ve sonuçların elde edilmesi 3-5 gün sürer 23,24. Lentivirüs-psödovirüs gibi diğer psödotip sistemler, saptanabilir bir raportör sinyali üretmek için 24-72 saate ihtiyaç duyar12. Buna karşılık, Ha-CoV-2 nötralizasyon testi 18 saat içinde sonuç verebilir. Ha-CoV-2, viral varyantların hızlı taranması ve miktarının belirlenmesi ve pandemik izleme için antikorları nötralize etmek için uygun bir araç sağlar.
SARS-CoV-2'nin bulaşıcılığının izlenmesi, daha fazla endişe verici varyant (VOC) ortaya çıkmaya devam ettikçe çok önemlidir. Ha-CoV-2, VOC'lerin bulaşıcılığını hızlı bir şekilde belirleme avantajı sunar. Önceki çalışmalar, Omicron alt varyantının ve Delta varyantı25 gibi diğer SARS-CoV-2 varyantlarının bulaşıcılığını nicel olarak analiz etmek için yapay zeka (AI) tabanlı modelleme kullanmıştır. Bu çalışmalar, Omicron varyantının orijinal virüsten daha bulaşıcı olduğunu ve nötralize edici antikorlardan kaçma olasılığının daha yüksek olduğunu göstermiştir25. Bu çalışmalarda Ha-CoV-2 kullanılarak benzer fenotipler gözlenmiştir. Ek olarak, antikor nötralizasyon testlerinde, Omicron varyantının 27BV tarafından nötralize edilme olasılığı Wuhan ve Delta suşlarından on kat daha azdır. Bu sonuçlar aynı zamanda, reseptör bağlanma alanında (RBD) en az 15 mutasyona sahip olan Omicron varyantının bildirilen daha yüksek bulaşıcılığı ile tutarlıdır ve muhtemelen daha yüksek bulaşıcılık ve daha fazla bağışıklık kaçışı için ACE2 reseptörüne viral bağlanma afinitesini arttırır26.
Açıklamalar
George Mason Üniversitesi tarafından bir patent başvurusu yapıldı ve ürün geliştirme için Virongy Biosciences Inc.'e lisanslandı. YW, Virongy Biosciences'ın kurucusu ve danışma kurulu üyesidir. BH şu anda Virongy Biosciences'ın CEO'su ve Baş Bilim Sorumlusudur. Yazarların başka bir çıkar çatışması yoktur.
Teşekkürler
Bu çalışma George Mason Üniversitesi iç araştırma fonu tarafından desteklenmiştir.
Malzemeler
| Name | Company | Catalog Number | Comments |
| 27VB1 20 µg SARS-CoV-2 Standard Neutralizing Antibody | Virongy Biosciences | 27VBI-01 | |
| 500 mL - US Origin FBS | Neuromics | FBS001 | |
| AB Mixing Plate: Olympus 96-Well PCR Plate, Non-Skirted UltraThin Wall, Natural, 25 Plates/Unit | Genesee Scientific | Cat# 24-300 | |
| Allegra 6R Centrifuge | Beckman Coulter | 2043-30-1158 | |
| DMEM (1x) | ThermoFisher | 11995-073 | |
| GenClone 25-209, TC Treated Flasks, 250ml, Vent Growth Area: 75.0cm2, 5 per Sleeve, 100 Flasks/Unit | Genesee Scientfic | 25-209 | |
| GlowMax Discover Microplate reader | Promega | GM3000 | |
| Ha-CoV-2 E Vector | Virongy Biosciences | pCoV2_E | |
| Ha-CoV-2 M Vector | Virongy Biosciences | pCoV2_M | |
| Ha-CoV-2 N Vector | Virongy Biosciences | pCoV2_N | |
| Ha-CoV-2 WT S Vector | Virongy Biosciences | pCoV2_WT S | |
| Hek293T cells | ATCC | CRL-3214 | |
| Illumination Firefly Luciferase Enhanced Assay Kit 1000 assays | Gold Bio | I-930-1000 | |
| Infection Plate: 96-Well Tissue Culture Plate, Greiner Bio-One (With Lid, μClear White Flat Round, Chimney) | VWR | Cat# 82050-758 | |
| pAlphaPro-Luc-GFP-PreΨ (Ha-CoV-2 Genome) Vector | In house | ||
| PEI-based Transfection Reagent | Virongy Biosciences | Transfectin | |
| Penicillin-Streptomycin-Glutamine (100X) | Invitrogen | 10378016 | |
| Polyethylenimine, branched | Millipore Sigma | 408727-100ML | |
| QuantStudio 7 Pro Real-Time PCR System | ThermoFisher | A43163 | |
| Ready to use (HEK293T)(ACE2/TMPRSS2) Cells | Virongy Biosciences | Ready-To-Use-Cells | |
| SARS-CoV-2 S Omicron (B.1.1.529) Vector | Virongy Biosciences | pCoV2-B.1.1.529 | |
| SARS-CoV-2 S Delta (B.1.617.2) Vector | Virongy Biosciences | pCoV2- B.1.617.2 | |
| Syringe Filters, PES, 0.22µm | Genesee Scientfic | 25-244 | |
| TaqMan Fast Virus 1-Step Master Mix | ThermoFisher | 4444432 | |
| Trypan Blue Solution, 0.4% | ThermoFisher | 15250061 |
Referanslar
- World Health Organization. Weekly epidemiological update on COVID-19. 143, 1(2023).
- Dhama, K., et al. Global emerging Omicron variant of SARS-CoV-2: Impacts, challenges and strategies. Journal of Infection and Public Health. 16 (1), 4-14 (2023).
- Dhama, K., et al. Coronavirus Disease 2019-COVID-19. Clinical Microbiology Reviews. 33 (4), e00028-e00020 (2020).
- El-Shabasy, R. M., et al. Three waves changes, new variant strains, and vaccination effect against COVID-19 pandemic. International Journal of Biological Macromolecules. 204, 161-168 (2022).
- CDC. Interim laboratory biosafety guidelines for handling and processing specimens associated with coronavirus disease 2019 (COVID-19). , https://www.cdc.gov/coronavirus/2019-nCoV/lab/lab-biosafety-guidelines.html (2021).
- Kaufer, A., Theis, T., Lau, K., Gray, J., Rawlinson, W. Laboratory biosafety measures involving SARS-CoV-2 and the classification as a Risk Group 3 biological agent. Pathology. 52 (7), 790-795 (2020).
- Vanderheiden, A., et al. Development of a Rapid Focus Reduction Neutralization Test Assay for Measuring SARS-CoV-2 Neutralizing Antibodies. Current Protocols in Immunology. 131 (1), e116(2020).
- Dieterle, M. E., et al. A Replication-Competent Vesicular Stomatitis Virus for Studies of SARS-CoV-2 Spike-Mediated Cell Entry and Its Inhibition. Cell Host & Microbe. 28 (3), 486-496 (2020).
- Nie, J., et al. Quantification of SARS-CoV-2 neutralizing antibody by a pseudotyped virus-based assay. Nature Protocols. 15 (11), 3699-3715 (2020).
- Nie, J., et al. Establishment and validation of a pseudovirus neutralization assay for SARS-CoV-2. Emerging Microbes & Infections. 9 (1), 680-686 (2020).
- Yang, R., et al. Development and effectiveness of pseudotyped SARS-CoV-2 system as determined by neutralizing efficiency and entry inhibition test in vitro. Biosafety and Health. 2 (4), 226-231 (2020).
- Hetrick, B., et al. Development of a hybrid alphavirus-SARS-CoV-2 pseudovirion for rapid quantification of neutralization antibodies and antiviral drugs. Cell reports methods. 2 (3), 100181(2022).
- Jackson, C., Farzan, M., Chen, B., Choe, H. Mechanisms of SARS-CoV-2 entry into cells. Nature Reviews. Molecular Cell Biology. 23 (1), 3-20 (2022).
- Jackson, L. A., et al. An mRNA Vaccine against SARS-CoV-2 - Preliminary Report. The New England Journal of Medicine. 383 (20), 1920-1931 (2020).
- Polack, F. P., et al. Safety and Efficacy of the BNT162b2 mRNA Covid-19 Vaccine. The New England Journal of Medicine. 383 (27), 2603-2615 (2020).
- Li, F. Structure, function, and evolution of coronavirus spike proteins. Annual Review of Virology. 3 (1), 237-261 (2016).
- Donofrio, G. A Simplified SARS-CoV-2 Pseudovirus Neutralization Assay. Vaccines. 9 (4), 389(2021).
- Crawford, K. H. D., et al. Protocol and Reagents for Pseudotyping Lentiviral Particles with SARS-CoV-2 Spike Protein for Neutralization Assays. Viruses. 12 (5), 513(2020).
- Zettl, F., et al. Rapid Quantification of SARS-CoV-2-Neutralizing Antibodies Using Propagation-Defective Vesicular Stomatitis Virus Pseudotypes. Vaccines. 8 (3), 386(2020).
- Li, Q., Liu, Q., Huang, W., Li, X., Wang, Y. Current status on the development of pseudoviruses for enveloped viruses. Reviews in Medical Virology. 28 (1), e1963(2018).
- Lundin, A. Optimization of the firefly luciferase reaction for analytical purposes. Advances in Biochemical Engineering/Biotechnology. 145, 31-62 (2014).
- Deshpande, G. R., et al. Neutralizing antibody responses to SARS-CoV-2 in COVID-19 patients. The Indian Journal of Medical Research. 152 (1 & 2), 82-87 (2020).
- Chen, C., et al. Research progress in methods for detecting neutralizing antibodies against SARS-CoV-2. Analytical Biochemistry. 673, 115199(2023).
- Manischewitz, J., et al. Development of a novel vaccinia-neutralization assay based on reporter-gene expression. The Journal of Infectious Diseases. 188 (3), 440-448 (2003).
- Chen, J., Wang, R., Gilby, N., Wei, G. Omicron Variant (B.1.1.529): Infectivity, Vaccine Breakthrough, and Antibody Resistance. Journal of Chemical Information and Modeling. 62 (2), 412-422 (2022).
- Saxena, S. K., et al. Characterization of the novel SARS-CoV-2 Omicron (B.1.1.529) variant of concern and its global perspective. Journal of Medical Virology. 94 (4), 1738-1744 (2022).
Yeniden Basımlar ve İzinler
Bu JoVE makalesinin metnini veya resimlerini yeniden kullanma izni talebi
Izin talebiDaha Fazla Makale Keşfet
This article has been published
Video Coming Soon
JoVE Hakkında
Telif Hakkı © 2020 MyJove Corporation. Tüm hakları saklıdır