Method Article
Применение псевдовируса Ha-CoV-2 для быстрого количественного определения вариантов SARS-CoV-2 и нейтрализующих антител
В этой статье
Резюме
В этом протоколе описывается применение нового гибридного псевдовируса альфавируса SARS-CoV-2 (Ha-CoV-2) в качестве платформы для быстрой количественной оценки инфекционности вариантов SARS-CoV-2 и их чувствительности к нейтрализующим антителам.
Аннотация
Пандемия коронавирусной инфекции 2019 г. (COVID-19) выявила необходимость экспресс-анализов для точного измерения заразности новых вариантов SARS-CoV-2 и эффективности нейтрализующих антител, индуцированных вакциной, против вариантов вируса. Эти анализы необходимы для эпиднадзора за пандемией и валидации вакцин и бустерных доз, специфичных для конкретных вариантов. В данной статье демонстрируется применение нового гибридного псевдовируса альфавируса SARS-CoV-2 (Ha-CoV-2) для быстрой количественной оценки инфекционности варианта SARS-CoV-2 и индуцированных вакциной нейтрализующих антител к вариантам вируса. Ha-CoV-2 представляет собой вирусоподобную частицу SARS-CoV-2, состоящую из вирусных структурных белков (S, M, N и E) и генома РНК с быстрой экспрессией, полученного из альфавируса Семликского леса (SFV). Ha-CoV-2 также содержит зеленый флуоресцентный белок (GFP) и репортерные гены люциферазы, которые позволяют быстро количественно оценить инфекционность вируса. В качестве примера можно количественно оценить инфекционность вариантов SARS-CoV-2 Delta (B.1.617.2) и Omicron (B.1.1.529), а также измерить их чувствительность к нейтрализующим антителам (27VB). Эти примеры демонстрируют огромный потенциал Ha-CoV-2 в качестве надежной платформы для быстрого количественного определения вариантов SARS-CoV-2 и их восприимчивости к нейтрализующим антителам.
Введение
По состоянию на май 2023 г. в настоящее время зарегистрировано более 766миллионов случаев COVID-191. Несмотря на всемирные кампании вакцинации, SARS-CoV-2 постоянно циркулирует и заражает людей, в основном из-за появления новых вариантов, таких как «Дельта» (B.1.617.2) и «Омикрон» (B.1.1.529), которые вызывают новые волны инфекции 2,3,4. Учитывая, что SARS-CoV-2 постоянно эволюционирует, важно разработать быстрые тесты, которые могут точно измерить заразность новых вариантов и эффективность нейтрализующих антител, индуцированных вакциной, против этих вариантов. Эти анализы необходимы для эпиднадзора за пандемией и для определения эффективности вакцин и их бустерных доз, специфичных для конкретных вариантов.
Из-за высокой контагиозности SARS-CoV-2 Центр по контролю и профилактике заболеваний (CDC) требует, чтобы изучение SARS-CoV-2 и его вариантов проводилосьв учреждениях уровня биобезопасности (BSL) 3 5,6. Это требование BSL-3 ограничивает использование живых вирусов для количественной оценки заразности вариантов вируса и их нейтрализующих антител в обычных исследовательских и клинических лабораториях. Кроме того, традиционные анализы на нейтрализацию SARS-CoV-2, такие как анализы на основе бляшек или цитопатических эффектов с использованием репликационно-компетентных живых вирусов, отнимают много времени и требуют длительных инкубационных периодов7. Для количественной оценки эффективности нейтрализующих антител было разработано несколько псевдовирусов SARS-CoV-2 с псевдотипом спайкового (S) белка 8,9,10,11,12. В SARS-CoV-2 S-белок является основным белком, опосредующим проникновение вируса13, и основным антигеном, используемым в вакцинах против SARS-CoV-2 9,10,14,15,16. Псевдотипированные вирионы S-белка, такие как вирионы вируса везикулярного стоматита (VSV-G) или лентивируса, были использованы для количественного определения нейтрализующих антител 17,18,19. Тем не менее, псевдовирусу, основанному на лентивирусе, обычно требуется от 2 до 3 дней инфекции для количественной оценки репортерных сигналов. Псевдовирусные системы на основе VSV часто содержат остаточные вирусы VSV, что может привести к высокому уровню ложноположительных результатов и, как правило, требует24 ч заражения 20.
Новая псевдовирусная система SARS-CoV-2, гибридный альфавирус-псевдовирус SARS-CoV-2 (Ha-CoV-2), была недавно разработана Hetrick et al12. Ha-CoV-2 представляет собой новый инструмент для быстрой количественной оценки инфекционности вируса и чувствительности вируса к нейтрализующим антителам в обычных лабораториях BSL-2. Структурно Ha-CoV-2 напоминает вирионную частицу SARS-CoV-2, состоящую из структурных белков SARS-CoV-2, включая S-белок (S), мембрану (M), нуклеокапсид (N) и оболочку (E), и нет структурного белка у других вирусов. Кроме того, частица Ha-CoV-2 содержит быстро экспрессирующийся геном РНК альфавируса для быстрой репортерной экспрессии в клетках. Было показано, что Ha-CoV-2 быстро измеряет нейтрализующую активность антител в сыворотках вакцинированных и выздоравливающих лиц12. Как показали Hetrick et al., при сравнении с псевдовирусом SARS-CoV-2 на основе лентивируса в анализе с течением времени, Ha-CoV-2 экспрессировал репортера Luc уже через 2-4 ч после заражения, в то время как лентивирус-псевдовирус экспрессировал Luc через 24 ч12. Кроме того, потенциальное применение вариантов Ha-CoV-2 для количественного определения нейтрализующих антител дополнительно демонстрируется с использованием стандартного моноклонального нейтрализующего антитела 27BV (см. дополнительный рисунок 1)12. В данной работе подробно описывается использование платформы Ha-CoV-2 для быстрой количественной оценки инфекционности вариантов SARS-CoV-2 на примере вариантов «Дельта» (B.1.617.2) и «Омикрон» (B.1.1.529). Кроме того, потенциальное применение вариантов Ha-CoV-2 для количественного определения нейтрализующих антител дополнительно демонстрируется с использованием стандартного моноклонального нейтрализующего антитела 27BV12.
протокол
1. Сборка вирусов и вирусных частиц
- Переносчики: Приобретите векторы экспрессии для SARS-CoV-2 M, E или N, а также SARS-CoV-2 S (дикого типа, Wt), Delta (B.1.617.2) и Omicron (B.1.1.529) на коммерческой основе.
ПРИМЕЧАНИЕ: Белковые последовательности векторов экспрессии приведены в Дополнительном файле 1. Поставщика этих векторов выражений также можно найти в таблице материалов. - Клетки и клеточная культура: Поддерживайте HEK293T клеток в модифицированной среде Eagle's Medium (DMEM) Dulbecco, содержащей 10% термически инактивированную эмбриональную бычью сыворотку (FBS), 50 ЕД/мл пенициллина и 50 мкг/мл стрептомицина.
ПРИМЕЧАНИЕ: Все работы с клеточными культурами должны выполняться в шкафу биобезопасности с ламинарным воздушным потоком. Для трансфекции полиэтиленимина (PEI) обычно требуется 5-6 часов инкубации. Время начала необходимо тщательно продумать заранее. - Сборка вирусов и котрансфекция на основе PEI: Сборка частиц Ha-CoV-2 путем котрансфекции HEK293T клеток. Засевают клетки в чашку Петри с 10 см клеточной культуры (4-5 x 10,6 клеток в чашке) в 10 мл полной среды DMEM за день до котрансфекции. В этом исследовании три чашки Петри используются для посева клеток для сборки Ha-CoV-2 дикого типа, «Дельты» и «Омикрона» соответственно.
- Чашки Петри инкубируют в течение ночи в инкубатореСО2 при температуре 37 °C. На следующее утро проверьте посуду, чтобы убедиться, что ячейки сливаются на 80%. Удалите всю среду и замените ее 9 мл среды, не содержащей сыворотки DMEM.
- Для каждого блюда приготовьте смесь для котрансфекции с 2,5 мкг каждого из векторов экспрессии структурных белков SARS-CoV-2 (N, E, M), 10 мкг pAlphaPro-Luc-GFP-PreΨ (геном HaCoV2) и 2,5 мкг вектора экспрессии S-белка, вариантов Delta или Omicron S, и 45 мкл реагента для трансфекции на основе PEI. Дайте котрансфекционной смеси образовать комплексы, инкубируя в течение 13 мин (не инкубируйте дольше 30 мин).
- После инкубации медленно добавляйте котрансфекционную смесь в каждую чашку Петри, капля за каплей. Поместите посуду в инкубатор CO2 при температуре 37 °C на 6 ч. Через 6 ч удалите ДМЭМ без сыворотки и замените его полной средой ДМЭМ. Собирают вирус через 48-60 ч после котрансфекции.
- Сбор и хранение вирусов: Сбор частиц через 48 ч после котрансфекции. Отделите клетки путем многократного пипетирования по поверхности монослоя и соберите клетки из каждой чашки, поместите в центрифужные пробирки объемом 15 мл и центрифугируйте при 400 x g в течение 5 минут. Соберите надосадочную жидкость и пропустите ее через фильтр 0,22 мкМ. Храните псевдовирус Ha-CoV-2 при температуре -80 °C.
2. Анализ на вирусную заразность
- Клетки и клеточная культура: Поддерживайте клетки HEK293T(ACE2/TMPRSS2) в модифицированной среде Eagle's (DMEM) Dulbecco, содержащей 10% термоинактивированного FBS, 50 единиц/мл пенициллина и 50 мкг/мл стрептомицина.
- Посев клеток HEK293T(ACE2/TMPRSS2): За день до анализа на вирусную инфекционность высевают клетки HEK293T(ACE2/TMPRSS2) в 96-луночный планшет в 50 мкл полной среды DMEM. Для каждой 96-луночной пластины засейте 2,5 x 104 ячейки в каждую лунку, а всего для одной пластины необходимо 2,5 x 106 ячеек. Поместите 96-луночный планшет в инкубатор CO2 при температуре 37 °C на ночь.
- Инфекция HEK293T(ACE2/TMPRSS2): используйте частицы вариантов Ha-CoV-2 для заражения клеток HEK293T(ACE2/TMPRSS2). Утром в день заражения удалите 50 мкл DMEM из предварительно засеянной 96-луночной пластины. Замените носитель 50 мкл Ha-CoV-2 дикого типа, Delta или Omicron на 18 ч при 37 °C.
ПРИМЕЧАНИЕ: Протокол может быть остановлен здесь до тех пор, пока инфекция не достигнет 18 часов инкубации и планшет не будет готов к анализу с помощью люциферазного анализа. Успешность инфекции определяется методом люциферазы, полученным в результате экспрессии репортерного гена люциферазы в инфицированных клетках, поэтому чем больше сигнала вырабатывается, тем успешнее инфекция вариантом Ha-CoV-2. - Анализ люциферазы: После 18 ч инкубации добавьте 7,5 мкл буфера для лизиса клеток непосредственно в каждую лунку и перемешайте путем орбитального встряхивания в течение 2 мин. Лизируйте клетки в лизисном буфере не менее 5 мин при комнатной температуре.
- Приготовьте раствор люциферазы Firefly, смешав раствор D-люциферина с раствором люциферазы Firefly в соотношении 1:50. Для получения целой 96-луночной планшетной пластины смешайте 3 мл раствора субстрата люциферазы с 60 мкл раствора D-люциферина с 2940 мкл буферного раствора люциферазы Firefly.
- Добавьте 25 мкл раствора люциферазы Firefly к клеточным лизатам и перемешайте планшет орбитальным встряхиванием в течение 1 мин. Проанализируйте активность люциферазы с помощью коммерческого считывателя микропланшетов люциферазы.
3. РНК-экстракция Ha-CoV-2 и количественная ПЦР с обратной транскриптазой (ОТ-кПЦР)
- Экстракция вирусной РНК: Извлеките вирусную РНК из частиц Ha-CoV-2 дикого типа и Ha-CoV-2 вариантов Delta и Omicron с помощью коммерческого набора для экстракции вирусной РНК в соответствии с инструкциями производителя. Выделенную вирусную РНК хранят при температуре -80 °C или сразу используют для ОТ-кПЦР.
- ОТ-кПЦР: Проведите ОТ-кПЦР на вирусной РНК с использованием одноэтапной мастер-смеси. Проведите реакцию в коммерческом ПЦР-аппарате. Обратите внимание, что мишенью амплификации является геномная РНК Ha-CoV-2. Используйте векторную ДНК Ha-CoV-2 в качестве стандарта для создания стандартной кривой и вычисления числа копий РНК каждого варианта.
4. Анализ нейтрализующих антител
- Посев клеток HEK293T(ACE2/TMPRSS2): За день до анализа высевают клетки HEK293T(ACE2/TMPRSS2) в 96-луночный планшет в 50 мкл полной среды DMEM. Элементы HEK293T(ACE2/TMPRSS2) приобретаются в промышленных масштабах.
- Для подсчета клеток берут 20 мкл клеток из колбы Т75, содержащей HEK293T(ACE2/TMPRSS2) клетки, и смешивают с 20 мкл раствора трипанового синего. Добавьте 20 мкл этой смеси в камеру для подсчета клеток и подсчитайте количество клеток в мл. Чтобы засеять 96-луночную пластину для заражения, используйте 2,5 х 104 ячейки на лунку, а всего потребуется 2,5 х 106 клеток. Поместите 96-луночный планшет в инкубатор CO2 при температуре 37 °C на ночь.
- Анализ нейтрализующих антител: В стерильной полипропиленовой 96-луночной планшете приготовьте стандартную смесь нейтрализующих антител 27BV и Ha-CoV-2. Добавьте 8 мкл 27BV (45 мг/мл) в планшет и выполните серийные разведения антител с 6 мкл безсывороточного DMEM.
ПРИМЕЧАНИЕ: Обязательно меняйте наконечники пипеток между лунками и убедитесь, что антитела и среда, не содержащая сыворотки, тщательно перемешаны для получения точных результатов. - К серийно разведенному антителу добавляют 54 мкл частицы Ha-CoV-2 и смешивают вирус и антитело. Предварительную инкубацию частиц Ha-CoV-2 с последовательно разбавленным 27BV в течение 1 ч при 37 °C при 5% CO2. После 1 ч инкубации нанести 50 мкл смеси антител и Ha-CoV-2 на 96-луночный планшет, содержащий клетки HEK293T(ACE2/TMPRSS2) (2,5 x 104 клетки на лунку), высеянные накануне.
- Для контроля оставьте по крайней мере три лунки, содержащие только ячейки HEK293T(ACE2/TMPRSS2). Добавьте 50 мкл полной среды в эти лунки, чтобы они служили неинфицированными лунками для фонового сигнала показаний анализа люциферазы.
ПРИМЕЧАНИЕ: Протокол может быть остановлен до тех пор, пока инфекция не достигнет 18 часов инкубации при 37 °C, после чего планшет будет готов к анализу с помощью люциферазного анализа. - Анализ люциферазы: После 18 ч инкубации добавьте 7,5 мкл лизисного буфера непосредственно в каждую лунку и перемешайте путем орбитального встряхивания в течение 2 минут. Лизируйте клетки в лизисном буфере не менее 5 мин при комнатной температуре.
- Приготовьте раствор люциферазы Firefly, смешав раствор D-люциферина с раствором люциферазы Firefly в соотношении 1:50. Для получения целого 96-луночного планшета смешайте 3 мл раствора люциферазного субстрата с 60 мкл раствора D-люциферина с 2940 мкл буферного раствора люциферазы светлячка.
- Добавьте 25 мкл раствора люциферазы Firefly к клеточным лизатам и перемешайте планшет орбитальным встряхиванием в течение 1 мин. Проанализируйте активность люциферазы с помощью коммерческого считывателя микропланшетов люциферазы.
5. Количественная оценка и статистический анализ
- Сбор данных: Проведите анализ на инфекцию и люциферазу в трех экземплярах, как указано (рис. 1). Количественная оценка экспрессии люциферазы с помощью показаний анализа люциферазы. Среднее значение – это среднее значение трех показаний анализа люциферазы. Из этого среднего значения вычитаются показания фоновых сигналов от незараженных скважин. Стандартное отклонение (SD) определяется по среднему значению показаний люциферазного анализа.
- Анализ данных: Постройте график активности нейтрализации антител и рассчитайте значения ID50 (50% дозировка ингибирования) с помощью коммерческого программного обеспечения для построения графиков. Значение ID50 определяется как ингибирующие антитела разведения, при которых достигается 50%-ное снижение инфицирования клеток HEK293T(ACE2/TMPRSS2) (на основе показаний анализа люциферазы).
Результаты
Частицы Ha-CoV-2 были собраны с использованием пяти различных ДНК-векторов, экспрессирующих геном РНК Ha-CoV-2 и структурные белки (M, N, E и S) SARS-CoV-2 в HEK293T клетках. Вектор S-белка варьируется в зависимости от S-варианта. S-белок из оригинального уханьского штамма Ha-CoV-2 (Wild-type, Wt) был использован в качестве положительного контроля, и он был собран вместе с S-белком каждого из двух других вариантов: Дельта (B.1.617.2) или Омикрон (B.1.1.529). Одни и те же M, N, E использовались во всех вариантах. Ha-CoV-2(Wt) и его варианты собирали через 48 ч после котрансфекции, а затем использовали для инфицирования клеток HEK293T(ACE2/TMPRSS2). Инфекционность определяли по экспрессии люциферазы через 18 ч после заражения. В этой системе более высокие уровни экспрессии сигнала люциферазы отражают более высокую инфекцию клеток Ha-CoV-2. Сигнал люциферазы нормализовали копиями геномной РНК методом ОТ-кПЦР для каждого варианта. Как показано на рисунке 1, вариант Ha-CoV-2 «Омикрон» генерировал в 4–10 раз более высокий уровень сигнала, чем исходный вариант Ha-CoV-2(Wt), что свидетельствует о более высокой заразности.
Кроме того, была проведена количественная оценка способности 27BV нейтрализовать варианты HaCoV-2(Wt), «Дельта» и «Омикрон». 27BV представляет собой моноклональное антитело кролика, которое было разработано против домена RBD белка SARS-COV-2 S1. Для нейтрализации проводили серийные разведения 27BV в 96-луночном планшете, предварительно инкубировали с Ha-CoV-2, а затем добавляли к клеткам-мишеням HEK293T(ACE2/TMPRSS2). Результаты показали, что 27BV обладает нейтрализующей активностью в отношении всех протестированных вариантов (рис. 2). Интересно, что ID50 27VB для Омикрона был примерно в 10 раз менее мощным, чем ID50 для Ha-CoV-2(WT) и Ha-CoV-2 (Delta; Рисунок 2). Эти результаты показывают, что платформа Ha-COV-2 может быть использована в качестве быстрого метода количественной оценки вакциноиндуцированных нейтрализующих антител в новых вариантах.
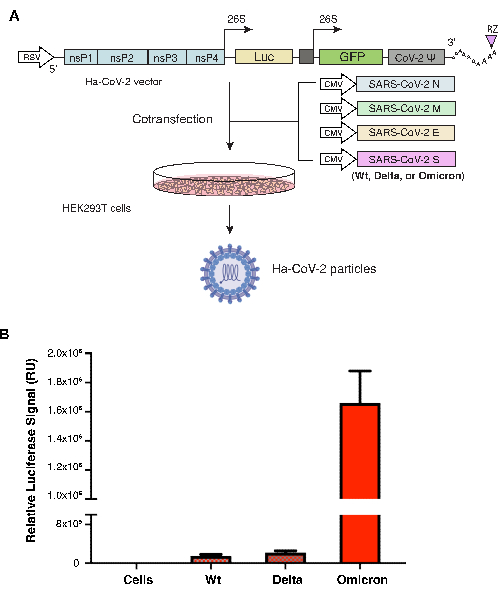
Рисунок 1. Сборка и количественное определение вариантов Ha-CoV-2. (А) Иллюстрация сборки Ha-CoV-2 и вариантных частиц. Векторы, экспрессирующие репортерный геном Ha-CoV-2 и структурные белки (M, S, N и E), котрансфицируются в HEK293T клетках. Частицы собирали через 48 ч после котрансфекции (визуализация вирионных частиц и HEK293T клеток создавалась с помощью Biorender.com). (B) Количественная оценка инфекционности вариантов Ha-CoV-2. Относительная инфекционность двух вариантов («Дельта» и «Омикрон») количественно оценивается и нормализуется с использованием геномных РНК-копий отдельных вариантов Ha-CoV-2 (Luc). Диким типом является Ha-COV-2 (Wt), который используется в качестве контроля для сравнения. Анализы на инфекцию и люциферазу проводили 3x. RU, относительная единица. Показаны среднее значение и стандартное отклонение (SD). Пожалуйста, нажмите здесь, чтобы увидеть увеличенную версию этого рисунка.
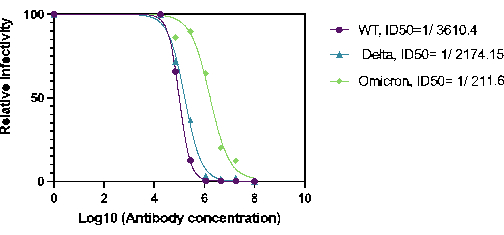
Рисунок 2. Количественная оценка нейтрализующей активности 27BV в отношении вариантов Ha-CoV-2(Luc) Нейтрализующая активность 27BV была проанализирована через 18 ч после инфицирования клеток HEK293T(ACE2/TMPRSS2). ID50 был рассчитан с использованием относительной частоты инфицирования (активности люциферазы) в зависимости от концентрации 27BV. Пожалуйста, нажмите здесь, чтобы увидеть увеличенную версию этого рисунка.
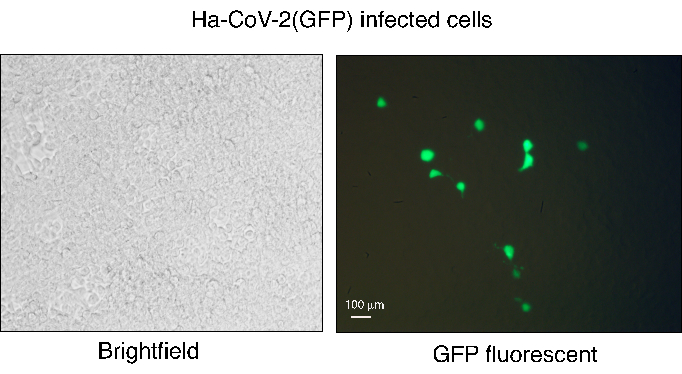
Рисунок 3. Инфицирование HEK293T(ACE2/TMPRSS2) Ha-CoV-2 (GFP). Частицы Ha-CoV-2 (GFP) были собраны, а затем использованы для заражения клеток HEK293T(ACE2/TMPRSS2). Экспрессию GFP наблюдали через 48 ч после заражения с помощью флуоресцентной микроскопии. Слева показано белое поле инфицированных клеток, а справа — GFP-изображение. Белая полоса соответствует 100 мкм. Пожалуйста, нажмите здесь, чтобы увидеть увеличенную версию этого рисунка.
Дополнительный рисунок 1. Графическая аннотация. Структура и применение псевдовируса Ha-CoV-2. Изображение создано с помощью Biorender.com. Пожалуйста, нажмите здесь, чтобы скачать этот файл.
Дополнительный файл 1. Белковые последовательности. Список последовательностей S, M, N и E-белков SARS-CoV-2. Последовательности S-белка также включают варианты SARS-CoV-2 «Омикрон» (B.1.1.529) и «Дельта» (B.1.617.2). Пожалуйста, нажмите здесь, чтобы скачать этот файл.
Обсуждение
Платформа Ha-CoV-2 обеспечивает быстрый, надежный и простой рабочий процесс для количественной оценки вариантов вируса и нейтрализации антител. Тем не менее, есть несколько важных шагов, на которые следует обратить внимание. Производство псевдовируса Ha-CoV-2 должно осуществляться с использованием HEK293T клеток с высокой жизнеспособностью. Эффективность котрансфекции можно контролировать через 24 ч после трансфекции с помощью репортерного гена GFP из генома Ha-CoV-2. Геном Ha-CoV-2 может содержать двух репортеров (GFP и Luc), а GFP может экспрессироваться во время котрансфекции и после заражения клетками-мишенями Ha-CoV-212. Инфицированные клетки GFP+ обычно имеют низкий процент (от 1% до 5%), но каждая инфицированная клетка экспрессирует сильные сигналы GFP (рис. 3). Этот низкий процент GFP может ограничивать использование GFP в качестве надежного индикатора для количественной оценки нейтрализации антител по сравнению с репортером Luc, который количественно оценивает всю популяцию инфицированных клеток.
При выполнении анализа на нейтрализацию важно менять наконечники пипеток между переносами лунок и следить за тем, чтобы антитела и среда, не содержащая сыворотки, тщательно смешивались для получения точных результатов. Кроме того, при проведении протокола анализа люциферазы клетки должны быть полностью лизированы в течение не менее 3 мин, чтобы обеспечить полный лизис клеток и высвобождение фермента люциферазы. Это обеспечит точность анализа. Кроме того, после того, как раствор люциферазы Firefly добавляется к оптическим белым стенкам на 96-луночные планшеты, планшет должен быть проанализирован в течение 10 минут, так как начальное световое излучение высокое, но уменьшается со временем по мере истощения АТФ21.
По мере того, как все больше вариантов SARS-CoV-2 продолжают эволюционировать, возрастает потребность в таких платформах, как Ha-CoV-2, для быстрого скрининга на инфекционность вариантов и чувствительность вариантов к нейтрализующим антителам, индуцированным вакциной. Платформа Ha-CoV-2 обеспечивает более высокую скорость, более высокое соотношение сигнал/шум и простой протокол по сравнению с существующими анализами нейтрализации на основе псевдовирусов 8,9,10,11. Преимущество платформы Ha-CoV-2 также заключается в том, что она может использоваться в лабораториях BSL-2 и не требует использования установок BSL-3. Это позволяет проводить исследования SARS-CoV-2 в обычных исследовательских и клинических лабораториях. Кроме того, платформа Ha-CoV-2 дает более быстрые результаты по сравнению с другими системами. Например, при исследовании нейтрализующих антител против инфекционного вируса SARS-CoV-2 часто используется тест нейтрализации бляшек (PRINT)22. Несмотря на то, что PRINT дает надежные результаты, ручной подсчет зубеобразующих единиц (ГОУ) выполняется медленно и требует 3-5 дней для получения результатов23,24. Другим системам псевдотипов, таким как лентивирус-псевдовирус, требуется 24-72 ч для получения обнаруживаемого репортерного сигнала12. Для сравнения, анализ нейтрализации Ha-CoV-2 может дать результаты в течение 18 часов. Ha-CoV-2 представляет собой удобный инструмент для быстрого скрининга и количественной оценки вариантов вируса и нейтрализующих антител для мониторинга пандемии.
Мониторинг заразности SARS-CoV-2 имеет важное значение в связи с появлением новых вариантов, вызывающих озабоченность (ЛОС). Преимущество Ha-CoV-2 заключается в быстром определении инфекционности летучих органических соединений. В предыдущих исследованиях использовалось моделирование на основе искусственного интеллекта (ИИ) для количественного анализа заразности подварианта «Омикрон» и других вариантов SARS-CoV-2, таких как вариант «Дельта»25. Эти исследования показали, что вариант «Омикрон» более заразен, чем исходный вирус, и с большей вероятностью избегает нейтрализующих антител25. В этих исследованиях с использованием Ha-CoV-2 наблюдались сходные фенотипы. Кроме того, в анализах нейтрализации антител вероятность того, что вариант «Омикрон» будет нейтрализован штаммом 27BV, в десять раз ниже, чем штаммы «Ухань» и «Дельта». Эти результаты также согласуются с сообщениями о более высокой трансмиссивности варианта «Омикрон», который имеет не менее 15 мутаций в своем рецептор-связывающем домене (RBD), что, вероятно, повышает сродство связывания вируса с рецептором ACE2 для более высокой трансмиссивности и большего иммунного уклонения26.
Раскрытие информации
Патент был подан Университетом Джорджа Мейсона и лицензирован компанией Virongy Biosciences Inc. на разработку продукта. Y.W. является основателем и членом консультативного совета Virongy Biosciences. В настоящее время Б. Х. является генеральным директором и главным научным сотрудником Virongy Biosciences. Других конфликтов интересов у авторов нет.
Благодарности
Эта работа была поддержана внутренним исследовательским фондом Университета Джорджа Мейсона.
Материалы
| Name | Company | Catalog Number | Comments |
| 27VB1 20 µg SARS-CoV-2 Standard Neutralizing Antibody | Virongy Biosciences | 27VBI-01 | |
| 500 mL - US Origin FBS | Neuromics | FBS001 | |
| AB Mixing Plate: Olympus 96-Well PCR Plate, Non-Skirted UltraThin Wall, Natural, 25 Plates/Unit | Genesee Scientific | Cat# 24-300 | |
| Allegra 6R Centrifuge | Beckman Coulter | 2043-30-1158 | |
| DMEM (1x) | ThermoFisher | 11995-073 | |
| GenClone 25-209, TC Treated Flasks, 250ml, Vent Growth Area: 75.0cm2, 5 per Sleeve, 100 Flasks/Unit | Genesee Scientfic | 25-209 | |
| GlowMax Discover Microplate reader | Promega | GM3000 | |
| Ha-CoV-2 E Vector | Virongy Biosciences | pCoV2_E | |
| Ha-CoV-2 M Vector | Virongy Biosciences | pCoV2_M | |
| Ha-CoV-2 N Vector | Virongy Biosciences | pCoV2_N | |
| Ha-CoV-2 WT S Vector | Virongy Biosciences | pCoV2_WT S | |
| Hek293T cells | ATCC | CRL-3214 | |
| Illumination Firefly Luciferase Enhanced Assay Kit 1000 assays | Gold Bio | I-930-1000 | |
| Infection Plate: 96-Well Tissue Culture Plate, Greiner Bio-One (With Lid, μClear White Flat Round, Chimney) | VWR | Cat# 82050-758 | |
| pAlphaPro-Luc-GFP-PreΨ (Ha-CoV-2 Genome) Vector | In house | ||
| PEI-based Transfection Reagent | Virongy Biosciences | Transfectin | |
| Penicillin-Streptomycin-Glutamine (100X) | Invitrogen | 10378016 | |
| Polyethylenimine, branched | Millipore Sigma | 408727-100ML | |
| QuantStudio 7 Pro Real-Time PCR System | ThermoFisher | A43163 | |
| Ready to use (HEK293T)(ACE2/TMPRSS2) Cells | Virongy Biosciences | Ready-To-Use-Cells | |
| SARS-CoV-2 S Omicron (B.1.1.529) Vector | Virongy Biosciences | pCoV2-B.1.1.529 | |
| SARS-CoV-2 S Delta (B.1.617.2) Vector | Virongy Biosciences | pCoV2- B.1.617.2 | |
| Syringe Filters, PES, 0.22µm | Genesee Scientfic | 25-244 | |
| TaqMan Fast Virus 1-Step Master Mix | ThermoFisher | 4444432 | |
| Trypan Blue Solution, 0.4% | ThermoFisher | 15250061 |
Ссылки
- World Health Organization. Weekly epidemiological update on COVID-19. 143, 1(2023).
- Dhama, K., et al. Global emerging Omicron variant of SARS-CoV-2: Impacts, challenges and strategies. Journal of Infection and Public Health. 16 (1), 4-14 (2023).
- Dhama, K., et al. Coronavirus Disease 2019-COVID-19. Clinical Microbiology Reviews. 33 (4), e00028-e00020 (2020).
- El-Shabasy, R. M., et al. Three waves changes, new variant strains, and vaccination effect against COVID-19 pandemic. International Journal of Biological Macromolecules. 204, 161-168 (2022).
- CDC. Interim laboratory biosafety guidelines for handling and processing specimens associated with coronavirus disease 2019 (COVID-19). , https://www.cdc.gov/coronavirus/2019-nCoV/lab/lab-biosafety-guidelines.html (2021).
- Kaufer, A., Theis, T., Lau, K., Gray, J., Rawlinson, W. Laboratory biosafety measures involving SARS-CoV-2 and the classification as a Risk Group 3 biological agent. Pathology. 52 (7), 790-795 (2020).
- Vanderheiden, A., et al. Development of a Rapid Focus Reduction Neutralization Test Assay for Measuring SARS-CoV-2 Neutralizing Antibodies. Current Protocols in Immunology. 131 (1), e116(2020).
- Dieterle, M. E., et al. A Replication-Competent Vesicular Stomatitis Virus for Studies of SARS-CoV-2 Spike-Mediated Cell Entry and Its Inhibition. Cell Host & Microbe. 28 (3), 486-496 (2020).
- Nie, J., et al. Quantification of SARS-CoV-2 neutralizing antibody by a pseudotyped virus-based assay. Nature Protocols. 15 (11), 3699-3715 (2020).
- Nie, J., et al. Establishment and validation of a pseudovirus neutralization assay for SARS-CoV-2. Emerging Microbes & Infections. 9 (1), 680-686 (2020).
- Yang, R., et al. Development and effectiveness of pseudotyped SARS-CoV-2 system as determined by neutralizing efficiency and entry inhibition test in vitro. Biosafety and Health. 2 (4), 226-231 (2020).
- Hetrick, B., et al. Development of a hybrid alphavirus-SARS-CoV-2 pseudovirion for rapid quantification of neutralization antibodies and antiviral drugs. Cell reports methods. 2 (3), 100181(2022).
- Jackson, C., Farzan, M., Chen, B., Choe, H. Mechanisms of SARS-CoV-2 entry into cells. Nature Reviews. Molecular Cell Biology. 23 (1), 3-20 (2022).
- Jackson, L. A., et al. An mRNA Vaccine against SARS-CoV-2 - Preliminary Report. The New England Journal of Medicine. 383 (20), 1920-1931 (2020).
- Polack, F. P., et al. Safety and Efficacy of the BNT162b2 mRNA Covid-19 Vaccine. The New England Journal of Medicine. 383 (27), 2603-2615 (2020).
- Li, F. Structure, function, and evolution of coronavirus spike proteins. Annual Review of Virology. 3 (1), 237-261 (2016).
- Donofrio, G. A Simplified SARS-CoV-2 Pseudovirus Neutralization Assay. Vaccines. 9 (4), 389(2021).
- Crawford, K. H. D., et al. Protocol and Reagents for Pseudotyping Lentiviral Particles with SARS-CoV-2 Spike Protein for Neutralization Assays. Viruses. 12 (5), 513(2020).
- Zettl, F., et al. Rapid Quantification of SARS-CoV-2-Neutralizing Antibodies Using Propagation-Defective Vesicular Stomatitis Virus Pseudotypes. Vaccines. 8 (3), 386(2020).
- Li, Q., Liu, Q., Huang, W., Li, X., Wang, Y. Current status on the development of pseudoviruses for enveloped viruses. Reviews in Medical Virology. 28 (1), e1963(2018).
- Lundin, A. Optimization of the firefly luciferase reaction for analytical purposes. Advances in Biochemical Engineering/Biotechnology. 145, 31-62 (2014).
- Deshpande, G. R., et al. Neutralizing antibody responses to SARS-CoV-2 in COVID-19 patients. The Indian Journal of Medical Research. 152 (1 & 2), 82-87 (2020).
- Chen, C., et al. Research progress in methods for detecting neutralizing antibodies against SARS-CoV-2. Analytical Biochemistry. 673, 115199(2023).
- Manischewitz, J., et al. Development of a novel vaccinia-neutralization assay based on reporter-gene expression. The Journal of Infectious Diseases. 188 (3), 440-448 (2003).
- Chen, J., Wang, R., Gilby, N., Wei, G. Omicron Variant (B.1.1.529): Infectivity, Vaccine Breakthrough, and Antibody Resistance. Journal of Chemical Information and Modeling. 62 (2), 412-422 (2022).
- Saxena, S. K., et al. Characterization of the novel SARS-CoV-2 Omicron (B.1.1.529) variant of concern and its global perspective. Journal of Medical Virology. 94 (4), 1738-1744 (2022).
Перепечатки и разрешения
Запросить разрешение на использование текста или рисунков этого JoVE статьи
Запросить разрешениеСмотреть дополнительные статьи
This article has been published
Video Coming Soon
Авторские права © 2025 MyJoVE Corporation. Все права защищены