يحدد ثابت ربط التوازن (Kb) قوة تفاعل البروتين الرابط. Kb يمكن حسابه على النحو التالي عندما يكون التفاعل في حالة توازن:
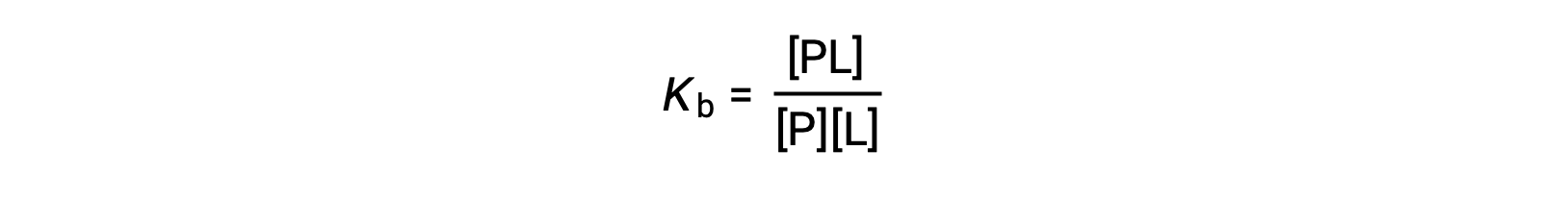
حيث أن P و L هما البروتين غير المرتبط و الرابطة، على التوالي، و PL هو مركب بروتين-رابطة.
نظراً لأن كمية الترابط المرتبط أيضاً مرتبطة بمعدل الارتباط بالرابط، يمكن للتجارب أيضاً تحديد Kb من خلال فحص معدلات ارتباط البروتين الرابط (kon) والتفكك (koff) باستخدام النسبة التالية:
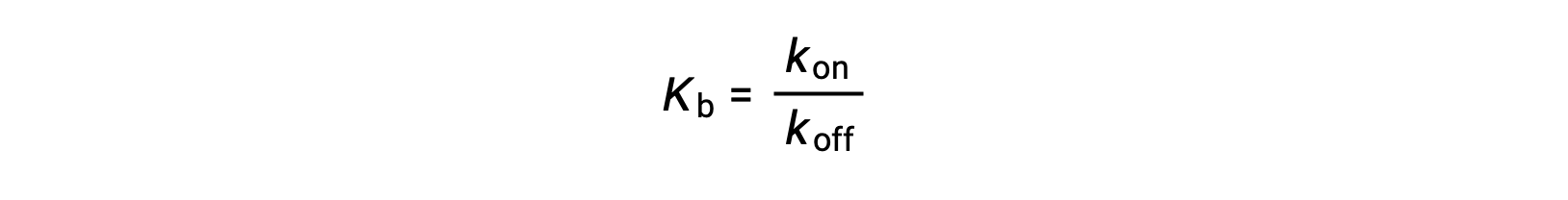
وهكذا، فئتان من ؛ تُستخدم فحوصات الربط لتحديد ثابت ربط التوازن –؛ تلك التي تقيس تركيزات التوازن وتلك التي تقيس حركية التفاعل. في حالة ما، يجب أن يكون التفاعل في حالة توازن في وقت القياس.
تعتمد طريقة تحديد تركيزات التوازن على الحساسية المرغوبة وسهولة اكتشاف الإشارة. لهذه الأسباب، يتم استخدام المقايسات الطيفية على نطاق واسع. في هذه التجارب، ينتج التفاعل تغيرًا في امتصاص مادة متفاعلة أو منتج عند طول موجة معين، يمكن اكتشافه بواسطة مقياس الطيف الضوئي بالأشعة المرئية وفوق البنفسجية. وبدلاً من ذلك، يمكن وسم المادة المتفاعلة أو المنتج بمسبار فلوري أو قد يحتوي على حامل فلور جوهري. بعد ذلك، يمكن قياس تقدم التفاعل من التغير في التألق. يتم إجراء هذه الاختبارات عن طريق تغيير تركيزات متفاعل واحد بينما تبقى بقية التجربة ثابتة. يمكن بعد ذلك رسم النتائج وتحليلها باستخدام طرق مختلفة لتناسب المنحنيات.
تتم أيضاً دراسة التفاعلات بين البروتينات والروابط باستخدام مجموعة متنوعة من التقنيات البيوكيميائية والطيفية. يساعد التحليل الهيكلي، باستخدام علم البلورات بالأشعة السينية والتحليل الطيفي للرنين المغناطيسي النووي، في التنبؤ بتفاعلات البروتين - الرابطة من خلال المحاكاة الجزيئية. تُستخدم المناهج النظرية والحاسوبية، مثل دراسات الالتحام بالبروتين، على نطاق واسع لتوصيف موضع وتفاعلات روابط الجزيئات الصغيرة، بما في ذلك الأدوية المرشحة. يُعد تصميم الأدوية بمساعدة الكمبيوتر بديلاً سريعاً ومنخفض التكلفة لتسريع وتيرة التجارب التقليدية واختبار العقاقير الخاطئة.
From Chapter 3:

Now Playing
3.7 : The Equilibrium Binding Constant and Binding Strength
Energy and Catalysis
12.7K Views

3.1 : القانون الأول للديناميكا الحرارية
Energy and Catalysis
5.3K Views

3.2 : القانون الثاني للديناميكا الحرارية
Energy and Catalysis
4.9K Views

3.3 : المحتوى الحراري داخل الخلية
Energy and Catalysis
5.7K Views

3.4 : الانتروبيا داخل الخلية
Energy and Catalysis
10.2K Views

3.5 : مقدمة في الطاقة الحرة
Energy and Catalysis
8.0K Views

3.6 : التفاعلات الداخلية والطاردة للطاقة في الخلية
Energy and Catalysis
14.2K Views

3.8 : الطاقة الحرة والتوازن
Energy and Catalysis
6.0K Views

3.9 : عدم التوازن في الخلية
Energy and Catalysis
4.1K Views

3.10 : أكسدة وتقليل الجزيئات العضوية
Energy and Catalysis
5.8K Views

3.11 : مقدمة في الإنزيمات
Energy and Catalysis
16.7K Views

3.12 : الإنزيمات وطاقة التنشيط
Energy and Catalysis
11.4K Views

3.13 : مقدمة في حركية الإنزيم
Energy and Catalysis
19.4K Views

3.14 : رقم الدوران والكفاءة الحفازة
Energy and Catalysis
9.7K Views

3.15 : إنزيمات مثالية تحفيزيا
Energy and Catalysis
3.8K Views
See More
Copyright © 2025 MyJoVE Corporation. All rights reserved