Method Article
جيل من تفرقوا Presomitic الأديم المتوسط الثقافات خلية التصوير من اسماك الزرد الإنقسام على مدار الساعة في خلايا واحدة
In This Article
Summary
Somitogenesis هو عملية التنموية الإيقاعية التي مكانيا أنماط محور الجسم من أجنة الفقاريات. سابقا، قمنا بتطوير خطوط الزرد المعدلة وراثيا التي تستخدم للصحفيين الفلورسنت لمراقبة الجينات التي تدفع دوري هذه العملية. هنا، ونحن ثقافة فرقت الخلايا من هذه الخطوط والصورة التذبذبات على مر الزمن في المختبر.
Abstract
تجزئة هو عملية التخلق دورية ومتتابعة في الفقاريات. هذا التشكيل الإيقاعي من كتل من الأنسجة تسمى somites على طول محور الجسم هو دليل على وجود مذبذب الوراثية الزخرفة الجنين النامية. في الزرد، وتتكون على مدار الساعة داخل الخلايا تجزئة الدافعة للأعضاء عامل النسخ عائلتها / هس تنظيمها في الحلقات ردود فعل سلبية. لقد ولدت مؤخرا المعدلة وراثيا خطوط مراسل الفلورسنت لher1 الجين دوري أن ألخص نمط المكانية والزمانية من التذبذبات في الأديم المتوسط presomitic (PSM). باستخدام هذه الخطوط، قمنا بتطوير نظام الثقافة في المختبر الذي يسمح التحليل في الوقت الحقيقي من خلال تجزئة التذبذبات على مدار الساعة، والخلايا المعزولة PSM احد. عن طريق إزالة الأنسجة PSM من الأجنة وراثيا ومن ثم تفريق الخلايا من المناطق تتأرجح على الأطباق الزجاجية القاع، ونحن ولدت الثقافات مناسبة للالوقت الفاصل بين التصوير من إشارة مضان منالخلايا الفردية على مدار الساعة. ويوفر هذا النهج إطارا التجريبية والمفاهيمية للتلاعب المباشر على مدار الساعة لقرار تجزئة وحيدة الخلية غير مسبوقة، مما يسمح للخصائص خلية مستقلة وعلى مستوى الأنسجة لتمييزها وتشريح.
Introduction
تشكيل دورية للقطاعات على طول محور الجسم الفقاريات، أو somitogenesis، هو دليل على وجود مذبذب المكانية والزمانية في الجنين النامية. آلية يفضل السيطرة somitogenesis والمفاهيمية وصفها ب "على مدار الساعة واجهة الموجة" نموذج 1، حيث "ساعة" التي تتألف من مؤشرات التذبذب الخلوية، ويعتقد الآن أن تكون مدفوعة من قبل داخل الخلية التعبير الايقاعي من مجموعة من الجينات دوري 2، القراد قبالة تشكيل من somites من الأديم المتوسط presomitic (PSM). مع تطور الجنين، والنضج "واجهة الموجة" في PSM يتحرك بالتنسيق مع الأنسجة تراجع نحو الخلفي، وتباطؤ واعتقال مؤشرات التذبذب الخلوية لأنها تمر 3. معا، ويطلق على هذا النظام الديناميكي spatiotemporally على مدار الساعة تجزئة. النهج الحالي لدراسة تجزئة مدار الساعة فترة ثلاثة مستويات متزايدة من التنظيم من مذبذب الوراثية في الخلايا واحد إلى عشرة اقتران المحليةفي يحدث بين الخلايا، وأخيرا إلى التنظيم العالمي للمعلومات الموضعية في PSM الأنسجة الجماعية 4.
وتشير الدراسات السابقة إلى تجزئة مذبذب خلية مستقلة في الزرد يتكون من الجينات ومنتجات البروتين من النسخ لها / هس] factorfamily، التي يعتقد أنها تشكل رد الفعل السلبي من خلال القمع النسخي 5-7. إشارات الطريق دلتا / الشق بمزامنة التذبذبات بين الخلايا المجاورة وينظم الفترة الجماعي للسكان 8-10. جمعية جيل المستقبل تظهر إشارات الجزيئات التي تنتج في tailbud لبناء التدرج عبر PSM الزرد، وبالتالي افترض أن تساهم في تباطؤ واعتقال خلايا تتأرجح في 11 الأمامي. حتى الآن، وقد تم التحقيق في الأدوار الوظيفية لكل من هذه الجزيئات في somitogenesis التي كتبها طفرة جينية، حقن morpholino الحرارية صدمة الإفراط في التعبير، وخصم trea المخدراتtment من مكونات مدار الساعة والإشارات بين الخلايا 5،7،10،12. باستخدام هذه الاضطرابات، وقد يستدل تجزئة ظيفة على مدار الساعة من أوصاف مستوى الأنسجة من العيوب الجسيدة وفقدان التذبذبات موحدة في التعبير عن الجينات دوري مثل her1، her7، ودلتا C. ومع ذلك، وكلها تقريبا من هذه البيانات هي من أجنة الثابتة وتفشل في التقاط بدقة التغييرات التي هي متأصلة في وظيفة حيوية على مدار الساعة تجزئة. في الآونة الأخيرة، كشفت متعددة الأجنة الوقت الفاصل بين التصوير المسوخ الأولى مع الفترة مذبذب تتغير، ولكن قدمت هذه الملاحظات أيضا على مستوى 7،13 الأنسجة. وبالتالي، لم يحترم سلوك مذبذب خلايا مستقلة افترض خلال somitogenesis.
لقطات ثابتة من somitogenesis إعطاء صورة مكتملة لأنه، بطبيعته، هو الدافع وراء العملية من خلال نظام متذبذبة. أظهر العمل في وقت سابق من خلايا فأر وفرخ أن مستويات النصوارتفاع البروتين والخريف، ولكن أخذ العينات التذبذب ما يقرب من 2 ساعة كل 30 أو 45 دقيقة يقيد بالضرورة البيانات التي تم جمعها، وبالتالي فإن الاستنتاجات التي يمكن استخلاصها 14،15. دراسة مؤشرات التذبذب البيولوجية الأخرى، وأبرزها، والساعات الإيقاعية، تحركت بعيدا عن قياسات نظم الجينات والبروتينات التعبير لرصد الوقت الحقيقي باستخدام الفلورسنت وصحفيين للإضاءة الحيوية 16،17. هذه الأدوات ضرورية لإظهار الخصائص على مدار الساعة من الخلايا واحد 18. وقد تم تطوير مراسل إضاءة الحيوية للجين دوري Hes1 وتتميز الخلايا واحد في الماوس PSM 19 لفترة وجيزة. تم حساب متوسط فترة والتباين لعدد صغير من الخلايا، وتبين أن التذبذبات تستمر لعدة دورات في المختبر. ومع ذلك، فإن هذه الدراسات لم تتناول كميا استقرار ومتانة تردد المذبذب والسعة، ما إذا كانت الخلايا يمكن أن تدخل بشكل عفوي أو التذبذبات الخروج،وكيف تحافظ على خلايا العلاقات مرحلتها. بالإضافة إلى ذلك، لم يتم اختبارها آثار إشارات الجزيئات الموجودة في الجنين على مدار الساعة خلية مستقلة مباشرة. وبالتالي، هذه الخصائص الأساسية للمذبذب خلية واحدة لا تزال مجهولة تماما.
وقد وضعنا مؤخرا خطوط الأسماك المعدلة وراثيا باستخدام BAC recombineering 20 لدفع فينوس (YFP) للصحفيين مضان من her1 التعبير 30. هذه الخطوط استغلال العظة التنظيمية للموضع الكروموسومات سليمة التي تضمهم وألخص ديناميات الزماني والمكاني للنمط her1. هذا اختراق يسمح للرصد في الوقت الحقيقي من التعبير الجيني في الجنين الزرد النامية في الجسم الحي. لدراسة الخصائص الأساسية للالتذبذبات خلية مستقلة وكيف يتم تنظيم مثل هذا التعبير مع مرور الوقت، ونحن في الآونة الأخيرة وضعت طريقة موثوق بها لعزل وسجل من الخلايا في المختبر PSM. هذا بروتوويصف العقيد كيف يمكننا استخدمت خطوط مراسل المعدلة وراثيا لدينا لتوليد مزارع الخلايا المشتتة، يمكننا من خلاله توصيف التذبذبات على مدار الساعة تجزئة الزرد في الخلايا واحد. يمكننا بالتالي معالجة المسائل العالقة في الحقل الذي لم تكن في متناول مع تحليل ثابتة أو على مستوى الأنسجة، فضلا عن التلاعب مباشرة على مدار الساعة تجزئة على مستوى خلية واحدة مع إشارات الجزيئات ومثبطات.
Protocol
1. قبل تشريح
- في اليوم قبل التشريح، والحصول على أجنة من تزاوج متماثلي الجينات من أزواج الزرد متخالف لأليل المعدلة وراثيا.
- رفع الأجنة في E3 المتوسطة دون الميثيلين الأزرق في 28 درجة مئوية حتى الدرع المرحلة (6 ساعة بعد الإخصاب).
- نقل الأجنة في E3 المتوسطة دون الميثيلين الأزرق إلى 20 س CO / N. في 20 درجة مئوية، سوف تشكل الأجنة 1 الجسيدة في ساعة بمجرد وصولها إلى مرحلة tailbud. بعد 17-20 ساعة O / N عند 20 درجة مئوية، وينبغي أن تكون الأجنة في 5-8 الجسيدة المرحلة في صباح اليوم التالي في بداية البروتوكول تشريح.
- تجميع الأدوات والكواشف اللازمة للتشريح.
- الزجاج المصقول النار ماصة لنقل الأجنة والأنسجة
- زوج من ملقط غرامة لإزالة chorions من الأجنة
- Sylgard المغلفة 35 ملم طبق للتشريح - صب Sylgard البوليمر في طبق 35 ملم وعلاج O / N في 37 درجة مئوية. جعل تشريح جيدا باستخدامتلميح إبرة لإزالة كمية صغيرة من البوليمر علاجه. الطبق يمكن تنظيفها وإعادة استخدامها في وقت لاحق.
- شحذ، بالارض أدوات سلك التنغستن لPSM التلاعب الأنسجة
- الدقيقة مشرط لقطع قطعة المرجوة من PSM للثقافة
- 35 ملم طبق من البلاستيك لالتربسين الحضانة
- L15 المتوسطة التي تحتوي على 10٪ مصل بقري جنيني
- 0.25٪ حل التربسين / EDTA
- Sigmacoted نصائح هلام التحميل للتشتت
- أطباق بتري بلاستيكية تحتوي على E3 المتوسطة دون الميثيلين الأزرق.
- تغطية صحن التصوير أسفل الزجاج مع Fibronectin1 الركيزة (10 ميكروغرام / مل في برنامج تلفزيوني). يترك الطبق على مقاعد البدلاء لمعطف أثناء تشريح.
- استخدام المجسام مع مرشحات مضان المناسبة لتحديد والأجنة وراثيا إيجابية نوع (مرحلة 5-8 الجسيدة).
- تحديد الأجنة وراثيا عن طريق فحص الأديم المتوسط presomitic (PSM) للYFP التعبير تحت قناة مضان (الشكل 1A). مضان شويونيتبول تكون مرئية في المنطقة من الجسيدة شكلت مشاركة لtailbud. تحديد الأجنة مع ألمع إشارة؛ يجب أن يكون 25٪ من الأجنة ذرية متماثلة اللواقح تحمل 2 نسخ من التحوير. يختلف عدد الأجنة التي تم تحديدها اللازمة على أساس التجربة. قطعة واحدة tailbud تشريح سوف تسفر 1،000 الخلايا، في المتوسط. عادة، عدد قليل من الأجنة إيجابية إضافية مفيدة في حالة مصنوعة أخطاء أثناء تشريح.
- استخدام الضوء المرسل كمرجع الموضعية للتمييز أي تألق ذاتي، ولا سيما في الخلية صفار، من إشارة.
- نقل الأجنة إيجابية إلى طبق بتري بلاستيكية منفصلة تحتوي على E3 المتوسطة دون الميثيلين الأزرق.
2. PSM تشريح والتشتيت
- إعداد الأجنة للتشريح.
- تحت المجهر تشريح، وذلك باستخدام ملقط غرامة، وإزالة بعناية المشيماء من كل جنين في E3 المتوسطة. تأكد من عدم تلف الجنين أو تعطيل الخلية صفار.
- ملء Sylgard المغلفة تشريح الطبق مع L15 المتوسطة مع المصل. باستخدام ملقط أو أداة أخرى مسطحة، وإزالة أي فقاعات الهواء من سطح Sylgard.
- نقل الأجنة dechorionated باستخدام الزجاج ماصة النار مصقول لطبق تشريح.
- باستخدام أدوات الأسلاك، نقل جميع الأجنة إلى جانب واحد من الطبق تشريح.
- تشريح PSM من جنين واحد.
- توجيه جنين واحد على جانبها الوحشي في صغيرة مصنوعة جيدا في طبقة Sylgard داخل الطبق تشريح (الشكل 1B).
- باستخدام مشرط الصغرى، من خلال شريحة الجنين والخلايا البيض فقط الأمامي إلى الدماغ المؤخر وعبر القطب البطني للجنين (الشكل 1B، منقط خط أحمر).
- إزالة قطعة الأمامي من الجنين من البئر، ونقله بعيدا إلى جانب الطبق، ثم استخدام أدوات سلك لكشط بعيدا المتبقية حبيبات الخلية صفار من قسم الخلفي بما في ذلك PSM.
- بمجرد كشط صفار البيض بعيدا، تتسطح وتوجيه PSM مع نهاية الأمامي لافتا بعيدا عن المجرب والخلفي لافتا نحو مجرب (الشكل 1C).
- إذا كانت طبقة رقيقة من الأديم الظاهر لم اقتلع من خلال هذه النقطة، واستخدام الأدوات والأسلاك لقشر بعيدا عن الجزء العلوي من الأنسجة PSM.
- باستخدام مشرط الصغرى قطع tailbud، الطرف الأكثر الخلفي من PSM الماضي نهاية الحبل الظهري، بعيدا عن بقية الأنسجة (الشكل 1C، منقط خط أحمر). ملاحظة: قطعة أخرى من نسيج PSM، لPSM سبيل المثال الأمامي أقرب إلى الجسيدة شكلت مشاركة، ويمكن أيضا أن تؤخذ في الثقافة، وهذا يتوقف على مسألة تجريبية.
- تحريك قطعة tailbud لزاوية واحدة من الطبق بعيدا عن منطقة تشريح. استخدام أدوات سلك لمسح أي حطام الأنسجة والأجنة غير المرغوب فيها من مجال تشريح.
- كرر مع الجنين القادم.
- قطعة تجمع tailbud من عدة الإلكترونيةmbryos، اعتمادا على كيفية العديد من الخلايا سوف تكون هناك حاجة للتجربة. في المتوسط، وقطعة واحدة من النسيج tailbud غلة 1،000 الخلايا.
- ملء فارغة 35 ملم طبق من البلاستيك مع كمية صغيرة من التربسين EDTA-.
- باستخدام ماصة الزجاج المصقول النار، ونقل قطعة من tailbud تشريح الطبق في صحن يحتوي التربسين / EDTA. احتضان قطعة tailbud في التربسين / EDTA لمدة 20 دقيقة في RT.
- بينما يتم تحضين الأنسجة في التربسين، وإزالة الحل Fibronectin1 من الطبق التصوير القاع الزجاجي.
- غسل الحل من الزجاج 3 مرات مع الماء MilliQ. استخدام الشفط لإزالة كل غسل وضمان الطبق هو جاف تماما.
- تفريق قطعة tailbud في المتوسط للتصوير.
- ماصة 100 ميكرولتر من L15 المتوسطة مع المصل في صحن التصوير.
- باستخدام هلام طرف المغلفة، وإزالة قطع tailbud من التربسين / EDTA في صغيرة مثل حجم ممكن.
- ماصة القطع tailbud في المتوسط فيطبق التصوير. ماصة القطع صعودا وهبوطا عدة مرات لكسر بينهما ووقف الخلايا في المتوسط. يجب الحرص على عدم إدخال فقاعات الهواء. التحقق من وجود كتل الخلايا تحت المجهر وتفريق أكثر حسب الحاجة.
- تسمح الخلايا المتفرقة في تعليق ليستقر على الزجاج Fibronectin1 المغلفة لمدة 20 دقيقة في RT.
- إضافة كمية صغيرة من متوسطة إضافية L15 مع المصل إلى الخلايا قبل البدء في التصوير. استخدام الحرص على عدم تعطيل الخلايا المستقرة.
- بالنظر إلى مسألة تجريبية، إضافة تكميلية أو أي علاجات دوائية للثقافة.
3. التصوير من خلايا متناثرة PSM
- إعداد طبق التصوير في غرفة درجة الحرارة على المجهر الوقت الفاصل بين التصوير. تعيين وارنر غرفة لدرجة الحرارة المطلوبة للتجربة. تسمح طبق لكي تتوازن لمدة 30 دقيقة على الأقل قبل البدء في الحصول على الصور. درجة الحرارة شيك مسطر مع التحقيق في درجة الحرارة الخارجية وضعها في الطبق، إذا لزم الأمر. ملاحظة: نظرا لالعلاقة بين درجة الحرارة ومعدل somitogenesis 21 التحكم في درجة الحرارة مستقرة أمر ضروري لقياسات دقيقة من فترة في الخلايا PSM احد.
- الحصول على صور الاختبار في القناة مضان للتأكد من أن وقت التعرض وزيادة توفير مجموعة ديناميكية كبيرة من شدة دون التشبع لضمان اشارة جيدة لمستويات الضوضاء. صورة مضان نموذجية تم الحصول عليها من خلايا متناثرة المتولدة من خطوطنا باستخدام هذا البروتوكول يتطلب 400 مللي ثانية و 40 مللي ثانية للحصول على صورة الضوء المرسل مع كاميرا EMCCD العاملة في لEM الربح من 85، بالإضافة إلى تحقيق مكاسب قبل أمبير وسرعة قراءات من الكاميرا ضرورية لتحقيق أقصى قدر من الضجيج أكثر من إشارة أيضا.
- باستخدام القناة الضوء المرسل، واختيار مجالات الخلايا لاكتساب الوقت الفاصل.
- تشغيل الوقت الفاصل بين بروتوكول اقتناء لمدة من الوقت المطلوب.
- الحصول على ضوء واحد وصورة واحدة تنتقل مضان لكل حقل. ملاحظة: تعيين فاصل زمني بين ريال عماني الاستحواذجهاز الأمم المتحدة الإنمائي التي من شأنها التقاط صورة ديناميكية الزمنية دون تبيض أكثر من التصوير الموسعة أو سمية حمل في الخلايا. يستخدم هذا البروتوكول فاصل 2 دقيقة.
- تحقق الوقت الفاصل بين انشاء أحيانا أثناء التسجيل لضمان أن الخلايا تظل في التركيز، لا البرمجيات أو الأجهزة الأخطاء، الخ
4. معالجة الصور من الأفلام متلازمة الوقت الفاصل
- ملف الفيلم مفتوحة لحقل المكتسبة في برامج معالجة الصور. ملاحظة: تم استخدام فيجي لتجهيز جميع في هذا البروتوكول.
- انقسام تنتقل ضوء ومضان إطارات من حقل واحد لخلق 2 رزمة من الصور.
- تتبع خلية واحدة في القناة الضوء المرسل.
- وضع ROI دائرية (منطقة الفائدة) حول الخلية المحددة في الإطار الأول في القناة الضوء المرسل. ملاحظة:. الخلايا فقط أن 1 يتمتعون بصحة جيدة في نهاية التسجيل، 2 لا تتحرك خارج الميدان، و 3 لا تتلامس مع اوربا أخرى.يتم تعقب LLS.
- حفظ ROI كل بضعة إطارات إلى مدير العائد على الاستثمار. تتبع الخلية حتى الإطار الأخير.
- قياس كثافة استخدام رويس المحفوظة على قناة مضان.
- حدد كومة مضان ومع حفظ رويس، استخدم دائرة العرف interpolator المكونات في والكلي لقياس كثافة الخلية تعقب على مر الزمن.
- تحقق تتبع الإخراج من الماكرو. إذا التتبع يلتقط نوعيا ملامح مضان الوقت الفاصل، تصدير القيم إلى ورقة عمل Excel.
- حفظ قائمة العائد على الاستثمار للخلية.
- تكرار تتبع في قناة تبث في قناة وقياس مضان للخلايا الأخرى في هذا المجال.
- تكرار جميع الخطوات لحقول إضافية من التجربة.
النتائج
هذا البروتوكول تنتج ثقافات، وفرقت، وخلايا PSM واحدة قابلة للالوقت الفاصل بين التصوير من إشارة مضان (الشكل 2). لدينا التحوير يولد مراسل الذين دورة الإنتاج وتدهور تحدث مع ديناميات مماثلة لهذا الجين الذاتية والبروتين في الجنين، بناء على أمر من نصف ساعة. بسبب دوران سريع لها، ويجب أن يتم الكشف عن إشارة YFP في الخلايا واحد بسرعة لتقليل تبيض ومع القرار الزماني عالية لالتقاط ملامح كل دورة متذبذبة. أيضا، بالنظر إلى الخفوت النسبي للإشارة، تم ضبطها الظروف الثقافة واكتساب بعناية لضمان نتائج حساسة وقوية. لقد تم العثور على العوامل التالية إلى أن تكون مهمة في توليد الأمثل الثقافات الخلية PSM للتصوير: 1 إن الركيزة ECM تستخدم لطلاء الأطباق ثقافة أسفل الزجاج. 2. إضافة مصل للتشريح والمتوسطة التصوير. 3. تشريح PSM من الأجنة التي تم تحديدها اتخذت بعد التزاوج HETEأزواج rozygous، التي يحتمل أن تكون ذرية تحمل 2 نسخ من التحوير. 4. اقتناء صورة ضمن نطاق التكبير الأمثل، وذلك باستخدام الهدف NA أعلى لضمان كفاءة التقاط إشارة مضان. 5. الإضاءة مع مصدر ضوء الحالة الصلبة للحد من تقلبات الكثافة التي يمكن أن تسهم في ضجيج الخلفية. 6. كشف الإشارات مع كاميرا حساسة للغاية EM-CCD لتعظيم إشارة قراءات.
والثقافات الفرعية الأمثل تحتوي على الخلايا التي لا تبقى مدورة وصحية في جميع أنحاء التسجيل. افترضنا أن لدينا الركيزة ECM، جزء من fibronectin1 الزرد تبقي الخلايا في PSM مثل حالة غير متمايزة، بالمقارنة مع غيرها من ركائز استخداما مثل بولي يسين أو laminin. ركائز أخرى اختبرنا تسبب الخلايا للشد على الزجاج وفقدان إشارة الفلورسنت تتأرجح على مدار التسجيل. وجدنا أيضا أن إضافة مصل إلى متوسطة أثناء تشريح، تشتت،وكان تسجيل ليس فقط مهم لإرواء التربسين المستخدمة لتفارق، ولكن أيضا زيادة كثافة مضان على الخلفية، على الأرجح بسبب تحسن بقاء الخلية. لضمان التقاط إشارة الأمثل من الخلايا واحد كنا هدفا 40X مصممة خصيصا للتصوير مضان (زايس خطة NeoFluor سلسلة) مع ارتفاع NA. وجدنا أيضا أن مصدر ضوء الحالة الصلبة تقديم إضاءة أكثر استقرارا من مصابيح الزئبق التقليدية، وهو أمر حاسم للحد من تقلبات الخلفية التي تسهم في الصور صاخبة. هذه التعديلات مهمة لضمان تحقيق نتائج قوية.
باستخدام هذا البروتوكول نتوقع الثقافات التي يتم فلوري غالبية الخلايا في مجال معين في مرحلة ما أثناء التسجيل. نجد أن الخلايا الفلورسنت تبقى عادة مدورة وأحيانا متحركة جدا خلال التسجيلات. وهناك عدد قليل الخلايا، بما في ذلك الخلايا الفلورسنت، قد تصبح أفكارك أثناء التسجيل. وتستبعد هذه الخلايا من أي أحدnalysis. نحن أيضا استبعاد الخلايا التي تتلامس مع خلايا أخرى أو نقلها خارج مجال الرؤية. في المتوسط، ونحن نرى انخفاضا بنسبة 12٪ في عدد الخلايا لكل حقل من نهاية التسجيل 10 ساعة كما تم قياسها عن طريق حساب عدد الخلايا السليمة في القناة الضوء المرسل. وتشمل هذه الخسارة على حد سواء موت الخلايا والخلايا التي انتقلت من مجال. ونظرا لهذه المحاذير وسعنا، في المتوسط، المسار 5 خلايا لكل حقل الفلورسنت التي لا تزال قابلة للحياة ومرئية، وعادة ما تسجل 6 حقول في الشرط. على سبيل المثال، سوف تجربة مع 4 شروط دينا 24 مجموع الحقول المكتسبة وعادة حوالي 30 خلية في تعقب الشرط. في ظل ظروف التصوير القياسية مع L15 المتوسطة التي تحتوي على 10٪ مصل بقري جنيني، نجد أن الخلايا PSM (ن = 101 الخلايا من 4 مكررات التجريبية) يمكن أن تنتج ما بين 2 و 7 قمم، مع متوسط والانحراف المعياري 3 ± 1 قمم (2 دورات -3). عدد الذروة الوسيط، وكذلك المئين 25٪، هو 2 القمم و75٪ المئين طق 3 قمم. باستخدام لدينا تتبع وتحليل شبه الآلي، ونحن يمكن أن تولد بسرعة كثافة مضان على آثار الوقت لخلايا PSM الفردية، مع اثر خلية ممثل هو مبين في الشكل 2C. ويمكن بعد هذه آثار الخام أن تستخدم لجعل القياسات الكمية من خصائص الخلايا PSM تتأرجح، مثل تردد، والسعة، وعدد الدورات، وتوقيت القمم.
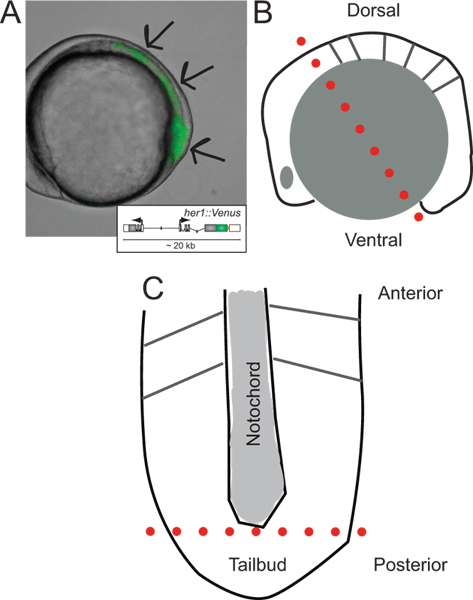
الشكل 1. تحديد الأجنة والخطط المعدلة وراثيا من تشريح بهم. (A) عرض الجانبي للجنين الزرد المعدلة وراثيا معربا عن YFP مضان في مرحلة ~ 5 الجسيدة. الصورة تراكب الضوء المرسل وقناة مضان. السهام تشير إلى مجالات إشارة البدء في غيض من tailbud، في جميع أنحاء PSM، نحو لتر AST شكلت الجسيدة. يظهر أقحم التخطيطي من التحوير مراسل (لمزيد من المعلومات حول تطوره والسلوك في الجسم الحي الرجوع إلى Soroldoni وآخرون 30. (B) تخطيطي للعرض الوحشي من الجنين قبل أن يقطع لأول مرة خلال تشريح. يشير خط أحمر منقط في أول خطوة من نوعها قدمت عبر الدماغ المؤخر، على الرغم من الخلية صفار فقط وراء tailbud. (C) عرض تخطيطي بالارض PSM التالية إزالة حبيبات الصفار وطبقة البشرة، الموجهة على طول المحور الأمامي الخلفي لها. يشير خط أحمر منقط خفض ثانية لإزالة غيض من tailbud للتشتت والثقافة. الرجاء انقر هنا لمشاهدة نسخة أكبر من هذا الرقم.
07fig2.jpg "/>
الشكل 2. صور الممثل وآثار من خلية واحدة في ثقافة PSM فرقت. (A) مونتاج الصور المنقولة من ضوء خلية PSM واحد في 6 ساعات تسجيل الوقت الفاصل. لاحظ أن الخلية ما زالت مدورة وصحية طوال فترة التسجيل. (B) الموافق المونتاج من الصور مضان من خلية واحدة PSM. يتم ترقيم قمم في كثافة الخلية على مدار التسجيل. (C) متوسط الكثافة مع مرور الوقت يقاس من العائد على الاستثمار وضعت على هذه الخلية. تؤخذ القيم من كل إطار من الفيلم مع معدل الإطار الواحد في 2 دقيقة باستخدام دائرة interpolator المكونات في وماكرو مخصصة مكتوب في فيجي. يتم ترقيم قمم في شدة مرة أخرى في جميع أنحاء التتبع. الرجاء انقر هنا لمشاهدة نسخة أكبر من هذا الرقم.
Discussion
لدراسة عملية الخلوية التي تجري على مدى التطور الجنيني، وعلماء الأحياء عادة استخدام هذا النهج في سياق الجنين بأكمله. ومع ذلك، ولكي نفهم تماما كيف يتصرف خلية واحدة ضمن إطار زمني التنموية، وهي طريقة لدراسة والتشويش على الخلايا الفردية في عزلة هو أيضا مفيد للغاية. عن طريق توليد فرقت الثقافات الخلية PSM باستخدام الأجنة الزرد المعدلة وراثيا لدينا الآن أداة لدراسة الخلية مباشرة الطابع المستقل من التذبذبات الوراثية في ساعة تجزئة بطريقة الكمي. فمن الممكن لقياس ديناميكية التذبذبات في مراسل الفلورسنت لدينا في مئات من الخلايا تحت مجموعة متنوعة من الظروف.
فترة احظ واحد من الخلايا في الثقافة أطول من الفترة somitogenesis في الجنين سليمة. نلاحظ أن ازدراع PSM سليمة في الثقافة يسلك أيضا التذبذبات أبطأ من الجنين سليمة (لا تظهر البيانات)، مما يوحي ثار فترة أطول لوحظ في خلايا معزولة لا يعود ببساطة إلى الأضرار الناجمة عن تشتت. ويلاحظ وجود فترة متغير والسعة في معظم لدينا وحيدة الخلية سلسلة زمنية. مصدر هذا التباين هو معروف، ولكن ينبغي أن تكشف تفاصيل مهمة عن دوائر صنع تيرة على مدار الساعة في تجزئة.
مع هذا الأسلوب يمكننا دراسة المكونات الجينية للتجزئة على المستوى الخلوي، والأسئلة العنوان الذي يتحدون لدراسة في الجنين كله. على سبيل المثال، من خلال إضافة للرقابة من جزيئات إشارة معروفة وجدت في الجنين النامية لثقافاتنا، يمكن أن ندرس آثارها على PSM مذبذب الخلوية واحد في مقايسة قوية وقابلة للتكرار. يفتح نظامنا الثقافة PSM الباب أمام إجراء تقييم دقيق للعوامل ما، وحده، أو بالاشتراك تعزيز التذبذبات في هذه الخلايا، ما هي العوامل التي تحول دون هذه التذبذبات، واختبار التفاعل بين هذه الجزيئات. مع هذه الأدوات في متناول اليد، ونحن نهدف إلىتقييم النماذج القائمة من somitogenesis التي تستند إلى بيانات على مستوى الأنسجة المنشورة، فضلا عن نتائج استخدام في الخلايا وحيدة لتوليد التنبؤات التي يمكن اختبارها في الجنين كله.
على حد علمنا، هذا هو أول الزرد بروتوكول الثقافة الخلية الأولية للالحاد تسجيل الوقت الفاصل بين مضان في الخلايا واحد؛ مزيد من التطوير والتنقيح من هذا البروتوكول هو بلا شك ممكن. بروتوكولات أخرى غالبا ما تستخدم الأجنة الزرد لتوليد خطوط الخلايا المستقرة التي يمكن transfected مع صحفيين وتستخدم للتصوير على المدى الطويل 27-29. بينما خطوط مستقرة هي مفيدة لتصوير عملية ليست مرتبطة توقيت التنمية، مثل الساعة اليومية، مسألة تجزئة الجنينية يتطلب التصوير على الفور في حين أن الخلايا لا تزال في متذبذبة، دولة السلف الخاصة بهم. مرة واحدة خلايا وقف تتأرجح، فإنها تفترض مصير الخلايا المتمايزة، وعندما تكون في الأنسجة، وستدرج في الجسيدة. فمن بوssible أنه مع عامل الحق أو عوامل موجودة في المختبر فإننا يمكن أن تولد الزرد خطوط خلية ثقافة PSM مثل التي من شأنها أن تبقى متذبذبة، مما يتيح بشكل ملحوظ الملاحظات على المدى الطويل، اضطرابات متتابعة متعددة، أو الفرز الفائق الإنتاجية.
ونحن نتوقع أن هذا الأسلوب في إعداد الثقافات الأولية من خلايا متناثرة للتصوير مرور الزمن هو مناسبة تماما لدراسة أي عملية الخلوية التي تحدث ضمن إطار زمني التنموية التي ليس دود باستخدام خطوط الخلايا الزرد مستقرة. عزلة متميزة الخلية الأنواع في مراحل نمو متميزة من خطوط مراسل المعدلة وراثيا المناسب، إما عن طريق تشريح أو عن طريق نظام مراقبة الأصول الميدانية بعد التفكك الجنينية، يمكن أن توفر الخلايا تبدأ. بعض التحسين من ظروف الثقافة، مسترشدة في ذلك المنشأ الجنينية من الخلايا، قد تكون مطلوبة. من خلال الجمع بين هذا البروتوكول مرنة وحساسة مع مجموعة متنامية بسرعة من الزرد المعدلة وراثياخطوط، ونحن نأمل أن تسهل في المختبر التنموية نهج البيولوجيا التي هي مكملة لأساليب الوراثية والجنينية الكلاسيكية.
Disclosures
المؤلف المساهمات:
ABW تطوير وصقل تشتت، والثقافة، والتصوير، والبروتوكولات تتبع الخلية. DS إنشاء خطوط المعدلة وراثيا وأشرف على تصميم المجهر مضان الوقت الفاصل المستخدمة في هذا البروتوكول. رائدة AO الأولي إثبات صحة المبدأ التجارب لفصل الخلايا والصورة PSM في الثقافة. كتب JS الأداة المساعد دائرة interpolator في فيجي تستخدم لقياس كثافة مضان من الأفلام مرور الزمن. ABW وأكو كتب مخطوطة.
Acknowledgements
وأيد هذا العمل من قبل EMBO طويل الأجل الزمالة (ABW)، وزمالة الدولية المؤسسة الوطنية للعلوم ما بعد الدكتوراه البحوث (ABW)، وماكس بلانك غزلشافت (ABW، DS، JS، أكو)، وهو يحفر-BB الزمالة (AO)، ومجلس البحوث الأوروبي في إطار الإطاري السابع المجتمعات الأوروبية برنامج STG-207634 (DS، أكو). نشكر رافي ديساي للتعليقات مفيدة على المخطوطة. نود أيضا أن نشكر MPI-CBG مرفق تعبير البروتين لإنتاج Fibronectin1 جزء الزرد، وموظفي مرفق الأسماك MPI-CBG للرعاية وصيانة خطوط الأسماك لدينا وMPI-CBG مرفق المجهر الضوئي للحصول على الدعم التصوير.
Materials
| Name | Company | Catalog Number | Comments |
| Epifluorescence microscope | Olympus | Model: SZX16 | |
| Epifluorescence microscope | X-cite Illumination | Series: 120Q | |
| Dissection microscope | Olympus | Model: SZX12 | |
| Fine forceps no. 55 | Fine Science Tools | 11295-51 | |
| Glass transfer pipettes | Assistent | 567/2 | |
| 35 mm plastic petri dishes | Greiner | 627102 | |
| 60 mm plastic petri dishes | Greiner | 628102 | |
| Sylgard polymer | SASCO | 266727 | |
| Manipulation tools | Made in-house | For description of manipulation tools Ref. 22 | |
| Microsurgical knife | World Precision Instruments | 500249 | |
| L15 medium | Invitrogen | 57322 | |
| Penicillin/streptomyocin | PAA | P11-010 | |
| Fetal bovine serum | Invitrogen | 257322 | |
| 0.05% trypsin / 0.02% EDTA | PAA | L11-004 | |
| Gel loading tips | Fisher Scientific | 253188 | |
| Sigmacote | Sigma Aldrich | 254589 | |
| Micropipette set | Gilson International | F167300 | |
| Zebrafish Fibronectin1 70 kD fragment | MPI-CBG protein facility | Generated in-house from construct based on previously published work Ref. 23-25 | |
| Glass bottom imaging dishes | Mattek (single well) | P35G-1.5-14-C | |
| Glass bottom imaging dishes | Greiner (CellView -multi-well) | 262502 | |
| E3 medium without methylene blue | Made in-house | From The Zebrafish Book, 5th Ed. Ref. 26 | |
| Plastic transfer pipettes | Ratiolab | 260011 | |
| Warner heating/cooling chamber | Warner Instruments | TC-324B/344B | |
| EM-CCD camera | Andor | Model: iXOn 888 | |
| Wide-field fluorescence microscope with Venus filter set | Zeiss | Model: Axiovert 200M | |
| Wide-field fluorescence microscope with Venus filter set | NeoFluor 40x, NA 0.75 | ||
| Wide-field fluorescence microscope with Venus filter set | Lumencor Light Engine | Model: Spectra X | |
| Wide-field fluorescence microscope with Venus filter set | BrightLine HC 575/15 | F39-575 |
References
- Cooke, J., Zeeman, E. C. A clock and wavefront model for control of the number of repeated structures during animal morphogenesis. J Theor Biol. 58, 455-476 (1976).
- Oates, A. C., Morelli, L. G., Ares, S. Patterning embryos with oscillations: structure, function and dynamics of the vertebrate segmentation clock. Development. 139, 625-639 (2012).
- Dequeant, M. L., Pourquie, O. Segmental patterning of the vertebrate embryonic axis. Nat Rev Genet. 9, 370-382 (2008).
- Oates, A. C., Gorfinkiel, N., Gonzalez-Gaitan, M., Heisenberg, C. P. Quantitative approaches in developmental biology. Nat Rev Genet. 10, 517-530 (2009).
- Oates, A. C., Ho, R. K. Hairy/E(spl)-related (Her) genes are central components of the segmentation oscillator and display redundancy with the Delta/Notch signaling pathway in the formation of anterior segmental boundaries in the zebrafish. Development. 129, 2929-2946 (2002).
- Lewis, J. Autoinhibition with transcriptional delay: a simple mechanism for the zebrafish somitogenesis oscillator. Curr Biol. 13, 1398-1408 (2003).
- Schroter, C., Oates, A. C. Segment Number and Axial Identity in a Segmentation Clock Period Mutant. Curr Biol. 20, 1254-1258 (2010).
- Riedel-Kruse, I. H., Muller, C., Oates, A. C. Synchrony dynamics during initiation, failure, and rescue of the segmentation clock. Science. 317, 1911-1915 (2007).
- Ozbudak, E. M., Lewis, J. Notch signalling synchronizes the zebrafish segmentation clock but is not needed to create somite boundaries. PLoS Genet. 4, e15 (2008).
- Herrgen, L., et al. Intercellular Coupling Regulates the Period of the Segmentation Clock. Curr Biol. 20, 1244-1253 (2010).
- Sawada, A., et al. Fgf/MAPK signalling is a crucial positional cue in somite boundary formation. Development. 128, 4873-4880 (2001).
- Giudicelli, F., Ozbudak, E. M., Wright, G. J., Lewis, J. Setting the tempo in development: an investigation of the zebrafish somite clock mechanism. PLoS Biol. 5, e150 (2007).
- Herrgen, L., Schroter, C., Bajard, L., Oates, A. C. Multiple embryo time-lapse imaging of zebrafish development. Methods Mol Biol. 546, 243-254 (2009).
- Hirata, H., et al. Oscillatory expression of the bHLH factor Hes1 regulated by a negative feedback loop. Science. 298, 840-843 (2002).
- Maroto, M., Dale, J. K., Dequeant, M. L., Petit, A. C., Pourquie, O. Synchronised cycling gene oscillations in presomitic mesoderm cells require cell-cell contact. Int J Dev Biol. 49, 309-315 (2005).
- Reppert, S. M., Weaver, D. R. Coordination of circadian timing in mammals. Nature. 418, 935-941 (2002).
- Welsh, D. K., Imaizumi, T., Kay, S. A. Real-time reporting of circadian-regulated gene expression by luciferase imaging in plants and mammalian cells. Methods Enzymol. 393, 269-288 (2005).
- Soroldoni, D., Oates, A. C. Live transgenic reporters of the vertebrate embryo's Segmentation Clock. Curr Opin Genet Dev. 21, 600-605 (2011).
- Masamizu, Y., et al. Real-time imaging of the somite segmentation clock: revelation of unstable oscillators in the individual presomitic mesoderm cells. Proc Natl Acad Sci USA. 103, 1313-1318 (2006).
- Soroldoni, D., Hogan, B. M., Oates, A. C. Simple and efficient transgenesis with meganuclease constructs in zebrafish. Methods in molecular biology. 546, 117-130 (2009).
- Schroter, C., et al. Dynamics of zebrafish somitogenesis. Dev Dyn. 237, 545-553 (2008).
- Picker, A., Roellig, D., Pourquie, O., Oates, A. C., Brand, M. Tissue micromanipulation in zebrafish embryos. Methods in molecular biology. 546, 153-172 (2009).
- Mould, A. P., et al. Identification of multiple integrin beta1 homologs in zebrafish (Danio rerio). BMC Cell Biol. 7, 24 (2006).
- Mould, A. P., Koper, E. J., Byron, A., Zahn, G., Humphries, M. J. Mapping the ligand-binding pocket of integrin alpha5beta1 using a gain-of-function approach. Biochem J. 424, 179-189 (2009).
- Zhao, Q., Liu, X., Collodi, P. Identification and characterization of a novel fibronectin in zebrafish. Exp Cell Res. 268, 211-219 (2001).
- Westerfield, M. In The zebrafish book : a guide for the laboratory use of zebrafish (Brachydanio rerio). , (1993).
- Vallone, D., Santoriello, C., Gondi, S. B., Foulkes, N. S. Basic protocols for zebrafish cell lines: maintenance and transfection. Methods Mol Biol. 362, 429-441 (2007).
- Carr, A. J., Whitmore, D. Imaging of single light-responsive clock cells reveals fluctuating free-running periods. Nat Cell Biol. 7, 319-321 (2005).
- Whitmore, D., Foulkes, N. S., Sassone-Corsi, P. Light acts directly on organs and cells in culture to set the vertebrate circadian clock. Nature. 404, 87-91 (2000).
- Soroldoni, D., et al. A Doppler effect in embryonic pattern formation. Science. 345, 222-225 (1126).
Reprints and Permissions
Request permission to reuse the text or figures of this JoVE article
Request PermissionExplore More Articles
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. All rights reserved