A subscription to JoVE is required to view this content. Sign in or start your free trial.
Method Article
إجراء تجارب ميلر أوري
In This Article
Summary
كانت تجربة ميلر أوري دراسة رائدة حول التوليف غير الحيوية من المركبات العضوية ذات الأهمية المحتملة لأصل الحياة. أدخلت الغازات بسيطة في جهاز الزجاج وتخضع لالتفريغ الكهربائي، ومحاكاة آثار البرق في نظام الغلاف الجوي والمحيطات والأرض البدائية. وقد أجريت التجربة لمدة أسبوع، وبعد ذلك، تم تحليل العينات التي تم جمعها من أنها لبنات البناء الكيميائي للحياة.
Abstract
في عام 1953، حسبما ذكرت ستانلي ميلر إنتاج الجزيئات الحيوية من المواد الأولية الغازية بسيطة، وذلك باستخدام جهاز شيدت لمحاكاة نظام الغلاف الجوي والمحيطات والأرض البدائية. قدم ميلر 200 مل من الماء، و 100 ملم زئبقي من H 2، 200 ملم زئبقي من CH 4، و 200 ملم زئبقي من NH 3 في الجهاز، ثم تعرض هذا الخليط، تحت التكثيف، إلى التفريغ الكهربائي لمدة أسبوع، في حين كان الماء في وقت واحد ساخنة. الغرض من هذا المخطوط هو تزويد القارئ مع بروتوكول التجريبية العامة التي يمكن استخدامها لإجراء نوع ميلر أوري التجربة تصريف شرارة، وذلك باستخدام مبسطة 3 L رد فعل قارورة. منذ التجربة ينطوي على تعريض غازات قابلة للاشتعال لتفريغ كهربائي عالي الجهد، يجدر تسليط الضوء على الخطوات الهامة التي تقلل من خطر الانفجار. يمكن استقراء الإجراءات العامة وصفها في هذا العمل لتصميم وإجراء مجموعة واسعة من تجربة التفريغ الكهربائيق محاكاة بيئات الكواكب البدائية.
Introduction
طبيعة أصل الحياة على الأرض لا تزال واحدة من أعقد المسائل العلمية غامض. في 1920s اقترح عالم الأحياء الروسي الكسندر Oparin والبريطانية والوراثة التطوري الأحياء جون هالدين مفهوم "الحساء البدائي" 1،2، واصفا المحيطات الأرضية البدائية التي تحتوي على المركبات العضوية التي قد تكون سهلت التطور الكيميائية. ومع ذلك، لم يكن حتى 1950s عندما بدأت الكيميائيين لإجراء الدراسات المختبرية متعمدة تهدف إلى فهم كيف يمكن أن الجزيئات العضوية قد تم تصنيعه من المواد الأولية البسيطة على الأرض في وقت مبكر. كان واحدا من التقارير الأولى لهذه الغاية تخليق حمض الفورميك من تشعيع مائي CO 2 حلول عام 1951 3.
في عام 1952، ستانلي ميلر، ثم وهو طالب دراسات عليا في جامعة شيكاغو، اقترب هارولد أوري عن القيام تجربة لتقييم إمكانية أن المركبات العضويةالمهم لأصل الحياة قد تشكلت abiologically على الأرض في وقت مبكر. وقد أجريت التجربة باستخدام جهاز الزجاج مبنية خصيصا (الشكل 1A) مصممة لمحاكاة الأرض البدائية. تجربة ميلر تحاكي البرق بفعل التفريغ الكهربائي على مزيج من الغازات التي تمثل الغلاف الجوي في وقت مبكر، في وجود خزان للمياه السائلة، التي تمثل المحيطات في وقت مبكر. أيضا محاكاة جهاز التبخر وهطول الأمطار من خلال استخدام عباءة التدفئة ومكثف، على التوالي. تفاصيل محددة عن جهاز يستخدم ميلر يمكن العثور في أي مكان آخر 4. بعد أسبوع من اثارة، تم تحويل محتويات القارورة بشكل واضح. الماء تحولت عكر، اللون المحمر 5 والأصفر والبني المواد المتراكمة على الأقطاب 4. ويعتبر هذا العمل الرائد لتكون أول المتعمد، والتوليف كفاءة من الجزيئات الحيوية في ظل ظروف الأرض البدائية المحاكاة.
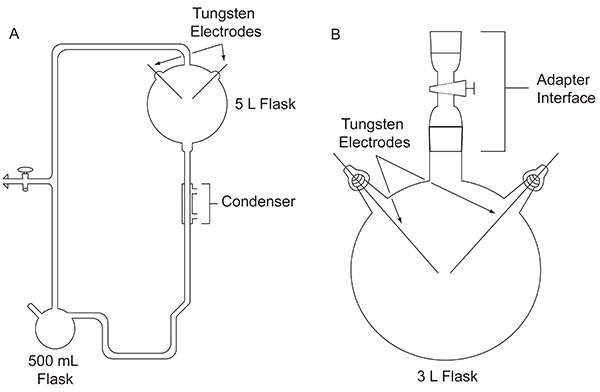
الشكل 1. المقارنة بين هذين النوعين من الأجهزة التي تمت مناقشتها في هذه الورقة. الجهاز الكلاسيكية المستخدمة للتجربة ميلر أوري الأصلي (A) وأجهزة مبسطة المستخدمة في بروتوكول المذكورة هنا (B). اضغط هنا لمشاهدة صورة بشكل اكبر .
بعد نشر عام 1953 من نتائج التجربة الكلاسيكية ميلر، اختلافات عديدة من التجربة تصريف شرارة، على سبيل المثال باستخدام خليط من غازات أخرى أجريت، لاستكشاف معقولية إنتاج المركبات العضوية الهامة للحياة في إطار مجموعة من الشروط الأرض مبكرة محتملة. على سبيل المثال، CH 4 / H 2 O / NH 3 / H تم اختبار 2 خليط الغاز S لقدرته على إنتاج الأحماض المحتوية على الكبريت مشفرة α-الأمينية، وعلى الرغم من أن هذه لم يتم اكتشاف 6. أظهرت اللوني الشامل الغاز الطيف (GC-MS) تحليل لCH 4 / NH 3 خليط تخضع لتفريغ كهربائي تركيب α-aminonitriles، والتي الأمينية حمض السلائف 7. في عام 1972، وذلك باستخدام جهاز أبسط، لأول مرة من قبل ووادي الذهب 8 (الشكل 1B)، تظاهر ميلر وزملاؤه تركيب جميع الأحماض الأمينية α-9 مشفرة والأحماض الأمينية اللابروتيني 10 التي تم تحديدها في نيزك مورشيسون حتى الآن، بإخضاع CH 4، N 2، وكميات صغيرة من NH 3 إلى التفريغ الكهربائي. في وقت لاحق، وذلك باستخدام نفس هذا التصميم التجريبي مبسطة، مخاليط الغاز التي تحتوي على H 2 O، N 2، وCH 4، CO 2، CO أو وأثار لستودى العائد من سيانيد الهيدروجين، والفورمالديهايد، والأحماض الأمينية بوصفها وظيفة من الدولة أكسدة الأنواع الكربون في الغلاف الجوي 11.
بالإضافة إلى استكشاف التصاميم التجريبية البديلة على مدى السنوات، حدثت التطورات التحليلية كبيرا منذ تجربة ميلر الكلاسيكية، والتي ساعدت مؤخرا تحقيقات أكثر تفحصا من العينات التجريبية التفريغ الكهربائي أرشفة بواسطة ميلر، من شأنه أن تم بتسهيل من التقنيات كان ميلر الوصول إلى في 1950s. تجربة ميلر البركانية 12، لاول مرة في عام 1955 4، و1958 H 2 عرضت S المحتوية على تجربة 13 قد شكلت مجموعة متنوعة أوسع، وفرة أكبر، العديد من الأحماض الأمينية والأمينات من التجربة الكلاسيكية، بما في ذلك كثير منها أن لم يتم تحديدها من قبل في تجارب التفريغ شرارة.
ويمكن إجراء هذه التجربة وصفها في هذه الورقة باستخداممجموعة متنوعة من مخاليط الغاز. عادة، على أقل تقدير، سوف تحتوي على مثل هذه التجارب غاز C الحاملة، وهو غاز N-اضعة، والماء. مع بعض التخطيط، أي ما يقرب من خليط من الغازات يمكن استكشافها، ومع ذلك، فمن المهم النظر في بعض الجوانب الكيميائية للنظام. على سبيل المثال، يمكن أن درجة الحموضة من المرحلة المائية يكون لها تأثير كبير على الكيمياء التي تحدث هناك 14.
تم الطريقة الموصوفة هنا مصممة لإرشاد الباحثين كيفية إجراء تجارب التفريغ الشرارة التي تشبه التجربة ميلر أوري باستخدام مبسطة عاء التفاعل 3 L، كما هو موضح في عام 1972 المنشورات ميلر 9،10. منذ هذه التجربة ينطوي على القوس الكهربائي ذات الجهد العالي تعمل على غازات قابلة للاشتعال، لا بد من إزالة O 2 من دورق التفاعل للقضاء على خطر الانفجار، والتي يمكن أن تحدث عند احتراق خفض الغازات الحاملة للكربون مثل الميثان أو غاز أول أكسيد الكربون، أو رد فعل سو H 2 مع الأكسجين.
هناك تفاصيل إضافية التي يجب أن يوضع في الاعتبار عند إعداد لإجراء التجربة تمت مناقشتها هنا. الأولى، عندما تعمل مع خطوط فراغ الزجاج والغازات المضغوطة، هناك الخطر المتأصل في كل من الانهيار والإفراط في الضغط، لذلك، يجب إرتداء نظارات السلامة في جميع الأوقات، وثانيا، وعادة ما تجرى التجربة في أقل من الضغط الجوي. هذا يقلل من خطر الإفراط في الضغط على مشعب ودورق التفاعل. الأواني الزجاجية قد يتم تقييم عند أو فوق الضغط الجوي، ومع ذلك، لا ينصح الضغوط أعلاه 1 أجهزة الصراف الآلي. الضغوط قد تزيد في هذه التجارب كما H غير قابلة للذوبان في الماء 2 يتحرر من خفض الغازات (مثل CH 4 و NH 3). يمكن أن يؤدي الإفراط في الضغط إلى تسرب الختم، والتي يمكن أن تسمح O 2 في الغلاف الجوي للدخول في دورق التفاعل، مما يجعل من الممكن للحث على الاحتراق، مما أدى إلى انفجار. الثالثة،ينبغي أن يوضع في الاعتبار أن تعديل هذا البروتوكول لإجراء أشكال مختلفة من التجربة يتطلب التخطيط الدقيق لضمان عدم خلق ظروف غير آمنة. الرابع، يوصى بشدة أن المجرب المحتملين من خلال قراءة البروتوكول بأكمله عدة مرات بعناية قبل محاولة هذه التجربة للتأكد من انه أو انها على دراية المزالق المحتملة وأن جميع الأجهزة اللازمة متوفرة في مكان و. أخيرا، إجراء التجارب التي تنطوي على الغازات القابلة للاحتراق تتطلب الامتثال الصحة البيئية والسلامة المبادئ التوجيهية للإدارات المؤسسة المضيفة المجرب ل. يرجى مراعاة هذه التوصيات قبل الشروع في أي تجارب. جميع الخطوات المفصلة في البروتوكول هنا هي في الامتثال المضيف المبادئ التوجيهية الصحة البيئية والسلامة المؤسسية المؤلفين.
Protocol
1. وضع نظام المنوع / فراغ
- استخدام الزجاج متعددة لإدخال الغازات في دورق التفاعل. هذا مشعب يمكن شراؤها أو التي شيدت من قبل منشأة نفخ الزجاج، ولكن يجب أن تشمل الموانئ فراغ ضيق التي يمكن توصيلها إلى نظام فراغ، واسطوانات الغاز، وهو مقياس فراغ، وعاء التفاعل.
- استخدام الزجاج المفاصل الأرض والمقابس الزجاج مع الصمامات على مشعب. التأكد من أن جميع حلقات O على المقابس قادرون على صنع الاختام اللازمة. في حالة استخدام الزجاج المفاصل، وكمية كافية من الشحوم فراغ يمكن تطبيقها للمساعدة في جعل ختم، إذا لزم الأمر. السيليكون الشحوم فراغ يمكن استخدامها لتجنب التلوث العضوية المحتملة.
- استخدام الصمامات الزجاج على مشعب. تطبيق الحد الأدنى من فراغ الشحوم اللازمة لجعل الختم.
- قياس حجم متعددة. سيتم استخدام هذا المجلد لإجراء العمليات الحسابية المتعلقة الضغوط الغاز النهائية في 3 L رد فعل قارورة وينبغي أن يكون معروفا على وجه الدقة.
- ما لم يكن لديها ما يكفي متعددة اتصالات لاستيعاب جميع اسطوانات الغاز في وقت واحد، وربط اسطوانة واحدة في وقت لمشعب. تدرج في هذا الصدد، حنفية السماح مشعب أن تكون معزولة عن الجو المحيط.
- استخدام مناسبة ونظيفة، خامل، والكيميائية وتسرب أنابيب مقاومة والتجهيزات فراغ ultratorr لتوصيل اسطوانات الغاز الى مشعب. التجهيزات Ultratorr، حيث استخدمت، أن تكون تشديد إصبع.
- اتصال متعددة، ومضخة فراغ قادرة على إنشاء فراغ <1 مم زئبق. يجب أن يكون موجودا العادم مضخة فراغ داخل غطاء الدخان، أو تنفيس بشكل صحيح عن طريق وسائل أخرى.
- لضمان تحقيق السريع للفراغ وحماية المضخة، اضافة الى وجود فخ بين متعددة ومضخة فراغ. ينصح السائل النيتروجين الاصبع فخ لأنها سوف تمنع المواد المتطايرة مثل NH 3، CO 2 و H 2 O من دخول المضخة. ينبغي توخي الحذر، والمواد المتطايرة المحاصرين، عند واrming، قد مشعب الضغط الزائد وتؤدي إلى تمزق الزجاج.
- الاتصال المتعددة، ومقياس ضغط الدم أو غيرها من قياس الفراغ قادر على 1 مم زئبق القرار أو أفضل منه. بينما الأجهزة المختلفة يمكن استخدامها، ومقياس ضغط الدم الزئبق، أو مقياس ماكلويد، يفضل كما هو الزئبق متأخرا إلى حد ما.
- قياس وتسجيل درجة الحرارة المحيطة باستخدام ميزان حرارة مناسبة.
2. إعداد رد فعل قارورة
- تسخين جميع الأواني الزجاجية عند 500 درجة مئوية لمدة لا تقل عن 3 ساعة في الهواء قبل استخدامها، لإزالة الملوثات العضوية.
- تنظيف أقطاب التنغستن عن طريق غسل بلطف مع مناديل المختبر نظيفة والميثانول، والتجفيف في الهواء.
- صب 200 مل من الماء عالى النقاء (18.2 MΩ سم، <5 جزء في البليون TOC) في 3 L رد فعل قارورة.
- يعرض شريط مغناطيسي precleaned وتعقيمها، والتي سوف ضمان حل سريع للغازات القابلة للذوبان وخلط المواد المتفاعلة أثناء السابقينperiment.
- نعلق الأقطاب الكهربائية التنغستن إلى 3 L دورق التفاعل باستخدام كمية ضئيلة من الشحوم فراغ، مع نصائح مفصولة حوالي 1 سم داخل القارورة. ربط مع لقطات.
- إدراج محول مع محبس المدمج في في الرقبة من 3 L رد فعل قارورة وتأمين مع مقطع.
- نعلق 3 L رد فعل قارورة لمشعب الغاز عبر محول. استخدام المشبك مقطع أو للمساعدة في تأمين القارورة.
- بخفة الشحوم كافة الاتصالات لضمان ختم فراغ جيدة.
- فتح جميع الصمامات والصمامات على مشعب، باستثناء صمام محبس 6 و 1 (الشكل 4)، وتشغيل مضخة فراغ لاجلاء متعددة. مرة واحدة وقد تم تحقيق قراءة مستقرة من فراغ <1 ملم زئبقي، صمام إغلاق 1 والسماح متعددة للجلوس ل~ 15 دقيقة للتحقق من وجود تسرب فراغ. إذا تم الكشف عن لا شيء، انتقل إلى الخطوة 2.8. خلاف ذلك استكشاف الاتصالات المختلفة حتى يمكن التعرف على التسريبات وإصلاحها.
- Aبتقديم طلب التحريك المغناطيسي لوعاء التفاعل. فتح صمام محبس 1 و 1 (الشكل 4) لاخلاء فراغ الرأس من 3 L رد فعل قارورة حتى وصلت الى الضغط <1 مم زئبق.
- إغلاق صمام 1 (الشكل 4) ومراقبة الضغط داخل 3 L رد فعل قارورة. قياس الضغط يجب أن يرتفع إلى ضغط بخار الماء. لضمان عدم تسرب موجودة، انتظر ~ 5 دقائق في هذه المرحلة. إذا كان الضغط (كما قرأت على مقياس ضغط الدم) يزيد أثناء إغلاق صمام 1 خلال هذه الخطوة، والتحقق من وجود تسرب في محبس 1 ومختلف الاتصالات دورق التفاعل. إذا تم العثور على أي تسرب، انتقل إلى الخطوة التالية.
3. إدخال الغازية NH 3
- حساب الضغط اللازم من الغازية NH 3 لندخل في مشعب بحيث 200 ملم زئبقي من NH 3 سيتم إدخالها في دورق التفاعل. وتقدم التفاصيل حول كيفية القيام بذلك في قسم مناقشة.
- وثيقة صمامات1 و 6، ومحبس 1 (الشكل 4) قبل إدخال أي غاز في مشعب. ترك الصمامات الأخرى ومحبس مفتوحة.
- أعرض NH 3 في مشعب حتى يتم التوصل إلى الضغط صغيرة (حوالي 10 مم زئبق) ومن ثم إخلاء متعددة لضغط من <1 مم زئبق عن طريق فتح صمام 1 (الشكل 4). تكرار 3X.
- أعرض NH 3 في مشعب للوصول إلى ضغط تحديدها في الخطوة 3.1.
- فتح محبس 1 (الشكل 4) لإدخال 200 ملم زئبقي من NH 3 في 3 L رد فعل قارورة. فإن NH 3 تذوب في الماء في دورق التفاعل وسوف تقع الضغط ببطء.
- بمجرد الضغط يتوقف اسقاط وثيقة محبس 1 (الشكل 4) وتسجيل ضغط تلاه مقياس ضغط الدم. تمثل هذه القيمة الضغط داخل القارورة وسوف تستخدم لحساب الضغوط للغازات الأخرى التي سيتم إدخالها في مشعب في وقت لاحق. فتح صمام 1 (الشكل 4) لاخلاء متعددة لضغط من <1 مم زئبق.
- إغلاق صمام 2 (الشكل 4) وافصل اسطوانة الغاز NH 3 من مشعب.
4. إدخال CH 4
- حساب الضغط اللازم من CH 4 إلى إدخالها في مشعب بحيث 200 ملم زئبقي من CH 4 سيتم إدخالها في 3 L رد فعل قارورة. وتظهر الحسابات سبيل المثال في قسم مناقشة.
- توصيل أسطوانات الغاز CH 4 إلى مشعب.
- فتح جميع الصمامات والصمامات، باستثناء صمام محبس 6 و 1 (الشكل 4)، وإخلاء متعددة لضغط من <1 مم زئبق.
- وثيقة صمام 1 مرة واحدة وقد تم اجلاء مشعب (الشكل 4).
- أعرض CH 4 في مشعب حتى يتم الحصول على الضغط صغيرة (حوالي 10 مم زئبق). هذا التطهير خط أي غازات ملوثة الابالسابقة ام الخطوات. فتح صمام 1 (الشكل 4) لاخلاء متعددة ل<1 مم زئبق. تكرار 2X أكثر من ذلك.
- أعرض CH 4 في مشعب حتى الضغط المحسوبة في الخطوة 4.1، يتم التوصل إليه.
- فتح محبس 1 (الشكل 4) لإدخال 200 ملم زئبقي من CH 4 إلى 3 L رد فعل قارورة.
- وثيقة محبس 1 مرة واحدة وقد تم إدخال الضغط المقصود من CH 4 إلى 3 L رد فعل قارورة (الشكل 4) وتسجيل ضغط يقاس مقياس ضغط الدم.
- فتح صمام 1 (الشكل 4) لاخلاء متعددة ل<1 مم زئبق.
- إغلاق صمام 2 (الشكل 4) وفصل CH 4 أسطوانات من مشعب.
5. إدخال مزيد من غازات (مثل N 2)
- عند هذه النقطة، فإنه ليس من الضروري أن أعرض الغازات إضافية. ومع ذلك، إذا رغبت في ذلك، فمن المستحسن لإضافة 100 ملم زئبقي من N 2. في هذه الحالة، وحساب الضغط اللازم من N 2 إلى إدخالها في مشعب مثل أن 100 ملم زئبقي من N 2 سيتم عرضه في 3 L رد فعل قارورة. وتظهر الحسابات سبيل المثال في قسم مناقشة.
- توصيل اسطوانة غاز N 2 إلى مشعب.
- فتح جميع الصمامات والصمامات، باستثناء صمام محبس 6 و 1 (الشكل 4)، وإخلاء متعددة لضغط من <1 مم زئبق.
- وثيقة صمام 1 مرة واحدة وقد تم اجلاء مشعب (الشكل 4).
- أعرض N 2 في مشعب حتى يتم الحصول على الضغط صغيرة (حوالي 10 مم زئبق). فتح صمام 1 (الشكل 4) لاخلاء متعددة ل<1 مم زئبق. تكرار 2X أكثر من ذلك.
- أعرض N 2 في مشعب حتى يتم الوصول إلى الضغط المحسوب في الخطوة 5.1.
- فتح محبس 1 (الشكل 4) لإدخال 100 ملم زئبقي من N 2 في دورق التفاعل.
- وثيقة محبس 1 مرة واحدة وقد تم إدخال الضغط المقصود من N 2 في دورق التفاعل، (الشكل 4) وتسجيل الضغط باستخدام مقياس ضغط الدم.
- فتح صمام 1 (الشكل 4) لاخلاء متعددة ل<1 مم زئبق.
- إغلاق صمام 2 (الشكل 4) وقطع الاسطوانة N 2 من مشعب.
6. بداية التجربة
- فصل دورق التفاعل من مشعب عن طريق إغلاق محبس 1 وصمام 1 (الشكل 4) مرة واحدة وقد تم إدخال جميع الغازات في دورق التفاعل، بحيث الهواء المحيط قد تدخل المتعددة وتقديم متعددة تصل إلى الضغط المحيط.
- بعد فصل بعناية دورق التفاعل من متعددة، وتعيين القارورة في مكان ما لن تكون منزعجة ذلك (على سبيل المثال داخل غطاء الدخان فارغة).
- افصل مضخة الفراغ وإزالة بعناية في فخ الباردة والسماح التنفيس داخل بالكاملالتشغيلية غطاء الدخان.
- تأمين لفائف تسلا متصلا عالية التردد مولد شرارة.
- الاتصال العكس التنغستن القطب إلى الأرض الكهربائية لتمكين مرور كفاءة من التيار الكهربائي عبر الفجوة بين القطبين.
- تعيين الجهد الناتج من المولد إلى ما يقرب من 30،000 شرارة V، على النحو الذي فصله الوثائق المتاحة من الشركة المصنعة.
- قبل بدء شرارة، أغلق غطاء الدخان وشاح، لتكون بمثابة درع السلامة بين أجهزة والمجرب. تحويل لفائف تسلا على أن تبدأ التجربة، والسماح مما أثار أن يستمر لمدة 2 أسابيع (أو فترة أخرى مرغوبة) في 1 ساعة تشغيل / إيقاف دورات.
7. نهاية التجربة
- إيقاف التجربة عن طريق إيقاف لفائف تسلا.
- فتح محبس 1 (الشكل 4) لإدخال الهواء المحيط ببطء في دورق التفاعل وتسهيل إزالة محول والأقطاب الكهربائية التنغستن ذلك ساويمكن جمع mples. إذا رغبت في ذلك، فراغ يمكن استخدامها لإخلاء دورق التفاعل من الغازات الضارة رد فعل.
8. جمع عينة السائل
- باستخدام ماصة الزجاج pyrolyzed، وإزالة عينات السائل من دورق التفاعل، والحرص على التقليل من التعرض للملوثات، مثل تلك التي قد تكون أدخلت عن طريق لمس ماصة للالشحوم فراغ أو الأسطح غير المعقمة الأخرى.
- نقل العينة إلى بلاستيكية معقمة أو الزجاج عاء. أوعية من البلاستيك هي أقل عرضة للتشقق أو كسر على تجميد، مقارنة أوعية زجاجية.
- حاويات ختم العينة وتخزينها في الفريزر قادرة على الوصول إلى درجة حرارة -20 درجة مئوية أو أقل، كما قد تمنع منتجات غير قابلة للذوبان في محلول العينة من التجمد في 0 درجة مئوية.
9. تنظيف جهاز
- استخدام المختبر نظيفة مناديل لإزالة الشحوم فراغ بعناية من عنق الجهاز، والتكيفإيه ومحبس، والزجاج المحيطة أقطاب التنغستن.
- تماما تنظيف الأسطح نفسه هو موضح في الخطوة 9.1 مع التولوين لإزالة الشحوم فراغ كامل العضوية من الأواني الزجاجية. في حالة استخدام الشحوم السيليكون، قد تبقى الشحوم فراغ عالية على الأواني الزجاجية بعد الانحلال الحراري، وخلق مشاكل في المستقبل، كما هو مفصل في القسم مناقشة.
- تنظيف شامل في دورق التفاعل مع فرشاة والمذيبات التالية بالترتيب: الماء عالى النقاء (18.2 MΩ سم، <5 جزء في البليون TOC)، الماء عالى النقاء (18.2 MΩ سم، <5 جزء في البليون TOC) مع 5٪ التنظيف والمنظفات والميثانول، التولوين، الميثانول والماء عالى النقاء (18.2 MΩ سم، <5 جزء في البليون TOC) مع 5٪ التنظيف والمنظفات، وأخيرا الماء عالى النقاء (18.2 MΩ سم، <5 جزء في البليون TOC).
- تغطية جميع فتحات مفتوحة من دورق التفاعل مع رقائق الألومنيوم والتفاف محول ومكوناته في رقائق الألومنيوم.
- مرة واحدة وقد تم التفاف جميع الأواني الزجاجية في رقائق الألومنيوم، pyrolyze لا يقل عن 3 في ساعةالهواء في 500 درجة مئوية.
- أقطاب نظيفة بلطف مع الميثانول والسماح الهواء الجاف.
10. تحليل عينة
ملاحظة: عند إعداد العينات للتحليل، وقد وصفت استخدام بروتوكول التحلل حمض مثل بالتفصيل في مكان آخر 15، مفيد للحصول على الأحماض الأمينية أكثر. التحلل من جزء من العينة المستردة يتيح الفرصة لتحليل كل من الأحماض الأمينية الحرة وكذلك السلائف حمض عطوب الخاصة التي يتم توليفها في ظل ظروف غير الحيوية.
- لتحليل الأحماض الأمينية، واستخدام تقنية مناسبة (مثل اللوني السائل والأساليب المستندة إلى مطياف الكتلة، أو النهج مناسبة أخرى). وتشمل هذه التقنيات التحليلية عالية الأداء اللوني السائل مع الكشف عن مضان (HPLC-FD) 14، وعالية جدا الأداء اللوني السائل مع الكشف عن مضان بالتوازي مع مرور الوقت من الطيران إيجابية مطياف الكتلة electrospray التأين (UHPLC-FD/ToF-MS) 12،13. يصف هذا المخطوط التحليل الطيفي الشامل باستخدام تحليلات عن طريق الثلاثي رباعية مطياف الكتلة (MS-QQQ) بالتزامن مع HPLC-FD.
النتائج
المنتجات توليفها في تجارب التفريغ الكهربائي يمكن أن تكون معقدة جدا، وهناك العديد من المقاربات التحليلية التي يمكن استخدامها لدراستها. وتناقش بعض التقنيات المستخدمة أكثر شيوعا في الأدبيات لتحليل الأحماض الأمينية هنا. طرق الطيفي الكروماتوغرافي والكتلة هي تقنيات مع?...
Discussion
خطوات عديدة في بروتوكول الموصوفة هنا هي الحاسمة لإجراء تجارب ميلر أوري نوع بأمان وبشكل صحيح. الأولى، وجميع الأواني الزجاجية والتعامل مع عينة الأدوات التي سوف تأتي في اتصال مع دورق التفاعل أو عينة تحتاج إلى أن تكون معقمة. ويتحقق التعقيم من قبل الشطف بدقة العناصر في ال...
Disclosures
الكتاب تعلن أي المصالح المالية المتنافسة.
Acknowledgements
وأيد هذا العمل بشكل مشترك من قبل جبهة الخلاص الوطني وبرنامج البيولوجيا الفلكية ناسا، في إطار جبهة الخلاص الوطني مركز للتطور الكيميائي، CHE-1004570، ومركز غودارد للالبيولوجيا الفلكية. سوف ETP ترغب في الاعتراف التمويل الإضافية التي تقدمها لبرنامج علم الأحياء متدرب ناسا الكواكب. نريد الكتاب أيضا أن أشكر الدكتور عسيري Galhena للمساعدة لا تقدر بثمن في إنشاء مرافق المختبرات الأولي.
Materials
| Name | Company | Catalog Number | Comments |
| Glass Plugs for Manifold | Chemglass | CG-983-01 | |
| High Vacuum Grease | Apiezon | N/A | Type M/N |
| Silicon High Vacuum Grease | Dow Corning | 1597418 | |
| Teflon PFA Tubing | McMaster-Carr | 51805K54 | |
| Ultra-Torr Vacuum Fittings | Swagelok | SS-4-UT-6 | |
| Dry Scroll Vacuum Pump | Edwards | A72401905 | |
| U-Tube Manometer | Alta-Robbins | 100SS | |
| Tungsten Electrodes | Diamond Ground Products | TH2-1/16 | 2% thoriated |
| Methanol | Alfa Aesar | N/A | Ultrapure HPLC Grade |
| Teflon-Coated Magnetic Stir Bar | McMaster-Carr | 5678K127 | |
| Gaseous NH3 | Airgas | AMAHLB | 99.99% purity |
| Gaseous CH4 | Airgas | ME UHP300 | 99.99% purity |
| Gaseous N2 | Airgas | NI UHP300 | 99.999% purity |
| Tesla Coil | Electro-Technic Products | 15001 | Model BD-50E |
| 24 hr Plug-in Basic Timer | General Electric Company | 15119 | |
| Cleaning Detergent | Alconox | 1104 | |
| Toluene | Thermo Fisher Scientific | N/A | Optima Grade |
| Luna Phenyl-Hexyl HPLC Column | Phenomenex | 00G-4257-E0 | Brand: Luna |
| Formic Acid | Sigma-Alrich | F0507 | Used to make 50 mM ammonium formate |
References
- Oparin, A. I. . The Origin of Life. , (1924).
- Haldane, J. B. The origin of life. Rationalist Annu. 148, 3-10 (1929).
- Garrison, W. M., Morrison, D. C., Hamilton, J. G., Benson, A. A., Calvin, M. Reduction of Carbon Dioxide in Aqueous Solutions by Ionizing Radiation. Science. 114, 416-418 (1951).
- Miller, S. L. Production of Some Organic Compounds under Possible Primitive Earth Conditions. J. Am. Chem. Soc. 77, 2351-2361 (1955).
- Miller, S. L. A Production of Amino Acids Under Possible Primitive Earth Conditions. Science. 117, 528-529 (1953).
- Heyns, H. K., Walter, W., Meyer, E. Model experiments on the formation of organic compounds in the atmosphere of simple gases by electrical discharges (Translated from German). Die Naturwissenschaften. 44, 385-389 (1957).
- Ponnamperuma, C., Woeller, F. α-Aminonitriles formed by an electric discharge through a mixture of anhydrous methane and ammonia. Biosystems. 1, 156-158 (1967).
- Oró, J. Synthesis of Organic Compounds by Electric Discharges. Nature. 197, 862-867 (1963).
- Ring, D., Wolman, Y., Friedmann, N., Miller, S. L. Prebiotic Synthesis of Hydrophobic and Protein Amino Acids. Proc. Natl. Acad. Sci. U.S.A. 69, 765-768 (1972).
- Wolman, Y., Haverland, W. J., Miller, S. L. Nonprotein Amino Acids from Spark Discharges and Their Comparison with the Murchison Meteorite Amino Acids. Proc. Natl. Acad. Sci. U.S.A. 69, 809-811 (1972).
- Roscoe, S., Miller, S. L. Energy Yields for Hydrogen Cyanide and Formaldehyde Syntheses: The HCN and Amino Acid Concentrations in the Primitive Ocean. Orig. Life. 17, 261-273 (1987).
- Johnson, A. P., et al. The Miller Volcanic Spark Discharge Experiment. Science. 322, 404 (2008).
- Parker, E. T., et al. Primordial synthesis of amines and amino acids in a 1958 Miller H2S-rich spark discharge experiment. Proc. Natl. Acad. Sci. U.S.A. 108, 5526-5531 (2011).
- Cleaves, H. J., Chalmers, J. H., Lazcano, A., Miller, S. L., Bada, J. L. A reassessment of prebiotic organic synthesis in neutral planetary atmospheres. Orig. Life Evol. Biosph. 38, 105-115 (2008).
- Glavin, D. P., et al. Amino acid analyses of Antarctic CM2 meteorites using liquid chromatography-time of flight-mass spectrometry. Meteorit. Planet. Sci. 41, 889-902 (2006).
- Zhao, M., Bada, J. L. Determination of α-dialkylamino acids and their enantiomers in geologic samples by high-performance liquid chromatography after a derivatization with a chiral adduct of o-phthaldialdehyde. J. Chromatogr. A. 690, 55-63 (1995).
- Strecker, A. About the artificial formation of lactic acid and a new Glycocoll the homologous body Justus Liebigs Annalen der Chemie. 75, 27-45 (1850).
- Miyakawa, S., Yamanashi, H., Kobayashi, K., Cleaves, H. J., Miller, S. L. Prebiotic synthesis from CO atmospheres: implications for the origins of life. Proc. Natl. Acad. Sci. U.S.A. 99, 14628-14631 (2002).
- Kobayashi, K., Kaneko, T., Saito, T., Oshima, T. Amino Acid Formation in Gas Mixtures by Particle Irradiation. Orig. Life Evol. Biosph. 28, 155-165 (1998).
- Sagan, C., Khare, B. N. Long-Wavelength Ultraviolet Photoproduction of Amino Acids on the Primitive Earth. Science. 173, 417-420 (1971).
- Harada, K., Fox, S. W. Thermal Synthesis of Natural Amino-Acids from a Postulated Primitive Terrestrial Atmosphere. Nature. 201, 335-336 (1964).
- Ponnamperuma, C., Lemmon, R. M., Mariner, R., Calvin, M. Formation of Adenine by Electron Irradiation of Methane Ammonia, and Water. Proc. Natl. Acad. Sci. USA. 49, 737-740 (1963).
- Bar-Nun, A., Bar-Nun, N., Bauer, S. H., Sagan, C. Shock Synthesis of Amino Acids in Simulated Primitive Environments. Science. 168, 470-473 (1970).
Reprints and Permissions
Request permission to reuse the text or figures of this JoVE article
Request PermissionExplore More Articles
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. All rights reserved