A subscription to JoVE is required to view this content. Sign in or start your free trial.
Method Article
وسطحي جدا وصديقة للبيئة الطريق إلى افتعال بولي (حمض اللاكتيك) السقالات مع متدرج مسام الحجم
In This Article
Summary
In this work, poly(lactic acid)/polyethylene glycol (PLA/PEG) scaffolds were prepared by using a combination of melt mixing and selective leaching. The method herein discussed permitted to develop three-layer scaffolds by highly controlling both porosity and pore size. The mechanical properties were also evaluated in a physiological environment.
Abstract
Over the recent years, functionally graded scaffolds (FGS) gaineda crucial role for manufacturing of devices for tissue engineering. The importance of this new field of biomaterials research is due to the necessity to develop implants capable of mimicking the complex functionality of the various tissues, including a continuous change from one structure or composition to another. In this latter context, one topic of main interest concerns the design of appropriate scaffolds for bone-cartilage interface tissue. In this study, three-layered scaffolds with graded pore size were achieved by melt mixing poly(lactic acid) (PLA), sodium chloride (NaCl) and polyethylene glycol (PEG). Pore size distributions were controlled by NaCl granulometry and PEG solvation. Scaffolds were characterized from a morphological and mechanical point of view. A correlation between the preparation method, the pore architecture and compressive mechanical behavior was found. The interface adhesion strength was quantitatively evaluated by using a custom-designed interfacial strength test. Furthermore, in order to imitate the human physiology, mechanical tests were also performed in phosphate buffered saline (PBS) solution at 37 °C. The method herein presented provides a high control of porosity, pore size distribution and mechanical performance, thus offering the possibility to fabricate three-layered scaffolds with tailored properties by following a simple and eco-friendly route.
Introduction
The interest in biodegradable polymers has grown in importance during the last years both in academia and in the industry, due to the rising concerns regarding plastic waste and the reduction in using non-renewable sources1-7. In particular, biocompatible and biodegradable synthetic polymers are widespread in several biomedical application fields, such as drug controlled release8,9, absorbable suture threads8,10, bioprocess intensification11 and tissue engineering12.
Tissue engineering focuses on the development of devices capable to restore and maintain normal function in diseased or injured tissues. Most of the native tissues are composed by different types of cells and extracellular matrices (ECMs) in specific spatial hierarchies. For example, articular cartilage (AC) consists of different zones with varying types and orientations of collagen fibers and collagen-binding proteins. Moreover, cartilage and bone show significantly different hierarchical structures. In this context, the preparation of multilayer scaffolds with engineered properties in each layer could allow replacing heterogeneous tissues by taking into accounts all the local microenvironments of these complex systems13,14.
Based on the cellular/biological and/or physical-chemical characteristics of the scaffolds, the main strategies adopted by the tissue engineering can be divided into monophasic, biphasic, and triphasic. Biphasic and triphasic approaches (BTA) use two or three different pores architectures, materials, or fillers to prepare multilayered functional devices. Furthermore, a single material can be used to achieve biphasic or triphasic devices, as long as it is possible to create a gradient in its physical properties12.
Cell migration plays a key-role in the morphogenesis, inflammation, wound healing and tumor metastasis. Cell movement is encouraged by the presence of a gradient of chemical-physical properties from the surface to the core of the device. Therefore, biomaterials fulfilling the above discussed requirements can be helpful in studying cell migration. In addition to chemical gradients that trigger cells migration (chemotaxis), mechanical properties of cells culture substrate can also lead to cell movement (mechanotaxis)15.
The multilayer structure can also provide the tunable release of specific drugs incorporated within the polymer matrix, by changing the specific area of the layer or the amount of loaded drugs.
Over the past decade, in order to develop scaffolds possessing a discrete or continuous gradient of morphological properties, such as porosity or pore size, several approaches have been presented16-31. The most recent papers focused on the preparation of BTA by adopting: particle leaching 12,28,32, gas foaming technique16, electrospinning17-19, layer by layer casting technique20, rapid prototyping21,22, thermally induced phase separation (TIPS)22, centrifugation freeze drying24,25, triply periodic minimal surfaces (TPMS)26, freeze casting27-30.
Within the frame of this work, we present a fast and simple route to achieve PLA-based three-layer porous scaffolds (TLS), by combining melt mixing, compression molding and salt leaching. Differently from most of the technologies commonly used for scaffold production, the strategy herein adopted can be considered fully eco-friendly, since it does not require any toxic solvent potentially dangerous for environment and for living cells and tissues32. The basic processing-structure-property relationships established in this study by analyzing both morphological features and mechanical behavior of fabricated devices provide guidance to future advances in designing multifunctional graded scaffolds with specific target properties.
Protocol
1. سقالة تلفيق
- طحن كلوريد الصوديوم في الخلاط مختبر لمدة 20 دقيقة وجففها على سخان عند 100 درجة مئوية.
- وضع كلوريد الصوديوم المجفف (45 غرام في الساعة) في آلة النخل لمدة 30 دقيقة على أعلى تردد متاح بدون تحدث في الرنين. جمع ستة كسور الملح، والتي تتراوح بين 500 ميكرون الى 1000 ميكرون (M 500)؛ من 300 ميكرون إلى 500 ميكرون (M 300)؛ من 100 ميكرون إلى 200 ميكرون (100 م)؛ من 90 ميكرون إلى 100 (م 90). من 45 ميكرون إلى 65 ميكرون (M 45)، وأخيرا M 10 مع جزيئات الملح حجم أصغر من 45 ميكرون كما schematized في الشكل 1.
- فراغ تجف بين عشية وضحاها جميع المواد وذلك لتجنب انفصال متحلل بالماء أثناء معالجة. لكل مادة، حدد درجة حرارة من أجل تحقيق أقصى درجة من تجفيف دون التغلب على - في حالة البوليمرات - الانتقال الزجاج. لذلك، اختيار T = 90 درجة مئوية لمدة جيش التحرير الشعبى الصينى و T = 25 درجة مئوية لمدة PEG، T = 105 درجة مئوية لمدة كلوريد الصوديوم.
- تغذيةجيش التحرير الشعبى الصينى، PEG وكلوريد الصوديوم، مع تكوين الوزن نسبة 20/5/75 على التوالي، لتشغيل دفعة خلاط في T = 190 درجة مئوية و n = 60 دورة في الدقيقة ثم معالجتها حتى تحقيق قيمة ثابتة من عزم الدوران، وعادة بعد حوالي 10 دقائق. بعد ذلك، وجمع بسرعة المواد الناتجة.
- إعداد أحادية الطبقات باستخدام اضغط المختبرات التي تعمل على 210 درجة مئوية، وضعت يمزج في قوالب اسطوانية المناسبة التي يبلغ قطرها 10 ملم وارتفاعه 3 مم والاحتفاظ بها لمدة 60 ثانية في الضغط المحيط و 3 دقائق في 180 شريط . بعد ذلك، تبريد يمزج في درجة حرارة الغرفة، والحفاظ على ضغط 180 بار.
- جمعية ثلاث طبقات عبر ضغط صب
- إعداد كل طبقة واحدة وبنفس الطريقة التي وصفها في (1.5) ولكن باستخدام قوالب مختلفة، أي التي يبلغ قطرها 10 ملم وارتفاعه 1 مم. وأخيرا، يجب الحصول 6 الأقراص التي يبلغ قطرها 10 ملم وارتفاعه من 1 ملم، تحتوي على ستة أحجام الجسيمات مختلفة: M 500، M 300، 100 م،
- فوص تجميع ثلاث طبقات سقالة ألف (TLS أ)، تتراكم M 500، M 300 و 100 م داخل القالب الأسطواني وضغط العفن لهم في الصحافة المختبرات التي تعمل على 210 درجة مئوية لمدة 60 ثانية في الضغط المحيط و 3 دقائق في 180 شريط ثم يبرد في درجة حرارة الغرفة، والحفاظ على ضغط 180 بار.
ملاحظة: إعداد TSL ب التراص على كل M 90، M 45 و M 10 في نفس القوالب وإجراء عملية أخرى صب ضغط باتباع نفس الإجراءات التي تستخدم لTLS أ.
- إزالة الأقراص من قوالب اسطوانية ووضعها في الغليان المنزوعة حمام مائي، من دون اثارة. 3 ساعة بعد إزالة الهياكل التي يسهل اختراقها الناتجة من الحمام والسماح لهم الجافة لمدة 12 ساعة في درجة حرارة الغرفة في غطاء الكيميائية.
2. تحليل الصرفي
- تقييم الأشكال التضاريسية من السقالات بواسطة المجهر الإلكتروني.
- كسر العينات تحت النيتروجين السائل ثم نعلقعينات على كعب الألومنيوم باستخدام الشريط اللاصق الكربون. وأخيرا، تفل-coate مع الذهب لمدة 90 ق تحت جو الأرجون قبل التصوير من أجل تجنب التفريغ الكهربائي أثناء الاختبار.
3. سقالة مسام الحجم
- وضع الصور التي تم الحصول عليها عن طريق تحليل SEM مع برنامج معالجة الصور قادرا على التعرف على توزيع حجم المسام من السقالة.
ملاحظة: في هذا العمل تم إجراء تحليل توزيع حجم المسام من استخدام البرمجيات القائمة على MATLAB-الموصوفة سابقا 33
4. المسامية
- وزن العينات قبل الترشيح وتقييم المسامية النظرية وفقا إلى التعبير التالي:
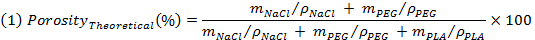
ملاحظة: م كلوريد الصوديوم، م PEG وM جيش التحرير الشعبى الصينى، هي على التوالي الكتلة النظرية من كلوريد الصوديوم، PEG، وجيش التحرير الشعبى الصينى، بافتراض يمزج متجانسة. تانه الكثافات (ρ) من كلوريد الصوديوم، PEG وجيش التحرير الشعبى الصينى هي على التوالي 2،16 جم / سم 3، 1،12 جم / سم 3 ه 1،24 جم / سم 3. - وزن العينات بعد الغسل والتجفيف وذلك لتقييم كثافة واضحة من العينات (ρ سقالة)، ومن ثم تقييم المسامية الحقيقية كما مقلوب النسبة بين كثافة واضحة من السقالة وكثافة غير قابلة للاختراق جيش التحرير الشعبى الصينى من قبل استخدام تعبير (2).
ملاحظة: إنه يعبر عن النسبة بين حجم فارغة من السقالة وحجم الكامل للسقالة (فارغ + كامل).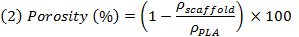
5. الخصائص الميكانيكية
- اختبار العينات تحت وضع الضغط باستخدام آلة الشد، ومجهزة خلية تحميل كيلو نيوتن 1. تعيين معدل الضغط ثابت من 1 ملم دقيقة -1.
- من أجل تحقيق أداء الميكانيكية من العينات في البيئة الفسيولوجية، تجهيز dynamometeص مع حمام تحتوي على (PBS)، (الرقم الهيدروجيني = 7.4) عند 37 درجة مئوية، وإجراء اختبار مع نفس الإعداد التي وصفها عند نقطة 5.1.
- قبل كل قياس في بيئة رطبة، نقع العينات مع برنامج تلفزيوني في قارورة فراغ لمدة 5 دقائق من أجل السماح لبرنامج تلفزيوني ملء جميع المسام. بعد ذلك، والسماح للالسقالات بالبقاء في برنامج تلفزيوني في 37 درجة مئوية لمدة 15 دقيقة للوصول إلى درجة الحرارة المحددة نقطة.
- تحديد قوة التصاق بينية (IAS) بين طبقات TL ألف وTL B باستخدام بينية معدات اختبار قوة مصمم خصيصا، متصلة آلة اختبار الميكانيكية التالية طريقة وصفها في الأدب 32،34.
- إصلاح سقالة على منصة وضمان المحاذاة الصحيحة مع خلية الحمل وقاعدة الصوانى الجهاز. إرفاق عينات سقالة إلى بذرة اختبار الألمنيوم باستخدام مادة لاصقة لزوجة عالية ووضعها في معدات لاختبار.
- لاختبار حالة الرطب، هيدرات العينات في برنامج تلفزيوني لمدة 1 ساعة الحزب الثوري المؤسسيأو الاختبار. استخدام الخلايا تحميل كيلو نيوتن 1، تحت تحميل الشد المطبقة بمعدل سلالة من 1 ملم دقيقة -1.
ملاحظة: خذ بعين الاعتبار أن الفشل قد تحدث إما في نهاية المطاف قوة الشد واحدة من طبقات أو بسبب التبطين في الواجهات. تقييم معيار المحاسبة الدولي باعتبارها القوة القصوى للمنحنى الإجهاد والانفعال.
النتائج
تم تقييم تأثير كلوريد الصوديوم حجم الجسيمات على بنية المسام من السقالات نوعيا وكميا من خلال التحقيق في التشكل من العينات وحساب توزيع حجم المسام عن طريق تحليل صورة، على التوالي الشكل 2A - معارض و الميكروسكوب SEM السقالات أحادية الطبق...
Discussion
الخطوة الأولى الحاسمة هي الأمثل من النخل الكفاءة. سيطرة عالية من حجم الجسيمات كلوريد الصوديوم أساسية لإعداد سقالة مع توزيع حجم المسام المطلوب. خطوة حاسمة أخرى هو تجنب كسر من الطبقات الوحيدة جيش التحرير الشعبى الصينى رقيقة خلال استخراج عينة من القالب. قد لا يكون تحلي?...
Disclosures
The authors declare that they have no competing financial interests.
Acknowledgements
This work was financially supported by INSTM.
Materials
| Name | Company | Catalog Number | Comments |
| Poly(lactic acid) | NatureWorks | PLA 2002D | |
| Poly(ethylene glycol) | Sigma | 83797-1KG-F | |
| Sodium Cloride | Sigma | 793566-5KG-D | |
| Phosfate Buffer Solution | Sigma | P5368-10PAK | |
| Laboratory Mixer | Brabender | PLE 330 - Plasticorder | |
| Laboratory Press | Carver | ||
| Scanning Electron Microscopy | Phenom-world | ProX | |
| Universal Testing Machine | Instron | 3365 (UK) | |
| BioPuls Bath | Instron, Norwood | ||
| Sieving Machine | Endecotts | E.V.F.1. | |
| Vacuum Oven | ISCO | NSV9035 | |
| Precision Balance | Sartorius | AX224 |
References
- Scaffaro, R., Morreale, M., Lo Re, G., Mantia, F. P. La Degradation of Mater-Bi®/wood flour biocomposites in active sewage sludge. Polymer Degradation and Stability. 94 (8), 1220-1229 (2009).
- Scaffaro, R., Botta, L., Passaglia, E., Oberhauser, W., Frediani, M., Di Landro, L. Comparison of different processing methods to prepare poly(lactid acid)-hydrotalcite composites. Polymer Engineering & Science. 54 (8), 1804-1810 (2014).
- Thakur, V. K., Thakur, M. K. Recent advances in graft copolymerization and applications of chitosan: A review. ACS Sustainable Chemistry and Engineering. 2 (12), 2637-2652 (2014).
- Thakur, V. K., Thakur, M. K. Recent advances in green hydrogels from lignin: A review. International Journal of Biological Macromolecules. 72, 834-847 (2015).
- Thakur, V. K., Kessler, M. R. Self-healing polymer nanocomposite materials: A review. Polymer. 69, 369-383 (2015).
- Thakur, V. K., Thakur, M. K. Recent trends in hydrogels based on psyllium polysaccharide: a review. Journal of Cleaner Production. 82, 1-15 (2014).
- Voicu, S. I., Condruz, R. M., et al. Sericin Covalent Immobilization onto Cellulose Acetate Membrane for Biomedical Applications. ACS Sustainable Chemistry & Engineering. 4 (3), 1765-1774 (2016).
- Scaffaro, R., Botta, L., Sanfilippo, M., Gallo, G., Palazzolo, G., Puglia, A. M. Combining in the melt physical and biological properties of poly(caprolactone) and chlorhexidine to obtain antimicrobial surgical monofilaments. Applied Microbiology and Biotechnology. 97 (1), 99-109 (2013).
- Scaffaro, R., Maio, A., et al. Synthesis and self-assembly of a PEGylated-graphene aerogel. Composites Science and Technology. 128, 193-200 (2016).
- Scaffaro, R., Botta, L., Gallo, G., Puglia, A. M. Influence of Drawing on the Antimicrobial and Physical Properties of Chlorhexidine-Compounded Poly(caprolactone) Monofilaments. Macromolecular Materials and Engineering. 12 (300), 1268-1277 (2015).
- Scaffaro, R., Lopresti, F., et al. Effect of PCL/PEG-Based Membranes on Actinorhodin Production in Streptomyces coelicolor Cultivations. Macromolecular bioscience. 16 (5), 686-693 (2016).
- Scaffaro, R., Lopresti, F., Botta, L., Rigogliuso, S., Ghersi, G. Melt Processed PCL/PEG Scaffold With Discrete Pore Size Gradient for Selective Cellular Infiltration. Macromolecular Materials and Engineering. 301 (2), 182-190 (2016).
- Yousefi, A. -. M., Hoque, M. E., Prasad, R. G. S. V., Uth, N. Current strategies in multiphasic scaffold design for osteochondral tissue engineering: A review. Journal of Biomedical Materials Research Part A. 103 (7), 2460-2481 (2015).
- Gillette, B. M., Rossen, N. S., et al. Engineering extracellular matrix structure in 3D multiphase tissues. Biomaterials. 32 (32), 8067-8076 (2011).
- Seidi, A., Ramalingam, M., Elloumi-Hannachi, I., Ostrovidov, S., Khademhosseini, A. Gradient biomaterials for soft-to-hard interface tissue engineering. Acta Biomaterialia. 7 (4), 1441-1451 (2011).
- Son, J. S., Kim, S. G., et al. Hydroxyapatite/polylactide biphasic combination scaffold loaded with dexamethasone for bone regeneration. Journal of Biomedical Materials Research - Part A. 99 (4), 638-647 (2011).
- Sundararaghavan, H. G., Burdick, J. A. Gradients with depth in electrospun fibrous scaffolds for directed cell behavior. Biomacromolecules. 12 (6), 2344-2350 (2011).
- Zou, B., Liu, Y., Luo, X., Chen, F., Guo, X., Li, X. Electrospun fibrous scaffolds with continuous gradations in mineral contents and biological cues for manipulating cellular behaviors. Acta biomaterialia. 8 (4), 1576-1585 (2012).
- Nedjari, S., Schlatter, G., Hébraud, A. Thick electrospun honeycomb scaffolds with controlled pore size. Materials Letters. 142, 180-183 (2015).
- Yusong, P., Qianqian, S., Chengling, P., Jing, W. Prediction of mechanical properties of multilayer gradient hydroxyapatite reinforced poly(vinyl alcohol) gel biomaterial. Journal of Biomedical Materials Research - Part B Applied Biomaterials. 101 (5), 729-735 (2013).
- Kim, Y. B., Kim, G. Functionally graded PCL/β-TCP biocomposites in a multilayered structure for bone tissue regeneration. Applied Physics A: Materials Science and Processing. 108 (4), 949-959 (2012).
- Sudarmadji, N., Tan, J. Y., Leong, K. F., Chua, C. K., Loh, Y. T. Investigation of the mechanical properties and porosity relationships in selective laser-sintered polyhedral for functionally graded scaffolds. Acta biomaterialia. 7 (2), 530-537 (2011).
- Molladavoodi, S., Gorbet, M., Medley, J., Kwon, H. J. Investigation of microstructure, mechanical properties and cellular viability of poly(L-lactic acid) tissue engineering scaffolds prepared by different thermally induced phase separation protocols. Journal of the mechanical behavior of biomedical materials. 17, 186-197 (2013).
- Oh, S. H., Kim, T. H., Il Im, G., Lee, J. H. Investigation of pore size effect on chondrogenic differentiation of adipose stem cells using a pore size gradient scaffold. Biomacromolecules. 11 (8), 1948-1955 (2010).
- Lin, L., Gao, H., Dong, Y. Bone regeneration using a freeze-dried 3D gradient-structured scaffold incorporating OIC-A006-loaded PLGA microspheres based on β-TCP/PLGA. Journal of Materials Science: Materials in Medicine. 26 (1), 3 (2015).
- Yoo, D. Heterogeneous minimal surface porous scaffold design using the distance field and radial basis functions. Medical engineering & physics. 34 (5), 625-639 (2012).
- Soon, Y. -. M., Shin, K. -. H., Koh, Y. -. H., Lee, J. -. H., Choi, W. -. Y., Kim, H. -. E. Fabrication and compressive strength of porous hydroxyapatite scaffolds with a functionally graded core/shell structure. Journal of the European Ceramic Society. 31 (1-2), 13-18 (2011).
- Scaffaro, R., Lopresti, F., Botta, L., Maio, A. Mechanical behavior of Polylactic acid/Polycaprolactone porous layered functional composites. Composites Part B: Engineering. 98, 70-77 (2016).
- Halili, A. N., Hasirci, N., Hasirci, V. A multilayer tissue engineered meniscus substitute. Journal of Materials Science: Materials in Medicine. 25 (4), 1195-1209 (2014).
- Bai, H., Wang, D., et al. Biomimetic gradient scaffold from ice-templating for self-seeding of cells with capillary effect. Acta Biomaterialia. 20, 113-119 (2015).
- Algul, D., Sipahi, H., Aydin, A., Kelleci, F., Ozdatli, S., Yener, F. G. Biocompatibility of biomimetic multilayered alginate-chitosan/β-TCP scaffold for osteochondral tissue. International Journal of Biological Macromolecules. 79, 363-369 (2015).
- Scaffaro, R., Lopresti, F., Botta, L., Rigogliuso, S., Ghersi, G. Preparation of three-layered porous PLA/PEG scaffold relationship between morphology , mechanical behavior and cell permeability. Journal of the Mechanical Behavior of Biomedical Materials. 54, 8-20 (2016).
- Lo Re, G., Lopresti, F., Petrucci, G., Scaffaro, R. A facile method to determine pore size distribution in porous scaffold by using image processing. Micron. 76, 37-45 (2015).
- Levingstone, T. J., Matsiko, A., Dickson, G. R., O'Brien, F. J., Gleeson, J. P. A biomimetic multi-layered collagen-based scaffold for osteochondral repair. Acta Biomaterialia. 10 (5), 1996-2004 (2014).
- Scaffaro, R., Botta, L., Maio, A., Mistretta, M. C., La Mantia, F. P. Effect of Graphene Nanoplatelets on the Physical and Antimicrobial Properties of Biopolymer-Based Nanocomposites. Materials. 9 (5), 351 (2016).
- Maio, A., Fucarino, R., Khatibi, R., Rosselli, S., Bruno, M., Scaffaro, R. A novel approach to prevent graphene oxide re-aggregation during the melt compounding with polymers. Composites Science and Technology. 119, 131-137 (2015).
- Maio, A., Agnello, S., et al. A rapid and eco-friendly route to synthesize graphene-doped silica nanohybrids. Journal of Alloys and Compounds. 664, 428-438 (2015).
- Maio, A., Giallombardo, D., Scaffaro, R., Piccionello, A. P., Pibiri, I. Synthesis of a fluorinated graphene oxide-silica nanohybrid: improving oxygen affinity. RSC Advances. 6 (52), 46037-46047 (2016).
Reprints and Permissions
Request permission to reuse the text or figures of this JoVE article
Request PermissionExplore More Articles
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. All rights reserved