Method Article
اختبار فعالية المضادات الحيوية في نموذج الجسم الحي السابق من Pseudomonas aeruginosa والمكورات العنقودية أوريوس بيو فيلمز في الرئة التليف الكيسي
In This Article
Summary
يمكن استخدام سير العمل هذا لإجراء اختبار قابلية المضادات الحيوية باستخدام نموذج الجسم الحي السابق الراسخ للبيو فيلم البكتيري في رئتي الأفراد المصابين بالتليف الكيسي. استخدام هذا النموذج يمكن أن تعزز الصحة السريرية لل MBEC (الحد الأدنى من تركيز الاستئصال بيو فيلم) المقايسات.
Abstract
إن الوصفة الفعالة للمضادات الحيوية للأغشية الحيوية البكتيرية الموجودة داخل رئتي الأفراد المصابين بالتليف الكيسي (CF) محدودة بسبب ضعف الارتباط بين نتائج اختبار قابلية المضادات الحيوية (AST) باستخدام طرق التشخيص القياسية (على سبيل المثال ، microdilution المرق ، نشر القرص ، أو Etest) والنتائج السريرية بعد العلاج بالمضادات الحيوية. تظهر محاولات تحسين AST من خلال استخدام منصات نمو بيو فيلم الجاهزة تحسنا طفيفا في النتائج. القدرة المحدودة لأنظمة بيو فيلم في المختبر لمحاكاة البيئة الفيزيائية الكيميائية للرئة CF، وبالتالي علم وظائف الأعضاء البكتيرية والهندسة المعمارية بيو فيلم، كما يعمل كفرامل على اكتشاف علاجات جديدة لعدوى CF. هنا، نقدم بروتوكولا لأداء AST من مسببات الأمراض CF نمت ناضجة، في بيو فيلم حي مثل فيفو في نموذج الرئة السابق فيفو CF تتألف من أنسجة الشعب الهوائية الخنزير والبلغم CF الاصطناعية (ex vivo خنزير الرئة، EVPL).
توجد العديد من المقايسات في المختبر لاختبار قابلية الأغشية الحيوية ، وذلك باستخدام إما المتوسط المختبري القياسي أو تركيبات مختلفة من البلغم CF الاصطناعية في لوحات microtiter. كل من النمو المتوسطة والركيزة بيو فيلم (لوحة البوليسترين مقابل الأنسجة القصبية) من المرجح أن تؤثر على التسامح المضادات الحيوية biofilm. نظهر التسامح المعزز من السريرية Pseudomonas aeruginosa و Staphylococcus أوريوس يعزل في نموذج الجسم الحي السابق; لا ترتبط آثار العلاج بالمضادات الحيوية من الأغشية الحيوية مع الحد الأدنى من التركيز المثبط (MIC) في المقايسات microdilution القياسية أو تصنيف حساسة / مقاومة في المقايسات نشر القرص.
يمكن استخدام منصة الجسم الحي السابق ل AST بيو فيلم مفصل من عينات المرضى وكبرنامج اختبار معزز لعوامل أنتيبيو فيلم المحتملة أثناء البحث والتطوير الصيدلانية. تحسين وصفة طبية أو تسريع اكتشاف الأدوية antibiofilm من خلال استخدام أكثر في منصات الاختبار مثل الجسم الحي يمكن أن تحسن بشكل كبير النتائج الصحية للأفراد الذين يعانون من CF، فضلا عن خفض تكاليف العلاج السريري والبحوث الاكتشاف.
Introduction
تؤثر العدوى المزمنة بالبيو فيلم على الأفراد الذين تتعرض دفاعاتهم المناعية العادية للخطر. وتشمل المجموعات المعرضة للخطر أولئك الذين يعانون من حالة وراثية التليف الكيسي (CF)1. استعمار سميكة بشكل غير طبيعي، مخاط لاصق في الجهاز التنفسي في مرحلة الطفولة المبكرة يؤدي إلى التهابات بيو فيلم مستعصية من القصيبات2،3. نمو البكتيريا والأغشية الحيوية واسعة النطاق مغلفة مصفوفة هو أحد العوامل التي تميز العدوى المزمنة من الناس منقوص المناعة من الالتهابات الحادة للمضيفين الأصحاء والدولة بيو فيلم على حد سواء يحمي البكتيريا من التعرض للمضادات الحيوية (بسبب انخفاض الانتشار من خلال المصفوفة) ويقلل من قابلية المضادات الحيوية (على سبيل المثال، من خلال تحريض من الهدوء أو upregulation من مضخات efflux)4،5. ومع ذلك، فإن التعديلات الخاصة بالأمراض في فسيولوجيا الأنسجة المضيفة والكيمياء تزيد من تغيير فسيولوجيا البكتيريا من تلك التي لوحظت في العدوى الحادة أو في ظروف نمو المختبر القياسية. ومن الأمثلة الرئيسية في CF استخدام مصادر الكربون غير العادية، مثل الأحماض الدهنية والأحماض الأمينية المنبعثة من السطحي الرئة وتنتج عن التدهور الميكروبي للموسين، وإطلاق المغذيات الدقيقة، مثل الحديد من الأنسجة التالفة، وداء الميكروبات6و7و8.
وبالتالي فإن الظروف الفيزيائية الكيميائية المحددة في سياق عدوى بيو فيلم معين يمكن أن تؤثر على الاستجابات للمضادات الحيوية. أولا، يعتمد هيكل وعمق المصفوفة خارج الخلية على الظروف البيئية المحلية، مثل المواد الغذائية أو قوى القص. ثانيا، يمكن أن تؤدي الإشارات البيئية إلى التعبير عن جينات محددة لمقاومة المضادات الحيوية. على سبيل المثال، فإن العامل الممرض CF Pseudomonas aeruginosa يظهر زيادة التعبير عن بيتا لاكتاماز وانخفاض التعبير عن البورين في البلغم CF مقابل في المختبر9،في حين أن آخر CF الممرض، Burkholderia cenocepacia،upregulates بيتا lactamases ومضخات efflux عندما تزرع في CF البلغم10. ثالثا، يمكن للظروف في المضيف أن تشير إلى تحول فسيولوجي أو وراثي إلى الأنماط الظاهرية التي تتحمل المضادات الحيوية، والتي يصعب تلخيصها في المختبر. وتشمل هذه المتغيرات مستعمرة صغيرة من المكورات العنقودية المكورات العنقودية المسببةللأمراضCF 11,12.
تشير جميع هذه البيانات إلى أنه عندما تعزل مختبرات التشخيص المستنسخين الفرديين عن البيو فيلم الإمراضي وتؤدي AST على الثقافات المزروعة العوالق أو لوحة أجار في وسائل الإعلام المختبرية القياسية (microdilution مرق، نشر القرص أو Etest)، والنتائج في كثير من الأحيان لا تتوقع المضادات الحيوية التي ستعمل فعلا في الجسم الحي. حتى لو تم استخدام المقايسات بيو فيلم في المختبر، فإنها قد لا جديلة في النمط الظاهري بيو فيلم في الجسم الحي مثل بسبب الاختلافات في سطح المتوسطة والمرفق المستخدمة، لذلك يمكن أن المقايسات باستخدام خلايا التدفق أو منصات microplate عالية الإنتاجية الإفراط في تقدير حساسية المضادات الحيوية13. وتنطبق نفس المشكلة على الباحثين في الأوساط الأكاديمية والصناعة الذين يسعون إلى تطوير عوامل جديدة مضادة للبيو فيلم: اختبار إمكانات المخدرات باستخدام منصات المختبر مثل خلايا التدفق، لوحات الميكروتر، أو مركز السيطرة على الأمراض مفاعلات بيو فيلم قد تعيين شريط فعالية بيو فيلم منخفضة جدا وتنتج إيجابيات كاذبة في البحث، وتطوير خط أنابيب.
العلاقة السيئة بين نتائج AST والنتيجة السريرية بعد العلاج بالمضادات الحيوية في CF معروفة جيدا. يتجاهل العديد من الأطباء ببساطة مختبر التشخيص AST حيث لا توجد إرشادات موحدة ومحددة CF لتفسير هذه النتائج وبدلا من ذلك يتخذون قرارات كل حالة على حدة للوصف. وقد بذلت محاولات لتحسين CF AST باستخدام جهاز بيو فيلم كالجاري، الذي يستخدم الأغشية الحيوية التي تزرع على سطح أوتاد بلاستيكية مجموعة داخل آبار لوحة صغيرة تحتوي على معيار AST المتوسطة (على سبيل المثال، cation المعدلة مولر-هينتون مرق)14،15. هذا المقايسة لا أفضل في التنبؤ المضادات الحيوية التي ستعمل في الجسم الحي من العوالق القياسية AST16. التأثير على المرضى الذين يعانون من CF صارخ. على الرغم من إعطاء المضادات الحيوية المتكررة (المضادات الحيوية المستنشقة العادية ومتوسط 27 يوما في السنة تلقي المضادات الحيوية عن طريق الوريد للأفراد الذين يعانون من CF في المملكة المتحدة)17، تؤدي نوبات متكررة وغير متوقعة من تفاقم الرئة الحاد إلى تلف الرئة التدريجي ، وفي حوالي 90٪ من الحالات ، تؤدي الوفاة بسبب فشل الجهاز التنفسي. في تحليل حديث ، كانت عدوى الرئة البكتيرية أقوى مؤشر على تكاليف الدواء في CF ، حيث أضافت في المتوسط 3.6K يورو / مريض / سنة إلى تكاليف الرعاية الصحيةالمباشرة 18،19.
بالنسبة للعدوى الحادة للأفراد الأصحاء ، فإن الأبحاث والسياسات الحالية التي تركز على AST السريع استنادا ، على سبيل المثال ، إلى التنبؤ الجينومي في نقطة الرعايةمثالية 20. ولكن في حالة الالتهابات المزمنة CF، فمن الواضح أن هناك حاجة إلى نهج مختلف: تنفيذ AST في نماذج محاكاة المضيف التي تلخص بشكل أفضل في بيئة الجسم الحي والحالة الأيضية المسببة للأمراض والسماح لتشكيل هيكل بيو فيلم واقعية.
لقد سبق لنا أن وضعت نموذج بيو فيلم CF التي تضم أقسام من قصبات الخنازير المحتضنة في البلغم CF الاصطناعية والمصابة P. aeruginosa أو S. أوريوس. EVPL غير المصابة يحتفظ الأمراض النسيجية العادية لمدة 7 أيام ولكن المختبر أو العزل السريري من P. aeruginosa و S. أوريوس شكل مستنسخ في المجاميع مثل الجسم الحي حول الأنسجة, محاكاة مسببات العدوى CF21,22,23. نحن نقدم بروتوكولا لاستخدام هذا النموذج عالي الصلاحية وعالي الإنتاجية كمنصة بيو فيلم AST مصممة خصيصا ل CF وتقديم نتائج مثالية تظهر التسامح العالي للأغشية الحيوية المسببة للأمراض للمضادات الحيوية المستخدمة سريريا عند زراعتها في النموذج. ويمكن دمج النموذج بسهولة في البحوث، وخطوط أنابيب التنمية لإدارة أو منع تشكيل بيو فيلم وربما في AST التشخيص. يمكن العثور على معظم المعدات المستخدمة (انظر جدول المواد) بسهولة في مختبر الميكروبيولوجيا النموذجي ، على الرغم من أن مضرب الخرز ضروري ، وقد وجدنا من العمل مع المتعاونين أن خزانة مبيدات الجراثيم فوق البنفسجية المناسبة قد تحتاج أيضا إلى شراء. وبما أن الرئتين مصدرها الجزارون التجاريون أو المسالخ، فإن النموذج لا يمثل أي مخاوف أخلاقية.
Protocol
يستخدم هذا البروتوكول رئتي الخنازير من مسلخ تجاري يزود اللحوم للاستهلاك البشري. بموجب تشريعات المملكة المتحدة، لا يتطلب استخدام بقايا الأنسجة من الحيوانات المذبوحة للحوم موافقة أخلاقية؛ ننصح القراء بالتحقق من القوانين المحلية ذات الصلة والمبادئ التوجيهية المؤسسية قبل بدء العمل.
1. إعداد الاصطناعية CF البلغم وسائل الإعلام (SCFM)
- لجعل SCFM للاستخدام مع أنسجة EVPL، اتبع الوصفة التي حددها بالمر وآخرون24 مع التعديل الذي تتم إزالة الجلوكوز من وصفة.
ملاحظة: وصفة بالمر وآخرون يحتوي على الأحماض الأمينية الحرة، والكاتيونات، والأيونات واللاكتات بتركيزات ممثلة لمتوسط التركيزات الموجودة في مجموعة مختارة من عينات البلغم من المرضى CF. وقد ثبت أن جديلة مسارات استخدام الكربون مماثلة والتعبير عن إشارات استشعار النصاب القانوني من قبل P. aeruginosa PA14 للنمو في المتوسطة المصنوعة من البلغم المريض lyophilised24. يتم توفير وصفة ل1 L تعديل SCFM في الجدول S1. - تصفية تعقيم SCFM مباشرة بعد إعداد وتخزينها في 4 درجة مئوية لمدة تصل إلى 1 شهر.
2. تشريح والعدوى من رئة خنزير الجسم الحي السابق (EVPL) الأنسجة
- قبل تشريح، وإعداد لوحة أجار / ثانية من سلالة البكتيرية المطلوبة / ثانية للعدوى باستخدام أي أجار هو المعيار في المختبر لP. aeruginosa/S. أوريوس (على سبيل المثال، مرق lysogeny + 1.2٪ أجار).
- احسب عدد قطع أنسجة الشعب الهوائية البورسينية المطلوبة للتجربة، بما في ذلك قطع أنسجة التحكم غير المصابة. ضرب هذا العدد من قبل اثنين لتكرار التجربة في اثنين من الرئتين تكرار لتأكيد تكرار النتائج.
- مضاعفة العدد الإجمالي لقطع الأنسجة المطلوبة من قبل 0.5 لتحديد حجم Agarose SCFM (مل) اللازمة لجعل منصات agarose لجعل ما يكفي من المتوسطة ل400 ميكرولتر / قطعة الأنسجة بالإضافة إلى أجار SCFM الغيار لحساب أي أخطاء الأنابيب أو التبخر أثناء التحضير.
- إضافة 0.12 غرام من الآجاروز إلى كل 15 مل من SCFM المطلوبة لجعل الحجم الإجمالي المطلوب من SCFM مع 0.8٪ الوزن / حجم agarose.
- سخني محلول Agarose SCFM حتى يذوب الآجاروز بالكامل. يوصى بميكروويف محلي على طاقة منخفضة. يعتمد الوقت المطلوب على القوة الكهربائية للميكروويف. السماح للgarose لتبرد إلى ما يقرب من 50 درجة مئوية (دافئة للمس ولكن مريحة لعقد). لا تسمح لتبرد أكثر من ذلك.
- باستخدام ماصة، إضافة 400 ميكرولتر من Agarose SCFM إلى بئر واحد من لوحة 24 جيدا لكل قطعة الأنسجة اللازمة.
- تعقيم SCFM agarose التي تحتوي على 24-جيدا لوحة / ثانية تحت الأشعة فوق البنفسجية لمدة 10 دقيقة.
- إعداد ثلاثة يغسل تكرار لكل الرئة سليمة يجري تشريح باستخدام 20 مل من دولبيكو المعقمة المتوسطة النسر المعدلة (DMEM) بالإضافة إلى 20 مل من معهد روزويل بارك التذكاري المعقم (RPMI) 1640 تكملها مع 50 ميكروغرام / مل أمبيسلين.
- جعل aliquot من 40 مل SCFM كغسول النهائي لكل الرئة سليمة يجري تشريحها. يمكن تخزين جميع الغسالات بين عشية وضحاها عند 4 درجات مئوية أو استخدامها على الفور.
- الحصول على الرئتين من المصدر المحدد في أقرب وقت ممكن بعد الذبح، وضمان أنها تبقى باردة عن طريق نقلها إلى المختبر في صندوق تبريد محلي.
ملاحظة: الرئتين أقرب إلى يوم الذبح تظهر أقل كدمات من التخزين، ولكن الأنسجة المحفوظة في التخزين البارد لمدة تصل إلى 4 أيام من الذبح يمكن أيضا أن تستخدم. وبما أن صندوق التبريد يحتاج إلى أن يؤخذ إلى متجر الجزار أو مسلخه، يجب تطهيره باتباع إرشادات المختبر المحلي بعد كل استخدام وتخزينه خارج مختبر الأحياء المجهرية عندما لا يكون قيد الاستخدام، للحد من خطر التلوث وخرق الاحتواء. - العمل على سطح معقم وتحت لهب، وضع الرئتين على لوحة تقطيع بلاستيكية نظيفة مغطاة رقائق الألومنيوم autoclaved. تأكد من أن القصيبات تبقى سليمة. إذا كان هناك أي ضرر في المسلخ أو أثناء النقل الرئتين ليست مناسبة للاستخدام.
- سخني سكين لوحة تحت اللهب والمسي السكين لفترة وجيزة إلى منطقة الرئة المحيطة بالبرونيكول لتعقيم سطح الأنسجة.
- قطع الأنسجة السطحية المحيطة القصيبات باستخدام شفرة حلاقة محمولة معقمة. جعل شقوق موازية لبرونيكول لمنع أي ضرر.
- مرة واحدة وقد تعرض القصيبات، وجعل شق المقطع العرضي من خلال القصيبات في أعلى نقطة مرئية لتحرير الشعب الهوائية.
- باستخدام ملقط معقم، عقد طفيفة نهاية حرة من القصيبات وقطع أي الأنسجة غير المرغوب فيها المتبقية باستخدام شفرة حلاقة محمولة عقيمة. إجراء شق المقطع العرضي النهائي عبر الشعب الهوائية قبل أي تفريع مرئية لإزالة القصيبات من الرئتين.
- وضع القصيبات في أول غسل DMEM / RPMI 1640. اتركي القصيبات في الغسيل وكرري الخطوات 2.11-2.14 لحصاد أجزاء إضافية من القصبات الهوائية من نفس الرئة كما هو مطلوب لتسفر عن أقسام أنسجة كافية للتجربة المخطط لها.
- ضع أي أقسام إضافية من القصبات الهوائية من نفس الرئة في الغسيل (الخطوة 2.16). يترك في الغسيل لمدة دقيقتين على الأقل.
- إزالة القصيبات من غسل DMEM/RPMI 1640 الأولى ووضع العينات في طبق بيتري معقمة.
- عقد كل القصيبات طفيفة باستخدام ملقط معقمة، مع التأكد من عدم تلف الأنسجة. إزالة أكبر قدر ممكن من الأنسجة الرخوة المتبقية وقطع الأنسجة إلى شرائح ~ 5 ملم واسعة باستخدام مقص تشريح معقمة.
- ضع جميع شرائط الأنسجة القصبية في غسل DMEM/RPMI 1640 الثاني. يترك في الغسيل لمدة دقيقتين على الأقل.
- إزالة شرائط الأنسجة من الغسيل الثاني باستخدام ملقط معقم، مع الحرص على عدم تلف الأنسجة. ضع الأنسجة في طبق بيتري نظيف ومعقم.
- إزالة أي الأنسجة الرخوة المتبقية تعلق على القصيبات وقطع شرائح إلى مربعات (~ 5 ملم × 5 ملم) باستخدام مقص تشريح معقمة.
- إضافة الثالث DMEM / RPMI 1640 يغسل في طبق بيتري. مزيج طفيفة قطع الأنسجة في الغسيل عن طريق تدوير الطبق.
- صب غسل الثالث من طبق بيتري دون إزالة قطع الأنسجة.
- أضف غسل SCFM النهائي إلى طبق بيتري المحتوي على الأنسجة، مما يضمن تغطية جميع قطع الأنسجة.
- تعقيم قطع الأنسجة في SCFM تحت ضوء الأشعة فوق البنفسجية لمدة 5 دقائق.
- استخدام ملقط معقم لنقل كل قطعة أنسجة الشعب الهوائية المعقمة في الآبار الفردية من لوحة 24 جيدا / ثانية تحتوي على منصات Agarose SCFM.
- لإصابة كل قطعة نسيج بالسلالة البكتيرية المطلوبة، المس مستعمرة تزرع على طبق أجار مع طرف إبرة 29 G متصلة بحقنة الأنسولين المعقمة 0.5 مل. ثم المس المستعمرة على قطعة الأنسجة ، وخز بلطف سطح الأنسجة.
ملاحظة: استخدام حقنة الأنسولين مجهزة بإبرة 29 G يسمح الإبرة أن تعقد بدقة وراحة مع الحفاظ على أصابع مسافة آمنة من كل من إبرة وأنسجة الرئة. من الممكن تنفيذ هذه الخطوة باستخدام إبر 29 G غير المرفقة بحقنة ، ولكن هذا يتطلب المزيد من البراعة ويزيد من خطر إصابة عصا الإبرة. حقن الأنسولين متاحة بسهولة. - بالنسبة للعناصر التحكم غير المصابة، قم بوخز سطح كل قطعة من قطعة الأنسجة بلطف مع طرف إبرة 29 G متصلة بحقنة الأنسولين المعقمة 0.5 مل.
- استخدام ماصة لإضافة 500 ميكرولتر من SCFM إلى كل بئر.
- تعقيم غشاء الختم تنفس لكل لوحة 24 جيدا تحت الأشعة فوق البنفسجية لمدة 10 دقيقة (جدول المواد).
- إزالة الغطاء / ثانية من لوحة 24 جيدا / ثانية واستبدالها مع غشاء تنفس.
- احتضان لوحات في 37 درجة مئوية لحضن المطلوب (العدوى) الوقت دون اهتزاز. تأكد من عدم وجود نمو مرئي لمسببات الأمراض الملقحة على قطع التحكم غير المصابة (التحكم في التلوث).
ملاحظة: إذا رغبت في ذلك، يمكن إضافة أمبيسلين إلى منصات Agarose SCFM في الخطوة 2.5 وتغطي SCFM في الخطوة 2.30 إلى تركيز نهائي قدره 20 ميكروغرام/مل. وهذا سوف قمع نمو معظم البكتيريا الذاتية على الرئتين دون التأثير على P. aeruginosa أو S. نمو الحالب ولكن, كما وجود أمبيسلين قد تؤثر على التعرض للمضادات الحيوية الأخرى, ويترك القارئ لجعل هذا الاختيار اعتمادا على سلالات والمضادات الحيوية التي يرغبون في اختبار.
3. تحديد فعالية المضادات الحيوية
ملاحظة: يتم توفير تخطيطي تفاصيل خطوات هذا المقايسة في الشكل S1.
- لقياس تحمل المضادات الحيوية للأغشية الحيوية التي تشكلت على EVPL ، يجب إعداد مجموعات من قطع الرئة ، من رئتين مستقلتين على الأقل ، أثناء التشريح والعدوى. هناك حاجة إلى مجموعة واحدة من القطع للسيطرة السلبية (لا علاج المضادات الحيوية)، وهناك حاجة إلى مجموعة واحدة لكل تركيز من المضادات الحيوية ليتم اختبارها.
- بعد 48 ساعة من الحضانة، تفقد بصريا قطع الأنسجة غير المصابة. قد يكون حدث بعض نمو البكتيريا الذاتية لرئة الخنزير، مما يؤدي إلى SCFM حول هذه الأقسام لتكون عكر. إذا لوحظ نمو نموذجي لأنواع الدراسة المختارة (على سبيل المثال ، تشخيص التصبغ الأزرق والأخضر ل P. aeruginosa) ، فإعادة بدء التجربة مع الرئتين الطازجتين.
- إذا لم تظهر أقسام الأنسجة غير المصابة نموا بكتيريا ضئيلا أو ضئيلا فقط ، فعد لوحة غسيل واحدة من 24 بئرا ولوحة علاج واحدة من 24 بئرا ، يحتوي كل منها على 500 ميكرولتر من SCFM الطازج بدون مضادات حيوية أو مع مضاد حيوي مهم لكل بئر لكل قطعة أنسجة الرئة.
- إزالة كل قطعة الأنسجة المصابة من لوحة الحضانة مع ملقط اللهب المعقمة، دوامة لفترة وجيزة في بئر جديدة من لوحة الغسيل لإزالة أي الخلايا البكتيرية المرتبطة غير بيو فيلم، ونقل إلى البئر المناسب من لوحة العلاج.
- ختم لوحات العلاج مع غشاء تنفس جديدة.
- احتضان لوحة العلاج / ثانية في 37 درجة مئوية دون اهتزاز لمدة 18-24 ساعة.
- باستخدام ملقط اللهب المعقم، قم بإزالة كل قطعة رئوية من لوحة 24 بئر ووضع أنبوب تجانس معقم سعة 2 مل يحتوي على 1 مل من المالحة العازلة بالفوسفات (PBS) و1 غرام من الخرز المعدني(جدول المواد).
- فاز حبة لمدة 40 ثانية في 4 م / ثانية.
ملاحظة: حبة الضرب مع الخرز محددة ومتجانس المقترحة في جدول المواد لا يسبب تحلل كبير من البكتيريا، ولكن كل مختبر باستخدام البروتوكول يجب التحقق من آثار الخرز والمتجانس التي اختاروها قبل بدء المقايسات AST. - تخفيف تسلسلي تجانس الرئة باستخدام برنامج تلفزيوني ولوحة على مرق Lysogeny (LB) أجار لتحديد وحدات تشكيل مستعمرة (CFU) في قطع الأنسجة الفردية غير المعالجة والمضادات الحيوية وفقا لطرق الطلاء القياسية.
ملاحظة: اختياري: إعداد لوحات مكررة على وسائط انتقائية لتأكيد هويات المستعمرة؛ على سبيل المثال، باستخدام مانيتول الملح أجار لS. أوريوس.
النتائج
يوفر نموذج EVPL منصة عالية الإنتاجية ، مما يجعل من الممكن فحص عدد كبير من العزلات البكتيرية لقابلية المضادات الحيوية في وقت واحد(الشكلان 1 و 2)أو فحص السلالات ضد مجموعة من تركيزات المضادات الحيوية في تجربة واحدة (الشكل 3). مع الممارسة، وجدنا أن ما يقرب من 200 أقسام الأنسجة القصبية يمكن إعدادها من الرئتين في 2 ساعة. يمكن إكمال التجربة بأكملها ل AST في غضون ساعات العمل العادية. نمو Pseudomonas aeruginosa و Staphylococcus aureus يعزل وإنشاء 48 ساعة بيو فيلم في النموذج موثوق بها، وعندما رصدت من قبل عدد الخلايا قابلة للحياة، وتنتج الأحمال البكتيرية متسقة (الشكلين 1 و 2). ويمكن الاطلاع على صور الأغشية الحيوية المرتبطة بالأنسجة من Pseudomonas aeruginosa والمكورات العنقودية أوريوس نمت في EVPL، جنبا إلى جنب مع بروتوكولات للتحضير للتنظير المجهري الخفيفة وتلطيخ النسيجية، في منشوراتنا21،23. ومع ذلك ، فإن استنساخ التهم CFU يختلف لأنواع البكتيريا المختلفة. ويمكن قياس ذلك باستخدام حسابات التكرار القياسية بعد ANOVA25؛ لقد وجدنا أن هناك عادة اختلاف أكبر بين CFU في عينات الرئة تكرار لS. أوريوس من لP. aeruginosa. ونوصي بأن تجرى، عند اعتماد المختبر للنموذج، عمليات حسابية متكررة على تجارب تجريبية لتحسين التقنيات التجريبية وتحديد أحجام العينات التي ستستخدم في التجارب النهائية (يمكن العثور على مثال على ذلك في ملحق البيانات الخاص بسويني وآخرين26).
عندما تزرع في EVPL، biofilms من P. aeruginosa و S. aureus إظهار زيادة التسامح مع المضادات الحيوية مقارنة مع قابلية في المعيار، وافق الصناعة مرق هيئة التصنيع العسكري (الشكل 1) وأقراص المقايسات باستخدام وسائل الإعلام القياسية (الشكل 2). الآثار المختلفة للمضادات الحيوية المختلفة على EVPL المنشأة بيو فيلم يمكن تمييزها، على سبيل المثال يتم تحقيق P. aeruginosa القتل في EVPL مع 4-16X هيئة التصنيع العسكري ciprofloxacin ولكن ليس مع 4-8X هيئة التصنيع العسكري الكلورامفينيكول (الشكل 1). جرعة مرتين يوميا من 600 ملغ linezolid يحقق تركيز المصل فوق هيئة التصنيع العسكري90 لمسببات الأمراض المعرضة (4 ميكروغرام / مل)27 ويعتبر التعرض الكافي دون آثار جانبية ضارة28. وتبين البيانات الواردة في الشكل 2 أن مجموعات S. aureus، المعرضة للانزوليد في المقايسة القرصية، قادرة على البقاء على قيد الحياة تركيزات المصل المستهدفة، وأعلى (12 ميكروغرام/مل)، في EVPL. لا يوجد ارتباط واضح بين هيئة التصنيع العسكري وتأثيرات المضادات الحيوية على الأغشية الحيوية التي تزرعها EVPL ل P. aeruginosa (الشكل 1). الحصول على مقياس أكثر دقة من التسامح في الجسم الحي المضادات الحيوية مهم لأن المخدرات دون المستوى الأمثل من المضادات الحيوية يمكن أن تزيد من خطر اختيار المقاومة في العدوى المزمنة.
ومن المعروف جيدا أن طريقة بيو فيلم النمو يمكن أن تقلل بشكل كبير من قابلية البكتيريا للمضادات الحيوية. وقد أدى هذا إلى تطوير العديد من المقايسات بيو فيلم في المختبر واستخدام الحد الأدنى من تركيز الاستئصال بيو فيلم (MBEC)14،15 بدلا من هيئة التصنيع العسكري كمنبئ أكثر دقة من التعرض في العدوى المزمنة. كما تم التوصية باستخدام SCFM (في تركيبات مختلفة) للاستخدام في اختبار هيئة التصنيع العسكري أو MBEC29. هنا نظهر أنه حتى المقايسة المثلى في المختبر لا يمكن التنبؤ بدقة P. aeruginosa التعرض للكوليستين في EVPL. كمية المضادات الحيوية المطلوبة لتحقيق 3 سجل10 قتل البكتيريا المزروعة EVPL غالبا ما يكون أعلى بكثير من هيئة التصنيع العسكري أو MBEC محسوبة من المقايسات القياسية في المختبر، حتى عندما يستخدم SCFM لهذه المقايسات(الشكل 3). وهذا يتفق مع مراجعة كوكرين التي ذكرت أن التطبيقات الحالية لاختبار قابلية الأغشية الحيوية في المختبر لا توفر أي قوة تنبؤية متزايدة لوصف المضادات الحيوية في CF مقارنة باختبار الحساسية القياسي16.
كما أنه من السهل استخدام النموذج لتقييم تأثير المضادات الحيوية على بكتيريا بيو فيلم مع مرور الوقت ، حيث يمكن تلقيح قطع طبق الأصل كافية من الرئة للسماح بأخذ عينات مدمرة. بالإضافة إلى التمييز بين الاختلافات بين العوامل المضادة للميكروبات، يمكن للنموذج تسليط الضوء على التغيرات في الحساسية في مراحل النمو البكتيرية المختلفة أو عمر بيو فيلم وفترات الزمام المضادة للمضادات الحيوية المختلفة. ويوضح الشكل 4 التسامح المتزايد للأغشية الحيوية P. aeruginosa إلى ميروبينيم عندما تنضج. وهذا يمكن أن يكون مفيدا لتحديد فعالية وكلاء الرواية، على سبيل المثال ما إذا كانت أكثر فعالية خلال انقسام الخلايا السريع. قد يكون أيضا اعتبارا هاما عند وضع قيود تجربة، كما قد يكون من الضروري لتوحيد والتحقق من صحة العمر بيو فيلم لتجنب السن لها تأثير على النتائج.
في الشكل 5، ق. تم قياس بقاء الحالب عند 4 ساعة و 24 ساعة بعد التعرض للفلوكلوكساسيلين وكان من الممكن ملاحظة الاختلافات في الحد من عدد الخلايا البكتيرية عبر الزمن وبين العزلات. قد يكون هذا مفيدا لتطوير الأدوية ، على سبيل المثال عند تعريف المعلمات الدوائية والديناميكية الدوائية أو عند توضيح طريقة عمل وكيل جديد.
الاختلافات في الحمل البكتيري غالبا ما تزيد مع تمديد أوقات الثقافة. ويمكن رؤية ذلك في السيطرة غير المعالجة في الشكل 5 بعد 48 ساعة تطوير بيو فيلم والتعرض 24 ساعة أخرى لحساب الفاصل الزمني الزواية المضادات الحيوية. الاختلاف هو جوهري للنموذج؛ كل عينة الرئة مستقلة عن غيرها ويعكس الاختلاف الطبيعي للرئتين. ولذلك، من المهم ضمان إدراج عدد كاف من النسخ المتماثلة للسماح بالتحقق من النتائج وتفسيرها بدقة. ونحيل القارئ مرة أخرى إلى توصيتنا بإجراء حسابات متكررة على البيانات لتمكين اختيار أحجام عينات قوية.
للبساطة، قدمنا بيانات تمثيلية مأخوذة من أقسام الأنسجة المتماثلة المكتسبة من زوج واحد من الرئتين في كل تجربة، ولكن من الناحية العملية من الضروري إجراء تجارب متكررة على أقسام الأنسجة المأخوذة من الحيوانات المتماثلة. وينبغي أن يتم ذلك من أجل حساب أي اختلاف بيولوجي بين الخنازير الفردية، ونحن نحيل القارئ إلى عملنا المنشور للحصول على أمثلة على مدى اتساق النتائج يمكن أن تكون بين الأنسجة المأخوذة من الخنازير المتماثلة وكيف يتم حساب هذا الاختلاف في التحليل الإحصائي للبيانات باستخدام تحليل التباين (ANOVA) / النماذج الخطية العامة (GLM)21،26.
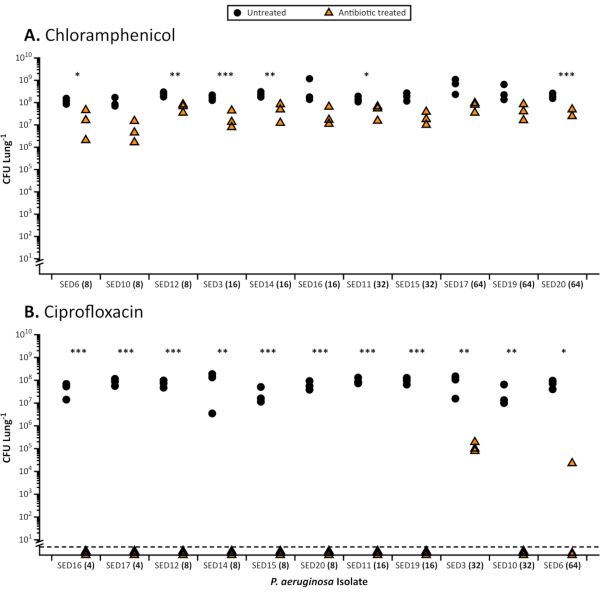
الشكل 1. مجموع CFU من 11 CF Pseudomonas aeruginosa العزلات السريرية تعافى من نموذج EVPL بعد العلاج بالمضادات الحيوية. النتائج التمثيلية للعلاج بالمضادات الحيوية من P. aeruginosa في نموذج EVPL. نمت كل سلالة على الأنسجة EVPL لمدة 48 ساعة ثم نقلها إلى المضادات الحيوية (مثلثات) أو برنامج تلفزيوني كتحكم (دوائر) لمدة 18 ساعة وCFU / الرئة تحديد. يظهر هيئة التصنيع العسكري للمضادات الحيوية المناسبة المحددة في معيار التخدير المعدلة MHB بين قوسين بجانب كل سلالة (س المحور). يتم ترتيب السلالات عن طريق زيادة قيم هيئة التصنيع العسكري. تم تحليل البيانات باستخدام اختبارات t عند الاقتضاء واختبارات Mann-Whitney U لمجموعات البيانات غير البارامترية. الاختلافات الهامة بين الأنسجة المعالجة بالمضادات الحيوية وغير المعالجة تدل عليها النجمة(P < 0.05). أ. 4 - الكميات المستردة القابلة للتطبيق من الأغشية الحيوية P. aeruginosa التي تزرع في نموذج EVPL وتعامل ب 64 ميكروغرام/مل كلورامينيكول (أعلى قيمة مسجلة لهيئة التصنيع العسكري). لكل عزل، تم حساب الفرق المتوسط الموحد في CFU بين أقسام الأنسجة المعالجة بالكلورامفينيكول وغير المعالجة باستخدام كوهين د. لم يكن هناك ارتباط بين قيمة هيئة التصنيع العسكري في الاختبار القياسي والانخفاض في أعداد الخلايا القابلة للتطبيق في نموذج EVPL كما يقاس ب D كوهين (ارتباط رتبة سبيرمان، صق = 0.45، ص = 0.16) B. نتائج P. aeruginosa بيو فيلم نمت في نموذج EVPL وتعامل مع 64 ميكروغرام / مل سيبروفلوكساسين (أعلى قيمة هيئة التصنيع العسكري المسجلة). كانت القيم أسفل الخط المتقطع أقل من حد الكشف. يرجى النقر هنا لعرض نسخة أكبر من هذا الرقم.
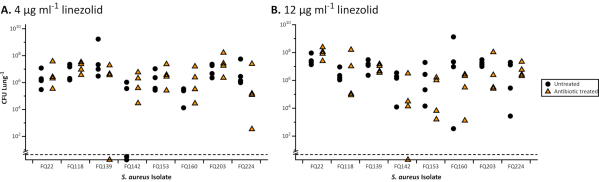
الشكل 2. مجموع CFU من 8 المكورات العنقودية أوريوس CF العزلات السريرية تعافى من نموذج EVPL بعد العلاج مع linezolid. نمت كل سلالة على أنسجة EVPL لمدة 48 ساعة ثم نقلت إلى linezolid (مثلثات) لمدة 24 ساعة أو لم تعالج كعنصر تحكم (دوائر). تم العثور على جميع السلالات لتكون حساسة ل linezolid باستخدام المقايسة نشر القرص القياسية التالية المبادئ التوجيهية EUCAST30 (منطقة تثبيط > 21 ملم). تم تحليل البيانات باستخدام t-tests عند الاقتضاء واختبارات Mann-Whitney U لمجموعات البيانات غير البارامترية(P < 0.05). لم يتم العثور على اختلافات كبيرة بين المضادات الحيوية المعالجة وغير المعالجة لأي من السلالات. كانت القيم أسفل الخط المتقطع أقل من حد الكشف. أ. نتائج S. أوريوس بيو فيلم في نموذج EVPL تعامل مع 4 ميكروغرام / مل linezolid (نقطة توقف السريرية للحساسية / مقاومة وفقا لتصنيف EUCAST31). باء - ال 20 في المائ نتائج S. aureus بيو فيلم في نموذج EVPL تعامل مع 12 ميكروغرام / مل linezolid (البيانات المستنسخة من سويني وآخرون23). يرجى النقر هنا لعرض نسخة أكبر من هذا الرقم.
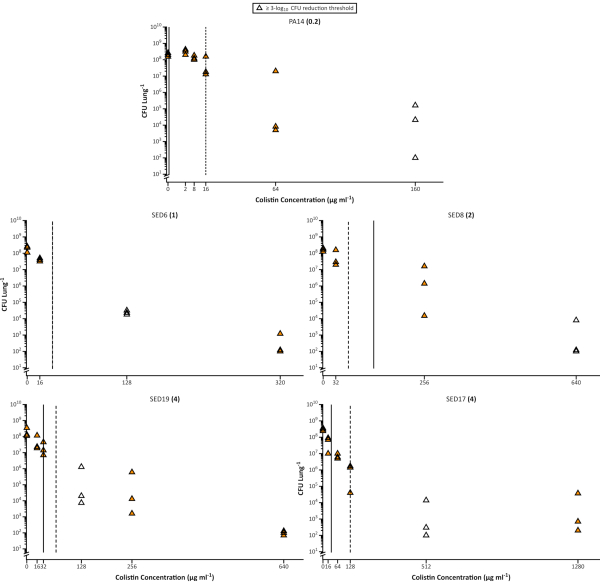
الشكل 3. قابلة للحياة Pseudomonas aeruginosa عدد الخلايا من سلالة مختبر PA14 و 4 CF العزلات السريرية تعافى من نموذج EVPL بعد العلاج مع تركيزات متزايدة من الكوليستين. نمت كل سلالة على أنسجة EVPL لمدة 48 ساعة ثم تعرضت للكوليستين لمدة 18 ساعة. يتم عرض هيئة التصنيع العسكري المحددة في المتوسطة MHB القياسية المعدلة cation بين قوسين بجانب كل اسم سلالة. تظهر الخطوط العمودية قيمة MBEC المحددة في MHB (متصل) و SCFM (متقطعة) ، باستثناء SED6 ، حيث كانت القيمة هي نفسها في كل من الوسائط. تمثل نقاط البيانات غير المعبأة أدنى تركيز للكوليستين الذي تم اختباره والذي أدى إلى انخفاض ≥ 3-log10 في CFU / lungcompared إلى العينات غير المعالجة (0 ميكروغرام / مل colistin) (البيانات المستنسخة من Sweeney et al26). يرجى النقر هنا لعرض نسخة أكبر من هذا الرقم.
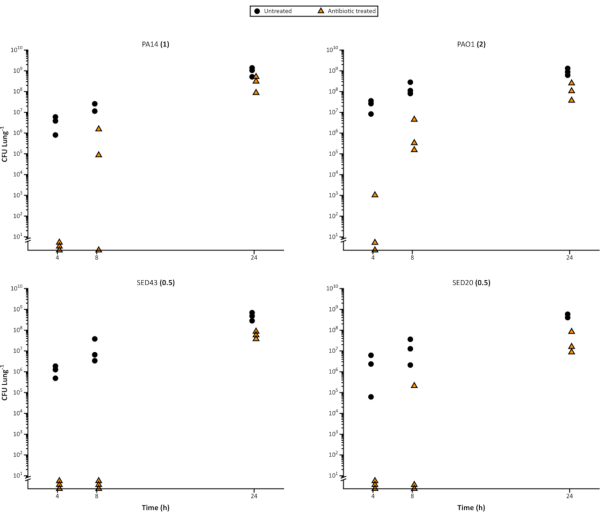
الشكل 4. ممثل قابلة للحياة Pseudomonas aeruginosa خلية التهم من مسار زمني للنمو على نموذج EVPL أكثر من 24 ساعة, والعلاج اللاحق مع 64 ميكروغرام / مل meropenem. تمت زراعة السلالة المختبرية P. aeruginosa PA14 و 3 CF العزلات السريرية على أنسجة EVPL للوقت المبين على المحور x، ثم نقلها إلى meropenem (مثلثات) لمدة 24 ساعة أو تركت دون علاج كعنصر تحكم (دوائر). ثم تم تحديد CFU / الرئة. يتم عرض هيئة التصنيع العسكري المحددة في المتوسط MHB ضبط cation بين قوسين بجانب كل اسم سلالة. يرجى النقر هنا لعرض نسخة أكبر من هذا الرقم.
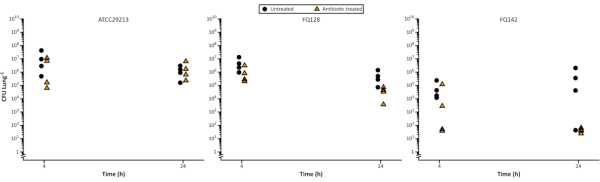
الشكل 5. ممثل قابلة للحياة المكورات العنقودية المريورية العد بعد النمو على نموذج EVPL ثم تعامل مع 5 ميكروغرام / مل فلوكلوكساسيلين على مدى 24 ساعة دورة زمنية. تمت زراعة سلالة التحكم ATCC29213 واثنين من العزلات السريرية CF على أنسجة EVPL لمدة 48 ساعة ثم تم نقلها إلى فلوكلوكساسيلين (مثلثات) أو تركت دون علاج كتحكم (دوائر) لمدة 4 ساعة و 24 ساعة ، قبل تحديد CFU / الرئة (البيانات المستنسخة من Sweeney et al23). يرجى النقر هنا لعرض نسخة أكبر من هذا الرقم.
الشكل S1- الأرقام 1- الأرقام 1 يرجى الضغط هنا لتحميل هذا الرقم.
الجدول S1- الجداول الرجاء الضغط هنا لتحميل هذا الجدول.
Discussion
نموذج الرئة فيفو السابق هو الإنتاجية العالية وغير مكلفة، ولأنه يستخدم النفايات ما بعد المستهلك من صناعة اللحوم، فإنه لا يمثل أي مخاوف أخلاقية. وهي مصممة لمحاكاة الخطوط الجوية CF البشرية المصابة بشكل مزمن أفضل مما هو متاح حاليا، في منصات AST المختبر. تظهر النتائج المعروضة هنا أنه قد يتنبأ بدقة أكبر بقابلية المضادات الحيوية في ظل هذه الظروف.
وتشمل الخطوات الحاسمة في البروتوكول، التي ستضمن نتائج موثوقة وقابلة للاستنساخ ما يلي:
- استخدام الوقت وأساليب التخزين المتسقة بين ذبح وجمع ومعالجة عينات الرئة. من المهم استخدام الرئتين في أقرب وقت ممكن بعد الذبح والحفاظ على احتمال التلوث إلى أدنى حد ممكن. وقد لوحظت اختلافات في قدرة الثقافات التجريبية على النمو في الرئتين إذا لم تكن طازجة قدر الإمكان.
- الحفاظ على العقم في إنتاج SCFM وتشريح قطع الرئة أمر ضروري. الرئتين السليمة ليست معقمة، وبالتالي فإن وجود البكتيريا كومنسال قد تعكس بيئة "طبيعية" للعدوى المزمنة. ومع ذلك، وكما لوحظ سابقا، فإن التفاعلات البكتيرية بين المجموعات السكانية المتعددة الأنواع قد تغير النتائج والتعرض للمضادات الحيوية، لذلك ينبغي تجنب التلوث وتعقيم الرئتين قبل الاستخدام. نحن ندعو إلى استخدام التعقيم بالأشعة فوق البنفسجية، لأنه لا يبدو أنه يسبب تغييرات سلامة الأنسجة القصديرية، وإذا لزم الأمر، يغسل المضادات الحيوية إضافية. ومع ذلك، ينبغي استخدام المضادات الحيوية بحذر، لأنها قد تؤثر على النتائج من خلال إدخال ضغوط انتقائية وقد تغير التعبير الجيني في مجموعات البكتيريا الاختبارية.
- استخدم عينات أنسجة التحكم السلبية المصابة بالقيلة ولوحات تعداد الخلايا المزروعة على وسيط غني غير انتقائي لتسليط الضوء على نمو أي بكتيريا ملوثة أو كومينسال لم تتم إزالتها أثناء التعقيم. وهذا أمر ضروري للتخفيف من أي تأثير لهذه البكتيريا على AST. ومن المفيد أيضا لإنتاج مكررة، وأجار انتقائية، لوحات عدد الخلايا محددة للكائن الحي من الفائدة، لوحات مكررة تسريع تحديد مستعمرة وعدد الخلايا.
- إجراء تجارب تجريبية عند استخدام النموذج لأول مرة وعند استخدامه مع سلالات جديدة أو النمط الجيني من البكتيريا لتقييم الاختلافات CFU بيو فيلم بين أقسام الأنسجة، مما يسمح باختيار أحجام العينة التجريبية المثلى (على سبيل المثال، كم عدد أقسام الأنسجة تكرار للحصول على من عدد تكرار الرئتين) من خلال استخدام حسابات الطاقة.
- يستخدم الفحص inoculum غير موحدة ، لأن هذا يسمح التطعيم السريع بعد 48 ساعة من الحضانة وتشكيل الأحمال biofilms متسقة نسبيا (وخاصة بالنسبة P. aeruginosa). لتقييم فعالية مضادة للبكتيريا في مراحل نمو بيو فيلم في وقت مبكر، والنظر في تلقيح مع CFU موحدة من البكتيريا المزروعة مستعمرة علقت في ASM. نحن لا نوصي بالتطعيم بالبكتيريا العوالق: أظهرت التجارب التجريبية المبكرة أن هذا يؤدي إلى نمو حاد وغازي لا يمكن الاعتماد عليه لتشكيل بيو فيلم.
هذا البروتوكول ينتج نموذج نموذج قوي للاستخدام مع P. aeruginosa, مع إمكانات كبيرة لتطوير للاستخدام مع S. أوريوس, ولكن لديها بعض القيود التي سوف تحتاج إلى معالجة لتطبيقات معينة في المستقبل. تم تلقيح الأنسجة من مستعمرات واحدة للسماح بتطور المجموعات السكانية اللاستنساخية. وتظهر النتائج أن, لP. aeruginosa, هذا له تأثير يذكر على أرقام الخلايا في 48 ح. ومع ذلك ، لوحظ تباين أكبر في الحمل البكتيري ل S. aureus ، وبالنظر إلى أن البكتيريا المختلفة قد تنمو بشكل مختلف داخل النموذج ، قد يعتمد الإنتاج الموحد بدءا والإنتاج الدقيق لعينات الأنسجة من الحجم والوزن المتماثلين على الكائن الحي للدراسة. قد تكون هناك أيضا اختلافات بين المختبرات بسبب الاختلافات في تقنيات التشريح الدقيق / العدوى أو سلالة الخنازير المحلية / سباق الأراضي. ولتقييم قابلية المجموعات البكتيرية للاستنساخ من أجل التطبيقات الفردية للنموذج، نقترح استخدام حسابات التكرار كجزء من التحليل الإحصائي للنتائج25 واستخدام حسابات التكرار/القدرة على أساس التجارب التجريبية لحساب الحجم الأمثل للعينة لاستخدامها في التجارب النهائية.
واحدة من المزايا الرئيسية للEVPL على المقايسات لوحة التقليدية هو أنه، بدلا من اختبار للبكتيريا تنمو العوالق أو على الأسطح اللاأحيائية، فإنه يسمح لهيكلة المكانية من الأغشية الحيوية البكتيرية داخل بيئة المضيف ومع تمايز الخلايا. وهذا له آثار هامة على النظر في تأثير التدرجات الفيزيوكيميائية والمغذيات على نشاط العوامل المضادة للميكروبات وكذلك تقديم وتوافر العلاجات النشطة في مختلف البيئات الدقيقة داخل عدوى مزمنة والتفاعل بين الخلايا الخلوية بين البكتيريا. وهذه النقطة الأخيرة هامة بشكل خاص، حيث لوحظت العدوى المتعددة الأنواع بشكل روتيني في CF وأصبحت ذات أهمية متزايدة للعدوى المرتبطة بحالات تنفسية أخرى، مثل الربو ومرض الانسداد الرئوي المزمن. هناك إمكانية لتطوير هذا النموذج ل AST لأخذ عينات البلغم المريض الفردية في التشخيص السريري. وهناك تجربة مماثلة جارية بالفعل باستخدام نموذج محاكاة الجرح في المختبر للنمو و AST من بيو فيلم حطام من الجروح المزمنة (جنوب غرب مركز الرعاية الإقليمية للجروح في لوبوك، تكساس، الدكتور ر. وولكوت).
وعلاوة على ذلك، يستخدم النموذج أنسجة ما بعد الوفاة، وبالتالي فإن تأثير الاستجابة المناعية المضيفة على قابلية المضادات الحيوية محدود. النماذج الحالية في المختبر أيضا لا تمثل استجابات المناعة المضيف، لذلك نحن لا نرى هذا كحاجز أمام الاستخدام المستقبلي للنموذج في تطبيقات AST. ومع ذلك ، تؤخذ الاستجابة المناعية في الاعتبار عند تحديد المعلمات الدوائية والصيدلانية والمبادئ التوجيهية لدواسة المضادات الحيوية. على الرغم من أن دراساتنا قد أظهرت أدلة على الخلايا المناعية المتبقية والاستجابات داخل الأنسجة23 (وS. Azimi، الاتصالات الشخصية)، وهذا هو المجال الرئيسي لمزيد من التحسين وتطوير النموذج إذا كان من المرغوب فيه مباراة أكبر في ظروف الجسم الحي.
إن توفير المزيد من العلاج المضاد للأمراض الصالحة سريريا ل CF سيساعد في تلبية توصية رئيسية من قانون الرعاية الصحية والاجتماعية في المملكة المتحدة لعام 2008 بأن "الإجراءات يجب أن تكون قائمة لضمان الوصف الحصيف والإشراف على مضادات الميكروبات". ونحن نعتقد أن EVPL هو نموذج مثالي للمرشح للمساعدة في تلبية هذه الحاجة.
Disclosures
وليس لدى صاحبي البلاغ ما يكشفان عنه.
Acknowledgements
ونشكر جميع المشاركين في كتابتنا على الورقات الأصلية التي حصلنا منها على نتائج مثالية. تم تمويل العمل من خلال منحة أبحاث محقق جديد MRC (رقم المنحة MR/R001898/1)الممنوحة ل FH؛ من قبل طلاب الدكتوراه من BBSRC ميدلاندز شراكة التدريب التكاملي للعلوم الحيوية (MIBTP) الممنوحة لNEH وIA؛ وجائزة جامعة وارويك الجامعية خطة دعم البحوث إلى الاتحاد الانجليزي لإجراء مشروع بحثي عطلة الصيف. نشكر ستيف كويغلي وأولاده (كوبينغتون، وارويكشاير) وجون تايلور، سون (إيرلسدن، كوفنتري) على تزويد الرئتين. ونود أيضا أن نعترف بمساعدة مرفق إعداد وسائط الإعلام في كلية علوم الحياة في جامعة وارويك، مع شكر خاص لسيريث هاريز وكارولين ستيوارت، ومساعدة أنيتا كاثروود في مرفق وارويك لفحص مضادات الميكروبات.
Materials
| Name | Company | Catalog Number | Comments |
| 0.5 mL insulin syringes with 29G needle attached | |||
| 24-well culture plates | |||
| 70% ethanol or similar for surface sterilizaton and flamin gof dissection equipment | |||
| Agar plates to prepare streaks of P. aeruginosa/S. aureus (any suitable medium) | |||
| Agarose | |||
| Aluminum foil - pre-sterilised by autoclaving - to cover the chopping board on whcih you wil dissect lungs. | |||
| Bead beater designed to take 2 mL tubes | MP Biomedicals | 116004500 | FastPrep-24 Classic bead beating grinder and lysis system |
| Breathe-easy or Breathe-easier sealing membrane for multiwell plates | Diversified Biotech | BEM-1 or BERM-2000 | |
| Bunsen burner | |||
| Chopping board - we recommend a plastic board to allow for easy decontamination with alcohol. | |||
| Coolbox to transport lungs to lab | |||
| Dissection scissors in different sizes | |||
| Dulbecco’s modified Eagle medium (DMEM) | |||
| Fisherbrand 2 mL reinforced tubes | Thermo Fisher | 15545809 | |
| Fisherbrand 2.38 mm metal beads | Thermo Fisher | 15505809 | |
| Germicidal UV cabinet | |||
| Insulin syringes - 0.5 mL with 29G needle attached. | VWR | BDAM324892 | |
| Large pallet knife | |||
| LB agar plates to assess CFU in lung biofilm homogenate | |||
| Mounted razor blades | |||
| Nalgene RapidFlow PES 75 mm x 0.1 µm x 500 ml sterile filter unit | Thermo Fisher | 10474415 | For filter-sterilizing SCFM |
| Petri dishes | |||
| Phosphate-buffered saline | |||
| Plastic chopping board and aluminium foil to create a sterile and cleanable dissection surface | |||
| Roswell Park Memorial Institute (RPMI) 1640 medium | |||
| SCFM ingredients as listed in Table S1 | |||
| Selection of forceps (blunt tips recommended) | |||
| Selective agar plates to specifically assess P. aeruginosa / S. aureus CFU in lung biofilm homogenate, if required. | |||
| Suitable containers for disposing of contaminated sharps and pig ung tissue, according to your institution's health & safety policies. |
References
- Elborn, J. S. Cystic fibrosis. The Lancet. 388 (10059), 2519-2531 (2016).
- Høiby, N., et al. Diagnosis of biofilm infections in cystic fibrosis patients. APMIS. 125, 339-343 (2017).
- Bjarnsholt, T., et al. Pseudomonas aeruginosa biofilms in the respiratory tract of cystic fibrosis patients. Pediatric Pulmonology. 44 (6), 547-558 (2009).
- Høiby, N., Bjarnsholt, T., Givskov, M., Molin, S., Ciofu, O. Antibiotic resistance of bacterial biofilms. International Journal of Antimicrobial Agents. 35 (4), 322-332 (2010).
- Penesyan, A., Gillings, M., Paulsen, I. Antibiotic discovery: Combatting bacterial resistance in cells and in biofilm communities. Molecules. 20 (4), 5286(2015).
- Son, M. S., Matthews, W. J., Kang, Y., Nguyen, D. T., Hoang, T. T. In vivo evidence of Pseudomonas aeruginosa nutrient Acquisition and pathogenesis in the lungs of cystic fibrosis patients. Infection and Immunity. 75 (11), 5313-5324 (2007).
- Flynn, J. M., Niccum, D., Dunitz, J. M., Hunter, R. C. Evidence and role for bacterial mucin degradation in cystic fibrosis airway disease. PLoS Pathogens. 12 (8), 1005846(2016).
- Stites, S. W., Plautz, M. W., Bailey, K., O'Brien-Ladner, A. R., Wesselius, L. J. Increased concentrations of iron and isoferritins in the lower respiratory tract of patients with stable cystic fibrosis. American Journal of Respiratory and Critical Care Medicine. 160 (3), 796-801 (1999).
- Cornforth, D. M., et al. Pseudomonas aeruginosa transcriptome during human infection. Proceedings of the National Academy of Sciences. 115 (22), 5125-5134 (2018).
- Drevinek, P., et al. Gene expression changes linked to antimicrobial resistance, oxidative stress, iron depletion and retained motility are observed when Burkholderia cenocepacia grows in cystic fibrosis sputum. BMC Infectious Diseases. 8, 121(2008).
- Goerke, C., Wolz, C. Regulatory and genomic plasticity of Staphylococcus aureus during persistent colonization and infection. International Journal of Medical Microbiology. 294 (2-3), 195-202 (2004).
- Wolter, D. J., et al. Staphylococcus aureus small-colony variants are independently associated with worse lung disease in children with cystic fibrosis. Clin Infect Dis. 57 (3), 384-391 (2013).
- Roberts, A. E. L., Kragh, K. N., Bjarnsholt, T., Diggle, S. P. The limitations of in vitro experimentation in understanding biofilms and chronic infection. Journal of Molecular Biology. 427, 3646-3661 (2015).
- Ceri, H., et al. The Calgary biofilm device: New technology for rapid determination of antibiotic susceptibilities of bacterial biofilms. Journal of Clinical Microbiology. 37 (6), 1771-1776 (1999).
- Moskowitz, S. M., Foster, J. M., Emerson, J., Burns, J. L. Clinically feasible biofilm susceptibility assay for isolates of Pseudomonas aeruginosa from patients with cystic fibrosis. Journal of Clinical Microbiology. 42 (5), 1915-1922 (2004).
- Smith, S., Waters, V., Jahnke, N., Ratjen, F. Standard versus biofilm antimicrobial susceptibility testing to guide antibiotic therapy in cystic fibrosis. Cochrane Database of Systematic Reviews. (6), (2020).
- Trust, C. F. Annual Data Report 2019. , (2019).
- Angelis, A., et al. Social and economic costs and health-related quality of life in non-institutionalised patients with cystic fibrosis in the United Kingdom. BMC Health Services Research. 15 (1), 428(2015).
- Eidt-Koch, D., Wagner, T. O. F., Mittendorf, T., von der Schulenburg, J. M. G. Outpatient medication costs of patients with cystic fibrosis in Germany. Applied Health Economics and Health Policy. 8 (2), 111-118 (2010).
- Longitude Prize. , Available from: http://longitudeprize.org (2020).
- Harrington, N. E., Sweeney, E., Harrison, F. Building a better biofilm - Formation of in vivo-like biofilm structures by Pseudomonas aeruginosa in a porcine model of cystic fibrosis lung infection. Biofilm. 2, 100024(2020).
- Harrison, F., Diggle, S. An ex vivo lung model to study bronchioles infected with Pseudomonas aeruginosa biofilms. Microbiology. 162, 1755-1760 (2016).
- Sweeney, E., et al. An ex vivo cystic fibrosis model recapitulates key clinical aspects of chronic Staphylococcus aureus infection. Microbiology. , DOI: 10.1099/mic.0.000987 (2020).
- Palmer, K. L., Aye, L. M., Whiteley, M. Nutritional cues control Pseudomonas aeruginosa multicellular behavior in cystic fibrosis sputum. Journal of Bacteriology. 189 (22), 8079-8087 (2007).
- Nakagawa, S., Schielzeth, H. Repeatability for Gaussian and non-Gaussian data: A practical guide for biologists. Biological Reviews. 85 (4), 935-956 (2010).
- Sweeney, E., Sabnis, A., Edwards, A. M., Harrison, F. Effect of host-mimicking medium and biofilm growth on the ability of colistin to kill Pseudomonas aeruginosa. Microbiology. 166 (12), 1171-1180 (2020).
- Stalker, D. J., Jungbluth, G. L., Hopkins, N. K., Batts, D. H. Pharmacokinetics and tolerance of single- and multiple-dose oral or intravenous linezolid, an oxazolidinone antibiotic, in healthy volunteers. Journal of Antimicrobial Chemotherapy. 51 (5), 1239-1246 (2003).
- Ager, S., Gould, K. Clinical update on linezolid in the treatment of Gram-positive bacterial infections. Infection and Drug Resistance. 5, 87-102 (2012).
- Kirchner, S., et al. Use of Artificial Sputum Medium to Test Antibiotic Efficacy Against Pseudomonas aeruginosa in Conditions More Relevant to the Cystic Fibrosis Lung. Journal of Visualized Experiments: JoVE. (64), e3857(2012).
- The European Committee on Antimicrobial Susceptibility Testing. EUCAST Disk Diffusion Method for Antimicrobial Susceptibility Testing - Version 8.0. , Available from: www.eucast.org (2020).
- The European Committee on Antimicrobial Susceptibility Testing. Breakpoint tables for interpretation of MICs and zone diameters. Version 10.0. , Available from: http://www.eucast.org (2020).
Reprints and Permissions
Request permission to reuse the text or figures of this JoVE article
Request PermissionExplore More Articles
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. All rights reserved