Method Article
تصوير الخلايا الحية للنشاط النسخي في فواصل الحمض النووي مزدوجة ستراند
In This Article
Summary
يقدم هذا البروتوكول نظام جين مراسل جديد والإعداد التجريبي للكشف عن النسخ في فواصل حبلا مزدوجة الحمض النووي مع حساسية جزيء واحد.
Abstract
فواصل حبلا مزدوجة الحمض النووي (DSB) هي النوع الأكثر حدة من تلف الحمض النووي. على الرغم من العواقب الكارثية على سلامة الجينوم ، فإنه لا يزال بعيد المنال حتى الآن كيف تؤثر DSBs على النسخ. وكان السبب في ذلك هو عدم وجود أدوات مناسبة لرصد النسخ في وقت واحد وتحريض DSB genic مع دقة زمنية ومكانية كافية. يصف هذا العمل مجموعة من المراسلين الجدد الذين يتصورون النسخ مباشرة في الخلايا الحية مباشرة بعد تحريض DSB في قالب الحمض النووي. وتستخدم البكتيريا الحمض النووي الريبي الجذعية الحلقات لرصد النسخ مع حساسية جزيء واحد. لاستهداف DSB إلى منطقة جين محددة ، تم تصميم جينات المراسل لاحتواء تسلسل اعتراف واحد من الإندونوكلياز I-SceI ، غائبة عن الجينوم البشري. تم دمج نسخة واحدة من كل جين مراسل في جينوم خطوط الخلايا البشرية. يسمح هذا النظام التجريبي بالكشف عن جزيئات الحمض النووي الريبي المفردة الناتجة عن النسخ الجيني الكنسي أو عن طريق بدء النسخ الناجم عن كسر الحمض النووي. يوفر هؤلاء المراسلون فرصة غير مسبوقة لتفسير التفاعلات المتبادلة بين النسخ وتلف الحمض النووي والكشف عن جوانب غير مقدرة حتى الآن من النسخ الناجم عن كسر الحمض النووي.
Introduction
فواصل حبلا مزدوجة الحمض النووي (DSBs) هي آفات الحمض النووي السامة التي تعطل وظيفة الخلية وتساهم في تمرد العديد من الأمراض والشيخوخة1. الطفرات الناتجة عن إصلاح غير دقيق للDSBs تؤثر على التعبير الجيني ووضع الأساس للانخفاض الوظيفي للخلية. ويشير الرأي الناشئ بأن مركبات DSBs تقود النسخ الناجم عن كسر نوفو في موقع الآفة2،3،4،5،6،7 إلى أن DSBs قد تؤثر أيضا على الوظيفة الخلوية من خلال الرنانات الناجمة عن الكسر. وتشير عدة دراسات حديثة إلى أن مركبات ثنائي الفينيل متعددة المستويات كافية لبدء النسخ المبرمج (على سبيل المثال، في الجينات غير القابلة للانزكزاز) والنسخ غير المجدول (على سبيل المثال، لدى المروجين غير الكنسيين)4,5,7. ومع ذلك ، على الرغم من العديد من الدراسات التي تستكشف الروابط بين تلف الحمض النووي والنسخ ، لا يزال الحقل متخلفا في قدرته على تقديم توصيف دقيق (أي جزيء واحد) للأحداث النسخية في مواقع كسر الحمض النووي. وكان أحد الأسباب الهامة لذلك هو عدم وجود أدوات تجريبية مناسبة. إن تشعيع الخلايا (أشعة γ، والأشعة السينية، والأيونات الثقيلة)، والعلاجات الدوائية (مثل مثبطات توبويسوميراز أو عوامل التوليل) تفتقر إلى الدقة المكانية وتحفز آفات الحمض النووي غير مركبات ثنائي الفينيل متعددة الخلايا، بما في ذلك فواصل الخيط الواحد ووكلاء الحمض النووي8. تولد الخلايا الإندونوكلية، مثل I-PpoI و AsiSI، DSBs خاصة بالجراد ولكن لم يتم دمجها مع نظام يسمح بالتصور المتزامن للخلايا الحية للنسخ في مكان واحد بدقة زمنية عالية8. لتجاوز هذا القيد، قاد مختبرنا تطوير مجموعة من المراسلين المتطورين الذين يتصورون النسخ مباشرة بدقة جزيء واحد عند الحث الخاضع للرقابة ل DSB4 فريدة من نوعها. هنا، نصف هؤلاء المراسلين، ونقدم بروتوكولا مفصلا لتصوير النسخ بالخلايا الحية في DSBs ونعرض البيانات التي تكشف عن بدء النسخ في DSB واحد.
تستند أنظمة الجينات المراسل المستخدمة في هذا البروتوكول على الجين مراسل IgM الماوس تتميز جيدا وتحتوي على exons M1 و M2 من شكل غشاء ملزمة (μm) من IgM μ سلسلة ثقيلة9,10,11. فصل intron الهجين exons اثنين مع نص قوي adenovirus الرئيسية في وقت متأخر (AdML) PY tract12. يتم التحكم في التعبير عن جينات المراسل من قبل مروج الفيروس المضخم للخلايا البشري (CMV) ، حيث تم إدخال نسختين مترادفتين من تسلسل مشغل تيت (TetO). يتم إدخال جينات المراسل في ناقل بلازميد يحتوي على موقع هدف إعادة دمج Flp (FRT) وإدراجها في موقع مستهدف محدد ل FRT في جينوم خط الخلية المضيف HEK293. هذا الخط الخلية يعبر أيضا بشكل تأسيسي البروتين قمع تيت لتنظيم التعبير عن الجين مراسل عن طريق وجود أو عدم وجود التتراسيكلين / دوكسيسيكلين. وللسماح بتصور النسخ الجيني للمراسل، تم إدراج 24 تكرارا مترادفا لتسلسل الحلقة الجذعية MS2 و24 تكرارا مترادفا لتسلسل الحلقة الجذعية PP7 في مواقع مختلفة فيما يتعلق بموقع بدء النسخ وهيكل exon/intron لجين المراسل. تتشكل الحلقات الجذعية من MS2/PP7 RNA عند النسخ وترتبط على وجه التحديد ببروتينات معطف MS2/PP7 المعبر عنها خارج الرحم الموسومة بالبروتينات الفلورية الخضراء والحمراء ، وهي استراتيجية تستخدم على نطاق واسع من قبل لتصوير النسخ13،14،15. بالإضافة إلى ذلك، تم إدراج نسخة واحدة من تسلسل التعرف على 18 bp لedonuclease توجيه I-SceI التي تحيط بها مباشرة صفائف تسلسل حلقة الجذعية الحمض النووي الريبي في الجينات مراسل. واستخدمت تقنيات الاستنساخ القياسية لتوليد جميع البلازميدات، وتم توليف الجزء الذي يحتوي على حلقة الجذعية I-SceI-24xMS2 من جين مراسل PROP بواسطة خدمة توليف الجينات التجارية.
تم بناء الجين مراسل DSB المروج القريبة (PROP) عن طريق إدراج موقع القطع I-SceI 45 أزواج قاعدة (bp) المصب من موقع بدء النسخ المفترض في exon I، تليها 149 bp حتى بداية كاسيت حلقة الجذعية MS2 24x، الذي تم تصميمه دي نوفو مع اثنين من تسلسل حلقة الجذعية غير متطابقة بالتناوب16 وخمسة إضافية غير المتكررة 20 بت تسلسل المسافة للحد من التكرار. يتبع صفيف حلقة الجذعية MS2 72 نقطة أساس حتى بداية intron 1844 bp و 1085 bp exon II حتى موقع الانقسام والتعددية. يقوم exon II بترميز بروتين فلوري سماوي (CFP) منصهر في تسلسل استهداف بيروكسيسومال C-terminal (PTS) من أوكسيداز أسيل بيروسومال الإنسان للسماح بفحص مستقل للتعبير الجيني للمراسل (الشكل 1A).
الجين مراسل EXON II DSB (EX2) يتكون من exon 167 bp أنا تليها intron و exon II ترميز CFP-PTS. وفي اتجاه مجرى النهر على مسافة 169 نقطة أساس، تم إدخال كاسيت يحتوي على حلقات جذعية 24x MS2، يليه تسلسل وصلة 84 نقطة أساس مع موقع I-SceI في الوسط، يليه حلقات جذعية 24x PP7 و221 نقطة أساس حتى موقع الانقسام والتعددية 17 (الشكل 1B).
وأخيرا ، فإن الجين مراسل EXON II DSB مع وضع العلامات النسخ المضادة (EX2AS) يستند إلى نص الجين UBB-201 في كل مكان B (UBB) البشري ويحتوي على اثنين من exons وintron واحد. exon لدي طول إجمالي قدره 1534 نقطة أساس مع إدراج عكسي من 24x MS2 الجذعية حلقة التسلسل. لذلك ، سيتم نسخ تسلسل الحمض النووي الريبي الصحيح MS2 stem-loop في اتجاه مضاد فيما يتعلق بالنسخ المنطقي لجين المراسل من مروج CMV. يبلغ طول الإنترون 490 نقطة أساس، يليه exon II مع موقع I-SceI ، وتم إدراج منطقة ترميز لوحدات فرعية في كل مكان داخل الإطار. المصب من الجين UBB هو التسلسل الذي يشكل 24x PP7 الجذعية حلقة عند نسخ الجين مراسل في اتجاه المعنى (الشكل 1C).
يسمح التحويل العابر للبناء غير القابل للاختزال ل I-SceI بالتحكم في إنشاء DSB في موقع التعرف المدرج داخل كل جين مراسل18. يتم دمج الإندونوكليز I-SceI في الإطار مع المجال الملزم لليجند لمستقبلات الجلوكوكورتيكويد وبروتين فلوري أحمر بعيد iRFP713. هذا البناء هو السيتوبلازمية في غياب الأسيتونيد تريامسينولون (TA) ولكن يهاجر بسرعة إلى النواة عند إضافة TA إلى متوسط النمو للخلايا (الشكل 1D). إن تحريض DSBs من قبل نظام I-SceI قوي ، كما هو موضح قبل 18،19،20. ويمكن رصد النسخ الجيني للمراسل بالتوازي من خلال تصور أنظمة الحمض النووي الريبي الموسومة بالفلورسنت MS2 و PP7.
Protocol
1. إعداد ونقل الخلايا للفحص المجهري للخلايا الحية
- إعداد قارورة ثقافة الخلية 25 سم2 من خط خلية المراسل (EX2، EX2-AS، أو PROM) مع 5 مل من DMEM لتحقيق التقاء 80-90٪ في اليوم السابق لتجربة المجهر الخلية الحية.
- يستنشق الوسط مع ماصة من قارورة 25 سم2 ثقافة الخلية وغسل الخلايا مع 2.5 مل من برنامج تلفزيوني 1x.
- أضف 1 مل من التريبسين-EDTA (0.05٪) واحتضن عند 37 درجة مئوية لمدة 2-3 دقائق لمفرزة الخلايا.
- بعد انفصال الخلية، إضافة 4 مل من DMEM دون فينول الأحمر الذي يحتوي على العازلة HEPES، تكملها مع 10٪ (v/v) مصل البقر الجنيني جردت الفحم، وإعادة إنفاق الخلايا بلطف.
- لوحة 1 مل من محلول الخلية في طبق دائري 35 ملم مع 10 ملم الزجاج القاع جيدا (قطرها رقم 1.5) ومتجانسة. قم بتخزين طبق دائري مقاس 35 مم داخل طبق قياسي استزراع الخلايا مقاس 100 مم واحتضنه عند 37 درجة مئوية في جو رطب مع 5٪ من ثاني أكسيد الكربون.
- ~ 6 ساعة بعد البذر، وtransfect الخلايا في طبق أسفل الزجاج. لكل خليط من خليط العدوى، قم بإعداد حلين بالطريقة التالية:
- في أنبوب 1.5 مل من أجهزة الطرد المركزي الدقيق، قم بإعداد الحل A الذي يحتوي على 150 ميكرولتر من الحد الأدنى من المتوسط الأساسي للمصل المنخفض (MEM)، والحمض النووي البلازميد (كما هو موضح في الجدول 1)، و2.5 ميكروغرام/ميكرولتر من الحمض النووي لكواشف مساعد العدوى (انظر جدول المواد).
- وبالتوازي مع ذلك، قم بإعداد المحلول B، الذي يحتوي على 150 ميكرولتر من MEM منخفض المصل و1.5 ميكروغرام/ميكرولتر من الحمض النووي لموشف العدوى القائم على الدهون (انظر جدول المواد).
- احتضان كلا الحلين في درجة حرارة الغرفة (RT) لمدة 5 دقائق. ثم، أضف الحل بلطف A إلى الحل B واحتضان 20 دقيقة في RT.
- لتضمين الخلايا، أضف 300 ميكرولتر من الحل A+B إلى كل طبق واوزعه برفق. تخزين طبق القاع الزجاجي داخل طبق زراعة الخلايا القياسية 100 ملم واحتضانه في 37 درجة مئوية في جو رطب مع 5٪ CO2.
- إعداد أنبوب 1.5 مل من أجهزة الطرد المركزي الدقيق مع 200 ميكرولتر من DMEM مع HEPES، دون فينول الأحمر تكملها مع 10٪ (v/v) مصل البقر الجنيني جردت الفحم وإضافة TA إلى تركيز 7.5 × 10-7 M.
2. الإعداد التجريبي
- تعيين درجة حرارة غرفة حضانة المجهر الزجاجي الكبير وغرفة حضانة المرحلة العليا إلى 37 درجة مئوية في وحدة التحكم المشتركة. ضبط الظروف البيئية داخل غرفة حضانة المرحلة إلى 5٪ CO2 والرطوبة 100٪.
ملاحظة: يجب إعداد قفص المجهر ودرجة حرارة حاضنة المرحلة على الأقل 1 ساعة قبل بدء التجربة للسماح بتسخين النظام الكامل لتقليل تقلبات درجة الحرارة. بدء تشغيل جميع وحدات التحكم والتشغيل الأخرى في المجهر في نفس الوقت. - حث النسخ من الجينات مراسل بإضافة دوكسيسيكلين (0.5 ميكروغرام / مل) إلى متوسط النمو ومزيج بلطف عن طريق الأنابيب صعودا وهبوطا مع 200 ميكروبايت ميكروبينيت ~ 1 ساعة قبل البدء في مراقبة المجهر.
ملاحظة: الحفاظ على طبق الزجاج القاع مع الخلايا المصابة داخل طبق ثقافة الخلية القياسية 100 ملم لسهولة التعامل مع ونقل من ثقافة الخلية إلى غرفة المجهر في حاوية الستايروفوم للحفاظ على درجة الحرارة مستقرة قدر الإمكان. - نقل الخلايا إلى المجهر على الأقل 30 دقيقة قبل بدء الملاحظة وعند الوصول، وضع طبق 100 ملم مع الخلايا مباشرة داخل غرفة حضانة المجهر كبيرة ساخنة مسبقا.
- ضع أنبوب الطرد المركزي الدقيق مع TA المخفف مسبقا من الخطوة 1.7. داخل غرفة المجهر البيئية الكبيرة لتسخين ما يصل إلى 37 درجة مئوية.
- استبدل غطاء طبق القاع الزجاجي المشابه للغطاء الذي تم إعداده من قبل بثقب قطره 3 مم محفور في الغطاء (الشكل 2A).
ملاحظة: سيتم إضافة TA لاحقا إلى الخلايا من خلال ثقب صغير في الغطاء دون التلاعب الطبق شنت على مرحلة المجهر. - حدد هدف غمر الزيت 100x (الهدف الأبوكروماتيكي، الفتحة العددية 1.4) في لوحة التحكم بالمجهر. تطبيق قطرة من زيت الغمر إلى الهدف.
- تعيين طبق الزجاج القاع مع الخلايا داخل غرفة حضانة مرحلة المجهر وقفل في مكانها. أغلق غطاء حاضنة المسرح وجميع أبواب سكن المجهر.
- بدء تشغيل المجهر والتحكم في البرامج، افتح إطار التحكم التركيز (الشكل 2B)، انقر على جزء النطاق ، وفي جزء تحديد الانبعاثات ، انقر فوق مربع العين 100٪ لتعيين مسار شعاع العين للمراقبة العين مباشرة بالعين.
- في القائمة تصفية تعيين ، قم بالتبديل إلى تعيين فلتر العين وانقر فوق برايتفيلد، واضغط على الزر فتح برايتفيلد .
- حرك هدف المجهر نحو طبق القاع الزجاجي حتى يلمس الزيت الزجاج. ثم ننظر من خلال العين والتركيز يدويا على مستوى الخلايا. قم بإيقاف تشغيل الزر فتح برايتفيلد .
- اترك الخلايا لمدة 30 دقيقة قبل البدء في الملاحظات التجريبية للتكيف مع الظروف البيئية ومنع الانجراف البؤري أثناء التصوير بواسطة تدرجات درجة الحرارة.
- ضع 200 ميكروبايت ميكروبايت و200 ميكرولتر نصائح مرشح جاهزة للاستخدام جانبا في درجة حرارة الغرفة.
3. الحصول على صورة
- في إطار التحكم البؤري لبرنامج التحكم بالمجهر، قم بتعيين كثافة الليزر إلى 5٪ وأدخل قيمة 50 مللي ثانية لوقت التعرض (الشكل 2B).
- افتح نافذة Capture لضبط الإعدادات لتنفيذ عملية اقتناء تلقائي للصورة من الفواصل الزمنية ثلاثية الأبعاد (3D) (الشكل 2C).
- حدد نوع اكتساب الالتقاط ثلاثي الأبعاد وحدد 12 إلى 16 شريحة بصرية مفصولة ب 0.4 ميكرومتر، وحدد مربعات الاختيار الخاصة بالنطاق حول الحالي والعودة إلى الوضع الحالي بعد الالتقاط.
- في جزء التقاط Timelapse أدخل قيمة 120 ل # من نقاط الوقت و 30 ثانية للفاصل الزمني.
- حدد مرشح confocal تعيين وفقا لتسميات البروتين الفلورية المصابة مع λ = 488 نانومتر لGFP، λ = 561 نانومتر لTagRFPt، و λ = 640 نانومتر ل iRFP713 وتعيين وقت التعرض لكل قناة إلى 50 مللي ثانية.
- استخدم الإعداد الحالي لطاقة الليزر لاستخدام قيمة 5٪ المحددة في إطار التركيز (الشكل 2C).
- في إطار التحكم في التركيز ، انتقل إلى جزء الكاميرا ، وحدد عنصر التحكم في عرض صورة Scale واختر الزر يدوي لإعداد نطاق ثابت من شدة الصورة ليتم عرضه. أدخل قيم منخفض: 500 وأعلى: 5000 (راجع الشكل 2B).
ملاحظة: يحد هذا الإعداد من النطاق الديناميكي لالتقاط الكاميرا المعروض في طريقة العرض المباشرة لتحديد الخلايا ضمن نفس النطاق من كثافة الفلورسينس (الشكل 2D). - حدد الخلايا للتصوير الفاصل الزمني ثلاثي الأبعاد لمواقع النسخ عند تحريض DSB. قم بفحص الخلايا وحدد ثلاثة حقول للعرض وفقا للشروط الموضحة في المناقشة.
- التركيز على كل خلية مختارة موجودة سابقا في وسط مجال الرؤية مع موقع النسخ في المستوى الأوسط من المكدس Z.
ملاحظة: توسيط الخلية وموقع النسخ في XYZ يستوعب لبعض حركة الخلية. - وضع علامة على كل موضع XYZ في جزء XY من إطار التحكم في التركيز بالنقر فوق تعيين نقطة.
ملاحظة: إعادة زيارة المناصب المختارة 2-3 مرات على مدى 5 دقائق التالية لتأكيد النسخ المستمر لجينات المراسل والاستقرار الموضعي النسبي لمواقف الخلايا في أبعاد XYZ. - أضف 200 ميكرولتر من TA المخفف مسبقا من الخطوة 1.7. إلى الخلايا كما هو موضح في الشكل 2F.
ملاحظة: الحرص الشديد على عدم لمس طبق الزجاج القاع أو الغطاء أثناء إضافة TA لمنع أي تحول من المواقف XY ملحوظ. بعد التعريفي DSB، تأكد من أن تتركز الخلايا داخل مجال الرؤية، وموقع النسخ في وسط Z-الطائرة. يجب أن يستغرق تحديث إعادة التركيز والموقع ما لا يزيد عن 1-2 دقيقة. - ابدأ التصوير ثلاثي الأبعاد من خلال النقر على البدء في نافذة Capture .
- حفظ بيانات التصوير في تنسيق بيانات برنامج التحكم بالمجهر على القرص الصلب للكمبيوتر التحكم بالمجهر.
4. تحليل البيانات
- افتح بيانات التصوير في برنامج التحكم بالمجهر واصدر كملفات بتنسيق TIFF 16 بت.
- افتح الملفات المصدرة باستخدام برنامج StaQtool21 . حدد الوضع 3D بقعة واحدة وتحميل ملفات الصور عن طريق الضغط على الذهاب.
ملاحظة: يتم فتح السلسلة الزمنية المحددة في عارض الفاصل الزمني ل Max Projection، حيث تظهر إسقاط الحد الأقصى للكثافة لبنية z لنقطة المرة الأولى (الشكل 3A). - اضبط شاشة شدة الصورة مع شريط تمرير MAX العمودي على الجانب الأيسر.
- حدد نقطة التوقيت للتحليل باستخدام شريط تمرير Timepoint الأفقي.
- مرر المؤشر إلى موضع موقع النسخ المسمى لوضع علامة يدويا على وظيفة الكشف التلقائي أو استخدامها واضغط على موقع النسخ المعني إذا تم اكتشاف العديد من الكائنات.
- استخدم وظيفة المسار التلقائي لتحديد مواقع XYZ لموقع النسخ بمرور الوقت.
ملاحظة: إذا لم يتم تعقب موضع معين بشكل صحيح، حدد موقع النسخ يدويا وفقا لدليل برامج StaQtool. - اضغط على الزر تلقائي لإجراء تركيب الغاوس لكل نقطة زمنية وقياس كثافة الفلورسينس الكلية (TFI).
ملاحظة: إذا توقف نشاط النسخ، تبقى أداة التتبع في الموضع الأخير حيث تم اكتشاف كائن محدود الحيود (موقع نسخ يحمل علامة). إذا تحركت الخلية في اتجاه XY بعد اختفاء تسمية موقع النسخ، يلزم إجراء تغيير موضع يدوي لمربع البحث . - بعد الانتهاء من قيمة TFI المناسب لكل نقطة زمنية، اضغط على الزر إنهاء الفاصل الزمني لإغلاق ملف صورة السلسلة الزمنية الحالي والمتابعة إلى الملف التالي.
ملاحظة: يتم تصدير قيم TFI تلقائيا وحفظها في ملف Excel.
5. قياسات معايرة المجهرية وتحليل
- خلايا البذور في 35 مم أطباق الزجاج القاع وtransfect مع MS2 الموسومة فلوريا وPP7 معطف البروتينات كما هو موضح في القسم 1.
ملاحظة: بالنسبة لقياسات المعايرة، استخدم نفس خطوط الخلايا الجينية للمراسل الموضحة في المقدمة. - إضافة 0.5 ميكروغرام / مل من دوكسيسيكلين إلى متوسط النمو للخلايا 1 ساعة قبل البدء في اكتساب صورة المجهر.
- قم بتركيب طبق القاع الزجاجي داخل غرفة حضانة مرحلة المجهر واستعد لاكتساب الصورة كما كان من قبل (انظر القسم 2).
ملاحظة: لا يتم استبدال الغطاء الأصلي للطبق السفلي الزجاجي لتجارب المعايرة. - استخدم نفس إعدادات كثافة الليزر والتعرض كما هو موضح في النقطة 3.1.
- تعيين إعدادات التقاط لسلسلة زمنية ثنائية الأبعاد (إلغاء تحديد الخيار ثلاثي الأبعاد في جزء "نوع الالتقاط ") وتعيين 120 timepoints على فترات زمنية من 500 مللي ثانية في لوحة التقاط Timelapse (الشكل 2C).
ملاحظة: سيؤدي إعداد الحصول على الصورة هذا إلى سلسلة زمنية داخل مستوى بصري واحد على فترات قصيرة جدا. - الحصول على العشرات من سلسلة زمنية المعايرة من مواقع متعددة لتوليد مجموعات البيانات لحساب عدة مئات من النصوص واحد قياسات TFI.
- لتحليل سلسلة زمنية المعايرة تحويل الملفات إلى ملفات تنسيق TIFF 16 بت وفقا لذلك إلى نقطة 4.1.
- افتح الملفات المصدرة باستخدام برنامج StaQtool21 (الشكل 3). اضغط على الزر Select LOG file ، اختر Logfile من سلسلة الوقت 2D المعنية المكتسبة كما هو موضح في النقطة 4.2.
- حدد خانة الاختيار 2D البقع المتعددة واضغط على زر GO لتحميل السلسلة الزمنية في برنامج التحليل.
- في إطار عارض Timelapse (الشكل 3A) ، في PSF FWHM ، يدخل حقل الإدخال القيمة المحسوبة لنظام المجهر والهدف كما هو موضح21.
- لبدء عملية التحليل، اضغط على الزر الكشف التلقائي للكشف عن جميع الكائنات ذات الحيود المحدودة للنقطة الزمنية الحالية المعروضة. ثم انقر فوق AutoFit لتنفيذ "المناسب الغاوسي" لتحديد قيمة TFI لكل كائن (الشكل 3A).
- بدلا من ذلك، أشر المؤشر فوق كائن محدود الحيود وانقر لتحديده (تظهر دائرة خضراء داخل مربع أبيض)، واضغط على زر الغاوسية صالح للاختيار اليدوي وإجراء تركيب الغاوس.
ملاحظة: ينصح الوضع الأخير لاستبعاد الكائنات التي لم يتم حسابها، مثل مواقع النسخ الساطع مع العديد من النسخ الوليدة الموجودة في نفس النواة. - اضغط على الزر إنهاء الفاصل الزمني لإنهاء الخطوة السابقة.
ملاحظة: يتم حفظ النتائج تلقائيا بتنسيق ملف Microsoft Excel في نفس المجلد كملف الصورة. - بدء وحدة توزيعات TFI و W لعدة نقاط بالضغط على الزر المعني (الشكل 3B).
- تحميل ملفات Excel عبر الزر إضافة ملف وبدء تحليل TFI بالضغط على زر الانتقال.
ملاحظة: الإخراج هو قيمة TFI المتوسطة المحددة من عدة نصوص مفردة تم قياسها TFIs. - بدء تحليل W عن طريق إدراج FWHM PSF المستخدمة سابقا في نقطة 5.10. واضغط على الزر الانتقال باستخدام القيمة الافتراضية للسلة.
ملاحظة: المعلمة W هو مراقبة الجودة للقياسات TFI نص واحد للامتثال لقيمة FWHM PSF الصحيح لنظام المجهر المستخدمة.
6. دمج البيانات والمعايرة
- أدخل قيم TFI السلسلة الزمنية التي تم الحصول عليها من ورقة Excel المحفوظة في النقطة 4.8. إلى ورقة Excel جديدة وقسمة كل قيمة نقطة زمنية على متوسط TFI للنصوص المفردة التي تم الحصول عليها في النقطة 5.15.
ملاحظة: لتوحيد هذه العملية، تم استخدام نماذج قالب Excel معدة خصيصا.
النتائج
تسمح خطوط الخلية التي تؤوي جينات المراسل الموصوفة في الشكل 1A-C بدراسة ديناميكيات النسخ في DSB واحد في الخلايا الحية. تشير الأرقام في الشكل 1A-C أسفل كل تمثيل جيني مراسل رسومي إلى الطول في أزواج الكيلوبيس (kbp). تشير CMV إلى أن مروج الفيروس المضخم للخلايا ، TetO هو تسلسل مشغل Tet ، ويسلط pA الضوء على موقع الانقسام وتعدد الأدينيل 3 في نهاية الجين. CFP-PTS هو بروتين فلوري سماوي مشفر منصهر في إشارة استهداف بيروكسيسومال ، و2UBB هي وحدة الترادف البشري المشفرة في كل مكان B. باتباع البروتوكول وإجراءات التحليل الموضحة أعلاه، يمكن الحصول على رسوم بيانية تعرض عدد النصوص الجينية للمراسلات ذات العلامات الفلورية بمرور الوقت، مع دقة زمنية لثوان على فترات تصل إلى ساعات (الشكل 4A-D). يعرض الرسم البياني في الشكل 4A المسار الزمني لقيم TFI لموقع نسخ الجينات لمراسل PROM المسمى بتراكم جزيئات MS2-GFP على النصوص الوليدة. يمثل هذا الرسم البياني الخاص تجربة تحكم بدون إضافة TA؛ لذلك، يتم حث أي DSB. النسخ لا يزال مع قمم انفجار مثل و2-8 النصوص في وقت واحد على مدى فترة المراقبة بأكملها من 60 دقيقة. تم الحصول على نتائج مماثلة لجينات المراسل EX2 و EX2-AS (البيانات غير الموضحة هنا)4. يسمح تحريض DSBs واحد في جينات المراسل (باستخدام I-SceI-GR-iRFP) بدراسة تأثير DSB على النسخ الجيني للمراسل المستمر ورصد أحداث النسخ الناشئة من موقع DSB ، وهي النسخ الناجم عن الكسر (الشكل 4B-D).
تعتمد ديناميكيات النسخ الناجم عن كسر الحمض النووي على موقع DSB داخل الجين
يؤدي تحريض DSB واحد من قبل I-SceI-GR-iRFP في جين المراسل مع موقع التعرف على I-SceI المروج القريب إلى إسكات النسخ لجين المراسل بعد حوالي 11 دقيقة بعد إضافة TA ، ولا يتم استعادة النسخ خلال فترة الملاحظة البالغة 60 دقيقة (الشكل 4B). عند مراقبة النسخ الجيني لمراسل EX2 ، تم اكتشاف القمع الكامل للنسخ الكنسي الذي يحركه المروج من خلال فقدان كامل في وقت واحد لكل من إشارات MS2-GFP و PP7-RFP حوالي 30 دقيقة بعد إضافة TA. ومع ذلك ، في غضون 10 دقائق ، وإعادة تشغيل النسخ ، كما كشفت عن القمم التي تظهر من جديد PP7 - RFP الفلورسينس. يظهر الاسترداد الكامل لإشارة PP7-RFP (وليس مضان MS2-GFP) بدء النسخ الناجم عن الكسر (الشكل 4C). النسخ الناجم عن كسر ليست مستقرة على مدى فترات طويلة; يبدو انفجار مثل وانخفاض كثافة الذروة، مما يدل على أن بدأت سوى عدد قليل من النصوص الناجمة عن كسر من موقع DSB.
الجين مراسل EX2AS، الذي يحتوي على 24x PP7 الجذعية حلقة الصفيف في exon II المصب من موقع I-SceI للكشف عن النسخ الشعور، ويبين النسخ الكنسي يحركها المروج إنهاء داخل الجين مراسل EX2AS في غضون ما يقرب من 25 دقيقة بعد إضافة TA. ثم يتم استبداله النسخ المضادة للاستراحة الناجمة، كما كشفت عن تراكم البروتين MS2-GFP ملزمة للجيش الملكي النيبالي ولدت من تسلسل حلقة الجذعية MS2 antisense (الشكل 4D). كان النشاط النسخي المضاد للمنطق غائبا قبل انقطاع النسخ المنطقي بسبب تحريض DSB ويظهر في هذا المثال أن العديد من النصوص بدأت من موقع الاستراحة في غضون حوالي 15 دقيقة. وتظهر البيانات التمثيلية التي تم الحصول عليها هنا أن DSBs لها تأثيرات مختلفة على النسخ اعتمادا على موقعها داخل الجين ، كما تم الإبلاغ عنه مؤخرا4. وتكشف البيانات أيضا عن تقلب خلية إلى خلية في توقيت تحريض DSB بواسطة I-SceI-GR-iRFP، والذي يتراوح من 12 إلى 30 دقيقة بعد إضافة TA. وعلاوة على ذلك، فإن الكشف عن النصوص الفردية يسمح باكتشاف الاختلافات بين الخلية والخلية وكسر الموقع نحو كثافة النشاط النسخي الناجم عن الكسر. يتم الكشف عن النسخ الناجم عن كسر فقط في DSBs داخل الجين. وهي غائبة في DSBs المروج القريبة ، حيث يتوقف النسخ الكنسي عند DSB لفترة المراقبة المتبقية.
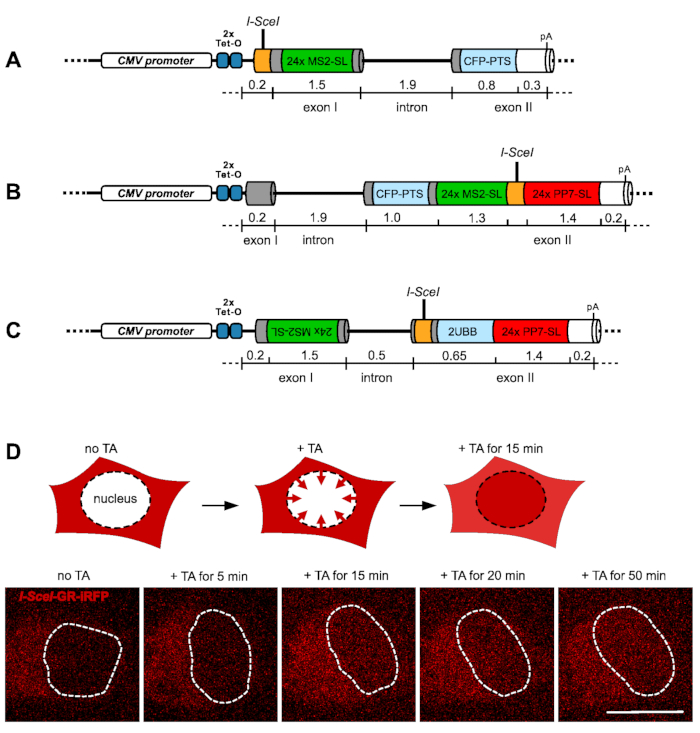
الشكل 1: جينات المراسل والنظام للحث على فواصل الحمض النووي المزدوج حبلا. يظهر التمثيل التخطيطي في (A) إلى (C) بنية جينات المراسلين الثلاثة المستخدمة لدراسة النسخ عند تحريض كسر حبلا مزدوج الحمض النووي. يصور الجين مراسل مع المروج القريبة I-SceI الموقع في exon الأولى (PROM) محاطة المصب من قبل 24x MS2 الجذعية حلقة (MS2-SL) صفيف تسلسل في (A). يظهر جين المراسل مع موقع I-SceI في exon الثاني (EX2) المحاط بالمصب مع تسلسل حلقة جذعية MS2 24x ومصب النهر من خلال صفيف حلقة جذعية 24x PP7 (PP7-SL) في (B). يظهر في (C) جين المراسل مع موقع I-SceI الموجود في exon II مع إدخال مضاد لالتوازي لتسلسل حلقة الجذعية MS2 24x في المنبع لموقع I-SceI للكشف عن النسخ المضاد (EX2-AS). يتم تصوير وظيفة بناء بروتين الاندماج I-SceI-GR-iRFP في (D) من خلال شاشة رسومية وصور مناظرة للخلايا الحية أدناه. عند التعبير العابر عن البناء (اللون الأحمر) في خطوط الخلايا الجينية للمراسل ، يكون البروتين سيتوبلازميا حصريا ، مما يمنع حدوث شق سابق لأوانه للموقع المستهدف بواسطة الإندونوكليز I-SceI. عند إضافة TA ، يبدأ بروتين الاندماج في الهجرة إلى نواة الخلية (المشار إليها بخط متقطع) ويبدأ في التراكم بين 5-15 دقيقة. Scalebar = 10 ميكرومتر الرجاء الضغط هنا لعرض نسخة أكبر من هذا الرقم.
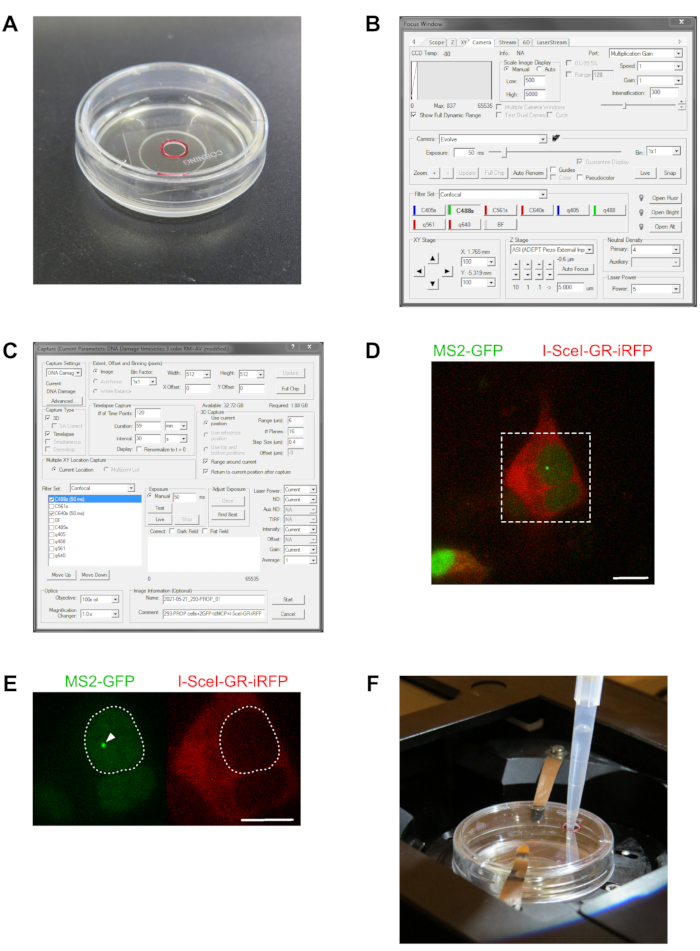
الشكل 2: اختيار خلايا للتصوير ثلاثي الأبعاد الفاصل الزمني لمواقع النسخ. تظهر الصورة في (A) طبقا زجاجيا سفليا مقاس 35 مم يستخدم لتصوير الخلايا الحية ، مع غطاء معدل مخصص ، حيث تم حفر ثقب قطره 3 مم لإضافة TA المخفف في متوسط النمو مباشرة. تم وضع علامة على موقع الحفرة بدائرة حمراء. تعرض اللوحة في (B) لقطة شاشة لنافذة "Focus" لبرنامج التحكم في المجهر لإعداد وقت التعرض للعرض المباشر وإعداد التصفية وكثافة الليزر وعرض صورة المقياس على الشاشة للخلايا للتصوير اللاحق بفاصل زمني في (C) ، وهي لقطة شاشة نافذة "Capture" المقابلة لضبط جميع الإعدادات للحصول على الفاصل الزمني ثلاثي الأبعاد للخلايا الحية. يتم وصف الإعدادات المحددة لعوامل التصفية، ونوع الالتقاط، والالتقاط الزمني، وأجزاء الالتقاط ثلاثي الأبعاد في القسم 3. في المنظر الموضح هنا ، يتم تعديل الإعدادات للحصول على الفاصل الزمني ثلاثي الأبعاد لخط جين مراسل PROM المصاب مع MS2-GFP و I-SceI-GR-iRFP لبناء نسخ التصوير عند تحريض كسر مزدوج الخيط للحمض النووي في المنطقة القريبة من الجين المراسل. يتم دمج الصورة في (D) لقنوات GFP و iRFP وتظهر مجال الرؤية كما رأينا من خلال نظام المجهر ، مع العديد من خلايا خط الخلية الجينية لمراسل 293-PROM. تم دمج الخلايا مع بناء بروتين معطف MS2 dimer جنبا إلى جنب تنصهر في تسلسل التعريب النووي ، واثنين من البروتينات الفلورية الخضراء (GFP-MS2CP) ، وبناء I-SceI-GR-iRFP. تظهر العديد من الخلايا تعبيرا عن بناء GFP-MS2CP ، وبالتالي تسليط الضوء على النواة وبناء I-SceI-GR-iRFP الذي يسلط الضوء على السيتوبلازم. يشير المربع المتقطع إلى المنطقة المكبرة الموضحة في (E). بالنسبة للتصوير ثلاثي الأبعاد، يتم اختيار الخلايا وفقا للمتطلبات الممنوحة في المناقشة، مثل الخلية ذات النواة الأكبر في المنطقة المكبرة في (D). يتم تحويل هذه الخلية مع كل من بنيات الفلورسنت ويظهر موقع النسخ المسمى الزاهية (رأس السهم) عن طريق تجميع GFP-MS2CP على دي نوفو المنسوخة مراسل الجينات قبل mRNAs (الصورة اليسرى). لا يحتوي متوسط النمو للخلايا على TA؛ لذلك ، فإن بناء I-SceI-GR-iRFP هو سيتوبلازمي حصرا (الصورة اليمنى). في (F)، يتم تركيب طبق القاع الزجاجي في غرفة حضانة مرحلة المجهر لتجارب التصوير ثلاثي الأبعاد المزودة بغطاء مخصص يحتوي على ثقب تحميل TA. يتم إدخال طرف 200 ميكروبايت ميكروبايت بعناية في الحفرة لتطبيق TA المخفف على وسيط النمو في الخلايا. Scalebar = 10 ميكرومتر الرجاء الضغط هنا لعرض نسخة أكبر من هذا الرقم.
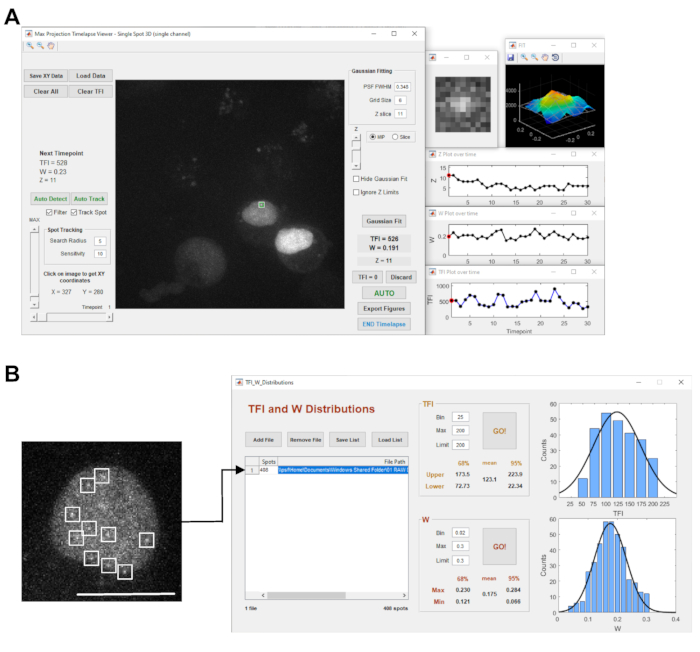
الشكل 3: برنامج اقتناء الصور وتحليلها. لوحة في (أ) يظهر لقطة شاشة من STaQTool: بقعة تتبع وكمية أداة. تعرض الصورة مثالا للسلسلة الزمنية لخط الخلية الجيني لمراسل PROM مع موقع نسخ يحمل علامة مع دائرة خضراء / مربع أبيض في عرض الإسقاط الأقصى الكثافة في الوسط. تعرض النوافذ الموجودة على الجانب الأيمن عرضا مكبرا لبقعة موقع النسخ المحددة ، ومؤامرة سطح الكثافة المظللة ثلاثية الأبعاد المقابلة مع شبكة الملاءمة الغاوسية 2D للنقطة الزمنية الحالية بالإضافة إلى مؤامرات لموقع النسخ بقعة Z موضع داخل z-stack وعرض الملاءمة الغاوسية (W) وقياس TFI بمرور الوقت. تظهر الصورة المجهرية في (B) مستوى بصري واحد مكبر لنواة خط الخلايا الجينية لمراسل PROM المصاب ب MS2-GFP. تمثل الصورة نقطة لمرة واحدة لسلسلة زمنية معايرة 2D مع 120 نقطة زمنية. تظهر النواة العديد من النصوص المسماة بالفلورسنت التي تظهر ككائنات محدودة الحيود في النيوكليوبلازم (التي تتميز بمربعات بيضاء). تعرض اللوحة اليمنى لقطة شاشة لأداة توزيع TFI وW في STaQTool لتحليل نقاط متعددة في عمليات الاستحواذ على الفاصل الزمني 2D. في هذا التحليل المثال، اكتشفت الأداة 408 بقع محدودة الحيود تمثل نصوص الجينات مراسل المسمى مع MS2-GFP التي تنتشر في النيوكليوبلازم. تعرض الرسوم البيانية الموجودة على اليمين مخططات توزيع عرض TFI وGassian المناسبة للكائنات ومنحنيات الملاءمة الغاوسية. يتم عرض قيم المتوسط TFI و W المستمدة من موضع الذروة الوسطى لمنحنى الملاءمة الغاوسية وفواصل الثقة المحسوبة في الجزء المعني. Scalebar = 10 ميكرومتر الرجاء الضغط هنا لعرض نسخة أكبر من هذا الرقم.
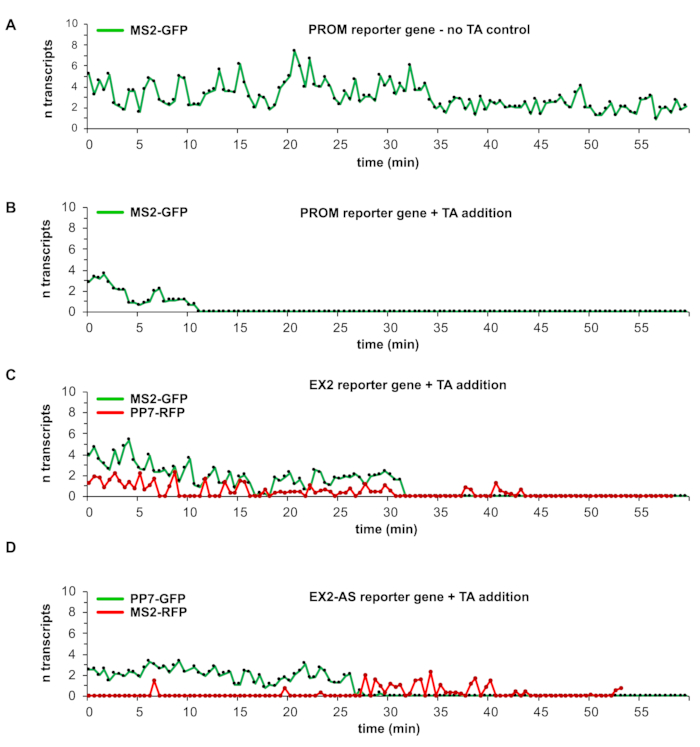
الشكل 4: النتائج التمثيلية للكشف عن النسخ في مواقع فواصل حبلا مزدوجة الحمض النووي. تمثل الرسوم البيانية في (A) إلى (D) منحنى TFI معايرة من موقع نسخ واحد مع مرور الوقت. يتم تحويل قيم TFI إلى نصوص باستخدام متوسط TFI من النصوص الفردية التي تقاس في تجارب المعايرة لبناء جين المراسل المعني والبروتين الرابط الحلقي الجذعي الحمض النووي الريبي الموسوم بالفلورسنت MS2 أو PP7 المستخدم في التجربة المعنية. في (A)، يظهر رسم بياني من تجربة تحكم باستخدام جين مراسل PROM بدون إضافة TA. وتشير النصوص المسماة ب MS2-GFP إلى استمرار النشاط النسخي طوال فترة المراقبة. يمثل الرسم البياني في (B) جين مراسل PROM عند إضافة TA وتحريض DSB مما يؤدي إلى قمع النسخ لوقت المراقبة المتبقي. الرسم البياني الجينات مراسل EX2 في (C) يظهر قمع النسخ من النسخ الكنسي يحركها المروج على إضافة TA. وفي وقت لاحق من نفس الفاصل الزمني، لا يظهر سوى نشاط النسخ المسمى PP7-RFP. في الرسم البياني في (D) ، يتم قمع النسخ الجيني لمراسل EX2-AS من المروج الكنسي في اتجاه المعنى بالمثل عند إضافة TA إلى جين مراسل EX2 في (C). ومع ذلك ، فإن ظهور MS2 - RFP المسمى النصوص الناشئة من المدرجة عكسي MS2 الجذعية حلقة تسلسل يشير إلى النسخ antisense غائبة خلال نشاط النسخ الشعور قبل إضافة TA. يرجى النقر هنا لعرض نسخة أكبر من هذا الرقم.
| خط خلية المراسل | EX2 و EX2-AS | الحفله الراقصه |
| بلازميدات إلى ترانسفيكت | 1.5 ميكروغرام pI-SceI-GR-iRFP | 1.5 ميكروغرام pI-SceI-GR-iRFP |
| 0.65 ميكروغرام pUBC-mCherry-nls-tdPP7-mCherry | 0.5 ميكروغرام pUBC-GFP-nls-tdMS2-GFP | |
| 0.35 ميكروغرام pUBC-GFP-nls-tdMS2-GFP |
الجدول 1: نقل خطوط الخلايا الجينية للمراسل. يصف الجدول مخططات العدوى وكميات البلازميدات المختلفة المستخدمة لتدوير خطوط الخلايا الجينية المراسلة المختلفة بشكل عابر.
Discussion
وقد تم تحديد الصراعات بين العمليات البيولوجية الأساسية مثل النسخ المتماثل والنسخ وتلف الحمض النووي وإصلاح الحمض النووي كمصدر حاسم لعدم استقرار الجينوم22. وقد أدت هذه الدراسات أيضا إلى اكتشاف النسخ في مواقع تلف الحمض النووي وعزت دورا وظيفيا إلى النصوص الناجمة عن الكسر في تنظيم عمليات إصلاح تلف الحمض النووي23. تسمح الأدوات الجديدة والبروتوكول الموصوف هنا بإجراء مزيد من التحقيق في ديناميكيات نسخ الحمض النووي الريبي Pol II في DSBs. ومن النقاط الحاسمة في هذا البروتوكول توليد خطوط الخلايا التي تحتوي على نسخة واحدة من جين المراسل المدمج في الجينوم. هذه الميزة الرئيسية يزيل الضوضاء الناجمة عن نسخ العديد من الجينات مراسل متكاملة مع نسخ متعددة داخل مكان الجينوم واحد ويسمح بجمع المعلمات الحركية من ديناميات النسخ والنصوص الحمض النووي الريبي الفردية. ومن المتطلبات التقنية الحاسمة لمراقبة نسخ التكامل الجيني لمراسل واحد هو توافر نظام المجهر الذي يسمح بالكشف عن نصوص الحمض النووي الريبي المفرد المسمى بنظام MS2 أو PP7 في الخلايا الحية4,12. هنا، يتم إجراء المجهر الحي الخلية على نظام قرص الغزل Confocal محمولة على المجهر مقلوب، ومجهزة 100 كيلوواط ليزر الحالة الصلبة إلى جانب مرشح الصوتية البصرية غير قادر على النحو المبين في مكان آخر24. وعلاوة على ذلك، لدراسة النسخ في DSB واحد باستخدام المراسلين، يجب مراقبة الخلايا الفردية بعناية لتحقيق أعلى دقة الوقت، الأمر الذي يتطلب خلايا التصوير لعدة ساعات، مما يجعل هذا المقايسة الإنتاجية منخفضة. ومع ذلك ، نلاحظ العديد من الخلايا بالتوازي مع تحديد المواقع التي تسيطر عليها مرحلة المجهر التي تحركها بيزو. لضمان الظروف البيئية المثلى لمراقبة الخلايا الحية على مدى ساعات، يتم وضع جسم المجهر، بما في ذلك مرحلة العينة، داخل غرفة بيئية زجاجية. بالإضافة إلى ذلك ، يتم تركيب غرفة حضانة مرحلة مغلقة على مرحلة المجهر وتوصيلها بوحدات التحكم في إمدادات ثاني أكسيد الكربون والرطوبة.
الخطوة الحاسمة الأولى في البروتوكول هي اختيار المناطق ذات الاهتمام مع الخلايا للتصوير. يجب أن يحتوي كل موضع XY الذي تم وضع علامة عليه للتصوير على خلية واحدة أو أكثر تظهر العدوى مع بروتينات الربط الحلقي الجذعية الحمض النووي الريبي الفلوري وفقا لمخطط الجينات والإصابة بالمراسل الموصوف في القسم 1 ، الجدول 1 ، وكذلك في الشكل 2D ، E. وعلاوة على ذلك، يجب أن تظهر الخلايا مواقع النسخ المسماة مشرق يجب أن تكون مشتركة مع بناء I-SceI-GR-iRFP713، ويجب أن يتم توطين البروتين في البداية في السيتوبلازم (الشكل 2D و E).
يجب أن تظهر الخلايا مستوى كثافة مضان من MS2 الموسومة بالفلورسنت غير المنضم و / أو بروتين معطف PP7 منخفض بما يكفي للكشف عن النصوص ذات العلامات المفردة على مستوى الفلورية الخلفية. وفي الوقت نفسه، من الضروري وجود مستوى قوي من كثافة الفلورسنت لبروتينات معطف MS2 و/أو PP7 الموسومة بفلورسنت للسماح بالتصوير على مدى 60 دقيقة على الأقل دون فقدان الكثير من الفلورسنت بسبب بعض التبييض الذي يحدث. يتم استخدام "عرض صورة المقياس" مع نطاق ثابت كما هو موضح في القسم 3.7 للسماح باختيار موحد للخلايا وفقا لمستوى كثافة الفلورسينس.
خطوة البروتوكول الحرجة الثانية هي إضافة TA إلى الخلايا على مواقع XY المحددة مسبقا من خلال ثقب صغير في غطاء طبق القاع الزجاجي. أي تلاعب في طبق أسفل الزجاج من شأنه أن يسبب تحولا من موقف XY ملحوظ من الخلايا ويجب تجنبها. لذلك ، فإن التعامل بعناية مع micropipette مع إضافة TA المخفف في وسيط النمو الخلوي أمر حيوي لمراقبة ناجحة للخلايا المختارة مسبقا ، كما هو موضح في الشكل 2F. وسيتطلب تكييف نظم مختلفة لإضافة أدوية إلى الخلايا المثبتة على مرحلة المجهر، مثل نظام التشوه، غرفة حضانة مرحلة منفصلة مع فتحات مدخل أنبوب وخروج ومضخة أو نظام حقن لإدارة المخدرات. وتؤدي طرق أخرى مثل شرائح القناة ذات الأسطح السفلية الشبيهة بالأغطية إلى الانتشار البطيء للأدوية الخاضعة للإدارة في القناة وتسبب تأخيرا إضافيا بين إضافة الأدوية وتأثيرها. وأخيرا، قد يؤدي الأنابيب غير الحذرة إلى فتح شريحة قناة إلى تغيير موضع العينة أيضا. لذلك ، فإن النظام الحالي مع ثقب حفر مخصص في غطاء طبق زجاجي القاع واضح للتكيف ، ومنخفض التكلفة ، ومناسب لإدارة وسائل الإعلام المختلفة للنمو والأدوية والمكونات. القطر الصغير للثقب والغلاف الجوي المرطب في غرفة حضانة المرحلة يمنع أيضا الجفاف من وسط الخلية.
والخطوة الحاسمة الثالثة في هذا البروتوكول هي تحليل البيانات، الذي يتطلب تفتيشا يدويا للنقاط الزمنية التي يتوقف فيها النسخ بسبب تحريض جهاز DSB. يشار إلى النقطة الزمنية لإنهاء النسخ من خلال إصدار النصوص الأخيرة من الموقع المسمى سابقا مشرق من النسخ الجيني المراسل. وبالمثل، يجب فحص أحداث بدء النسخ الناجم عن الكسر بعناية للكشف عن أحداث النسخ الفردية مع نسبة الإشارة إلى الضوضاء المنخفضة نسبيا من الرنانات المفردة المسماة بالفلورسنت.
وتضيف ديناميات إصلاح ال DSB المستحث طبقة إضافية من التعقيد إلى تحليلات البيانات المتولدة باستخدام هؤلاء المراسلين، مما يحد منها بالدقائق الأولى مباشرة بعد تحريض DSB. قد تجمع الطبيعة المعدلة وراثيا لجينات المراسل والطبيعة الغنية المتكررة للصفائف الحلقية الجذعية MS2 و PP7 مشهدا فريدا من الكروماتين ، مما يتعارض مع إنشاء برامج نسخ مستقرة مفترضة ناتجة عن الكسر. ومع ذلك ، بالمقارنة مع التأين - أو الأشعة فوق البنفسجية ، وI - SceI بوساطة التعريفي من DSB في الجينات مراسل هو نظام أكثر قوة للتحقيق في النسخ في DSBs الفردية.
يمكن الجمع بين أنظمة الإندونوكليز المختلفة مثل I-CreI أو I-PpoI أو AsiSI التي لديها أو ليس لديها مواقع اعتراف إضافية داخل الجينوم البشري مع أنظمة الجينات المراسلة الحالية لتحقيق كفاءة أعلى محتملة لتوليد DSBs. ومع ذلك ، فإنها تتطلب أولا إدخال موقع التعرف على الإندونوكليا في جينات المراسل. ثانيا، قد يكون لديهم تباين مماثل في توقيت وكفاءة التعريفي من DSB في الخلايا الفردية. من ناحية أخرى، قد يؤدي إدخال نسخ مترادفة من مواقع التعرف على الإندونوكلياز إلى زيادة كفاءة تحريض DSB. وعلاوة على ذلك، فإن اختبار أنظمة الجينات المراسل المعروضة في خطوط الخلايا المختلفة من شأنه أن يسمح بالمقارنة بين ديناميات النسخ في مواقع DSB بين الخلفيات الخلوية المختلفة وتوافر مسارات مختلفة لإصلاح تلف الحمض النووي كما هو الحال في الخلايا السرطانية والخلايا الأولية والخلايا غير الدراجاتية المتباينة. ومع ذلك ، فإن بناء الجينات مراسل لتكون متوافقة مع نظام Flp / FRT حاليا الحد من الاندماج في خطوط الخلية المضيفة Flp / FRT المتاحة.
بالإضافة إلى التطبيقات المستندة إلى المجهر ، يمكن أيضا دمج جينات المراسل الحالي مع المقايسات الكيميائية الحيوية ، مثل التحلل المناعي للكروماتين ، لدراسة توظيف عوامل إصلاح الحمض النووي أو النسخ إلى DSB واحد أو لتقييم إشغال النيوكليوسوم ، وتعديلات الهستون ، وحالة الكروماتين حول موقع DSB. وعلاوة على ذلك، فإن الجمع مع نظم المراسلات المختلفة من شأنه أن يسمح بدراسة الروابط الوظيفية بين تلف الحمض النووي وعمليات مثل تنظيم الجينوم أو تكرار الحمض النووي.
Disclosures
ولا يوجد لدى صاحبي البلاغ تضارب في المصالح يكشفان عنه.
Acknowledgements
نشكر RH Singer، J.A. Chao، T. Misteli، M. كارمو فونسيكا لهدايا من البلازميدات والكواشف. ونحن مدينون أيضا لموظفي مرفق التصوير الحيوي التابع ل iMM، أ. تيمودو، أ. ناسيمنتو، وجي رينو، بقراءة المخطوطة بشكل نقدي. تم تمويل هذا العمل من قبل PTDC/MED-OUT/32271/2017، PTDC/BIA-MOL/30438/2017 وPTDC/MED-OUT/4301/2020 من فونداساو بارا A Ciência e a Tecnologia (FCT)، البرتغال ومن LISBOA-01-0145-FEDER-007391، مشروع بتمويل مشترك من فيدر من خلال بور ليسبوا، البرتغال 2020-Programa الأوبرالية الإقليمية دي لشبونة، وFCT. كما تم تلقي التمويل من برنامج الاتحاد الأوروبي للأبحاث والابتكار (RiboMed 857119). حاصل على زمالة دكتوراه FCT 2020.05899.BD.
Materials
| Name | Company | Catalog Number | Comments |
| 100 mW solid-state Lasers | Coherent Inc., Santa Clara, CA, USA | ||
| 3i Marianas SDC Confocal Spinning Disk system | Intelligent Imaging Innovations Inc. | ||
| Air-cooled EMCCD Camera Evolve 512 | Photometrics, Tucson, AZ USA | ||
| Axio Observer Z1 inverted microscope | Carl Zeiss MicroImaging, Germany | ||
| Blasticidin | InvivoGen | ant-bl-1 | |
| charcoal-stripped fetal bovine serum | Sigma-Aldrich | F6765-500 ML | |
| CO2 module S | PeCon GmbH, Erbach, Germany | ||
| CSU-X1 confocal spinning disk unit | Yokogawa Electric, Tokyo, Japan | ||
| DMEM | Gibco | 41966029 | |
| DMEM with Hepes no PhenolRed | Gibco | 21063-029 | |
| Doxicyclin | Sigma-Aldrich | D9891 | for induction of reporter gene expression; stock solution of 0.5 mg/ml was used at 1:1000 dillution in cell growth medium |
| FBS | Gibco | 10270106 | |
| Flp-In T-REx 293 cell line | Thermo Fischer Scientific Invitrogen | R75007 | |
| I-SceI-24x MS2 stem loop sequence | GeneArt, Thermo Fischer Scientific | custom synthesized DNA fragment containing a single I-SceI recognition sequence and 24 tandem MS2 stem loop sequences | |
| Heating Device Humidity 2000 | PeCon GmbH, Erbach, Germany | ||
| Hygromycin B | Roche | 10843555001 | |
| Immersion oil Immersol 518 F | Carl Zeiss MicroImaging Inc.) | 444960-0000-000 | |
| L-glutamine | Thermo Fisher Scientific | 25030081 | |
| Lipofectamin 3000 helper reagent P3000 | Thermo Fisher Scientific | L3000001 | transfection helper reagent |
| Lipofectamine 3000 reagent | Thermo Fisher Scientific | L3000001 | lipid-based transfection reagent |
| MatTek 35 mm dish, Glass bottom No. 1.5 | MatTek Corporation, Ashland, MA, USA | P35G-1.5-10-C | |
| microscope incubation chamber | PeCon GmbH, Erbach, Germany | ||
| pcDNA5/FRT/TO | Thermo Fischer Scientific Invitrogen | V652020 | |
| pOG44 plasmid | Thermo Fischer Scientific Invitrogen | V600520 | |
| SlideBook 6.0 Software | Intelligent Imaging Innovations Inc. | ||
| stage incubation chamber PeCon P-Set 2000 | PeCon GmbH, Erbach, Germany | ||
| StaQtool Software | iMM-JLA Lisbon, Portugal | available at: https://imm.medicina.ulisboa.pt/facility/bioimaging/lib/exe/fetch.php?media=STaQTool_setup.zip | |
| triamcinolone acetonide (TA) | Sigma-Aldrich | T6501 | synthetic glucocorticoid; induces the glucocorticoid receptor to migrate from the cytoplasm to the nucleus |
| Trypsin/EDTA Solution (TE) | Thermo Fisher Scientific | R001100 |
References
- Jackson, S. P., Bartek, J. The DNA-damage response in human biology and disease. Nature. 461 (7267), 1071-1078 (2009).
- Capozzo, I., Iannelli, F., Francia, S., d'Adda di Fagagna, F. Express or repress? The transcriptional dilemma of damaged chromatin. FEBS Journal. 284 (14), 2133-2147 (2017).
- Michelini, F., et al. Damage-induced lncRNAs control the DNA damage response through interaction with DDRNAs at individual double-strand breaks. Nature Cell Biology. 19 (12), 1400-1411 (2017).
- Vítor, A. C., et al. Single-molecule imaging of transcription at damaged chromatin. Science Advances. 5 (1), (2019).
- Michalik, K. M., Böttcher, R., Förstemann, K. A. Small RNA response at DNA ends in Drosophila. Nucleic Acids Research. 40 (19), 9596-9603 (2012).
- Wei, W., et al. A role for small RNAs in DNA double-strand break repair. Cell. 149 (1), 101-112 (2012).
- Francia, S., et al. Site-specific DICER and DROSHA RNA products control the DNA-damage response. Nature. 488 (7410), 231-235 (2012).
- Vítor, A. C., Huertas, P., Legube, G., de Almeida, S. F. Studying DNA double-strand break repair: An ever-growing toolbox. Frontiers in Molecular Biosciences. 7, 24 (2020).
- Alt, F. W., et al. Synthesis of secreted and membrane-bound immunoglobulin mu heavy chains is directed by mRNAs that differ at their 3' ends. Cell. 20 (2), 293-301 (1980).
- Watakabe, A., Tanaka, K., Shimura, Y. The role of exon sequences in splice site selection. Genes & Development. 7 (3), 407-418 (1993).
- Guth, S., Martínez, C., Gaur, R. K., Valcárcel, J. Evidence for substrate-specific requirement of the splicing factor U2AF(35) and for its function after polypyrimidine tract recognition by U2AF(65). Molecular and Cellular Biology. 19 (12), 8263-8271 (1999).
- Martin, R. M., Rino, J., Carvalho, C., Kirchhausen, T., Carmo-Fonseca, M. Live-cell visualization of pre-mRNA splicing with single-molecule sensitivity. Cell Reports. 4 (6), 1144-1155 (2013).
- Peabody, D. S. The RNA binding site of bacteriophage MS2 coat protein. The EMBO Journal. 12 (2), 595-600 (1993).
- Lim, F., Peabody, D. S. RNA recognition site of PP7 coat protein. Nucleic Acids Research. 30 (19), 4138-4144 (2002).
- Chao, J. A., Patskovsky, Y., Almo, S. C., Singer, R. H. Structural basis for the coevolution of a viral RNA-protein complex. Nature Structural & Molecular Biology. 15 (1), 103-105 (2008).
- Bertrand, E., Chartrand, P., Schaefer, M., Shenoy, S. M., Singer, R. H., Long, R. M. Localization of ASH1 mRNA particles in living yeast. Molecular Cell. 2 (4), 437-445 (1998).
- Larson, D. R., Zenklusen, D., Wu, B., Chao, J. A., Singer, R. H. Real-time observation of transcription initiation and elongation on an endogenous yeast gene. Science. 332 (6028), 475-478 (2011).
- Soutoglou, E., et al. Positional stability of single double-strand breaks in mammalian cells. Nature Cell Biology. 9 (6), 675-682 (2007).
- Rouet, P., Smih, F., Jasin, M. Introduction of double-strand breaks into the genome of mouse cells by expression of a rare-cutting endonuclease. Molecular and Cellular Biology. 14 (12), 8096 (1994).
- Roukos, V., Voss, T. C., Schmidt, C. K., Lee, S., Wangsa, D., Misteli, T. Spatial Dynamics of Chromosome Translocations in Living Cells. Science. 341 (6146), 660 (2013).
- Rino, J., de Jesus, A. C., Carmo-Fonseca, M. STaQTool: Spot tracking and quantification tool for monitoring splicing of single pre-mRNA molecules in living cells. Methods. 98, 143-149 (2016).
- Hamperl, S., Bocek, M. J., Saldivar, J. C., Swigut, T., Cimprich, K. A. Transcription-replication conflict orientation modulates R-Loop levels and activates distinct DNA damage responses. Cell. 170 (4), 774-786 (2017).
- D'Alessandro, G., d'Adda di Fagagna, F. Transcription and DNA Damage: Holding Hands or Crossing Swords. Journal of Molecular Biology. 429 (21), 3215-3229 (2017).
- Boulant, S., Kural, C., Zeeh, J. C., Ubelmann, F., Kirchhausen, T. Actin dynamics counteract membrane tension during clathrin-mediated endocytosis. Nature Cell Biology. 13 (9), 1124-1131 (2011).
Reprints and Permissions
Request permission to reuse the text or figures of this JoVE article
Request PermissionExplore More Articles
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. All rights reserved