Method Article
تصنيع قوي للأنسجة من أجل زراعة طويلة الأمد لعضويات الدماغ المشتقة من iPSC لأبحاث الشيخوخة
In This Article
Summary
يوفر البروتوكول الحالي إجراء خطوة بخطوة لتوليد وصيانة وتشيخ الكائنات العضوية الدماغية المشتقة من الخلايا الجذعية متعددة القدرات التي يسببها الإنسان (iPSCs). تتيح هذه الطريقة زراعة ونضج العضويات الدماغية لفترات طويلة ، مما يسهل نمذجة العمليات التي تنطوي عليها شيخوخة الدماغ والتسبب في الأمراض المرتبطة بالعمر.
Abstract
لا تلخص النماذج الحيوانية والخلوية المتاحة حاليا بشكل كامل تعقيد التغييرات التي تحدث في الدماغ البشري المسن. إن التطور الأخير للإجراءات التي تصف توليد العضويات الدماغية البشرية ، المشتقة من الخلايا الجذعية متعددة القدرات التي يسببها الإنسان (iPSCs) ، لديه القدرة على تحويل القدرة بشكل أساسي على نمذجة وفهم شيخوخة الدماغ البشري والعمليات المسببة للأمراض ذات الصلة. هنا ، يتم تقديم بروتوكول محسن لتوليد وصيانة وتشيخ وتوصيف الكائنات العضوية الدماغية البشرية المشتقة من iPSC. يمكن تنفيذ هذا البروتوكول لتوليد عضويات الدماغ بطريقة قابلة للتكرار ويعمل كدليل خطوة بخطوة ، ويتضمن أحدث التقنيات التي تؤدي إلى تحسين النضج العضوي والشيخوخة في الثقافة. تتم معالجة القضايا المحددة المتعلقة بالنضج العضوي ، والنخر ، والتباين ، وتأثيرات الدفعات. مجتمعة ، ستسمح هذه التطورات التكنولوجية بنمذجة شيخوخة الدماغ في المواد العضوية المستمدة من مجموعة متنوعة من المتبرعين البشريين الشباب والمسنين ، وكذلك الأفراد المصابين باضطرابات الدماغ المرتبطة بالعمر ، مما يسمح بتحديد الآليات الفسيولوجية والمسببة للأمراض لشيخوخة الدماغ البشري.
Introduction
أصبحت نماذج أمراض الشيخوخة ذات أهمية متزايدة مع استمرار ارتفاع متوسط العمر المتوقع للإنسان. كشفت الدراسات الجينومية واسعة النطاق عن السكان المسنين الذين يعانون من عدم تنظيم العمليات الجزيئية والتغيرات الجينية التي تؤثر على نوعية الحياة1. تتميز عملية الشيخوخة بفقدان عام لوظائف الكائن الحي ، بما في ذلك فقدان الوظيفة الإدراكية ، وزيادة خطر الإصابة بالاضطرابات التنكسية العصبية ، ومجموعة من الأمراض المزمنة2.
لا تمثل تقنيات زراعة الخلايا الحالية بشكل مناسب الطبيعة متعددة العوامل للشيخوخة ، حيث لا يمكن تكرار هذه الاختلالات بشكل صحيح باستخدام الطفرات أو السموم أو العدوى3. غالبا ما ترتبط النماذج الحيوانية التي تستكشف عملية الشيخوخة بأوقات تجريبية طويلة وتكاليف عالية ، ولكنها تجلب أيضا اعتبارات أخلاقية معها. يمكن أن يؤدي استخدام الخلايا الجذعية المستحثة متعددة القدرات (iPSCs) من المرضى إلى توضيح الآليات الجزيئية التي تكمن وراء تطور المرض حيث تسمح iPSCs بالتطور الطبيعي للخلايا إلى أنسجة ناضجة3. أصبحت iPSCs الحصان العامل للعديد من المختبرات التي تحقق في الاضطرابات التنكسية العصبية ، حيث لا يبدو أن إعادة البرمجة الخلوية للخلايا المحصودة تمحو المرض أو بصمات الشيخوخة للمتبرعين4. تلخص هذه البصمات الأنماط الظاهرية الخلوية التي تم إثباتها في النماذج البشرية والحيوانية ، مما يجعل iPSCs مناسبة لفحص التدهور الخلوي الفردي لأنسجة المخ عالية الكثافة 5,6. أصبحت المواد العضوية المشتقة من IPSC النموذج البارز لزراعة الأنسجة ثلاثية الأبعاد ، مما يتيح تفاعلات أكثر تعقيدا من خلية إلى أخرى وتحسين التلخيص التنموي. على الرغم من استخدامها في المقام الأول للبيانات التنموية ، فقد تم تطبيق المواد العضوية بشكل متزايد نحو نمذجة الأمراض ، وتحديدا نماذج الالتهاب والتنكس العصبي والشيخوخة7. بناء على دراسات iPSC السابقة ، تحتفظ الكائنات العضوية بالأنماط الظاهرية للمرض والأنماط الظاهرية الخلوية في السياق الفسيولوجي لاتصالات الشبكة الشبيهة بالأنسجة 8,9. ومع ذلك ، فإن زراعة الأنسجة ثلاثية الأبعاد ذات الأبعاد المعينة يمكن أن يكون أمرا صعبا ، خاصة لفترات طويلة من الزمن.
يقدم هذا العمل طريقة مفصلة للتوليد القابل للتكرار من العضويات الدماغية التي تسمح للأنسجة بالنضوج بشكل كبير في الحجم لفترات أطول. ظل إنشاء الأعضاء الدماغية موحدا نسبيا ، حيث اعتمد طرقا من عدة بروتوكولات بارزة10,11. ومع ذلك ، تم اقتراح العديد من التعديلات لتحسين التمايز والصيانة. تشمل هذه الطرق البديلة استخدام العوامل العصبية لتعزيز التمايز العصبي12 ، وسقالات إضافية لتحسين تبادل المغذيات لتعزيز طول العمر الخلوي 13 ، وإثارة الإجهاد المنخفض للثقافة والنمو لفترات طويلة14. تم دمج هذه التحسينات في هذه الطريقة لتطوير عضويات ناضجة قادرة على التعبير عن الأنماط الظاهرية التنكسية العصبية والشيخوخة.
Protocol
تمت الموافقة على دراسات المرضى من قبل مجلس المراجعة المؤسسية. وقع جميع المشاركين على موافقة خطية مستنيرة وموافقة مستودع للسماح بإعادة استخدام بياناتهم وعيناتهم الحيوية. تم إنشاء خطوط iPSC وفقا لإرشادات IRB والمؤسسية. يوضح الشكل 1 نظرة عامة تخطيطية لسير عمل هذا البروتوكول.
1. إعادة برمجة وصيانة iPSC
- اجمع 8 مل من دم الشخص (المسن أو المريض المرضي ؛ الذين تتراوح أعمارهم بين 65 وما فوق) في أنابيب تحضير الخلايا (CPT) مع سترات الصوديوم أو في EDTA أو أنابيب الهيبارين.
- جهاز طرد مركزي عند 1800 × جم لمدة 30 دقيقة في درجة حرارة الغرفة (RT) لجمع الحبيبات التي تحتوي على الدم المحيطي فقط ولا تحتوي على مصل15.
- استخدم متجهات إعادة البرمجة المتخصصة وفقا لبروتوكول الشركة المصنعة (انظر جدول المواد) للحصول على iPSCs16.
- استزراع iPSCs في خالية من التغذية ، خالية من فيروس رفع نازعة هيدروجين اللاكتوز (LDEV) مصفوفة غشاء القاعدية ذات عامل نمو مخفض مغلفة بألواح استزراع 6 آبار في وسائط أساسية 8 (E8) (انظر جدول المواد) عند 37 درجة مئوية في جو مرطب مع 5٪ CO2.
- حافظ على iPSCs في وسائط E8 لمدة 3-4 أيام لتجنب الاكتظاظ أو التمايز التلقائي.
- التحقق من تعدد قدرات خطوط iPSC باستخدام علامات الفلورسنت المناعي (الخطوة 2) واختبار الميكوبلازما (الخطوة 3).
2. تلطيخ تعدد القدرات
- للحفاظ على المحاليل والأجسام المضادة ، قم بزرع الخلايا على ألواح استزراع 24 بئرا مغلفة (الخطوة 1.4) قبل 3-4 أيام من التحليل. نضح الوسط باستخدام ماصة وإصلاح الخلايا بنسبة 4٪ فورمالديهايد في محلول ملحي مخزن بالفوسفات (1x PBS) لمدة 15-20 دقيقة في RT.
- اغسل الخلايا 3x باستخدام 1x PBS وتخلل مع 0.1٪ Triton-X 100 في 1٪ ألبومين مصل البقر (BSA) في PBS لمدة 15 دقيقة على الأقل ، ولكن ليس أكثر من 1 ساعة في RT.
- اغسل 3x باستخدام 1x PBS وكتلة مع 5٪ BSA في PBS لمدة 30 دقيقة في RT.
- اغسل مرة أخرى 3x باستخدام 1x PBS وأضف الأجسام المضادة Sox2 و Oct3/4 (تخفيف 1: 100 ؛ انظر جدول المواد) ، والبقع النووية DAPI في 1٪ BSA (1: 4000 تخفيف) بين عشية وضحاها عند 4 درجات مئوية. لف بورق الألمنيوم للحماية من الضوء.
- اغسل 3x باستخدام 1x PBS واترك الخلايا في PBS. صورة بمجهر مضان بتكبير 10-20x. تأكد من أن علامات تعدد القدرات Sox2 و Oct3 / 4 موضعية في نوى الخلايا17,18.
3. اختبار الميكوبلازما
ملاحظة: راجع بروتوكول مجموعة الكشف (انظر جدول المواد) للحصول على خطوات مفصلة لتنفيذ الفحص وتحليله. توفر مجموعة الكشف الكاشف والركيزة والمخزن المؤقت للفحص لاختبار الميكوبلازما.
- قبل تمرير الخلايا أو الوسط المنعش ، اجمع 2-3 مل من وسط زراعة الخلايا في أنبوب طرد مركزي وقم بتجميع أي خلايا أو حطام عند 200 × جم لمدة 5 دقائق في RT. قم بتخزين المادة الطافية في درجة حرارة 4 درجات مئوية لمدة ≤5 أيام. احتضان الخلايا بالوسط لمدة 24 ساعة على الأقل لضمان إشارة قابلة للكشف.
- أضف 100 ميكرولتر من طافية الخلية إلى أنبوب جديد أو بئر من صفيحة ذات 96 بئرا ذات جدران بيضاء (يوصى بقاع معتم ، انظر جدول المواد). أعد تكوين الكاشف والركيزة في مخزن الفحص المؤقت وازن لمدة 15 دقيقة في RT.
- أضف 100 ميكرولتر من الكاشف إلى العينة واحتضانها لمدة 5 دقائق في RT. قم بقياس التلألؤ باستخدام مقياس اللمعان (القياس #1).
- أضف 100 ميكرولتر من الركيزة إلى العينة واحتضانها لمدة 10 دقائق في RT. قياس التلألؤ (القياس #2).
- تحديد تلوث الميكوبلازما بنسبة القياس # 2 إلى # 1. راجع دليل المجموعة لتفسير النتائج.
4. إعداد الشعيرات الدقيقة
- ابدأ في تحضير خيوط دقيقة بولي (حمض اللاكتيك المشترك الجليكوليك) (PLGA ، انظر جدول المواد) عن طريق تآكل حبلا الخيط بنهاية حادة لمشرط. تعقيم الألياف المهترئة برفق مع 70٪ من الإيثانول.
- تحت المجهر وباستخدام المسطرة ، ابدأ في قطع ألياف PLGA إلى أجزاء من خيوط بطول 500 ميكرومتر إلى 1 مم. قطع حوالي 25 ملم من الألياف في المجموع. احتفظ بالخيوط في أنبوب سعة 15 مل بمحلول مضاد حيوي ومضاد حيوي سعة 1 مل.
- في الغطاء ، قم بتخفيف محلول الألياف ب 10 مل من DMEM / F-12 (الجدول 1). دوامة جيدا لخلط الحل.
ملاحظة: العمل في غطاء تدفق زراعة الخلايا في بيئة معقمة.
- في الغطاء ، قم بتخفيف محلول الألياف ب 10 مل من DMEM / F-12 (الجدول 1). دوامة جيدا لخلط الحل.
- أضف 20 ميكرولتر من محلول الألياف إلى ثلاثة أجسام جنينية (EB) تشكل آبارا من صفيحة 96 بئرا. تحت المجهر برايتفيلد ، عد ومتوسط الألياف لكل بئر. تمييع أو التركيز إلى متوسط 5-10 خيوط دقيقة PLGA لكل بئر. تحضير كل بئر بهذه الطريقة.
- الآبار جاهزة الآن للبذر بالخلايا. قم بتخزين اللوحة في درجة حرارة الغرفة لحين الحاجة أو في درجة حرارة 4 درجات مئوية لليوم التالي.
5. تشكيل الجسم الجنيني (EB)
ملاحظة: يجب تسخين جميع الوسائط والحلول إلى RT.
- بمجرد أن تصل iPSCs إلى التقاء 70٪ -80٪ (الشكل 2A) ، فإنها تكون جاهزة للمرور واستخدامها لتشكيل EB. تحقق من الخلايا باستخدام المجهر عند التكبير 10x-20x. تأكد من أن المستعمرات تعرض الحد الأدنى (<10٪) من مناطق التمايز التلقائي.
- نضح الوسط باستخدام ماصة وغسل الخلايا مرة واحدة باستخدام DPBS. فصل المستعمرات عن طريق إضافة 500 ميكرولتر من محلول انفصال الخلايا (انظر جدول المواد) أو 0.5 مللي متر من حمض الإيثيلين ديامينيترايتيك (EDTA) واحتضانها لمدة 3-5 دقائق عند 37 درجة مئوية.
ملاحظة: العمل في غطاء تدفق زراعة الخلايا في بيئة معقمة. - اجمع الخلايا التي تم إطلاقها عن طريق إضافة 1 مل من وسائط E8 الطازجة إلى كل بئر وماصة برفق حتى يتم فصل جميع الخلايا.
- انقل 1.5 مل من معلق الخلية إلى أنبوب سعة 15 مل ، وأضف 1 مل آخر من وسائط E8 الجديدة للوصول إلى حجم إجمالي قدره 2.5 مل.
- أجهزة الطرد المركزي في 290 × ز لمدة 3 دقائق في RT.
- نضح المادة الطافية باستخدام ماصة ، وأعد تعليق حبيبات الخلية في 1 مل من الوسائط الأساسية 6 (E6 ، انظر جدول المواد) المكملة بمثبط 50 ميكرومتر ROCK ، وعد الخلايا باستخدام مقياس الدم19.
- تحضير معلق خلية من 60000-90000 خلية / مل ، اعتمادا على كثافة البذر المطلوبة ، في وسط E6 المكمل ب 50 ميكرومتر من مثبط ROCK (انظر جدول المواد).
- أضف 150 ميكرولتر من معلق الخلية في كل بئر من صفيحة ULA ذات 96 بئرا (أو صفيحة مقعرة معدة20). البذور 9000-11000 خلية لكل بئر.
- أجهزة الطرد المركزي لوحة لتجميع الخلايا بالقوة عند 290 × جم لمدة 1 دقيقة في RT. ضع اللوحة في الحاضنة عند 37 درجة مئوية في جو مرطب مع 5٪ CO2.
6. الحث العصبي الظهاري
- بعد 24 ساعة ، استنشق بعناية 120 ميكرولتر من الوسائط باستخدام ماصة. تأكد من عدم استنشاق EB عن طريق خفض طرف الماصة بعيدا جدا في البئر.
- أضف 150 ميكرولتر من وسائط E6 (في RT) مكملة ب 2 ميكرومتر من XAV939 ومثبطات SMAD: 10 ميكرومتر من SB431542 و 500 نانومتر من 193189 LDN لكل بئر (انظر جدول المواد).
- قم بتغيير الوسط يوميا باستخدام وسائط E6 المحضرة حديثا مع 2 ميكرومتر من XAV939 و 10 ميكرومتر من SB431542 و 500 نانومتر من LDN 193189.
ملاحظة: بحلول اليوم السادس (DIV6) ، يجب أن يكون قطر EBs 550-600 μm وأن تكون جاهزة لمزيد من التمايز.
7. التمايز العضوي والنضج
ملاحظة: يجب تسخين جميع الوسائط إلى RT.
- عند DIV7 تقريبا ، تحقق مما إذا كانت جميع EBs قد وصلت إلى قطر 550-600 ميكرومتر وعرض حافة ناعمة وواضحة (الشكل 2B) ؛ في هذه المرحلة ، تكون جاهزة للتضمين في مصفوفة خارج الخلية (ECM).
ملاحظة: العمل في بيئة معقمة. - قم بإعداد صفائح التضمين المدملة من فيلم الختم بالحرارة (انظر جدول المواد) عن طريق وضع ورقة فيلم (طولها حوالي 4 بوصات) على صندوق P200 فارغ. باستخدام أنبوب مخروطي سعة 15 مل أو أنبوب طرد مركزي دقيق سعة 500 ميكرولتر ، اضغط برفق على ورقة الفيلم في الثقوب لعمل 12 غمازة. رش ورقة الفيلم بإيثانول 70٪ واتركها تجف داخل غطاء التدفق مع تشغيل ضوء الأشعة فوق البنفسجية لمدة 30 دقيقة على الأقل.
- قم بإذابة كمية كافية من مصفوفة الغشاء القاعدي (Matrigel ، انظر جدول المواد) على الثلج وضعه داخل غطاء التدفق.
ملاحظة: لكل EB ، هناك حاجة إلى حوالي 30 ميكرولتر من مصفوفة الغشاء غير المخفف. احتفظ دائما بمصفوفة الغشاء أقل من 4 درجات مئوية لمنعها من التبلور. يوصى أيضا بأطراف الماصة المبردة مسبقا لأنها تبطئ المصفوفة من البلمرة في الطرف أثناء السحب ، وبالتالي تقليل فقد المواد. - باستخدام طرف P200 عريض التجويف ، انقل EB واحدا إلى كل غمازة ، وقم بإزالة أكبر قدر ممكن من الوسائط باستخدام طرف ماصة عادي. ضع في اعتبارك عدم ترك EBs يجف. باستخدام طرف P200 عادي ، أضف ~ 30 ميكرولتر من مصفوفة الغشاء غير المخففة إلى كل عنصر عضوي ، مما يضمن أن EB في مركز القطرة.
- بمجرد تضمين جميع EBs في المصفوفة ، ضع ورقة الفيلم التي تحتوي على EBs في طبق بتري معقم.
ملاحظة: اختياريا ، يمكن وضع طبق بتري صغير مملوء بالماء المعقم في طبق بتري الأكبر بجوار ورقة الفيلم لمنع التبخر.- انقل الطبق إلى حاضنة واحتضانه عند 37 درجة مئوية في جو مرطب مع 5٪ CO2 لمدة 10 دقائق تقريبا للسماح لمصفوفة الغشاء بالتصلب.
- لكل مجموعة من 12 عضويا مدمجا ، قم بإعداد 5 مل من وسائط التمايز مع B27 بدون فيتامين أ (الجدول 1) في بئر واحد من لوحة ULA ذات 6 آبار. قم بتسخين اللوحة مسبقا إلى 37 درجة مئوية في حاضنة.
- بمجرد الانتهاء من وقت الحضانة ، انقل EBs المضمنة إلى لوحة ULA ذات 6 آبار عن طريق أخذ ورقة الفيلم ودفع الدمامل من الجزء الخلفي من الورقة. إذا لزم الأمر ، خذ 1 مل من البئر وماصة على الورقة لمساعدة القطرات على الانفصال عن الفيلم.
ملاحظة: يمكن رؤية التغييرات المورفولوجية الهامة 1 يوم بعد التضمين. تنتقل EBs من وجود حواف ناعمة إلى نتوءات منتفخة تشكل براعم (الشكل 2C). - بعد يومين (DIV9) ، قم بإجراء تغيير نصف الوسائط. احرص على عدم استنشاق أو إتلاف قطرات مصفوفة الغشاء في هذه العملية.
- بعد يومين آخرين (DIV11) ، قم بإجراء تغيير كامل للوسائط ، مع استكمال الوسائط ب 3 ميكرومتر من CHIR99021 (انظر جدول المواد).
- في DIV14 ، قم بتغيير الوسائط إلى وسائط التمايز مع B27 مع فيتامين A (الجدول 1) لزيادة تدريجية في حجم العضوي.
- في DIV16 ، ضع لوحة البئر على شاكر مداري عند 90 دورة في الدقيقة داخل حاضنة. تغيير وسائل الإعلام كل 2 أيام.
- كل 40 DIV ، قم بتخفيف 500 ميكرولتر من مصفوفة الغشاء لكل 50 مل من الوسائط للحصول على مغذيات إضافية في الوسائط.
النتائج
يؤدي دمج ألياف PLGA وتضمين الدمل والإثارة إلى جيل قوي من الكائنات العضوية الدماغية التي تمكن من الحفاظ على الثقافات المشتقة من iPSC لفترات طويلة من الزمن (الشكل 1).
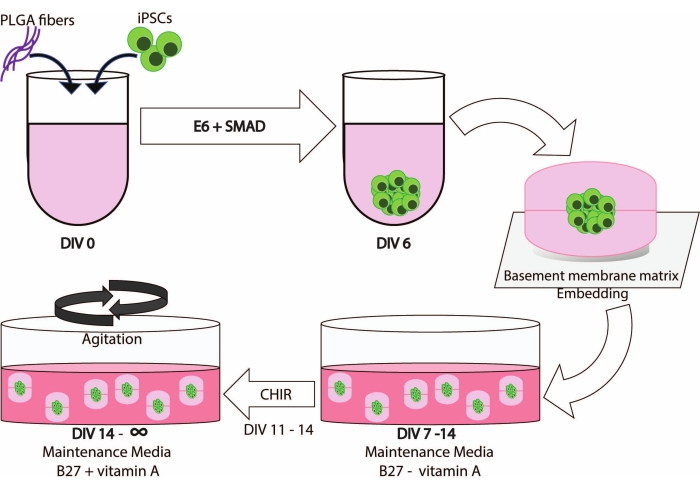
الشكل 1: رسم تخطيطي لسير العمل والجدول الزمني لهذه الطريقة. يرجى النقر هنا لعرض نسخة أكبر من هذا الشكل.
فترة الحث العصبي الأولية قابلة للمقارنة مع الإجراءات المنشورة مسبقا11. تبدأ الأجسام الجنينية (EB) كمجاميع دائرية (الشكل 2B) بحواف بيضاء أو شفافة. مع تغير EB من وسائط الحث العصبي إلى وسائط الصيانة العصبية في DIV7 ، تظهر النتوءات والتبرعم في غضون 24 ساعة من الأنسجة الدائرية (الشكل 2C). علاوة على ذلك ، مع استمرار نمو العضو العضوي ، تساعد مساحة سطح ألياف PLGA العضو العضوي على الاستطالة (الشكل 2 د). أثناء النضج ، يجب أن تظل حواف العضو سليمة ، لأنها علامة جيدة على الخلايا السليمة والتطور ؛ خلاف ذلك ، يجب توفير مغذيات إضافية13 (الشكل 2E). يتم تسهيل نمو المواد العضوية بشكل أكبر من خلال إثارة الثقافة العضوية ، لأن هذا يحسن التروية بالمواد المغذية.
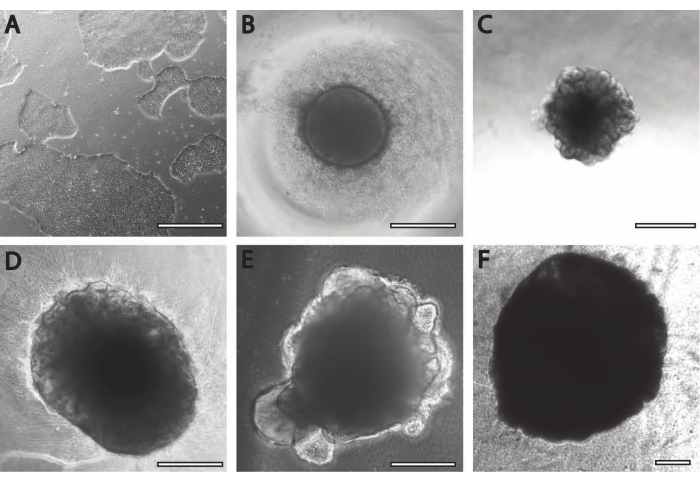
الشكل 2: تمايز ونضج العضويات الدماغية . (أ) صورة تمثيلية لثقافة iPSC عند التقاء 70٪ -80٪. (ب) تم إنشاء الأجسام الجنينية (EBs) وتم تحفيز التكوين العصبي الظهاري حتى DIV7. ثم تم تضمين EBs في مصفوفة الغشاء وتمييزها بشكل أكبر نحو الكائنات العضوية الدماغية. (ج) عضويات في DIV10 تعرض تكوينات ناشئة متميزة. يمكن أن تنضج الكائنات العضوية بشكل أكبر في مصفوفة الغشاء باستخدام إما (D) الدمل أو (E) تضمين شطيرة ، كما هو موضح هنا في DIV30. (F) تظهر الثقافة طويلة الأجل نمو عضويات دماغية إلى أحجام كبيرة (DIV70). شريط المقياس = 500 ميكرومتر. يرجى النقر هنا لعرض نسخة أكبر من هذا الرقم.
وتستكمل الأبعاد والتشكل الخارجي للعضوي ببنية معقدة داخل العضو العضوي. بعد تثبيت الأنسجة في DIV7 بعد المرحلة الأولى من التمايز ، تعبر خلايا EB عن SOX2 ، وهو عامل نسخ صندوق HMG يعمل كعلامة للخلايا الجذعية العصبية متعددة القدرات21 ، بالإضافة إلى صندوق البروتين المقترن Pax-6 ، مما يشير إلى الخلايا السلفية العصبية (الشكل 3). يمكن بالفعل رؤية الخلايا العصبية غير الناضجة التي تتميز ب TuJ1 (الفئة الثالثة β-tubulin)22 منتشرة في جميع أنحاء الأنسجة.
في هذه المرحلة ، يصبح مثال على التنظيم الذاتي الذي تمر به هذه الكائنات العضوية واضحا. يشبه تنظيم الهياكل الشعاعية ، التي تسمى الوريدات ، الأنبوب العصبي ، مع خلايا SOX2 + في مركز الوردة21 و PAX6 باتجاه محيط الوردة. هذه الوريدات تؤدي إلى الخلايا العصبية أثناء هجرتها. هذه الخلايا المشعة هي في البداية إيجابية مزدوجة لعلامة الخلايا الجذعية / السلفية العصبية Nestin23 والبروتين الحمضي الليفي الدبقي (GFAP) ، على غرار الدبقية الشعاعية الموجودة في المناطق العصبية في الدماغ في الجسم الحي . عندما تنضج هذه الخلايا العصبية المهاجرة ، تعكس علامات الهيكل الخلوي هذا التغيير22. تظهر علامة التمايز العصبي في المرحلة المبكرة TuJ122 في الدائرة الداخلية للوردة وتتحول إلى البروتين 2 المرتبط بالأنابيب الدقيقة 2 (MAP2) 24 ، وهي علامة نضج خاصة بالخلايا العصبية في المحيط.
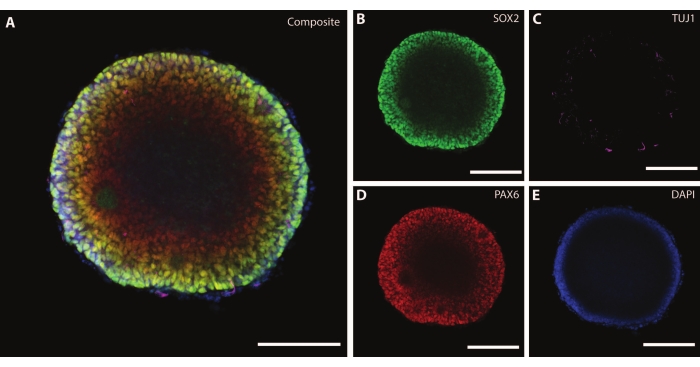
الشكل 3: تظهر الأجسام الجنينية في DIV7 تنظيما هيكليا وتوصيف غير ناضج. صورة كاملة للكيمياء المناعية ل EB في DIV7. (أ) صورة مركبة ل EB تعرض (B) وريدات عصبية SOX2 + ، (C) خلايا عصبية غير ناضجة (TUJ1) منتشرة في جميع أنحاء EB ، (D) خلايا السلف العصبي (PAX6) ، و (E) نوى تصورها DAPI. شريط المقياس = 100 ميكرومتر. يرجى النقر هنا لعرض نسخة أكبر من هذا الشكل.
مع تقدم الكائنات العضوية في العمر ، يبدأ تنظيم وعلامات الخلايا العصبية النامية في تكرار الظروف الفسيولوجية. في DIV30 ، يمكن ملاحظة العديد من الوريدات التي تؤدي إلى ظهور مناطق عصبية مكافئة للدماغ النامي25. بواسطة DIV60 ، هذه المناطق العصبية SOX2 + غير موجودة ويتم استبدالها ب MAP2 و NeuN26 الناضجين ، وعلامة تمايز الخلايا العصبية ، والخلايا العصبية الإيجابية (الشكل 4 والشكل 5).
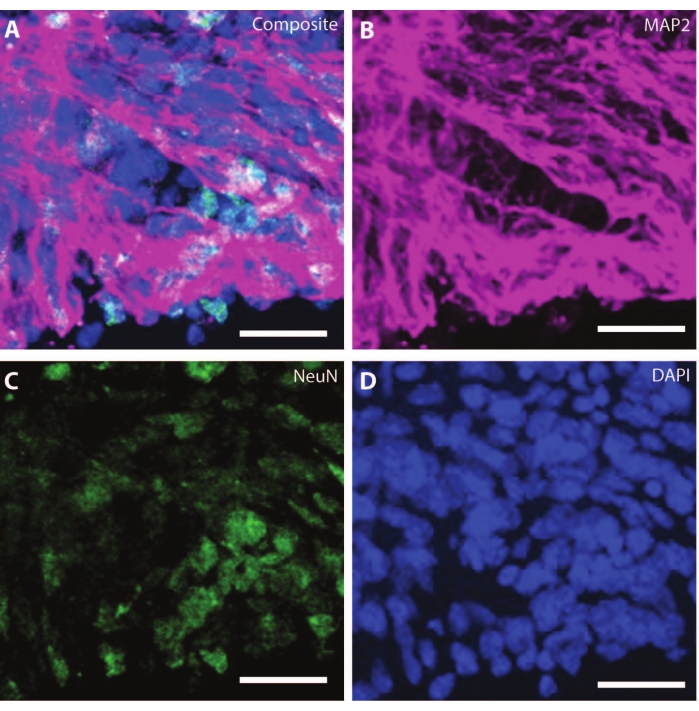
الشكل 4: تظهر الكائنات العضوية في DIV120 توصيفا عصبيا ناضجا. صورة الكيمياء الهيستولوجية المناعية لقسم عضوي في DIV 120. (أ) صورة مركبة للمقطع توضح علامات عصبية ناضجة للعدد (ب) MAP2 (أرجواني) و(ج) نيوون (أخضر). (د) تصور النوى بواسطة DAPI. شريط المقياس = 20 ميكرومتر. يرجى النقر هنا لعرض نسخة أكبر من هذا الشكل.
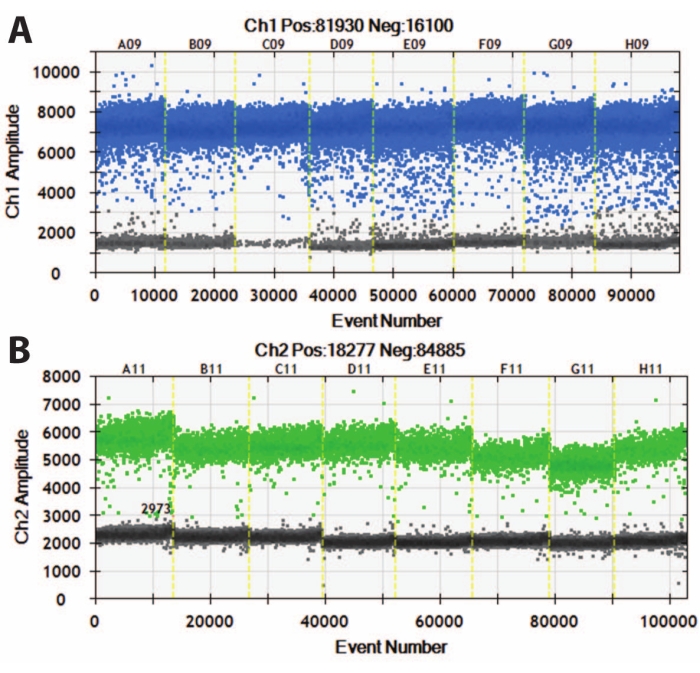
الشكل 5: تفاعل البوليميراز المتسلسل الرقمي للقطرات العضوية DIV120. الرسوم البيانية الرقمية لتفاعل البوليميراز المتسلسل بالقطرات التي توضح قيمة التعبير المطلق ل (A) MAP2 (أعلى ، أزرق) و (B) NeuN (أسفل ، أخضر). تفصل الخطوط الصفراء المائلة بين خطوط iPSC المختلفة (A ، B ، C ، إلخ) ، وقد تم تجميع المواد العضوية معا. ن = 5. يرجى النقر هنا لعرض نسخة أكبر من هذا الرقم.
يمكن استخدام هذه الواسمات الهيكلية الخلوية جنبا إلى جنب مع علامات ما بعد الانقسام (مثل doublecortin27 و synapsin28) للتحقيق في اللدونة المشبكية وغيرها من الانخفاضات المرتبطة بالعمر (الشكل 6) ، بالإضافة إلى أنسجة المخ الإضافية مثل الخلايا النجمية والدبقية (الشكل 7).
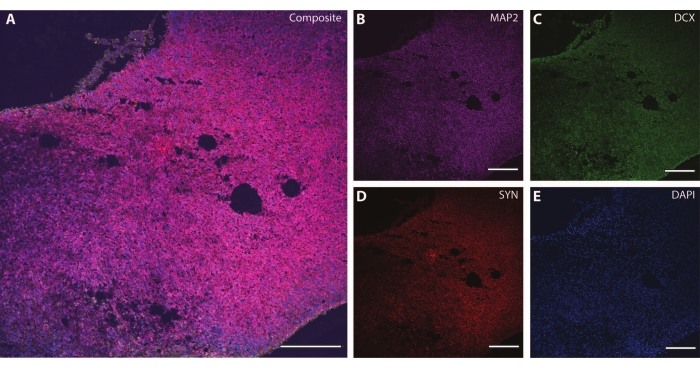
الشكل 6: مثال على التحليل التشابكي الطرفي. صورة الكيمياء الهيستولوجية المناعية لقسم من العضو العضوي في DIV 120. (أ) صورة مركبة للمقطع ملطخة ب (ب) MAP2 و (ج) دبل كورتين (DCX) و (د) المشبك الأول (SYN). (ه) تصورت النوى بواسطة DAPI. شريط المقياس = 200 ميكرومتر. يرجى النقر هنا لعرض نسخة أكبر من هذا الشكل.
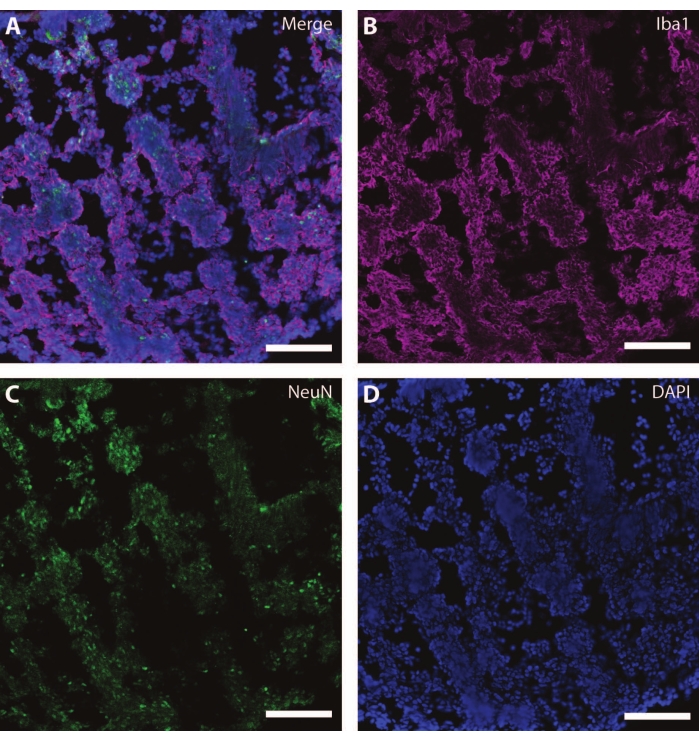
الشكل 7: دليل على تطور الخلايا الدبقية. صورة الكيمياء الهيستولوجية المناعية لقسم من العضو العضوي في DIV 120. أ: صورة مركبة للمقطع الملون للجزيء 1 (Iba1) و(ج) NeuN: (ب) (د) تصور النوى بواسطة DAPI. شريط المقياس = 100 ميكرومتر. يرجى النقر هنا لعرض نسخة أكبر من هذا الشكل.
| الكاشف | التركيز النهائي | الحجم (إجمالي 50 مل) |
| DMEM-F12 | 50% | 25 مل |
| الوسط العصبي القاعدي | 50% | 25 مل |
| ملحق N2 (100x) | 1x | 0.25 مل |
| مكمل B27 - / + فيتامين أ (50x) | 0.5 مرة | 0.5 مل |
| إنسولين | 0.25% | 12.5 ميكرولتر |
| جلوتا ماكس (100x) | 1x | 0.5 مل |
| MEM-NEAA (100x) | 0.5 مرة | 0.25 مل |
| هيبس (1 م) | 10 مللي متر | 0.5 مل |
| مضاد حيوي / مضاد حيوي (100x) | 1x | 0.5 مل |
| 2-β-ميركابتوإيثانول | 50 ميكرومتر | 17.5 ميكرولتر |
| * ملاحظة: بعض DMEM-F12 يحتوي بالفعل على GlutaMAX ، لا حاجة لإضافة إضافية. | ||
الجدول 1: تركيب وسائط التمايز المستخدمة في هذه الدراسة.
Discussion
يعد التكوين الموحد ل EBs خطوة حاسمة في التحويل القابل للتكرار للخلايا الجذعية متعددة القدرات إلى عضويات دماغية. يمكن أن يختلف تجميع قوة الخلايا الجذعية إلى أنسجة مفردة اعتمادا على هندسة الآبار المقعرة وكثافة البذر ومعالجة البئر. على الرغم من أن الطريقة الحالية تشير إلى نطاق قطر يتراوح بين 500 و 600 ميكرومتر بعد 6 أيام ، إلا أن هذه الأقطار لا تستبعد الأقطار الأخرى للتكوين العضوي السليم ، حيث أثبتت العديد من الأقطار الأخرى نجاحها. ومع ذلك ، فقد ثبت أن الأقطار المتفاوتة تؤثر على معدلات التمايز والنجاح29. لأغراض التكاثر ، يوصى بشدة بتغيرات القطر التي تقل عن 50 ميكرومتر20. بالإضافة إلى ذلك ، يمكن تمديد عدد أيام الحث العصبي من 6 إلى 10 أيام للسماح لقطر EBs بالنمو ، حيث ثبت أن استخدام مثبطات SMAD ينتج بكفاءة ويحافظ على تكوين الظهارة العصبية بعد 5 أيام فقط من التعرض30. في غياب مثبطات SMAD ، يمكن أن يؤدي الحث العصبي إلى نتائج غير متسقة ، مما يتطلب فترات تحريض أطول. مثبطات SMAD المذكورة في هذا العمل هي الأكثر فعالية ، ولكن يمكن استخدام جزيئات صغيرة أخرى من dorsomorphin و TGF β بتركيزها الفعال.
توفر مصفوفة الغشاء القاعدي ركيزة ممتازة للنمو ويمكن إدارتها بشكل مختلف. تضمنت الاستخدامات المبكرة للمصفوفة الغشاء القاعدي كطلاء جيد31. ومع ذلك ، أظهر استخدام المصفوفة لتضمين الأنسجة لتحسين التمايز والنضج في هذه الأنسجة32. بالنسبة للعضويات ، فقد ثبت أن استخدام المصفوفة يحسن تمايز EB إلى عضويات ، ويعزز النضج ، ويطيل فترات الاستزراع33. في حين أنه لا يزال من الممكن تشكيل المواد العضوية بدون المصفوفة ، حيث سعت العديد من المجموعات إلى تحقيق زراعة أنسجة خالية من المصفوفة 34,35 ، فقد وجدت الدراسات أن الكائنات العضوية المضمنة فيالمصفوفة لديها فرصة أكبر لأوقات استزراع طويلة وتتطلب صيانة أقل 36. توفر طريقة الدمل للتضمين تغطية متساوية للسطح العضوي ، مما يضمن انتشارا مشابها ، والوصول إلى العناصر الغذائية ، والتمايز القابل للتكرار. بدلا من ذلك ، يمكن استخدام تضمين القبة لتغليف المواد العضوية بالكامل37.
يعد نقل EBs إلى غمازات مصفوفة الغشاء خطوة حاسمة. على الرغم من أن طرف ماصة سعة 1 مل له فتحة واسعة بما يكفي لنقل EBs ، إلا أنه يفضل استخدام طرف 200 ميكرولتر لسهولة النقل. يجب قطع أطراف 200 ميكرولتر لإنشاء فتحة كبيرة بما يكفي ، مما يضمن حافة ناعمة لتقليل إجهاد القص عند الماصة. بدلا من ذلك ، توجد أطراف عريضة التجويف 200 ميكرولتر لسهولة النقل. يجب أن يتم السحب ببطء ، لأن السحب السريع قد يعطل محيط العضو ويعيق النمو السليم. يجب إيلاء اهتمام خاص لضمان نقل وسيط كاف لتوفير العناصر الغذائية. القليل جدا من الوسط يتعرض لخطر جفاف العضو العضوي ، مما يسبب النخر. يمكن أن يؤدي نقل EB مع الكثير من وسائط الثقافة إلى تخفيف المصفوفة بشكل كبير والفشل في تغليف العضو العضوي بشكل آمن. من الناحية المثالية ، يجب عدم تخفيف المصفوفة بأكثر من 50٪ لضمان بلمرتها وعملها كوحدة تحكم في المحتوى المؤسسي ل EBs. إذا لم ينجح التضمين ، فيمكن استرداد EB وإعادة تغليفه. يمكن إجراء إعادة التغليف في المصفوفة الجديدة في أي وقت لتزويد العضو العضوي بدعم إضافي.
على غرار تضمين المصفوفة للسقالات ، توفر ألياف PLGA دعما إضافيا للنمو ثلاثي الأبعاد. تم دمجها في الأصل لإنتاج عضويات ممدودة وزيادة مساحة السطح38 ، وقد تم تحديد دمج ألياف PLGA تدريجيا كأداة إضافية لتحسين التمايز العضوي والنضج39. نظرا لأن المزيد من المختبرات تتطلع إلى تقليل استخدام المصفوفة أو إلغائها تماما ، فإن خصائص التنظيم الذاتي للعضويات المدعومة بالألياف المدمجة توفر سقالات كافية لإنشاء الأنسجة ثلاثية الأبعاد والتمايز39. هنا ، تم الجمع بين كلتا الطريقتين لزيادة فرص الثقافة طويلة الأجل38,39. يعد دمج الألياف أثناء التجميع الأولي أمرا بالغ الأهمية ، حيث قد لا يتم إدخالها في مرحلة لاحقة. بعد الطرد المركزي ، فإن التحقق من وجود اثنين من الألياف بين الخلايا المجمعة سيضمن دمج الألياف في EB. إذا لم ينجح ، فإن الطموح اللطيف للبئر وإعادة الطرد المركزي يجب أن يضمن الخلط.
خطوة أخرى حاسمة في صيانة المواد العضوية هي إدخال شاكر مداري لتحسين تروية الوسائط. في التكرارات المبكرة لبروتوكولات الأعضاء ، تم استخدام مفاعل حيوي دوار لإنشاء التحريض11. يوفر الهزاز المداري عند 90 دورة في الدقيقة تحريضا كافيا دون تدمير قطرة المصفوفة أو إتلاف مورفولوجيا العضوي. تمتنع بعض المجموعات عن استخدام سقالة المصفوفة ولكنها تحتفظ بإثارة شاكر لتوفير بيئة مناسبة34. كما هو الحال مع جميع البروتوكولات ، يجب ضبط سرعة الدوران اعتمادا على شاكر لتقليل مقدار إجهاد القص. إذا تم اختيار تضمين قبة ، فيمكن استخدام شاكر مائل لتقليل مقدار إجهاد القص11,34.
مجتمعة ، يوفر تكامل العديد من التقنيات المختارة طريقة قوية لتشكيل عضوي مشتق من iPSC. هناك عدة طرق لإنشاء المواد العضوية والحفاظ عليها ، لكن العديد منها يركز على مسارات التمايز المبكرة. في هذا العمل ، تم الجمع بين العديد من التقنيات المختلفة لزرع المواد العضوية لفترات طويلة من الزمن ، بعد مرحلة التمايز ، وفي فترة النضج حيث يمكن أن تبدأ الأنماط الظاهرية للشيخوخة في التطور. يسمح دمج هذه التقنيات بالنضج المطول دون الحاجة إلى عوامل بيولوجية خارجية للحفاظ على الثقافات ، مع الاحتفاظ بالتنظيم الذاتي والتقدم الطبيعي للشيخوخة.
Disclosures
ليس لدى المؤلفين ما يكشفون عنه.
Acknowledgements
تم دعم هذا العمل من قبل مبادرة هولندا للأعضاء على الرقاقة ، وهو مشروع NWO Gravitation (024.003.001) بتمويل من وزارة التعليم والثقافة والعلوم في حكومة هولندا. ولحسن الحظ، تعترف DCB بالدعم المالي المقدم من المجلس الوطني للعلوم والتكنولوجيا (CONACyT) في شكل منحة دراسية للدكتوراه.
Materials
| Name | Company | Catalog Number | Comments |
| 2-β-Mercaptoethanol | Thermo Fisher Scientific | 31350010 | |
| 4′,6-Diamidino-2-phenylindoledihydrochloride (DAPI) | Invitrogen | D1306 | 1:4000 |
| 6-well Clear Flat Bottom CELLSTAR Cell Culture Multiwell Plate | Greiner Bio-One | 657185 | |
| 6-well Clear Flat Bottom Ultra-Low Attachment Well Plate | Corning | 3471 | |
| 96-well Clear Round Bottom Ultra-Low Attachment Microplate | Corning | 7007 | |
| 96-Well, Nunclon Delta-Treated, Flat-Bottom Microplate | Thermo Fisher Scientific | 136101 | |
| Accutase | Sigma-Aldrich | 46964 | cell detachment solution |
| Antibiotic-Antimycotic (100x) | Gibco | 15240062 | |
| B27 Suppement (with Vitamin A) (50x) | Gibco | 17504044 | |
| B27 Supplement (minus Vitamin A) (50x) | Gibco | 12587010 | |
| BD Vacutainer™ Glass Mononuclear Cell Preparation (CPT) Tubes | Thermo Fisher Scientific | 02-685-125 | |
| Bovine Serum Albumin | Sigma-Aldrich | A9418 | |
| Centrifuge | Eppendorf | 5810 R | With plate holders |
| CHIR99021 | Selleck Chemicals | S2924 | |
| CytoTune Sendai Reprogramming Vector | Thermo Fisher Scientific | A1378001 | |
| ddPCR primers | human | MAPT | Bio-Rad | dHsaCPE192234 | |
| ddPCR primers | human | RBFOX3 (NeuN) | Bio-Rad | dHsaCPE5052108 | |
| DMEM/F12 | Thermo Fisher Scientific | 11320074 | |
| Doublecortin (DCX) | Santa Cruz Biotechnology | SC-8066 | 1:500 |
| Dulbecco’s phosphate buffered saline (DPBS) | Thermo Fisher Scientific | 14190144 | no calcium, no magnesium |
| Eppendorf cups, 1.5 mL | Eppendorf | 0030 125.215 | |
| Essential 6 | Gibco | A1516401 | |
| Essential 8 | Gibco | A1517001 | |
| Ethylenediaminetetraacetic acid (EDTA) | Invitrogen | 15575020 | |
| Falcon tubes, 15 mL, conical | Greiner Bio-One | 188271-N | |
| Formaldehyde | Sigma-Aldrich | 252549 | 37% Stock solution, diluted to 4% in PBS |
| Geltrex LDEV-Free Reduced Growth Factor Basement Membrane Matrix | Thermo Fisher Scientific | A1413202 | |
| GlutaMax (100x) | Gibco | 35050038 | |
| Hemacytometer cell counter | Hausser scientific | 1490 | |
| HEPES Buffer | Thermo Fisher Scientific | 15-630-080 | |
| Insulin | Sigma-Aldrich | I9278 | |
| LDN 193189 | StemCell Technologies | 72147 | |
| MAP2 | Abcam | ab32454 | 1:200 |
| Matrigel Growth Factor Reduced (GFR) Basement Membrane Matrix, LDEV-free | Corning | 356230 | basement membrane matrix |
| MEM-Non Essential Amino Acid Solution (MEM-NEAA; 100x) | Thermo Fisher Scientific | 11140050 | |
| Multilabel Counter Victor 3 Plate Reader | Perkin Elmer | 1420 | luminometer |
| MycoAlert Mycoplasma Detection Kit | Lonza | LT07-318 | |
| N-2 Supplement (100x) | Thermo Fisher Scientific | 17502-048 | |
| NeuN | Millipore | MAB377 | 1:500 |
| Neurobasal Medium | Thermo Fisher Scientific | 21103049 | |
| Oct-3/4 Antibody (C-10) Alexa Fluor 647 | Santa Cruz Biotechnology | sc-5279 AF647 | 1:100 |
| Parafilm | Bemis | PM-996 | thermoplastic film sheet |
| PAX6 | Thermo Fisher Scientific | 42-6600 | 1:200 |
| Penicillin/Streptomycin | Gibco | 15070063 | |
| Poly(lactic-co-glycolic acid) (PLGA) microfilaments | Ethicon | J463 | |
| QX200 Droplet digital PCR system | Bio-Rad | 1864001 | |
| ROCK inhibitor (Y27632) | Selleck Chemicals | S1049 | |
| SB431542 | R&D Systems | 1614/50 | |
| SOX2 Monoclonal Antibody (Btjce), Alexa Fluor 488, eBioscience | Invitrogen | 53-9811-80 | 1:100 |
| Synapsin I (SYN) | Calbiochem | 574777 | 1:200 |
| Triton-X 100 | Sigma-Aldrich | T8787 | |
| TUJ1 | Santa Cruz Biotechnology | sc-80005 | Beta-3-tubulin; 1:500 |
| XAV939 | Tocris Bioscience | 3748 |
References
- Liu, G. H., et al. Aging Atlas: a multi-omics database for aging biology. Nucleic Acids Research. 49, 825-830 (2021).
- Ferrucci, L., et al. Measuring biological aging in humans: A quest. Cell. 19 (2), 13080 (2020).
- Mertens, J., Reid, D., Lau, S., Kim, Y., Gage, F. H. Aging in a dish: iPSC-derived and directly induced neurons for studying brain aging and age-related neurodegenerative diseases. Annu Rev Genet. 52, 271-293 (2018).
- Mertens, J., et al. Age-dependent instability of mature neuronal fate in induced neurons from Alzheimer's patients. Cell Stem Cell. 28 (9), 1533-1548 (2021).
- Lin, Y. T., et al. APOE4 causes widespread molecular and cellular alterations associated with Alzheimer's disease phenotypes in human iPSC-derived brain cell types. Neuron. 98 (6), 1141-1154 (2018).
- Fang, E. F., et al. Mitophagy inhibits amyloid-β and tau pathology and reverses cognitive deficits in models of Alzheimer's disease. Nature Neuroscience. 22 (3), 401-412 (2019).
- Hu, J. L., Todhunter, M. E., LaBarge, M. A., Gartner, Z. J. Opportunities for organoids as new models of aging. Journal of Cell Biology. 217 (1), 39-50 (2018).
- Choi, S. H., et al. A three-dimensional human neural cell culture model of Alzheimer's disease. Nature. 515 (7526), 274-278 (2014).
- Gonzalez, C., et al. Modeling amyloid beta and tau pathology in human cerebral organoids. Molecular Psychiatry. 23 (12), 2363-2374 (2018).
- Yoon, S. -. J., et al. Reliability of human cortical organoid generation. Nature Methods. 16 (1), 75-78 (2019).
- Lancaster, M. A., Knoblich, J. A. Generation of cerebral organoids from human pluripotent stem cells. Nature Protocols. 9 (10), 2329-2340 (2014).
- Muratore, C. R., Srikanth, P., Callahan, D. G., Young-Pearse, T. L. Comparison and optimization of hiPSC forebrain cortical differentiation protocols. PLoS ONE. 9 (8), 105807 (2014).
- Giandomenico, S. L., Sutcliffe, M., Lancaster, M. A. Generation and long-term culture of advanced cerebral organoids for studying later stages of neural development. Nature Protocols. 16 (2), 579-602 (2020).
- Goto-Silva, L., et al. Computational fluid dynamic analysis of physical forces playing a role in brain organoid cultures in two different multiplex platforms. BMC Developmental Biology. 19 (1), 1-10 (2019).
- Sommer, A. G., et al. Generation of human induced pluripotent stem cells from peripheral blood using the STEMCCA lentiviral vector. Journal of Visualized Experiments. (68), e4327 (2012).
- Beers, J., et al. A cost-effective and efficient reprogramming platform for large-scale production of integration-free human induced pluripotent stem cells in chemically defined culture. Scientific Reports. 5 (1), 1-9 (2015).
- Wakao, S., et al. Morphologic and gene expression criteria for identifying human induced pluripotent stem cells. PLoS ONE. 7 (12), e48677 (2012).
- Schlaeger, T. M., et al. A comparison of non-integrating reprogramming methods. Nature Biotechnology. 33 (1), 58-63 (2015).
- JoVE. Basic Methods in Cellular and Molecular Biology. Using a Hemacytometer to Count Cells. JoVE Science Education Database. , (2022).
- Choy Buentello, D., Koch, L. S., Trujillo-De Santiago, G., Alvarez, M. M., Broersen, K. Use of standard U-bottom and V-bottom well plates to generate neuroepithelial embryoid bodies. PLOS ONE. 17 (5), 0262062 (2022).
- Ellis, P., et al. SOX2, a persistent marker for multipotential neural stem cells derived from embryonic stem cells, the embryo or the adult. Developmental Neuroscience. 26 (2-4), 148-165 (2004).
- Lee, S., et al. TuJ1 (class III β-tubulin) expression suggests dynamic redistribution of follicular dendritic cells in lymphoid tissue. European Journal of Cell Biology. 84 (2-3), 453-459 (2005).
- Suzuki, S., Namiki, J., Shibata, S., Mastuzaki, Y., Okano, H. The neural stem/progenitor cell marker nestin is expressed in proliferative endothelial cells, but not in mature vasculature. Journal of Histochemistry and Cytochemistry. 58 (8), 721-730 (2010).
- Soltani, M. H., et al. Microtubule-associated protein 2, a marker of neuronal differentiation, induces mitotic defects, inhibits growth of melanoma cells, and predicts metastatic potential of cutaneous melanoma. The American Journal of Pathology. 166 (6), 1841-1850 (2005).
- Wilson, P. G., Stice, S. S. Development and differentiation of neural rosettes derived from human embryonic stem cells. Stem Cell Reviews. 2 (1), 67-77 (2006).
- Gusel'nikova, V. V., Korzhevskiy, D. E. NeuN as a neuronal nuclear antigen and neuron differentiation marker. Acta Naturae. 7 (25), 42-47 (2015).
- Rao, M. S., Hattiangady, B., Shetty, A. K. The window and mechanisms of major age-related decline in the production of new neurons within the dentate gyrus of the hippocampus. Aging Cell. 5 (6), 545-558 (2006).
- Meng, L., et al. A synapsin I cleavage fragment contributes to synaptic dysfunction in Alzheimer's disease. Aging Cell. 21 (5), 13619 (2022).
- Moon, S. H., et al. Optimizing human embryonic stem cells differentiation efficiency by screening size-tunable homogenous embryoid bodies. Biomaterials. 35 (23), 5987-5997 (2014).
- Chambers, S. M., et al. Highly efficient neural conversion of human ES and iPS cells by dual inhibition of SMAD signaling. Nature Biotechnology. 27 (3), 275-280 (2009).
- Lee, S. -. W., et al. Optimization of Matrigel-based culture for expansion of neural stem cells. Animal Cells and Systems. 19 (3), 175-180 (2015).
- Zhang, J., et al. Extracellular matrix promotes highly efficient cardiac differentiation of human pluripotent stem cells: The matrix sandwich method. Circulation Research. 111 (9), 1125-1136 (2012).
- Hocevar, S. E., Liu, L., Duncan, R. K. Matrigel is required for efficient differentiation of isolated, stem cell-derived otic vesicles into inner ear organoids. Stem Cell Research. 53, 102295 (2021).
- Birey, F., et al. Assembly of functionally integrated human forebrain spheroids. Nature. 545 (7652), 54-59 (2017).
- Kozlowski, M. T., Crook, C. J., Ku, H. T. Towards organoid culture without Matrigel. Communications Biology. 4 (1), 1-15 (2021).
- Kaiser, A., Kale, A., Novozhilova, E., Olivius, P. The effects of Matrigel® on the survival and differentiation of a human neural progenitor dissociated sphere culture. The Anatomical Record. 303 (3), 441-450 (2020).
- Kakni, P., et al. Intestinal organoid culture in polymer film-based microwell arrays. Advanced Biosystems. 4 (10), 2000126 (2020).
- Lancaster, M. A., et al. Guided self-organization and cortical plate formation in human brain organoids. Nature Biotechnology. 35 (7), 659-666 (2017).
- Tejchman, A., Znój, A., Chlebanowska, P., Frączek-Szczypta, A., Majka, M. Carbon fibers as a new type of scaffold for midbrain organoid development. International Journal of Molecular Sciences. 21 (17), 5959 (2020).
Reprints and Permissions
Request permission to reuse the text or figures of this JoVE article
Request PermissionExplore More Articles
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. All rights reserved