Method Article
فحص للكشف عن حماية الأوعية الدموية في شبكية العين من الموت المرتبط بمرض السكري في الفئران
In This Article
Summary
تم تطوير مقايسة حماية لمراقبة مرونة الأوعية الدموية في شبكية العين حتى الموت من الإهانات المرتبطة بمرض السكري / اعتلال الشبكية السكري مثل الإجهاد التأكسدي والسيتوكينات.
Abstract
اعتلال الشبكية السكري (DR) هو مرض عيني معقد وتدريجي يتميز بمرحلتين متميزتين في التسبب فيه. تتضمن المرحلة الأولى فقدان الحماية من الأضرار التي يسببها مرض السكري في شبكية العين ، بينما تركز المرحلة الثانية على تراكم هذا الضرر. تركز المقايسات التقليدية في المقام الأول على تقييم التنكس الشعري ، وهو ما يدل على شدة الضرر ، ويعالج بشكل أساسي المرحلة الثانية من DR. ومع ذلك ، فإنها توفر فقط بشكل غير مباشر نظرة ثاقبة حول ما إذا كانت آليات الحماية للأوعية الدموية في شبكية العين قد تعرضت للخطر. لمعالجة هذا القيد ، تم تطوير نهج جديد لتقييم آليات حماية شبكية العين بشكل مباشر - على وجه التحديد ، مرونتها ضد الإهانات التي يسببها مرض السكري مثل الإجهاد التأكسدي والسيتوكينات. على الرغم من أن اختبار الحماية هذا مصمم في البداية لاعتلال الشبكية السكري ، إلا أنه يحمل إمكانية تطبيقات أوسع في كل من السياقات الفسيولوجية والمرضية. باختصار ، ينطوي فهم التسبب في اعتلال الشبكية السكري على التعرف على المراحل المزدوجة لفقدان الحماية وتراكم الضرر ، مع اختبار الحماية المبتكر هذا الذي يوفر أداة قيمة للبحث وربما يمتد إلى حالات طبية أخرى.
Introduction
اعتلال الشبكية السكري (DR) هو أحد مضاعفات الأوعية الدموية الدقيقة لمرض السكري (DM) ، والسبب الرئيسي للعمى لدى الأفراد في سن العمل في البلدان المتقدمة1. عوامل الخطر الرئيسية لاعتلال الشبكية السكري هي مدة ودرجة ارتفاع السكر في الدم2،3،4. في حين أن DM يسبب خللا في كل من المكونات الوعائية والعصبية للشبكية5 ، فإن تشخيص DR يعتمد على السمات المورفولوجية للأوعية الدموية في شبكيةالعين 6.
الإجهاد التأكسدي الناجم عن ارتفاع السكر في الدم هو أحد محركات التسبب في DR7. يؤدي الإجهاد التأكسدي المتزايد إلى تلف واسع النطاق ، مما يضر بوظائف الميتوكوندريا وبالتالي يزيد من مستوى أنواع الأكسجين التفاعلية. ويرافق هذه الأحداث تسرب الأوعية الشبكية ، وزيادة في مستوى السيتوكينات الالتهابية ، وموت كل من أنواع الخلايا العصبية والأوعية الدموية داخل شبكية العين. يؤدي فقدان الخلايا الوعائية ، وبالتالي وظائف الشبكة الشعرية الواسعة للشبكية ، إلى نقص الأكسجة ، وهو حافز قوي لمجموعة متنوعة منالاستجابات 5. وتشمل هذه الاستجابات زيادة التعبير عن عامل نمو بطانة الأوعية الدموية (VEGF) الذي يدفع كلا من النفاذية وتكوين الأوعية الدموية ، والسمات الأساسية للمراحل المتقدمة التي تهدد البصر من DR - الوذمة البقعية السكرية ، واعتلال الشبكية السكريالتكاثري 6.
تشير بعض ميزات DR إلى أن الكائن الحي (كل من المرضى التجارب) لديه قدرة جوهرية على مقاومة هذا المؤشر. يعاني المرضى من عدة عقود من DM قبل أن يصابوا ب DR8،9،10،11،12،13 التي تهدد البصر. في حين أن نماذج القوارض من DM لا تطور المراحل المتقدمة التي تهدد البصر من DR14 ، فإن الشكل الأولي / المعتدل من DR الذي يظهر لا يفعل ذلك إلا بعد فترة أسابيع أو أشهر من DM15،16. علاوة على ذلك ، في كل من المرضى التجارب ، يكون DR تقدميا ، ويزداد ضعف / تلف الشبكية مع إطالة مدة DM. أخيرا ، بعض المرضى الذين يعانون من DM لا يصابون أبدا ب DR. في بعض الحالات ، هذا لأن هؤلاء الأفراد لا يعانون من مرض السكري لفترة كافية لتطوير DR. في حالات أخرى ، يكون ذلك لأنهم يظهرون مقاومة غير عادية ل DR. كما هو الحال مع المشاركين في دراسة الميدالية ، الذين لا يصابون ب DR بعد 50 عاما أو أكثر منDM 17. وعلى الرغم من هذا الدعم المقنع لوجود الحماية من DR وأهميتها الانتقالية الهائلة، لم يتم التحقيق بقوة في الآلية الكامنة وراء الحماية.
تم تطوير مقايسة الحماية الموصوفة هنا لتسهيل التحقيق في سبب تأخر DR من بداية DM في الفئران المصابة بالسكري. تشمل الخطوات الرئيسية لهذا الفحص ، المطبقة على الفئران DM وغير DM ، (1) تقديم إهانة دون الحد الأقصى للموت للعين (خارج الجسم الحي أو في الجسم الحي) ، (2) عزل الأوعية الدموية في شبكية العين ، (3) تلطيخ الأوعية الدموية باستخدام TUNEL و DAPI ، (4) تصوير الصور الناتجة وتحديد النسبة المئوية لأنواع TUNEL / DAPI المزدوجة الإيجابية.
Protocol
تمت الموافقة على جميع الدراسات على من قبل مكتب رعاية والسلامة البيولوجية المؤسسية في جامعة إلينوي في شيكاغو. تم إيواء ذكور الفئران C57 / BL6 / J البالغة من العمر سبعة أسابيع في أقفاص جماعية في بيئة خالية من مسببات الأمراض في دورة 12 ساعة من الضوء / الظلام وتم توفير الطعام والماء مجانا. تم القتل الرحيم للفئران عن طريق الاختناق CO2 ، وتم استئصال العينين ومعالجتها على الفور18. تم الحصول على من مصدر تجاري (انظر جدول المواد). الأدوات الأساسية اللازمة للدراسة موضحة في الشكل 1.
1. توجيه الإهانة التي تسبب الموت
- أداء الإجهاد التأكسدي مع TBH (ex vivo).
- القتل الرحيم للفئران باتباع البروتوكولات المعتمدة مؤسسيا واستئصال عيونها18 (الشكل 2 أ).
- ضع مقل العيون مباشرة في الآبار الفردية للوحة 24 بئرا تحتوي على DMEM + 1٪ BSA ، مع أو بدون 5 mM Tert-butyl hydroperoxide (TBH) (انظر جدول المواد) ؛ احتضان لمدة 1 ساعة عند 37 درجة مئوية. تتم معالجة عينة تحكم إيجابية باستخدام DNase (50 وحدة / 100 ميكرولتر) لمدة 10 دقائق لتفتيت الحمض النووي.
ملاحظة: تم اختيار جرعة TBH (العامل الذي يحفز الإجهاد التأكسدي) للحث على مستوى يمكن اكتشافه بسهولة ودون الحد الأقصى لموت الخلايا داخل الأوعية الشبكية المعزولة18. - ثبت العينين في 10٪ من الفورمالين المخزن طوال الليل (16 ساعة كحد أدنى).
- استخدم كوكتيل السيتوكين للحث على الالتهاب (في الجسم الحي).
- تخدير الفئران بحقنة داخل الصفاق 100 مغ/كغ من الكيتامين و5 ملغ/كغ من الزيلازين.
- استخدم إبرة مخصصة 33 جم (انظر جدول المواد) لحقن 1 ميكرولتر / عين من كوكتيل السيتوكين في الجسم الزجاجي ؛ موقع الحقن هو 2-3 مم من النسيان (الشكل 2 ب).
ملاحظة: يحتوي كوكتيل السيتوكين على نسبة 1: 1: 1 من 1 ميكروغرام / مل TNF-α و 1 ميكروغرام / مل IL-1β و 1500 وحدة / ميكرولتر IFN-γ18 (انظر جدول المواد). - بعد 24 ساعة من الحقن ، قم بالقتل الرحيم للفئران (باتباع البروتوكولات المعتمدة مؤسسيا) ، وقم باستئصال عيونها وإصلاحها باستخدام 10٪ من الفورمالين المخزن طوال الليل.
ملاحظة: يمكن إيقاف التجربة مؤقتا بعد التثبيت لمدة 1 أسبوع كحد أقصى ثم إعادة تشغيلها لاحقا.
2. عزل الشبكية
- قطع فتح مقلة العين.
- استخدم ملقط مستقيم للإمساك بالعصب البصري برفق (الشكل 2C). امسك سكينا صغيرا باليد الأخرى لعمل شق من 2-3 مم خلف الطرف.
- قم بالتبديل من السكين الصغير إلى المقص الصغير للقطع بالتوازي مع الحافة أثناء تدوير مقلة العين مع العصب البصري حتى يتم قطع مقلة العين إلى نصفين.
- تخلص من النصف الأمامي من العين ، بما في ذلك العدسة (الشكل 2C).
- إزالة الصلبة.
- استخدم ملقط مستقيم لرفع الصلبة برفق 1-3 مم من شبكية العين.
- استخدم مقصا دقيقا لعمل قطعتين شعاعيتين في جزء الصلبة من الطريق إلى العصب البصري. تجنب قطع الشبكية الأساسية.
- استخدم زوجا من الملقط المنحني للإمساك بالسديلة الصلبة وتمزيقها من شبكية العين. ستؤتي طبقة RPE ثمارها مع الصلبة.
- اغسل شبكية العين.
- استخدم ملعقة صغيرة لنقل الشبكية المعزولة إلى بئر داخل طبق مكون من 24 بئرا مملوء بالماء المقطر المزدوج.
- هز الطبق برفق بسرعة متوسطة معتدلة في درجة حرارة الغرفة. قم بتغيير الماء كل 30 دقيقة إلى 1 ساعة ، على الأقل 4-5 مرات ، ثم اتركه طوال الليل.
3. عزل الأوعية الدموية في شبكية العين
- الهضم: استبدل الماء المقطر المزدوج ب 800 ميكرولتر من محلول YL trypsin (3٪ تريبسين في محلول Tris 0.1 M (درجة الحموضة 7.8)). احتضان في 37 درجة مئوية مع رج لطيف إلى عدم الرج لمدة 4 ساعات و 15 دقيقة19 (الشكل 2 د).
ملاحظة: تجنب الاهتزاز السريع لأن ذلك قد يؤدي إلى تلف الأوعية الدموية. - الزرع: اغمس الطرف العريض لماصة نقل الزجاج بمحلول YL trypsin لنقل شبكية العين إلى طبق بتري 35 مم يحتوي على ماء مقطر مزدوج خال من النسالة.
- قم بإزالة الطبقة النووية الخارجية (المستقبلات الضوئية) (الشكل 2E).
- اقلب نصف كرة الشبكية إلى الأسفل. استخدمي فرشاة الشعر الواحد المستقيمة للضغط برفق على شبكية العين في قاع الطبق.
- استخدم الفرشاة الحلقية لإزالة المستقبلات الضوئية لشبكية العين برفق. يتم تطبيق ضربات الفرشاة في اتجاه من العصب البصري نحو محيط الشبكية. يمكن أن تنفصل المستقبلات الضوئية في صفائح كبيرة لأنها لا ترتبط ببقية شبكية العين بواسطة الأوعية الدموية.
- استخدام ماصة 200 ميكرولتر لجمع وتجاهل صفائح الأنسجة العصبية.
- إزالة الجسم الزجاجي.
- اقلب نصف كرة الشبكية بحيث تكون متجهة لأعلى. استخدم زوجا من الملقط المنحني (A) للإمساك بالجسم الزجاجي قدر الإمكان تحت مجهر تشريح.
ملاحظة: يبدو الجسم الزجاجي وكأنه ورقة من الأنسجة الشفافة متصلة بالعصب البصري أو شبكية العين. - استخدم ملقط منحني آخر (B) للإمساك بنهاية الجسم الزجاجي حيث يربط العصب البصري. قم بإزالة الجسم الزجاجي عن طريق سحب الملقط A بعيدا عن الملقط B.
- تخلص من الجسم الزجاجي. افحص بقايا الجسم الزجاجي وكرر هذه الخطوة لإزالة كل الجسم الزجاجي لأن المتبقي سيعيق الخطوات التالية.
- اقلب نصف كرة الشبكية بحيث تكون متجهة لأعلى. استخدم زوجا من الملقط المنحني (A) للإمساك بالجسم الزجاجي قدر الإمكان تحت مجهر تشريح.
- قم بإزالة الأنسجة العصبية والدبقية المتبقية (الشكل 2F).
- اقلب نصف كرة الشبكية بحيث تكون متجهة لأسفل مرة أخرى. مرة أخرى ، استخدم الفرشاة المستقيمة للضغط برفق على شبكية العين في أسفل الطبق (لا تستخدم طرف الشعر).
- استخدم فرشاة الحلقة لتنظيف الأوعية الدموية برفق من رأس العصب البصري باتجاه المحيط لإزالة الأنسجة العصبية المتبقية20.
- قم بتدوير الشبكية ببطء باستخدام الفرشاة المستقيمة واستخدم فرشاة الحلقة لإزالة جميع الأجزاء الصغيرة من الأنسجة العصبية على الأوعية الدموية في الشبكية ، حتى يتم تنظيف شبكة الأوعية الدموية جيدا (الشكل 2G ، H).
4. تركيب الأوعية الدموية الشبكية المعزولة على شريحة المجهر
- ضع شريحة المجهر.
- ضع كاسيت تثبيت نظيف (انظر جدول المواد) تحت مجهر تشريح. املأ الكاسيت بالماء المقطر المزدوج.
- استخدم خلفية سوداء تحت مجهر التشريح للمساعدة في توليد التباين لرؤية الأوعية الدموية الشفافة المضيئة.
- استخدم ملقط لوضع شريحة مجهر نظيفة تحمل علامة في الجزء السفلي من شريط التثبيت.
- نقل الأوعية الدموية في شبكية العين.
- اغمس الطرف العريض لماصة نقل الزجاج بمحلول YL trypsin.
- انقل الأوعية الدموية الشبكية التي تم تنظيفها وقم بإزاحة الأوعية الدموية برفق إلى الماء المقطر المزدوج داخل شريط التثبيت وفوق شريحة المجهر.
- جبل الأوعية الدموية في شبكية العين.
ملاحظة: بينما تطفو الأوعية الدموية فوق شريحة المجهر ، ستكتسب الأوعية الدموية المعزولة شكلها الطبيعي للوعاء.- استخدم الفرشاة الحلقية لقلب نصف كرة الشبكية المتجهة لأعلى وادفع الأوعية الدموية برفق لأسفل على الشريحة الزجاجية ، ثم استخدم الشعر للصق الأوعية الدموية المفتوحة على مركز الشريحة. يجب أن تلتصق الأوعية الدموية بالشريحة أثناء لمسها.
- قم بتركيب الأوعية الدموية بشكل مسطح عن طريق تنظيف وعاء الشبكية على شكل وعاء من العصب البصري إلى المحيط.
- كرر تنظيف الأسنان بالفرشاة في جميع الاتجاهات حتى تلتصق الأوعية الدموية بالشريحة تماما.
- جفف الأوعية الدموية في الشبكية بالهواء.
- بمجرد أن تلتصق الأوعية الدموية في شبكية العين بالكامل بالشريحة ، أخرج الشريحة من الماء إما عن طريق رفع حافة واحدة برفق أو عن طريق تصريف المياه ببطء في زاوية الكاسيت لتقليل التيارات ، ثم سحبها للخارج (الشكل 2I).
ملاحظة: ستصبح الأوعية الدموية مرئية بسهولة بمجرد تجفيفها بالهواء (الشكل 2J). - ضع علامة على محيط الأوعية الدموية في شبكية العين على الجزء الخلفي من الشريحة باستخدام قلم علامة.
- تابع تلطيخ العينة دون توقف.
- بمجرد أن تلتصق الأوعية الدموية في شبكية العين بالكامل بالشريحة ، أخرج الشريحة من الماء إما عن طريق رفع حافة واحدة برفق أو عن طريق تصريف المياه ببطء في زاوية الكاسيت لتقليل التيارات ، ثم سحبها للخارج (الشكل 2I).
5. كشف الوفاة مع تلطيخ TUNEL
ملاحظة: للحصول على تفاصيل حول هذا الإجراء، يرجى الرجوع إلى Zheng et al.21. يصور الشكل 3 صورا تمثيلية لنقص التروية +/- الأجسام المبرمج التي يسببها إجهاد الثور في أوعية الشبكية المعزولة.
- إعادة ترطيب الأوعية الدموية المعزولة مع برنامج تلفزيوني. شطفه 3 مرات في برنامج تلفزيوني ثم احتضانه مع 1٪ Triton X-100 في برنامج تلفزيوني لمدة 2 دقيقة على الجليد لنفاذية الأوعية الدموية المعزولة.
- شطف الشرائح مرتين مع PBS لإزالة بقايا Triton X-100. جفف المنطقة المحيطة بالعينة.
- أضف 50 ميكرولتر من خليط تفاعل TUNEL (انظر جدول المواد) إلى العينة. احتضن الشريحة في جو مرطب لمدة 60 دقيقة عند 37 درجة مئوية في الظلام.
- اشطف الشريحة 3 مرات باستخدام PBS لإزالة خليط تفاعل TUNEL. جفف المنطقة المحيطة بالعينة.
- أضف قطرة من وسائط تركيب DAPI لتلطيخ النوى باستخدام DAPI وقم بتركيب العينة بغطاء زجاجي. يحفظ في درجة حرارة 4 درجات مئوية في الظلام.
ملاحظة: يمكن إيقاف البروتوكول مؤقتا لمدة تصل إلى 1 أسبوع قبل التقاط الصور. - قم بتصوير الأوعية الدموية الناتجة باستخدام مجهر مضان متحد البؤر (انظر جدول المواد). التقط ستة إلى ثمانية حقول مختارة عشوائيا في المحيط البعيد المحيط بالعصب البصري (الشكل 4).
ملاحظة: يوضح الشكل 5 صورا تمثيلية للأجسام المبرمج التي يسببها السيتوكين في الأوعية الشبكية المعزولة. - تحليل النتائج.
- بالنسبة للعينات خارج الجسم الحي والمعالجة ب TBH ، قم بتنفيذ الخطوات التالية.
- احسب عدد الأجسام المبرمج (الأنواع المزدوجة الإيجابية TUNEL / DAPI) في كل حقل باستخدام الصورة J (انظر جدول المواد). احسب متوسط الأجسام المبرمج في جميع مجالات العينة الواحدة.
- احسب تغير الطي في عدد الأجسام المبرمج بين زوج تم اختياره عشوائيا من العينات غير DM و DM.
- حدد ما إذا كان هناك فرق ذو دلالة إحصائية باستخدام اختبار t للطالب ثنائي الطرف18.
ملاحظة: قم بتلطيخ العينات الضابطة والتجريبية (غير DM و DM) في نفس المناسبة لأن مدى تلطيخ TUNEL يمكن أن يختلف ، حتى عند القيام به بنفس الطريقة. نظرا لأنه يمكن تنظيف ما يصل إلى 10 شبكية وتركيبها يوميا بواسطة مستخدم متمرس ، خطط لمعالجة عدد متساو من شبكية العين الضابطة والتجريبية قبل بدء هذا البروتوكول.
- بالنسبة للعينات المعالجة بكوكتيل السيتوكينات في الجسم الحي ، قم بتنفيذ الخطوات التالية.
- عد يدويا عدد الأجسام المبرمج (الأنواع الإيجابية المزدوجة TUNEL / DAPI) في الأوعية الدموية الشبكية بأكملها.
- احسب تغير الطي في عدد الأجسام المبرمج بين زوج تم اختياره عشوائيا من العينات غير DM و DM.
- حدد ما إذا كان هناك فرق ذو دلالة إحصائية باستخدام اختبار t للطالب ثنائي الذيل.
- بالنسبة للعينات خارج الجسم الحي والمعالجة ب TBH ، قم بتنفيذ الخطوات التالية.
النتائج
ينتج عن العزل الناجح للأوعية الدموية في شبكية العين جبل مسطح للشبكة الكاملة للأوعية الدموية في شبكية الفأر ، مع سلامة البنية (الشكل 2J). عند تلطيخ الهيماتوكسيلين الحمضي الدوري (PASH) ، من الممكن التمييز بين نوعي الخلايا الوعائية: الخلايا البطانية (ECs) والخلايا المحيطة (PCs) (الشكل 6). نوى الخلايا البطانية ممدودة وملطخة قليلا وتوجد بالكامل داخل جدران الوعاء الدموي. نوى Pericyte دائرية ، ملطخة بكثافة ، وتبرز من جدران الشعيرات الدموية. تكشف العينات الملطخة بالباش أيضا عن الشعيرات الدموية اللاخلوية التي تفتقر إلى النوى.
واسترشد نهج الحث على الموت بالأساس المنطقي التالي. تم التكهن بأن الحماية محدودة ، أي يمكن أن تطغى عليها إهانة قوية جدا تؤدي إلى الموت. وبالتالي ، تم تحسين الإهانات (كل من نقص التروية / الإجهاد التأكسدي والسيتوكينات18) بحيث تؤدي إلى زيادة يمكن اكتشافها بسهولة ولكن مع ذلك دون الحد الأقصى للوفاة (الشكل 3 والشكل 5).
من المهم تسليط الضوء على أن وجود نوى TUNEL الإيجابية كان مشروطا بنوع معين من الإهانة المستخدمة لتحفيز موت الخلايا. أدت إهانة نقص التروية / الإجهاد التأكسدي إلى نمط مسار الترام من موت الخلايا المبرمج ، كما هو موضح في الشكل 3 ، في حين أدت إهانة السيتوكين إلى نمط مميز ومحدد جيدا ، كما هو موضح في الشكل 5. يمكن ملاحظة كلا النمطين في الأوعية الشبكية من مرضى DR22 ، مما يشير إلى أن كلا النوعين من العوامل يحفز موت الخلايا لدى البشر. علاوة على ذلك ، توفر الفروق المورفولوجية المرصودة وسيلة لتقييم ما إذا كان علم الأمراض مدفوعا بالإجهاد التأكسدي أو السيتوكينات.
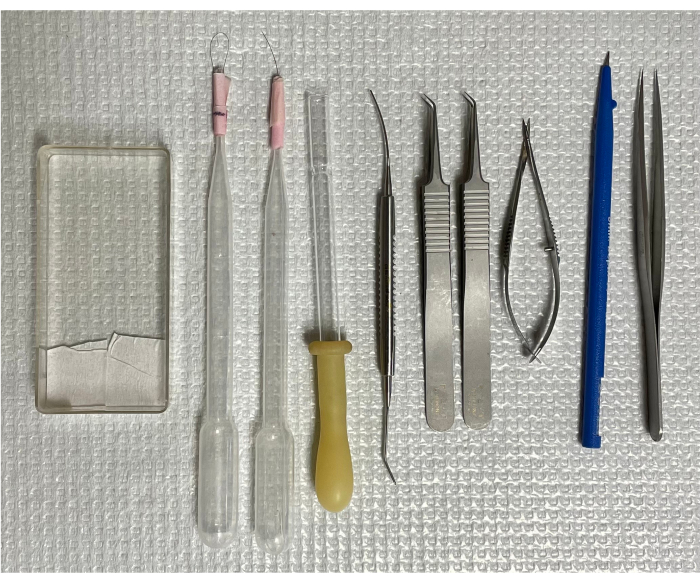
الشكل 1: أدوات لعزل الأوعية الدموية في شبكية الفأر. من اليسار إلى اليمين: كاسيت التثبيت ، وفرشتان للشعر الواحد ، وماصة نقل مقلوبة ، وملعقة صغيرة ، وملقطان منحنيان ، ومقص زنبركي ، وسكين صغير ، وملقط بأطراف مستقيمة. يرجى النقر هنا لعرض نسخة أكبر من هذا الرقم.

الشكل 2: رسم تخطيطي يوضح الخطوات الرئيسية لتوجيه إهانة تحفز الموت ثم عزل الأوعية الدموية في شبكية العين عن عين الفأر. (أ) تحريض نقص التروية/الإصابة التأكسدية، خارج الجسم الحي. بعد الاستئصال ، تتعرض مقلة العين لنقص التروية في وجود TBH. ب: إعطاء السيتوكينات في الجسم الحي (الحقن داخل الجسم الزجاجي). ج: تقطيع مقلة العين إلى نصفين. د: الهضم الإنزيمي للشبكية: إزالة الصلبة وغسل الشبكية بالماء المقطر مرتين طوال الليل. الحضانة في محلول YL trypsin عند 37 درجة مئوية لمدة 4 ساعات و 15 دقيقة في بئر من صفيحة 24 بئرا. ه: إزالة المستقبلات الضوئية. (و) إزالة الأنسجة العصبية والدبقية المتبقية. (ز) شبكة أوعية دموية نظيفة على شكل وعاء متجهة لأعلى. (H) شبكة وعائية معزولة في طبق 35 مم مع خلفية سوداء على مرحلة المجهر التشريحي. (I) الأوعية الدموية الشبكية المسطحة المثبتة على شريحة. (ي) الأوعية الدموية الشبكية المجففة بالهواء على شريحة. تم تعديل هذا الرقم من Li et al.18. يرجى النقر هنا لعرض نسخة أكبر من هذا الرقم.
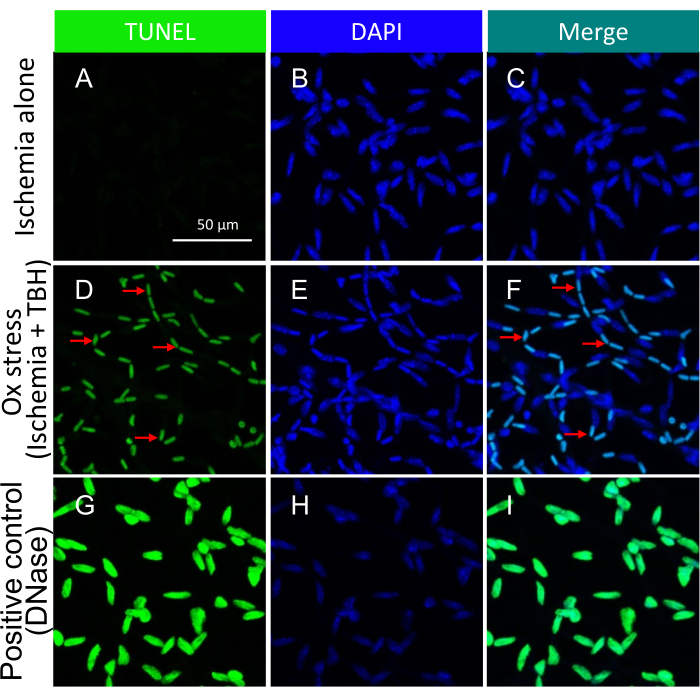
الشكل 3: الكشف عن الأجسام المبرمج داخل أوعية شبكية الفأر المعالجة خارج الجسم الحي بنقص التروية +/- TBH. صور تمثيلية لنقص التروية +/- الأجسام المبرمج الناجمة عن إجهاد الثور في الأوعية الشبكية المعزولة. يشير عنوان كل عمود إلى التلطيخ. (أ-ج) الأوعية الشبكية المعزولة من مقل العيون التي خضعت ل 1 ساعة من نقص التروية وحده. (مد-واو) نفس (A-C) ، باستثناء إهانة 1 h كانت مزيجا من نقص التروية والإجهاد التأكسدي (5 mM TBH). تشير الأسهم الحمراء إلى الأنواع المزدوجة الإيجابية المزدوجة TUNEL / DAPI التمثيلية. (ز-ط) السيطرة الإيجابية تعامل مع DNase. شريط المقياس = 50 ميكرومتر. تم تعديل هذا الرقم من Li et al.18. يرجى النقر هنا لعرض نسخة أكبر من هذا الرقم.

الشكل 4: رسم توضيحي لاختيار المجال للقياس الكمي للنتائج. مسح البلاط 5 × 5 للأوعية الدموية في شبكية العين مع دمج إشارة TUNEL و DAPI. يظهر اختيار ستة إلى ثمانية حقول في المحيط البعيد المحيط بالعصب البصري بمربعات حمراء. التكبير ، 200x. شريط المقياس = 100 ميكرومتر. يرجى النقر هنا لعرض نسخة أكبر من هذا الشكل.
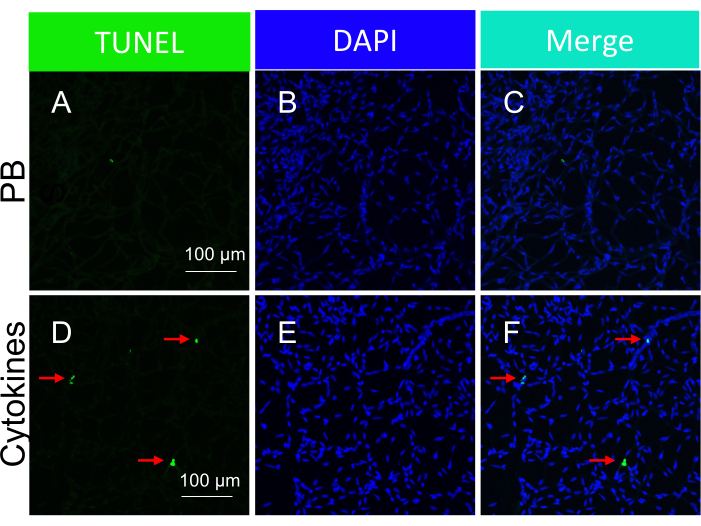
الشكل 5: الكشف عن الأجسام المبرمج داخل أوعية شبكية الفأر استجابة للحقن داخل الجسم الزجاجي للسيتوكينات (في إدارة الجسم الحي). صور تمثيلية للأجسام المبرمج التي يسببها السيتوكين في أوعية الشبكية المعزولة. يشير عنوان كل عمود إلى التلطيخ. (أ-ج) صور الأوعية الشبكية المعزولة من الفئران داخل الجسمحقن حقا مع برنامج تلفزيوني. (مد-واو) مثل (A-C) ، باستثناء كوكتيل السيتوكين الذي تم حقنه مع برنامج تلفزيوني. تشير الأسهم الحمراء إلى الأنواع التمثيلية الإيجابية TUNEL. قضبان المقياس = 100 ميكرومتر. تم تعديل هذا الرقم من Li et al.18. يرجى النقر هنا لعرض نسخة أكبر من هذا الرقم.
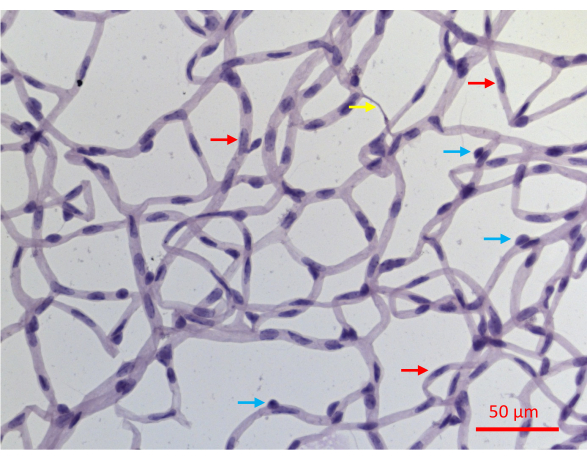
الشكل 6: صورة تمثيلية لأوعية شبكية ملطخة بالباش. تم عزل الأوعية الشبكية للفأر التي شهدت 20 أسبوعا من DM الناجم عن STZ كما هو موضح في الشكل 2 ، ملطخة بالباش ، وتم تصويرها أثناء إضاءتها بالضوء المرئي. تميل نوى pericyte في الشعيرات الدموية إلى أن تكون أكثر دائرية وملطخة بكثافة (الأسهم الزرقاء) ، في حين أن النوى الممدودة والأقل كثافة هي تشخيص الخلايا البطانية (الأسهم الحمراء). يشير السهم الأصفر إلى الشعيرات الدموية اللاخلوية. شريط المقياس = 50 ميكرومتر. يرجى النقر هنا لعرض نسخة أكبر من هذا الشكل.
Discussion
في هذه الدراسة ، تم إنشاء اختبار للكشف عن مقاومة / ضعف الأوعية الدموية في شبكية العين حتى الموت الناجم عن الإهانات المتعلقة ب DM / DR مثل نقص التروية / الإجهاد التأكسدي والسيتوكينات. تقدم هذه المخطوطة وصفا تفصيليا لهذا الفحص ، وهو تعديل للعديد من البروتوكولات المنشورة19،20،21.
ويشمل البروتوكول عدة مراحل حاسمة. أولا ، من الضروري تشريح شبكية العين بدقة ، وضمان الحفاظ على شبكة الأوعية الدموية ومنع التمزقات الكبيرة. يمكن تحقيق ذلك عن طريق إجراء شق 2-3 مم خلف النسيان لأن الشبكية تلتصق بإحكام بأورا سيراتا ، وفصلها يمثل تحديا. ثانيا ، قم بتغطية جميع الأدوات التي تتلامس مع الأوعية (على سبيل المثال ، فرش الشعر الفردي ، ونقل الماصة ، والملقط) بالتربسين عن طريق غمس هذه الأدوات في محلول YL trypsin طوال الإجراء. هذا يمنع الأوعية الدموية من الالتصاق بالأدوات المستخدمة في هذا البروتوكول. ثالثا ، نظرا لأن الأوعية الدموية الدقيقة غير مرئية تقريبا تحت الضوء العادي ، فإن اليقظة العالية مطلوبة أثناء شفط الحطام ونقله إلى شريحة المجهر من أجل منع الفقد العرضي.
درجة مناسبة من الهضم الأنزيمي للطبقات المختلفة من شبكية العين أمر بالغ الأهمية. يمنع الهضم غير الكافي فصل الأنسجة العصبية عن شبكة الأوعية الدموية ، بينما يذوب الهضم المفرط الضفيرة الوعائية. تم الإبلاغ عن أوقات هضم مختلفة تتراوح من 1 ساعة و19 إلى 23 بين عشية وضحاها. بناء على الملاحظات ، فإن وقت الهضم البالغ 4 ساعات و 15 دقيقة ينتج عنه أفضل النتائج مقارنة بفترات 2 ساعة و 3 ساعات و 4 ساعات. من غير المرجح أن يؤدي إطالة عملية الهضم إلى ما بعد هذه النقطة إلى تعزيز العملية وقد يضر بدلا من ذلك بسلامة الأوعية الدموية.
في الحالات التي تلتصق فيها شبكية العين المهضومة بفرشاة الشعر الواحد ، اغمس الشعر في محلول YL trypsin عدة مرات. هذا يقلل من المناطق اللزجة للفرشاة. إذا كانت فرشاة الشعر لا تزال تلتصق بأنسجة الأوعية الدموية ، فقم بفحصها بحثا عن الأجزاء المتبقية من الجسم الزجاجي ، وقم بإزالتها بالملقط.
اللحظة المثلى لإزالة الجسم الزجاجي الكامل هي بعد القضاء على المستقبلات الضوئية ، ولكن قبل إزالة الأنسجة العصبية والدبقية المتبقية. تحافظ شبكية العين على الصلابة حتى تتم إزالة المستقبلات الضوئية. استخراج الجسم الزجاجي في هذه المرحلة يمكن أن يمزق الشبكية / الأوعية الدموية. تلعب الطبقات الحساسة من الأنسجة العصبية والدبقية المتبقية دورا محوريا في الحفاظ على الشكل المنحني لهيكل الأوعية الدموية. تمنع شبكية العين من التمزق في مركزها عندما يتم فصل الجسم الزجاجي عن العصب البصري.
إذا لم تلتصق الأوعية الدموية المعزولة بشريحة المجهر على الإطلاق ، فهذا يشير إلى أن قسم الشريحة الذي من المتوقع أن يحدث فيه الالتصاق متسخ. حاول تحريك الأوعية عبر سطح الشريحة لتحديد مكان لزج ، أو التبديل إلى شريحة مختلفة أو تنظيف الشريحة بدقة والمحاولة مرة أخرى. إذا التصقت الأوعية بالشريحة قبل أن تنفتح في شكلها الشبيه بالوعاء ، ارفع الأوعية الدموية من الشريحة للسماح لها بالطفو بحرية في الماء مرة أخرى. قم بهذه الخطوة باستخدام الملقط الذي تم غمسه بشكل متكرر في محلول YL trypsin.
تم الإبلاغ عن العديد من التقنيات البديلة لعزل الأوعية الدموية ، والتي لن تكون مناسبة لمقايسة الحماية الموصوفة هنا. على سبيل المثال ، تم استخدام التحلل التناضحي لعزل الأوعية الدموية من عينات شبكية العين غير الثابتة ، مما يسهل التحقيقات الكيميائية الحيوية للأنسجة24،25. ومع ذلك ، قد لا يحافظ هذا الإجراء على تشريح الأوعية الدموية وكذلك النهج المستخدم في هذه المقالة. وبالمثل ، في حين أن طريقة طباعة الأنسجة لعزل أجزاء كبيرة من الأوعية الدموية الدقيقة تمكن من تحليل البنية الكهروتونية للأوعيةالدموية 26 ، فإن السرير الوعائي بأكمله لا يتم استرداده عادة.
تم تطوير هذا الاختبار لأن الأساليب الحالية لرصد تنكس الشعيرات الدموية لا تعالج مسألة الحماية. يشير التنكس الشعري ، الذي يحدث بعد DM لفترة طويلة ، إلى ما إذا كان DR قد تطور. بالإضافة إلى تشخيص DR ، هذه النتيجة مفيدة لتقييم ما إذا كان العامل / العلاج يمنع DR. ومع ذلك ، فإن مقايسات تنكس الشعيرات الدموية الحالية لا تتحدث عن الآلية الأساسية لعمل العامل. مثل هذا العامل قد يمنع الأحداث المرضية التي تدفع DR مثل زيادة الإجهاد التأكسدي أو السيتوكينات. بدلا من ذلك ، قد يفرض العامل الحماية من خلال تعزيز المرونة في الإجهاد التأكسدي والسيتوكينات و / أو تعزيز إصلاح الضرر. يمكن استخدام اختبار الحماية الجديد هذا لتحديد ما إذا كان التأثير المفيد لعلاج معين ينطوي على فرض النظام الداخلي الذي يحمي من الموت المرتبط ب DM.
عيب مقايسة الحماية هذه هو أنها لا تميز بين نوعي الخلايا داخل الأوعية الشبكية: الخلايا البطانية (ECs) والخلايا المحيطة (PCs). في حين أن مظهر نواتها في أقسام ملطخة بالباش خاص بنوع الخلية (الشكل 6) ، لا تعرض كل نواة ميزات تشخيصية. لا يمكن تعريف ما يقرب من 30٪ من النوى بشكل لا لبس فيه على أنها EC أو PC جزئيا على الأقل لأن الصور ثنائية الأبعاد التي تم الحصول عليها من العينات الملطخة بالباش تحل بشكل غير كامل البنية ثلاثية الأبعاد للضفيرة الوعائية. يمكن التغلب على هذه العقبة من خلال تحليل إضافي مثل تلطيخ الفلورسنت المناعي بعلامات خاصة بنوع الخلية. مثل هذه الصور ، التي تميز بين نوعي الخلايا ، يمكن تلطيخها بالاشتراك مع TUNEL لتحديد مقاومة / ضعف كل نوع من أنواع الخلايا الوعائية.
لا يوفر هذا الفحص الذي يركز على الأوعية الدموية أي معلومات تتعلق بالشبكية العصبية. ويمكن وضع مقايسات إضافية لتوفير هذه المعلومات. على سبيل المثال ، بدلا من عزل الأوعية الدموية في شبكية العين ، يمكن إنشاء تعليق خلية واحدة لشبكية العين بأكملها ثم تحليلها (عن طريق فرز الخلايا المنشطة بالفلورسنت) للمقاومة / الضعف. إن إدراج علامات خاصة بنوع الخلية (العصبية والأوعية الدموية على حد سواء) جنبا إلى جنب مع مؤشرات موت الخلايا من شأنه أن يوفر صورة أكثر اكتمالا لأنواع خلايا الشبكية التي لديها القدرة على الحماية من الموت بوساطة DM / DR.
في الختام ، يوفر اختبار الحماية الموصوف هنا نهجا قويا للتحقيق في الآلية المسؤولة عن التأخير بين ظهور DM وظهور DR في الفئران.
Disclosures
ليس لدى المؤلفين أي تضارب في المصالح للإبلاغ عنه.
Acknowledgements
تم دعم هذا العمل بمنح من جمعية إلينوي للوقاية من العمى والمعهد الوطني للصحة (EY031350 و EY001792) ومنحة غير مقيدة من مؤسسة أبحاث الوقاية من العمى.
Materials
| Name | Company | Catalog Number | Comments |
| 10% neutral buffered formalin | Fischer Scientific | SF100-4 | Fixation |
| 24-well plates | Falcon | 353047 | |
| 33 G needle | Hamilton | customized | |
| Ammonium hydroxide | Sigma | 221228-1L-PCA | |
| C57/BL6/J mice | The Jackson Laboratory | Jax #000664 | |
| Cytokine cocktail | consisted of a 1:1:1 ratio of 1 µg/mL TNF-α, 1 µg/mL IL-1 β and and 1500 U/µLIFN- γ | ||
| Dissecting microscope | Any microscope that allows good visualization of the retina is adequate. | ||
| Dumont #3 forceps | Fine Science Tools (FST) | 11231-30 | Straight tips |
| Dumont #5 forceps | Fine Science Tools (FST) | 11253-25 | Micro-blunted tips |
| Easy-Grip Tissue Culture Dishes | Falcon | 353001 | 35 x 10 mm |
| Glass transfer pipet | Fischer Scientific | 1367820A | snap off the thin end of a Pasteur pipet and fit the “broken” end with a rubber bulb. |
| Harris modified hematoxylin | Sigma | HHS32 | |
| Image J | NIH, Bethesda | https://imagej.nih.gov/ij/ | |
| In Situ Cell Death Detection Kit, Fluorescein | Milipore | 11684795910 | TUNEL reaction mixture |
| Micro cover glasses | VWR | 48366-227 | 22 mm x 22 mm |
| Microknife | Sharpoint | 72-1551 | |
| Micro-spatula | Fine Science Tools | 10091-12 | |
| Mounting cassette | Any transparent cassette that is slightly bigger than the microscope slide | ||
| Periodic acid | Sigma | 3951 | |
| Periodic acid solution | 35 mM periodic acid with 12 mM sodium acetate in H2O | ||
| Permount mounting medium | Fischer Scientific | SP15- 100 | |
| Prism 9 | GraphPad | ||
| Prolog Gold antifade reagent with DAPI | Invitrogen | P36935 | |
| Recombinant human IFN- γ | Peprotec | 300-02 | |
| Recombinant human IL-1 β | Peprotec | 200-01B | |
| Recombinant human TNF-α | Peprotec | 300-01A | |
| Schiff reagent base | Sigma | 3952016 | |
| Shaker Incubator (belly button shaker) | IBI Scientific | BBUAAUV1S | |
| Sodium acetate | Sigma | 71196 | |
| Steritop sterile vacuum bottle | Millipore | SCGPS05RE | Create filtered water |
| Superfrost Plus treated microscope slides | Fischer Scientific | 12-550-15 | use slides from unopened box |
| Tert-butyl hydroperoxide (TBH) | Sigma | 75-91-2 | |
| TRIZMA base | Fischer Scientific | 11-101-5522 | make 100 mM Tris, adjust pH to 7.8 using HCl) |
| Trypsin 1:250 | Amresco | 0458-50G | |
| Two “brushes” | made from single black hair taped to the end of plastic transfer pipet. One brush with a free end. The other brush with a loop | ||
| Vannas Spring Scissors | Fine Science Tools (FST) | 15000-00 | |
| Xylene | Sigma | 65351-M | |
| YL trypsin solution | 3% trypsin in 0.1 M Tris (pH 7.8) | ||
| Zeiss LSM 710 fluorescence microscope | Zeiss Microscopy |
References
- Teo, Z. L., et al. Global prevalence of diabetic retinopathy and projection of burden through 2045: Systematic review and meta-analysis. Ophthalmology. 128 (11), 1580-1591 (2021).
- Lee, R., Wong, T. Y., Sabanayagam, C. Epidemiology of diabetic retinopathy, diabetic macular edema and related vision loss. Eye Vis (Lond). 2, 21 (2015).
- Lima, V. C., Cavalieri, G. C., Lima, M. C., Nazario, N. O., Lima, G. C. Risk factors for diabetic retinopathy: A case-control study. Int J Retina Vitreous. 2, 21 (2016).
- Sabanayagam, C., Yip, W., Ting, D. S., Tan, G., Wong, T. Y. Ten emerging trends in the epidemiology of diabetic retinopathy. Ophthalmic Epidemiol. 23 (4), 209-222 (2016).
- Antonetti, D. A., Silva, P. S., Stitt, A. W. Current understanding of the molecular and cellular pathology of diabetic retinopathy. Nat Rev Endocrinol. 17 (4), 195-206 (2021).
- Wong, T., Cheung, C., Larsen, M., Sharma, S., Simó, R. Diabetic retinopathy. Nat Rev Dis Primers. 2, 16012 (2016).
- Wu, M. Y., Yiang, G. T., Lai, T. T., Li, C. J. The oxidative stress and mitochondrial dysfunction during the pathogenesis of diabetic retinopathy. Oxid Med Cell Longev. 2018, 3420187 (2018).
- Hietala, K., Harjutsalo, V., Forsblom, C., Summanen, P., Groop, P. H. Age at onset and the risk of proliferative retinopathy in type 1 diabetes. Diabetes Care. 33 (6), 1315-1319 (2010).
- Aiello, L. P., et al. Diabetic retinopathy. Diabetes Care. 21 (1), 143-156 (1998).
- Klein, R., Klein, B. E., Moss, S. E., Davis, M. D., Demets, D. L. The wisconsin epidemiologic study of diabetic retinopathy. Prevalence and risk of diabetic retinopathy when age at diagnosis is less than 30 years. Arch Ophthalmol. 102 (4), 520-526 (1984).
- Nathan, D. M., et al. The effect of intensive treatment of diabetes on the development and progression of long-term complications in insulin-dependent diabetes mellitus. N Engl J Med. 329 (14), 977-986 (1993).
- . Clustering of long-term complications in families with diabetes in the diabetes control and complications trial. The diabetes control and complications trial research group. Diabetes. 46 (11), 1829-1839 (1997).
- Cruickshanks, K. J., Moss, S. E., Klein, R., Klein, B. E. Physical activity and proliferative retinopathy in people diagnosed with diabetes before age 30 yr. Diabetes Care. 15 (10), 1267-1272 (1992).
- Robinson, R., Barathi, V. A., Chaurasia, S. S., Wong, T. Y., Kern, T. S. Update on animal models of diabetic retinopathy: From molecular approaches to mice and higher mammals. Dis Model Mech. 5 (4), 444-456 (2012).
- Samuels, I. S., Bell, B. A., Pereira, A., Saxon, J., Peachey, N. S. Early retinal pigment epithelium dysfunction is concomitant with hyperglycemia in mouse models of type 1 and type 2 diabetes. J Neurophysiol. 113 (4), 1085-1099 (2015).
- Sergeys, J., et al. Longitudinal in vivo characterization of the streptozotocin-induced diabetic mouse model: Focus on early inner retinal responses. Invest Ophthalmol Vis Sci. 60 (2), 807-822 (2019).
- Sun, J. K., et al. Protection from retinopathy and other complications in patients with type 1 diabetes of extreme duration: The joslin 50-year medalist study. Diabetes Care. 34 (4), 968-974 (2011).
- Li, Y., et al. The slow progression of diabetic retinopathy is associated with transient protection of retinal vessels from death. Int J Mol Sci. 24 (13), 10869 (2023).
- Chou, J. C., Rollins, S. D., Fawzi, A. A. Trypsin digest protocol to analyze the retinal vasculature of a mouse model. J Vis Exp. 76, e50489 (2013).
- Veenstra, A., et al. Diabetic retinopathy: Retina-specific methods for maintenance of diabetic rodents and evaluation of vascular histopathology and molecular abnormalities. Curr Protoc Mouse Biol. 5 (3), 247-270 (2015).
- Zheng, L., Gong, B., Hatala, D. A., Kern, T. S. Retinal ischemia and reperfusion causes capillary degeneration: Similarities to diabetes. Invest Ophthalmol Vis Sci. 48 (1), 361-367 (2007).
- Mizutani, M., Kern, T. S., Lorenzi, M. Accelerated death of retinal microvascular cells in human and experimental diabetic retinopathy. J Clin Invest. 97 (12), 2883-2890 (1996).
- Weerasekera, L. Y., Balmer, L. A., Ram, R., Morahan, G. Characterization of retinal vascular and neural damage in a novel model of diabetic retinopathy. Invest Ophthalmol Vis Sci. 56 (6), 3721-3730 (2015).
- Dagher, Z., et al. Studies of rat and human retinas predict a role for the polyol pathway in human diabetic retinopathy. Diabetes. 53 (9), 2404-2411 (2004).
- Podestà, F., et al. Bax is increased in the retina of diabetic subjects and is associated with pericyte apoptosis in vivo and in vitro. Am J Pathol. 156 (3), 1025-1032 (2000).
- Puro, D. G. Retinovascular physiology and pathophysiology: New experimental approach/new insights. Prog Retin Eye Res. 31 (3), 258-270 (2012).
Reprints and Permissions
Request permission to reuse the text or figures of this JoVE article
Request PermissionExplore More Articles
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. All rights reserved