16.9 : 多质子酸的滴定
多质子酸含有多种可电离氢,并采用逐步电离过程。 如果可电离质子的酸性解离常数相互之间差异很大,那么此类多质子酸的滴定曲线会为其每一个可电离氢原生成一个不同的对等点。 因此,双质子酸滴定会形成两个等效点,而三质子酸滴定会导致滴定曲线上形成三个等效点。
粘性酸 H2CO3 是弱双质子酸的一个示例。 碳酸的首次电离会产生少量的水合氢离子和碳酸二酯离子。
首次电离:
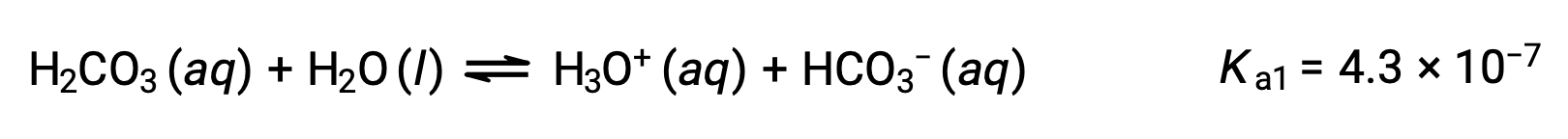
二碳酸盐离子也可用作酸。 它可以使水合氢离子和碳酸盐离子的电离和形成更小的数量。
第二次电离:
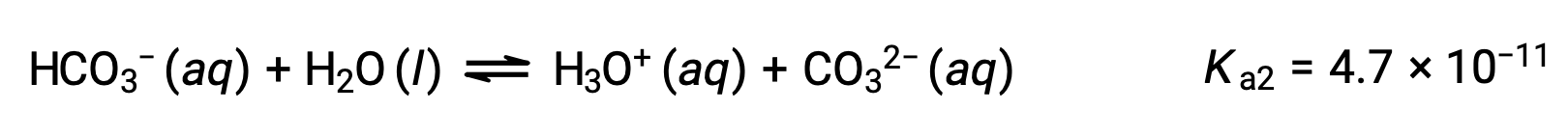
Ka1 比K2大104倍。 因此,当 H2CO3 与 NaOH 等强碱进行了分层时,它会为每一种可电离氢产生两个不同的等效点。
磷酸是一种三质子酸,电离分为三个步骤:
首次电离:
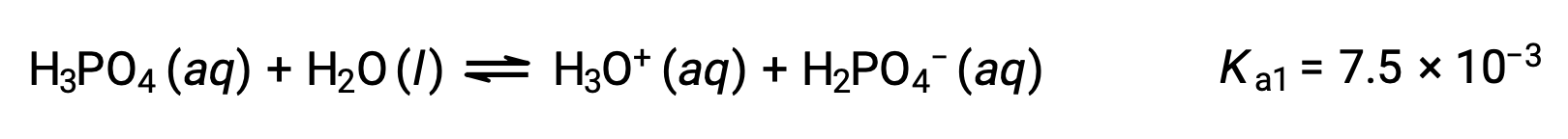
第二次电离:
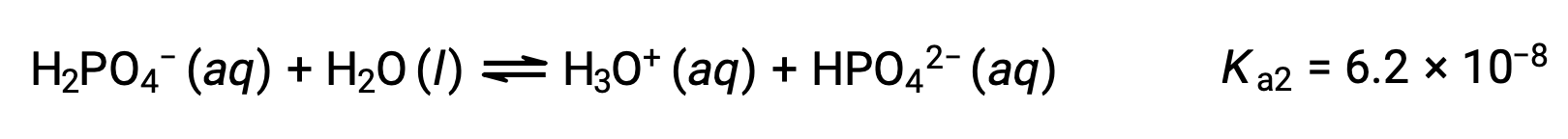
第三次电离:
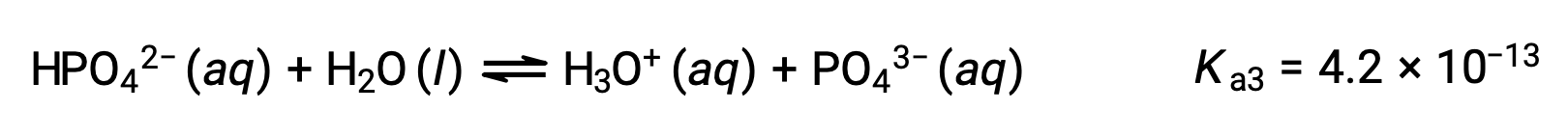
当 H3PO4 与象 KOH 这样的强碱进行了分层时,它会为每一种可电离氢产生三个等效点。 但是,由于 HPO42− 是一个非常弱酸,因此在滴定曲线上不容易识别第三个等效点。
来自章节 16:

Now Playing
16.9 : 多质子酸的滴定
酸碱和溶解度平衡
95.5K Views

16.1 : 同离子效应
酸碱和溶解度平衡
40.8K Views

16.2 : 缓冲液
酸碱和溶解度平衡
163.2K Views

16.3 : 亨德森-哈塞尔巴尔赫方程(Henderson-Hasselbalch Equation)
酸碱和溶解度平衡
67.9K Views

16.4 : 计算缓冲溶液中的 pH 值变化
酸碱和溶解度平衡
52.4K Views

16.5 : 缓冲液效力
酸碱和溶解度平衡
48.3K Views

16.6 : 滴定计算:强酸 - 强碱
酸碱和溶解度平衡
28.9K Views

16.7 : 滴定计算:弱酸 - 弱碱
酸碱和溶解度平衡
43.7K Views

16.8 : 指标
酸碱和溶解度平衡
47.6K Views

16.10 : 溶解度平衡
酸碱和溶解度平衡
51.8K Views

16.11 : 影响溶解度的因素
酸碱和溶解度平衡
32.9K Views

16.12 : 错合离子的形成
酸碱和溶解度平衡
23.0K Views

16.13 : 离子沉淀
酸碱和溶解度平衡
27.4K Views

16.14 : 定性分析
酸碱和溶解度平衡
20.0K Views

16.15 : 酸-碱 滴定曲线
酸碱和溶解度平衡
126.0K Views
版权所属 © 2025 MyJoVE 公司版权所有,本公司不涉及任何医疗业务和医疗服务。