需要订阅 JoVE 才能查看此. 登录或开始免费试用。
Method Article
布洛芬封装的输运性质环糊精Nanosponge凝胶:质子HR-MAS NMR光谱研究
* 这些作者具有相同的贡献
摘要
布洛芬包封在β环糊精纳米海绵聚合物网络的运动制度使用脉冲场梯度自旋回波(PGSE)NMR技术分析。合成,纯化,载药量,实施核磁共振脉冲序列和数据分析在几个观察时间制定出药物的均方位移的详细描述。
摘要
β环糊精(β-CD)与乙二胺四羧酸二酐(EDTA)的化学交联导致称为环糊精纳米海绵(CDNSEDTA)支化聚合物。 4和1:8的CD-EDTA的摩尔比两个不同的制剂以1所述。相应的交联的聚合物用布洛芬钠盐(IP)的主导的同质,无色,载药凝胶0.27 1M水溶液接触。
高分辨魔角旋转(HR-MAS)核磁共振光谱系统进行了表征。脉冲梯度场自旋回波(PGSE)核磁共振光谱来测定IP的聚合物凝胶内的均方位移(MSD)在不同的观察时间T d设定 。 MSD = F(T d)段 :数据以研究MSD的时间依赖关系被进一步处理。该建议的方法是表征不同的扩散制度有用,在原则上,溶质可以在水凝胶,即正常或异常的扩散内体验。全协议,包括在聚合物制备和纯化,载药凝胶的获得,该NMR样品制备,MSD的通过HR-MAS NMR谱的测定和最终数据处理实现的MSD的时间依赖性在这里报告并讨论。所呈现的实验表示一个典范壳体和数据的创新的方法来封装旅客的输运性质的表征方面用于药物递送的潜在应用的聚合物主体内讨论。
引言
有在设计和能够截留的聚合系统的配制剂的兴趣日益增长,通过非共价相互作用,小分子具有潜在生化活性。这种材料预期找到的活性成分运输至选择性目标应用程序和在外部刺激,例如pH的变化,温度, 等。在这样的背景下的动作释放,水凝胶被证明是对纳米灵活和强大的材料鉴于药物1控释的。聚合物水凝胶的形成可通过用i)物理的,非共价相互作用,如氢键,ⅱ)共价导致能够在存在膨胀的三维网络的链的交联的高分子链相互连接来实现的水溶液或iii)的两个上述方法2-4的组合。
特别多才多艺类三角钱8引起环糊精纳米海绵(CDNS) - nsional,用于有机和无机物质的封装溶胀性聚合物可以从天然β环糊精(β-CD)通过缩合具有四羧酸5的合适的,活化的衍生物开始来获得的。 CDNS的合成,表征和应用是我们小组的综合研究的主题。在过去的几年的结果表明,CDNS显示肿胀,吸收/增列化学品,以及小分子药物释放的有趣特性,在药物活性成分9控释应用- 11和环境化学12 - 14。
鉴于这些前提,两个主要的问题,以在聚合物凝胶和溶质流动在凝胶矩阵15的改进的了解来解决关注的活性化合物的有效载荷。文献同时提供了实验研究和大分子网络16,17与小分子扩散机制的理论。脉冲场梯度自旋回波(PGSE)NMR谱是广泛用于研究小分子在溶剂18中的平移扩散或纯液体的自扩散行之有效的结构的方法。最近的高分辨率魔角旋转(HR-MAS)NMR技术的发展使人们有可能收集移动分子的高分辨率核磁共振数据在异构的悬浮液19,凝胶和溶胀性聚合物20,21。事实上,实验装置结合HR-MAS核磁共振光谱和PGSE脉冲序列提供了观察主机的分子环境中的溶质分子的独特机会。因此,可以得到在凝胶基质中包裹的药物分子的输运性质的重要数据。因此高品质的实验数据可以是obtai斯内德让纳米主客体系统的设计更加合理。
在目前的工作中,我们描述了详细方案为以下步骤:i)合成和CDNS的两个不同的制剂纯化用EDTA聚合物( 图1)的交联,称为CDNSEDTA,和其特征在于由不同的CD /交联剂摩尔比率:1:4(CDNSEDTA 1:4)和1:8(CDNSEDTA 1:8);二)载药凝胶的制备CDNSEDTA 1两种:4和CDNSEDTA 1:8。在这个步骤中,我们使用作为模型药物分子,流行的非甾体抗炎布洛芬钠盐(IP);三)知识产权的CDNSEDTA内部的传输性能严查通过PGSE-HRMAS核磁共振光谱水凝胶。我们在这里提出的方法是基于在水凝胶接着将MSD的时间依赖性的分析内包封的药物的均方位移(MSD)的测量。
我们都很开心。十岁上下强调,上面概述的方法 - 这是集中在药物的的MDS矩阵中的时间依赖性 - 提供相比仅基于药物的扩散系数的测定的综合方法的信息更广泛。我们最近展示了21,允许通过IP在CDNS水凝胶密闭经历正常和反常扩散制度的歧视,这种做法。
因此,我们认为,高分子合成/净化,形成载药水凝胶,HR-MAS NMR表征和MDS数据进行数据处理,的一步一步的描述是有意刻画的纳米系统科学家强大的工具包约束和小分子的释放。
Access restricted. Please log in or start a trial to view this content.
研究方案
1. CDNSEDTA聚合物的合成
- 干β环糊精(β-CD)在烘箱中在80℃使用前4小时。 500ml干燥的二甲基亚砜(DMSO)和100毫升三乙胺(乙基3 N)在分子筛(4埃)24小时在该协议使用之前。
- 引入25毫升DMSO中入50毫升单颈圆底烧瓶中。在磁力搅拌,加5.675克β-CD(5毫摩尔)的。为了减少团块的形成,在小部分以DMSO添加β-CD粉。
- 大约30分钟后,用10毫升刻度吸管添加的Et 3 N的将6mL的均相溶液。保持在RT下搅拌15分钟下的混合物。投身烧瓶到室温水浴。
注:β-CD和EDTA之间的反应是放热的。因此,浸入烧瓶放入水浴利于热交换避免反应混合物的过热。 - 添加5.124克(20毫摩尔,准备CDNSEDT的A 1:4)或10.248克(40毫摩尔,准备CDNSEDTA 1:8)的下强烈搅拌EDTA二酐。
- 3小时后,除去固体物质(CDNSEDTA 1:4或CDNSEDTA 1:8)从使用刮刀并用研钵和研杵严重粉碎它烧瓶中。
- 在RT(100毫升×5次),用丙酮洗涤固体材料到滤纸,用HCl的0.1M(200毫升×5次)和去离子水(200ml×3次)。
- 最后,干燥全部空气中的固体材料在室温48小时,细粉碎成一个研钵和杵,然后保持真空(<15毫巴)下2小时,在45℃。
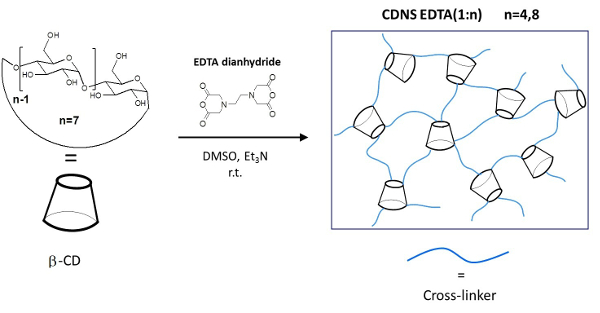
图1:该CDNSEDTA聚合物的示意图示意图合成路线。左:单体β环糊精(β-CD)和交联剂EDTA的二酐的分子结构。箭头上的整体的反应条件。对:交联聚合物的草图,请点击此处查看该图的放大版本。
2. HR-MAS NMR测量
- HR-MAS NMR样品制备
- 准备在重水(99.8%)布洛芬钠盐(IP)中的溶液0.27微米。
- 20毫克CDNSEDTA 1的添加:4和2mg无水碳酸钠( 的 Na 2 CO 3),以150微升在点2.1.1制备的溶液)到2ml玻璃小瓶中。混合用小铲将小瓶中的内容,以使之均匀。使用此过程形成的凝胶前等待2小时。重复此点,为CDNSEDTA 1:8的聚合物。
- 插入在适合于使用小刮勺的HR-MAS NMR实验采用5mm NMR转子的凝胶。凝胶使用的总量取决于转子的内部容积(推荐12微升)。
- HR-MAS 1 H-NMR实验
- 在MAS气动控制单元,在可变温度单位样品温度在305 K 4千赫的转子旋转速度:设置以下仪器参数。
- 获得在CDNSEDTA布洛芬的1 H HR-MAS NMR光谱(1:4)和CDNSEDTA(1:8),使用的质子共振的常规脉冲序列的聚合物体系。
- 创建一个新的数据集。点击"AcquPars"标签。选择PULPROG:ZG。
- 选择的扫描次数(NS = 4),并将其(D 1 = 5秒)。设置谱宽(SW = 8ppm的)之间的时间延迟,时域(TD = 16K)和所述接收器增益(RG = 32 )。
- 键入控制台上的"ZG"并且会有一个自由感应衰减(FID)在屏幕上。要处理"ProcPars"选项卡上的数据点击。设置的光谱的大小(SI = 32K),一个指数乘法窗口函数(WDW = EM)和线展宽(LB = 1)。键入"FT"来执行傅立叶变换。相使用屏幕上的相位片的光谱。获取高分辨率很好地解决频谱。

图2:双极脉冲对纵向涡流延迟(BPPLED)脉冲序列用于进行PFGSE实验脉冲序列的示意图。对于90°脉冲的相位周期是:P1:(0)16,P2:(0022)4,P 3:(0)4(2)4(1)4(3)4,P4:(0202 2020 1313 3131 ),P5:(0)4(2)4(1)4(3)4。 180°脉冲+ X。 (从ref.18修改) 点击此处查看该图的放大版本。
- HR-MAS 1 H-NMR实验PGSE
注意:使用在图 2中所报告的BPPLED脉冲序列18执行的PGSE实验。这是一个伪二维实验用梯度的斜坡的2%,在间接尺寸线性增加至100%。取决于扩散时间Δ和梯度脉冲δ的信号强度被衰减。这些参数的优化运行正确一个PGSE实验前是必需的。该优化是通过运行在其中Δ保持恒定几个1D测量完成,而δ是多种多样的。- 参数优化
- 创建一个新的数据集 - 实验编号1.单击"AcquPars"标签。选择PULPROG:ledbpgp2s1d扩散优化1D脉冲序列。
- 选择(NS = 16)扫描的数目和它们之间的时间延迟(D1 = 10秒)。设置的光谱宽度(SW = 8ppm的),叔他的时域(TD = 16K)和所述接收器增益(RG = 32)。
- 设置Δ等于恒定值和δ(P30)到试验值(该序列中D20)。启动值Δ= 50毫秒,δ(高分辨率仪器最大允许值)= 3毫秒。
- 读谱频率(SFO1)的,由1 H实验值和现在使用此值。设置GPZ6梯度强度至2%。重复步骤2.2.2.3。使用这个频谱作为用于优化参考。
- 在同一数据集建立实验号2.遵守所有的实验参数。增加GPZ6梯度强度至95%。重复步骤2.2.2.3。使用双显示图标比较该光谱与参考光谱和观察的信号强度的变化。
注:与参考频谱相比,减毒以及频谱应该有大约5%的残余信号强度。如果信号强度丢失,降低的δ和水库的值直到δ正确的价值被发现从点2.3.1.3挞的第2.3.1节的过程。 - 重复第2.3.1节中的参数优化程序为所有五个Δ值。
注:选择Δ= 50,80,110,140 5值和170毫秒和优化相应δ3,2.7,2.4,2.1,1.8毫秒(知识产权在CDNSEDTA 1:8)和成δ至2.7,2.4 2,1.7,1.4(知识产权在CDNSEDTA 1:4)。
- 二维扩散数据集采集
- 在相同的数据集创建实验编号3中,所有的1D实验参数将被加载。键入"EDA"。选择PULPROG:ledbpgp2s二维脉冲序列,改变parmode为2D。
- 设置FnMODE = QF。设置的时间域的TD在F2中尺寸等于32的梯度步骤的数目。所有其他的参数设置是否正确。输入"DOSY"和梯度的斜坡将被生成并存储在一个文件中。圣艺术和斜坡(2 - 95)的最终值给出作为输入参数。此次收购已启动。
- 参数优化
- 数据处理
- 键入"XF2"中的F2维度来执行傅立叶变换。键入"ABS2"在F2尺寸进行基线校正。类型"setdiffparm"召回实验参数(Δ,δ,和梯度清单)为下一个处理步骤。
- 在分析标签点击"的T1 / T2弛豫模块",并定义使用2D实验的第一频谱嵌合的峰值。定义峰值范围和执行拟合。获得在每个施加梯度步骤的信号强度。
注意:信号强度I(Q,T d)中 ,对于每个Δ值,取决于实验变量:根据施加脉冲日提交的梯度(克),时间变量(δ),magnetogyric比(γ)Q =(γgδ)在FOllowing公式:
与分子的MSD = Z 2。 - 导出的信号强度在电子表格中,并执行该数据的线性拟合,以获得Z 2的值对每一个观察到的扩散时间td。
注:MSD值与根据观测时间t D:
- 执行Z 2对T d设定的每个实验T d设定值数图。指数α值是线性回归的斜率。上述报道方程的物理方面更为详尽的讨论可以在文献中找到。 21,并在其中的参考文献。
注意:根据指数α的值,扩散机制的定义是:i)在α= 1,ⅱ)异常subdiffusiv各向同性无限制扩散0 <α<1,III)异常superdiffusive为α> 1政权Ë制度。
Access restricted. Please log in or start a trial to view this content.
结果
我们首先应用这个方法,以溶解在水中的溶液,以验证这种方法的可行性的IP药物分子。代表结果的完整描述可以在文献中找到。 21.相反,我们将在这里集中在方法学方面,螺母和螺栓的方式进行数据收集和数据分析。 如图3所示,在一个半对数刻度,标准化的实验信号衰减I(Q,T D) / I(0,T D)为q 2的功能(根据第2.4节)。?...
Access restricted. Please log in or start a trial to view this content.
讨论
我们提出了一个实验方法来确定封装内CDNSEDTA水凝胶的两个有代表性的剂型有小毒分子的扩散制度。 HR-MAS PGSE核磁共振允许在给定的扩散时间的小分子的均方位移的确定(在几毫秒的上升到第二范围内),在微米尺度然后监测距离。中观察到的范围内(50 - 170毫秒)只有一种类型的运动的观察对每个研究的系统。然而,应当强调的是,更长的观察时间不同的扩散制度之间的过渡,可以观察到22...
Access restricted. Please log in or start a trial to view this content.
披露声明
The authors have nothing to disclose.
致谢
The authors gratefully acknowledge PRIN 2010-2011 NANOMED prot. 2010 FPTBSH and PRIN 2010-2011 PROxy prot. 2010PFLRJR_005 for funding.
Access restricted. Please log in or start a trial to view this content.
材料
| Name | Company | Catalog Number | Comments |
| HR-MAS probe | BRUKER | N/A | Probe for NMR measurements on semi-solid samples |
| NMR Spectrometer | BRUKER | DRX 500 | FT NMR spectrometer for liquid ans semi-solis state |
| β-cyclodextrin (β-CD) | Alfa-Aesar | J63161 | Reagent |
| Ethylenediaminetetracetic (EDTA) dianhydride | Sigma-Aldrich | 332046 | Reagent |
| Dimethylsulfoxide (DMSO) | Alfa-Aesar | D0798 | Solvent |
| Triethylamine | Sigma-Aldrich | 471283 | Base (reagent) |
| Ibuprofen (IP) sadium salt | Sigma-Aldrich | I1892 | Antinflammatory drug |
| Excel 2010 | Microsoft | N/A | speadsheet for data analysis |
| Origin 8 SR0 | OriginLab Co. | speadsheet for data analysis |
参考文献
- Sharpe, L. A., Daily, A. M., Horava, S. D., Peppas, N. A. Therapeutic applications of hydrogels in oral drug delivery. Expert Opin. Drug Deliv. 11, 901-915 (2014).
- Hennik, W. E., van Nostrum, C. F. Novel crosslinking methods to design hydrogels. Adv. Drug Deliv. Rev. 54, 13-36 (2002).
- Yu, L., Ding, J. D. Injectable hydrogels as unique biomedical materials. Chem. Soc. Rev. 37, 1473-1481 (2008).
- Ma, M., Kuang, Y., Gao, Y., Zhang, Y., Gao, P., Xu, B. Aromatic-Aromatic Interactions Induce the Self-Assembly of Pentapeptidic Derivatives in Water To Form Nanofibers and Supramolecular Hydrogels. J. Am. Chem. Soc. 132, 2719-2728 (2010).
- Trotta, F., Tumiatti, W. Patent WO. , 03/085002 (2003).
- Trotta, F., Tumiatti, W., Cavalli, R., Zerbinati, O., Roggero, C. M., Vallero, R. Ultrasound-assisted synthesis of cyclodextrinbased nanosponges. Patent WO. , 06/002814 (2006).
- Trotta, F., Cavalli, R. Characterization and applications of new hyper-cross-linked cyclodextrins. Compos. Interface. 16, 39-48 (2009).
- Cavalli, R., Trotta, F., Tumiatti, W. Cyclodextrin-based nanosponges for drug delivery. J. Incl. Phenom. Macrocycl. Chem. 56, 209-213 (2006).
- Trotta, F., et al. Cyclodextrin-based nanosponges as a vehicle for antitumoral drugs. Patent WO. , 09/003656 (2009).
- Vyas, A., Shailendra, S., Swarnlata, S. Cyclodextrin based novel drug delivery systems. J. Incl. Phenom. Macrocycl. Chem. 62, 23-42 (2008).
- Swaminathan, S., Vavia, P. R., Trotta, F., Torne, S. Formulation of beta-cyclodextrin based nanosponges of itraconazole. J. Incl. Phenom. Macrocycl. Chem. 57, 89-94 (2007).
- Mamba, B. B., Krause, R. W., Malefetse, T. J., Gericke, G., Sithole, S. P. Cyclodextrin nanosponges in the removal of organic matter to produce water for power generation. Water SA. 34, 657-660 (2008).
- Mamba, B. B., Krause, R. W., Malefetse, T. J., Nxumalo, E. N. Monofunctionalized cyclodextrin polymers for the removal of organic pollutants from water. Environ.Chem. Lett. 5, 79-84 (2007).
- Mhlanga, S. D., Mamba, B. B., Krause, R. W., Malefetse, T. J. Removal of organic contaminants from water using nanosponge cyclodextrin polyurethanes. J. Chem. Technol. Biot. 82, 382-388 (2007).
- Lehmann, S., Seiffert, S., Richtering, W. Spatially Resolved Tracer Diffusion in Complex Responsive Hydrogels. J. Am. Chem. Soc. 134, 15963-15969 (2012).
- Ferrer, G. G., Pradas, M. M., Ribelles, J. L. G., Colomer, F. R., Castilla-Cortazar, I., Vidaurre, A. Influence of the nature of the porous confining network on the sorption, diffusion and mechanical properties of hydrogel IPNs. Eur. Polym. J. 46, 774-782 (2010).
- Santoro, M., Marchetti, P., Rossi, F., Perale, G., Castiglione, F., Mele, A., Masi, M. Smart approach to evaluate drug diffusivity in injectable agar-carbomer hydrogels for drug delivery. J. Phys. Chem B. 115, 2503-2510 (2011).
- Johnson, C. S. Diffusion ordered nuclear magnetic resonance spectroscopy: principles and applications. Prog. Nucl. Magn. Reson. Spectroscopy. 34, 203-256 (1999).
- Viel, S., Ziarelli, F., Caldarelli, S. Enhanced diffusion-edited NMR spectroscopy of mixtures using chromatographic stationary phases. Proc. Natl. Acad. Sci. U. S. A. 100, 9696-9698 (2003).
- Alam, T. M., Hibbs, R. M. Characterization of heterogeneous solvent diffusion environments in anion exchange membranes. Macromolecules. 47, 1073-1084 (2014).
- Ferro, M., Castiglione, F., Punta, C., Melone, L., Panzeri, W., Rossi, B., Trotta, F., Mele, A. Anomalous diffusion of Ibuprofen in cyclodextrin nanosponges hydrogels: an HR-MAS NMR study. Beilstein J. Org. Chem. 10, 2715-2723 (2014).
- Wolf, G., Kleinpeter, E. Pulsed Field Gradient NMR Study of Anomalous Diffusion in a Lecithin-Based Microemulsion. Langmuir. 21, 6742-6752 (2005).
- Rossi, F., Castiglione, F., Ferro, M., Marchini, P., Mauri, E., Moioli, M., Mele, A., Masi, M. Drug-Polymer interactions in hydrogel-based drug-delivery systems: an experimental and theoretical study. Chem. Phys. Chem. , (2015).
Access restricted. Please log in or start a trial to view this content.
转载和许可
请求许可使用此 JoVE 文章的文本或图形
请求许可探索更多文章
This article has been published
Video Coming Soon
版权所属 © 2025 MyJoVE 公司版权所有,本公司不涉及任何医疗业务和医疗服务。