Method Article
简捷方法对硫甙的提取与分析用高压液相色谱法(HPLC)
摘要
Here, we describe in great detail an established and robust protocol for the extraction of glucosinolates from ground plant materials. After an on-column sulfatase treatment of the extracts, the desulfoglucosinolates are eluted and analyzed by high-pressure liquid chromatography.
摘要
Glucosinolates are a well-studied and highly diverse class of natural plant compounds. They play important roles in plant resistance, rapeseed oil quality, food flavoring, and human health. The biological activity of glucosinolates is released upon tissue damage, when they are mixed with the enzyme myrosinase. This results in the formation of pungent and toxic breakdown products, such as isothiocyanates and nitriles. Currently, more than 130 structurally different glucosinolates have been identified. The chemical structure of the glucosinolate is an important determinant of the product that is formed, which in turn determines its biological activity. The latter may range from detrimental (e.g., progoitrin) to beneficial (e.g., glucoraphanin). Each glucosinolate-containing plant species has its own specific glucosinolate profile. For this reason, it is important to correctly identify and reliably quantify the different glucosinolates present in brassicaceous leaf, seed, and root crops or, for ecological studies, in their wild relatives. Here, we present a well-validated, targeted, and robust method to analyze glucosinolate profiles in a wide range of plant species and plant organs. Intact glucosinolates are extracted from ground plant materials with a methanol-water mixture at high temperatures to disable myrosinase activity. Thereafter, the resulting extract is brought onto an ion-exchange column for purification. After sulfatase treatment, the desulfoglucosinolates are eluted with water and the eluate is freeze-dried. The residue is taken up in an exact volume of water, which is analyzed by high-pressure liquid chromatography (HPLC) with a photodiode array (PDA) or ultraviolet (UV) detector. Detection and quantification are achieved by conducting comparisons of the retention times and UV spectra of commercial reference standards. The concentrations are calculated based on a sinigrin reference curve and well-established response factors. The advantages and disadvantages of this straightforward method, when compared to faster and more technologically advanced methods, are discussed here.
引言
据估计,植物产生超过20万不同类型的化合物1。只有这些化合物的少数人似乎发挥植物的初级代谢,其中燃料的生长繁殖的作用;多数是所谓的次级代谢产物。尽管他们的名字,次生代谢产物往往是植物生存和繁殖至关重要,因为它们有助于吸引授粉或抵御病原体和食草动物1工厂。
芥子油苷是一个非常多元化的类,已经研究了超过150年2次生代谢产物。迄今为止,130多个结构不同的硫代葡萄糖苷已经确定3。广义地说,硫代葡萄糖苷可以细分成基于从它们所合成的氨基酸上不同的类。吲哚芥子油苷,例如,从氨基酸合成色氨酸,而苯丙氨酸为芳香族硫甙4的合成的基本骨架。中的类,有结构的多样性,这是由在生物合成途径顺序链延伸的步骤,如在类脂肪族硫代葡萄糖苷的带来的,或由侧链修饰(如羟基化)4,5的一个高的水平。其中硫甙的植物物种可能包含属于不同结构类型6多达37种不同的硫代葡萄糖苷。尽管植物具有典型的硫甙配置文件,该类型的硫代葡萄糖苷种内变异个体和群体6,7中经常发现。完好苷存储在植物细胞的液泡,并且可以在任何地上或地下器官7可以发现,<SUP类="外部参照"> 8,9。当细胞破裂(如通过取食),硫甙被释放,并与酶的黑芥子酶混合,掀起了芥末油弹10。由于黑芥子酶的活性,并根据不同的芥子油苷,反应条件,和修饰酶的存在的结构中,形成不同的刺激性,毒性或有害化合物,例如腈和(异)硫氰酸11。反应产物具有高生物活性;例如,它们充当多面手植食性昆虫12的驱虫剂。硫代葡萄糖苷的遗传和生物合成途径是很好的研究,主要是因为它们对草食动物和病原体的抵抗力,它们的值作为芥末白菜和香味成分,其负(progoitrin)和对人体健康的5阳性(葡萄糖萝卜硫苷)的影响的重要性, 13,14。
因为在硫代葡萄糖苷作为基于反相高压液相色谱(HPLC)配备有紫外(UV)或光电二极管阵列的生物活性化合物,提取和检测方法的极大的兴趣(PDA)检测器已被广泛自20世纪80年代15使用。基于该方法,欧洲共同体发出被用于芥子油苷的油籽分析( 欧洲油菜 ,菜籽,油菜籽16)测试和验证在几个实验室的标准协议。他人加入到这一方法( 例如,通过确定不在油菜本苷附加响应因子)17。尽管液相色谱-质谱(LC-MS)的平台和高通量协议芥子油苷分析18中的增加的可用性P>,19日 ,原HPLC-UV / PDA方法仍然被广泛用科学家使用。其主要原因是,这种方法很简单,性价比高,而且相对访问实验室没有一个广泛的化学分析知识基础设施。为了服务于这个社会,我们在这里详细的协议硫代葡萄糖苷从植物原料提取和他们desulfo表单与HPLC-PDA进行分析。
研究方案
1.溶液的制备所需硫甙提取
- 在玻璃瓶中制备在水500毫升70%甲醇(MeOH)的(超纯)。对100个样品和5标准,420毫升70%是必要的MeOH。
- 加入0.82克醋酸钠或1.36克醋酸钠×3 h及准备20 mM醋酸钠(醋酸钠)(pH值= 5.5)2 O在500毫升的水;调节pH值用氯化氢(HCl)。在冰箱里存放的醋酸钠。对于需要100个样本和5个标准,水370毫升20毫米醋酸钠(pH值= 5.5)的。
- 为了制备柱材料,混合10克交联葡聚糖凝胶(类型G-25)用125毫升的超纯水的。储存在冰箱(4℃)将所得混合物。
- 所述硫酸溶液的制备
- 在30mL的超纯水溶解10,000单位芳硫酸酯酶(类型H-1从罗马蜗牛 ),并添加30毫升的无水乙醇(乙醇)。混合溶液很好,并将其传输给一个250毫升岑trifuge管或多个更小的管子,视情况而定。
- 离心混合物2,650×g离心,在室温(RT)下20分钟。转移上清液(S)到一个烧杯中;添加90毫升乙醇中,并混合。离心该混合物在一个或多个离心管在1,030×g离心在RT 15分钟。
- 弃去上清液。溶解并在总共25毫升的超纯水的结合的颗粒。涡好,取1毫升管,并存储在冷冻在-20℃;他们会保持在至少一年。
- 该sinigrin对照品溶液的制备
- 称重在大约9毫克sinigrin一水合物与1-微克精度( 例如,8.769毫克)。转移它到10-mL容量瓶中溶解sinigrin一水合物在10.0毫升的超纯水。
- 计算股票溶液的摩尔浓度和由储液稀释制备50-750微米之间的五个sinigrin引用。为详细的例子,见 补充文件S1 。
- 分配在1.5毫升反应管不同sinigrin引用和在20℃下冷冻。包括一系列在每个提取批次5 sinigrin引用。计算浓度时,必须使用正确的摩尔浓度值,当前使用的sinigrin引用。
2.提取安装的制备
- 准备用于巴斯德吸管列一列搁架(用于柱的制备,参见步骤3.1)。标号齿条或列来跟踪样品编号(参见图1)。
- 制备保持相同数量的标记的2-ml微量离心管的一个块(参见步骤3.3和图1)
5 / 55425fig1.jpg"/>
图1:机架甙提取。正视图(左)和一个自制柱架和块的芥子油苷的提取的俯视图(右侧)。高度:100毫米,间距错开孔(保持巴斯德吸管列):30毫米(x轴)×15毫米(y轴)。 请点击此处查看该图的放大版本。
3.列和离心管的制备
- 制备每个样品一列的五个sinigrin参照样品五个额外的列。
- 在每个玻璃吸管将一块玻璃纤维大约1厘米长×1厘米。使用木制或玻璃棒推玻璃棉向下到移液器变窄的点。玻璃棉应防止柱的材料从跑出来,但不使用过多,因为它会减缓列的溶出。戴上手套Wh是带玻璃棉工作。
- 放置在柱架的列(参见图1)。将在实验室托盘(废盘)列机架赶用于连续列洗淋洗液。
- 切断第一5毫米关闭的塑料1毫升枪头和吸管0.5毫升制备的柱材料的前端(G-25的凝胶在水,见步骤1.3)到每一列。含摇柱材料以及吸取之前的瓶子。丢弃泄漏列(通过玻璃棉层不多了G-25材料),并更换新的。
- 柱材料吹打入列之后,加入1毫升的超纯水冲洗下来的材料。
- 制备每采样1 2毫升反应管和五个sinigrin参考样品5管;贴上标签。用解剖针使在帽购买冷冻干燥孔和放置准备好的管到管块中的精确相同的图案的列(步骤2.2,参见图1)。
4.硫甙的提取
- 称重冻干和精细研磨的植物材料(通常为50.0-100.0毫克干重的;在提取物中的最终芥子油苷的浓度应在基准曲线的范围内),精确到0.1毫克的2-毫升,标记,圆汉字反应管。两个小金属球(直径3mm),为沸点阻燃剂到每个管中。
注:该协议也可以应用到新鲜,快速冷冻材料,已在液氮下研磨并冷冻保存,直至萃取。增加材料的称重提取在提取液中的量和MeOH的比例至85%的水在材料19,以补偿稀释。 - 吸取1毫升70%甲醇的每管和旋涡简要介绍。关闭管和将它们尽可能快地成热前W与安全帽它们密封亚特浴(90-92℃)几分钟(〜5分钟),直到70%的MeOH刚刚沸腾。注意:在此步骤中佩戴安全护目镜!
- 将样品管在15分钟的超声浴。同时,采取硫酸和五sinigrin参考样品从冰箱到室温解冻它们。
- 超声波处理后,离心2,700 xg离心样品管在台式离心机在室温下10分钟;粒料应该形成在每个管中。上清液加入标记列和吸取的五个标准样品到单独列。
- 同时吸取上清液,保持尖端超过颗粒,以免吸取植物材料。需要注意的是使用干燥的样品时,将上清液体积将小于1.0毫升。
- 加入1毫升70%的MeOH在样品管中的剩余的颗粒和将它们放置在超声浴中15分钟,然后涡管中。再次离心管,如在步骤4.4,并添加supernatants到相应的列;由于列材料的性能,在硫代葡萄糖苷的带负电荷的硫酸酯基团进行具体保留在柱上。
- 在三个顺序步骤的萃取液洗柱。
- 吸管2×1毫升70%的MeOH的到每一列。等待列添加下一个1毫升之前运行干燥;这将从提取物(如叶绿素)去除更多非极性化合物。
- 通过加入1毫升的超纯水对每一列冲洗掉MeOH中。
- 吸管2 20×1毫升毫醋酸钠缓冲液,以每一列来为硫酸反应的最佳条件。
- 采取与列齿条出废物托盘的并用纸巾擦干机架的脚。将在与小瓶和标记的管块机架。确保每个柱尖端在相应的,标记的,2-mL管中(参见图1)。
- 添加硫酸soluti的20微升上的列。确保硫酸到达柱材料的表面上。移液器50醋酸钠的缓冲微升到每个柱冲洗下来的硫酸。用铝箔覆盖的列,静置过夜。
注意:由于在硫酸酯酶的活性,硫酸基将被删除,释放从柱中desulfoglucosinolates以便它们可以与水洗脱。有关详细说明,请参见Crocoll 等。 19。 - 第二天,通过吸取2×0.75毫升的超纯水到每个柱洗脱desulfoglucosinolates。当所有列都干涸,提起柱架,并从反应管中取出。
- 盖上管(确保有在帽空穴)和冻结他们在液氮中或在-80℃冷冻30分钟。冷冻干燥的样品12-24小时(取决于样品的数量和冷冻干燥器的能力),以除去所有的水。
<利>冷冻干燥后,在超纯水中的精确体积(通常为1.0毫升)重新溶解残留物。转移的样品和五个sinigrin引用标记的HPLC小瓶。保持样品在长达两周冰箱(4℃)或冷冻(-20℃)为最多一年利用HPLC分析它们。 - 让引擎盖下的玻璃柱干通宵干燥时处理掉。恢复从步骤4.5重用使用的样品管的金属球,并把管道中的垃圾处理箱。
5.提取样品测定高效液相色谱法
- 分离在反相C18柱(4.6×150毫米,3微米,300埃)用乙腈-水梯度的硫代葡萄糖苷( 见表1)和0.75毫升/分钟的流速和40℃的柱温。在229处执行的检测和定量。
- 测量在同一列,但具有适于梯度sinigrin引用方法,以减少溶剂使用( 见表2)。开始与注射五sinigrin引用,用最低浓度的参考开始。然后注入样本,包括每个样本第十一个后注入甲醇(空白)清洗柱,防止峰的结转。
| 时间[分钟] | 流[毫升/分钟] | % 一杯水 | %B ACN |
| 1 | 0.750 | 98 | 2 |
| 35 | 0.750 | 65 | 35 |
| 40 | 0.750 | 98 | 2 |
| 柱温度40℃。 | |||
表1:乙腈-水梯度进行芥子油苷的分离和analysiS于反相HPLC。
| 时间[分钟] | 流[毫升/分钟] | % 一杯水 | %B ACN |
| 1 | 0.750 | 98 | 2 |
| 10 | 0.750 | 89.3 | 10.7 |
| 11 | 0.750 | 98 | 2 |
| 柱温度40℃。 | |||
表2:缩短乙腈-水梯度为用于芥子油苷的量化的五个sinigrin引用的定量。
6.硫代葡萄糖苷鉴定和定量
- 鉴定
- 比较峰的UV光谱和保留时间与市售果样品中能,纯硫甙引用。参见图2为从各种芥子油苷类UV光谱的例子。
- 识别未知苷参考标准或LC-MS 18,19,如果可能的话。
- 识别未知苷用核磁共振(NMR),如果可能的话。
- 与那些在图2和表3,数据库或文献参考比较峰的UV光谱和保留时间。
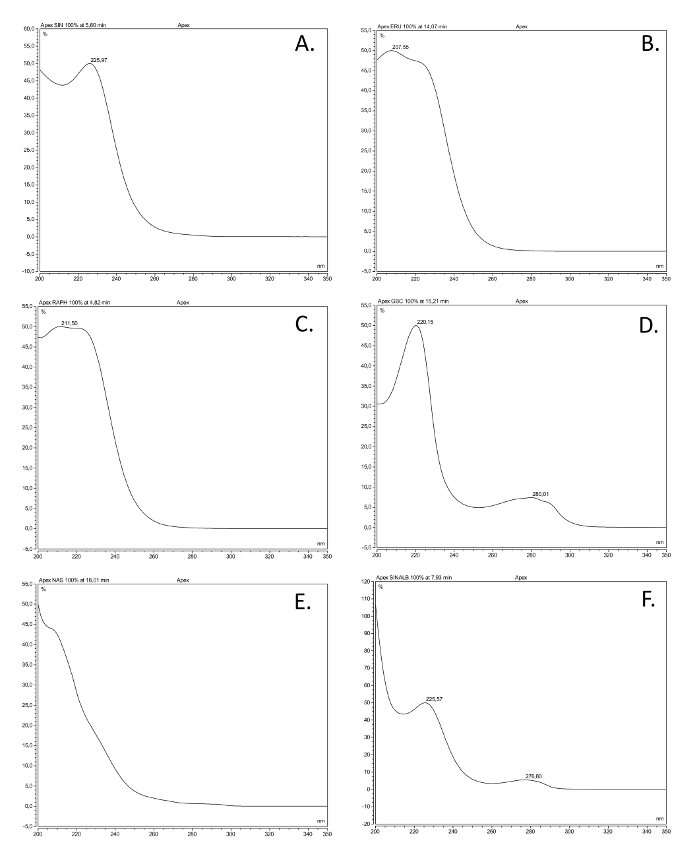
图2中最常见的芥子油苷类的UV光谱。六desulfoglucosinolates(GSL)紫外吸收光谱(200-350纳米)的基础上,提出这里描述,代表着最常见的结构类中提取的市售参考化合物的溶液。共同的名字,Structural名称(括号之间),和结构类中给出。 (A)中Sinigrin(2-丙烯基GSL),链烯基; (B)glucoerucin(4-甲硫基丁基GSL),thioalkenyl; (C)葡萄糖萝卜硫苷(4-methylsulfinlybutyl GSL),亚硫酰基; (D)的glucobrassicin(吲哚-3-基甲基GSL),吲哚; (E) - gluconasturtiin(2-苯乙基GSL),芳香族; (F)sinalbin(4-羟基苄GSL),芳族的。 请点击此处查看该图的放大版本。
- 量化
- 五个sinigrin引用和样品的峰下整合的区域。
- 计算基于所述积分面积的五个测量sinigrin引用的校准曲线。使用回归直线的方程(参见方程1)计算苷(见公式2)的内插数量。
- 计算不同芥子油苷的浓度,从EC乘以用于检测的响应因子(M)内插量(x)在229纳米(1990)16,布氏(1987)15,或Brown 等人。 (1993)17;最常检测desulphoglucosinolates的共有响应因子在表3中给出。
注:响应因素可能会有所不同的系统,这可能是原因,有不同的引用给定不同的值(请参阅参考资料15-17)。然而,这些值大多是相当接近,并以类似的范围具有结构类。以下惯例,不明芥子油苷的响应因子设置为1,虽然具有类似于glucobrassicin和其他吲哚芥子油苷( 图2)的UV光谱未知吲哚芥子油苷,这将是最好使用0.25作为响应因子,以获得浓度的实际的估计( 见表3)。 - 计算硫代葡萄糖苷的样品中的最终量(X t)的 ,取用于分析考虑稀释因子(D)和样品的质量(重量)(见公式3)。
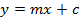 (1)
(1) 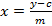 (2)
(2) 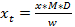 (3)
(3)
Y =峰面积
基准5点回归曲线的M =斜率
C =与y轴的回归直线的截距
X =提取物中的硫苷的量
x深=硫代葡萄糖甙的植物样品浓度
D =稀释因子
M =响应因子为在229纳米从布氏(1987)或Brown 等人的检测。 (1993)
W =样品的质量用于萃取
结果
这种方法能够检测和在所有的结构类通常发现desulfoglucosinolates分离( 图3)。有害-2- hydroxyglucosinolate progoitrin进来色谱相对早,显然从有利甙葡萄糖萝卜硫苷,在这种样品中的唯一methylsulfinylglucosinolate分离。 Sinigrin,gluconapin和glucobrassicanapin形成具有增加的侧链长度(C3,C4,和C5,分别地)的eluotropic系列烯硫代葡萄糖苷。类似的逻辑系列是可见的两个methylthioalkenyl硫代葡萄糖苷,glucoiberverin(C3)和glucoerucin(C4)。三吲哚芥子油苷,glucobrassicin的和4-羟基和1- methoxyglucobrassicin(neoglucobrassicin)的峰及其衍生物,也明确分开。应当指出的是neoglucobrassicin和glucoerucin的峰,以及gluconasturtiin,唯一的芳香族葡糖sinolate此示例中,是在该芸苔属提取物特别高由于加入根提取物的组合9。
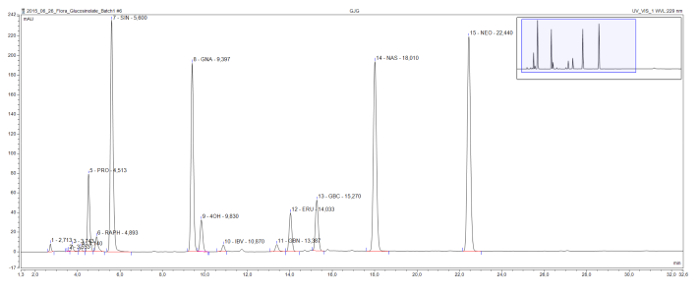
图3:芥子油苷提取物的色谱图。从黑芥结合根冠样本,白菜和 甘蓝的分析产生的HPLC色谱图的详细信息(1-32分钟)。该峰标签注明的保留时间和认定desulfoglucosinolates缩写(GSL)。 PRO = progoitrin(2-OH-3-丁烯基GSL); RAPH =葡萄糖萝卜硫苷(4-methylsulfinlybutyl GSL); SIN = sinigrin(2-丙烯基GSL),GNA = gluconapin(3-丁烯基GSL); 4OH = 4- hydroxyglucobrassicin; IBV = glucoiberverin(3-甲硫基丙基GSL); GBN = glucobrassicanapin(4-戊GSL); ERU = glucoerucin(4-甲硫基丁基GSL); GBC = glucobrassicin(吲哚-3-基甲基GSL); NAS = gluconasturtiin(2-苯乙基GSL); NEO = neoglucobrassicin(1-甲醇 - glucobrassicin)。 请点击此处查看该图的放大版本。
较长链的甲基亚硫苷,其在模式植物拟南芥中常见的,也显示出eluotropic系列,如在奥地利葶苈的根提取物可见。 Glucohesperalin(C 6),glucosiberin(C7),glucohirsutin(C8),和glucoarabin(C9)出现在色谱图上( 图4)定期。与峰的UV光谱一起,例如eluotropic逻辑系列可被用来进行分类,并暂时识别,未知芥子油苷。
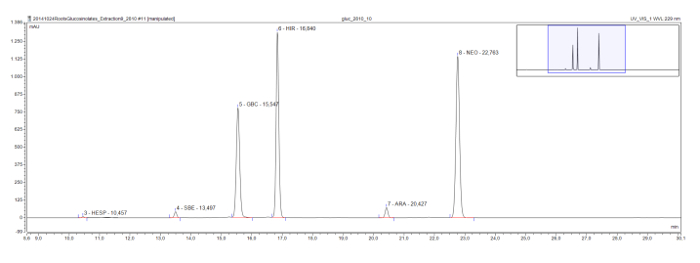
图4:色谱(帧9-30分钟)在奥地利葶苈根提取物的desulfoglucosinolates的。该峰标签注明的保留时间和认定desulfoglucosinolates缩写(GSL)。 HES = glucohesperin(6 methylsulfinylhexyl GSL); SBE = glucosiberin(7 methylsulfinylheptyl GSL); GBC = glucobrassicin(吲哚-3-基甲基GSL); HIR = glucohirsutin(8 methylsulfinlyoctyl GSL); ARA = glucoarabin(9- methylsulfinylnonylglucosinolate); NEO = neoglucobrassicin(1-甲醇 - glucobrassicin)。 请点击此处查看该图的放大版本。
| 统称 | 侧链结构 | RT(分钟)* | 229纳米 | 参考# |
| aliphatiç硫代葡萄糖苷 | ||||
| Glucocapparin | 甲基 | 3.5 | 1 | 棕色 |
| Sinigrin | 2-丙烯基 | 5.5 | 1 | 布朗,EC |
| Gluconapin | 3-丁烯基 | 9.5 | 1.11 | EC |
| Glucobrassicanapin | 4-戊烯基 | 13.5 | 1.15 | EC |
| Glucoiberverin | 3甲硫 | 10.9 | 0.8 | 棕色 |
| Glucoerucin | 4,甲硫基丁基 | 14.0 | 0.9 | 棕色 |
| Glucoiberin | 3 methylsulfinylpropyl | 3.7 | 1.2 | 棕色 |
| 葡萄糖萝卜硫苷 | 4 methylsulfinylbutyl | 4.9 | 0.9 | 棕色 |
| Glucoalyssin | 5 methylsulfinylpentyl | 7.6 | 0.9 | 棕色 |
| Glucohesperin | 6 methylsulfinylhexyl | 10.5 | 1 | 棕色 |
| Glucosiberin | 7 methylsulfinylheptyl | 13.5 | 1 | 棕色 |
| Glucohirsutin | 8 methylsulfinyloctyl | 16.8 | 1.1 | 棕色 |
| Glucoarabin | 9 methylsulfinylnonyl | 20.5 | 1 | |
| Glucocheirolin | 3 methylsulfonylpropyl | 4.2 | 0.9 | 棕色 |
| Progoitrin | -2(R)-OH -3-丁烯基 | 4.5 | 1.09 | 布氏,EC |
| Gluconapoleiferin | 2-OH-5-戊烯基 | 8.3 | 1 | EC |
| 吲哚硫甙 | ||||
| 4 hydroxyglucobrassicin | 4-羟基吲哚-3-基甲基 | 11.2 | 0.28 | 布氏,EC |
| Glucobrassicin | 吲哚-3-基甲基 | 15.3 | 0.29 | 布氏,EC |
| 4 Methoxyglucobrassicin | 4-甲氧基-3-甲基 | 18.2 | 0.25 | 布氏,EC |
| Neoglucobrassicin | 1-甲氧-3-基甲基 | 22.5 | 0.2 | 布氏,EC |
| 芳香硫代葡萄糖苷 | ||||
| Sinalbin | 4-羟基苄基 | 8.1 | 0.5 | 布氏 |
| Glucosibarin | -2(R)-OH -2-苯乙基 | 12.1 | 0.95 | 看下 |
| Glucobarbarin | -2(S)-OH -2-苯乙基 | 12.7 | 0.95 | 布氏 |
| Glucotropaeolin | 苄 | 13.8 | 0.95 | 布氏,EC |
| Gluconasturtiin | 2-苯乙基 | 18.0 | 0.95 | 布氏,EC |
| 未知-脂肪/芳香像紫外光谱 | 1 | EC | ||
| 未知-吲哚样谱 | 0.25 | EC | ||
| *近似保留时间(RT)四舍五入到最接近的0.1分钟(±0.3分钟取决于柱,洗脱剂质量)。保留时间在配备有C18柱(150×4.6毫米,3微米粒度)和C 18赛默飞/戴安终极性HPLC平台确定预柱(10×4.6毫米,5微米颗粒尺寸)用梯度程序如表1。 | ||||
| #参考响应因子:油菜籽布氏,R.在芥子油苷(ED JP Wathelet)50-58(马丁努斯Nijhoff出版社,1987年);布朗,PD,Tokuhisa,JG,艾香德,M.&赫尔申宗,不同的器官和拟南芥的发育阶段中硫甙的积累J.变化。植物化学。 62(3),471-481,DOI:10.1016 / S0031-9422(02)00549-6,(2003); EC。油菜籽 - 葡萄糖甙测定高效液相色谱法。官方公报欧洲共同体。大号二十八分之一百七十○。附件八03.07.27-34(1990年)。 | ||||
表3:响应因子中最常见的desulfo-苷植物提取物和它们的近似的保留时间上-C 18列。洗脱液,gradienT,柱温度和流速如表1。
讨论
这种建立并广泛使用的方法的最大优点是,它是强大的,而简单,每个样品成本相对较低。最需要的提取和分析设备应当以标准的实验室提供,或者可以是自建,用HPLC-PDA的异常。另一个优点是,保持冷却,并在气密法(HPLC)的小瓶中时溶解在水中desulfoglucosinolates是化学相当稳定,因此,提取物可以很容易地运用于HPLC分析别处。相对于LC-MS平台,这需要专门的培训和管理软件和分析数据丰富的实践经验,HPLC-UV /掌上电脑可以很容易地短暂培训后运行。这不仅降低了过程的成本,同时也使得该方法更容易获得的广泛的科学家,包括学生。
一般来说,当上述的过程遵循carefuLLY,应该会出现一些问题。在一般情况下,芥子油苷峰很好在色谱分离。如果不是这种情况下,该梯度程序可以通过降低洗脱液乙腈增加速率进行调整。另外,建设一个新的预柱(200-500注射)或列(1500 -2000注射)可以解决这个问题。偶尔,在分批单个样品的色谱图可以显示出非常小的或没有峰。这通常是由于移液误差添加硫酸时( 例如,一个列被跳过或硫酸未洗净,下入列)。或者,在试验材料的芥子油苷的浓度可能是低于预期并用于提取材料太少。如果是后者的情况下,注射量可增至100微升,或提取物的精确等分试样( 例如,800微升)可被浓缩。后者可以通过冷冻干燥来实现ING的提取物,将残余物溶解于水的体积较小( 例如,100μL),并使用相同的参考曲线回灌。在计算对提取物的初始浓度,数字应乘以稀释因子相乘。如果这没有解决的问题,材料应再次使用更多的原料萃取。如果这是超过100毫克时,萃取溶剂的体积和管的尺寸应按比例调整,以维持提取效率。
一个附加的优点是,这种方法已被充分验证的。这是因为它已被描述为用于芥子油苷的在油菜籽的量化,对于其中的程序和准确性被证实在几个实验室16的标准方法。此外,遗传背景,生物合成,和芥子油苷的生物学功能都受到紧张的研究努力,在模除其他4,6,12埃尔植物拟南芥 。因此,许多响应因子有关sinigrin desulfoglucosinolates的精确量化的明确界定和公众提供15,17。即使基于LS-MS-协议是更高通量,更敏感,并能够(暂定)确定苷的量没有标准是可用的18,19,20,用于LC-MS缺乏普遍响应因子限制硫甙含量18的精确量化。而且,这些方法通常不包括冷冻干燥步骤,并且水的量在新鲜植物材料是下落不明在计算中,使得精确量化困难。最后,因为我们的提取方法包括一列系纯化和浓缩步骤,它也可以适用于"脏"的样品浓度低硫代葡萄糖苷,如土壤21。
相比基于LC-MS的方法,通常提取新鲜冷冻的材料,使用96孔板进行萃取,并且不包括硫酸步骤18,19中 ,我们的方法是比较费时和劳动密集。用在本文中所述的柱支架,一个人可以在一天中提取约100-150样品。洗脱(次日),冷冻干燥(过夜),并重新溶解可以在随后的两天内进行。用自动HPLC注射器,每注射40-45分钟的运行和平衡时间,并且没有不可预见的事件,这将需要3-4天采集数据这一样本集。当HPLC软件允许基于sinigrin曲线,色谱图和PE的手动检查自动定量对100个样品AK分配可能只需要另一个1或2小时,可用于统计分析前的数据。
尽管甙标准的日益普及,只有130多个应聘者的一小部分目前可商用买来的。然而,对于每个生物合成类的一些参考;先前在植物物种中发现的接入文献数据库指定化合物( 如,费伊等人的22);色谱原则,如eluotropic系列的逻辑基本知识( 例如,对于在脂肪族化合物侧链增加Cs中的数字, 图3和4);单样本对LC-MS 19或23核磁共振孤立硫代葡萄糖苷的验证,人们可以很容易地克服这个限制。对于大多数的硫甙分析协议使用内部参考曲线( 即,在一定的浓度为sinigrin的提取或sinalbin到提取溶剂16,17,19)。原则上,内部基准曲线是比较合适的,以校正各试样处理错误,从而在理论上得到更高的精度。尽管这样的优势,我们更喜欢使用一个五点外部基准曲线,我们经常分析不同的野生物种,其中一些含有高含量sinigrin( 例如,黑芥 24)或sinalbin( 例如,白芥 25),该2甙引用为其响应因子可用。此外,添加内部标准,以每个样品增加了分析的成本,因为高品位甙参考标准通常是相当昂贵的。
总之,尽管耗时的步骤,该协议提供了一个简单和方便的方法来提取和植物样品中硫代葡萄糖苷定量。然而,要考虑到的芥子油苷水平本身只有一个在反应产物中的潜在的生物活性的指示,被视为有必要用芥子酶反应,和变化可以从一个单一的芥子油苷11出现是重要的。验证试验必须进行确认生物相关性。
披露声明
The authors have nothing to disclose.
致谢
NMvD thanks Dr. Michael Reichelt (Max-Planck-Institute for chemical Ecology, Jena, Germany) for providing the first reference samples when she started using this method 16 years ago. Ciska Raaijmakers (NIOO-KNAW, Wageningen, the Netherlands), Sebastian Krosse (B-Ware, Nijmegen, the Netherlands), and Christian Ristok (iDiv, Leipzig) are acknowledged for improving the protocol over the course of the years. Mirka Macel and Martine Huberty (University Tübingen, Germany) are acknowledged for their permission to use the Rorippa chromatogram. The authors gratefully acknowledge the support of the German Centre for Integrative Biodiversity Research (iDiv) Halle-Jena-Leipzig, funded by the German Research Foundation (FZT 118).
材料
| Name | Company | Catalog Number | Comments |
| Methanol HiPerSolv CHROMANORM® gradient grade for HPLC grade | VWR | 20,864,320 | |
| Sodium acetate (NaOAc) | Sigma-Aldrich | W302406-1KG-K | |
| HCL | VWR | 1,090,571,000 | |
| Sephadex | Sigma-Aldrich | A25120-10G | |
| (−)-Sinigrin hydrate from horseradish | Sigma-Aldrich | S1647-500MG | |
| Aryl Sulfatase | Sigma-Aldrich | S9626-10KU | |
| Ethanol | VWR | 20,816,298 | |
| Pasteur Pipette | Carl Roth | 4518.1 | |
| Glass Wool | Carl Roth | 7377.1 | |
| Glass /wooden stick | VWR | HERE1080766 | |
| 2 mL reaction tubes | VWR | 211-2606 | |
| Dissecting needle | Carl Roth | KX93.1 | |
| Rotilabo-lab dishes | Carl Roth | 0772.1 | Waste tray |
| Freeze Dryer Freezone 12 L | Labconco | 7960030 | |
| Acetonitril super gradient grade | VWR | 83,639,320 | |
| Water bath | VWR | 462-5112 | |
| Ultrasonic bath | Fisher Scientific | FB 15061 | |
| PH Electrode | Thermo Fisher Scientific | STARA2115 | |
| Centrifuge Heraeus Multifuge X1 | Thermo Fisher Scientific | 75004210 | |
| Pre-Column | Thermo Fisher Scientific | 69697 | C18 column (4.6 x 10 mm, 5 µm, 300 Å) |
| Column Acclaim 300 | Thermo Fisher Scientific | 60266 | C18 column (4.6 x 150 mm, 3 µm, 300 Å) |
| HPLC Ultimate 3000 | Thermo Fisher Scientific | with column oven and UV or PDA detector | |
| Flask 1000 mL | VWR | 215-1595 | |
| Glucosinolate reference compounds | Phytoplan | various | http://www.phytoplan.de/ |
参考文献
- Hartmann, T. From waste products to ecochemicals: Fifty years research of plant secondary metabolism. Phytochemistry. 68 (22-24), 2831-2846 (2007).
- Will, H., Laubenheimer, A. Ueber das Glucosid des weissen Senfsamens. Justus Liebigs Annalen der Chemie. 199 (1), 150-164 (1879).
- Agerbirk, N., Olsen, C. E. Glucosinolate structures in evolution. Phytochemistry. 77, 16-45 (2012).
- Halkier, B. A., Gershenzon, J. Biology and biochemistry of glucosinolates. Ann Rev Plant Biol. 57, 303-333 (2006).
- Sønderby, I. E., Geu-Flores, F., Halkier, B. A. Biosynthesis of glucosinolates - gene discovery and beyond. TIPS. 15 (5), 283-290 (2010).
- Kliebenstein, D. J., et al. Genetic control of natural variation in Arabidopsis glucosinolate accumulation. Plant Physiol. 126 (2), 811-825 (2001).
- van Leur, H., Raaijmakers, C. E., van Dam, N. M. A heritable glucosinolate polymorphism within natural populations of Barbarea vulgaris. Phytochemistry. 67 (12), 1214-1223 (2006).
- Kelly, P. J., Bones, A., Rossiter, J. T. Sub-cellular immunolocalization of the glucosinolate sinigrin in seedlings of Brassica juncea. Planta. 206 (3), 370-377 (1998).
- van Dam, N. M., Tytgat, T. O. G., Kirkegaard, J. A. Root and shoot glucosinolates: a comparison of their diversity, function and interactions in natural and managed ecosystems. Phytochem Rev. 8 (1), 171-186 (2009).
- Ratzka, A., Vogel, H., Kliebenstein, D. J., Mitchell-Olds, T., Kroymann, J. Disarming the mustard oil bomb. Proc Natl Acad Sci U S A. 99 (17), 11223-11228 (2002).
- Wittstock, U., Kliebenstein, D. J., Lambrix, V., Reichelt, M., Gershenson, J., Romeo, J. T. . Integrative Phytochemistry: From ethnobotany to molecular ecology: Recent Advances in Phytochemistry. 37, (2003).
- Hopkins, R. J., van Dam, N. M., van Loon, J. J. A. Role of glucosinolates in insect-plant relationships and multitrophic interactions. Ann Rev Entomol. 54 (1), 57 (2009).
- Kliebenstein, D. J., Gershenzon, J., Mitchell-Olds, T. Comparative quantitative trait loci mapping of aliphatic, indolic and benzylic glucosinolate production in Arabidopsis thaliana leaves and seeds. Genetics. 159 (1), 359-370 (2001).
- Mithen, R., Bennett, R., Marquez, J. Glucosinolate biochemical diversity and innovation in the Brassicales. Phytochemistry. 71 (17-18), 2074-2086 (2010).
- Buchner, R., Wathelet, J. P. . Glucosinolates in rapeseed. , 50-58 (1987).
- . Oil seeds - determination of glucosinolates High Perfomance Liquid Chromatography. Official Journal of the European Communities. , 27-34 (1990).
- Brown, P. D., Tokuhisa, J. G., Reichelt, M., Gershenzon, J. Variation of glucosinolate accumulation among different organs and developmental stages of Arabidopsis thaliana. Phytochemistry. 62 (3), 471-481 (2003).
- Glauser, G., Schweizer, F., Turlings, T. C. J., Reymond, P. Rapid Profiling of Intact Glucosinolates in Arabidopsis Leaves by UHPLC-QTOFMS Using a Charged Surface Hybrid Column. Phytochem Analysis. 23 (5), 520-528 (2012).
- Crocoll, C., Halkier, B. A., Burow, M. . Current Protocols in Plant Biology. , (2016).
- Griffiths, D. W., Bain, H., Deighton, N., Botting, N. P., Robertson, A. A. B. Evaluation of liquid chromatography-atmospheric pressure chemical ionisation-mass spectrometry for the identification and quantification of desulphoglucosinolates. Phytochem Analysis. 11 (4), 216-225 (2000).
- Gimsing, A. L., Kirkegaard, J. A. Glucosinolates and biofumigation: fate of glucosinolates and their hydrolysis products in soil. Phytochem Rev. 8 (1), 299-310 (2009).
- Fahey, J. W., Zalcmann, A. T., Talalay, P. The chemical diversity and distribution of glucosinolates and isothiocyanates among plants. Phytochemistry. 56, 5-51 (2001).
- de Graaf, R. M., et al. Isolation and identification of 4-α-rhamnosyloxy benzyl glucosinolate in Noccaea caerulescens showing intraspecific variation. Phytochemistry. 110, 166-171 (2015).
- van Dam, N. M., Raaijmakers, C. E. Local and systemic induced responses to cabbage root fly larvae (Delia radicum) in Brassica nigra and B. oleracea. Chemoecology. 16 (1), 17-24 (2006).
- Gols, R., et al. Temporal changes affect plant chemistry and tritrophic interactions. Bas Appl Ecol. 8 (5), 421-433 (2007).
转载和许可
请求许可使用此 JoVE 文章的文本或图形
请求许可探索更多文章
This article has been published
Video Coming Soon
版权所属 © 2025 MyJoVE 公司版权所有,本公司不涉及任何医疗业务和医疗服务。