需要订阅 JoVE 才能查看此. 登录或开始免费试用。
Method Article
用醋酸钠添加剂延长可溶性铅流电池的使用寿命
摘要
提出了一种用于构建寿命较长的可溶性铅流电池的协议, 该协议在甲磺酸电解液中供应醋酸钠作为添加剂。
摘要
在本报告中, 我们提出了一种构建具有延长循环寿命的可溶性铅流电池 (slfb) 的方法。通过向电解液中提供足够的醋酸钠 (galvanostatic),通过长期的静电充放电实验, 证明 slfb 的循环寿命延长超过50%。通过投掷指数 (ti) 测量,定量验证了正极上 pbo 2 电极上 pbo 2 电沉积的较高质量。当 slfb 使用 naoas 添加电解质操作时, 通过扫描电子显微镜 (sem) 获得的图像也会表现出更多集成的 pbo2表面形貌。这项工作表明, 电解质改性可以成为经济上使 slfb 能够大规模储能的可行途径。
引言
包括太阳能和风能在内的可再生能源已经开发了几十年, 但其间歇性构成了巨大挑战。对于包含可再生能源的未来电网来说, 电网稳定和负载均衡至关重要, 可以通过集成储能来实现。氧化还原流电池 (rfb) 是网秤储能的好选择之一。传统的 rfb 含有离子选择性膜, 分离了不溶解剂和阴极;例如, 全钒 rfb 已证明运行效率高, 循环寿命长 1,2。然而, 它们作为储能的市场份额非常有限, 部分原因是材料成本高昂, 离子选择性膜无效。另一方面, 由 plectcher 等人介绍了一种单流可溶性铅流电池 (slfb) .1,2,3 个,4 个,5. slfb 是无膜的, 因为它只有一个活性物种, 即铅 (ii) 离子。在充电过程中, 在正极上电镀铅 (ii) 离子作为 pbo2 , 在负极上作为铅, 在放电过程中, 将铅 (ii) 重新转换回铅 (ii)。因此, slfb 只需要一个循环泵和一个电解质储罐, 这反过来又可能导致与传统 rfb 相比降低资本和运营成本。然而, 在正常流动条件下, slfb 公布的循环寿命到目前为止被限制在不到 200个周期的情况下, 6、7、8、9、10。
导致 slfb 循环寿命较短的因素初步与 pbo 2 在正极的沉积溶解有关.在充放电过程中, 发现电解质酸度在深周期或重复周期11中增加, 并建议质子诱导产生非化学计量 pbox 12的钝化层,13. pbo2的脱落是与 slfb 降解有关的另一个现象。shed pbo 2颗粒是不可逆的, 不能再利用。由于电化学反应不平衡以及两个电极上的累积电沉积, slfb 的库仑效率 (ce) 随之下降。为了延长 slfb 的循环寿命, 稳定 ph 值波动和电镀沉积结构至关重要。最近的一篇论文证明了添加醋酸钠 (naoac) 在甲磺酸电解质11中的 slfb 的性能和延长的循环寿命。
本文介绍了在 slfb 中使用 naoac 作为甲磺酸电解质添加剂的详细协议。与不含 naoac 添加剂的 slfb 相比, slfb 性能得到了提高, 使用寿命可以延长50% 以上。此外, 还说明了投掷指数 (ti) 的测量程序, 以便对添加剂对电沉积的影响进行定量比较。最后, 介绍了 slfb 电极电沉积的扫描电子显微镜 (sem) 样品制备方法, 并在采集的图像中显示了加性对电镀的影响。
研究方案
1. 使用醋酸钠添加剂建造 slfb 烧杯电池
注: 本节介绍构建带有长期循环实验添加剂的 slfb 烧杯电池的过程。该协议包括带和不含添加剂的电解质制备、电极预处理、电池组装和效率计算。
-
铅甲磺酸的制备 (1 升, 1 m 为例)
- 在烟罩中, 加入274.6 克的甲磺酸 (msa, 70%), 搅拌用搅拌棒搅拌。用300毫升的去离子水溶解 mL。
- 准备 223.2 g 氧化铅 (ii) (98%), 并以增量的方式添加到上述烧杯, 直到制备的氧化铅完全溶解。
- 用70毫米纤维素滤纸过滤 büchner 漏斗, 以分离任何未溶解的氧化铅。
- 重复此过程3次。添加 di 水, 使其总体积达到1升。
-
不含添加剂的电解质的制备 (300 毫升)
- 在烧杯中加入20.595 克 (70%)。在同一烧杯上加入150毫升制备的 1 m 铅甲磺酸。
- 加入 di 水, 使其总体积达到300毫升, 搅拌电解质, 直到均匀混合, 从而形成 0.5 m 铅甲磺酸与 0.5 m mL 混合的溶液。
-
准备工作含有醋酸钠的电解质 (300 毫升)
- 在烧杯中加入20.595 克 (70%)。在同一烧杯上加入150毫升制备的 1 m 铅甲磺酸。
- 在烧杯中加入1.23 克 naoac (98%) 作为添加剂。
- 加入 di 水, 总体积达到300毫升, 搅拌电解质, 直到均匀混合, 从而形成 0.5 m 铅甲磺酸、0.5 m 甲磺酸和 50 mm 醋酸钠溶液。
-
正负电极的预处理
- 用砂纸 (氧化铝、p100) 反复擦亮正极 (商用碳复合材料) 和负极 (镍) 电极, 直到没有留下可见杂质, 然后用 di 水冲洗电极。
- 在200毫升 di 水中加入20.83 克氯化氢 (35%), 搅拌溶液, 直到所有氯化氢溶解。
- 将整个正极浸泡在制备的1m 氯化氢溶液中过夜, 以去除电极表面的杂质。
- 用 di 水彻底冲洗正极, 用精致的任务雨刷擦干电极。使用聚四氟乙烯 (ptfe) 胶带将每个电极的一侧胶带带在一起, 同时暴露电极的另一侧。
- 用3.03 克硝酸钾 (99%) 和300毫升 di 水制备另一种溶液, 从而产生 0.1 m 硝酸钾溶液。
- 将正极和负极浸入 0.1 m 硝酸钾中, 暴露表面面向每个电极。
- 在正极上施加 1.80 v对ag/agcl 的电位5分钟。随后, 将-1.0 v 与 ag/agcl的电位应用到正极中2分钟。
-
组装中.slfb 烧杯电池
- 将预处理后的正负电极连接到自制电极定位板上, 以获得固定的电极距离。将定位板与电极放在烧杯中, 如图 1所示, 并将电解质添加到烧杯中, 直到指定的浸入水平。
- 将磁力搅拌器放入烧杯中, 将烧杯放置在热板上, 并控制搅拌器的旋转速率。将电池测试仪连接到电极上, 并用塑料包装覆盖烧杯电池, 以防止蒸发。
-
计算电池效率
- 在静电充放电后, 将电池的效率计算如下:
库仑效率: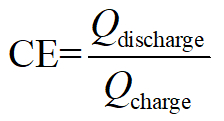
电压效率: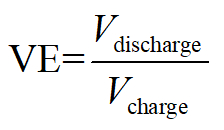
节能:
在这里, q表示电荷/放电等效电子的库仑, v表示应用输出电压, e表示总能量存储/消耗。
- 在静电充放电后, 将电池的效率计算如下:
2. 投掷指数测量
注: 本节介绍在 slfb 电池中测量正极电极上的投掷指数 (ti) 的过程。反转正极和负极的作用提供了另一组 ti 结果。在这里, ti 是通过使用自制的哈林百隆细胞进行研究的, 如图 2所示。
-
测量
- 实验前分别称量和记录两个正极。
- 将负极置于 haring-blum 电池的中心, 并将一个正极与负极的距离比保持在1。将第二个正极置于与负极的另一个距离比 (以图 2中的6为例)。
- 将两个正极和一个负极浸入哈林-布鲁姆电池中具有相同浸没表面积 (这里为2厘米2 ) 的两个正电极和一个负极, 并提供感兴趣的电解质。
- 使用电池测试仪在电极上施加可控电流密度 (20 ma·cm-2)。在一定时间内 (此处 30分钟) 执行静电。
- 电镀后, 用 di 水冲洗两个阳性电极, 在室温下过夜晾干。
- 分别再次称量和记录两个正极, 并根据下面列出的公式计算金属分布比 (mdr)。
- 重复上述实验, 将第二个正极置于各种线性距离比 (lr), 以获取 ti 图 (此处从6到1不等)。
-
计算
- 例如, 将阳极作为感兴趣的电极, 并通过测量的 mdr与lr 确定 ti 图上的每个数据, 这些数据的计算如下:
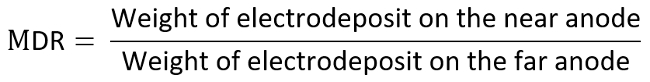
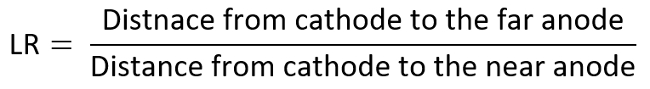
- 例如, 将阳极作为感兴趣的电极, 并通过测量的 mdr与lr 确定 ti 图上的每个数据, 这些数据的计算如下:
3. 扫描电镜样品制备
- 用 di 水冲洗石墨电极, 电镀后在室温下干燥。
- 小心地将石墨电极切割成所需的样品尺寸。冷贴电极样品, 然后用14、8和3μm 碳化硅砂纸对其进行机械抛光。
- 用1微米的金刚石悬浮液和0.05μm 的 al 2o3 对样品进行进一步的抛光.将冷装样品存放在铂金中, 并与铜带连接, 以确保扫描电镜观测的导电性。
结果
为了延长 slfb 的循环寿命, naoac 被作为电解质添加剂提供。同时研究了带有和不含有 naoac 添加剂的 slfb 的循环性能, 结果如图 3所示。为了更容易定量地比较循环寿命, 我们将 slfb 的 "死亡" 定义为在连续静电充放电下 ce 低于80% 时。图 3a和3a显示, 当在0.5m 铅甲磺酸和 0.5 m mM 的电解质中添加 50 mm 纳阿酚时, slfb 的循环?...
讨论
本文介绍了一种经济延长 slfb 循环寿命的方法: 采用 naoac 剂作为电解质添加剂。在长期循环试验之前, 对步骤1中提到的一批新鲜石墨电极和镍板进行了预处理。由于商用碳电极之间的不一致可能会导致 slfb 的性能偏差, 因此步骤1.4 中的物理化学预处理对于去除表面残留物至关重要。步骤1.4 的第二部分是采用电化学方法去除可能引起0至 1.8 v 电位对 ag/agcl之间氧化还原反应的杂质。如
披露声明
我们没有什么可透露的。
致谢
这项工作得到了科技部的支持, 其供资人数为 nsc 102-221-e-002-146-、最省 103-22-21-e-002-146-和最省 104-2628-e-0016-0016-my3。
材料
| Name | Company | Catalog Number | Comments |
| 70 mm cellulose filter paper | Advance | ||
| Autolab | Metrohm | PGSTA302N | |
| BT-Lab | BioLogic | BCS-810 | |
| commercial carbon composite electrode | Homy Tech,Taiwan | Density 1.75 g cm-3, and electrical conductivity 330 S cm-1 | |
| Diamond saw | Buehler | ||
| Hydrochloric Acid | SHOWA | 0812-0150-000-69SW | 35% |
| Lead (II) Oxide | SHOWA | 1209-0250-000-23SW | 98% |
| Lutropur MSA | BASF | 50707525 | 70% |
| nickel plate | Lien Hung Alloy Trading Co., LTD., Taiwan, | 99% | |
| Potassium Nitrate | Scharlab | 28703-95 | 99% |
| Scanning electron microscopy | JEOL | JSM-7800F | at accelerating voltage of 15 kV |
| Sodium Acetate | SHOWA | 1922-5250-000-23SW | 98% |
| water purification system | Barnstead MicroPure | 18.2 MΩ • cm |
参考文献
- Soloveichik, G. L. Flow batteries: current status & trends. Chemical Reviews. 115 (20), 11533-11558 (2015).
- Ravikumar, M. K., Rathod, S., Jaiswal, N., Patil, S., Shukla, A. The renaissance in redox flow batteries. Journal of Solid State Electrochemistry. 21 (9), 2467-2488 (2017).
- Hazza, A., Pletcher, D., Wills, R. A novel flow battery: A lead acid battery based on an electrolyte with soluble lead (II) Part I. Preliminary studies. Physical Chemistry Chemical Physics. 6 (8), 1773-1778 (2004).
- Pletcher, D., Wills, R. A novel flow battery: A lead acid battery based on an electrolyte with soluble lead (II) Part II. Flow cell studies. Physical Chemistry Chemical Physics. 6 (8), 1779-1785 (2004).
- Pletcher, D., Wills, R. A novel flow battery-a lead acid battery based on an electrolyte with soluble lead (II). III. The influence of conditions on battery performance. Journal of Power Sources. 149, 96-102 (2005).
- Hazza, A., Pletcher, D., Wills, R. A novel flow battery-a lead acid battery based on an electrolyte with soluble lead (II). IV. The influence of additives. Journal of Power Sources. 149, 103-111 (2005).
- Pletcher, D., Zhou, H., Kear, G., Low, C. T. J., Walsh, F. C., Wills, R. G. A. A novel flow battery-A lead-acid battery based on an electrolyte with soluble lead (II). V. Studies of the lead negative electrode. Journal of Power Sources. 180 (1), 621-629 (2008).
- Pletcher, D., Zhou, H., Kear, G., Low, C. T. J., Walsh, F. C., Wills, R. G. A. A novel flow battery-A lead-acid battery based on an electrolyte with soluble lead (II). Part VI. Studies of the lead dioxide positive electrode. Journal of Power Sources. 180 (1), 630-634 (2008).
- Li, X., Pletcher, D., Walsh, F. C. A novel flow battery: a lead acid battery based on an electrolyte with soluble lead (II). Part VII. Further studies of the lead dioxide positive electrode. Electrochimica Acta. 54 (20), 4688-4695 (2009).
- Krishna, M., Fraser, E. J., Wills, R. G. A., Walsh, F. C. Developments in soluble lead flow batteries and remaining challenges: An illustrated review. Journal of Energy Storage. 15, 69-90 (2018).
- Lin, Y. -. T., Tan, H. -. L., Lee, C. -. Y., Chen, H. -. Y. Stabilizing the electrodeposit-electrolyte interphase in soluble lead flow batteries with ethanoate additive. Electrochimica Acta. 263, 60-67 (2018).
- Oury, A., Kirchev, A., Bultel, Y., Chainet, E. PbO2/Pb2+ cycling in methanesulfonic acid and mechanisms associated for soluble lead-acid flow battery applications. Electrochimica Acta. 71, 140-149 (2012).
- Oury, A., Kirchev, A., Bultel, Y. Potential response of lead dioxide/Lead (II) galvanostatic cycling in methanesulfonic acid: a morphologico-kinetics interpretation. Journal of The Electrochemical Society. 160 (1), A148-A154 (2013).
转载和许可
请求许可使用此 JoVE 文章的文本或图形
请求许可探索更多文章
This article has been published
Video Coming Soon
版权所属 © 2025 MyJoVE 公司版权所有,本公司不涉及任何医疗业务和医疗服务。