É necessária uma assinatura da JoVE para visualizar este conteúdo. Faça login ou comece sua avaliação gratuita.
Method Article
Estendendo a vida útil das baterias de fluxo chumbo solúvel com um aditivo de acetato de sódio
Neste Artigo
Resumo
Um protocolo para a construção de uma bateria de fluxo de chumbo solúvel com uma vida útil prolongada, no qual sódio acetato é fornecido no eletrólito metanossulfônico como aditivo, é apresentado.
Resumo
Neste relatório, nós apresentamos um método para a construção de uma bateria de fluxo de chumbo solúvel (SLFB) com uma ciclo prolongado de vida. Fornecendo uma quantidade adequada de acetato de sódio (NaOAc) para o eletrólito, uma extensão de ciclo de vida de mais de 50% é demonstrada por SLFBs através de galvanostatic a longo prazo, carga/descarga e experimentos. Uma maior qualidade da eletrodeposição de2 PbO para o eletrodo positivo é validada quantitativamente para eletrólito NaOAc-adicionado lançando medições de índice (TI). Imagens adquiridas por microscopia eletrônica (SEM) também apresentam mais integrada PbO2 morfologia superficial quando o SLFB é operado com o eletrólito de NaOAc-adicionado. Este trabalho indica que a modificação do eletrólito pode ser um caminho plausível para habilitar economicamente SLFBs para armazenamento de energia em grande escala.
Introdução
Vento e fontes de energia renováveis, incluindo solar foram desenvolvidos há décadas, mas sua natureza intermitente coloca grandes desafios. Para uma rede de energia futura com fontes de energia renováveis incorporada, estabilização de grade e redistribuição de carga são críticas e podem ser alcançados através da integração de armazenamento de energia. Baterias de fluxo redox (RFBs) são uma das opções promissoras para o armazenamento de energia de grade escala. RFBs tradicionais contêm íon-seletivo membranas separando anolito e catholyte; por exemplo, a RFB tudo-vanádio tem mostrado para operar com alta eficiência e um longo ciclo de vida1,2. No entanto, a sua quota de mercado, como o armazenamento de energia é muito limitada em parte devido à composta de materiais caros e ineficazes membranas íon-seletivo. Por outro lado, uma bateria de fluxo único fluxo chumbo solúvel (SLFB) é apresentada por Plectcher et al . 1 , 2 , 3 , 4 , 5. the SLFB é membrana menos porque tem apenas uma espécie de ativa, íons Pb(II). PB(II) íons são galvanizadas para o eletrodo positivo como PbO2 e o elétrodo negativo como Pb simultaneamente durante o carregamento e converter de volta para Pb(II) durante o descarregamento. Um SLFB, portanto, precisa de um circulador e um eletrólito tanque de armazenamento, que por sua vez pode potencialmente levar a redução de capital e custos operacionais em relação ao convencionais RFBs. A vida de ciclo publicado de SLFBs, no entanto, até agora é limitada a menos de 200 ciclos sob fluxo normal condições6,7,8,9,10.
Fatores que conduzem a uma vida de ciclo curta SLFB são preliminarmente associadas com deposição/dissolução de PbO2 para o eletrodo positivo. Durante os processos de carga/descarga, encontra-se a acidez do eletrólito aumento profundo ou repetidos ciclos11e prótons são sugeridos para induzir a geração de uma camada de passivação de não-estequiométricos PbOx12, 13. o derramamento de PbO2 é um outro fenômeno relacionado à degradação SLFB. Galpão de PbO2 partículas são irreversíveis e já não podem ser utilizadas. A eficiência de coulombic (CE) do SLFBs consequentemente declina por causa de reações eletroquímicas desequilibradas, bem como electrodeposits acumuladas em ambos os eletrodos. Para estender o ciclo de vida de SLFBs, estabilizando o pH flutuação e estrutura de eletrodeposição são críticos. Um estudo recente demonstra um desempenho aprimorado e prolongado ciclo de vida de SLFBs com adição de acetato de sódio (NaOAc) em metanossulfônico eletrólito11.
Aqui, um protocolo detalhado para empregar NaOAc como um aditivo para o eletrólito metanossulfônico em SLFBs é descrito. O desempenho de SLFB é mostrado para ser aprimorado e a expectativa de vida pode ser estendida por mais de 50% em comparação com SLFBs sem aditivos de NaOAc. Além disso, os procedimentos para atirar a medição do índice (TI) são ilustrados para efeitos de comparação quantitativa dos efeitos aditivos na eletrodeposição. Finalmente, é descrito um varredura microscopia eletrônica de varredura (MEV) método de preparação de amostra para eletrodeposição em eletrodos SLFB e o aditivo impacto sobre eletrodeposição manifesta-se em imagens adquiridas.
Protocolo
1. construção de uma célula de copo SLFB com um aditivo de acetato de sódio
Nota: Esta seção descreve o procedimento para construir uma célula de copo SLFB com um aditivo para o experimento de ciclismo a longo prazo. O protocolo inclui a preparação do eletrólito com e sem aditivo, pré-tratamento do eletrodo, montagem de célula e cálculos de eficiência.
-
Preparação de Metanossulfonato de chumbo (1 L, 1 M, por exemplo)
- Na coifa, adicione 274,6 g de ácido metanossulfônico (MSA, 70%) para uma proveta, agitando com uma barra de agitação. Dissolva o MSA com 300 mL de água desionizada (DI).
- Prepare 223,2 g de óxido de chumbo (II) (98%) e adicionar em incrementos para o copo acima mencionado, até que o óxido de chumbo preparado é completamente dissolvido.
- Filtrar através do funil de Büchner com papel de filtro de celulose de 70 mm para separar qualquer óxido de chumbo não dissolvido.
- Repita este procedimento por 3 vezes. Adicione água DI para atingir 1 L de volume total.
-
Preparação do eletrólito sem aditivo (300ml)
- Adicione 20,595 g de MSA (70%) para um béquer. Adicione 150 mL de Metanossulfonato de chumbo de 1 M preparada para o mesmo copo.
- Adicione água para chegar a 300 mL de volume total e mexa o eletrólito até uniformemente misturado, que resulta em uma solução de 0,5 M Metanossulfonato de chumbo misturada com 0,5 M MSA.
-
Preparação do eletrólito com acetato de sódio (300 mL)
- Adicione 20,595 g de MSA (70%) para um béquer. Adicione 150 mL de Metanossulfonato de chumbo de 1 M preparada para o mesmo copo.
- Adicione 1,23 g de NaOAc (98%) para o copo como um agente aditivo.
- Adicione água para chegar a 300 mL de volume total e mexa o eletrólito até uniformemente misturado, que resulta em uma solução de acetato de sódio 50 mM, ácido metanossulfônico de 0,5 M e Metanossulfonato de chumbo de 0,5 M.
-
Pré-tratamento de eletrodos positivos e negativos
- Repetidamente, polir o positivo (composto de carbono comercial) e negativo (níquel) eletrodos com uma lixa (óxido de alumínio, P100) até sem impurezas visíveis estão à esquerda e em seguida enxaguar os eletrodos com água.
- Adicionar 20,83 g de cloreto de hidrogênio (35%) em DI de 200 mL de água e agitar a solução até que todo o cloreto de hidrogênio é dissolvido.
- Mergulhe o eletrodo positivo inteiro na 1 M cloreto de hidrogênio solução preparada durante a noite para remover as impurezas da superfície do eletrodo.
- Enxaguar o eletrodo positivo cuidadosamente com água e secar o eletrodo com limpadores de tarefa delicada. Fita de um lado de cada eletrodo usando fita de politetrafluoretileno (PTFE) ao expor o outro lado dos eletrodos.
- Preparar outra solução com 3,03 g de nitrato de potássio (99%) e água de 300 mL DI, o que resulta em uma solução de nitrato de potássio 0,1 M.
- Mergulhe os eléctrodos positivos e negativos em nitrato de potássio 0,1 M com a superfície exposta, enfrentando cada eletrodo.
- Aplica um potencial de 1.80 V vs Ag/AgCl o elétrodo positivo por 5 min. Posteriormente, aplicar um potencial de -1,0 V vs Ag/AgCl para o eletrodo positivo por 2 min.
-
Montar o Célula de copo SLFB
- Anexe os eletrodos positivos e negativos pré-tratados para um Conselho de posicionamento caseiras eletrodo para uma distância fixa do eletrodo. Coloque a placa posicionamento juntamente com eletrodos numa proveta conforme ilustrado esquematicamente na Figura 1 e adicione eletrólito para o copo até o nível designado de imersão.
- Coloque um agitador magnético para o copo, coloque o copo sobre um prato quente e controlar a taxa de rotação do agitador. Conectar o testador de bateria aos eletrodos e cobrir a célula béquer com filme plástico para evitar a evaporação.
-
Calcular a eficiência da bateria
- Depois de galvanostatic de carga e descarga, calcule a eficiência da bateria como a seguir:
Coulombic eficiência: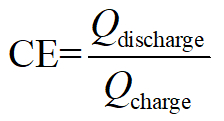
Eficiência de tensão: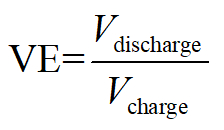
Eficiência energética:
Aqui, Q denota coulombs de elétrons equivalentes carregado/descarregado, V a tensão de saída/aplicar e E a energia total consumida/armazenados.
- Depois de galvanostatic de carga e descarga, calcule a eficiência da bateria como a seguir:
2. jogando a medição do índice
Nota: Esta seção descreve o procedimento para medir o índice de arremesso (TI) da eletrodeposição em eletrodos positivos nas células SLFB. Inverter o papel de eletrodos positivos e negativos entrega o outro conjunto de resultados de TI. Aqui, a TI é investigado por meio de uma célula de Haring-Blum caseiras como esquematicamente representada na Figura 2.
-
Medição
- Pesar e gravar dois eletrodos positivos respectivamente antes dos experimentos.
- Coloque o elétrodo negativo no centro de uma célula de Haring-Blum e um eletrodo positivo em uma relação de distância de 1 do elétrodo negativo. Coloque o eletrodo positivo segundo a outra relação de distância do elétrodo negativo (take 6 como um exemplo na Figura 2).
- Mergulhe os dois eléctrodos positivos e um elétrodo negativo com o mesmo imerso superfície (2cm2 aqui) na célula Haring-Blum com o eletrólito de interesse.
- Aplica uma densidade de corrente controlada (20 mA·cm-2 aqui) para os eletrodos, usando um testador de bateria. Realize a carga de galvanostatic para uma determinada duração (30 min aqui).
- Depois de chapeamento, enxágue os dois eléctrodos positivos com água e secá-las à temperatura ambiente durante a noite.
- Pesar e gravar dois eletrodos positivos novamente respectivamente e calcular a taxa de distribuição de metal (MDR) de acordo com a equação abaixo.
- Repeti os experimentos acima mencionados, colocando o segundo elétrodo positivo em várias relações de distância linear (LR) para adquirir o diagrama de TI (variado de 6 a 1 aqui).
-
Cálculo
- Como exemplo, considere o ânodo como o eletrodo de interesse e determinar cada dados no diagrama de TI pela medida MDR contra LR, que são calculados como o seguinte:
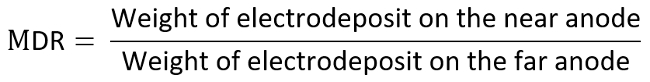
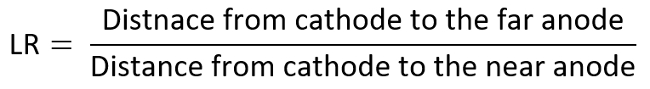
- Como exemplo, considere o ânodo como o eletrodo de interesse e determinar cada dados no diagrama de TI pela medida MDR contra LR, que são calculados como o seguinte:
3. preparação da amostra SEM
- Enxaguar o eletrodo de grafite com água e secar em temperatura ambiente após a galvanização.
- Eletrodos de grafite de fatia para o tamanho da amostra desejada pelo diamante viram com cuidado. Frio montar a amostra de eletrodo e depois mecanicamente lustrá-la com 14, 8 e 3 papéis de carboneto de silício areia μm, posteriormente.
- Mais polonês as amostras com suspensão de diamante 1 μm e 0,05 μm Al2O3. Deposite a amostra fria-montado com platina e anexá-lo com fitas de cobre para garantir a condutividade para observação SEM.
Resultados
Para estender o ciclo de vida de SLFBs, NaOAc é fornecido como um aditivo de eletrólito. Desempenho de SLFBs com e sem aditivo de NaOAc de ciclismo são examinados em paralelo, e os resultados são mostrados na Figura 3. Para mais fácil quantitativa comparação do ciclo de vida, nós definimos a "morte" de um SLFB como quando seu CE for inferior a 80% sob galvanostatic contínua de carga/descarga. Figura 3a e 3b
Discussão
Este artigo descreve um método econômico para estender a ciclo de vida de SLFBs: empregando NaOAc agente como um aditivo de eletrólito. Um lote de eletrodos de grafite fresco e placas de níquel são pré-processados como acima mencionado na etapa 1 antes experimentos de ciclismo a longo prazo. Porque inconsistência entre os elétrodos do carbono comercial pode causar desvio de desempenho dos SLFBs, o pré-tratamento físico-químicas na etapa 1.4 é fundamental para remover os resíduos de superfície. A segunda par...
Divulgações
Nós não temos nada para divulgar.
Agradecimentos
Este trabalho foi financiado pelo Ministério da ciência e tecnologia, R.O.C., sob o número de financiamento de NSC 102-2221-E-002 - 146-, a maioria dos 103-2221-E-002 - 233 - e a maioria dos 104-2628-E-002-016-MY3.
Materiais
| Name | Company | Catalog Number | Comments |
| 70 mm cellulose filter paper | Advance | ||
| Autolab | Metrohm | PGSTA302N | |
| BT-Lab | BioLogic | BCS-810 | |
| commercial carbon composite electrode | Homy Tech,Taiwan | Density 1.75 g cm-3, and electrical conductivity 330 S cm-1 | |
| Diamond saw | Buehler | ||
| Hydrochloric Acid | SHOWA | 0812-0150-000-69SW | 35% |
| Lead (II) Oxide | SHOWA | 1209-0250-000-23SW | 98% |
| Lutropur MSA | BASF | 50707525 | 70% |
| nickel plate | Lien Hung Alloy Trading Co., LTD., Taiwan, | 99% | |
| Potassium Nitrate | Scharlab | 28703-95 | 99% |
| Scanning electron microscopy | JEOL | JSM-7800F | at accelerating voltage of 15 kV |
| Sodium Acetate | SHOWA | 1922-5250-000-23SW | 98% |
| water purification system | Barnstead MicroPure | 18.2 MΩ • cm |
Referências
- Soloveichik, G. L. Flow batteries: current status & trends. Chemical Reviews. 115 (20), 11533-11558 (2015).
- Ravikumar, M. K., Rathod, S., Jaiswal, N., Patil, S., Shukla, A. The renaissance in redox flow batteries. Journal of Solid State Electrochemistry. 21 (9), 2467-2488 (2017).
- Hazza, A., Pletcher, D., Wills, R. A novel flow battery: A lead acid battery based on an electrolyte with soluble lead (II) Part I. Preliminary studies. Physical Chemistry Chemical Physics. 6 (8), 1773-1778 (2004).
- Pletcher, D., Wills, R. A novel flow battery: A lead acid battery based on an electrolyte with soluble lead (II) Part II. Flow cell studies. Physical Chemistry Chemical Physics. 6 (8), 1779-1785 (2004).
- Pletcher, D., Wills, R. A novel flow battery-a lead acid battery based on an electrolyte with soluble lead (II). III. The influence of conditions on battery performance. Journal of Power Sources. 149, 96-102 (2005).
- Hazza, A., Pletcher, D., Wills, R. A novel flow battery-a lead acid battery based on an electrolyte with soluble lead (II). IV. The influence of additives. Journal of Power Sources. 149, 103-111 (2005).
- Pletcher, D., Zhou, H., Kear, G., Low, C. T. J., Walsh, F. C., Wills, R. G. A. A novel flow battery-A lead-acid battery based on an electrolyte with soluble lead (II). V. Studies of the lead negative electrode. Journal of Power Sources. 180 (1), 621-629 (2008).
- Pletcher, D., Zhou, H., Kear, G., Low, C. T. J., Walsh, F. C., Wills, R. G. A. A novel flow battery-A lead-acid battery based on an electrolyte with soluble lead (II). Part VI. Studies of the lead dioxide positive electrode. Journal of Power Sources. 180 (1), 630-634 (2008).
- Li, X., Pletcher, D., Walsh, F. C. A novel flow battery: a lead acid battery based on an electrolyte with soluble lead (II). Part VII. Further studies of the lead dioxide positive electrode. Electrochimica Acta. 54 (20), 4688-4695 (2009).
- Krishna, M., Fraser, E. J., Wills, R. G. A., Walsh, F. C. Developments in soluble lead flow batteries and remaining challenges: An illustrated review. Journal of Energy Storage. 15, 69-90 (2018).
- Lin, Y. -. T., Tan, H. -. L., Lee, C. -. Y., Chen, H. -. Y. Stabilizing the electrodeposit-electrolyte interphase in soluble lead flow batteries with ethanoate additive. Electrochimica Acta. 263, 60-67 (2018).
- Oury, A., Kirchev, A., Bultel, Y., Chainet, E. PbO2/Pb2+ cycling in methanesulfonic acid and mechanisms associated for soluble lead-acid flow battery applications. Electrochimica Acta. 71, 140-149 (2012).
- Oury, A., Kirchev, A., Bultel, Y. Potential response of lead dioxide/Lead (II) galvanostatic cycling in methanesulfonic acid: a morphologico-kinetics interpretation. Journal of The Electrochemical Society. 160 (1), A148-A154 (2013).
Reimpressões e Permissões
Solicitar permissão para reutilizar o texto ou figuras deste artigo JoVE
Solicitar PermissãoThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Todos os direitos reservados