需要订阅 JoVE 才能查看此. 登录或开始免费试用。
Method Article
马萨霉素的合成,一种革兰氏阳性细菌生长的小分子抑制剂
摘要
提出了制备抑菌二酰胺马萨霉素的详细方案,马萨里霉素是一种小分子探针,通过靶向细胞壁降解来抑制 枯草芽孢杆菌 和 肺炎链球菌 的生长。其作为化学探针的应用在与 枯草芽孢杆菌 和 肺炎链球菌的协同作用/拮抗作用测定和形态学研究中得到证明。
摘要
细菌细胞壁中的肽聚糖(PG)是一种独特的大分子结构,赋予形状和保护周围环境。了解细胞生长和分裂的核心是了解PG降解如何影响生物合成和细胞壁组装。最近,已经报道了通过引入改性糖或氨基酸来标记PG的代谢标记。虽然用小分子抑制剂对生物合成步骤进行化学询问是可能的,但研究自身溶酶降解PG的化学生物学工具尚不发达。细菌自溶素是一类广泛的酶,参与PG的紧密协调降解。这里提出了制备小分子探针masarimycin的详细方案,masarimycin是 枯草芽孢杆菌 中N-乙酰葡萄糖苷酶LytG的抑制剂,以及 肺炎链球菌中的细胞壁代谢。 提供通过 微波辅助和经典有机合成制备抑制剂的方法。介绍了其作为研究生物测定中革兰氏阳性生理学的工具的适用性。
引言
肽聚糖(PG)是一种网状聚合物,可描绘革兰氏阳性和革兰氏阴性细菌1,2中的细胞形状和结构。这种杂聚物是由短肽3,4,5,6与由β-(1,4)连接的交替的N-乙酰葡糖胺(GlcNAc)和N-乙酰基壁氨酸(MurNAc)残基组成的主链的氨基糖基质(图1)1。附着在MurNAc的C-3乳酰基部分的是茎肽。PG的代谢涉及生物合成和降解酶的紧密协调系统,以将新材料掺入细胞壁7,8。PG的降解由统称为自溶蛋白9的酶进行,并根据切割的键的特异性进一步分类。自溶蛋白参与许多细胞过程,包括细胞生长,细胞分裂,运动,PG成熟,趋化性,蛋白质分泌,遗传能力,分化和致病性10,11。解开单个自溶蛋白的特定生物学功能可能令人生畏,部分原因是功能冗余。然而,最近的生物物理8,12,13和计算研究12为它们在PG代谢中的作用提供了新的见解。此外,最近的报告提供了对PG代谢中合成14和膜介导的15,16,17步骤的进一步了解。对PG代谢的降解和合成途径之间关系的透彻理解可能会产生以前未开发的抗生素靶标。
虽然在研究真核生物糖生物学的方法上取得了重大进展,但细菌糖生物学,特别是PG代谢并没有以类似的速度发展。目前研究PG代谢的化学方法包括荧光标记的抗生素18,荧光探针19,20和代谢标记21,22,23,24。这些新方法为询问细菌细胞壁代谢提供了新的方法。虽然其中一些策略能够在体内标记PG , 但它们可以是物种特异性的19,或者仅在缺乏特定自溶素25的菌株中起作用。许多PG标记策略旨在用于分离的细胞壁26 或与 体外 重建的PG生物合成途径20,27,28。荧光标记抗生素的使用目前仅限于生物合成步骤和转吞18。
目前细菌自身溶解素及其在细胞壁代谢中的作用的知识来自遗传和 体外 生化分析11,29,30,31,32。虽然这些方法提供了有关这种重要酶类的大量信息,但破译它们的生物学作用可能具有挑战性。例如,由于功能冗余33,在大多数情况下,自动溶血素的缺失不会导致细菌生长停止。尽管它们在细胞生长和分裂中隐含着作用7,12。另一个并发症是细菌自身溶解素的遗传缺失可引起元表型34。元表型源于受遗传缺失影响的途径与其他相互关联的途径之间的复杂相互作用。例如,元表型可以通过直接 效应(例如 缺乏酶)或间接效应(例如调节剂的破坏)而产生。
目前,只有少数糖苷酶自溶蛋白抑制剂,如N-乙酰氨基葡萄糖酶(GlcNAcase)和N-乙酰基muramidases,可用作化学探针来研究PG的降解。为了解决这个问题,已经鉴定并表征了35 作为 枯草芽孢杆菌 生长的抑菌抑制剂,其靶向GlcNAcase LytG32 (图1)。LytG是一种 外源作用的GlcNAcase36,是糖基水解酶家族73(GH73)中簇2的成员。它是营养生长过程中的主要活性GlcNAcase32。据我们所知,马沙霉素是抑制细胞生长的PG作用GlcNAcase的第一种抑制剂。马沙霉素与 肺炎链球菌 的进一步研究发现,马沙霉素可能抑制该生物体中的细胞壁代谢37。在这里,据报道,马沙霉素的制备被用作化学生物学探针,以研究革兰氏阳性生物 枯草芽孢 杆菌和 肺炎链球菌 的生理学。本文介绍了用马沙霉素进行亚最小抑制浓度治疗的形态学分析实例,以及协同/拮抗作用测定。使用具有明确定义的作用模式的抗生素进行协同作用和拮抗作用测定可以是探索细胞过程38,39,40之间连接的有用方法。
研究方案
1. 一般方法
注意:所有化合物均从标准供应商处购买,无需进一步纯化即可使用。
- 在预涂有硅胶XG F254的铝板上进行薄层色谱(TLC)。通过浸入对茴香醛污渍或暴露于I2蒸气来检测紫外灯下的斑点。
- 在 400 MHz 光谱仪上记录所有核磁共振 (NMR) 光谱。
注意: 1H-NMR和 13C-NMR光谱参考残留溶剂峰。耦合常数以 [Hz] 为单位,化学位移以 [ppm] 为单位。 - 在配备大气固体分析探针的紧凑型质谱仪上记录马萨霉素的大气压力化学电离(APCI)质谱。
2.马萨霉素制备的一般程序
注:在通风橱中执行以下步骤。
- 在每种反应物的甲醇中制备0.1M溶液:环己胺,环己基甲醛, 邻碘苯甲酸和环己基异腈35。
注意:环己胺、环己基异腈和环己基甲醛易燃。它们可引起皮肤腐蚀并诱发口腔、皮肤、呼吸或生殖毒性。使化合物远离明火、热表面和火源。穿戴适当的皮肤和眼睛防护用品,在通风良好的地方工作,避免吸入蒸气或雾气。储存时,请保持瓶子密闭,并将其存放在阴凉干燥的地方。将环己基甲醛储存在干燥器中,在N2 气氛下。 - 将5mL环己胺(0.1M甲醇溶液)和5mL环己基甲醛(甲醇中0.1M)混合在带盖的圆底烧瓶中,并使用磁力搅拌棒在搅拌/热板上在沙浴中在40°C下搅拌30分钟。使用放置在沙子表面以下约1厘米的温度计监测温度。
- 30分钟后,向步骤2.2的溶液中加入5mL环己基异腈(0.1M甲醇溶液),并在50°C下再搅拌20分钟。 最后,向反应混合物中加入5mL 邻碘苯甲酸(甲醇中0.1M溶液),并在55°C下继续搅拌3-5小时。
- 在上述反应混合物搅拌3小时后,约每小时通过TLC定期监测反应的进展。
- 切割一块 3 cm x 6 cm 的铝背 TLC 板条。使用#2铅笔,从底部画一条距离约1厘米的线。使用玻璃微毛细管,将约5μL反应混合物点到TLC板上并使其干燥。
- 在 150 mL 烧杯中,加入足够的流动相(90:10 己烷:异丙醇)以覆盖烧杯的底部。使用一对镊子,小心地将上面的TLC板放入烧杯中,确保TLC板均匀地进入流动相。用一块锡箔纸盖住烧杯的顶部。
注意:确保流动相不覆盖管路和斑点样品。 - 让流动相沿着TLC板向上移动,直到它在板顶部下方约1厘米处。取下TLC板,用铅笔画一条线,指示流动相行进的距离。让TLC板在通风橱中干燥。
- 干燥后,将TLC板放入含有少量固体I2 的烧杯中,并用一块锡箔覆盖烧杯。监测TLC中黄色/棕色斑点的发展。显影后,取下TLC板并使用铅笔标记斑点的位置(补充图1)。
注意:如果我2个 斑点没有标记,污渍会随着时间的推移而消散。也可以通过紫外光、 对茴香醛染色或高锰酸钾染色在TLC板上看到斑点(参见 补充信息)。 - 使用以下公式计算所有可视化点的 Rf 值:
Rf =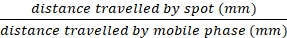
- 当TLC板上只有一个Rf = 0.3的斑点可见时,考虑反应完成。在减压下在旋转蒸发器中除去溶剂,并在高真空下干燥粗产物(以黄褐色油的形式获得),直到所有甲醇蒸发。
- 将干燥的粗产物溶解在30mL乙酸乙酯中,并将其转移到分液漏斗中。依次用1 M HCl(2 x 30 mL),H2O(30 mL),饱和NaHCO 3溶液(2 x30 mL),H2O(30 mL)和饱和NaCl溶液(2 x 30 mL)提取乙酸乙酯。丢弃水层。
注意:乙酸乙酯层是每种提取液中的顶层。对于每次提取,用力摇动含有乙酸乙酯和水溶液(HCl,H2O,NaHCO3或NaCl)的分液漏斗,并使各层完全分离。 - 从分液漏斗中取出乙酸乙酯层,并将其收集在锥形瓶中。加入充满Na2SO4 (无水)的刮刀,以除去乙酸乙酯中的残留水。
注意:当烧瓶中的Na2SO4 自由运行并且不结块时,乙酸乙酯溶液被认为是干燥的。如果 Na2SO4 结块,可以添加额外的 Na2SO4 刮刀。 - 通过#1滤纸过滤干燥的乙酸乙酯溶液,以除去Na2SO4。用少量乙酸乙酯清洗滤纸。将过滤的乙酸乙酯溶液置于圆底烧瓶中,并在减压下在旋转蒸发器上除去溶剂,一旦除去所有乙酸乙酯,即可获得油状马萨霉素。
- 将上述获得的马萨霉素油以最小量(1-2mL)的9∶1己烷:异丙醇溶解,并在磁力搅拌板上搅拌,直到所有化合物溶解。
- 使用12g正相二氧化硅闪光柱通过闪蒸色谱纯化溶解的马沙霉素。
- 用10柱体积的流动相(99:1己烷:异丙醇)平衡闪蒸柱,并将仪器设置为15 mL / min。
注:平衡完成后,停止流动并断开色谱柱顶部与系统连接。 - 使用5 mL注射器提取溶解的马沙霉素。将注射器直接连接到平衡的闪蒸柱的顶部,并将溶液注入塔中。将上样柱重新连接到闪光色谱系统并启动梯度洗脱。
- 使用梯度洗脱从色谱柱中洗脱马沙霉素至最终流动相浓度为10∶90的己烷:异丙醇超过12柱体积。监测马萨利霉素在230和254nm处 通过 吸收的洗脱。
- 通过馏分收集器从色谱柱中洗脱的化合物,该级分收集器每级集收集20 mL溶剂。
注意:如果没有闪蒸色谱系统,马沙霉素的纯化可以通过具有3:1(己烷:乙酸乙酯)流动相的重力二氧化硅柱进行。含有马沙霉素的组分可以通过TLC使用相同的流动相来鉴定。TLC斑点的可视化是用紫外光,I2蒸汽或高锰酸钾染色完成的。 - 通过TLC(步骤2.5-2.9)或在配备大气固体分析探针的紧凑型质谱仪上进行质谱鉴定含有马沙霉素的馏分。在真空(~0.3毫巴)下干燥最终产品。
注意:马沙霉素通常以无色油或固体的形式获得,相对于加入到反应中的环己基甲醛的mmol,收率为55%-70%。通过获得纯化的马沙霉素的质量并使用以下公式计算反应的理论产率来计算马沙霉素的最终产量:
% 产量 = x 100%
x 100%
- 用10柱体积的流动相(99:1己烷:异丙醇)平衡闪蒸柱,并将仪器设置为15 mL / min。
- 通过 NMR 确认马沙霉素的结构。
- 将〜10mg马萨利霉素样品溶解在0.5mL CDCl3中。使用巴斯德移液管,将溶液转移到5 mm NMR管中并盖上管。将 NMR 管放入光谱仪中。
- 使用制造商预设实验采集 1H 和 13C NMR 光谱。化学位移分配和代表性光谱在 补充图3-4中提供。
- 将马萨霉素干燥或溶解在DMSO(25mM终浓度)中,在-20°C直至使用。
3.马沙霉素制备的微波程序
- 在乙腈中制备0.6 M环己胺,环己基甲醛,环己基异腈和邻碘苯甲酸溶液。
- 将搅拌棒和10 mL乙腈加入玻璃微波反应瓶中。
- 向小瓶中加入2mL环己胺(0.6M在乙腈中),2mL环己基甲醛(0.6M在乙腈中)和7mL乙腈。
- 将微波反应瓶放入微波转盘中。搅拌混合物,在400 W的功率设置下在50°C下加热30分钟,并使其冷却至室温。
- 向小瓶中加入2 mL邻碘苯甲酸(甲醇中0.6 M)和2mL环己基异腈(0.6 M在乙腈中)。搅拌混合物,在400 W的功率设置下在微波炉中将其加热至100°C40分钟,并使其冷却至室温。
- 通过TLC(90∶10己烷:异丙醇)监测反应进程,步骤3.5完成后使用I2 蒸气。
注意:如果TLC显示反应不完整(即TLC上的多个斑点),请将反应瓶放回微波中并设置步骤3.5中描述的微波条件。 - 反应完成后,将溶液倒入100 mL圆底烧瓶中,并使用旋转蒸发器将其蒸发至干燥。
- 按照上述步骤2.6-2.16完成马沙霉素的水性检查、纯化和表征。
4. 协同作用和拮抗作用
- 在厌氧条件下,在37°C下在含有5%(v / v)绵羊血的Mueller-Hinton(MH)琼脂平板上生长 肺炎链球菌R6 。在所有实验中,使用在厌氧条件下在37°C下在5mLMH肉汤中生长的第二传代细胞,直到OD600 为〜0.4。
- 将抑制剂masarimycin和optochin置于各自溶剂中的连续1:2稀释液中,所得浓度与每种抑制剂的最小抑制浓度(MIC)值两侧。
- 使马沙霉素在二甲基亚砜(DMSO)中的初始稀释,直到达到100μM的浓度。从这一点开始,在MH肉汤中制作马沙霉素稀释液。通过将市售的视通蛋白(见 材料表)溶解在无菌MH肉汤中来制备视通素储备溶液(3.5mM)。
注意:Masarimycin储备溶液在DMSO中以25 mM制成。
- 使马沙霉素在二甲基亚砜(DMSO)中的初始稀释,直到达到100μM的浓度。从这一点开始,在MH肉汤中制作马沙霉素稀释液。通过将市售的视通蛋白(见 材料表)溶解在无菌MH肉汤中来制备视通素储备溶液(3.5mM)。
- 向无菌的96孔微量滴定板中,向板的每行加入2μL等分试样中每种视通星稀释液。在同一平板中,向每个色谱柱中加入2μL等分试样,将每种马沙霉素稀释液加入到每个色谱柱中,以在平板上产生一系列视通星和马沙霉素浓度(图2)。
- 向含有上述抑制剂的每个孔中加入无菌MH肉汤(93μL)。从步骤4.1中用5μL培养物(OD600 〜0.4)接种微量滴定板。
注意:96孔板的接种通常在厌氧条件下在厌氧工作站中进行。孔中的最终体积为100μL。 - 在厌氧条件下在37°C下培养18小时,然后加入30μL0.01%(m / v)刃天青钠盐溶液。将板在室温下孵育15分钟,以允许形成和稳定颜色。
注意:通过将化合物溶解在蒸馏水中来制备刃天青溶液,并且可以在4°C下储存长达两周。 - 直接从板中读取浓度值,并将未观察到细菌生长的最低抑制剂浓度(蓝色)指定为[X](参见步骤4.7.1),即在助剂存在下药物的最低抑制浓度。
注意:通过利沙林染料变成粉红色来识别孔中的阳性细菌生长。单独使用雷唑啉MIC测定35 与每种药物以类似的方式测定每种药物的MIC值(即,在没有共药的情况下)以类似的方式测定(补充图5)。 肺炎链球菌 的 MIC 分别为 7.8 μM 和 15.85 μM,用于 masarimycin 和 optochin。 - 使用以下等式确定分数抑制浓度(FIC)和FIC指数(FICI)。
- FIC= [X]/MICx,其中[X](来自步骤4.6)是共药存在下药物的最低抑制浓度,MICx 是没有助剂药物的情况下药物的最低抑制浓度。
- FICI = FIC马沙霉素 + FIC抗生素
注:FICI < 0.5 = 协同,0.5 < FICI < 1 = 添加剂,1 < FICI < 4 = 无差异,FICI > 4 = 拮抗。
5. 形态学研究
- 在含有1.5%Bacto琼脂的Luria-Bertani(LB)琼脂平板(10 g / L色蛋白,5 g / L酵母提取物和5 g / L NaCl)上生长 枯草芽孢杆菌 11774,在37°C下。 在所有实验中,使用在37°C下在5mL LB肉汤中生长的第二传代细胞,直到OD600 = 1。以与步骤4.1相同的方式种植 肺炎链球 菌。
- 在获得OD600nm = 1( 枯草芽孢杆菌)或OD600nm = 0.4( 肺炎链球菌)的细胞培养密度后,使用移液管将masarimycin加入到标记为"处理"的培养管中,最终浓度为3.8μM(枯 草芽孢杆菌为0.75x MIC)或5.85μM( 肺炎链球菌为0.75x MIC)。向标有"对照"的第二培养管中,加入等量的DMSO。
- 对于 枯草芽孢杆菌,将样品置于37°C的培养箱中90分钟,以150rpm振荡。对于 肺炎链球菌, 在厌氧条件下孵育细胞而不摇晃。
- 90分钟后,在4°C下化学固定培养物在培养基和固定缓冲液(20mM HEPES,1%甲醛(pH 6.8))的1:10混合物(v / v)中过夜。固定完成后,使用移液器将10-20μL样品涂在玻璃显微镜载玻片上,并使其风干。通过使用本生燃烧器加热载玻片来固定风干样品。
- 加热固定后,加入100μL0.1%(m / v)亚甲基蓝(在20%(v / v)乙醇中的溶液)染色样品。将染色的载玻片孵育10分钟,并用dH2O洗去多余的染料。然后,在烤箱中轻轻加热染色载玻片至60°C15-20分钟,将细胞带到共同的焦平面。
- 通过在染色的细胞上放置显微镜盖玻片来密封染色的样品。然后,使用显微镜载玻片水泥密封边缘。将密封的显微镜载玻片放在显微镜载物台上,并使用明场显微镜以100倍放大倍率将图像聚焦。
- 在显微镜载玻片上滴一滴浸油,并使用1000倍放大倍率将视场聚焦。使用连接到显微镜及其相关软件的相机获取显微照片。使用软件上的自动白平衡和光圈设置采集图像。
注意:或者,可以使用开源ImageJ软件处理图像。
结果
马萨里霉素是枯草芽孢杆菌和肺炎链球菌的小分子抑菌抑制剂,已被证明可抑制枯草芽孢杆菌35,37中的外效GlcNAcase LytG,并靶向肺炎链球菌37中的细胞壁。马沙霉素可以通过经典或微波辅助有机合成有效制备,收率在55%-70%范围内。微波辅助合成的优点是可以显著缩短合成化合物的时间。微波辅助合成将合成?...
讨论
马沙霉素是 枯草芽孢杆菌35 和肺炎链球菌37 生长的单微摩尔抑菌抑制剂。在 枯草芽孢杆菌中, 马萨利霉素已被证明可以抑制GlcNAcase LytG35,而 肺炎链球菌 细胞壁中的精确分子靶标尚未确定37。使用经典的有机合成或微波程序合成马萨霉素为抑制剂提供了良好的产量和高纯度。马沙霉素的低产率通常可归?...
披露声明
Reid, C. W. 拥有涉及马萨里霉素特定应用的知识产权。
致谢
研究得到了美国国家科学基金会的支持,拨款编号为2009522。马沙霉素的NMR分析得到了美国国家科学基金会重大研究仪器计划奖的支持,授予号为1919644。本材料中表达的任何意见,发现和结论或建议均为作者的观点,并不一定反映美国国家科学基金会的观点。
材料
| Name | Company | Catalog Number | Comments |
| 2-Iodobenzoic acid | SIGMA-ALDRICH | I7675-25G | corrosive, irritant, light yellow to orange-brown powder |
| 2-Propanol | SIGMA-ALDRICH | 109827-4L | flammable, irritant, colorless liquid |
| Acetonitrile | SIGMA-ALDRICH | 34851-4L | flammable, irritant, colorless liquid |
| Aluminum backed silica plates | Sorbtech | 4434126 | silica gel XG F254 on aluminum backed plates |
| chloroform-d | SIGMA-ALDRICH | 151823-50G | solvent for NMR |
| Compact Mass Spectrometer | Advion-Interchim | Advion CMS | compact mass spectrometer equiped with APCI source and atmospheric solids analysis probe |
| Corning Costar 96 well flat bottom plates-sterile | fisher chemical | 07-200-90 | for synergy/antagonism assays |
| cover slips | fisher chemical | 12-547 | for microscopy |
| Cyclohexanecarboxaldehyde | CHEM-IMPEX INT'L INC. | 24451 | flammable, irritant, colorless to pink liquid |
| Cyclohexyl isocyanide | SIGMA-ALDRICH | 133302-5G | irritant, colorless liquid, extremly unpleasant odor |
| Cyclohexylamine | SIGMA-ALDRICH | 240648-100ML | corrosive, flammable, irritant, colorless liquid unless contaminated |
| Ethyl acetate | SIGMA-ALDRICH | 537446-4L | flammable, irritant, colorless liquid |
| flash silica cartridge (12g) | Advion-Interchim | PF-50SIHP-F0012 | pack of flash silica columns (12g) for purification of masarimycin |
| formaldehyde | SIGMA-ALDRICH | F8775-25ML | fixing agent for microscopy |
| HEPES | SIGMA-ALDRICH | H8651-25G | buffer for microscopy fixing solution |
| Hexane, mixture of isomers | SIGMA-ALDRICH | 178918-4L | environmentally damaging, flammable, irritant, health hazard, colorless liquid |
| High performance compact mass spectrometer | Advion | expression | Atmospheric Solids Analysis Probe (ASAP), low resolution |
| High Vac | eppendorf | Vacufuge plus | vacuum aided by centrifugal force and temperature |
| Hydrochloric acid | SIGMA-ALDRICH | 258148-2.5L | corrosive, irritant, colorless liquid |
| hydrochloric acid | SIGMA-ALDRICH | 320331-2.5L | strong acid |
| immersion oil | fisher chemical | 12-365-19 | for microscopy |
| Iodine, resublimed crystals | Alfa Aesar | 41955 | environmentally damaging, irritant, health hazard, dark grey/purple crystals |
| Mestre Mnova | MestreLab Research | software for processing NMR spectra | |
| Methanol | SIGMA-ALDRICH | 439193-4L | flammable, toxic, health hazard, colorless liquid |
| methylene blue | SIGMA-ALDRICH | M9140-25G | microscopy stain for staining cell walls |
| meuller-hinton agar plates + 5% sheep blood | fisher chemical | B21176X | growth media for Streptococcus pneumoniae |
| meuller-hinton broth | fisher chemical | DF0757-17-6 | growth media for Streptococcus pneumoniae |
| microscope slides | fisher chemical | 22-310397 | for microscopy |
| Microwave Synthesis Labstation | MILESTONE | START SYNTH | device that requires the ventilation of a fume hood, equipped with synthesis carousel |
| NMR tubes | SIGMA-ALDRICH | Z562769-5EA | 5mm NMR tubes 600 MHz |
| Nuclear Magnetic Resonance (NMR) | Bruker | Ascend 400 | large superconducting magnet (400MHz) |
| optochin | fisher chemical | AAB21627MC | ethylhydrocupreine hydrochloride |
| petrie plates | Celltreat | 229695 | for preparing agar plates for bacterial growth |
| Primo Star Bright field/Phase contrast Microscope with ERc5s camera | Zeiss | for morphology studies | |
| puriFlash | interchim | XS520plus | flash chromatography purification system |
| resazurin | SIGMA-ALDRICH | R7017-1G | for synergy/antagonism assays |
| Rotary Evaporator | Heidolph | Hei-VAP Value "The Collegiate" | solvent evaporator |
| Sodium bicarbonate | SIGMA-ALDRICH | S6014-500G | irritant, white powder |
| Sodium chloride | fisher chemical | S271-1 | crystalline, colorless |
| Sodium chloride | SIGMA-ALDRICH | S5886-500G | for growth of B.subtilis and preparation of LB media |
| Sodium sulfate | SIGMA-ALDRICH | 7985592-500G | anhydrous, granular, white |
| tryptone | fisher chemical | BP1421-500 | for growth of B.subtilis and preparation of LB media |
| Whitney DG250 Workstation | Microbiology International | DG250 | anaerobic workstation. Anaerobic gas mixture used: 5% hydrogen, 10% carbon dioxide, balance nitrogen |
| yeast extract | fisher chemical | BP1422-500 | for growth of B.subtilis and preparation of LB media |
| Zen Lite (blue) software | Zeiss | for acquiring micrographs |
参考文献
- Vollmer, W., Blanot, D., de Pedro, M. A. Peptidoglycan structure and architecture. FEMS Microbiology Review. 32 (2), 149-167 (2008).
- Munita, J. M., Bayer, A. S., Arias, C. A. Evolving resistance among Gram-positive pathogens. Clinical Infectious Diseases. 61, 48-57 (2015).
- Vollmer, W., Bertsche, U. Murein (peptidoglycan) structure, architecture and biosynthesis in Escherichia coli. Biochimica Biophysica Acta. 1778 (9), 1714-1734 (2008).
- Vollmer, W., Höltje, J. -. V. The architecture of the murein (peptidoglycan) in Gram-negative bacteria: vertical scaffold or horizontal layer(s). Journal of Bacteriology. 186 (18), 5978-5987 (2004).
- Clarke, A. J. Compositional analysis of peptidoglycan by high-performance anion-exchange chromatography. Analytical Biochemistry. 212 (2), 344-350 (1993).
- Kim, S. J., Chang, J., Singh, M. Peptidoglycan architecture of Gram-positive bacteria by solid-state NMR. Biochimica Biophysica Acta. 1848, 350-362 (2014).
- Koch, A. L., Doyle, R. J. Inside-to-outside growth and turnover of the wall of gram-positive rods. Journal of Theoretical Biology. 117 (1), 137-157 (1985).
- Beeby, M., Gumbart, J. C., Roux, B., Jensen, G. J. Architecture and assembly of the Gram-positive cell wall. Molecular Microbiology. 88 (4), 664-672 (2013).
- Shockman, G. D., Daneo-Moore, L., Kariyama, R., Massidda, O. Bacterial walls, peptidoglycan hydrolases, autolysins, and autolysis. Microbial Drug Resistance. 2 (1), 95-98 (1996).
- Dijkstra, A. J., Keck, W. Peptidoglycan as a barrier to transenvelope transport. Journal of Bacteriology. 178 (19), 5555-5562 (1996).
- Blackman, S. A., Smith, T. J., Foster, S. J. The role of autolysins during vegetative growth of Bacillus subtilis 168. Microbiology. 144, 73-82 (1998).
- Misra, G., Rojas, E. R., Gopinathan, A., Huang, K. C. Mechanical consequences of cell-wall turnover in the elongation of a Gram-positive bacterium. Biophysical Journal. 104 (11), 2342-2352 (2013).
- Wheeler, R., et al. Bacterial cell enlargement requires control of cell wall stiffness mediated by peptidoglycan hydrolases. mBio. 6 (4), 00660 (2015).
- Taguchi, A., Kahne, D., Walker, S. Chemical tools to characterize peptidoglycan synthases. Current Opinion in Chemical Biology. 53, 44-50 (2019).
- Welsh, M. A., Schaefer, K., Taguchi, A., Kahne, D., Walker, S. Direction of chain growth and substrate preferences of shape, elongation, division, and sporulation-family peptidoglycan glycosyltransferases. Journal of the American Chemial Society. 141 (33), 12994-12997 (2019).
- Rubino, F. A., et al. Detection of transport intermediates in the peptidoglycan flippase MurJ identifies residues essential for conformational cycling. Journal of the American Chemical Society. 142 (12), 5482-5486 (2020).
- Sjodt, M., et al. Structure of the peptidoglycan polymerase RodA resolved by evolutionary coupling analysis. Nature. 556 (7699), 118-121 (2018).
- Tiyanont, K., et al. Imaging peptidoglycan biosynthesis in Bacillus subtilis with fluorescent antibiotics. Proceedings of the National Academy of Science U S A. 103 (29), 11033-11038 (2006).
- Lebar, M. D., et al. Reconstitution of peptidoglycan cross-linking leads to improved fluorescent probes of cell wall synthesis. Journal of the American Chemical Society. 136 (31), 10874-10877 (2014).
- Do, T., Page, J. E., Walker, S. Uncovering the activities, biological roles, and regulation of bacterial cell wall hydrolases and tailoring enzymes. Journal of Biological Chemistry. 295 (10), 3347-3361 (2020).
- Liang, H., et al. Metabolic labelling of the carbohydrate core in bacterial peptidoglycan and its applications. Nature Communications. 8, 15015 (2017).
- DeMeester, K. E., et al. Metabolic incorporation of N-acetyl muramic acid probes into bacterial peptidoglycan. Current Protocol in Chemical Biology. 11 (4), 74 (2019).
- Lazor, K. M., et al. Use of Bioorthogonal N-acetylcysteamine (SNAc) analogues and peptidoglycan O-acetyltransferase B (PatB) to label peptidoglycan. The FASEB Journal. 32, 630 (2018).
- Wang, Y., Leimkuhler-Grimes, C. Fluorescent labeling of the carbohydrate backbone of peptidoglycan to track degradation in vivo. The FASEB Journal. 29, (2015).
- Kuru, E., et al. In probing of newly synthesized peptidoglycan in live bacteria with fluorescent D-amino acids. Angewandte Chemie International Edition. 51 (50), 12519-12523 (2012).
- Zhou, R., Chen, S., Recsei, P. A dye release assay for determination of lysostaphin activity. Analytical Biochemistry. 171 (1), 141-144 (1988).
- Qiao, Y., et al. Lipid II overproduction allows direct assay of transpeptidase inhibition by β-lactams. Nature Chemical Biology. 13 (7), 793-798 (2017).
- Lebar, M. D., et al. Forming cross-linked peptidoglycan from synthetic Gram-negative lipid II. Journal of the American Chemical Society. 135 (12), 4632-4635 (2013).
- Chen, R., Guttenplan, S. B., Blair, K. M., Kearns, D. B. Role of the D-dependent autolysins in Bacillus subtilis population heterogeneity. Journal of Bacteriology. 191 (18), 5775-5784 (2009).
- Yukie, S., Miki, K., Yoshio, N., Kuniaki, T., Yoshihisa, Y. Identification and characterization of an autolysin-encoding gene of Streptococcus mutans. Infection and Immunity. 73 (6), 3512-3520 (2005).
- Domenech, M., García, E., Moscoso, M. In vitro destruction of Streptococcus pneumoniae biofilms with bacterial and phage peptidoglycan hydrolases. Antimicrobial Agents and Chemotherapy. 55 (9), 4144-4148 (2011).
- Horsburgh, G. J., Atrih, A., Williamson, M. P., Foster, S. J. LytG of Bacillus subtilis is a novel peptidoglycan hydrolase: the major active glucosaminidase. Biochemistry. 42 (2), 257-264 (2003).
- Vermassen, A., et al. Cell wall hydrolases in bacteria: insight on the diversity of cell wall amidases, glycosidases and peptidases toward peptidoglycan. Frontiers in Microbiology. 10, 331 (2019).
- Martin-Galiano, A. J., Yuste, J., Cercenado, M. I., de la Campa, A. G. Inspecting the potential physiological and biomedical value of 44 conserved uncharacterised proteins of Streptococcus pneumoniae. BMC Genomics. 15, 652 (2014).
- Nayyab, S., et al. Diamide inhibitors of the Bacillus subtilis N-acetylglucosaminidase LytG that exhibit antibacterial activity. ACS Infectioius Diseases. 3 (6), 421-427 (2017).
- Lipski, A., et al. Structural and biochemical characterization of the β-N-acetylglucosaminidase from Thermotoga maritima: Toward rationalization of mechanistic knowledge in the GH73 family. Glycobiology. 25 (3), 319-330 (2014).
- Haubrich, B. A., et al. Inhibition of Streptococcus pneumoniae autolysins highlight distinct differences between chemical and genetic inactivation. bioRxiv. , 300541 (2020).
- Farha, M. A., et al. Inhibition of WTA synthesis blocks the cooperative action of PBPs and sensitizes MRSA to β-lactams. ACS Chemical Biology. 8 (1), 226-233 (2013).
- Lehár, J., et al. Chemical combination effects predict connectivity in biological systems. Molecular Systems Biology. 3 (1), 80 (2007).
- Farha, M. A., et al. Antagonism screen for inhibitors of bacterial cell wall biogenesis uncovers an inhibitor of undecaprenyl diphosphate synthase. Proceedings of the National Academy of Science U S A. 112 (35), 11048-11053 (2015).
- Palomino, J. C., et al. Resazurin microtiter assay plate: simple and inexpensive method for detection of drug resistance in Mycobacterium tuberculosis. Antimicrobial Agents and Chemotherapy. 46 (8), 2720-2722 (2002).
- Odds, F. C. Synergy, antagonism, and what the chequerboard puts between them. Journal of Antimicrobial Chemotherapy. 52 (1), 1 (2003).
- Arrigucci, R., Pozzi, G. Identification of the chain-dispersing peptidoglycan hydrolase LytB of Streptococcus gordonii. PLoS One. 12 (4), 0176117 (2017).
- Bai, X. -. H., et al. Structure of pneumococcal peptidoglycan hydrolase LytB reveals insights into the bacterial cell wall remodeling and pathogenesis. of Biological Chemistry. 289 (34), 23403-23416 (2014).
- Garcia, P., Gonzalez, M. P., Garcia, E., Lopez, R., Garcia, J. L. LytB, a novel pneumococcal murein hydrolase essential for cell separation. Molecular Microbiology. 31 (4), 1275-1281 (1999).
- Giladi, M., Altman-Price, N., Levin, I., Levy, L., Mevarech, M. FolM, a new chromosomally encoded dihydrofolate reductase in Escherichia coli. Journal of Bacteriology. 185 (23), 7015-7018 (2003).
- Chua, P. R., et al. Effective killing of the human pathogen Candida albicans by a specific inhibitor of non-essential mitotic kinesin Kip1p. Molecular Microbiology. 65 (2), 347-362 (2007).
- Rico-Lastres, P., et al. Substrate recognition and catalysis by LytB, a pneumococcal peptidoglycan hydrolase involved in virulence. Scientific Reports. 5, 16198 (2015).
- Vollmer, W., et al. The cell wall of Streptococcus pneumoniae. Microbiology Spectrum. 7 (3), (2019).
- Massidda, O., Nováková, L., Vollmer, W. From models to pathogens: how much have we learned about Streptococcus pneumoniae cell division. Environmental Microbiology. 15 (12), 3133-3157 (2013).
转载和许可
请求许可使用此 JoVE 文章的文本或图形
请求许可探索更多文章
This article has been published
Video Coming Soon
版权所属 © 2025 MyJoVE 公司版权所有,本公司不涉及任何医疗业务和医疗服务。