Method Article
可分散陶红四武片的形成
摘要
本文讨论了用于配制和制备陶虹四武(一种中药)作为分散片剂的过程。我们进行了单因素和正交实验,筛选处方辅料,优化配方工艺,生产出可分散的陶虹思武片。
摘要
在这里,我们优化了用于配制和制备可分散的陶虹思武片的工艺,并为扩大其临床应用奠定了基础。以分散均匀性和崩解时间为研究指标,采用单因素检验对桃红思武片的赋形剂类别进行匹配和过滤。通过正交试验设计对配方进行优化。采用超高效液相色谱(UPLC)法测定了可分散乳香四物片中有效物质的含量和溶出率,并确定了最佳制备工艺。
桃红四物可再分散片的最佳成分为17%桃红四武提取物粉、1%硬脂酸镁、49%微晶纤维素、20%交联聚乙烯吡咯烷酮、13%羧甲基淀粉钠。直接压片制备可再分散的陶虹四物片,优化后的处方粉在3 min内均匀分散,50 min内溶出率达到90%以上。按优化方法制备可分散的桃红四物片在水中崩解迅速,分散均匀性好,质量可控。
引言
桃红思武汤是由桃仁、红花、当归、白牡丹、川芎、地黄1,2组成的处方,可用于促进血液流动,减轻肿胀和疼痛3,4。先前的研究发现,桃红四武堂难以保存,容易受霉变等因素的影响。此外,常用的临床煎剂运输不方便,而煎煮过程费力且质量参差不齐。因此,迫切需要开发桃红四武片的新配方。
分散片是那些可以在水中迅速崩解并以均匀悬浮液分布的片剂5。在中药(TCM)中,分散片中的主要药物通常由中药粉,提取物和其他适当的赋形剂6的原料制备。与常规液体制剂和普通片剂相比,分散片作为一种新型剂型,在人体内吸收更快,表现出更好的稳定性,易于服用和运输,并表现出崩解快、生物利用度高、分散均匀性好等一系列有益特性7,8。
正交试验设计方法利用正交表科学地选择试验条件,安排合理的试验方案,然后利用范围和方差的数学概念对试验结果进行分析,生成最优方案9,10。在这项研究中,我们对某些关键特征特别感兴趣:分散的均匀性、整洁度和可比性。正交实验设计也可以适应合并分数和因子设计。本研究采用正交实验设计筛选和优化可分散陶红思武片的赋形剂类型、赋形剂配比和载药量数据。与传统的中药汤剂相比,本文所述方法制备的桃红四武分散片具有服用方便、保存方便、防霉性强等优点。
研究方案
1. 桃红提取物的制备
- 测量39.6克准备好的地黄根(地黄[Gaetn。利博斯。前菲施。等Mey.),桃仁29.7克(Prunus persica [L.] Batsch),19.8克红花(Carthamus tinctorius L.),29.7克当归(Angelica sinensis [Oliv.]。)、白牡丹根29.7克、川芎19.8克,共药材168.3克11,放入汤剂砂锅中。
- 进行煎煮三次。
- 每轮加入 1,683 mL 水,将成分煮沸 1.5 小时。
- 合并滤液,用纱布过滤所得液体。将液体浓缩在旋转蒸发器中至最终体积为 400 mL。
- 将浓缩物均匀倒入蒸发盘中,并置于90°C的水浴中以干燥多余的水。
- 将增稠的提取物置于85°C的真空干燥箱中,干燥8小时以获得干燥的提取物。
- 随后,将干燥的提取物在研钵中研磨成粉末,然后用80目筛子过筛。
注意:所得的干提取物是含有四种药用成分的粉红色草药粉的形式。
2. 填充剂的筛选
- 使用乳糖、预糊化淀粉和微晶纤维素作为填充剂。
- 使用交联聚乙烯吡咯烷酮(PVPP)作为崩解剂,硬脂酸镁作为润滑剂。
注意:使用三个公式来生成用于测试的处方。 - 制备配方1:0.5克药粉和3.4克微晶纤维素(MCC)生产填料,1克PVPP和0.1克硬脂酸镁生产润滑剂。
- 制备配方2:药粉0.5克,预糊化淀粉3.4克为填充剂,PVPP1克为崩解剂,硬脂酸镁0.1克为润滑剂。
- 制备配方3:药粉0.5克,乳糖3.4克为填充剂,PVPP1克为崩解剂,硬脂酸镁0.1克为润滑剂。
- 彻底混合每个处方,并通过80目筛网。将均匀混合的粉末放入单冲孔片剂机中,然后冲出一片。
- 分别测试每个平板电脑。将片剂放入装有1L37°C蒸馏水的烧杯中。
- 将烧杯放入溶出度测试仪(材料表)。
- 启动溶出度测试仪,并计时反应。当片剂完全崩解时,停止计时器,观察片剂是否均匀分散。
注意:我们将崩解时间和分散均匀性作为后续实验的指标。每个处方产生的数据在 表1中给出。
3. 崩解剂的选择
- 将三种赋形剂成对混合以创建三种不同的处方,并测试组合。
- 用 PVPP 和低取代羟丙基纤维素 (L-HPC) (1:1) 制备配方 1。
- 用L-HPC和羧甲基淀粉钠(CMS-NA)(1:1)制备配方2。
- 用PVPP和CMS-Na(1:1)制备配方3。
- 彻底混合每个处方,并通过80目筛网。将均匀混合的粉末放入单冲压片机中。
- 调查片剂的外观和形状。将平板电脑放在白色背景上,观察颜色的外观是否均匀。按照步骤2.7-2.9测量崩解时间。
注意:结果如 表2所示。
4. 优化填料和崩解剂用量
- 通过使用微晶纤维素的剂量作为因子A,交联聚乙烯吡咯烷酮的剂量作为因子B,羧甲基纤维素钠的剂量作为因子C,空白误差作为因子D进行正交实验,优化填充剂(步骤2)和崩解剂(步骤4)的特定剂量。
- 根据 表3制备赋形剂。分别称量赋形剂,并将三种配方混合均匀。
- 将配方通过筛网直径为0.18毫米的筛子。
- 将制剂压入片剂中。按照步骤2.7-2.9测量崩解时间。
注意:表 3 和 表4 显示了因子水平排列和正交实验安排。 - 将获得的数据导入电子表格软件进行数据分析。
注意: 表 5 显示了方差分析的结果, 图 1 显示了每个测试指数的趋势。
5. 药物负荷的筛选
注意:在填充剂和崩解剂测试之后,确定微晶纤维素,交联聚乙烯吡咯烷酮,羧甲基淀粉钠和硬脂酸镁的最佳含量分别为4.4g,1.8g,1.2g和0.1g。
- 在保持填充剂、崩解剂和润滑剂的相对含量恒定的同时,用 1 g 药粉准备处方 1,用 1.5 g 药粉准备处方 2,用 2 g 药粉准备处方 3,用 2.5 g 药粉准备处方 4。
- 充分混合每个处方中使用的粉末、填充剂、崩解剂和润滑剂,并通过 80 目筛。
- 按下片剂,然后将片剂放入崩解时间测试仪中。
- 启动仪器和时间;平板电脑完全分解后停止计时器。
注意:处方方案如 表6所示。
6. 桃红思武分散片的质量评价
- 外观评价
注:根据2020年版《中国药典通则010112》的要求,片剂外观应完整光滑,颜色应均匀。- 从三批中每批随机抽取六片,观察可再分散片表面是否光滑,颜色是否均匀。
- 重量变化
- 为了评估湿重,从每批中取出20片,并准确确定总重量。确定平均片剂重量。
- 分别称量每片。
- 将每片的重量与平均重量进行比较。
注意:平均重量与单个片剂重量之间的差异不应超过0.30克±7.5%。重量差异不应超过两片,任何单片的重量均不应超过限量一倍。
- 崩解和分散均匀性测试
注:根据中国药典第12通则0921的规定,我们确定了每批片剂的崩解时间。- 将吊舱挂在支架上,上端有不锈钢轴。将设备浸入 1 L 烧杯中,并调整吊舱的位置,使屏幕在下降到最低点时距离烧杯底部 25 毫米。
- 在烧杯中装满温度为37°C±1°C的水,并调整水位的高度,使当吊舱上升到最高点时,筛子位于水面以下15毫米。确保吊舱的顶部在任何时候都没有浸没在溶液中。
- 从每个测试批次中取出六片,并将它们放入吊舱的玻璃管中。
- 激活溶出度测试仪。
注意:每个片剂需要在15分钟内完全分解。 - 如果一片没有完全崩解,则再服用六片进行重新测试。所有平板电脑必须符合要求的规定。
7. 表征
- 色谱条件
- 使用色谱柱为2.1 mm x 100 mm(例如,ACQUITY UPLC BEH C18 1.7 μm)。
- 使用100%乙腈(A)和0.5%磷酸水溶液(B)的流动相。
- 对于梯度洗脱,请使用以下洗脱程序:0-4分钟(10%-30%),4-10分钟(30%-60%),10-15分钟(60%-85%),15-17分钟(85%-50%),17-20分钟(50%-110%),20-22分钟(10%-10%)。
- 使用0.2 mL/min的流速、260 nm的检测波长、30 °C的柱温、2 μL的进样体积。
- 溶液制备
- 准备苦杏仁苷参比溶液。将苦杏仁苷溶解在甲醇中,浓度为0.2 mg·mL−1。
- 准备测试溶液。
- 对于每个样品,用研钵压碎五片,并放入装有 25 mL 80% 甲醇的 25 mL 容量瓶中,体积按比例。
- 在150W和40kHz下超声处理每个样品30分钟以溶解。
- 将每个样品冷却至室温,然后加入 80% 甲醇至总体积为 25 mL。
- 最后,用微孔膜(0.22μm)过滤样品。使用基材作为产品进行测试。
- 线性关系分析
- 取1 mL参比溶液,用微孔滤膜(0.22 μm)过滤。
- 将0.5 μL、1 μL、1.5 μL、2 μL、2.5 μL和3 μL的参比溶液转移到色谱柱中,并按照第7.1节所述进行色谱。
- 进样样品,并记录峰面积。
- 使用峰面积(y)和进样体积(x)作为变量进行线性回归。
注意:获得的回归方程为 y = 18115x − 2386.6 (R² = 0.9993),因此表明苦杏仁苷在 0.0492-0.3101 mg 的范围内表现出良好的线性关系。 图 2 显示了标准曲线。
- 精密测试
- 取2 μL对照品溶液(按第5.2.1节所述制备)连续6次注入色谱仪。
- 记录峰面积,并计算相对标准偏差(RSD)值。
注意:苦杏仁苷峰面积的测量RSD值为2.7%,因此表明该仪器表现出良好的精密度。
- 重复性实验
- 为了评估重复性,将30片可分散片研磨成细粉,并将所得粉末混合在一起。
- 将混合的粉末分成六批,每批重约 1 克。
- 按照第 7.2.2 节中所述准备测试溶液。
- 每个样品进样 2 μL,记录峰面积,并计算 RSD 值。
注:测得的峰面积RSD值为1.8%,表明该方法具有良好的重复性。
- 稳定性实验
- 使用相同的测试溶液,在0小时,2小时,4小时,6小时,8小时,12小时和14小时注入2μL溶液。
- 记录峰面积,并计算RSD值。
注意:苦杏仁苷峰面积的测定RSD值为2.8%,因此表明供试品溶液在室温下稳定24小时。
- 样品回收测试
- 取分散片6个样品,按第7.2.2节所述方法制备供试品溶液。
- 向同一进样瓶中加入1 mL对照物质,根据第7.1节所述的条件测量样品含量,并计算回收率。
注:分析表明,苦杏仁苷的平均回收率为101%,RSD值为2.8%,表明该方法具有良好的准确性。
- 样品含量的测定
- 用三批分散片按照第7.2.2节给出的方法配制供试品溶液。
- 在第7.1节所述的色谱条件下,每个样品进样2 μL。
- 记录峰面积,并测量含量。
注:三批分散片中苦杏仁苷的平均含量为0.257mg/片。
- 溶出度测定
- 取6批分散片,照2020年版《中国药典12》规定的溶出度测定小杯法测定溶出率。
- 使用0.1M盐酸(250mL)作为溶解介质,并在37°C±0.5°C和100rpm下进行测试50分钟。
- 立即将样品通过微孔膜(0.22μm)。
- 进样并按照第7.1节所述的色谱条件进行测试。
- 记录峰面积和溶出速率。
注:六批样品的溶出率分别为98%、99%、96%、97%、97%和98%。
结果
本研究采用传统方法制备桃红四武汤液体提取物,经浓缩干燥制备中药粉。通过保持草药粉、崩解剂和润滑剂不变,我们筛选了 r-乳糖、预胶化淀粉和微晶纤维素作为填充剂,以确定崩解时间。虽然乳糖作为崩解剂的崩解时间优于预胶化淀粉和微晶纤维素,但硬度和表面光洁度不符合要求标准;因此,选择微晶纤维素作为填料。
为了选择合适的崩解剂,我们使用相同的草药粉末、填充剂和润滑剂建立了三种处方:处方 1(交联聚乙烯吡咯烷酮和低取代羟丙基纤维素)、处方 2(低取代羟丙基纤维素和羧甲基淀粉钠)和处方 3(交联聚乙烯吡咯烷酮和羧甲基淀粉钠);每种情况下的比例均为1:1。以外观、崩解时间和分散均匀性为检验指标,发现交联聚乙烯吡咯烷酮与钠的组合崩解时间和分散均匀性最优。接下来,我们进行了正交测试,以确定最佳的填料和崩解剂含量。使用4.4 g微晶纤维素(MCC,因子A),1.8 g交联聚乙烯吡咯烷酮(PVPP,因子B)和1.2 g羧甲基淀粉钠(CMS-Na,因子C)获得最佳结果。一旦我们确定了填充剂和崩解剂的最佳剂量和比例,我们接下来通过研究不同比例的崩解时间、分散均匀性和硬度来确定草药粉的最佳用量。 图3 显示,四种处方通过了色散均匀性评估。然而,随着药物负荷的增加,我们观察到分解时间更长,安全带减少。最终处方被确定为1.5克药粉,4.4克微晶纤维素,1.8克交联聚乙烯吡咯烷酮,1.2克羧甲基淀粉钠和0.1克硬脂酸镁。最终规格为每片0.30g,每次给药4片(每天3次);这相当于1.068克生药。
含量测定和溶出度试验表明,每片分散片中苦杏仁苷的含量为0.257 mg。在溶出度试验中,6批分散片在50 min时的溶出率分别为98%、99%、96%、97%、97%和98%,表明分散式桃红思武片溶出率良好。

图 1:测试指数的平均趋势。 测试指标的平均趋势图。图中因子A为桃红思武药粉含量,因子B为PVPP含量,因子C为CMS-Na含量,因子D为空白误差组。每个因子中的数字代表不同的内容(详见 表3 )。y 轴上的值表示 K 值,K 值越低表示结果越好。 请点击此处查看此图的大图。
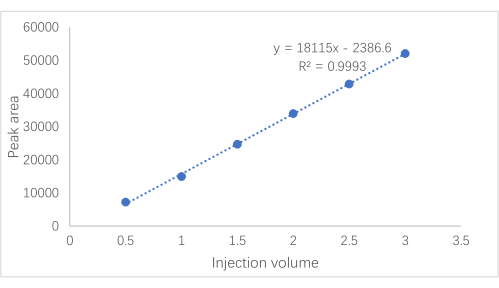
图 2:苦杏仁苷标准曲线。 苦杏仁苷的标准曲线,其中x轴代表进样体积,y轴代表峰面积。 请点击此处查看此图的大图。
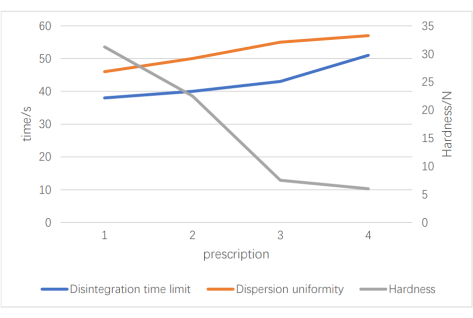
图3:药物负荷筛查结果。 该图显示了载药量结果;左Y轴是时间,右Y轴是硬度,X轴上的四个处方代表不同的载药量。 请点击此处查看此图的大图。
| 序号 | 药粉(g) | 聚氯乙烯 (g) | 世纪挑战委员会 (g) | 预胶化淀粉(g) | 乳糖 (g) | 解体时限 (s) | 外部 |
| 1 | 0.5 | 1 | 3.4 | 26 | 干净 | ||
| 2 | 0.5 | 1 | 3.4 | 54 | 干净 | ||
| 3 | 0.5 | 1 | 3.4 | 16 | 常见 |
表 1:填料选择结果。 3个处方中主要药物含量和PVPP剂量保持不变;处方1使用MCC作为填充剂,处方2使用预胶化淀粉作为填充剂,处方3使用乳糖作为填充剂。从这些中,乳糖作为填料的崩解时间最短,但光泽度不达标。
| 崩解剂处方 | 外部 | 解体时限 (s) | 分散均匀性 (s) |
| PVPP+L-HPC | 干净 | 39 | 39 |
| L-HPC+CMS-NA | 干净 | 40 | 52 |
| PVPP+CMS-Na | 干净 | 42 | 40 |
表2:崩解剂组合筛选。 在主药和填充剂不变的条件下,测试不同崩解剂组合的崩解时间限制和分散均匀性。处方1为PVPP + L-HPC,处方2为L-HPC + CMS-Na,处方3为PVPP + CMS-Na,其中PVPP + CMS-Na的组合具有最短的崩解时间限制。
| 水平 | 一(g) | 乙(g) | C(g) | D(g) |
| 1 | 3.4 | 0.6 | 0.4 | 空白 |
| 2 | 4.4 | 1.2 | 0.8 | 空白 |
| 3 | 5.4 | 1.8 | 1.2 | 空白 |
表 3:正交设计的因子水平。 每个处方的主要药物剂量保持不变。因子A是填料MCC的用量,因子B是PVPP的用量,因子C是CMS-Na的用量,因子D是空白误差。
| 编号 | 一(g) | 乙(g) | C(g) | D(空白) | 解体时限 (s) |
| 1 | 1 | 1 | 1 | 1 | 69 |
| 2 | 1 | 2 | 2 | 2 | 123 |
| 3 | 1 | 3 | 3 | 3 | 40 |
| 4 | 2 | 1 | 2 | 3 | 43 |
| 5 | 2 | 2 | 3 | 1 | 31 |
| 6 | 2 | 3 | 1 | 2 | 39 |
| 7 | 3 | 1 | 3 | 2 | 78 |
| 8 | 3 | 2 | 1 | 3 | 59 |
| 9 | 3 | 3 | 2 | 1 | 34 |
| K1 | 232 | 190 | 167 | 134 | |
| K2 | 113 | 213 | 200 | 240 | |
| K3 | 171 | 113 | 149 | 142 | |
| K1 | 77.333 | 66.333 | 55.667 | 44.667 | |
| K2 | 37.667 | 71 | 66.667 | 80 | |
| K3 | 57 | 37.667 | 49.667 | 47.333 | |
| R | 39.667 | 33.333 | 17 | 35.333 | |
| 主要和次要 | RA>RD>RB>RC |
表4:正交实验排列和实验结果。
| 差异来源 | 偏差平方和 | 自由度 | 均方 | F 值 | 凸显 |
| 一个 | 236.667 | 2 | 1180.333 | 1.016 | >0.05 |
| B | 1828.667 | 2 | 914.333 | 0.787 | >0.05 |
| C | 446 | 2 | 223 | 0.192 | >0.05 |
| D(错误) | 2322.667 | 2 | 1161.333 |
表 5:方差分析结果。
| 处方 | 药粉(g) | 世纪挑战委员会 (g) | 聚氯乙烯 (g) | CMS-Na (g) | 硬脂酸镁(g) |
| 1 | 1 | 4.4 | 1.8 | 1.2 | 0.1 |
| 2 | 1.5 | 4.4 | 1.8 | 1.2 | 0.1 |
| 3 | 2 | 4.4 | 1.8 | 1.2 | 0.1 |
| 4 | 2.5 | 4.4 | 1.8 | 1.2 | 0.1 |
表6:载药量制剂。 每个处方的MCC,PVPP和CMS-Na的剂量保持不变。处方1中主要药物的剂量为1g,处方2为1.5g,处方3为2g,处方4为2.5g。
| 批号 | 外部 | 平均纸张重量(g) | 重量差(g) | 平均硬度 (N) | 解体时限 (s) | 分散均匀性 (s) |
| 20220710 | 干净 | 0.1978 | 合格 | 22 | 39 | 43 |
| 20220711 | 干净 | 0.186 | 合格 | 21 | 35 | 41 |
| 20220712 | 干净 | 0.1948 | 合格 | 18 | 29 | 32 |
表7:桃红四物分散片的质量评价。 对3批样品进行了外观分析、平均重量分析、重量差检查、硬度检查、崩解时限检查和分散均匀性检查。
讨论
本研究采用正交设计,测试了填充剂、崩解剂和药粉剂用量对分散片崩解时间和分散均匀性的影响。我们发现优选的配方迅速崩解。在选择最合适的填充剂时,我们发现虽然乳糖表现出最短的崩解时间,但这些片剂的硬度不足。此外,片剂的表面不够光滑,有粉末损失和片剂松散的证据。因此,乳糖不符合适当填充剂的要求;因此,我们选择了微晶纤维素作为最佳填料。微晶纤维素是粉末或短棒形式的聚合物,具有很强的流动性,没有纤维结构13。而且,微晶纤维素无味,无毒,易崩解,与药物不反应。这种聚合物是制药工业中重要的赋形剂,可以有效地粘合药物成分以促进药物成型14。此外,该聚合物可促进药物组分的分解,同时增强药物强度,主要用作赋形剂、填充剂或药物释放改性剂,用于制备药片、药物颗粒和药物胶囊15,16。
崩解剂具有良好的吸水溶胀性能,可促进分散片在水中的均匀分散。目前,分散片中最常用的崩解剂是L-HPC,交联PVPP和CMS-Na17。本实验中,交联PVPP和CMS-Na的组合表现出最短的崩解时间。大多数分散片使用两种或多种崩解剂。崩解剂组合可改善崩解效果,降低成本18.在筛选载药量时,我们发现随着载药量的增加,片剂的硬度降低;这种作用可能与药材粉末19的性质有关。最后,通过配方优化用于制备分散片(含4种成分)的工艺。随后对崩解时间和分散均匀性进行索引。最终成分是药粉(17%),微晶纤维素(49%),交联聚乙烯吡咯烷酮(20%),羧甲基淀粉钠(13%)和硬脂酸镁(1%)。
与传统中药汤剂相比,分散片可发挥良好的治疗效果,生物利用度高,稳定性好,便于携带,特别是对于服用煎剂困难和吞咽困难的患者20,21。在中药中,分散片中的主要药物通常不是单一化合物;相反,该药物由复杂的成分混合物组成。此外,这种粉末具有相对较高的粘度,通常能够吸收水分。以中药粉为主要药物的普通片剂存在崩解时间长、分散均匀性差等多种问题,影响疗效。因此,在本次研究中,我们设计了一种新的配方——分散片,为桃红四物汤解决了传统煎剂的相关问题,从而扩大了应用范围,促进了体内吸收22.在这项研究中,我们应用水提取方法从药材中提取干粉。传统的煎煮方法涉及复杂的成分,可以根据有效成分和活性成分的特性提取。此外,在分散片中可以增加活性成分的含量。药材中杂质的分离及其活性成分的保存是制备过程中应仔细考虑的问题。为后续分散片的制备提供有利条件也很重要。传统的汤剂,如桃红四武汤,通常含糖量很高。草药粉可以很容易地制备,以便它们吸收水分。因此,在制备过程中干燥时采取预防措施很重要。此外,成品片剂应防潮。
需要注意的是,本研究在含量测定实验中仅调查了一个指标成分;这代表了这项研究的一个显着局限性,尽管我们的工作为随后的深入研究提供了关键的基础。将桃红思武汤剂改造成方便患者、更实用、更可行的分散片,也符合中药制剂的发展趋势。
披露声明
作者声明不存在利益冲突。
致谢
本研究得到了国家自然科学基金(批准号82074059)、安徽中医药大学新安医学教育部重点实验室开放基金(No.2022XAYX07)、安徽省中药复方重点实验室开放基金项目(No.2019AKLCMF03)、安徽省学术带头人储备人资助项目(No. 2022H287), 安徽省卫生科研重点项目(AHWJ2022a013)
材料
| Name | Company | Catalog Number | Comments |
| Acetonitrile | OCEANPAK | A22T0218 | |
| Carboxymethyl starch sodium | Maclean | C12976293 | |
| Crosslinked Polyvinylpyrrolidone | Maclean | C12976293 | |
| Disintegration time limit tester | Tianjin Guoming Pharmaceutical Equipment Co., Ltd. | BJ-2 | |
| Electric heating constant temperature drying oven | Shanghai Sanfa Scientific Instrument Co., Ltd. | DHG-9202·2 | |
| Electric thermostatic water bath | Shanghai Sanfa Scientific Instrument Co., Ltd. | DK-S24 | |
| Electronic Balance | Sartorius Scientific Instruments (Beijing) Co., Ltd. | SQP | |
| Intelligent Dissolution Tester | Tianda Tianfa Technology Co., Ltd. | ZRS-8L | |
| Lactose | Maclean | C12942141 | |
| Low-Substituted Hydroxypropyl Cellulose | Anhui Shanhe Pharmaceutical Excipients Co., Ltd. | 190219 | |
| Magnesium stearate | Maclean | C12894996 | |
| Methyl Alcohol | TEDIA High Purity Solvents | 22075365 | |
| Microcrystalline cellulose | Maclean | 13028716 | |
| Single punch tablet machine | Nantong Shengkaia Machinery Co., Ltd. | TDP-2A | |
| Tablet hardness tester | Shanghai Huanghai Drug Testing Instrument Co., Ltd. | YPJ-200B | |
| Taohong Siwu Soup Extract | self made | ||
| Taoren, Honghua, etc. traditional Chinese medicine | The First Affiliated Hospital of Anhui University of Chinese Medicine | ||
| Waters Acquity H-Class Ultra High Liquid Chromatography |
参考文献
- Wang, J. Y., et al. Effects of Erchen decoction and Taohong Siwu decoction on Nox4/NF-κB/HIF-1αsignaling pathway in aorta of ApoE~(-/-) atherosclerosis mice. China Journal of Traditional Chinese Medicine and Pharmacy. , (2019).
- Aslani, A., Ghasemi, A., Esfahani, S. K. Design, formulation and physicochemical evaluation of dimenhydrinate orally disintegrating tablets. Galen Medical Journal. 7, 936 (2018).
- Chen, K. X., Jiang, H. L., Luo, X. M., Shen, J. H. Drug discovery in post-genome era: Trend and practice. Chinese Journal of Natural Medicines. 2, 257-260 (2004).
- Wang, M., Liu, Z., Hu, S., Duan, X., Han, L. Taohong Siwu decoction ameliorates ischemic stroke injury via suppressing pyroptosis. Frontiers in Pharmacology. 11, 590453 (2020).
- Xin, R. H., Liang, G., Zheng, J. F. Design and content determination of Genhuang dispersible tablet herbal formulation. Pakistan Journal of Pharmaceutical Sciences. 30, 655-661 (2017).
- Yulin, D., Junxue, P., Rong, L., Jianlin, Y. Comparison of oral preparations of Chinese medicine dispersible tablets and traditional Chinese medicine. Chinese Journal of Ethnomedicine and Ethnopharmacy. 26 (8), 63-65 (2017).
- Yinghua, X., et al. Study on albendazole dispersible tablets based on solubilization effect. Journal of Hebei University of Science and Technology. 42 (6), 619-626 (2021).
- Mengzhu, Y., Kai, Y., Yi, H. Study on the prescription optimization and dissolution of Baicalin Dispersible Tablets. China Medical Herald. 10 (1), 122-123 (2013).
- Zhongan, X., et al. Introduction to the orthogonal experimental design method. Sci-Tech Information Development & Economy. (5), 1005 (2002).
- Liu Ruijiang, Z. Y., Chongwei, W., Jian, T. Study on the design and analysis methods of orthogonal experiment. Experimental Technology and Management. 27 (9), 4 (2010).
- Xianchun, D. Based on network pharmacology and transcriptomics to explore the main material basis and mechanism of ThaoHongSiWu Decoction in treating ischemic stroke. Anhui University of Chinese Medicine. , (2019).
- Pharmacopoeia Commission of the Ministry of Health of the People's Republic of China. . Pharmacopoeia of the People's Republic of China. , (2020).
- Jiaqiang, Y., et al. Research progress on preparation and application of microcrystalline cellulose. China Pulp & Paper Industry. 42 (10), 8-13 (2021).
- Nakamura, S., Tanaka, C., Yuasa, H., Sakamoto, T. Utility of microcrystalline cellulose for improving drug content uniformity in tablet manufacturing using direct powder compression. AAPS PharmSciTech. 20 (4), 151 (2019).
- Jinbao, L., et al. Effect of alkali pretreatment on preparation of microcrystalline cellulose. China Pulp & Paper. 39 (01), 26-32 (2020).
- Nsor-Atindana, J., et al. Functionality and nutritional aspects of microcrystalline cellulose in food. Carbohydrate Polymers. 172, 159-174 (2017).
- Wang, C., et al. Formulation and evaluation of nanocrystalline cellulose as a potential disintegrant. Carbohydrate Polymers. 130, 275-279 (2015).
- Huba, K., István, A. Drug excipients. Current Medicinal Chemistry. 13 (21), 2535-2563 (2006).
- Ping, Z., Jie, G. Talking about some problems of hardness and disintegration in traditional Chinese medicine tablets. Science and Wealth. 6 (181), 181 (2020).
- Pabari, R. M., McDermott, C., Barlow, J., Ramtoola, Z. Stability of an alternative extemporaneous captopril fast-dispersing tablet formulation versus an extemporaneous oral liquid formulation. Clinical Therapeutics. 34 (11), 2221-2229 (2012).
- Fini, A., Bergamante, V., Ceschel, G. C., Ronchi, C., de Moraes, C. A. F. Fast dispersible/slow releasing ibuprofen tablets. European Journal of Pharmaceutics and Biopharmaceutics. 69 (1), 335-341 (2008).
- Meidan, W. Study on compound Rhodiola relieving physical fatigue dispersible tablets. Jilin University. , (2009).
转载和许可
请求许可使用此 JoVE 文章的文本或图形
请求许可探索更多文章
This article has been published
Video Coming Soon
版权所属 © 2025 MyJoVE 公司版权所有,本公司不涉及任何医疗业务和医疗服务。