Method Article
Formação de comprimidos de Taohong Siwu dispersíveis
Neste Artigo
Resumo
Este artigo discute o processo usado para formular e preparar Taohong Siwu, uma medicina tradicional chinesa, como um comprimido dispersível. Realizamos experimentos ortogonais e de fator único para selecionar os excipientes de prescrição, otimizar o processo de formulação e produzir comprimidos de Taohong Siwu dispersíveis.
Resumo
Aqui, otimizamos o processo usado para formular e preparar comprimidos Taohong Siwu dispersíveis e fornecemos uma base para expandir sua aplicação clínica. Tomando a uniformidade de dispersão e o tempo de desintegração como índices para investigação, usamos um teste de fator único para combinar e filtrar as categorias de excipientes para comprimidos de Taohong Siwu. A formulação foi otimizada por um desenho de teste ortogonal. O conteúdo e as taxas de dissolução das substâncias efetivas em comprimidos dispersíveis de Taohong Siwu quando preparados com prescrições otimizadas foram determinados por cromatografia líquida de ultra-alta eficiência (UPLC), e o processo de preparação ideal foi determinado.
A composição ótima para os comprimidos dispersíveis de Taohong Siwu foi 17% de extrato de Taohong Siwu em pó, 1% de estearato de magnésio, 49% de celulose microcristalina, 20% de polivinilpirrolidona reticulada e 13% de carboximetilamido sódico. Quando comprimidos de Taohong Siwu dispersíveis foram preparados por compressão direta e o pó de prescrição otimizado foi uniformemente disperso dentro de 3 min, a taxa de dissolução atingiu mais de 90% dentro de 50 min. Quando preparados de acordo com os métodos otimizados, os comprimidos de Taohong Siwu dispersíveis se desintegram rapidamente em água com boa uniformidade de dispersão e qualidade controlável.
Introdução
A decocção de Taohong Siwu é uma prescrição composta por semente de pêssego, cártamo, angélica, peônia branca, ligusticum chuanxiong e rehmannia 1,2 que pode ser usada para promover o fluxo sanguíneo e reduzir a detumescência e a dor 3,4. Pesquisas anteriores descobriram que Taohong Siwu Tang é difícil de preservar e facilmente afetado pelo míldio e outros fatores. Além disso, a decocção clínica comumente usada é inconveniente para o transporte, enquanto o procedimento de decocção é trabalhoso e sujeito a variações na qualidade. Portanto, há uma necessidade urgente de desenvolver uma nova formulação para comprimidos de Taohong Siwu.
As pastilhas dispersíveis são aquelas que podem ser rapidamente desintegradas em água e distribuídas em suspensões uniformes5. Na medicina tradicional chinesa (MTC), o principal fármaco em comprimidos dispersíveis é normalmente preparado a partir das matérias-primas do pó de MTC, extratos e outros excipientes apropriados6. Comparados às preparações líquidas convencionais e aos comprimidos comuns, os comprimidos dispersíveis, como uma nova forma farmacêutica, são mais rapidamente absorvidos no corpo humano, apresentam melhor estabilidade, são fáceis de tomar e transportar e exibem uma série de características benéficas, como rápida desintegração, alta biodisponibilidade e boa uniformidade de dispersão 7,8.
O método de planejamento de teste ortogonal utiliza uma tabela ortogonal para selecionar cientificamente as condições de teste, organizar um plano de teste razoável e, em seguida, usar os conceitos matemáticos de amplitude e variância para analisar os resultados do teste e gerar um plano ótimo 9,10. Neste estudo, estamos particularmente interessados em algumas características-chave: a uniformidade da dispersão, a limpeza e a comparabilidade. Planejamentos experimentais ortogonais também podem ser adaptados para incorporar um planejamento fracionário e fatorial. No presente estudo, usamos um planejamento experimental ortogonal para selecionar e otimizar os tipos de excipientes, as razões de excipientes e os dados de carregamento de fármacos para comprimidos de Taohong Siwu dispersíveis. Em comparação com decocções tradicionais da medicina chinesa, os comprimidos dispersíveis de Taohong Siwu preparados pela metodologia aqui descrita são fáceis de tomar, fáceis de preservar e altamente resistentes ao mofo.
Protocolo
1. Preparação do extracto de Taohong
- Medir 39,6 g de raiz de rehmannia preparada (Rehmannia glutinosa [Gaetn.] Libosch. ex Fisch. et Mey.), 29,7 g de amêndoa de pêssego (Prunus persica [L.] Batsch), 19,8 g de cártamo (Carthamus tinctorius L.), 29,7 g de angélica (Angelica sinensis [Oliv.] Diels), 29,7 g de raiz de peônia branca (Cynanchum otophyllum Schneid) e 19,8 g de ligusticum chuanxiong (Ligusticum chuanxiong hort), totalizando 168,3 g demedicamentos11, e colocar esses ingredientes em uma caçarola de decocção.
- Execute a decocção três vezes.
- Para cada rodada, adicione 1.683 mL de água e ferva os ingredientes por 1,5 h.
- Combine o filtrado e filtre o líquido resultante com gaze. Concentrar o líquido em um evaporador rotativo até um volume final de 400 mL.
- Despeje uniformemente o concentrado em uma placa de evaporação e coloque em banho-maria a 90 °C para secar o excesso de água.
- Colocar o extracto espessado numa estufa de secagem a vácuo a 85 °C e secar durante 8 h para obter um extracto seco.
- Posteriormente, triture o extrato seco em pó em uma argamassa e, em seguida, peneire com uma peneira de 80 malhas.
NOTA: O extrato seco resultante foi na forma de um pó de ervas rosa contendo os quatro ingredientes medicinais.
2. Triagem dos preenchedores
- Use lactose, amido pré-gelatinizado e celulose microcristalina como cargas.
- Use polivinil pirrolidona reticulada (PVPP) como desintegrante e estearato de magnésio como lubrificante.
OBS: Foram utilizadas três fórmulas para gerar as prescrições dos exames. - Preparar a Fórmula 1: 0,5 g de pó medicinal e 3,4 g de celulose microcristalina (MCC) para produzir o enchimento e 1 g de PVPP e 0,1 g de estearato de magnésio para produzir o lubrificante.
- Preparar a Fórmula 2: 0,5 g de pó medicinal, 3,4 g de amido pré-gelatinizado como enchimento, 1 g de PVPP como desintegrante e 0,1 g de estearato de magnésio como lubrificante.
- Prepare a Fórmula 3: 0,5 g de pó medicinal, 3,4 g de lactose como enchimento, 1 g de PVPP como desintegrante e 0,1 g de estearato de magnésio como lubrificante.
- Misture bem cada prescrição e passe por uma tela de 80 mesh. Coloque o pó misturado uniformemente em uma única máquina de comprimidos perfurados e perfure um comprimido.
- Teste cada comprimido separadamente. Colocar o comprimido num copo com 1 L de água destilada a 37 °C.
- Coloque o copo em um testador de dissolução (Tabela de Materiais).
- Inicie o testador de dissolução e cronometre a reação. Quando os comprimidos estiverem completamente desintegrados, pare o temporizador e observe se os comprimidos estão uniformemente dispersos.
NOTA: Consideramos o tempo de desintegração e a uniformidade de dispersão como indicadores nos experimentos subsequentes. Os dados decorrentes de cada prescrição encontram-se na Tabela 1.
3. Seleção de desintegrantes
- Misture os três excipientes em pares para criar três prescrições diferentes e teste as combinações.
- Preparar a formulação 1 com PVPP e hidroxipropilcelulose de baixa substituição (L-HPC) (1:1).
- Preparar a formulação 2 com L-HPC e carboximetilamido sódico (CMS-NA) (1:1).
- Preparar a formulação 3 com PVPP e CMS-Na (1:1).
- Misture bem cada prescrição e passe por uma tela de 80 mesh. Coloque o pó misturado uniformemente em uma única máquina de comprimidos perfurados.
- Investigue a aparência e a forma dos comprimidos. Coloque os comprimidos em um fundo branco e observe se a aparência da cor é uniforme. Meça o tempo de desintegração de acordo com as etapas 2.7-2.9.
NOTA: Os resultados são mostrados na Tabela 2.
4. Otimização da dosagem de enchimento e desintegrante
- Otimizar a dosagem específica dos preenchedores (etapa 2) e desintegrantes (etapa 4) realizando um experimento ortogonal utilizando a dosagem de celulose microcristalina como fator A, a dosagem de polivinilpirrolidona reticulada como fator B, a dosagem de carboximetilcelulose sódica como fator C e o erro em branco como fator D.
- Preparar os excipientes de acordo com a Tabela 3. Pese os excipientes separadamente e misture as três formulações uniformemente.
- Passar as formulações por uma peneira com diâmetro de tela de 0,18 mm.
- Pressione as formulações em comprimidos. Meça o tempo de desintegração de acordo com as etapas 2.7-2.9.
OBS: A Tabela 3 e a Tabela 4 mostram o arranjo fatorial e o arranjo ortogonal do experimento. - Importar os dados obtidos para um software de planilha eletrônica para análise dos dados.
NOTA: A Tabela 5 mostra os resultados da análise de variância e a Figura 1 mostra as tendências para cada índice de teste.
5. Triagem da carga medicamentosa
NOTA: Após os testes de carga e desintegrante, os teores ótimos de celulose microcristalina, polivinilpirrolidona reticulada, carboximetilamido de sódio e estearato de magnésio foram determinados em 4,4 g, 1,8 g, 1,2 g e 0,1 g, respectivamente.
- Mantendo constante o conteúdo relativo do enchimento, desintegrante e lubrificante, prepare a prescrição 1 com 1 g de pó medicinal, a prescrição 2 com 1,5 g de pó medicinal, a prescrição 3 com 2 g de pó medicinal e a prescrição 4 com 2,5 g de pó medicinal.
- Misture bem o pó, o agente de enchimento, o desintegrante e o lubrificante usados em cada prescrição e passe por uma peneira de 80 malhas.
- Pressione os tablets e coloque um tablet no testador de tempo de desintegração.
- Iniciar o instrumento e o tempo; Pare o temporizador depois que o tablet se desintegrou completamente.
NOTA: O cronograma de prescrição é mostrado na Tabela 6.
6. Avaliação da qualidade dos comprimidos dispersíveis Taohong Siwu
- Avaliação da aparência
NOTA: De acordo com os requisitos da edição de 2020 da Farmacopeia Chinesa Regra Geral 010112, a aparência do comprimido deve ser completa e suave, e a cor deve ser uniforme.- Selecione aleatoriamente seis peças de cada um dos três lotes para observar se a superfície da folha dispersível é lisa e se a cor é uniforme.
- Variação de peso
- Para a avaliação do peso úmido, tome 20 comprimidos de cada lote e determine com precisão o peso total. Determine o peso médio do comprimido.
- Pese cada comprimido separadamente.
- Compare o peso de cada comprimido com o peso médio.
NOTA: A diferença entre o peso médio e o peso de um comprimido individual não deve exceder 0,30 g ± 7,5%. A diferença de peso não deve exceder a de dois comprimidos, e o peso de nenhum comprimido deve exceder o limite por um fator de um.
- Testes de uniformidade de desintegração e dispersão
NOTA: De acordo com as disposições da Regra Geral 0921 da FarmacopeiaChinesa 12, determinamos o tempo de desintegração para cada lote de comprimidos.- Pendure uma gôndola em um suporte com o eixo de aço inoxidável na extremidade superior. Mergulhe o aparelho em um copo de 1 L e ajuste a posição da gôndola de modo que a tela fique a 25 mm da parte inferior do copo quando ela cair para seu ponto mais baixo.
- Encha o copo com água a uma temperatura de 37 °C ± 1 °C e ajuste a altura do nível de água de modo a que a peneira esteja 15 mm abaixo da superfície da água quando a gôndola subir ao seu ponto mais alto. Certifique-se de que a parte superior da gôndola não esteja submersa em solução em nenhum ponto.
- Tome seis comprimidos de cada lote de teste e coloque-os em um tubo de vidro na gôndola.
- Ative o testador de dissolução.
NOTA: Cada tablet precisa ser completamente desintegrado dentro de 15 min. - Se um comprimido não estiver completamente desintegrado, tome outros seis comprimidos para novo teste. Todos os comprimidos devem atender aos regulamentos exigidos.
7. Caracterização
- Condições cromatográficas
- Use uma coluna cromatográfica com uma coluna de 2,1 mm x 100 mm (por exemplo, ACQUITY UPLC BEH C18 1,7 μm).
- Utilizar uma fase móvel de acetonitrila a 100% (A) e solução aquosa de ácido fosfórico a 0,5% (B).
- Para eluição do gradiente, use o seguinte programa de eluição: 0-4 min (10%-30%), 4-10 min (30%-60%), 10-15 min (60%-85%), 15-17 min (85%-50%), 17-20 min (50%-110%), 20-22 min (10%-10%).
- Use um fluxo de 0,2 mL/min, um comprimento de onda de detecção de 260 nm, uma temperatura da coluna de 30 °C e um volume de injeção de 2 μL.
- Preparação da solução
- Prepare uma solução de referência de amígdala. Dissolver a amígdala em metanol na concentração de 0,2 mg·mL−1.
- Prepare uma solução de teste.
- Para cada amostra, triturar cinco comprimidos com uma argamassa e colocar num balão volumétrico de 25 ml com 25 ml de metanol a 80%, volumétrico a escalonamento.
- Ultrasonicate cada amostra a 150 W e 40 kHz por 30 min para dissolver.
- Arrefecer cada amostra à temperatura ambiente e, em seguida, adicionar 80% de metanol a um volume total de 25 ml.
- Finalmente, filtrar a amostra com uma membrana microporosa (0,22 μm). Use o substrato como produto para teste.
- Análise de relações lineares
- Tomar 1 ml da solução de referência e filtrar com uma membrana filtrante microporosa (0,22 μm).
- Transferir 0,5 μL, 1 μL, 1,5 μL, 2 μL, 2,5 μL e 3 μL da solução de referência para a coluna de cromatografia e efectuar a cromatografia conforme descrito no ponto 7.1.
- Injete a amostra e registre a área do pico.
- Realizar regressão linear utilizando a área do pico (y) e o volume de injeção (x) como variáveis.
OBS: A equação de regressão obtida foi y = 18115x − 2386,6 (R² = 0,9993), indicando que a amígdala apresenta boa relação linear na faixa de 0,0492-0,3101 mg. A Figura 2 mostra a curva padrão.
- Testes de precisão
- Injectar 2 μL da solução de referência (preparada como descrito no ponto 5.2.1) no cromatógrafo seis vezes sucessivas.
- Registre a área do pico e calcule o valor do desvio padrão relativo (RSD).
OBS: O valor medido da RSD para a área do pico da amigdalina foi de 2,7%, indicando que o instrumento apresentou boa precisão.
- Experimentos de repetibilidade
- Para avaliar a repetibilidade, triture 30 comprimidos dispersíveis em um pó fino e misture os pós resultantes.
- Divida o pó agrupado em seis lotes pesando aproximadamente 1 g cada.
- Preparar a solução de ensaio conforme descrito no ponto 7.2.2.
- Injetar 2 μL de cada amostra, registrar a área do pico e calcular o valor de RSD.
OBS: O valor medido da área do pico de RSD foi de 1,8%, indicando que o método apresentou boa repetibilidade.
- Experimentos de estabilidade
- Usando a mesma solução de teste, injetar 2 μL de solução a 0 h, 2 h, 4 h, 6 h, 8 h, 12 h e 14 h.
- Registre a área de pico e calcule o valor RSD.
NOTA: O valor medido de RSD da área de pico da amígdala foi de 2,8%, indicando que a solução teste foi estável por 24 h à temperatura ambiente.
- Teste de recuperação de amostra
- Colher seis amostras de comprimidos dispersíveis e preparar soluções de ensaio de acordo com o método descrito no ponto 7.2.2.
- Adicionar 1 ml da substância de controlo ao mesmo frasco de injecção, medir o teor da amostra de acordo com as condições descritas no ponto 7.1 e calcular a taxa de recuperação.
OBS: A análise mostrou que a taxa média de recuperação da amígdala (n = 6) foi de 101% e que o valor de RSD foi de 2,8%, indicando que o método apresentou boa acurácia.
- Determinação do teor da amostra
- Utilizar três lotes de comprimidos dispersíveis para preparar soluções de ensaio de acordo com o método indicado no ponto 7.2.2.
- Injectar 2 μL de cada amostra nas condições cromatográficas descritas no ponto 7.1.
- Registre a área do pico e meça o conteúdo.
NOTA: O teor médio de amigdalina nos três lotes de comprimidos dispersíveis foi de 0,257 mg/comprimido.
- Determinação da dissolução
- Tome seis lotes de comprimidos dispersíveis e meça a taxa de dissolução de acordo com o método de copo pequeno para determinação de dissolução descrito na edição de 2020 da Farmacopeia Chinesa12.
- Utilizar 0,1 M de ácido clorídrico (250 ml) como meio de dissolução e efectuar os ensaios a 37 °C ± 0,5 °C e 100 rpm durante 50 minutos.
- Passar imediatamente as amostras através de uma membrana microporosa (0,22 μm).
- Injectar e ensaiar de acordo com as condições cromatográficas descritas no ponto 7.1.
- Registre a área do pico e a taxa de dissolução.
NOTA: As taxas de dissolução dos seis lotes de amostras foram de 98%, 99%, 96%, 97%, 97% e 98%, respectivamente.
Resultados
Neste estudo, foi utilizado um método tradicional para preparar extratos líquidos de decocção de Taohong Siwu e preparado um pó de ervas por concentração e secagem. Mantendo o pó de ervas, desintegrante e lubrificante inalterados, selecionamos r-lactose, amido pré-gelatinizado e celulose microcristalina como cargas para determinar o tempo de desintegração. Embora o tempo de desintegração com lactose como desintegrante tenha sido melhor do que com amido pré-gelatinizado e celulose microcristalina, a dureza e o acabamento superficial não atenderam aos padrões exigidos; assim, a celulose microcristalina foi selecionada como carga.
Para selecionar um desintegrante adequado, estabelecemos três prescrições com o mesmo pó de ervas, carga e lubrificante: prescrição 1 (polivinilpirrolidona reticulada e hidroxipropilcelulose de baixa substituição), prescrição 2 (hidroxipropilcelulose de baixa substituição e carboximetilamido de sódio) e prescrição 3 (polivinilpirrolidona reticulada e carboximetilamido de sódio); a proporção foi de 1:1 em cada caso. Tomando a aparência, o tempo de desintegração e a uniformidade de dispersão como indicadores de inspeção, descobrimos que o tempo combinado de desintegração e uniformidade de dispersão de polivinilpirrolidona reticulada e sódio foi ótimo. Em seguida, realizamos testes ortogonais para identificar o conteúdo ideal de preenchimento e desintegrante. Os melhores resultados foram obtidos com 4,4 g de celulose microcristalina (CCM, Fator A), 1,8 g de polivinilpirrolidona reticulada (PVPP, Fator B) e 1,2 g de carboximetilamido sódico (CMS-Na, Fator C). Uma vez identificadas a dosagem e as proporções ideais de enchimento e desintegrante, identificamos a quantidade ótima de pó vegetal investigando o tempo de desintegração, uniformidade de dispersão e dureza de diferentes proporções. A Figura 3 mostra que as quatro prescrições passaram na avaliação da uniformidade de dispersão. No entanto, com uma carga maior de drogas, observamos um maior tempo de desintegração e uma redução no arnês. A prescrição final foi identificada como 1,5 g de pó medicinal, 4,4 g de celulose microcristalina, 1,8 g de polivinilpirrolidona reticulada, 1,2 g de carboximetilamido sódico e 0,1 g de estearato de magnésio. A especificação final foi de 0,30 g por comprimido e quatro comprimidos por administração (três vezes ao dia); Isso equivalia a 1,068 g da droga bruta.
A determinação do conteúdo e os testes de dissolução mostraram que o conteúdo de amigdalina em cada comprimido dispersível foi de 0,257 mg. No teste de dissolução, as taxas de dissolução dos seis lotes de comprimidos dispersíveis em 50 min foram de 98%, 99%, 96%, 97%, 97% e 98%, respectivamente, indicando que a taxa de dissolução dos comprimidos dispersíveis Taohong Siwu foi boa.

Figura 1: Tendência média dos índices de teste. O gráfico de tendência média para os indicadores de teste. O fator A na figura é o conteúdo do pó de medicamento Taohong Siwu, o fator B é o conteúdo de PVPP, o fator C é o conteúdo de CMS-Na, e o fator D é o grupo de erro em branco. Os números em cada fator representam conteúdos diferentes (veja a Tabela 3 para detalhes). O valor no eixo y representa o valor de K, e valores K mais baixos indicam melhores resultados. Clique aqui para ver uma versão maior desta figura.
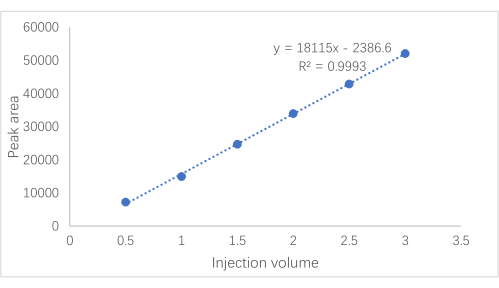
Figura 2: Curva padrão de Laetrile. A curva padrão da amigdalina, com o eixo x representando o volume de injeção e o eixo y representando a área do pico. Clique aqui para ver uma versão maior desta figura.
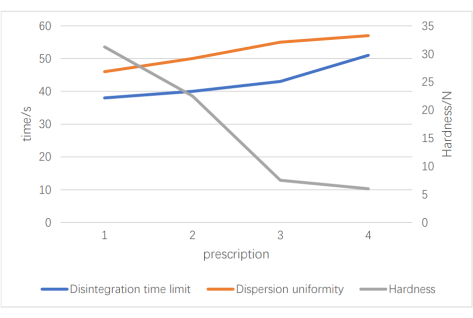
Figura 3: Resultados da triagem da carga de drogas. Esta figura mostra os resultados da carga de medicamentos; O eixo y esquerdo é o tempo, o eixo y direito é a dureza e as quatro prescrições no eixo x representam diferentes volumes de carga de fármacos. Clique aqui para ver uma versão maior desta figura.
| número de série | Pó medicinal (g) | PVPP (g) | CCM (g) | amido pré-gelatinizado (g) | lactose (g) | Prazo(s) de desintegração | Exterior |
| 1 | 0.5 | 1 | 3.4 | 26 | limpo | ||
| 2 | 0.5 | 1 | 3.4 | 54 | limpo | ||
| 3 | 0.5 | 1 | 3.4 | 16 | comum |
Tabela 1: Resultados da seleção do preenchimento. O conteúdo principal do medicamento e a dosagem de PVPP nas três prescrições permaneceram inalterados; a prescrição 1 utilizou CCM como preenchimento, a prescrição 2 utilizou amido pré-gelatinizado como preenchedor e a prescrição 3 utilizou lactose como preenchimento. Destes, a lactose como preenchimento teve o menor tempo de desintegração, mas o brilho não estava à altura.
| Prescrição desintegrante | Exterior | Prazo(s) de desintegração | Uniformidade de dispersão (s) |
| PVPP+L-HPC | limpo | 39 | 39 |
| L-HPC+CMS-Na | limpo | 40 | 52 |
| PVPP+CMS-Na | limpo | 42 | 40 |
Tabela 2: Triagem de combinações desintegrantes. Sob condições em que o fármaco principal e o preenchedor permaneceram inalterados, diferentes combinações de desintegrantes foram testadas em termos de seu limite de tempo de desintegração e uniformidade de dispersão. A prescrição 1 foi PVPP + L-HPC, a prescrição 2 foi L-HPC + CMS-Na, e a prescrição 3 foi PVPP + CMS-Na, dentre as quais a combinação de PVPP + CMS-Na teve o menor tempo limite de desintegração.
| Nível | A (g) | B (g) | C (g) | D g) |
| 1 | 3.4 | 0.6 | 0.4 | em branco |
| 2 | 4.4 | 1.2 | 0.8 | em branco |
| 3 | 5.4 | 1.8 | 1.2 | em branco |
Tabela 3: Níveis de fatores para desenhos ortogonais. A dosagem do medicamento principal de cada prescrição permaneceu inalterada. O fator A é a dosagem do MCC de preenchimento, o fator B é a dosagem do PVPP, o fator C é a dosagem do CMS-Na e o fator D é o erro em branco.
| Numeração | A (g) | B (g) | C (g) | D (em branco) | Prazo(s) de desintegração |
| 1 | 1 | 1 | 1 | 1 | 69 |
| 2 | 1 | 2 | 2 | 2 | 123 |
| 3 | 1 | 3 | 3 | 3 | 40 |
| 4 | 2 | 1 | 2 | 3 | 43 |
| 5 | 2 | 2 | 3 | 1 | 31 |
| 6 | 2 | 3 | 1 | 2 | 39 |
| 7 | 3 | 1 | 3 | 2 | 78 |
| 8 | 3 | 2 | 1 | 3 | 59 |
| 9 | 3 | 3 | 2 | 1 | 34 |
| K1 | 232 | 190 | 167 | 134 | |
| K2 | 113 | 213 | 200 | 240 | |
| K3 | 171 | 113 | 149 | 142 | |
| K1 | 77.333 | 66.333 | 55.667 | 44.667 | |
| K2 | 37.667 | 71 | 66.667 | 80 | |
| K3 | 57 | 37.667 | 49.667 | 47.333 | |
| R | 39.667 | 33.333 | 17 | 35.333 | |
| primário e secundário | RA>RD>RB>RC |
Tabela 4: Arranjo experimental ortogonal e resultados experimentais.
| Fonte de variância | soma dos desvios quadrados | graus de liberdade | quadrado médio | Valor F | Salience |
| Um | 236.667 | 2 | 1180.333 | 1.016 | >0.05 |
| B | 1828.667 | 2 | 914.333 | 0.787 | >0.05 |
| C | 446 | 2 | 223 | 0.192 | >0.05 |
| D (erro) | 2322.667 | 2 | 1161.333 |
Tabela 5: Resultados da análise de variância.
| Receita | Pó medicinal (g) | CCM (g) | PVPP (g) | CMS-Na (g) | Estearato de magnésio (g) |
| 1 | 1 | 4.4 | 1.8 | 1.2 | 0.1 |
| 2 | 1.5 | 4.4 | 1.8 | 1.2 | 0.1 |
| 3 | 2 | 4.4 | 1.8 | 1.2 | 0.1 |
| 4 | 2.5 | 4.4 | 1.8 | 1.2 | 0.1 |
Tabela 6: Formulações de carga de medicamentos. A dosagem de CCM, PVPP e CMS-Na para cada prescrição permaneceu inalterada. A dosagem do medicamento principal na prescrição 1 foi de 1 g, na prescrição 2 foi de 1,5 g, na prescrição 3 foi de 2 g e na prescrição 4 foi de 2,5 g.
| Número do lote | Exterior | Peso médio da folha (g) | Diferença de peso (g) | Dureza média (N) | Prazo(s) de desintegração | Uniformidade de dispersão (s) |
| 20220710 | limpo | 0.1978 | qualificado | 22 | 39 | 43 |
| 20220711 | limpo | 0.186 | qualificado | 21 | 35 | 41 |
| 20220712 | limpo | 0.1948 | qualificado | 18 | 29 | 32 |
Tabela 7: Avaliação da qualidade dos comprimidos dispersíveis Taohong Siwu. Para os três lotes de amostras foram realizadas análises de aparência, análise de peso médio, verificação de diferença de peso, verificação de dureza, verificação de limite de tempo de desintegração e verificação de uniformidade de dispersão para os três lotes de amostras.
Discussão
Neste estudo, testamos o efeito da dosagem de carga, desintegrante e pó medicinal sobre o tempo de desintegração e uniformidade de dispersão de comprimidos dispersíveis usando um desenho ortogonal. Verificamos que a formulação preferida se desintegrou rapidamente. Ao selecionar o preenchedor mais adequado, observamos que, embora a lactose apresentasse o menor tempo de desintegração, a dureza desses comprimidos não era suficiente. Além disso, a superfície dos comprimidos não era lisa o suficiente, e havia evidências de perda de pó e comprimidos soltos. Como tal, a lactose não satisfazia os requisitos de um enchimento adequado; portanto, selecionamos a celulose microcristalina como a carga ideal. A celulose microcristalina é um polímero na forma de pó ou hastes curtas, com forte fluidez e sem estrutura fibrosa13. Além disso, a celulose microcristalina é inodora, atóxica, fácil de desintegrar e não reativa com drogas. Esse polímero é um importante excipiente na indústria farmacêutica e pode ligar eficientemente componentes de fármacos para promover a moldagem de fármacos14. Além disso, esse polímero pode facilitar a decomposição de componentes de fármacos ao mesmo tempo em que aumenta a força do fármaco e é usado principalmente como excipiente, preenchedor ou modificador de liberação de fármacos para a preparação de comprimidos, grânulos de fármacos e cápsulas de fármacos15,16.
Os desintegrantes têm boas propriedades de absorção e inchaço de água e podem promover a dispersão uniforme de comprimidos dispersíveis em água. Atualmente, os desintegrantes mais comumente usados em comprimidos dispersíveis são L-HPC, PVPP reticulado e CMS-Na17. Neste experimento, a combinação de PVPP reticulado e CMS-Na exibiu o menor tempo de desintegração. A maioria dos comprimidos dispersíveis usa dois ou mais desintegrantes. Combinações de desintegrantes podem melhorar o efeito de desintegração e reduzir custos18. Ao rastrear a carga de medicamentos, verificamos que, à medida que a carga de medicamentos aumentava, a dureza dos comprimidos diminuía; Esse efeito pode estar relacionado à natureza do pó do material medicinal19. Finalmente, o processo de preparação dos comprimidos dispersíveis (contendo quatro ingredientes) foi otimizado pela formulação. Seguiu-se a indexação do tempo de desintegração e uniformidade de dispersão. Os ingredientes finais foram pó medicinal (17%), celulose microcristalina (49%), polivinilpirrolidona reticulada (20%), carboximetilamido sódico (13%) e estearato de magnésio (1%).
Comparados às decocções da medicina tradicional chinesa, os comprimidos dispersíveis podem exercer bons efeitos terapêuticos com alta biodisponibilidade, boa estabilidade e fácil portabilidade, especialmente para pacientes que têm dificuldade em tomar decocções e dificuldades de deglutição20,21. Na medicina tradicional chinesa, a principal droga em comprimidos dispersíveis não é geralmente um único composto; Em vez disso, a droga é composta de uma mistura complexa de ingredientes. Além disso, tais pós têm uma viscosidade relativamente alta e geralmente são capazes de absorver umidade. Comprimidos comuns contendo pó de fitoterapia chinesa como a principal droga estão associados a uma ampla variedade de problemas, incluindo um longo tempo de desintegração e baixa uniformidade de dispersão, que influenciam o efeito curativo. Portanto, na presente pesquisa, projetamos uma nova formulação, comprimidos dispersíveis, para a decocção de Taohong Siwu para resolver os problemas associados às decocções tradicionais, ampliando assim o leque de aplicações e promovendo absorção no organismo22. Nesta pesquisa, extraímos um pó seco de materiais medicinais aplicando o método de extração em água. Os métodos tradicionais de decocção envolvem ingredientes complexos que podem ser extraídos de acordo com os componentes eficazes e as características dos ingredientes ativos. Além disso, o conteúdo dos ingredientes ativos pode ser aumentado em comprimidos dispersíveis. A separação de impurezas em materiais medicinais e a preservação de seus princípios ativos é um problema que deve ser considerado cuidadosamente durante a preparação. Também é importante fornecer condições favoráveis para a preparação de comprimidos dispersíveis subsequentes. Decocções tradicionais, como a decocção Taohong Siwu, geralmente têm um alto teor de açúcar. Pós de ervas podem ser prontamente preparados para que absorvam a umidade. Por isso, é importante tomar precauções ao secar durante o preparo. Além disso, os comprimidos acabados devem ser resistentes à umidade.
Ressalta-se que este estudo investigou apenas um componente do índice nos experimentos de determinação de conteúdo; Isso representa uma limitação notável para este estudo, embora nosso trabalho forneça uma base fundamental para pesquisas subsequentes em profundidade. Transformar uma decocção de Taohong Siwuem um comprimido dispersível que é conveniente para os pacientes, mais prático e mais viável também está de acordo com as tendências em desenvolvimento em preparações da medicina tradicional chinesa.
Divulgações
Os autores declaram não haver conflitos de interesse.
Agradecimentos
Esta pesquisa foi apoiada pela Fundação Nacional de Ciências Naturais da China (Grant No. 82074059), o Fundo Aberto para o Laboratório Chave do Ministério da Educação Médica de Xin'an, a Universidade de Medicina Tradicional Chinesa de Anhui (No.2022XAYX07), o projeto financiado pelo Fundo Aberto do Laboratório Chave Provincial de Anhui da Medicina Tradicional Chinesa (No.2019AKLCMF03), o Projeto de Financiamento de Candidato à Reserva de Líder Acadêmico da Província de Anhui (No. 2022H287), e o Projeto Chave de Pesquisa em Saúde da Província de Anhui (AHWJ2022a013)
Materiais
| Name | Company | Catalog Number | Comments |
| Acetonitrile | OCEANPAK | A22T0218 | |
| Carboxymethyl starch sodium | Maclean | C12976293 | |
| Crosslinked Polyvinylpyrrolidone | Maclean | C12976293 | |
| Disintegration time limit tester | Tianjin Guoming Pharmaceutical Equipment Co., Ltd. | BJ-2 | |
| Electric heating constant temperature drying oven | Shanghai Sanfa Scientific Instrument Co., Ltd. | DHG-9202·2 | |
| Electric thermostatic water bath | Shanghai Sanfa Scientific Instrument Co., Ltd. | DK-S24 | |
| Electronic Balance | Sartorius Scientific Instruments (Beijing) Co., Ltd. | SQP | |
| Intelligent Dissolution Tester | Tianda Tianfa Technology Co., Ltd. | ZRS-8L | |
| Lactose | Maclean | C12942141 | |
| Low-Substituted Hydroxypropyl Cellulose | Anhui Shanhe Pharmaceutical Excipients Co., Ltd. | 190219 | |
| Magnesium stearate | Maclean | C12894996 | |
| Methyl Alcohol | TEDIA High Purity Solvents | 22075365 | |
| Microcrystalline cellulose | Maclean | 13028716 | |
| Single punch tablet machine | Nantong Shengkaia Machinery Co., Ltd. | TDP-2A | |
| Tablet hardness tester | Shanghai Huanghai Drug Testing Instrument Co., Ltd. | YPJ-200B | |
| Taohong Siwu Soup Extract | self made | ||
| Taoren, Honghua, etc. traditional Chinese medicine | The First Affiliated Hospital of Anhui University of Chinese Medicine | ||
| Waters Acquity H-Class Ultra High Liquid Chromatography |
Referências
- Wang, J. Y., et al. Effects of Erchen decoction and Taohong Siwu decoction on Nox4/NF-κB/HIF-1αsignaling pathway in aorta of ApoE~(-/-) atherosclerosis mice. China Journal of Traditional Chinese Medicine and Pharmacy. , (2019).
- Aslani, A., Ghasemi, A., Esfahani, S. K. Design, formulation and physicochemical evaluation of dimenhydrinate orally disintegrating tablets. Galen Medical Journal. 7, 936 (2018).
- Chen, K. X., Jiang, H. L., Luo, X. M., Shen, J. H. Drug discovery in post-genome era: Trend and practice. Chinese Journal of Natural Medicines. 2, 257-260 (2004).
- Wang, M., Liu, Z., Hu, S., Duan, X., Han, L. Taohong Siwu decoction ameliorates ischemic stroke injury via suppressing pyroptosis. Frontiers in Pharmacology. 11, 590453 (2020).
- Xin, R. H., Liang, G., Zheng, J. F. Design and content determination of Genhuang dispersible tablet herbal formulation. Pakistan Journal of Pharmaceutical Sciences. 30, 655-661 (2017).
- Yulin, D., Junxue, P., Rong, L., Jianlin, Y. Comparison of oral preparations of Chinese medicine dispersible tablets and traditional Chinese medicine. Chinese Journal of Ethnomedicine and Ethnopharmacy. 26 (8), 63-65 (2017).
- Yinghua, X., et al. Study on albendazole dispersible tablets based on solubilization effect. Journal of Hebei University of Science and Technology. 42 (6), 619-626 (2021).
- Mengzhu, Y., Kai, Y., Yi, H. Study on the prescription optimization and dissolution of Baicalin Dispersible Tablets. China Medical Herald. 10 (1), 122-123 (2013).
- Zhongan, X., et al. Introduction to the orthogonal experimental design method. Sci-Tech Information Development & Economy. (5), 1005 (2002).
- Liu Ruijiang, Z. Y., Chongwei, W., Jian, T. Study on the design and analysis methods of orthogonal experiment. Experimental Technology and Management. 27 (9), 4 (2010).
- Xianchun, D. Based on network pharmacology and transcriptomics to explore the main material basis and mechanism of ThaoHongSiWu Decoction in treating ischemic stroke. Anhui University of Chinese Medicine. , (2019).
- Pharmacopoeia Commission of the Ministry of Health of the People's Republic of China. . Pharmacopoeia of the People's Republic of China. , (2020).
- Jiaqiang, Y., et al. Research progress on preparation and application of microcrystalline cellulose. China Pulp & Paper Industry. 42 (10), 8-13 (2021).
- Nakamura, S., Tanaka, C., Yuasa, H., Sakamoto, T. Utility of microcrystalline cellulose for improving drug content uniformity in tablet manufacturing using direct powder compression. AAPS PharmSciTech. 20 (4), 151 (2019).
- Jinbao, L., et al. Effect of alkali pretreatment on preparation of microcrystalline cellulose. China Pulp & Paper. 39 (01), 26-32 (2020).
- Nsor-Atindana, J., et al. Functionality and nutritional aspects of microcrystalline cellulose in food. Carbohydrate Polymers. 172, 159-174 (2017).
- Wang, C., et al. Formulation and evaluation of nanocrystalline cellulose as a potential disintegrant. Carbohydrate Polymers. 130, 275-279 (2015).
- Huba, K., István, A. Drug excipients. Current Medicinal Chemistry. 13 (21), 2535-2563 (2006).
- Ping, Z., Jie, G. Talking about some problems of hardness and disintegration in traditional Chinese medicine tablets. Science and Wealth. 6 (181), 181 (2020).
- Pabari, R. M., McDermott, C., Barlow, J., Ramtoola, Z. Stability of an alternative extemporaneous captopril fast-dispersing tablet formulation versus an extemporaneous oral liquid formulation. Clinical Therapeutics. 34 (11), 2221-2229 (2012).
- Fini, A., Bergamante, V., Ceschel, G. C., Ronchi, C., de Moraes, C. A. F. Fast dispersible/slow releasing ibuprofen tablets. European Journal of Pharmaceutics and Biopharmaceutics. 69 (1), 335-341 (2008).
- Meidan, W. Study on compound Rhodiola relieving physical fatigue dispersible tablets. Jilin University. , (2009).
Reimpressões e Permissões
Solicitar permissão para reutilizar o texto ou figuras deste artigo JoVE
Solicitar PermissãoThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Todos os direitos reservados