需要订阅 JoVE 才能查看此. 登录或开始免费试用。
Method Article
基于CRITIC结合Box-Behnken响应面法的铁邦岀与赞坝加工工艺优化
摘要
本协议描述了一种使用CRITIC结合Box-Behnken反应面法的Zanba炒铁棒净的高效和标准的解毒处理方法。
摘要
乌头摆的干根,中文称为铁棒翠(TBC),是最著名的藏药之一。它是中国西北地区广泛使用的草药。然而,由于TBC的强烈毒性以及其治疗剂量和毒性剂量相似,发生了许多中毒病例。因此,寻找一种安全有效的方法来降低其毒性是一项紧迫的任务。翻阅藏药典籍,《青海省藏药加工规范(2010)》中记载了TBC炖炒的加工方法。但是,具体的加工参数尚不清楚。因此,本研究旨在优化和规范赞巴炒TBC的加工工艺。
首先,对TBC切片厚度、Zanba用量、加工温度和时间4个因素进行单因素试验。以赞巴炒TBC中单酯和二酯生物碱含量为指标,采用CRITIC结合Box-Behnken响应面法优化赞巴炒TBC的加工工艺。赞巴炒TBC的优化加工条件为TBC切片厚度为2 cm,赞巴是TBC的3倍,加工温度为125 °C,翻炒60 min。本研究确定了赞巴炒TBC使用的优化和标准加工条件,从而为赞巴炒TBC的安全临床使用和工业化生产提供了实验依据。
引言
乌头摆布希和黄头的干根,最著名的藏药之一,在中国1,2中被称为铁棒翠(TBC)。TBC的干燥根有助于驱寒和风,减轻疼痛和镇静休克。记录在《中华人民共和国卫生部药品标准(藏药)》第一卷中,其中指出TBC的干根通常用于治疗类风湿性关节炎,跌打损伤和其他感冒疾病3。但TBC的临床治疗剂量与其毒性剂量相似,由于使用不当,中毒或死亡事件屡见不鲜有报道4。因此,降低TBC的毒性,保持疗效成为多年来的研究热点。
在藏药中,加工是减轻TBC毒性的最有效方法之一。根据《青海省藏药加工规范(2010)》,原药材(待定)放入铁锅中,与赞巴一起炒至赞巴变黄,取出赞巴,空气晒干5,6。然而,没有具体的工艺参数记录,这使得控制加工技术和Zanba炒TBC的质量变得困难。CRITIC法是一种客观的权重方法,可以避免模糊化和主观性,增强称重的客观性7.Box-Behnken响应面法可以通过多项式拟合8直接反映各因子之间的相互作用。Box-Behnken响应面和CRITIC方法的组合通常用于优化处理技术,以获得优化的处理协议9,10。本文以单酯-二萜类生物碱(MDA)(苯甲酰乌头碱)和两种二酯-二萜类生物碱(DDAs)(乌头碱、3-脱氧乌头碱)为评价指标。采用CRITIC结合Box-Behnken响应面法优化赞巴炒TBC加工工艺,建立临床安全使用标准加工方法。
Access restricted. Please log in or start a trial to view this content.
研究方案
采用CRITIC结合Box-Behnken响应面法对赞巴炒TBC加工方法进行了优化和标准化。在此过程中,苯甲酰乌头碱、乌头碱和3-脱氧乌头碱用作评价指标。
1. 样品溶液制备
- 制备对照品储备溶液。在电子分析天平上精确称取9.94 mg苯甲酰乌头碱、8.49 mg乌头碱和6.25 mg3-脱氧乌头碱(材料表),并将它们放入10 mL容量瓶中。然后,加入0.05%盐酸甲醇溶液溶解固体,并将体积补足至10 mL。最后,摇晃混合物,得到质量浓度为0.9940 mg/mL苯甲酰乌头碱、0.8490 mg/mL乌头碱和0.6250 mg/mL 3-脱氧乌头碱的对照物质储备溶液。
注意:盐酸是一种高腐蚀性材料11.使用适当的保护措施,例如手套、实验室外套、护目镜和通风橱。 - 准备测试样品溶液。
- 在锥形烧瓶中称取2克Zanba炒TBC粉。
- 称量30克TBC(2厘米)和90克Zanba,然后将它们加入预热的炒菜机中,准备Zanba炒TBC。将炒菜机的时间和温度分别设置为40分钟和140°C。将机器设置为完成处理。
- 使用高速粉碎机将 Zanba-炒制的 TBC 分别研磨成粉末样品,这些样品可以通过 50 目(0.355 毫米)的筛子。
- 根据先前的研究,将3mL氨溶液和50mL异丙醇和乙酸乙酯的混合溶液(比例为1:1 v / v)加入上述锥形烧瓶中12,13。
注意:要制备氨溶液,请将40 mL浓氨溶液加入100 mL容量瓶中,并向测量线中注入纯净水。使用浓氨溶液时采取适当的保护措施,因为它有强烈的气味。 - 称取上述样品和锥形瓶并记录重量。超声处理 30分钟 (电压:220 V,频率:40 kHz)。
注意:乌头碱生物碱容易受热分解。因此,超声波提取的温度必须低于25°C。 - 超声提取后称取样品和锥形烧瓶。
- 通过添加异丙醇和乙酸乙酯的混合物(比例为1:1 v / v)来弥补损失的重量。
- 过滤示例溶液。使用旋转蒸发器在40°C下蒸发25mL滤液至干。
- 通过加入5mL的0.05%盐酸甲醇溶液溶解残留物,通过0.2μm注射器过滤器过滤溶液,并通过高效液相色谱(HPLC)进行分析。
- 在锥形烧瓶中称取2克Zanba炒TBC粉。
- 制备含有0.1988 mg/mL苯甲酰乌头碱、0.0509 mg/mL乌头碱和0.0938 mg/mL 3-脱氧乌头碱的混合参比溶液。
注意:将每种标准品(0.9940mg苯甲酰乌头碱,0.2545mg乌头碱和0.4690mg3-脱氧乌头碱)溶解在0.05%盐酸甲醇中的5mL容量瓶中作为溶解介质。 - 通过将6.16g乙酸铵(材料表)溶解在2L超纯水(流动相A)中来制备0.04 M乙酸铵缓冲液。使用氨将pH调节至8.50。
注意:氨是一种有害物质。使用适当的保护措施,例如手套、实验室外套、护目镜和通风橱。 - 过滤2L超纯100%乙腈(流动相B)并脱气。
注意:乙腈是一种有害物质13.使用适当的保护措施,例如手套、实验室外套、护目镜和通风橱。
2. 色谱条件
- 将 10 μL 预处理的样品溶液注入带有二元泵的 HPLC 系统中。使用采用ODS-3色谱柱(5 μm x 4.6 mm x 250 mm;在30 °C下工作)的HPLC系统,流动相A和B进行MDA和DDA分离。每个样品进样三次以进行技术复制。
- 对ODS-3色谱柱的方法进行编程,如 表1 所示。将 流速 设置为 1.0 mL/min , 检测波长 设置为 235 nm。
- 记录每种目标化合物的峰面积。
注意:仪器的详细信息可以在 材料表中找到。
3. 系统适应性测试
注意:有关执行步骤3.1-3.5的色谱条件,请参阅第2节。
- 研究浓度与峰面积之间的线性关系。
- 制备各种浓度 - 19.88、39.76、59.64、159.04、198.80 和 497.00 μg/mL - 苯甲酰乌头碱溶液。
- 制备各种浓度 - 8.49、16.98、25.47、33.96、50.94 和 169.80 μg/mL - 乌头碱溶液。
- 制备各种浓度 - 1.875、12.50、37.50、62.50、93.75 和 125.00 μg/mL - 3-脱氧乌头碱溶液。
- 从低质量浓度到高质量浓度进样上述对照品溶液,并记录峰面积。
- 从参比溶液浓度(μg/L)与峰面积的关系图中获得三个线性回归方程。
注意:确保苯甲酰乌头碱、乌头碱和 3-脱氧乌头碱的浓度在此标准曲线的线性范围内。
- 通过将 10 μL 样品溶液连续进样六次重复进行精密测试,并在第 2 节所述的相同 HPLC 条件下运行样品。记录苯甲酰乌头碱、乌头碱和3-脱氧乌头碱的峰面积。
- 通过注入10μL制备的样品溶液进行稳定性测试实验,并在0小时,2小时,4小时,8小时,12小时和24小时后测定峰面积。
注意:峰面积由参考的HPLC系统自动记录。这些时间点基于相关文献15,16,17。 - 按照步骤1.2中的方法,取同一批Zanba-炒TBC平行制备6种供试样品溶液,进行重现性试验。将每个样品 10 μL 注入 HPLC 系统,并按照第 2 节所述运行样品。
注意:通过比较六个样品之间的浓度差异来评估重现性。 - 通过制备六份同批赞巴炒TBC作为供试品溶液来进行回收实验。然后,将各指示组分的~100%对照品加入供试品溶液的六份中,计算回收率。在第 2 节所述的相同条件下将这些样品 (10 μL) 注入 HPLC 系统,并使用公式 (1) 计算回收率:
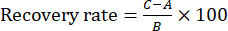 (1)
(1)
注:在公式(1)中,A是供试品溶液中待测组分的量,B是添加对照品的量,C是含有对照品和赞巴炒TBC样品的溶液的测量值。
4. 单因素实验
- 切片厚度比较
- 准备五组进行测试,每组含 30 克 TBC,其中 TBC 的厚度分别为 0.5、1、2、3 和 4 厘米。称量赞巴的量是TBC(90克)的三倍。
注意:待定是有毒的。使用适当的保护措施,例如手套、实验室外套、护目镜和通风橱,并在切割过程中小心。通过前期实验,发现TBC和赞巴完全接触所需的赞巴量是其三倍。因此,在正式的实验设计中,研究在检查切片厚度时选择了三倍的Zanba量。 - 将自动炒菜机的温度和时间分别设置为 140°C 和 40分钟。
- 在自动炒菜机加热到设定温度后,将~30克TBC和90克Zanba加入机器中。
- 按照步骤 1.2 准备示例解决方案。根据标准曲线计算不同加工产品中MDA和DDA的含量(表2)。通过第 6 节中的 CRITIC 方法根据结果计算综合分数。
- 通过这种方式,比较赞巴的量,以及加工温度和时间,以优化条件。
- 准备五组进行测试,每组含 30 克 TBC,其中 TBC 的厚度分别为 0.5、1、2、3 和 4 厘米。称量赞巴的量是TBC(90克)的三倍。
- 赞巴的量比较
- 进行五组测试,每组含 30 克 TBC(2 厘米),其中 Zanba 的含量分别为 TBC 的 1 倍、2 倍、3 倍、4 倍和 5 倍。
- 打开炒菜机进行处理。将炒菜机的时间和温度设置为 40分钟 和 140°C。
- 按照步骤 1.2 准备示例解决方案。根据标准曲线计算不同加工产品中MDA和DDA的含量(表2)。通过第 6 节中的 CRITIC 方法 根据 结果计算综合分数。
- 加工温度比较
- 进行五组测试,每组用30克TBC(2厘米)和90克赞巴。
- 打开炒菜机进行处理。将处理温度设置为 100 °C、120 °C、140 °C、160 °C 和 180 °C。 将处理时间设置为 40 分钟。
注意:通过前期实验发现,加工温度低于100°C时,赞巴黄变的速度很低,如果温度过高(180°C以上),赞巴容易燃烧变黑。因此,100 °C和180 °C分别设置为加工过程中的最小和最高温度值。 - 按照步骤 1.2 准备示例解决方案。记录MDA和DDA的峰面积。根据标准曲线计算不同加工产品中MDA和DDA的含量(表2)。通过第 6 节中的 CRITIC 方法 根据 结果计算综合分数。
注意:该实验涉及160°C和180°C的高温。 根据实验室的安全规范,在实验过程中注意安全。
- 处理时间比较
- 进行五组测试,每组用30克TBC(2厘米)和90克赞巴。
- 打开炒菜机进行处理。将处理时间设置为 20、40、60、80 和 100 分钟。将温度设置为 140 °C。
- 按照步骤 1.2 中的说明准备示例解决方案。记录MDA和DDA的峰面积。根据标准曲线计算不同加工产品中MDA和DDA的质量(表2)。通过第 6 节中的 CRITIC 方法 根据 结果计算综合分数。
5. 基于响应面法(RSM)的炒TBC加工工艺优化
- 博克斯-本肯响应面设计
- 通过使用单因素测试(步骤4.1-4.4)的初步实验,确定切片厚度的范围(A,1-3厘米),赞巴的量(B,2-4x),处理温度(C,100-140°C)和处理时间(D,40-80分钟)。
注意:四个变量的编码值及其电平如 表3所示。每个变量的三个级别分别编码为 -1、0 和 1。
- 通过使用单因素测试(步骤4.1-4.4)的初步实验,确定切片厚度的范围(A,1-3厘米),赞巴的量(B,2-4x),处理温度(C,100-140°C)和处理时间(D,40-80分钟)。
- 使用软件生成矩阵并分析响应面模型。
注:软件使用情况的屏幕截图显示在 补充文件 1 中。- 使用由 24 个实验组成的三水平四因子 Box-Behnken 设计(如本研究中所做的那样),并测量五个重复(运行顺序 1、9、14、16 和 25)来计算平方的纯误差和(表 4)。将综合分数 (Y) 设置为响应(步骤 1-4, 补充文件 1)。
- 在 主页上,单击“ 新建设计 ”(步骤 1, 补充文件 1),然后在“ 设计 ”页面的左侧面板中,单击 “响应面 |Box-Behnken 并设置表中四个因子的参数(步骤 2, 补充文件 1)。
- 单击下一步(步骤 2,补充文件 1),设置响应名称,然后单击完成(步骤 3,补充文件 1)。
- 通过上述操作生成响应面设计(步骤 4, 补充文件 1)。
- 使用由 24 个实验组成的三水平四因子 Box-Behnken 设计(如本研究中所做的那样),并测量五个重复(运行顺序 1、9、14、16 和 25)来计算平方的纯误差和(表 4)。将综合分数 (Y) 设置为响应(步骤 1-4, 补充文件 1)。
- 根据为响应曲面设计的 29 个方案完成试验。
- 按照步骤 1.2 准备示例解决方案。
- 记录MDA和DDA的峰面积。
注意:峰面积由参考的HPLC系统自动记录。 - 计算不同加工产品中MDA和DDA的质量。
- 通过步骤 6 中的 CRITIC 方法 根据 结果计算综合分数。
注意:具体方法如步骤 6 所示。 - 将获得的29次试验的综合分数输入计算机,并使用参考软件进行分析(步骤5, 补充文件1)。
- 通过软件对绘制在 3D 模型图中的多项式方程和响应面分析进行统计验证(步骤 6-8, 补充文件 1)。
- 在左侧导航窗格中的“分析 (+)”下,单击 Y,然后单击“配置”窗口中的“开始分析”(步骤 6,补充文件 1)。
- 单击顶部菜单中的方差分析,观察显示 方差分析 的结果表(步骤 7, 补充文件 1)。
- 在顶部菜单中,单击 模型图 ,然后单击 3D 表面 以获取反映处理参数对合成分数影响的响应曲面图(步骤 8, 补充文件 1)。
- 在预测的最佳条件下(步骤9, 补充文件1)一式三份对响应面模型进行验证,以验证加工技术的稳定性。在左侧 导航 窗格中的 优化下,单击 数字 ,然后在顶部菜单中单击 解决方案。观察预测的最佳条件。
6. 模型评估
注意:此步骤在每个单因素实验或响应面实验完成后执行。每个实验(例如,切片厚度的比较)完成后,根据步骤1.2和第2节测量不同样品中MDA和DDA的含量,以获得五个数据集。数据见 补充表S1。
- 指数的无量纲处理
注意:此步骤将测量值(Xij)转换为无量纲相对值,以便每个指数的值处于相同的数量水平。此操作可以便于对不同单位或数量级的指标进行综合分析和比较18.为了便于说明,切片厚度值已用于如下所示的计算(补充表S1)。- 规范MDA的内容(获得yMDA;MDA是指苯甲酰乌头碱),通过使用公式(2)中的公式。
注意:索引“i”代表四个因素之一,切片厚度是研究的第一个因素。因此,i 的值等于 1。指数“j”代表每个水平的因素;因此,当切片厚度为第一级(0.5厘米)时,J等于1;当切片厚度为第五级(4厘米)时,j等于5。厚度为0.5、1、2、3和4 cm的TBC中MDA(Xij)含量分别为0.9693、1.0876、1.3940、1.4185和1.3614 mg/g。因此,x j,最大值 为 1.4185,xj,最小 值为 0.9693。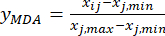 (二)
(二)
因此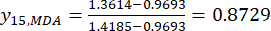
这里,Xij 是实验在第i个因子和第j个水平上的MDA的测量内容;xj,min 是本组实验中MDA的最小含量;和 xj,max 是这组实验中 MDA 的最大含量。因此, i = 1, 2, ..., m 和 j = 1, 2, ..., n。
注意: 因此,MDA 的标准化值是 0.0000、0.2634、0.9455、1.0000 和 0.8729,使用公式 (2)。 - 规范DDA的总内容(获得yDDA;DDAs是指乌头碱和3-脱氧乌头碱),使用公式(3)中的公式。
注意: i 是四个因素之一, j 是 每个水平的因素;Xij 是实验的DDA在第i个因子和第j个水平上的测量内容;xj,min 是本组数据实验中DDAs的最小含量;而xj,max是 本组数据实验中DDA的最大含量。这样, i = 1, 2, ..., m 和 j = 1, 2, ..., n。厚度为0.5、1、2、3和4 cm的TBC中DDAs(Xij)含量分别为0.3492、0.2692、0.2962、0.5354和0.5124 mg/g。因此,x j,最大值 为 0.5354,xj,最小 值为 0.2692。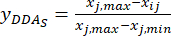 (三)
(三)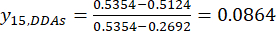
注意: 使用等式 (3) 的标准化值为 0.6995、1.0000、0.8986、0.0000 和 0.0864。
- 规范MDA的内容(获得yMDA;MDA是指苯甲酰乌头碱),通过使用公式(2)中的公式。
- 根据方程计算相应的对比度强度(S i)、冲突(δ i)、信息(C i)和指数权重(W i)。(4)至(7)分别为19、20。
注意:i = 1, 2, ..., m.y ij 是第 i 个因子和第 j 个因子实验的 MDA 或 DDA 含量的标准化数据。- 要估计对比度强度,请首先计算平均MDA值。
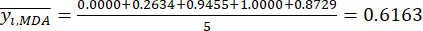
MDA的平均值在哪里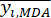 。
。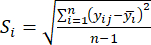 (四)
(四)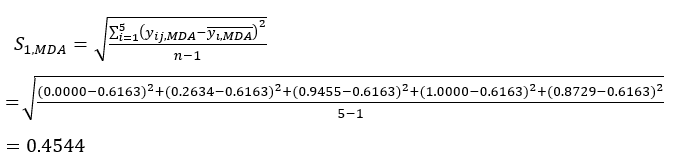
- 要计算冲突值,请首先使用 Excel21 中的 CORREL 函数估计ij γ相关系数。
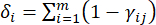 (五)
(五)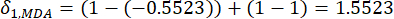
- 按如下方式计算信息值。
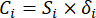 (六)
(六)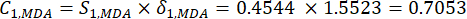
注意:同样,C1,DDAS = 0.7210 - 按如下方式计算指数权重。
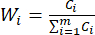 (七)
(七)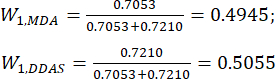
注意:因此,MDA和DDAs在比较切片厚度时的重量系数分别确定为0.4945和0.5055。
- 要估计对比度强度,请首先计算平均MDA值。
- 计算切片厚度的综合得分。
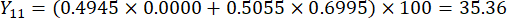
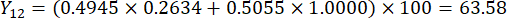
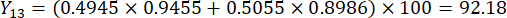
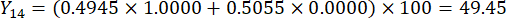
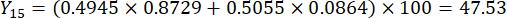
注意:Y13 是最大值。因此,切片厚度的最佳参数是第三级 - 2 厘米。
Access restricted. Please log in or start a trial to view this content.
结果
在这项研究中,使用的洗脱梯度对Zanba-炒-炒TBC中的三种指数组分具有良好的分辨率(图1),这是在重复调试后确定的。三霸炒TBC中的3种指标组分在特定浓度范围内具有良好的线性关系(表2)。炒TBC的精密度(表5)、稳定性(表6)、重复性(表7)和样品回收率(表8)均在中国药典(2020年第4卷)22规定?...
Access restricted. Please log in or start a trial to view this content.
讨论
TBC是一种重要的藏药,具有祛寒止痛的作用。数千年来,它在中国主要用于治疗创伤性损伤和风湿性关节痛24,25,26。二萜类生物碱是TBC 27,28,29的活性和毒性成分。TBC的乌头生物碱的主要毒性作用是神经毒性、心脏毒性和胃肠道毒性30
Access restricted. Please log in or start a trial to view this content.
披露声明
作者没有利益冲突需要披露。
致谢
这项工作得到了国家自然科学基金(第82130113号)、中国博士后科学基金(编号:2021MD703800)、四川省科技厅青年科学基金(编号:2022NSFSC1449)和成都中医药大学“杏林学者”研究推进计划(No.BSH2021009)。
Access restricted. Please log in or start a trial to view this content.
材料
| Name | Company | Catalog Number | Comments |
| 3-Deoxyaconitine | Chengdu Desite Biotechnology Co., Ltd. | DST221109-033 | |
| Aconitine | Chengdu Desite Biotechnology Co., Ltd. | DSTDW000602 | |
| Ammonium acetate | Tianjin Kermel Chemical Reagent Co., Ltd | Chromatographic grade | |
| Benzoylaconitine | Chengdu Desite Biotechnology Co., Ltd. | DSTDB005502 | |
| Design-Expert software | Stat-Ease, Inc., Minneapolis, MN, USA | version 13.0 | |
| Electronic analytical balance | Shanghai Liangping Instruments Co., Ltd. | FA1004 | |
| High performance liquid chromatography | SHIMADZU Co., Ltd. | LC-20A | |
| High-speed smashing machine | Beijing Zhongxing Weiye Instrument Co., Ltd. | FW-100 | |
| Millipore filter | Tianjin Jinteng Experimental Equipment Co., Ltd | φ13 0.22 Nylon66 | |
| stir-Fry machine | Changzhou Maisi Machinery Co., Ltd | Type 5 | |
| Tiebangchui | Gannan Baicao Biotechnology Development Co., Ltd | 20211012 | |
| Ultra pure water systemic | RephiLe Bioscience, Ltd. | Genie G | |
| Ultrasonic cleansing machine | Ningbo Xinyi Ultrasonic Equipment Co., Ltd | SB2200 | |
| Zanba | 27 Chuanzang Road, Ganzi County | - |
参考文献
- Li, C. Y., et al. Aconitum pendulum and Aconitum flavum: A narrative review on traditional uses, phytochemistry, bioactivities and processing methods. Journal of Ethnopharmacology. 292, 115216(2022).
- Wang, J., Meng, X. H., Chai, T., Yang, J. L., Shi, Y. P. Diterpenoid alkaloids and one lignan from the roots of Aconitum pendulum Busch. Natural Products and Bioprospecting. 9 (6), 419-423 (2019).
- Yu, L., et al. Traditional Tibetan medicine: therapeutic potential in rheumatoid arthritis. Frontiers In Pharmacology. 13, 938915(2022).
- Zhao, R., et al. One case of ventricular arrhythmia caused by poisoning of traditional Chinese medicine Aconitum pendulum Busch. Journal of People's Military Medical. 61 (4), 346-348 (2018).
- Qinghai Medical Products Administration. Processing specification of Tibetan medicine of Qinghai province. Qinghai Nationalities Publishing House. , 96-97 (2010).
- Li, J., et al. Comparison of three objective weighting methods to optimize the extraction process of Jianwei Chupi granules. Journal of Guangdong Pharmaceutical University. 38 (6), 91-97 (2022).
- Feng, Z. G., et al. Processing methods and the underlying detoxification mechanisms for toxic medicinal materials used by ethnic minorities in China: A review. Journal of Ethnopharmacology. 305, 116126(2023).
- Hsu, Y. T., Su, C. S. Application of Box-Behnken design to investigate the effect of process parameters on the microparticle production of ethenzamide through the rapid expansion of the supercritical solutions process. Pharmaceutics. 12 (1), 42(2020).
- Cheng, F., et al. Optimization of the baked drying technology of Cinnamomi Ramulus based on CRITIC combined with box-behnken response surface method. Journal of Chinese Medicinal Materials. 2022 (8), 1838-1842 (2022).
- Huang, X., et al. Optimization of microwave processing technology for carbonized Gardenia jasminoides by Box-Behnken response surface methodology based on CRITIC weighted evaluation. Chinese Herbal Medicines. 48 (6), 1133-1138 (2017).
- Elling, U., et al. Derivation and maintenance of mouse haploid embryonic stem cells. Nature Protocols. 14 (7), 1991-2014 (2019).
- Gu, J., Wang, Y. P., Ma, X. Simultaneous determinnation of three diester diterpenoid alkaloids in the toots of Aconiti flavi et penduli by HPLC method. Chinese Pharmaceutical Affairs. 28 (6), 618-621 (2014).
- Zhang, Y., Fu, X. UPLC simultaneous determination of six esteric alkaloids components in Aconitum Flaram Hand.Mazz. Asia-Pacific Traditional Medicine. 16 (5), 62-65 (2020).
- Rumachik, N. G., Malaker, S. A., Paulk, N. K. VectorMOD: Method for bottom-up proteomic characterization of rAAV capsid post-translational modifications and vector impurities. Frontiers In Immunology. 12, 657795(2021).
- Wang, Y. J., Tao, P., Wang, Y. Attenuated structural transformation of aconitine during sand frying process and antiarrhythmic effect of its converted products. Evidence-Based Complementary and Alternative Medicine. 2021, 7243052(2021).
- Wang, H. P., Zhang, Y. B., Yang, X. W., Zhao, D. Q., Wang, Y. P. Rapid characterization of ginsenosides in the roots and rhizomes of Panax ginseng by UPLC-DAD-QTOF-MS/MS and simultaneous determination of 19 ginsenosides by HPLC-ESI-MS. Journal of Ginseng Research. 40 (4), 382-394 (2016).
- vander Leeuw, G., et al. Pain and cognitive function among older adults living in the community. Journals of Gerontology Series A. Biological Sciences and Medical Sciences. 71 (3), 398-405 (2016).
- Lao, D., Liu, R., Liang, J. Study on plasma metabolomics for HIV/AIDS patients treated by HAART based on LC/MS-MS. Frontiers in Pharmacology. 13, 885386(2022).
- Li, Y., et al. Evaluation of the effectiveness of VOC-contaminated soil preparation based on AHP-CRITIC-TOPSIS model. Chemosphere. 271, 129571(2021).
- Zhong, S., Chen, Y., Miao, Y. Using improved CRITIC method to evaluate thermal coal suppliers. Scientific Reports. 13 (1), 195(2023).
- Lewis, N. S., et al. Magnetically levitated mesenchymal stem cell spheroids cultured with a collagen gel maintain phenotype and quiescence. Journal of Tissue Engineering. 8, (2017).
- Chinese Pharmacopoeia Committee. Pharmacopoeia of the People's Republic of China. 4, Chinese Medical Science and Technology Press. (2020).
- Li, G., et al. Effect of response surface methodology-optimized ultrasound-assisted pretreatment extraction on the composition of essential oil released from tribute citrus peels. Frontiers in Nutrition. 9, 840780(2022).
- Liu, X. F., et al. Hezi inhibits Tiebangchui-induced cardiotoxicity and preserves its anti-rheumatoid arthritis effects by regulating the pharmacokinetics of aconitine and deoxyaconitine. Journal of Ethnopharmacology. 302, 115915(2023).
- Smolen, J. S., et al. Rheumatoid arthritis. Nature Reviews.Disease Primers. 4, 18001(2018).
- Wang, F., et al. C19-norditerpenoid alkaloids from Aconitum szechenyianum and their effects on LPS-activated NO production. Molecules. 21 (9), 1175(2016).
- Wang, B., et al. Study on the alkaloids in Tibetan medicine Aconitum pendulum Busch by HPLC-MSn combined with column chromatography. Journal of Chromatographic Science. 54 (5), 752-758 (2016).
- Liu, S., et al. A review of traditional and current methods used to potentially reduce toxicity of Aconitum roots in Traditional Chinese Medicine. Journal of Ethnopharmacology. 207, 237-250 (2017).
- Qiu, Z. D., et al. Online discovery of the molecular mechanism for directionally detoxification of Fuzi using real-time extractive electrospray ionization mass spectrometry. Journal of Ethnopharmacology. 277, 114216(2021).
- El-Shazly, M., et al. Use, history, and liquid chromatography/mass spectrometry chemical analysis of Aconitum. Journal of Food and Drug Analysis. 24 (1), 29-45 (2016).
- Chan, T. Y. K. Aconitum alkaloid poisoning because of contamination of herbs by aconite roots. Phytotherapy Research. 30 (1), 3-8 (2016).
- Guo, L., et al. Exploring microbial dynamics associated with flavours production during highland barley wine fermentation. Food Research International. 130, 108971(2020).
- Guo, T. L., Horvath, C., Chen, L., Chen, J., Zheng, B. Understanding the nutrient composition and nutritional functions of highland barley (Qingke): A review. Trends in Food Science & Technology. 103, 109-117 (2020).
- Wu, H., et al. Anti-myocardial infarction effects of Radix Aconiti Lateralis Preparata extracts and their influence on small molecules in the heart using matrix-assisted laser desorption/ionization-mass spectrometry imaging. International Journal of Molecular Sciences. 20 (19), 4837(2019).
- Huang, G., et al. Study on cardiotoxicity and mechanism of "Fuzi" extracts based on metabonomics. International Journal of Molecular Sciences. 19 (11), 3506(2018).
- Li, S. L., et al. An insight into current advances on pharmacology, pharmacokinetics, toxicity and detoxification of aconitine. Biomedicine & Pharmacotherapy. 151, 113115(2022).
- Xie, Y., et al. Optimization of processing technology of braised Rehmanniae Raidx based on multiple indexes and response surface technology and correlation between components and color. Journal of Chinese Traditional Medicine. 47 (18), 4927-4937 (2022).
- Yang, X. Q., Xu, W., Xiao, C. P., Sun, J., Feng, Y. Z. Study on processing technology of Atractylodes chinensis with rice water and its pharmacodynamics of anti-diarrhea. Chinese Herbal Medicines. 53 (1), 78-86 (2022).
Access restricted. Please log in or start a trial to view this content.
转载和许可
请求许可使用此 JoVE 文章的文本或图形
请求许可探索更多文章
This article has been published
Video Coming Soon
版权所属 © 2025 MyJoVE 公司版权所有,本公司不涉及任何医疗业务和医疗服务。