Method Article
猪生物膜感染和隐形伤口模型
摘要
对抗生素耐药的慢性伤口是医疗保健系统的主要威胁。生物膜感染是顽固的和敌对的,可导致功能性伤口闭合不足。我们报告了一种临床相关的生物膜感染全层慢性伤口的猪模型。该模型对于机理研究以及测试干预措施都非常强大。
摘要
生物膜感染是导致伤口慢性化的主要原因。临床相关的实验性伤口生物膜感染的建立需要宿主免疫系统的参与。在这种临床相关的生物膜形成过程中,宿主和病原体的迭代变化只能 发生在体内。 猪伤口模型因其作为强大的临床前模型的优势而受到认可。据报道,有几种研究伤口生物膜的方法。体 外 和 离体 系统在宿主免疫反应方面存在缺陷。短期 体内 研究涉及急性反应,因此不允许生物膜成熟,正如临床上已知的那样。2014年报道了第一项长期猪伤口生物膜研究。该研究认识到,通过平面测量确定的生物膜感染伤口可能会闭合,但受影响部位的皮肤屏障功能可能无法恢复。后来,这一观察结果在临床上得到了验证。功能性伤口闭合的概念就这样诞生了。闭合但缺乏皮肤屏障功能的伤口可被视为看不见的伤口。在这项工作中,我们试图报告重现生物膜感染严重烧伤的长期猪模型所需的方法学细节,该模型具有临床相关性并具有转化价值。该方案提供了使用 铜绿假单胞菌 (PA01)建立8周伤口生物膜感染的详细指导。在家养白猪背部对称地形成8个全层烧伤创面,在烧伤后第3天接种(PA01);随后,使用激光散斑成像 (LSI)、高分辨率超声 (HUSD) 和经表皮失水 (TEWL) 在不同时间点对伤口愈合进行无创评估。接种的烧伤伤口用四层敷料覆盖。接种后第 7 天通过 SEM 建立和结构确认的生物膜损害了功能性伤口闭合。这种不良结局可能会因适当的干预措施而逆转。
引言
生物膜感染使烧伤和慢性伤口复杂化,并导致慢性 1,2,3,4,5。在微生物学中,主要研究生物膜机制,重点是微生物 1,6。从生物科学的角度来看,从这些研究中吸取的经验教训至关重要,但不一定适用于临床相关的致病性生物膜6,7,8。临床相关的生物膜结构聚集体应包括微生物和宿主因素8,9,10。这种微环境允许包含宿主-微生物迭代相互作用,这对于开发临床相关的生物膜至关重要 7,8。在这样的过程中,免疫细胞和血源性因子的参与至关重要11,12。在慢性伤口中,临床致病生物膜的宿主-微生物相互作用发生在很长一段时间内。因此,任何旨在开发生物膜感染翻译相关模型的实验方法都必须考虑这些因素。因此,我们试图开发一种临床上可重复的猪慢性生物膜感染模型。
虽然人体研究显然代表了研究愈合结果的最佳方法,但它们通常并不适合解决潜在的机制和新的机制范式。伦理问题限制了研究设计的使用,该研究设计需要在不同时间点从慢性伤口收集多个活检。因此,拥有一个成熟且可重复的动物模型至关重要,以便能够进行侵入性研究以彻底检查生物膜的命运 7,13。动物模型的选择取决于几个因素,包括科学/转化相关性和物流。猪系统被广泛认为是研究人类皮肤伤口的最具转化价值的实验模型7.因此,这项工作报道了一种已建立的生物膜感染全层烧伤的猪模型。这项工作基于文献2、7、13、14、15、16、17 中报道的几篇原始出版物。在这项研究中,选择一种临床分离的多重耐药铜绿假单胞菌(PA01)来感染伤口。铜绿假单胞菌是伤口感染的常见原因2,18,19,20。它是一种革兰氏阴性细菌,由于其对某些抗生素的耐药性,可能难以治疗11,19,21。到目前为止,报告的猪生物膜模型均未涉及8周的长期研究22,23,24,25,26。慢性伤口是指持续 4 周或更长时间的伤口 14,27,28。文献中没有报道其他慢性伤口生物膜模型。这项工作涉及功能性伤口闭合的概念 2,7,13,15,17,29。
研究方案
所有动物研究均按照机构动物护理和使用委员会 (IACUC) #21147 批准的方案进行。该研究是在印第安纳大学实验动物资源中心(LARC)进行的。我们在本协议中使用了一头雌性家养白猪(70-80磅)。
1. 动物驯化
- 猪到达设施后,将动物单独饲养在同一房间内至少 3 天,以便适应环境和社交互动。
- 给猪喂均衡的饲料。根据重量确定喂食量,并遵循制造商的建议。
- 确保动物在手术前禁食 6-12 小时,以防止在麻醉下恶心、呕吐和吸入胃液。
2. 手术室布置
- 准备麻醉机,并确保它已准备好再呼吸回路。
- 如下所述安排手术室(图1A)。
- 用无菌窗帘盖住手术台,并在下面放置循环水毯以帮助调节体温。
- 摆放一张桌子,上面摆放着诱导用品和手术准备材料。用燃烧器装置和控制箱设置一张桌子。设置成像设备,并确保其已打开。
3.猪的镇静
- 肌内注射TKX(Telazol 4.4 mg/kg;氯胺酮2.2 mg/kg;甲苯噻嗪2.2 mg/kg),剂量为1mL/50 lb,镇静猪。在手术室中通过面 罩输送1 %-3%异氟醚。
- 根据IACUC方案给猪施用(术前)镇痛药;一些例子如下:丁丙诺啡0.3mg/mL,0.01-0.05mg/kg肌注;卡洛芬 50 mg/mL,4 mg/kg 肌注或 SQ;芬太尼透皮 100 mcg/h 放置在耳廓上;加巴喷丁 300 mg 胶囊,3-10 mg/kg PO。
注意:对于所有烧伤和活检程序,将在手术前一天给予 1 剂加巴喷丁,在手术当天给予 1 剂卡洛芬。对于主要燃烧程序,将放置芬太尼贴片,并在手术准备期间给予 1 次全剂量丁丙诺啡。
4.麻醉诱导
- 用交替的 2% 氯己定磨砂膏和酒精对耳朵进行消毒至少 3 次。将静脉导管中的A 22-18 G 1插入边缘耳静脉,并确认血流。用生理盐水冲洗导管,并用手术胶带固定导管(图1B)。
- 一旦 通过 面罩吸入麻醉实现肌肉松弛,就用适当大小的气管插管(7-9毫米)给猪插管。通过观察到下颌张力的丧失和睑反射来检查肌肉松弛。
- 打开管子,使用空气注射器测试袖带泄漏。借助喉镜30 插入管子。
- 给袖带充气,并在确认正确放置后固定管子。将清管器连接到再呼吸回路。
注意: 将管子绑在鼻子上,并使用卷纱布将其固定。用听诊器对胸部进行听诊,以确认管子的正确放置。
注意: 在麻醉期间,每 5-10 分钟通过关闭弹出阀并按下再呼吸袋供气一次,直到压力计达到 20 mm/Hg,以防止位置性肺不张。
- 监测动物和麻醉深度。
- 将清管器连接到多参数监视器。监护仪将连续读取血氧饱和度 (SpO 2)、脉搏率、呼气末二氧化碳 (EtCO2)、呼吸频率和体温。在整个手术过程中每 10 分钟记录一次生命体征。
- 在开始伤口之前,通过捏后腿脚趾测试疼痛反射来评估麻醉深度。
注意: 必要时,调整麻醉剂蒸发器以进行额外的麻醉,或等待几分钟。在整个手术过程中定期检查疼痛反射和睑反射。
5. 烧伤的动物准备
- 断开猪与麻醉机的连接,并将其移至手术台。将清管器置于胸骨卧位,并确保固定所有连接的管路和管子(图1C)。
- 将猪重新连接到麻醉机,并将O2 保持在0.8-1.5L / min,将异氟烷保持在1%-3%,直到手术结束。
- 以 8-10 mL/kg/h 的滴速向猪施用静脉输液 (LRS)。如步骤4.3所示监测麻醉。
6.皮肤烧伤部位的防腐剂和标记
- 如下所述,通过剃须和涂抹脱毛膏来准备伤口区域(图2)。
- 使用电动剪从脊柱一直到两侧腋窝约25厘米宽的区域内剃除猪背。
- 将脱毛膏涂抹在剪裁的区域,静置 3-7 分钟。使用干净的吸水毛巾将乳霜和头发一起去除。
- 烧伤部位的准备
- 用交替的2%氯己定擦洗膏和70%异丙醇擦洗要受伤的区域至少三次,持续约5分钟。确保由戴着无菌手套的人员以靶心模式(从中心开始,以螺旋状向外移动)涂抹磨砂膏。
- 使用无菌烧伤模板和手术皮肤标记标记伤口部位(图2B)。在背部对称地标记 6 到 8 个伤口(2 英寸 x 2 英寸)。
- 用无菌窗帘覆盖标记部位周围的区域以减少污染(图2C)。
7. 烧伤程序
- 使用燃烧装置,例如内部制造的定制燃烧器,该燃烧器由连接到金属手写笔的 2 英寸 x 2 英寸不锈钢块(重量:352 克)、电子微量器和电子秤(总重量:1,714 克; 图3)。
- 将燃烧器设置为所需温度。在150°C下调整全层伤口的目标温度(图3A)。为此,请将控制单元上的设定点 (SP) 调整为 150 °C。 将低设定点设置为145°C,将高设定点设置为155°C(图1D)。
- 通过使用连接到烧伤装置的加热不锈钢块并将它们放在皮肤上 60 秒,创建 2 英寸 x 2 英寸的全层烧伤伤口(图 3B、C)。在燃烧过程中,使用电子秤确保燃烧器施加均匀的压力。
8. 烧伤创面评估和影像学检查
- 数码摄影
- 使用数码单反相机和电焦短焦距 (EFS)、17-55 毫米超声波广角镜头和手电筒对伤口进行成像。
- 拍一张整头猪的数码照片,包括一张标有猪标识、时间点和日期的标语牌。然后,为每个伤口分别拍摄图像,显示带有猪 ID、伤口 ID 和时间点以及尺子的标语牌。
- 计算伤口面积作为每个收集时间点原始伤口大小的百分比,直到第 56 天。
注:在这项工作中,每个时间点(d0、d7、d14、d28 和 d56)的伤口面积计算为 d0 上原始伤口面积的百分比。
- 激光散斑成像 (LSI)
- 对于激光散斑成像,使用基于激光散斑对比分析(LASCA)技术的血液灌注成像仪来实时评估伤口微血管灌注。
- 在一次记录中拍摄所有伤口的图像。调整从激光相机到伤口的工作距离的测量值,使其与每个伤口的成像一致(图4A)。
- 通过在 10-15 秒内拍摄的一系列图像记录灌注。对伤口进行成像后,记录会自动暂停,一旦相机针对后续伤口进行调整,记录就会恢复。每次录制暂停时,都会添加一个标记来识别伤口。
- 经表皮失水 (TEWL)
- 使用标准装置,TEWL探头和软件测量每个伤口的TEWL(图4B)。对于每个伤口,在探头尖端上放置一个干净的探头盖,探头尖端将与伤口组织接触。
- 将探头轻轻均匀地放在皮肤上,然后按设备上的开始按钮 开始 读数。
- 测量每个伤口五次,首先在中心,然后在每个角落。然后,将所有读数导出到电子表格(图4B)。
- 谐波超声 (HUSD)
- 通过用超声(US)探针从中线(脊柱)扫描伤口来执行HUSD映射,从正常皮肤开始,到猪的外侧,再次出现正常皮肤。使用超声机在B模式和组织弹性成像模式下对每个伤口进行扫描模式(图4C)。
- 对于 B 模式扫描,将无菌超声凝胶涂抹在伤口区域,并在 ML-615 高分辨率探头上涂抹一些。用伤口识别标签对每个记录进行注释。开始记录,然后将探头从伤口中线缓慢向下移动,直到到达另一侧的正常皮肤。
注意: 完成扫描后,记录将被保存并从本机导出以供分析。 - 对于弹性成像,按下 Elasto 按钮将超声机切换到弹性波模式。以与B模式扫描相同的方式再次扫描伤口,确保探头保持均匀的压力,以使弹性成像颜色指示剂(绿色条)在整个记录过程中保持可见。
注意: 适当的压力可以通过记录上的比例尺确定,当进行正确的接触时,比例尺显示为绿色(图 4D)。 - 在 B 模式和弹性模式(每个伤口两次记录)下对每个伤口进行成像后更改注释。更改软件中的注释以包含下一个伤口的信息,然后对后续伤口重复该过程。
- 对于 B 模式扫描,将无菌超声凝胶涂抹在伤口区域,并在 ML-615 高分辨率探头上涂抹一些。用伤口识别标签对每个记录进行注释。开始记录,然后将探头从伤口中线缓慢向下移动,直到到达另一侧的正常皮肤。
- 通过用超声(US)探针从中线(脊柱)扫描伤口来执行HUSD映射,从正常皮肤开始,到猪的外侧,再次出现正常皮肤。使用超声机在B模式和组织弹性成像模式下对每个伤口进行扫描模式(图4C)。
9.包扎和敷料
- 用透明薄膜敷料或测试敷料单独覆盖烧伤伤口(图5A,B)。在整个伤口区域放置较大的透明薄膜敷料(图5C)。
- 在猪的整个躯干周围松散地涂上第二层卷纱布,以吸收来自伤口的任何液体渗出物。将猪从侧面来回滚动,稍微向后滚动,将绷带材料包裹在猪身上。
- 用一层柔性弹性绷带松散地覆盖纱布(图5D)。确保绷带不要太紧,因为绷带贴得太紧会限制呼吸并对腹部施加压力,从而导致直肠脱垂或其他并发症。
注意: 弹性绷带具有弹性,在使用过程中很容易过度收紧。将其从卷筒上拉下并让它放在前一个包裹的边缘上有助于防止过度拧紧。 - 用松紧带中的最后一层4覆盖弹性绷带(图4E)。同样,确保敷料不要太紧,但要确保敷料固定在顶部和底部边缘,以防止它在手术后猪四处走动时滑落。
10. 动物恢复和术后护理
- 恢复
- 完成伤口、成像程序和包扎后停止使用麻醉气体。让猪保持氧气至少5分钟。
- 返回主围栏后,将清管器从运输/升降台移至笼子中的泡沫回收垫上。抬起自动饮水器,并取下 j 型喂食器,以防止在恢复过程中对猪造成伤害。
- 如果存在体温过低,用毯子(包括暖风毯)盖住猪。每 10-15 分钟监测和记录一次生命体征,包括体温、脉搏、呼吸频率和 SpO2 。
- 持续监测猪,直到它能够独立保持胸骨卧位。一旦猪完全恢复,放下饮水器,然后也可以喂猪。
- 疼痛评估
- 使用改良的格拉斯哥疼痛评分表进行术后疼痛评估。确保在术后的前 3-4 天内,实验室或 LARC 工作人员至少每 12 小时完成一次疼痛评估。疼痛评分的频率由主治兽医决定。如果动物得分高于 5,则给予抢救镇痛(丁丙诺啡或氢吗啡酮)。
- 通过在术前给予一定剂量的丁丙诺啡 0.01-0.05 mg/kg 肌注来提供镇痛,并在 8-12 小时后给予第二剂。
- 在烧伤前将芬太尼贴片(100 mcg/h)放在耳廓上。
- 术前注射卡洛芬 4 mg/kg IM 或 SQ,然后每天一次 IM、SQ 或 PO,持续 2 天或按照 LARC 兽医的指示。
- 口服加巴喷丁 3-10 mg/kg,剂量在手术前一天、手术当天早上、手术后晚上给药,然后每 12 小时给药一次,持续 3-5 天。
- 节食
- 确保猪被恢复,然后根据其基于体重的日粮每天两次免费获得水和食物。
- 提供丰富的食物(新鲜水果和蔬菜、冷冻水果、棉花糖、酸奶、布丁等),如果观察到食欲下降,则用这些来诱食。
- 换药
- 每周至少更换一次绷带,如果绷带变脏或适应治疗策略,则更频繁地更换绷带。
- 在麻醉下成像后更换绷带,或仅用TKX镇静猪以更换敷料。
- 要更换绷带,首先要用李斯特绷带剪刀或创伤剪小心地去除弄脏的绷带,注意不要让敷料的外部与伤口接触。
- 如果需要,在干净的纱布上使用 0.9% NaCl 清洁伤口周围的区域,然后轻轻擦干该区域。按照第 9 节中概述的包扎程序步骤进行操作。
注意:如果正在使用实验性敷料,则可以在用透明薄膜敷料覆盖伤口之前使用这些敷料。
- 成像频率
- 在整个研究的不同时间点获得成像(数码照片、LSI、TEWL 和 HUSD)。收集接种后第 -3 天(烧伤)、第 0 天(接种)和第 7 天、第 14 天、第 28 天、第 35 天和第 56 天的影像学数据。
11. 生物膜制备和接种
- 接种物制备
- 从 铜绿假单胞菌 (PA01)的甘油冷冻原液中制备起始板,用于细菌的纯培养。在低盐Luria-Bertani琼脂(LBA)中培养 铜绿假单胞菌 培养物,并在37°C下孵育过夜。
- 第二天用单个 铜绿假单胞 菌菌落接种5mL低盐Luria-Bertani肉汤(LBB),并在37°C下孵育过夜,以200rpm振荡。
- 为了获得对数期细胞,将200μL过夜培养物接种到5mL LBB中,并在振荡器中以200rpm在37°C下孵育2.5小时。
- 使用分光光度计测量600nm(OD 600)处的光密度。在 900 μL 无菌 LBB 中使用 100 μL 培养物制备高达 1 x 10−9 的连续稀释液。
注意:我们从未稀释的样品开始,以1 x 10 7 CFU / mL结束,我们在1 x 107稀释液中获得了可计数的菌落,因此我们将该稀释度视为最终稀释度。 - 将100μL每种稀释液涂抹在LBA上,并在37°C下孵育过夜。 根据标准微生物学方案,使用显示可计数菌落(30-300)的稀释液进行菌落计数,并获得菌落形成单位(CFU)。
- 伤口接种
- 将200μL从过夜培养物接种到5mL的LB肉汤中,并在37°C的振荡器中孵育2.5小时。
- 在600nm(OD 600)处测量日培养物的光密度。对于 PA01 接种,使用 3 x 10 8 CFU/mL(每个伤口接种 250 μL 1 x 108 CFU/mL PA01)。将接种物装在生物危害容器中运输到动物设施。
- 在烧伤后第3天使用移液管将接种物分散在暴露伤口的表面上,并使用一次性撒布器均匀分布(图6)。在包扎之前,保持伤口开放约15分钟。
注意:所有外科手术、接种、组织活检、成像和包扎均在全身麻醉下进行,如第 3 节和第 4 节所示。
- 确认感染的确定
注意:为了确认伤口在接种后已成功感染,使用了几种方法,并将伤口样本与从正常皮肤收集的样本进行比较;以下是一些示例。- 对于在不同时间点收集的样本的基于病理学的分析,使用菌落形成单位的计数来估计感染 (CFU; 图 7E、F)。
- 通过穿刺活检收集 6 毫米的伤口组织。标记并称量空的 5 mL 圆底管。将样品转移到试管中,并用样品称量试管。
- 用手术刀在无菌表面上切碎组织。在 BSL2 引擎盖中执行所有步骤。
注意:为确保组织易于均质化,尺寸应非常小(但不小于 0.5 毫米) - 将样品放入试管中,加入 1mL PBS。使用硬组织研磨探针混合和研磨组织。
- 连续稀释(未稀释至1×10-5)匀浆,并在选择性(假单胞菌分离琼脂,PIA)和非选择性(LBA)培养基中接种50μL每种稀释液。
- 将所有稀释液在37°C的有氧条件下孵育18-24小时。在适当的照明条件下对板进行成像。
- 选择具有 30-300 个菌落的平板,如果没有一个平板达到该浓度,请使用未稀释的平板。使用ImageJ计算菌落数,并通过将平均值乘以最终稀释因子来计算每板的CFU。
- 使用扫描电子显微镜(SEM)从接种后第7天和其他时间点收集的样品中获取图像,以确认细菌生物膜的存在(图7G)。
注意:选择接种后第 7 天是因为这是生物膜感染建立和烧伤焦痂软化开始的日子,这允许 US 波的穿透,从而可视化更深的组织。 在图 4 中,检查第 3 天的 US 烧伤伤口图像,该图像显示了阻止 US 波通过更深层组织的厚皮革状焦痂。 - 用针对 铜绿假单胞菌 的特异性抗体对伤检切片进行染色,以确认特定细菌的存在,如先前的出版物13 所示(图7H)。
- 进行下一代测序 (NGS),发表在 Sinha 等人 31 中。定量从接种后第 7 天开始到研究结束的不同时间点收集的感染伤口和正常未感染皮肤样本中的细菌 16srRNA。
- 对于在不同时间点收集的样本的基于病理学的分析,使用菌落形成单位的计数来估计感染 (CFU; 图 7E、F)。
12. 活检采集
- 收集组织活检进行接种后第 7 天、第 14 天、第 28 天和第 56 天成像后的分析。仅从每个伤口收集一次活检,以尽量减少对愈合过程的干扰。
注意:所有外科手术、接种、组织活检、成像和包扎均在全身麻醉下进行,如第 3 节和第 4 节所示。- 用0.5%布比卡因浸润伤口周围区域。使用带有 10 号刀片的一次性手术刀,从伤口的一个边缘切开一条 3-4 毫米宽的条带,在两侧保持正常皮肤的小边缘。将条带放入装有 4% 缓冲福尔马林的标记锥形管中进行固定。
注意:对于早期时间点成像和活检程序,将在手术准备期间给予全剂量的丁丙诺啡。对于晚期活检程序,将在手术准备期间给予半剂量的丁丙诺啡。在所有烧伤和活检程序后,加巴喷丁将按照主治兽医的建议给予长达 7 天的 BID。卡洛芬将在术后几天或按照主治兽医的建议服用。 - 从伤口(从伤口床或伤口边缘)切出 6 毫米的穿孔活检。从伤口边缘收集,包括部分正常皮肤和伤口床,用于不同类型的分析。
- 使用灭菌的镊子和解剖剪刀取出样品。将活检样本放入适当的试管或盒中进行处理和分析。
- 对于 CFU、SEM、RNA 和 FPPE,使用适当的缓冲液将样品保存在试管中。例如,可以将样品放入盒式 OCT 中,用于激光捕获显微镜 (LCM) 和免疫组织化学 (IHC)。
- 收集样本后,用无菌纱布轻轻按压伤口,实现止血。用不粘连的敷料和绷带覆盖伤口,如第 9 节所示。
- 用0.5%布比卡因浸润伤口周围区域。使用带有 10 号刀片的一次性手术刀,从伤口的一个边缘切开一条 3-4 毫米宽的条带,在两侧保持正常皮肤的小边缘。将条带放入装有 4% 缓冲福尔马林的标记锥形管中进行固定。
13. 安乐死和组织采集
- 在安乐死当天用TKX镇静猪,并用异氟醚麻醉。按照第 3 节中概述的步骤将静脉导管放置在边缘耳静脉中。按照第 4 节中的步骤对猪进行插管。
- 猪被麻醉后取下绷带,并清洁伤口周围的区域。
- 完整的数码摄影、LSI、TEWL 和 HUSD 成像。按照第 12 节中概述的步骤从伤口和正常皮肤中收集样本。
- 一旦收集了所有必需的样本, 通过 静脉注射市售的安乐死溶液(戊巴比妥钠)对仍处于麻醉状态的猪进行人道安乐死。使用听诊器听诊以确认心跳停止和自主呼吸。
- 按照 SOM IACUC 的要求,使用手术刀诱发气胸,执行安乐死的辅助方法。将猪胴体转移到桶中,然后运输到冷冻室进行焚烧。
结果
使用标准化烧伤装置在150°C下创建全层烧伤创面1分钟,这导致均匀的深度烧伤,红斑和炎症边缘均匀(图3和图7)。每头猪的背部有八处全层烧伤,如图3C所示。
通过B型高分辨率超声对烧伤创面进行无创实时评估,以确认伤口深度和伤口愈合随时间推移的进展,显示皮下脂肪之前的所有皮肤层均被破坏(图4)。激光散斑成像(LSI)用于进一步表征伤口灌注(图4A)。
到接种后第7天,烧伤创面在创面上显示一层厚厚的化脓膜,从而证实了感染和烧伤创面生物膜的建立(图7A)。数字平面测量显示,由于伤口部位和边缘的炎症反应,接种 PAO1 后第 3 天伤口面积增加(图 7A、B)。尽管在接种后第14天伤口面积开始缩小,但在第56天观察到伤口愈合不完全至原始伤口大小的约25%,表明伤口的慢性(图7B)。TEWL 进一步证实了伤口慢性化和伤口愈合受损,其显示经表皮水分流失率高。TEWL结果反映了与正常皮肤相比,在所有测量的时间点上皮肤屏障功能的丧失,从而表明烧伤伤口愈合的功能障碍(图7B)。紧密连接蛋白 ZO-1 和 213 的抑制以及皮肤屏障功能恢复的损害也证实了这一点,这反映在第 35 天(中期)和第 56 天(晚期)的高 TEWL 值中,尽管视觉伤口闭合(图 7I)。
通过H&E染色进一步验证了烧伤深度,显示所有组织学皮肤层的变形和坏死,如图7C所示。在接种后第7天,通过CFU(图7E,F),SEM成像(图7G)和免疫荧光染色(图7H)进一步验证PA01的生物膜。

图 1:程序的设置 。 (A) 手术台准备。(B) 耳静脉插管静脉输液和给药。(C) 保温毯覆盖物,以保护猪在手术过程中免受体温过低的影响。(D) 燃烧器和定时器设置。 请点击这里查看此图的较大版本.
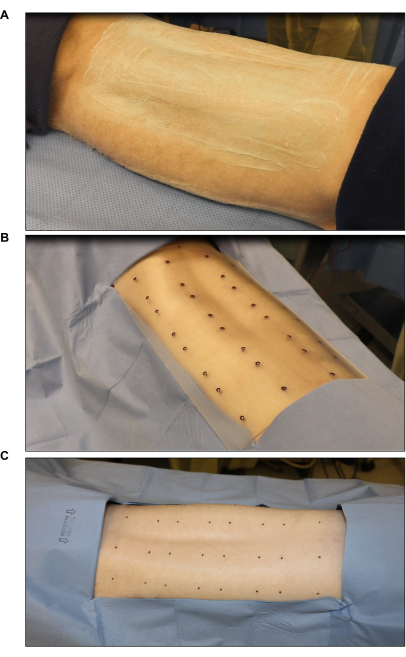
图 2:手术部位灭菌和标记 。 (A) 剪发和消毒。(B) 使用无菌八伤口标准模板标记烧伤部位(每个伤口为 2 英寸 x 2 英寸)。(C) 使用无菌皮肤标记进行最终标记。 请点击这里查看此图的较大版本.
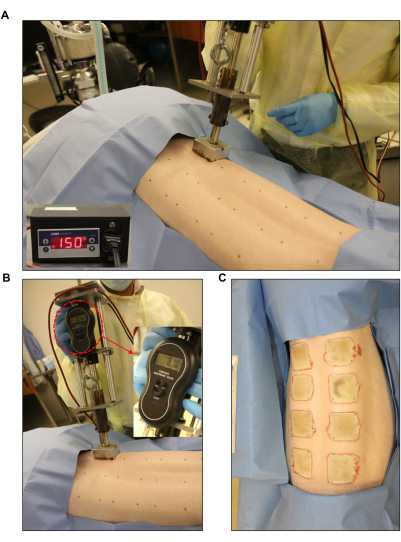
图 3:烧伤创面诱导。 (A,B) 标准化燃烧器,带有压力表和自动控制器单元(2 英寸 x 2 英寸),应用于预先标记的伤口部位。(C) 整个背部显示八个全层烧伤伤口。请点击这里查看此图的较大版本.
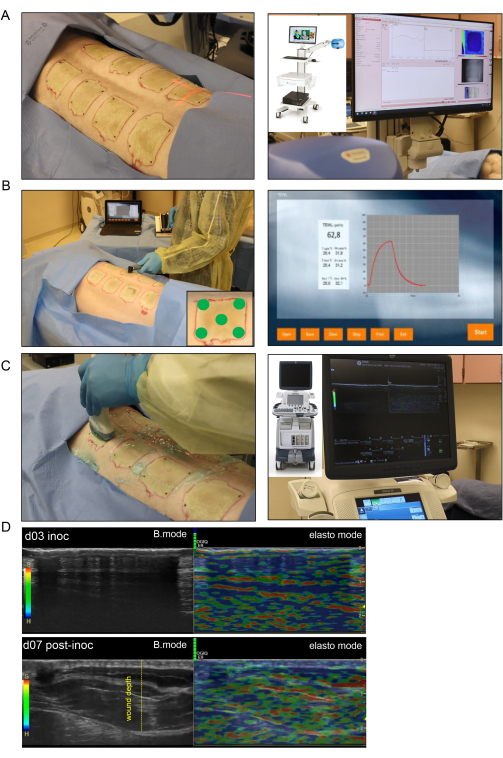
图 4:无创烧伤创面成像和评估。 (A) 激光散斑成像 (LSI) 激光束指示器正确指向伤口中心,如左侧图像所示;右图显示了LSI设备和实时皮肤血管灌注图。(B) 左侧图像显示了在五个不同点(四个伤口角和右下角图像中显示的中心)将经表皮失水 (TEWL) 探针应用于伤口部位;右侧图像是TEWL测量的代表性实时捕获屏幕。(C) 左侧显示使用高分辨率 16 MHz 超声探头对烧伤创面进行的谐波超声扫描;右图显示了超声设备和实时屏幕录制。(D) 接种日和接种后第 7 天烧伤创面部位的结构(B 型图像、灰度超声)和生物力学(弹性成像、彩色超声)图像。伤口深度由黄色虚线表示。 请点击这里查看此图的较大版本.
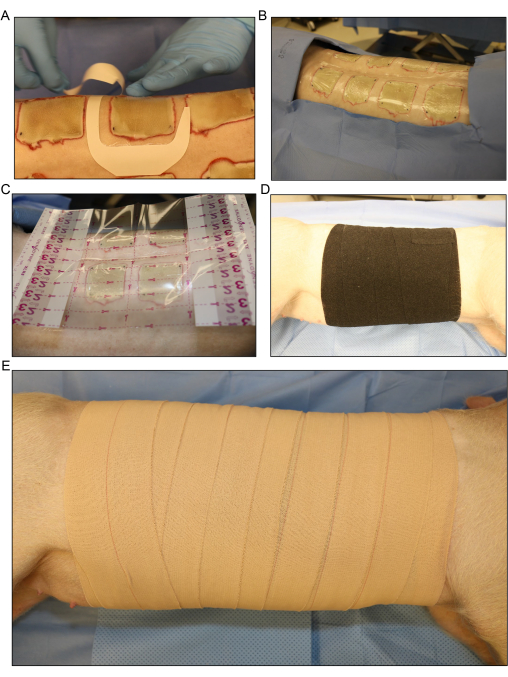
图 5:伤口敷料和包扎。 (A) 对每个伤口分别应用透明薄膜敷料。(B)所有背侧接种的烧伤创面均覆盖第一层敷料。(C) 在整个伤口区域放置较大的透明薄膜敷料。(D) 在猪的整个躯干周围涂上第二层纱布和一层松散的弹性绷带,以吸收来自伤口的任何液体渗出物。(E) 用最后一层 4 层粘性敷料覆盖整个伤口区域。请点击这里查看此图的较大版本.
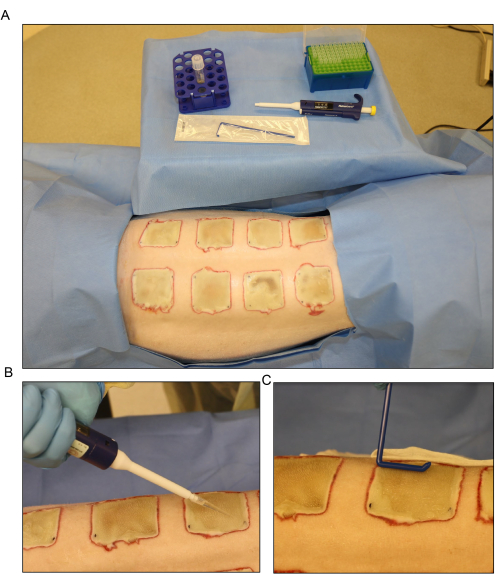
图6:细菌接种 。 (A) 烧伤后第 3 天铜 绿假单胞 菌 (PA01) 接种的设置。(B) 用移液管局部应用接种物,每个伤口使用 500 μL 体积。(C) 使用无菌一次性撒布器将接种物均匀地分散在伤口表面。 请点击这里查看此图的较大版本.
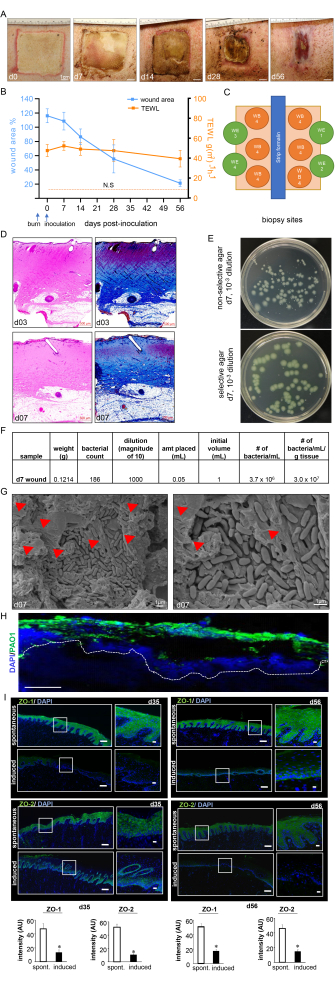
图 7:伤口愈合进度和生物膜确认。 (A) 研究时间线上伤口闭合的代表性图像。比例尺 = 1 厘米。 (B) 研究时间线上伤口面积和 TEWL 测量值的定量 (n = 6)。数据表示为平均值± SD.NS 是指正常皮肤的 TEWL 值。(C) 显示不同伤检部位的示意图。D.H&E 染色及其相应的 Masson 三色染色显示烧伤后第 3 天和接种后第 7 天所有皮肤层的变形和坏死。比例尺 = 500 μm。 (E) 非选择性琼脂(Luria-Bertani 琼脂)和选择性琼脂(假单胞菌分离琼脂)的代表性数字图像,其细菌菌落从猪伤口床组织生长。选择性培养基只能准确计数 PA01 菌落。(F) 显示了从接种后第 7 天伤检中取出的菌落计数计算的样本菌落形成单位 (CFU)。(G) 接种后第 7 天接种烧伤伤口的代表性扫描电子显微镜 (SEM) 图像显示已建立的 PA01 生物膜,右侧有放大图像。比例尺 = 1 μm。红色箭头指向细胞外聚合物物质(EPS)。(H) 使用抗假单胞菌(绿色)抗体观察烧伤创面上的铜绿假单胞菌;接种后第 7 天伤检的免疫荧光图像显示铜绿假单胞菌在伤口组织中大量定植。比例尺 = 100 μm。 (I) 接种后第 35 天和第 56 天 ZO-1 和 ZO-2 染色切片的代表性镶嵌(比例尺 = 200 μm)和相应的放大(比例尺 = 50 μm)图像,显示诱导感染后蛋白质表达降低。使用抗 ZO-1(绿色)或抗 ZO-2(绿色)对 OCT 包埋的冷冻切片 (10 μm) 进行染色。使用DAPI对切片进行复染。条形图显示了 ZO-1 和 ZO-2 信号强度的定量。数据以平均值表示±标准差 (n = 3);* 与自发<相比,p 为 0.05。采用Mann-Whitney或Kruskal-Wallis单因素方差检验分析检验显著性。图7H,I由Roy等人修改而来。请点击这里查看此图的较大版本.
讨论
本报告提供了用于建立用于实验研究的慢性伤口生物膜感染猪模型的详细方案。之前已经报道了几种猪生物膜模型22、23、24、25、26,但它们都不是涉及 8 周长期研究的猪模型。慢性伤口是指持续 4 周或更长时间的伤口 14,27,28。文献中没有报道其他慢性伤口生物膜模型。这项工作涉及功能性伤口闭合的概念 2,7,13,15,17,29。2014 年进行的一项研究首次报告说,生物膜感染的伤口可能会在不恢复屏障功能的情况下闭合7.本研究报道了使用经表皮失水 (TEWL) 测量愈合伤口中的皮肤屏障功能。
在解剖学和生理学上,猪的皮肤与其他小动物的皮肤相比,更接近人类皮肤32,33,34。猪和人的皮肤都有厚表皮33,猪的真皮-表皮厚度比在10:1至13:1之间,与人类34,35相当。在组织学和生物力学上,人和猪的皮肤在网状脊、皮下脂肪、真皮胶原蛋白、毛发分布、附件结构以及血管大小和分布方面显示出相似性36,37,38。在功能上,猪和人类在表皮层的脂质、蛋白质和角蛋白成分的组成以及可比的免疫组织学模式方面都有相似之处37,38。与其他小动物相比,猪的免疫系统与人类免疫系统具有更高的相似性,这意味着猪是研究宿主相互作用的合适模型,这些相互作用是伤口感染中病理生物膜复杂性不可或缺的一部分39。对各种动物模型提供的利弊的批判性评估导致人们一致认为,猪代表了研究伤口愈合的有效模型34,38。此外,家猪会自发发生慢性细菌感染,如在人类中观察到的那样10.用于制造伤口的烧伤装置是一种先进的自动烧伤装置,它根据从目标皮肤部位读出的温度22,40提供热能。这种方法提高了烧伤的严谨性和可重复性。使用人类临床细菌分离株感染猪伤口增加了作为临床前模型的价值。
烧伤很复杂,会引起一些全身性扰动20,41。因此,重要的是用足够的液体复苏猪,并防止麻醉和恢复期间体温过低。有几个因素会干扰伤口愈合,包括烧伤后的营养、液体和疼痛42。因此,密切监测营养和疼痛评估非常重要。烧伤后的疼痛可能很严重,并影响动物的行为和饮食。必须积极考虑解决行为问题的干预措施。定期和持续的疼痛评分和管理势在必行。该协议包括一份全面的疼痛评估表,其中包含非常详细的疼痛管理计划。为避免伤口之间的交叉污染,应特别注意在每个伤口上分别涂抹第一层敷料。在处理所有生物危害材料以及对设备、工具和整个手术室进行彻底消毒时,应格外小心。多层敷料的应用可以防止猪在努力揉搓或抓挠瘙痒的背部时暴露伤口。
当前模型中的猪没有受到潜在代谢紊乱(例如糖尿病)的影响,因此,正在研究的影响纯粹是细菌生物膜感染对伤口愈合的影响。然而,该模型适用于诱导糖尿病(例如使用链脲佐菌素),并可用于研究与潜在代谢紊乱相关的生物膜感染。该模型的另一个局限性是使用 铜绿假单胞菌(一种细菌)的受控感染设置。预计猪的正常皮肤微生物群落也可能在伤口中生长,并可能影响愈合。有必要使用NGS或其他先进技术进行进一步分析,以描绘伤口的微生物含量。目前的模型也可以应用于不同微生物物种(例如真菌、病毒等)的混合感染。这是一个重要因素,因为临床相关的伤口可能由混合微生物组成,这可能会对伤口愈合产生不同的影响。
该模型具有许多潜在优势,包括与人类慢性伤口的复杂性和长期后遗症的相似性,自动化和可重复的烧伤过程,以及临床分离细菌物种的使用。使用多种非侵入性成像方式代表了一种强大的方法,可以收集有用的生理数据来表征伤口。最后, 通过 基于TEWL的皮肤屏障功能恢复来评估功能性伤口愈合至关重要。总之,这项工作展示了一种稳健、简单、详细且易于使用的方案,用于使用猪模型系统开发生物膜感染的严重烧伤。
披露声明
作者声明没有利益冲突。
致谢
我们要感谢印第安纳大学实验动物资源中心(LARC)在研究期间对动物的支持和兽医护理。这项工作得到了美国国立卫生研究院拨款 NR015676、NR013898 和 DK125835 以及国防部拨款 W81XWH-11-2-0142 的部分支持。此外,这项工作还获得了以下美国国立卫生研究院的奖项:GM077185、GM069589、DK076566、AI097511和NS42617。
材料
| Name | Company | Catalog Number | Comments |
| Sedation | |||
| Ketamine | Zoetis | 10004027 | 100mg/ml |
| Telazol | Zoetis | 106-111 | 100mg/ml |
| Xylazine | Pivetal | 04606-6750-02 | 100mg/ml Anased |
| 3ml syringe w/ 20g needle | Covidien-Monoject | 8881513033 | |
| Winged infusion set 21g | Jorgensen Labs | J0454B | |
| Anesthetic | |||
| Isoflurane | Pivetal | 21295097 | |
| Surgery | |||
| Hair clippers | Wahl | 8787-450A | |
| Nair | Church and Dwight Co. Inc | 70506572 | |
| Chlorhexidine Solution | First Priority Inc. | 179925722 | |
| 70% Isopropyl Alcohol | Uline | S-17474 | |
| 0.9% Saline Solution | ICU Medical | RL-7282 | |
| Non-woven gauze | Pivetal | 21295051 | |
| Paper tape | McKesson | 455531 | |
| 2" Elastic tape | Pivetal | 21300869 | |
| 18-22g Intravenous Angiocath | SurVet | (01)14806017512306 | |
| Spay hook | Jorgensen Labs | J0112A | |
| Sterile lube | McKesson | 16-8942 | |
| Laryngoscope | Jorgensen Labs | J0449S | |
| Roll gauze | Pivetal | 21295032 | |
| Endotracheal tube (7-9mm) | Covidien | 86112 | Shiley Hi-Lo Oral Nasal Tracheal Tube Cuffed |
| 15gtt/ml IV administration set | ICU Medical | 12672-28 | |
| LRS 1000ml bag | ICU Medical | 07953-09 | |
| Three Quarter Drape Sheet | McKesson | 16-i80-12110G | |
| Analgesia | |||
| Buprenorphine | RX Generics | 42023-0179-05 | 0.3mg/ml |
| Fentanyl Transdermal | |||
| Carprofen | 21294548 | Pivetal | 50mg/ml Levafen |
| Bandaging | |||
| Transparent film dressing 26x30 | Genadyne Biotechnologies | A4-S00F5 | |
| Film dressing 4 x 4-3/4 Frame Style | McKesson | 886408 | |
| Vetrap | 3M | 1410BK BULK | |
| Elastic tape 4" | Pivetal | 21300931 | |
| Kerlix Roll Gauze | Cardinal Health | 3324 | |
| Imaging | |||
| Canon EOS 80D | Canon | 1263C004 | |
| Speedlight 600EX II-RT | Canon | 1177C002 | |
| EFS 17-55mm Ultrasonic | Canon | 1242B002 | |
| GE Logiq E9 | GE | 5197104-2 | |
| ML6-15 Probe | GE | 5199103 | |
| PeriCamPSI | Perimed | 90-00070 | |
| DermaLab | Cortex Technologies Inc | 4608D78 | |
| Biopsy/Tissue Collection | |||
| 6mm punch biopsy | Integra Lifesciences | 33-36 | |
| bupivicaine 0.5% | Auromedics Pharma | 55150017030 | |
| Size 10 Disposable Scalpel | McKesson | 16-63810 | |
| Dissection scissors | Pivetal | 21294806 | |
| Rat tooth thumb tissue forceps | Aesculap | BD512R | |
| Non-adherent Dressing | Covidien | 2132 | Telfa |
| 50ml Conical tube | Falcon | 352070 | |
| Eppendorf/microcentrifuge tube | Fisherbrand | 02-681-320 | |
| OCT Cassette | |||
| Non Woven Gauze 4x4 | Pivetal | 21295051 | |
| Inoculum | |||
| Low salt LB agar | Invitrogen | 22700-025 | |
| Low salt LB broth | Fisher scientific | BP1427-500 | |
| Petri plate | Falcon | REF-351029 | |
| Polyprophyline round bottom tubes (14 ml) | Falcon | REF-352059 | |
| Pseudomonas Agar Base (Dehydrated) | Thermo Scientific | OXCM0559B | |
| LB Agar, powder (Lennox L agar) | Thermo Fisher Scientific (Life Technologies) | 22700025 | |
| Gibco™ DPBS, calcium, magnesium | Gibco | 14040133 | |
| Euthanasia | |||
| 18-22g Intravenous Angiocath | SurVet | (01)14806017512306 | |
| Fatal Plus | Vortech Pharmaceuticals | 9373 |
参考文献
- Goodwine, J., et al. Pyruvate-depleting conditions induce biofilm dispersion and enhance the efficacy of antibiotics in killing biofilms in vitro and in vivo. Scientific Reports. 9 (1), 3763(2019).
- Sen, C. K., Roy, S., Mathew-Steiner, S. S., Gordillo, G. M. Biofilm management in wound care. Plastic and Reconstructive Surgery. 148 (2), 275-288 (2021).
- Church, D., Elsayed, S., Reid, O., Winston, B., Lindsay, R. Burn wound infections. Clinical Microbiology Reviews. 19 (2), 403-434 (2006).
- Nguyen, T. T., Gilpin, D. A., Meyer, N. A., Herndon, D. N. Current treatment of severely burned patients. Annals of Surgery. 223 (1), 14-25 (1996).
- Eriksson, E., et al. Chronic wounds: Treatment consensus. Wound Repair and Regeneration. 30 (2), 156-171 (2022).
- Lebeaux, D., Chauhan, A., Rendueles, O., Beloin, C. From in vitro to in vivo models of bacterial biofilm-related infections. Pathogens. 2 (2), 288-356 (2013).
- Ganesh, K., et al. Chronic wound biofilm model. Advances in Wound Care. 4 (7), 382-388 (2015).
- Bjarnsholt, T., et al. The in vivo biofilm. Trends in Microbiology. 21 (9), 466-474 (2013).
- Stewart, P. S. Biophysics of biofilm infection. Pathogens and Disease. 70 (3), 212-218 (2014).
- Jensen, L. K., Johansen, A. S. B., Jensen, H. E. Porcine models of biofilm infections with focus on pathomorphology. Frontiers in Microbiology. 8, 1961(2017).
- Mah, T. F., O'Toole, G. A. Mechanisms of biofilm resistance to antimicrobial agents. Trends in Microbiology. 9 (1), 34-39 (2001).
- Gonzalez, J. F., Hahn, M. M., Gunn, J. S. Chronic biofilm-based infections: Skewing of the immune response. Pathogens and Disease. 76 (3), 023(2018).
- Roy, S., et al. Mixed-species biofilm compromises wound healing by disrupting epidermal barrier function. Journal of Pathology. 233 (4), 331-343 (2014).
- Sen, C. K. Human wound and its burden: Updated 2020. Compendium of Estimates. Advances in Wound Care. 10 (5), 281-292 (2021).
- Barki, K. G., et al. Electric field based dressing disrupts mixed-species bacterial biofilm infection and restores functional wound healing. Annals of Surgery. 269 (4), 756-766 (2019).
- Dusane, D. H., et al. Electroceutical treatment of Pseudomonas aeruginosa biofilms. Scientific Reports. 9 (1), 2008(2019).
- Roy, S., et al. Staphylococcus aureus biofilm infection compromises wound healing by causing deficiencies in granulation tissue collagen. Annals of Surgery. 271 (6), 1174-1185 (2020).
- Ghanbari, A., et al. Inoculation density and nutrient level determine the formation of mushroom-shaped structures in Pseudomonas aeruginosa biofilms. Scientific Reports. 6, 32097(2016).
- Yin, R., Cheng, J., Wang, J., Li, P., Lin, J. Treatment of Pseudomonas aeruginosa infectious biofilms: Challenges and strategies. Frontiers in Microbiology. 13, 955286(2022).
- Norbury, W., Herndon, D. N., Tanksley, J., Jeschke, M. G., Finnerty, C. Infection in burns. Surgical Infections. 17 (2), 250-255 (2016).
- Nitz, F., et al. Molecular detection of drug-resistance genes of bla(OXA-23)-bla(OXA-51) and mcr-1 in clinical isolates of Pseudomonas aeruginosa. Microorganisms. 9 (4), 786(2021).
- Davis, S. C., et al. Microscopic and physiologic evidence for biofilm-associated wound colonization in vivo. Wound Repair and Regeneration. 16 (1), 23-29 (2008).
- Breuing, K., Kaplan, S., Liu, P., Onderdonk, A. B., Eriksson, E. Wound fluid bacterial levels exceed tissue bacterial counts in controlled porcine partial-thickness burn infections. Plastic and Reconstructive Surgery. 111 (2), 781-788 (2003).
- Nusbaum, A. G., et al. Effective method to remove wound bacteria: Comparison of various debridement modalities in an in vivo porcine model. Journal of Surgical Research. 176 (2), 701-707 (2012).
- Hirsch, T., et al. Enhanced susceptibility to infections in a diabetic wound healing model. BMC Surgery. 8, 5(2008).
- Roche, E. D., et al. Increasing the presence of biofilm and healing delay in a porcine model of MRSA-infected wounds. Wound Repair and Regeneration. 20 (4), 537-543 (2012).
- Hartoch, R. S., McManus, J. G., Knapp, S., Buettner, M. F. Emergency management of chronic wounds. Emergency Medical Clinics of North America. 25 (1), 203-221 (2007).
- Mustoe, T. Understanding chronic wounds: a unifying hypothesis on their pathogenesis and implications for therapy. American Journal of Surgery. 187 (5), 65-70 (2004).
- Bhattacharya, M., et al. Staphylococcus aureus biofilms release leukocidins to elicit extracellular trap formation and evade neutrophil-mediated killing. Proceedings of the National Academy of Sciences of the United States of America. 115 (28), 7416-7421 (2018).
- Chum, H., Pacharinsak, C. Endotracheal intubation in swine. Lab Animal. 41 (11), 309-311 (2012).
- Sinha, M., et al. Pseudomonas aeruginosa theft biofilm require host lipids of cutaneous wound. Annals of Surgery. 277 (3), e634-e647 (2023).
- Fan, G. Y., et al. Severe burn injury in a swine model for clinical dressing assessment. Journal of Visualized Experiments. (141), e57942(2018).
- Sullivan, T. P., Eaglstein, W. H., Davis, S. C., Mertz, P. The pig as a model for human wound healing. Wound Repair and Regeneration. 9 (2), 66-76 (2001).
- Meyer, W., Schwarz, R., Neurand, K. The skin of domestic mammals as a model for the human skin, with special reference to the domestic pig. Current Problems in Dermatology. 7, 39-52 (1978).
- Vardaxis, N. J., Brans, T. A., Boon, M. E., Kreis, R. W., Marres, L. M. Confocal laser scanning microscopy of porcine skin: implications for human wound healing studies. Journal of Anatomy. 190, 601-611 (1997).
- Heinrich, W., Lange, P. M., Stirtz, T., Iancu, C., Heidemann, E. Isolation and characterization of the large cyanogen bromide peptides from the alpha1- and alpha2-chains of pig skin collagen. FEBS Letters. 16 (1), 63-67 (1971).
- Marcarian, H. Q., Calhoun, M. L. Microscopic anatomy of the integument of adult swine. American Journal of Veterinary Research. 27 (118), 765-772 (1966).
- Sullivan, T. P., Eaglstein, W. H., Davis, S. C., Mertz, P. The pig as a model for human wound healing. Wound Repair and Regeneration. 9 (2), 66-76 (2001).
- Dawson, H. D., et al. Structural and functional annotation of the porcine immunome. BMC Genomics. 14, 332(2013).
- Kim, J. Y., Dunham, D. M., Supp, D. M., Sen, C. K., Powell, H. M. Novel burn device for rapid, reproducible burn wound generation. Burns. 42 (2), 384-391 (2016).
- Nielson, C. B., Duethman, N. C., Howard, J. M., Moncure, M., Wood, J. G. Burns: Pathophysiology of systemic complications and current management. Journal of Burn Care and Research. 38 (1), e469-e481 (2017).
- Rowan, M. P., et al. Burn wound healing and treatment: Review and advancements. Critical Care. 19 (1), 243(2015).
转载和许可
请求许可使用此 JoVE 文章的文本或图形
请求许可探索更多文章
This article has been published
Video Coming Soon
版权所属 © 2025 MyJoVE 公司版权所有,本公司不涉及任何医疗业务和医疗服务。