需要订阅 JoVE 才能查看此. 登录或开始免费试用。
Method Article
使用自由呼吸、自门控超短回声时间成像的肺部结构 MRI
摘要
描述了一种使用超短回波时间 (UTE) 磁共振成像 (MRI) 生成肺部高分辨率结构图像的协议。该协议允许在自由呼吸期间使用简单的 MRI 脉冲序列获取图像。
摘要
高质量的肺部 MRI 受到组织密度低、MRI 信号快速松弛以及呼吸和心脏运动的挑战。由于这些原因,肺部的结构成像几乎完全使用计算机断层扫描 (CT) 进行。然而,CT 成像提供电离辐射,因此不太适合某些弱势群体(例如儿科)或研究应用。作为替代方案,使用超短回波时间 (UTE) 的 MRI 引起了人们的兴趣。该技术可以在 ~5-10 分钟扫描过程中的自由呼吸过程中进行。呼吸运动信息与图像一起编码;此信息可用于“自我设控”图像。因此,自门控消除了对高级 MRI 脉冲序列编程的要求或使用呼吸波纹管,从而简化了图像采集。在该协议中,提出了用于获取肺部高质量 UTE MRI 的简单、稳健且计算高效的采集和重建方法。该协议是为在 3T MRI 扫描仪上使用而开发的,但相同的原理可以在较低的磁场强度下实现。该协议包括用于 3D 径向 UTE 图像采集的推荐参数设置以及自门控图像重建的方向,以在不同呼吸期生成图像。通过实施该协议,用户可以生成肺部的高分辨率 UTE 图像,运动伪影最小或最小甚至没有。这些图像可用于评估肺结构,可用于各种肺部疾病的研究用途。
引言
肺部结构的高分辨率成像是许多肺部疾病诊断性检查的重要组成部分。通常,这是使用计算机断层扫描 (CT) 成像进行的,该成像非常适合生成肺部的高分辨率图像1。然而,CT 成像提供非平凡剂量的电离辐射,使其不适合定期重复成像、多个不同呼吸期的成像或某些人群(例如儿科)的成像。磁共振成像 (MRI) 没有相同的电离辐射风险,因此适用于此类成像任务。然而,由于 MRI 的组织密度低、呼吸和心脏运动以及非常快的信号弛豫,因此使用 MRI 对肺部进行成像具有挑战性 2,3,4。
一种能够缓解这些挑战的 MRI 技术是超短回声时间 (UTE) MRI 4,5,6。在 UTE MRI 中,MRI 信号在信号激发后立即采样,这减少了快速信号弛豫的影响。此外,该技术从中心向外对 k 空间进行采样,这会导致 k 空间中心出现明显的过采样。k 空间中心的这种过采样使这种成像技术对运动具有鲁棒性。除了这种固有的运动稳健性外,对 k 空间中心的重复采样还编码有关呼吸运动的信息,从而实现图像的自门控 7,8,9。这种自设门可用于在各种呼吸阶段生成图像。由于人类在呼气期的大部分呼吸期都在度过,因此通常会生成呼气末期的图像,因为该期获得的成像数据最多。
肺部 MRI 中的呼吸自门控有多种策略。首先要做出的区别是基于图像的 vs.基于 k 空间的门控10(图 1)。在基于图像的门控中,通过重建成像数据的较小时间子集来生成一组具有高时间分辨率的图像。随后,这些图像中隔膜的位置用于识别一组给定图像投影的呼吸期10,11。在基于 k 空间的门控中,检查来自 k 空间中心(“k0”)的数据 8,9,12。图像的信号强度以 k0 编码,因此,k0 点的强度随呼吸而变化。因此,可以根据 k0 的强度将投影分为不同的呼吸阶段。在基于图像和基于 k 空间的门控中,具有相似呼吸相位的投影被分组以进行图像重建。有人提出,基于图像的门控在估计呼吸阶段时提供了更高的保真度,从而提供减少模糊的图像10,13。
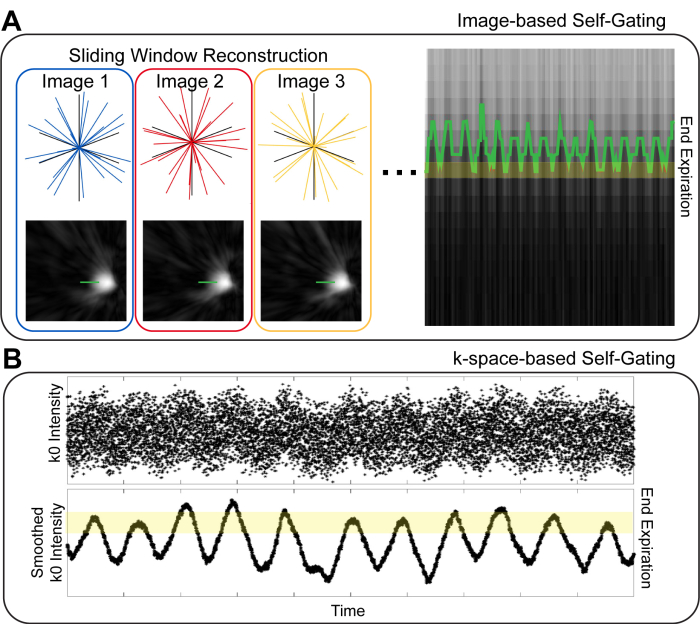
图 1:基于图像和基于 k 空间的自门控技术。 (A) 在基于图像的门控中,显示隔膜的低空间分辨率、高时间分辨率图像是从整体数据的时间子集生成的。使用横膈膜上的线,可以可视化呼吸运动并进行分箱以进行图像重建。(B) 在基于 k 空间的门控中,中心向外 k 空间投影上的第一个点(“k0”)用于可视化呼吸运动。平滑 k0 后,基于呼吸周期的信号强度差异清晰可见,可用于识别不同的呼吸阶段。 请单击此处查看此图的较大版本。
图像和基于 k 空间的门控都可以使用硬门控或软门控11,14 来执行。在硬门控中,仅重建与所需呼吸期相对应的投影。然而,这种丢弃不需要的投影会导致图像信噪比 (SNR) 降低和欠采样伪影增加。这些不良影响可以通过使用软门控来减轻。在软门控中,所有投影都用于图像重建,但来自不需要的呼吸期的投影被加权,以便它们对最终图像的影响较小。这样,可以以最少的伪影和高 SNR 重建图像,同时仍然抑制呼吸运动的影响。
通过将 UTE MRI 采集与采集后自门控相结合,可以生成高质量的图像,这些图像虽然不等同于 CT,但具有接近 CT 成像的对比度和分辨率 6,15,16,17,18,19。在此,提供了一种简单的方案,用于收集和重建 UTE MRI 图像以生成肺结构的高质量图像。
该协议主要是为 3T MRI 扫描仪编写的;3T 是研究 MRI 最常用的场强。较低的磁场强度,例如 1.5T 或最近可用的 0.55 T20 ,可以改善肺内的图像质量和信号强度,因为在这些场强下,肺内的信号弛豫速度较慢。
虽然已尽一切努力在该协议和提供的图像重建代码中提供清晰度和简单性,但该协议可能需要专门的 MRI 物理学家(或类似的 MRI 专家)在 MRI 扫描仪上建立适当的 UTE MRI 序列。MRI 序列应实现具有 Center-out k 空间轨迹的 3D 非笛卡尔编码策略。示例包括 3D 径向或 3D 螺旋(例如,“FLORET”)21,22 成像序列。重要的是,投影的顺序应该具有良好的时间稳定性:在任何给定的时间子集上,投影应覆盖 k-space23 的整个范围。具有良好时间稳定性的投影排序策略的示例是黄金均值或 Halton 随机阿基米德螺旋。如果使用时间稳定性较差的投影排序,则采集后自选通将省略大面积的 k 空间,从而导致图像伪影。最后,该序列应能够实现 <100 μs 的回波时间 (TE)。3T 时肺部的 T2* 弛豫时间为 <1 ms24,因此使用非常短的 TE 对于生成高质量图像至关重要。
研究方案
所有人体成像均经建国大学 IRB 批准进行。已获得所有参与者的书面知情同意书。本研究中的图像是根据通用技术开发方案获得的,并且纳入/排除标准故意宽泛。纳入标准:年龄 ≥ 18 岁。排除标准:根据对 MRI 筛查问卷的回答,MRI 禁忌症和怀孕。用于本研究的附件和设备列在 材料表中。
1. UTE图像采集
- 准备成像序列。准备一次成像序列,并对所有参与者使用相同的序列。
- 参数设置请参见 表 1。
- 将 MRI 模型放在 MRI 的中心并运行成像序列。
注意:由于此序列需要快速梯度性能和许多 RF 脉冲,因此在人体测试之前验证协议设置是否可以运行非常重要。
- 为参与者准备 MRI。使用机构标准的 MRI 安全筛查,以确保参与者可以安全地进入 MRI。
- 将参与者放在 MRI 床上,并在参与者的躯干上放置一个胸环。将线圈靠近参与者的下巴,以确保完全覆盖肺尖。
- 将参与者移动到 MRI 扫描仪中。将定位标志放在参与者胸骨的正下方。
- 收集定位器扫描以确保参与者的肺部在 UTE 扫描的视野内。不要移动 UTE 扫描的几何。如果参与者的肺部不在视野内,请移动参与者并收集额外的定位器扫描,直到肺部完全位于视野内。
- 运行 UTE 序列。在此序列中,参与者可以正常呼吸。
- 从扫描仪导出原始数据。根据所使用的成像序列,扫描仪可能会也可能不会在扫描仪上重建图像。对于拟议的回顾性门控重建,需要原始成像数据来确定图像是否在扫描仪上生成。请注意,原始数据将很大 (>10 GB)。
- 导出或计算 k-space 轨迹(即每个原始数据点在 k-space 中的位置)。
注意:对于某些成像序列,k 空间轨迹可能与原始数据一起存储在 MRI 扫描仪上,并且可以直接导出。对于其他成像序列,需要根据成像参数计算 k 空间轨迹。
| 参数 | 通用推荐设置 | 此处实现的设置 |
| 成像序列 | 具有中心出 k 空间轨迹的 3D 非笛卡尔 | 具有 Golden Means Projection 排序的 3D 径向 |
| 视野 | 400 x 400 x 400 毫米3 | 400 x 400 x 400 毫米3 |
| 矩阵大小 | 根据目标分辨率的需要 | 320 x 320 x 320(1.25 mm 各向同性分辨率) |
| 带宽 | 根据需要,读出持续时间< 1.0 ms | 888 Hz/像素 |
| TE 公司 | < 0.1 毫秒 | 0.07 毫秒 |
| TR 系列 | 最小(目标 3 – 4 毫秒) | 3.5 毫秒 |
| 翻转角度 | 约 5° | 4.8° |
| 投影数 | 最低 100,000 | 1,35,386 |
| 图像持续时间 | 最少 5 分钟 | 7 分 54 秒 |
表 1:UTE 成像的推荐设置。 提供了可用于指导协议设置的通用推荐设置。此外,还提供了用于数据的特定建议设置,如代表性结果所示。除带宽外,参数规范在供应商之间是通用的。一些主要的 MRI 供应商将带宽指定为 Hz/Pixel。其他主要 MRI 供应商指定了绝对带宽。建议的带宽 (888 Hz/Pixel) 对应于 284,160 Hz 的绝对带宽。
2. 使用基于图像的呼吸软门控进行 UTE 图像重建
注意:https://github.com/pniedbalski3/UTE_Reconstruction 中提供了完成以下步骤的 MATLAB 代码。
- 将数据和 k 空间轨迹导入 MATLAB。用于导入原始 MRI 数据的代码适用于所有主要的 MRI 供应商。
- 丢弃前 1000 个投影,以确保数据处于稳态磁化状态。
注意:如果使用的成像序列包括数据采集前的虚拟扫描,则可以跳过此步骤。 - 使用非常小的数据子集重建低分辨率图像。
- 使用 非均匀快速傅里叶变换 将图像重建为 96 x 96 x 96 的矩阵大小。
- 使用大约 200 个投影,对应于 0.6 秒到 0.8 秒的数据。
- 重建和存储来自所有线圈元件的图像以及最终的线圈组合图像。
- 在生成的线圈组合图像中,选择清晰显示光阑的 冠状切片 。
注意:提供的代码将提示用户选择包含隔膜的切片。 - 选择此切片后,查看此切片 的单个线圈 图像,并选择最能显示振膜的一个 或两个线圈 元件(图 2)。
注意: 提供的代码将提示用户选择线圈元件。 - 使用 滑动窗口 重建图像,以生成具有 ~0.5 秒时间分辨率的图像(图 2)。
- 仅从步骤 2.4 中选择的线圈单元中重建数据。
注意:虽然所有线圈元件都可以重建,但只需要最靠近隔膜的元件来可视化隔膜,以便进行呼吸自门控。通过仅重建最靠近图的线圈元件,重建时间和计算负担大大减少。 - 使用前 200 个投影使用非均匀快速傅里叶变换重建图像(图 2)。仅存储显示隔膜的切片(如步骤 2.4 所示)。
注意:最终,将生成多达 1500 张图像;只需要一个 2D 切片来可视化隔膜位置,并且为每个滑动窗口台阶存储 3D 图像将是令人望而却步的。 - 偏移 100 个投影(即,使用投影 1-200 重建第一个图像。第二个是使用投影 101 - 300 重建的)并重建一个附加图像,存储在步骤 2.4 中选择的切片。
- 继续操作,直到所有投影都用于生成图像。
- 仅从步骤 2.4 中选择的线圈单元中重建数据。
- 在第一个滑动窗口图像中,在 隔膜 上选择一条线。确保线足够长,可以通过 5-10 个体素延伸到肺部,通过 5-10 体素延伸到隔膜。
- 通过查看所有投影的 呼吸导航 仪来可视化呼吸运动。
- 确定所有呼吸导航仪的隔膜位置。有多种方法可以做到这一点,但一种简单的方法是使用 Otsu 的方法25 将较暗的一面(肺)与较亮的一面(隔膜)分开。
- 使用隔膜位置将突起标记为属于给定的 Respiratory Bin。如果给定的呼吸导航器在“位置 1”显示隔膜,那么用于为该导航器生成图像的 200 个投影将属于“bin 1”。
注意:由于图像是使用具有 100 个投影重叠的滑动窗口生成的,因此某些投影可能会被标记为属于多个素材箱。滑动窗口图像的粗略空间分辨率导致总共有 ~4-6 个分箱,涵盖了 Inspiration 到 Expiration 的整个范围。 - 通过确定哪个 bin 具有最多的投影(应对应于结束过期)来选择要重建的 bin 。
- 或者,根据呼吸导航仪的目视检查重建所需呼吸阶段的图像。
- 生成用于软门控的权重14.
- 使用 指数滤波器 为主 bin 内的投影提供权重 1,并为不同呼吸 bin 内的投影提供权重。
- 使用 Berkely Advanced Reconstruction Toolbox (BART;https://mrirecon.github.io/bart/)26,27 在所需的呼吸箱处重建高分辨率图像。
注意:BART 是一个免费提供的 MRI 图像重建工具箱。- 使用迭代密度组合计算 密度补偿权重 。
- 通过软门控权重缩放密度补偿权重。
- 基于密度补偿和软门控权重缩放数据
- 执行基本的非均匀快速傅里叶变换 (NUFFT) 以促进线圈组合。
- 将 NUFFT 图像转换为网格化 k 空间,用于线圈组合。
- 生成线圈组合矩阵,并使用它来组合原始数据和网格化 k 空间的线圈。
- 估计线圈灵敏度。
- 使用加权密度补偿、线圈组合数据和线圈灵敏度图执行并行成像压缩感知重建。
- 保存最终图像。NIFTI 格式很容易实现。如果要将图像上传到 PAC 系统,则可能需要 DICOM 格式。
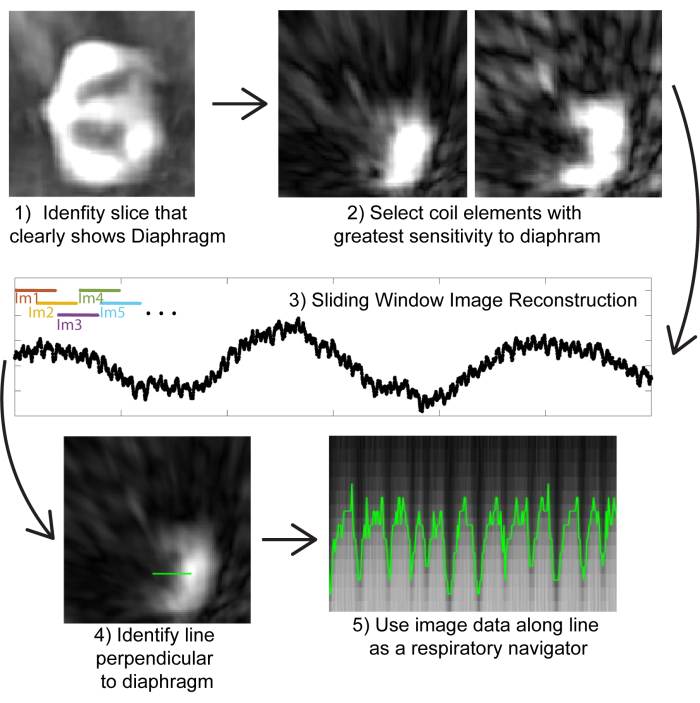
图 2:基于图像的自选通。 (1) 使用从少量投影重建的低分辨率图像(为了计算效率),识别清晰显示隔膜的冠状切片。(2) 通过检查来自各个线圈元件的图像,选择最靠近膜片的线圈元件。(3) 仅对最靠近隔膜的线圈元件进行滑窗重建(以提高计算效率)。可以从 200 个投影的子集(相当于 ~0.8 秒)生成图像;通过重叠投影,可以在图像中实现 ~0.5 秒的伪时间分辨率。(4) 确定一条垂直于隔膜的线,用作呼吸导航器。(5) 可视化此线上的图像数据显示呼吸运动,可用于对图像进行分箱。 请单击此处查看此图的较大版本。
3. 使用基于 k 空间的呼吸软门控进行 UTE 图像重建
- 完成步骤 2.1-2.4,以便识别最靠近隔膜的线圈元件。
- 为所选线圈元件的所有投影使用投影上第一个点的绝对值,生成 k0 时间序列跟踪。这将提供呼吸波形的可视化。
- 以 5000 次投影为步长,通过相同 k0 点28 的平均信号强度对 k0 进行归一化。这减轻了信号强度随时间推移的漂移,并提高了定量分箱投影的能力。
- 将每个 k0 点标记为在吸气或呼气期间发生。
- 对 k0 时间序列进行平滑处理,并采用导数来评估门控轨迹上每个点的斜率。
- 根据斜率的标志标记灵感点。正斜率对应于 expiration,而负斜率对应于 purination。
- 基于信号强度的 Bin 投影。由于呼吸深度可以是可变的,因此 bin 投影基于信号振幅,而不是在呼吸阶段的位置。
注意:实现此目的的一种简单快速的方法是实施 k-means 聚类来识别不同的信号强度水平。 - 对于介于吸气末和呼气末之间的区间,根据步骤 3.4 确定在吸气和呼气期间发生的投影。
- 按照步骤 2.10 到步骤 2.13 中提供的步骤完成图像重建。
- 如果需要,重建所有呼吸箱的图像,而不仅仅是在呼气结束时。
结果
代表性结果(图 3)是使用 表 1 中所示的设置生成的。使用的成像持续时间可提供大多数参与者可以忍受的高质量图像。
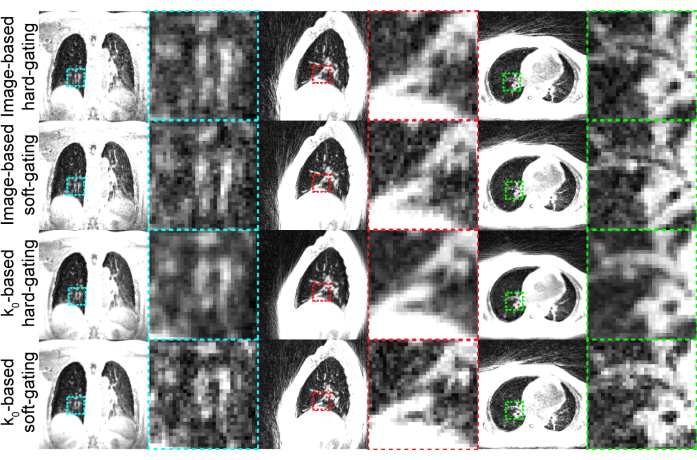
图 3:生成的代表性 UTE 图像。 显示了同一患者的冠状、矢状?...
讨论
在进行肺部 UTE 成像时,可以使用采集和重建的许多变体来生成肺部图像。该协议侧重于易于实现和计算效率。使用 3D 放射状 UTE 进行成像相对简单,成像序列通常可从主要 MRI 供应商处获得。提供了基于 MATLAB 的工具,用于数据处理和自门控。由于大多数学术机构都可以访问 MATLAB 许可证,因此此代码应广泛使用且易于实现。提供的 MATLAB 代码是为使用 Siemens 3T MRI 扫描仪?...
披露声明
Peter Niedbalski 获得了美国国家硬皮病基金会、美国心脏协会和 NIH 的研究资助。他是 Polarean Imaging Plc. 的顾问,该公司开发超极化 129Xe MRI 技术。
致谢
该协议的制定和显示为代表性结果的图像得到了美国国家硬皮病基金会的支持。
材料
| Name | Company | Catalog Number | Comments |
| Chest MRI Coil | Siemens, GE, Philips,, Other Clinical MRI Imaging Coil Vendor | N/A | A 26 - 32 channel Chest coil should be used |
| High Performance Workstation | HP, Apple, or other Computer Hardware company | N/A | A computer with a minimum of 64 GB of Memory is needed for image reconstruction |
| Matlab | Mathworks | R2016A or newer | A Matlab license is needed to run the provided computer code |
| MRI Phantom | Siemens, GE, Philips, or Other MRI Phantom Vendor | N/A | Any Phantom can be used to test the MRI sequence prior to its use in human subjects. |
| MRI Scanner | Siemens, GE, Philips, or Other Clinical MRI Scanner Vendor | N/A | The protocol was developed on a 3T scanner, but 1.5T or 0.55T would also work with minimal adaptation |
参考文献
- Raju, S., Ghosh, S., Mehta, A. C. Chest ct signs in pulmonary disease: A pictorial review. Chest. 151 (6), 1356-1374 (2017).
- Biederer, J., et al. MRI of the lung (2/3). Why, when, how. Insights Imaging. 3 (4), 355-371 (2012).
- Biederer, J., et al. MRI of the lung (3/3)-current applications and future perspectives. Insights Imaging. 3 (4), 373-386 (2012).
- Johnson, K. M., Fain, S. B., Schiebler, M. L., Nagle, S. Optimized 3D ultrashort echo time pulmonary MRI. Magn Reson Med. 70 (5), 1241-1250 (2013).
- Ma, W., et al. Ultra-short echo-time pulmonary MRI: Evaluation and reproducibility in COPD subjects with and without bronchiectasis. J Magn Reson Imaging. 41 (5), 1465-1474 (2015).
- Roach, D. J., et al. Ultrashort echo-time magnetic resonance imaging is a sensitive method for the evaluation of early cystic fibrosis lung disease. Ann Am Thorac Soc. 13 (11), 1923-1931 (2016).
- Tibiletti, M., et al. Multistage three-dimensional UTE lung imaging by image-based self-gating. Magn Reson Med. 75 (3), 1324-1332 (2016).
- Weick, S., et al. Dc-gated high-resolution three-dimensional lung imaging during free-breathing. J Magn Reson Imaging. 37 (3), 727-732 (2013).
- Fischer, A., et al. Self-gated non-contrast-enhanced functional lung imaging (SENCEFUL) using a quasi-random fast low-angle shot (FLASH) sequence and proton MRI. NMR Biomed. 27 (8), 907-917 (2014).
- Tibiletti, M., et al. Respiratory self-gated 3D UTE for lung imaging in small animal MRI. Magn Reson Med. 78 (2), 739-745 (2017).
- Jiang, W., et al. Motion robust high resolution 3D free-breathing pulmonary MRI using dynamic 3D image self-navigator. Magn Reson Med. 79 (6), 2954-2967 (2018).
- Higano, N. S., et al. Retrospective respiratory self-gating and removal of bulk motion in pulmonary UTE MRI of neonates and adults. Magn Reson Med. 77 (3), 1284-1295 (2016).
- Metze, P., et al. Non-uniform self-gating in 2D lung imaging. Front Phys. 10, (2022).
- Gandhi, D. B., et al. Comparison of weighting algorithms to mitigate respiratory motion in free-breathing neonatal pulmonary radial UTE-MRI. Biomed Phys Eng Express. 10 (3), 035030 (2024).
- Fauveau, V., et al. Performance of spiral UTE-MRI of the lung in post-covid patients. Magn Reson Imaging. 96, 135-143 (2023).
- Metz, C., et al. Comparison of diagnostic quality of 3D ultrashort-echo-time techniques for pulmonary magnetic resonance imaging in free-breathing. Acta Radiologica. 64 (5), 1851-1858 (2023).
- Periaswamy, G., et al. Comparison of ultrashort TE lung MRI and HRCT lungs for detection of pulmonary nodules in oncology patients. Indian J Radiol Imaging. 32 (04), 497-504 (2022).
- Darçot, E., et al. Comparison between magnetic resonance imaging and computed tomography in the detection and volumetric assessment of lung nodules: A prospective study. Frontiers in Medicine. 9, 858731 (2022).
- Dournes, G., et al. 3D ultrashort echo time MRI of the lung using stack-of-spirals and spherical k-space coverages: Evaluation in healthy volunteers and parenchymal diseases. J Magn Reson Imaging. 48 (6), 1489-1497 (2018).
- Campbell-Washburn, A. E. 2019 American Thoracic Society Bear Cage winning proposal: Lung imaging using high-performance low-field magnetic resonance imaging. Am J Respir Crit Care Med. 201 (11), 1333-1336 (2020).
- Robison, R. K., Anderson, A. G., Pipe, J. G. Three-dimensional ultrashort echo-time imaging using a FLORET trajectory. Magn Reson Med. 78 (3), 1038-1049 (2017).
- Willmering, M. M., Robison, R. K., Wang, H., Pipe, J. G., Woods, J. C. Implementation of the FLORET sequence for lung imaging. Magn Reson Med. 82 (3), 1091-1100 (2019).
- Chan, R. W., Ramsay, E. A., Cunningham, C. H., Plewes, D. B. Temporal stability of adaptive 3D radial MRI using multidimensional golden means. Magn Reson Med. 61 (2), 354-363 (2009).
- Yu, J., Xue, Y., Song, H. K. Comparison of lung T2* during free-breathing at 1.5 T and 3.0 T with ultrashort echo time imaging. Magn Reson Med. 66 (1), 248-254 (2011).
- Otsu, N. A threshold selection method from gray-level histograms. IEEE Trans Syst Man Cybern. 9 (1), 62-66 (1979).
- Martin Uecker, F. O., et al. Berkely advanced reconstruction toolbox. Proc Intl Soc Magn Reson Med. 23, 2486 (2015).
- . . Bart Toolbox for Computational Magnetic Resonance Imaging. , (2024).
- Munidasa, S. . Treatment monitoring of pediatric cystic fibrosis lung disease using free breathing lung MRI. , (2024).
- Zhu, X., Chan, M., Lustig, M., Johnson, K. M., Larson, P. E. Z. Iterative motion-compensation reconstruction ultra-short TE (IMOCO UTE) for high-resolution free-breathing pulmonary MRI. Magn Reson Med. 83 (4), 1208-1221 (2020).
- Tan, F., et al. Motion-compensated low-rank reconstruction for simultaneous structural and functional UTE lung MRI. Magn Reson Med. 90 (3), 1101-1113 (2023).
- Bhattacharya, I., et al. Oxygen-enhanced functional lung imaging using a contemporary 0.55 T MRI system. NMR Biomed. 34 (8), e4562 (2021).
- Kim, M., et al. Feasibility of dynamic T2*-based oxygen-enhanced lung MRI at 3T. Magn Reson Med. 91 (3), 972-986 (2024).
- Klimeš, F., et al. 3D phase-resolved functional lung ventilation MR imaging in healthy volunteers and patients with chronic pulmonary disease. Magn Reson Med. 85 (2), 912-925 (2021).
转载和许可
请求许可使用此 JoVE 文章的文本或图形
请求许可探索更多文章
This article has been published
Video Coming Soon
版权所属 © 2025 MyJoVE 公司版权所有,本公司不涉及任何医疗业务和医疗服务。