Se requiere una suscripción a JoVE para ver este contenido. Inicie sesión o comience su prueba gratuita.
Method Article
Resonancia magnética estructural pulmonar con imágenes de tiempo de eco ultracorto autocompulsivo y de respiración libre
En este artículo
Resumen
Se describe un protocolo para generar imágenes estructurales de alta resolución de los pulmones mediante imágenes de resonancia magnética (RMN) de tiempo de eco ultracorto (UTE). Este protocolo permite adquirir imágenes utilizando una simple secuencia de pulso de resonancia magnética durante la respiración libre.
Resumen
La resonancia magnética de alta calidad de los pulmones se ve desafiada por la baja densidad de tejido, la rápida relajación de la señal de resonancia magnética y el movimiento respiratorio y cardíaco. Por estas razones, las imágenes estructurales de los pulmones se realizan casi exclusivamente mediante tomografía computarizada (TC). Sin embargo, las imágenes por TC liberan radiación ionizante y, por lo tanto, son menos adecuadas para ciertas poblaciones vulnerables (por ejemplo, pediatría) o para aplicaciones de investigación. Como alternativa, la resonancia magnética que utiliza tiempos de eco ultracortos (UTE) está atrayendo interés. Esta técnica se puede realizar durante la respiración libre en el transcurso de una exploración de ~5-10 minutos. La información de movimiento respiratorio se codifica junto con las imágenes; Esta información se puede utilizar para "auto-gatear" las imágenes. Por lo tanto, la autocompuerta elimina la necesidad de una programación avanzada de la secuencia de pulsos de resonancia magnética o el uso de fuelles respiratorios, lo que simplifica la adquisición de imágenes. En este protocolo, se presentan métodos de adquisición y reconstrucción simples, robustos y computacionalmente eficientes para adquirir resonancias magnéticas UTE de alta calidad de los pulmones. Este protocolo fue desarrollado para su uso en un escáner de resonancia magnética 3T, pero los mismos principios se pueden implementar a una intensidad de campo magnético más baja. El protocolo incluye ajustes de parámetros recomendados para la adquisición de imágenes UTE radiales en 3D, así como instrucciones para la reconstrucción de imágenes autocompuerta para generar imágenes en distintas fases respiratorias. A través de la implementación de este protocolo, los usuarios pueden generar imágenes UTE de alta resolución de los pulmones con artefactos de movimiento mínimos, mínimos o nulos. Estas imágenes se pueden usar para evaluar la estructura pulmonar, lo que se puede implementar para uso de investigación en una variedad de afecciones pulmonares.
Introducción
Las imágenes de alta resolución de la estructura pulmonar son una parte esencial de los estudios de diagnóstico para muchas afecciones pulmonares. Por lo general, esto se realiza mediante imágenes de tomografía computarizada (TC), que es ideal para generar imágenes de alta resoluciónde los pulmones. Sin embargo, la tomografía computarizada administra una dosis no trivial de radiación ionizante, por lo que no es adecuada para la repetición regular de imágenes, la obtención de imágenes en múltiples fases respiratorias diferentes o la obtención de imágenes de ciertas poblaciones (p. ej., pediatría). La resonancia magnética (RM) no conlleva el mismo riesgo que la radiación ionizante y, por lo tanto, es susceptible de tales tareas de imagen. Sin embargo, es difícil obtener imágenes de los pulmones mediante resonancia magnética debido a la baja densidad de tejidos, el movimiento respiratorio y cardíaco y la relajación muy rápida de la señal 2,3,4.
Una técnica de resonancia magnética que puede mitigar estos desafíos es la resonancia magnética de tiempo de eco ultracorto (UTE) 4,5,6. En la resonancia magnética UTE, la señal de resonancia magnética se muestrea inmediatamente después de la excitación de la señal, lo que reduce el impacto de la relajación rápida de la señal. Además, esta técnica muestrea el espacio k desde el centro hacia afuera, lo que conduce a un sobremuestreo significativo en el centro del espacio k. Este sobremuestreo en el centro del espacio k hace que esta técnica de imagen sea robusta al movimiento. Además de esta robustez inherente al movimiento, el muestreo repetido del centro del espacio k codifica información sobre el movimiento respiratorio, lo que permite la auto-compuerta de las imágenes 7,8,9. Esta autocompuerta se puede utilizar para generar imágenes en una variedad de fases respiratorias. Debido a que los seres humanos pasan la mayor parte de la fase respiratoria en la espiración, es común generar una imagen para el final de la espiración, ya que esta fase tiene la mayor cantidad de datos de imagen adquiridos.
Existe una variedad de estrategias para la autoactivación respiratoria en la resonancia magnética pulmonar. La primera distinción que hay que hacer es la basada en imágenes frente a la compuerta basada en el espaciok 10 (Figura 1). En la compuerta basada en imágenes, se genera un conjunto de imágenes con alta resolución temporal mediante la reconstrucción de pequeños subconjuntos temporales de los datos de imagen. Posteriormente, la posición del diafragma en estas imágenes se utiliza para identificar la fase respiratoria para un conjunto dado de proyecciones de imágenes10,11. En la compuerta basada en el espacio k, se examinan los datos del centro del espacio k ("k0") 8,9,12. La intensidad de la señal de la imagen se codifica en k0 y, por lo tanto, la intensidad del punto k0 varía con la respiración. Por lo tanto, las proyecciones se pueden agrupar en diferentes fases respiratorias en función de la intensidad de k0. Tanto en las compuertas basadas en imágenes como en las basadas en el espacio k, las proyecciones con fases respiratorias similares se agrupan para la reconstrucción de imágenes. Se ha sugerido que la compuerta basada en imágenes proporciona una mayor fidelidad en la estimación de la fase respiratoria, proporcionando así imágenes con un desenfoque reducido10,13.
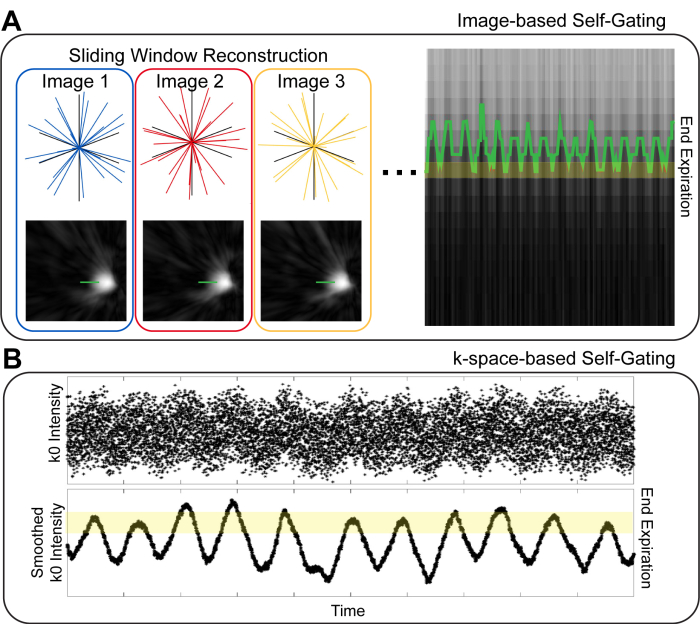
Figura 1: Técnicas de autocompuerta basadas en imágenes y en el espacio k. (A) En las compuertas basadas en imágenes, las imágenes de baja resolución espacial y alta resolución temporal que muestran el diafragma se generan a partir de subconjuntos temporales de los datos generales. Usando una línea sobre el diafragma, el movimiento respiratorio se puede visualizar y agrupar para la reconstrucción de imágenes. (B) En la compuerta basada en el espacio k, el primer punto en una proyección de espacio k centrada hacia afuera ("k0") se utiliza para visualizar el movimiento respiratorio. Después de suavizar k0, las diferencias de intensidad de la señal basadas en el ciclo respiratorio son claramente visibles y se pueden utilizar para identificar diferentes fases respiratorias. Haga clic aquí para ver una versión más grande de esta figura.
Tanto la compuerta basada en imagen como la basada en el espacio k se pueden realizar utilizando compuerta dura o compuerta suave11,14. En la compuerta dura, solo se reconstruyen las proyecciones correspondientes a la fase respiratoria deseada. Sin embargo, este descarte de proyecciones no deseadas puede conducir a una reducción de la relación señal-ruido (SNR) de la imagen y a un aumento de los artefactos de submuestreo. Estos efectos no deseados se pueden mitigar mediante el uso de compuertas suaves. En la compuerta suave, todas las proyecciones se utilizan para la reconstrucción de la imagen, pero las proyecciones de una fase respiratoria no deseada se ponderan de tal manera que tienen un menor impacto en la imagen final. Al hacerlo, las imágenes se pueden reconstruir con artefactos mínimos y una alta SNR, al tiempo que se suprime el impacto del movimiento respiratorio.
A través de la combinación de la adquisición de resonancia magnética UTE con la autoactivación posterior a la adquisición, se pueden generar imágenes de alta calidad que, si bien no son equivalentes a la TC, tienen un contraste y una resolución que se acercan a los de las imágenes de TC 6,15,16,17,18,19. En este artículo, se proporciona un protocolo simple para recopilar y reconstruir imágenes de resonancia magnética de UTE para generar imágenes de alta calidad de la estructura pulmonar.
Este protocolo está escrito principalmente para escáneres de resonancia magnética 3T; 3T es la intensidad de campo más común utilizada para la resonancia magnética de investigación. Las intensidades de campo magnético más bajas, como 1,5T o el recientemente disponible 0,55 T20 , pueden proporcionar una mejor calidad de imagen e intensidad de señal dentro de los pulmones, ya que la relajación de la señal dentro de los pulmones es más lenta a estas intensidades de campo.
Si bien se ha hecho todo lo posible para proporcionar claridad y simplicidad en este protocolo y el código de reconstrucción de imágenes proporcionado, es probable que el protocolo requiera un físico de resonancia magnética dedicado (o un experto en resonancia magnética similar) para establecer una secuencia de resonancia magnética UTE adecuada en el escáner de resonancia magnética. La secuencia de resonancia magnética debe implementar una estrategia de codificación 3D no cartesiana con trayectorias de espacio k centradas. Algunos ejemplos son las secuencias de imágenes radiales 3D o espirales 3D (p. ej., "FLORET")21,22. Es importante destacar que el orden de las proyecciones debe tener una buena estabilidad temporal: durante cualquier subconjunto de tiempo dado, las proyecciones deben cubrir todo el rango del espaciok 23. Ejemplos de estrategias de ordenación de proyecciones con buena estabilidad temporal son las medias áureas o la espiral de Arquímedes aleatorizada de Halton. Si se utiliza un orden de proyección con poca estabilidad temporal, la autocompuerta posterior a la adquisición omitirá grandes regiones del espacio k, lo que dará lugar a artefactos de la imagen. Por último, la secuencia debe ser capaz de alcanzar un tiempo de eco (TE) de <100 μs. El tiempo de relajación de T2* en los pulmones a 3T es de <1 ms24, por lo que el uso de un TE muy corto es esencial para generar imágenes de alta calidad.
Protocolo
Todas las imágenes de sujetos humanos se realizaron con la aprobación del KUMC IRB. Se obtuvo el consentimiento informado por escrito de todos los participantes. Las imágenes de este estudio se obtuvieron bajo un protocolo genérico de desarrollo técnico, y los criterios de inclusión/exclusión fueron deliberadamente amplios. Criterios de inclusión: Edad ≥ 18 años. Criterios de exclusión: Resonancia magnética contraindicada en función de las respuestas al cuestionario de cribado de resonancia magnética y embarazo. Los accesorios y el equipo utilizado para este estudio se enumeran en la Tabla de Materiales.
1. Adquisición de imágenes UTE
- Preparar la secuencia de imágenes. Prepare la secuencia de imágenes una vez y use esta misma secuencia para todos los participantes.
- Establezca los parámetros de acuerdo con la Tabla 1.
- Coloque un maniquí de resonancia magnética en el centro de la resonancia magnética y ejecute la secuencia de imágenes.
NOTA: Debido a que esta secuencia requiere un rendimiento de gradiente rápido y muchos pulsos de RF, es importante verificar que la configuración del protocolo se pueda ejecutar antes de la prueba en un ser humano.
- Prepare al participante para la resonancia magnética. Utilice la evaluación de seguridad de la resonancia magnética estándar institucional para garantizar que el participante pueda ingresar a la resonancia magnética de manera segura.
- Coloque al participante en la cama de resonancia magnética y coloque una bobina en el pecho sobre el torso del participante. Coloque la bobina cerca de la barbilla del participante para asegurar una cobertura total de los ápices pulmonares.
- Mueva al participante al escáner de resonancia magnética. Coloque el punto de referencia de posición justo debajo del esternón del participante.
- Recopile una exploración con localizador para asegurarse de que los pulmones del participante estén dentro del campo de visión para la exploración UTE. No mueva la geometría del escaneo UTE. Si los pulmones del participante no están dentro del campo de visión, mueva al participante y recoja exploraciones localizadoras adicionales hasta que los pulmones estén completamente dentro del campo de visión.
- Ejecute la secuencia UTE. Durante esta secuencia, el participante puede respirar normalmente.
- Exporte los datos sin procesar del escáner. Dependiendo de la secuencia de imágenes utilizada, el escáner puede o no reconstruir imágenes en el escáner. Para la reconstrucción retrospectiva de compuerta propuesta, se requieren datos de imágenes sin procesar para determinar si se generan o no imágenes en el escáner. Nota: los datos sin procesar serán grandes (>10 GB).
- Exporte o calcule trayectorias de k-space (es decir, la ubicación en k-space de cada punto de datos sin procesar).
NOTA: Para algunas secuencias de imágenes, las trayectorias del espacio k pueden almacenarse junto con los datos sin procesar en el escáner de resonancia magnética y se pueden exportar directamente. Para otras secuencias de imágenes, las trayectorias del espacio k deberán calcularse en función de los parámetros de imagen.
| Parámetro | Configuración genérica recomendada | Ajustes implementados en este documento |
| Secuencia de imágenes | 3D no cartesiano con trayectorias de espacio k centrado hacia afuera | Radial 3D con Oro Significa Proyección Ordenamiento |
| Campo de visión | 400 x 400 x 400 mm3 | 400 x 400 x 400 mm3 |
| Tamaño de la matriz | Según se desee para la resolución de destino | 320 x 320 x 320 (resolución isotrópica de 1,25 mm) |
| Ancho de banda | Según sea necesario para una duración de lectura < 1,0 ms | 888 Hz/píxel |
| TE | < 0,1 ms | 0,07 ms |
| TR | Mínimo (Objetivo 3 – 4 ms) | 3,5 ms |
| Ángulo de volteo | Aproximadamente 5° | 4.8° |
| Número de proyecciones | Mínimo 100.000 | 1,35,386 |
| Duración de la imagen | Mínimo 5 min | 7 min, 54 s |
Tabla 1: Ajustes recomendados para la obtención de imágenes UTE. Se proporcionan configuraciones genéricas recomendadas que se pueden usar para guiar la configuración del protocolo. También se proporcionan las configuraciones recomendadas específicas que se usaron para los datos, como se muestra como resultados representativos. Las especificaciones de los parámetros son genéricas en todos los proveedores, excepto en el ancho de banda. Algunos de los principales proveedores de resonancia magnética especifican el ancho de banda como Hz/píxel. Otros proveedores importantes de resonancias magnéticas especifican el ancho de banda absoluto. El ancho de banda recomendado (888 Hz/píxel) corresponde a un ancho de banda absoluto de 284.160 Hz.
2. Reconstrucción de imágenes UTE mediante compuerta respiratoria basada en imágenes
NOTA: El código de MATLAB para completar los siguientes pasos se proporciona en https://github.com/pniedbalski3/UTE_Reconstruction.
- Importe datos y trayectorias de espacio k en MATLAB. El código para importar datos brutos de resonancia magnética está disponible para todos los principales proveedores de resonancia magnética.
- Descarte las primeras 1000 proyecciones para asegurarse de que los datos estén en magnetización de estado estacionario.
NOTA: Si la secuencia de imágenes utilizada incluye exploraciones ficticias antes de la adquisición de datos, se puede omitir este paso. - Reconstruya una imagen de baja resolución utilizando un subconjunto muy pequeño de datos.
- Reconstruya la imagen utilizando una transformada rápida de Fourier no uniforme a un tamaño de matriz de 96 x 96 x 96.
- Utilice aproximadamente 200 proyecciones, correspondientes a datos de 0,6 s a 0,8 s.
- Reconstruya y almacene imágenes de todos los elementos de la bobina, así como una imagen final combinada de la bobina.
- En la imagen resultante combinada con bobinas, seleccione un corte coronal que muestre claramente el diafragma.
NOTA: El código proporcionado solicitará al usuario que seleccione una porción que contenga el diafragma. - Una vez que se haya seleccionado este corte, vea las imágenes de bobina individuales para este corte y seleccione uno o dos elementos de bobina que mejor muestren el diafragma (Figura 2).
NOTA: El código proporcionado solicitará al usuario que seleccione los elementos de la bobina. - Reconstruya las imágenes utilizando una ventana deslizante para generar imágenes con una resolución temporal de ~0,5 s (Figura 2).
- Reconstruya solo los datos de los elementos de la bobina seleccionados en el paso 2.4.
NOTA: Si bien todos los elementos de la bobina se pueden reconstruir, solo se necesitan los elementos más cercanos al diafragma para visualizar el diafragma con el fin de autocompuerta respiratorio. Al reconstruir solo los elementos de la bobina más cercanos al diagrama, el tiempo de reconstrucción y la carga computacional se reducen drásticamente. - Utilice las primeras 200 proyecciones para reconstruir una imagen utilizando una transformada rápida de Fourier no uniforme (Figura 2). Guarde solo el corte que muestra el diafragma (como se encuentra en el paso 2.4).
NOTA: En última instancia, se generarán hasta 1500 imágenes; solo se necesita un corte 2D para visualizar la posición del diafragma, y el almacenamiento de imágenes 3D para cada uno de los pasos de la ventana deslizante sería prohibitivo. - Desplazamiento en 100 proyecciones (es decir, la primera imagen se reconstruye utilizando las proyecciones 1-200. La segunda se reconstruye utilizando las proyecciones 101 - 300) y se reconstruye una imagen adicional, almacenando el corte seleccionado en el paso 2.4.
- Continúe hasta que se hayan utilizado todas las proyecciones para generar imágenes.
- Reconstruya solo los datos de los elementos de la bobina seleccionados en el paso 2.4.
- Seleccione una línea sobre el diafragma en la primera de las imágenes de la ventana deslizante. Asegúrese de que la línea sea lo suficientemente larga como para extenderse hacia los pulmones en 5-10 vóxeles y en el diafragma en 5-10 vóxeles.
- Visualice el movimiento respiratorio visualizando este navegador respiratorio para todas las proyecciones.
- Determine la ubicación del diafragma para todos los navegadores respiratorios. Hay una variedad de formas de hacer esto, pero un método sencillo es usar el método25 de Otsu para dividir el lado más oscuro (pulmón) del lado más brillante (diafragma).
- Utilice la ubicación del diafragma para etiquetar las proyecciones como pertenecientes a un compartimento respiratorio determinado. Si un navegador respiratorio determinado muestra el diafragma en la "posición 1", entonces las 200 proyecciones utilizadas para generar la imagen para ese navegador pertenecerían al "contenedor 1".
NOTA: Debido a que las imágenes se generaron utilizando una ventana deslizante con una superposición de 100 proyecciones, algunas proyecciones pueden etiquetarse como pertenecientes a varios bins. La resolución espacial aproximada de las imágenes de las ventanas correderas conduce a un total de ~ 4-6 contenedores que cubren toda la gama de inspiración hasta la caducidad. - Seleccione la ubicación que desea reconstruir determinando qué ubicación tiene el mayor número de proyecciones, que deben corresponder a la expiración final.
- Alternativamente, reconstruya las imágenes de las fases respiratorias deseadas basándose en la inspección visual del navegador respiratorio.
- Genere pesos para compuertas blandas14.
- Utilice un filtro exponencial para proporcionar un peso de 1 a las proyecciones dentro del intervalo primario y un peso drásticamente reducido a las proyecciones dentro de diferentes compartimentos respiratorios.
- Utilice la caja de herramientas de reconstrucción avanzada de Berkely (BART; https://mrirecon.github.io/bart/)26,27 para reconstruir una imagen de alta resolución en el compartimento respiratorio deseado.
NOTA: BART es una caja de herramientas disponible gratuitamente para la reconstrucción de imágenes de resonancia magnética.- Calcule los pesos de compensación de densidad mediante una combinación de densidad iterativa.
- Escale los pesos de compensación de densidad por los pesos de compuerta suave.
- Escala de datos basada en la compensación de densidad y los pesos de compuerta suave
- Realice una transformada rápida de Fourier (NUFFT) básica no uniforme para facilitar la combinación de bobinas.
- Convierta la imagen NUFFT en un espacio k cuadriculado que se utilizará para la combinación de bobinas.
- Genere una matriz de combinación de bobinas y utilícela para combinar bobinas tanto para los datos sin procesar como para el espacio k cuadriculado.
- Estimar las sensibilidades de las bobinas.
- Realice la reconstrucción de sensores comprimidos de imágenes paralelas utilizando la compensación de densidad ponderada, los datos combinados de la bobina y los mapas de sensibilidad de la bobina.
- Guarde la imagen final. El formato NIFTI es fácil de implementar. Si la imagen se va a cargar en un sistema PAC, es posible que se requiera un formato DICOM.
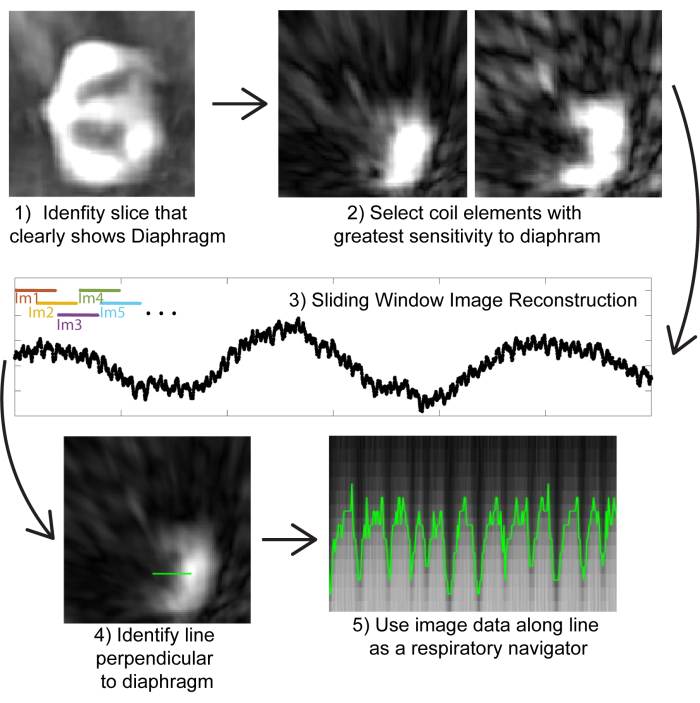
Figura 2: Autoactivación basada en imágenes. (1) Usando una imagen de baja resolución reconstruida a partir de un pequeño número de proyecciones (para eficiencia computacional), identifique un corte coronal que muestre claramente el diafragma. (2) Al examinar las imágenes de los elementos individuales de la bobina, seleccione los elementos de la bobina que estén más cerca del diafragma. (3) Realizar una reconstrucción de ventana deslizante solo de los elementos de la bobina más cercanos al diafragma (para eficiencia computacional). Las imágenes se pueden generar a partir de subconjuntos de 200 proyecciones (correspondientes a ~0,8 s); Mediante la superposición de proyecciones, se puede lograr una resolución pseudotemporal de ~0,5 s en las imágenes. (4) Identificar una línea que sea perpendicular al diafragma para ser utilizada como navegador respiratorio. (5) La visualización de los datos de la imagen en esta línea muestra el movimiento respiratorio, que se puede utilizar para agrupar imágenes. Haga clic aquí para ver una versión más grande de esta figura.
3. Reconstrucción de imágenes de UTE mediante conexión blanda respiratoria basada en k-space
- Complete los pasos 2.1-2.4 para que se pueda identificar el elemento de la bobina más cercano al diafragma.
- Genere una traza de serie temporal k0 utilizando el valor absoluto del primer punto de la proyección para todas las proyecciones del elemento de bobina seleccionado. Esto proporcionará una visualización de una forma de onda respiratoria.
- En pasos de 5000 proyecciones, normalice k0 por la intensidad media de la señal de esos mismos k0 puntos28. Esto mitiga la deriva de la intensidad de la señal a lo largo del tiempo y proporciona una capacidad mejorada para agrupar cuantitativamente las proyecciones.
- Etiqueta cada puntok 0 como si ocurriera durante la inspiración o la espiración.
- Suaviza la serie temporal k0 y toma la derivada para evaluar la pendiente de cada punto de la traza de compuerta.
- Etiquete los puntos de inspiración en función del signo de la pendiente. Una pendiente positiva corresponde a la espiración, mientras que una pendiente negativa corresponde a la inspiración.
- Proyecciones de bin basadas en la intensidad de la señal. Debido a que la profundidad de la respiración puede ser variable, las proyecciones de los compartimentos se basan en la amplitud de la señal y no en la ubicación en la fase respiratoria.
NOTA: Un método simple y rápido para lograr esto es implementar la agrupación de k-medias para identificar diferentes niveles de intensidad de señal. - En el caso de los bins intermedios entre el final de la inspiración y el final de la caducidad, identifique las proyecciones como si se produjeran durante la inspiración y la caducidad en función del paso 3.4.
- Reconstrucción completa de la imagen siguiendo los pasos proporcionados en los pasos 2.10 a 2.13.
- Si lo desea, reconstruya las imágenes de todos los compartimentos respiratorios en lugar de solo al final de la expiración.
Resultados
Los resultados representativos (Figura 3) se generaron utilizando la configuración que se muestra en la Tabla 1. La duración de las imágenes utilizadas proporciona imágenes de alta calidad que son tolerables por la mayoría de los participantes.
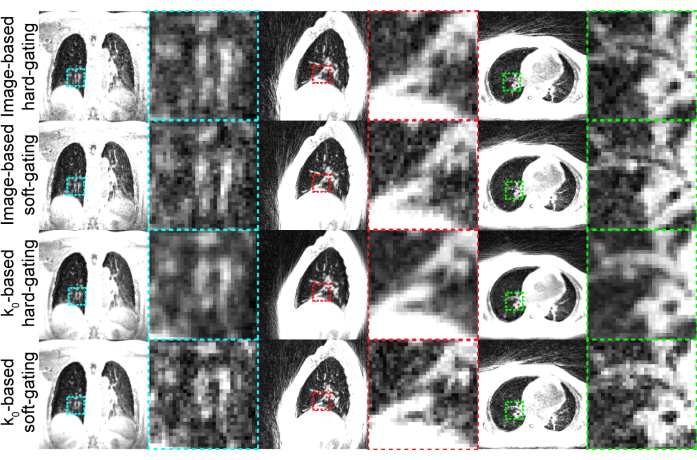
Figura 3<...
Discusión
Al realizar imágenes UTE de los pulmones, se pueden utilizar muchas variaciones tanto de adquisición como de reconstrucción para generar imágenes de los pulmones. Este protocolo se centra en la facilidad de implementación y la eficiencia computacional. La obtención de imágenes mediante UTE radial 3D es relativamente sencilla, con secuencias de imágenes generalmente disponibles en los principales proveedores de resonancia magnética. Se proporcionan herramientas basadas en MATLAB ...
Divulgaciones
Peter Niedbalski recibe fondos de investigación de la Fundación Nacional de Esclerodermia, la Asociación Americana del Corazón y los NIH. Es consultor de Polarean Imaging Plc., una empresa que desarrolla la tecnología de resonancia magnética hiperpolarizada 129Xe.
Agradecimientos
El desarrollo de este protocolo y las imágenes mostradas como resultados representativos fueron apoyados por la Fundación Nacional de Esclerodermia.
Materiales
| Name | Company | Catalog Number | Comments |
| Chest MRI Coil | Siemens, GE, Philips,, Other Clinical MRI Imaging Coil Vendor | N/A | A 26 - 32 channel Chest coil should be used |
| High Performance Workstation | HP, Apple, or other Computer Hardware company | N/A | A computer with a minimum of 64 GB of Memory is needed for image reconstruction |
| Matlab | Mathworks | R2016A or newer | A Matlab license is needed to run the provided computer code |
| MRI Phantom | Siemens, GE, Philips, or Other MRI Phantom Vendor | N/A | Any Phantom can be used to test the MRI sequence prior to its use in human subjects. |
| MRI Scanner | Siemens, GE, Philips, or Other Clinical MRI Scanner Vendor | N/A | The protocol was developed on a 3T scanner, but 1.5T or 0.55T would also work with minimal adaptation |
Referencias
- Raju, S., Ghosh, S., Mehta, A. C. Chest ct signs in pulmonary disease: A pictorial review. Chest. 151 (6), 1356-1374 (2017).
- Biederer, J., et al. MRI of the lung (2/3). Why, when, how. Insights Imaging. 3 (4), 355-371 (2012).
- Biederer, J., et al. MRI of the lung (3/3)-current applications and future perspectives. Insights Imaging. 3 (4), 373-386 (2012).
- Johnson, K. M., Fain, S. B., Schiebler, M. L., Nagle, S. Optimized 3D ultrashort echo time pulmonary MRI. Magn Reson Med. 70 (5), 1241-1250 (2013).
- Ma, W., et al. Ultra-short echo-time pulmonary MRI: Evaluation and reproducibility in COPD subjects with and without bronchiectasis. J Magn Reson Imaging. 41 (5), 1465-1474 (2015).
- Roach, D. J., et al. Ultrashort echo-time magnetic resonance imaging is a sensitive method for the evaluation of early cystic fibrosis lung disease. Ann Am Thorac Soc. 13 (11), 1923-1931 (2016).
- Tibiletti, M., et al. Multistage three-dimensional UTE lung imaging by image-based self-gating. Magn Reson Med. 75 (3), 1324-1332 (2016).
- Weick, S., et al. Dc-gated high-resolution three-dimensional lung imaging during free-breathing. J Magn Reson Imaging. 37 (3), 727-732 (2013).
- Fischer, A., et al. Self-gated non-contrast-enhanced functional lung imaging (SENCEFUL) using a quasi-random fast low-angle shot (FLASH) sequence and proton MRI. NMR Biomed. 27 (8), 907-917 (2014).
- Tibiletti, M., et al. Respiratory self-gated 3D UTE for lung imaging in small animal MRI. Magn Reson Med. 78 (2), 739-745 (2017).
- Jiang, W., et al. Motion robust high resolution 3D free-breathing pulmonary MRI using dynamic 3D image self-navigator. Magn Reson Med. 79 (6), 2954-2967 (2018).
- Higano, N. S., et al. Retrospective respiratory self-gating and removal of bulk motion in pulmonary UTE MRI of neonates and adults. Magn Reson Med. 77 (3), 1284-1295 (2016).
- Metze, P., et al. Non-uniform self-gating in 2D lung imaging. Front Phys. 10, (2022).
- Gandhi, D. B., et al. Comparison of weighting algorithms to mitigate respiratory motion in free-breathing neonatal pulmonary radial UTE-MRI. Biomed Phys Eng Express. 10 (3), 035030 (2024).
- Fauveau, V., et al. Performance of spiral UTE-MRI of the lung in post-covid patients. Magn Reson Imaging. 96, 135-143 (2023).
- Metz, C., et al. Comparison of diagnostic quality of 3D ultrashort-echo-time techniques for pulmonary magnetic resonance imaging in free-breathing. Acta Radiologica. 64 (5), 1851-1858 (2023).
- Periaswamy, G., et al. Comparison of ultrashort TE lung MRI and HRCT lungs for detection of pulmonary nodules in oncology patients. Indian J Radiol Imaging. 32 (04), 497-504 (2022).
- Darçot, E., et al. Comparison between magnetic resonance imaging and computed tomography in the detection and volumetric assessment of lung nodules: A prospective study. Frontiers in Medicine. 9, 858731 (2022).
- Dournes, G., et al. 3D ultrashort echo time MRI of the lung using stack-of-spirals and spherical k-space coverages: Evaluation in healthy volunteers and parenchymal diseases. J Magn Reson Imaging. 48 (6), 1489-1497 (2018).
- Campbell-Washburn, A. E. 2019 American Thoracic Society Bear Cage winning proposal: Lung imaging using high-performance low-field magnetic resonance imaging. Am J Respir Crit Care Med. 201 (11), 1333-1336 (2020).
- Robison, R. K., Anderson, A. G., Pipe, J. G. Three-dimensional ultrashort echo-time imaging using a FLORET trajectory. Magn Reson Med. 78 (3), 1038-1049 (2017).
- Willmering, M. M., Robison, R. K., Wang, H., Pipe, J. G., Woods, J. C. Implementation of the FLORET sequence for lung imaging. Magn Reson Med. 82 (3), 1091-1100 (2019).
- Chan, R. W., Ramsay, E. A., Cunningham, C. H., Plewes, D. B. Temporal stability of adaptive 3D radial MRI using multidimensional golden means. Magn Reson Med. 61 (2), 354-363 (2009).
- Yu, J., Xue, Y., Song, H. K. Comparison of lung T2* during free-breathing at 1.5 T and 3.0 T with ultrashort echo time imaging. Magn Reson Med. 66 (1), 248-254 (2011).
- Otsu, N. A threshold selection method from gray-level histograms. IEEE Trans Syst Man Cybern. 9 (1), 62-66 (1979).
- Martin Uecker, F. O., et al. Berkely advanced reconstruction toolbox. Proc Intl Soc Magn Reson Med. 23, 2486 (2015).
- . . Bart Toolbox for Computational Magnetic Resonance Imaging. , (2024).
- Munidasa, S. . Treatment monitoring of pediatric cystic fibrosis lung disease using free breathing lung MRI. , (2024).
- Zhu, X., Chan, M., Lustig, M., Johnson, K. M., Larson, P. E. Z. Iterative motion-compensation reconstruction ultra-short TE (IMOCO UTE) for high-resolution free-breathing pulmonary MRI. Magn Reson Med. 83 (4), 1208-1221 (2020).
- Tan, F., et al. Motion-compensated low-rank reconstruction for simultaneous structural and functional UTE lung MRI. Magn Reson Med. 90 (3), 1101-1113 (2023).
- Bhattacharya, I., et al. Oxygen-enhanced functional lung imaging using a contemporary 0.55 T MRI system. NMR Biomed. 34 (8), e4562 (2021).
- Kim, M., et al. Feasibility of dynamic T2*-based oxygen-enhanced lung MRI at 3T. Magn Reson Med. 91 (3), 972-986 (2024).
- Klimeš, F., et al. 3D phase-resolved functional lung ventilation MR imaging in healthy volunteers and patients with chronic pulmonary disease. Magn Reson Med. 85 (2), 912-925 (2021).
Reimpresiones y Permisos
Solicitar permiso para reutilizar el texto o las figuras de este JoVE artículos
Solicitar permisoExplorar más artículos
This article has been published
Video Coming Soon
ACERCA DE JoVE
Copyright © 2025 MyJoVE Corporation. Todos los derechos reservados