Method Article
Etablierung stabiler binärer Kulturen symbiotischer Saccharibakterien aus der Mundhöhle
* Diese Autoren haben gleichermaßen beigetragen
In diesem Artikel
Zusammenfassung
Wir demonstrieren eine Methode zur Isolierung schwer zu züchtender Mitglieder des neuartigen Bakterienstamms Saccharibacteria durch Filterung von Zahnbelag und Co-Kultivierung mit Wirtsbakterien.
Zusammenfassung
Viele Bakterienarten können nicht im Labor mit Standardmethoden kultiviert werden, was eine erhebliche Barriere für die Untersuchung des Großteils der mikrobiellen Vielfalt auf der Erde darstellt. Neuartige Ansätze sind erforderlich, um diese unkultivierten Bakterien zu kulturieren, damit die Forscher ihre Physiologie und ihren Lebensstil mit den im Labor verfügbaren leistungsstarken Werkzeugen effektiv untersuchen können. Die Candidate Phyla Radiation (CPR) ist eine der größten Gruppen von unkultivierten Bakterien und umfasst ~ 15% der lebenden Vielfalt auf der Erde. Das erste Isolat dieser Gruppe war ein Mitglied des Saccharibacteria-Stammes, desNanosynbacter lyticus-StammesTM7x. TM7x ist ein ungewöhnlich kleines Bakterium, das als Symbiont in direktem Kontakt mit einem bakteriellen Wirt, Schaalia odontolytica, Stamm XH001, lebt. Unter Ausnutzung der ungewöhnlich kleinen Zellgröße und ihres Lebensstils als symbiotischer Organismus entwickelten wir ein Protokoll, um Saccharibakterien schnell aus Zahnbelag zu züchten. Dieses Protokoll wird zeigen, wie man eine Suspension von Zahnbelag durch einen 0,2 μm-Filter filtert, dann die gesammelten Saccharibakterienzellen konzentriert und eine Kultur von Wirtsorganismen infiziert. Die resultierende Kokultur kann als jede normale Bakterienkultur durchfahren werden und die Infektion wird durch PCR bestätigt. Die resultierende binäre Kultur kann im Labor gepflegt und für zukünftige Experimente verwendet werden. Während eine Kontamination eine Möglichkeit ist, kann die binäre Kultur entweder durch weitere Filterung und Reinfektion des Wirts oder durch Beschichtung der binären Kultur und Screening auf infizierte Kolonien gereinigt werden. Wir hoffen, dass dieses Protokoll auf andere Probentypen und Umgebungen ausgeweitet werden kann, was zum Anbau vieler weiterer Arten in der CPR führt.
Einleitung
Die Kultivierung neuartiger Bakterienarten und ihre Einspessung ins Labor ermöglicht leistungsstarke Experimente, um ihre Physiologie und breitere Interaktionen innerhalb ihrer mikrobiellen Gemeinschaft besser zu verstehen. Während es kulturfreie Methoden gibt, diese Fragen zu hinterfragen (z.B. "Meta-Omics"), machen es die komplexen Interaktionen verschiedener mikrobieller Populationen schwierig, einzelne Variablen auseinander zu reißen und sinnvolle Schlussfolgerungen zu ziehen. Während die Kultivierung von Bakterien viele Vorteile hat, gibt es viele potenzielle Barrieren, um ein Bakterium zu isolieren und es in reiner Kultur anzubauen. Zu den potenziellen spezifischen Wachstumsanforderungen gehören pH-Wert, Sauerstoffspannung, Vitamine, Wachstumsfaktoren, Signalmoleküle oder sogar direkter Zellkontakt, um Wachstum hervorzubelocken1. Es wird jedoch angenommen, dass bestimmte Auxotrophien die primäre Abschreckung für die Kultivierung neuer Bakterienarten sind. Standard-Medienformulierungen fehlen viele Nährstoffe, die von unkultivierten Bakterien benötigt werden, wie z. B. bestimmte Vitamine oder Kohlenstoffquellen. Diese fehlenden Moleküle können der Schlüssel zur Physiologie der nicht kulturierten Bakterien sein und werden normalerweise entweder von einem anderen Organismus in der mikrobiellen Gemeinschaft oder einem Wirtsorganismus bereitgestellt. Zum Beispiel können komplexe Kohlenhydrate wie Mucin von tierischen Wirten bereitgestellt werden. Die Zugabe dieser bakterien zu den medien ermöglicht die Kultivierung mehrerer Bakterien aus tierischen Eingeweiden, darunter Akkermansia muciniphila und Mucinivorans hirudinis2,3,4. Viele pathogene Bakterien haben die Fähigkeit entwickelt, an Hämin gebundenes Eisen in tierischen Zellen zu verwenden, einschließlich des oralen Erregers Porphyromonas gingivalis5. Im Labor kann das Wachstum von Porphyromonas und anderen Organismen durch die Zugabe von Hemin6stimuliert werden.
In jüngster Zeit sind viele Durchbrüche bei der Kultivierung neuartiger Bakterienisolate durch Co-Culturing erzielt wurden, bei der ein "Feeder" -Organismus verwendet wurde, um unkultivierten Bakterien spezifische Faktoren zur Verfügung zu stellen, die für ihr Wachstum notwendig sind. Eine elegante Studie von Vartoukian und Kollegen zeigte, dass Siderophore, eisenbindende Moleküle, die von Bakterien produziert werden, das Wachstum mehrerer neuartiger oraler Isolate stimulierten. Es wurde gezeigt, dass Pyoverdine, eine Art Siderophor, das von Pseudomonadenarten produziertwird, das Wachstum einer neuartigen Prevotella-Art signifikant erleichtern7. In der gleichen Studie wurde das erste orale Isolat für den Stamm Chloroflexi kultiviert, wobei auch F. nucleatum als Helfer für die Bereitstellung einiger noch unbekannterVerbindungen 7verwendet wurde. In jüngerer Zeit wurde ein Bakterium aus der Gattung Ruminococcaceae mit Bacteroides fragilis als Helferorganismus isoliert8. Später zeigte sich, dass Gamma-Aminobuttersäure (GABA), ein hemmender Neurotransmitter, für das Wachstum auf Labormedien benötigt wurde. Die Verwendung von Feeder-Organismen hat sich als Schlüsselstrategie erwiesen, um bestimmte Mikroumgebungen nachzuahmen, in denen nicht kulturierte Bakterien wachsen, und ist effizienter als die kontinuierliche Neuformulierung von Wachstumsmedien mit verschiedenen Additiven in unterschiedlichen Konzentrationen.
Eine der größten Gruppen unkultivierter Bakterien besteht in der "Candidate Phyla Radiation" (CPR), einer monophyletischen Gruppe aus mehreren Kandidaten-Bakterienphyla9,10. Zum Zeitpunkt dieses Schreibens wurden nur Mitglieder des Saccharibakterien-Stammes innerhalb der CPR erfolgreich im Labor kultiviert. Das erste Isolat, derNanosynbacter lyticus-Stamm TM7x, wurde mit dem Antibiotikum Streptomycin isoliert, das sich für das unkultivierte TM711,12anreichern sollte. Eine Schlüsselentdeckung dieser Arbeit war, dass das neue Isolat als Parasit wuchs, der in direktem Kontakt mit einem bakteriellen Wirt, Schaalia odontolytica,wuchs, und die Mikroskopie zeigte, dass diese Parasiten ultrakleine Bakterien waren.
Unter Verwendung dieser Hinweise entwickelten wir eine Methode, um schnell binäre Kokulturen von Saccharibakterien mit ihren Partnern zu etablieren, indem wir Zahnbelag und andere orale Proben durch einen 0,2 μm-Filter filterten, Zellen im Filtrat durch Zentrifugation sammelten und sie verwendeten, um Kulturen von Kandidaten-Wirtsbakterien zu infizieren. Diese Methode hat den Vorteil, Anreicherungskulturen zu vermeiden, die mit schnell wachsenden Organismen überfordert sein können. Es vermeidet auch den Einsatz von Antibiotika, die das Wachstum entweder der anvisierten Saccharibakterien-Arten oder ihrer Wirte stoppen könnten. Mit der hier demonstrierten Methode haben wir erfolgreich 32 Isolate aus dem Stamm der Saccharibakterien kultiviert.
Protokoll
Bei der Entwicklung dieses Protokolls wurde die IRB-Genehmigung eingeholt und genehmigt (#14-10) und die Einwilligung aller Probanden nach Aufklärung eingeholt.
1. Vorbereitung
- Wenn Sie mit menschlichen Probanden arbeiten, holen Sie die erforderliche IRB-Genehmigung und die Einwilligung nach Aufklärung ein.
- Beginnen Sie Kulturen von Wirtsbakterien mit genügend Zeit, um in die frühe stationäre Phase zu wachsen. Zum Beispiel 2-5 ml tryptische Sojabrühe mit 0,1% Hefeextrakt (TSBY) mit Arachnia propionica impfen und bei 37 °C für 24 h inkubieren.
- Montieren Sie Filterhalter mit nachgeätzter 0,2 μm Filtermembran. Verpacken Sie die Baugruppe in Folie und sterilisieren Sie sie durch Autoklavieren.
- Zentrifugenröhrchen und Kappenbaugruppen sterilisieren.
2. Entnehmen Sie eine Probe von oralen Bakterien
HINWEIS: Während viele orale Proben Saccharibakterien enthalten (z. B. Speichel, Mandelabstriche, Zungenkratzer), ist Zahnbelag routinemäßig der erfolgreichste.
- Nehmen Sie eine Plaque mit einer sterilen Papierspitze, Gracey-Kurette, oder, wenn Sie sich selbst entsenden, verwenden Sie einen sterilen Zahnstocher oder eine Pipettenspitze. Übertragen Sie Plaque auf einen geeigneten Puffer, wie z. B. Maximales Erholungsverdünnungssit (MRD, 0,85% NaCl, 0,1% Pepton) oder PBS. Wenn sie nicht sofort verarbeitet wird, halten Sie die Probe auf Eis, bis sie bereit ist, fortzufahren.
- Den Zahnbelag im MRD-Puffer mit einer Kombination aus Wirbeln und Pipettieren mit einer kleinen Pipettspitze kräftig enuspendieren.
- Fügen Sie eine reuspendierte Plaqueprobe zu einem zusätzlichen 9 ml MRD-Puffer hinzu.
3. Filtrat aus oraler Probe vorbereiten
- Mit aseptischer Technik eine sterile Filterbaugruppe auspacken. Drehen Sie eine Vierteldrehung und ziehen Sie den Filterhalter wieder an, um sicherzustellen, dass die Gewinde richtig eingerast sind und das Gerät ordnungsgemäß geschlossen ist. Waschen Sie die Membran mit einer Spritze, indem Sie 10 ml MRD-Puffer durch das Gerät geben. Eine unsachgemäße Montage wird bei diesem Schritt durch Austreten von Flüssigkeit aus dem Filterhalter aufgedeckt. Wenn eine Leckage auftritt, besorgen Sie sich eine weitere Sterilefilterbaugruppe und wiederholen Sie den Waschschritt.
- Tragen Sie die Probe auf den gewaschenen Filter auf. Entfernen Sie den Kolben aus einer Spritze und befestigen Sie ihn an der Filtervorrichtung. Gießen Sie die dispergierte Zahnprobe, jetzt in 10 ml MRD-Puffer, in eine Spritze und laden Sie sie auf den Filter.
- Legen Sie ein steriles Zentrifugenrohr unter die Filtervorrichtung, um das Filtrat aufzufangen, und drücken Sie dann leichten Druck auf den Kolben aus, um die Probe durch den Filter zu drücken.
- Wiederholen Sie den Vorgang mit einem weiteren 10 ml MRD-Puffer, um die Membran zu waschen, und sammeln Sie den Durchfluss im selben Röhrchen wie die gefilterte Probe. Aseptisch das Röhrchen verschließen.
4. Saccharibakterienzellen durch Zentrifugation konzentrieren
- Machen Sie eine Orientierungsmarkierung auf dem Rohr und der Kappe und legen Sie das Rohr in eine Hochgeschwindigkeitszentrifuge mit der Markierung auf der Oberseite. Das durch Zentrifugation gebildete Pellet ist in der Regel unsichtbar. Die Markierung hilft zu bestimmen, wo sich das Pellet der Saccharibakterienzellen befindet, wenn die Zentrifugation durchgeführt und das Röhrchen aus der Zentrifuge entfernt wird.
- Zentrifuge die Proben bei 60.000 x g für 1 h bei 4 °C.
HINWEIS: Diese Kraft und Zeit reicht aus, um alle Saccharibakterienzellen zu pelletieren. Saccharibakterienzellen können jedoch zumindest teilweise durch Zentrifugieren für nur 20 minuten bei 20.000 x gpelletiert werden. - Entfernen Sie die Röhrchen vorsichtig aus der Zentrifuge. Gießen Sie die Flüssigkeit aus dem Rohr aus und halten Sie das Pellet auf der Oberseite des Rohres.
- Resuspend das normalerweise unsichtbare Pellet in 1-2 mL MRD-Puffer durch kräftiges Vortexing.
5. Wirtskulturen mit mit Saccharibakterien angereichertem Filtrat infizieren
- Bereiten Sie Kulturröhrchen vor, indem Sie 2 ml geeignete Wachstumsmedien (z. B. TSBY, BHI usw.) in Röhrchen aliquotieren.
- Fügen Sie 200 μL Nachtkultur von Wirtsorganismen zu jeder Röhre hinzu. 100-200 μL resuspendierte, gefilterte Probe werden in jedes Röhrchen gegeben.
- Inkubieren Sie kombinierte Proben, die für den Wirtsorganismus geeignet sind (z. B. 37 °C, in aerober Atmosphäre für A. propionica).
- Passage der Zellen alle zwei bis drei Tage, indem 200 μL binäre Kultur auf 2 ml frisches Wachstumsmedium in einem neuen Röhrchen übertragen werden. Wenn sich herausstellt, dass die durchgereichten Kulturen kein Wachstum zeigen (d.h. die Trübung / optische Dichte der Kultur nimmt nach dem Übergang in frische Medien nicht zu), könnten die Saccharibakterien den gesamten Wirtsorganismus überwältigen oder töten. Um dies zu beheben, fügen Sie 200 μL nicht infizierte Wirtskultur hinzu, wenn Sie die Zellen passieren. Wiederholen Sie dies für mindestens 5 Passagen.
6. Bestätigen Sie die Infektion durch PCR
- Nach 5 Passagen die Infektion mit PCR bestätigen. Fünf Passagen stellen sicher, dass alle nicht wachsenden Saccharibakterienzellen mit 25 PCR-Zyklen über die Nachweisgrenze hinaus erschöpft sind.
- Bereiten Sie einen PCR-Mastermix vor. Ein vorgeschlagenes Rezept ist wie folgt, für jedes benötigte Röhrchen 12,5 μL 2x PCR-Puffer, 0,75 μL 10 μM Forward Primer (580F12 - AYT GGG CGT AAA GAG TTG C), 0,75 μL 10 μM Reverse Primer (1177R13- GAC CTG ACA TCA TCC CCT CCT TCC), 1 μL 25 mM MgCl2 und 9 μL Wasser. Mischen Sie durch Wirbeln.
- Aliquot 24 μL Mastermix in eine 0,2 mL PCR-Röhre. Fügen Sie der PCR-Reaktion 1 μL Saccharibakterien-infizierte Kultur hinzu. Legen Sie das Rohr in einen Thermocycler und führen Sie das folgende Protokoll durch: Anfängliche Denaturierung 95 °C für 5 min, 25 Zyklen von 95 °C für 30 s, 60 °C für 30 s, 72 °C für 30 s, endgültige Dehnung bei 72 °C für 2 min, dann endgültiger Halt bei 4 °C.
- Laden und führen Sie die PCR-Produkte in einem 1% igen Agarosegel aus. Ein Band von ~ 600 Basen zeigt das Vorhandensein von Saccharibakterien an.
7. Auf Reinheit prüfen und kontaminierende Organismen entfernen
- Bestätigen Sie die Reinheit positiver Kulturen, indem Sie die Kokultur von Saccharibakterien auf Nährstoffagar plattieren, das für das Wachstum des Wirtsorganismus ausreicht. Führen Sie eine 10-fache serielle Verdünnung der Kultur in sterilem Puffer (z. B. MRD oder PBS) durch und verteilen Sie 100 μL auf einer Agarplatte. Führen Sie Verdünnungen durch, so dass etwa 20-200 Kolonien auf der Agarplatte wachsen.
- Inkubieren Sie die Kultur unter geeigneten Wachstumsbedingungen und beobachten Sie auf kontaminierende Organismen.
HINWEIS: Axenische Saccharibakterienkolonien wurden noch nie beobachtet, so dass nur der Wirtsorganismus auf diesen Platten wächst. Mehr als ein Kolonietyp weist in der Regel auf eine Kontamination hin. Sollte eine Kontamination auftreten, sollte die Kultur erneut gefiltert werden, um die unerwünschten Verunreinigungen zu entfernen, und erneut auf frischen Wirt geimpft werden. - Gelegentlich kommt es zu einer Doppelinfektion, bei der zwei Saccharibakterienarten denselben Wirt infizieren. Um die Saccharibakterien-Spezies zu trennen, resuspendieren Sie einzelne Kolonien in 20 μL sterilem PBS und verwenden Sie 1 μL Suspension in einer PCR-Reaktion, um Kolonien mit Saccharibakterien-Infektionen nachzuweisen.
- Übertragen Sie die Suspensionen, die ein positives Ergebnis lieferten, auf das Wachstumsmedium, um eine binäre Kultur zu starten. Die Erfolgsrate hängt vom Titer jeder Saccharibakterienart in der Kultur ab. Es kann notwendig sein, mehr als 50 Kolonien zu screenen, um eine infizierte für die Vermehrung zu finden.
8. Speicherung von Kulturen
- Wachsen Sie über Nacht eine binäre Kultur mit ausreichendem Volumen (10-50 ml).
- Pelletzellen durch Zentrifugation (4.000 x g für 10 min).
HINWEIS: Eine Hochgeschwindigkeitszentrifugation ist hier nicht notwendig, da Saccharibakterienzellen an die größeren, schwereren Zellen des Wirts gebunden werden und mit ihnen pelletieren. - Resuspend Zellen in Kryoprotektivum. Wachstumsmedien, die entweder mit 5% DMSO oder 20% Glycerin ergänzt werden, sind in der Regel ausreichend. Stellen Sie sicher, dass der Wirtsorganismus mit kryoprotektiven Medien kompatibel ist (z. B. wird das Wachstum von A. propionica durch Glycerin gehemmt und gefrorene Bestände können nicht wiederbelebt werden). Testen Sie die Lebensfähigkeit einer nicht infizierten Wirtskultur mit Kryoprotektivum, um sicherzustellen, dass die Bestände das Einfrieren überleben können.
- Zellpellet im gleichen Kulturvolumen (10-50 ml) wiederbewenden. Aliquot 0,5 ml in markierte Kryoviale. Zellkulturen bei -80 °C einfrieren.
Ergebnisse
PCR zum Nachweis von Saccharibakterien kann in anfänglichen Infektionskulturen aufgrund einer geringen Anzahl von Saccharibakterien-Symbionten negativ erscheinen (d. h. kein Produkt gesehen). Nach einigen Passagen sollte jedoch ein starkes PCR-Produkt erscheinen, das zeigt, dass eine stabile Infektion aufgetreten ist (Abbildung 1A). Umgekehrt erscheinen einige Infektionen zunächst positiv durch PCR, verringern sich aber nach 1-4 Passagen (nicht gezeigt) auf nicht nachweisbar. Dies deutet darauf hin, dass eine große Menge an Saccharibakterienzellen im Anfangsfiltrat vorhanden war, aber durch Passage verdünnt wurde und keine in der Lage war, eine stabile Symbiose mit der Wirtskultur einzugehen. Das Testen mehrerer Wirtsarten mit dem gleichen Saccharibakterienfiltrat aus der Mundhöhle hat in der Regel eine geringe Erfolgsrate (Abbildung 1B), da die Symbionten-Wirt-Interaktion sehr spezifisch ist. Ein Forscher kann auch den gleichen Wirt mit Filtraten von mehreren verschiedenen Probanden testen. Wird ein guter Wirtsorganismus (wie Arachnia propionica oder Schaalia odontolytica)eingesetzt, ist mit einer Erfolgsquote von 50% zu rechnen.
Die Prüfung mittels PCR ist entscheidend. Erfahrene Forscher haben versucht, eine Infektion durch Mikroskopie zu bestätigen, nur um falsch positive Ergebnisse zu melden. Die Saccharibakterienzellen sind klein und schwer zwischen Vesikeln oder unregelmäßigen Zellhüllenwölbungen zu unterscheiden. Ein PCR-Signal, das über mehrere Passagen stabil ist, ist der Schlüssel zur Bestätigung einer erfolgreichen Infektion.
Wenn die infizierten Kulturen wachsen, sollte ein normales trübes Wachstum auftreten. Wenn sich die Symbiose etabliert, erscheinen infizierte Kulturen weniger trüb als Kulturen nicht infizierter Wirtsorganismen (Abbildung 2A). In einigen Fällen scheinen infizierte Kulturen vollständig zu wachsen und überhaupt nicht trüb zu werden. Dies kann auf eine Infektion zurückzuführen sein, bei der die Saccharibakterienzellen den Wirtsorganismus überwältigen. Das Hinzufügen eines "frischen" (nicht infizierten) Wirts zu diesen Kulturen sollte eine ausreichende Wirtspopulation bieten, um das weitere Wachstum der Saccharibakterien-Parasiten zu unterstützen.
Überwucherung oder übermäßig trübe Kulturen können auf eine Kontamination durch einen Laborkontaminanten oder ein anderes kleines orales Bakterium hinweisen, das den 0,2-μm-Filter passieren konnte. Campylobacter und Capnocytophaga spp. sind typische orale Verunreinigungen dieser Experimente. Dies kann durch Beschichtung der Kultur und die Suche nach Kolonien, die für den Wirtsorganismus atypisch sind, gefolgt von einer 16S rRNA-Sequenzierung, bestätigt werden. Wenn eine Kontamination beobachtet wird, reicht die Filterung dieser Kulturen durch einen 0,2 μm-Filter in der Regel aus, um die Verunreinigungen zu entfernen. Sacchararibakterienzellen im Filtrat können durch Zentrifugation konzentriert und zur erneuten Infektion einer reinen Wirtskultur verwendet werden.
Eine andere Möglichkeit, eine kontaminierte Kultur zu reinigen, besteht darin, infizierte Kolonien aus der Beschichtung einer infizierten Kultur zu pflücken. Kolonien infizierter Wirte können manchmal durch unregelmäßige Kolonieform im Vergleich zu nicht infizierten Kolonien identifiziert werden (Abbildung 2B-D). Diese unregelmäßigen Kolonien sind abhängig vom Titer der Saccharibakterien in der binären Kultur und ein kleinerer Anteil der Kolonien erscheint unregelmäßig, wenn der Titer niedrig ist. Dies kann es leicht machen, infizierte Kolonien zu identifizieren, die ausgewählt und verwendet werden können, um eine reine binäre Kultur zu starten. Wenn bei der Beschichtung aus einer mit Saccharibacteria infizierten Kultur keine unregelmäßigen Kolonien zu sehen sind, ist es möglich, dass der Symbiont einen niedrigen Titer hat oder keine unregelmäßig geformten Kolonien verursacht. In einem solchen Fall können PCR-Screening-Kolonien mit normalem Aussehen eine Infektion durch Saccharibakterien zeigen, jedoch mit einer geringen Rate (2-10% aller Kolonien).
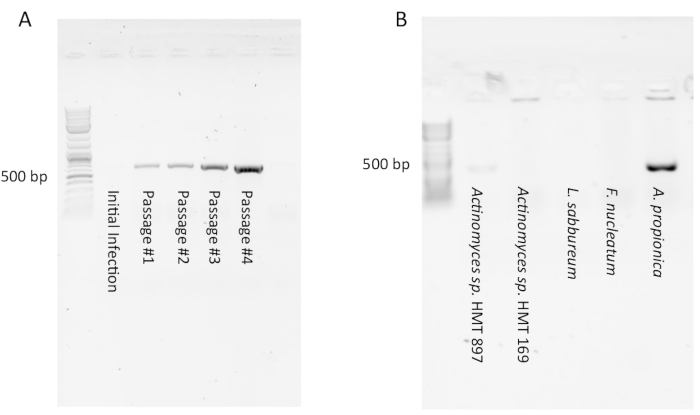
Abbildung 1: Typische PCR-Ergebnisse von Saccharibakterien-Infektionen von Wirtskulturen. (A) Ein PCR-Produkt, das auf das Vorhandensein von Saccharibakterien hinweist, kann jedoch bei der Erstinfektion nicht auftreten und in späteren Passagen stärker werden, wenn sich die Kokultur etabliert. (B) Die meisten Wirte, die mit Saccharibakterien angereichertem Filtrat infiziert sind, unterstützen ihr Wachstum aufgrund der Spezifität der Symbiose nicht. In diesem Beispiel wurde nur A. propionica erfolgreich infiziert. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.
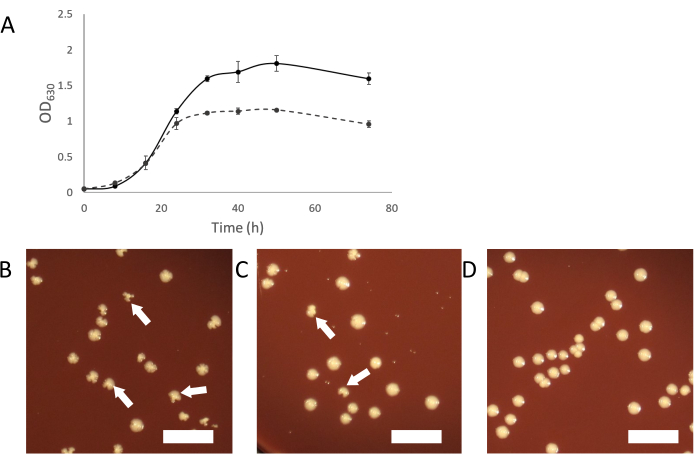
Abbildung 2: Wachstumsmerkmale von mit Saccharibakterien infizierten Kulturen. (A) Wachstumskurven von infizierten und nicht infizierten Kulturen von A. propionica, die eine infizierte Kultur zeigen, wachsen nicht auf die gleiche Dichte wie die nicht infizierte Kontrolle und erscheinen weniger trüb. (B-D) Das Plattieren von Kokulturen kann unregelmäßige Kolonien erzeugen, die durch Saccharibateria-Infektionen verursacht werden. Unregelmäßige Kolonien nehmen proportional zum Titer der Saccharibakterien in der Kokultur ab. (B) Wirt mit einem hohen Gehalt an Saccharibakterien. (C) 10-fach verdünnte Saccharibakterien (D) Nicht infizierte Wirtskultur. Weiße Pfeile zeigen Beispiele für unregelmäßige Kolonien an. Maßstabsleiste= 1 cm. Bitte klicken Sie hier, um eine größere Version dieser Figur zu sehen.
Diskussion
Unsere Methode, Plaque zu filtern und auf Reinkulturen von Wirtsorganismen aufzutragen, basiert weitgehend auf früheren Beobachtungen an den ersten kultivierten Saccharibakterien, dem' Nanosynbacter lyticus' Stamm TM7x11,14,15. Angesichts der geringen Zellgröße folgerten wir, dass sie mit einem Filter vom Zahnbelag getrennt und mit Zentrifugation konzentriert werden konnten. Zweitens, da diese Organismen als Parasiten leben, würde die Bereitstellung dieser Zellen reiner Kulturen von Wirten es ihnen ermöglichen, eine Symbiose einzugehen und als binäre Kulturen zu wachsen.
Ein Vorteil dieser Methode ist, dass sie keine Anreicherungskultur oder Selektivdruck benötigt. DerNanosynbacter lyticus-Stamm TM7x wurde aus einer Anreicherungskultur mit Streptomycin als selektivem Mittel kultiviert, von dem die Sequenzierung vorgeschlagen hatte, dass es bei der Anreicherung für Saccharibakterien wirksam wäre. Zufälligerweise ist bekannt, dass der Wirt für 'Nanosynbacter lyticus' Schaalia odontolytica, als resistent gegen Streptomycin16bekannt ist. Die Verwendung von Antibiotika als selektives Mittel könnte auch das Wachstum des Wirtsorganismus verhindern, was wiederum das Wachstum von Saccharibakterien ausschließen würde.
Ein größeres Problem bei der Verwendung von Anreicherungskulturen ist, dass schnell wachsende Organismen Schnell Organismen von Interesse verdrängen. In der Mundhöhle zum Beispiel können Streptokokken-Arten schnell wachsen und, wenn Zucker im Wachstumsmedium vorhanden ist, genug Säure produzieren, um das Medium zu säuern und sich weiter gegen interessierende Organismen zu selektionieren. Durch die Vermeidung einer Anreicherungskultur und selektiver Antibiotika bietet unsere Methode einen allgemeinen Ansatz, der ohne die Komplikationen dieser anderen Methoden auf eine breitere Palette von Saccharibakterien und potenziellen Wirten angewendet werden kann.
Es gibt einige Hindernisse für die hier vorgestellte Methode. Erstens geht diese Methode davon aus, dass Saccharibakterien in einer binären Kultur leben. Wir haben keine Kombinationen von trinären oder ternären Kulturen getestet, um ihre Wirksamkeit zu messen, aber es gibt wahrscheinlich Sacchararibakterien, die Wachstumsfaktoren benötigen, die ein einzelner Wirtsorganismus nicht liefern kann. Das Testen der riesigen Kombinationen von oralen Bakterien, die das Wachstum von Saccharibakterien unterstützen könnten, wäre eine entmutigende Aufgabe. Zweitens geht die Methode davon aus, dass alle Saccharibakterien klein genug sind, um einen 0,2 μm-Filter zu durchlaufen. Es könnte sein, dass andere Saccharibakterien größer sind als angenommen und der Filter gegen diese Organismen auswählt. Ein Filter mit einer größeren Porengröße könnte verwendet werden, aber dies birgt die Gefahr, dass mehr unerwünschte orale Bakterien in die infizierte Co-Kultur gelangt. Schließlich ist es sehr schwierig, Wirtsarten außerhalb der bereits veröffentlichten zu finden. Bisher sind die einzigen erfolgreichen Wirte Arten aus den Gattungen Actinomyces, Schaalia, Arachnia und Cellulosimicrobium,alle Mitglieder des Stammes Actinobakterien15,17,18. Diese Wirte unterstützen jedoch nur das Wachstum bestimmter Saccharibakterien. Um mehr Arten von Saccharibakterien zu kulturen, müssen viel mehr Wirte erforscht werden.
Wir hoffen, dass die hier vorgestellte Methode die zukünftige Erforschung der Saccharibakterien und anderer CPR-Organismen unterstützen wird. Die metagenomische Sequenzierung legt nahe, dass diese Organismen auch kleine Genome haben und im Verdacht stehen, Symbionten zu sein oder sich auf die lokale mikrobielle Gemeinschaft verlassen, um Metaboliten und andere Faktoren zu liefern, die für ihr Überleben entscheidend sind19. Eine ähnliche Filterstrategie könnte verwendet werden, um diese Organismen zu isolieren, vorausgesetzt, sie sind klein genug und ihre Wirtsorganismen können kultiviert werden. Die hier beschriebenen Methoden sind ein erster Schritt, um die mächtigen Werkzeuge der Laborkultur in diese große und vielfältige Bakteriengruppe zu bringen.
Offenlegungen
Die Autoren haben nichts preiszugeben.
Danksagungen
Die Autoren danken Anne Tanner, Bruce Paster, Heike Boisvert, Xuesong He und Batbileg Bor für hilfreiche Gespräche und für die Bereitstellung von Bakterienstämmen. Wir danken Susan Yost und Jessica Woods für die mikrobielle technische Unterstützung. Die in dieser Veröffentlichung berichtete Forschung wurde vom National Institute of Dental and Craniofacial Research der National Institutes of Health unter den Vergabenummern R37 DE016937 (FED), R01 DE024468 (FED) und T32 DE007327 (AJC) unterstützt. Der Inhalt liegt allein in der Verantwortung der Autoren und stellt nicht unbedingt die offiziellen Ansichten der National Institutes of Health dar.
Materialien
| Name | Company | Catalog Number | Comments |
| Agarose | Fisher Scientific | BP160-100 | |
| Alphaimager | Cell Biosciences | FluorChem HD2 | Or equivalent UV gel imaging system |
| Aluminum foil | Fisher Scientific | 01-213-101 | |
| Brain Heart Infusion Broth (dehydrated powder) | Becton-Dickinson | 211059 | Or other growth media suitable for target organisms |
| Centrifuge Rotor 70-Ti | Beckman Coulter | 337922 | |
| Cryovials | Fisher Scientific | 12-567-500 | |
| DMSO | Fisher Scientific | BP231-100 | |
| Electrophoresis Power Supply | Bio-Rad | 1645052 | |
| Electrophoresis Rig | Bio-Rad | 1704467 | |
| Filter Forceps | Millipore Sigma | XX6200006P | Not essential, helps ensure filters are not punctured during handling |
| Glycerol | Fisher Scientific | G33-500 | |
| GoTaq Green Mastermix | Promega | M7122 | |
| Mastercycler Pro Thermocycler | Eppendorf | 950040025 | Or equivalent thermocycler for PCR |
| MgCl2 solution 25mM | Promega | A3513 | |
| Molecular Biology grade water | Fisher Scientific | BP2819100 | |
| O2 Control InVitro Glove Box | Coy Laoratories | 031615 | If needed for microaerobic organisms |
| Optima L-100 XP High Speed Centrifuge | Beckman Coulter | 8043-30-1124 | |
| P-10 micro pipette | Gilson | F144802 | |
| P-1000 micro pipette | Gilson | F123601G | |
| P-2 micro pipette | Gilson | F144801 | |
| P-20 micro pipette | Gilson | F123600 | |
| P-200 micro pipette | Gilson | F123602G | |
| PBS | Fisher Scientific | BP399500 | |
| PCR tubes 0.2 mL | Fisher Scientific | 14-230-205 | |
| Peptone | Fisher Scientific | BP1420-500 | |
| Pipette tips - 10 μL | Fisher Scientific | 02-717-157 | |
| Pipette tips - 1000 μL | Fisher Scientific | 02-717-166 | |
| Pipette tips - 20 μL | Fisher Scientific | 02-717-161 | |
| Pipette tips - 200 μL | Fisher Scientific | 02-717-165 | |
| Polycarbonate filters - 47mm, 0.2 μm pore size | Millipore | GTTP04700 | |
| Screw-cap conical centrifuge tubes 15 mL | Falcon | 352096 | Or other tube suitable for bacterial culture |
| Sodium chloride | Fisher Scientific | BP358-1 | |
| Swin-Lok Filter - 47mm | Whatman | 4200400 | |
| SYBR Safe DNA Gel stain | ThermoFisher Scientific | S33102 | |
| Syringes - 20 mL | Fisher Scientific | 14-955-460 | |
| TAE Buffer (50x) concentrate | Fisher Scientific | P1332500 | |
| Thickwall Polycarbonate 25 x 89 mm (26.3mL capacity) centrifuge tubes with caps | Beckman Coulter | 355618 | |
| Tryptic Soy Blood Agar Plates | Northeast Laboratory Services | P1100 | Or other agar plate sufficient for growth of host organisms |
| Tryptic Soy Broth (dehydrated powder) | Becton-Dickinson | 211825 | Or other growth media suitable for target organisms |
| Vinyl Anaerobic Chamber | Coy Laboratories | 032714 | If needed for anaerobic organisms |
| Vortex mixer | Scientific Industries | SI-0236 | |
| Yeast Extract | Fisher Scientific | BP1422-500 |
Referenzen
- Stewart, E. J. Growing unculturable bacteria. Journal of Bacteriology. 194 (16), 4151-4160 (2012).
- Bomar, L., Maltz, M., Colston, S., Graf, J. Directed culturing of microorganisms using metatranscriptomics. mBio. 2 (2), 00012 (2011).
- Derrien, M., Vaughan, E. E., Plugge, C. M., de Vos, W. M. Akkermansia muciniphila gen. nov., sp. nov., a human intestinal mucin-degrading bacterium. International Journal of Systematic and Evolutionary Microbiology. 54, 1469-1476 (2004).
- Nelson, M. C., Bomar, L., Maltz, M., Graf, J. Mucinivorans hirudinis gen. nov., sp. nov., an anaerobic, mucin-degrading bacterium isolated from the digestive tract of the medicinal leech Hirudo verbana. International Journal of Systematic and Evolutionary Microbiology. 65, 990-995 (2015).
- Scott, J. C., Klein, B. A., Duran-Pinedo, A., Hu, L., Duncan, M. J. A two-component system regulates hemin acquisition in porphyromonas gingivalis. PLoS One. 8 (9), 0073351 (2013).
- Martin, B., et al. New growth media for oral bacteria. Journal of Microbiological Methods. 153 (22), 10-13 (2018).
- Vartoukian, S. R., et al. In vitro cultivation of 'unculturable' oral bacteria, facilitated by community culture and media supplementation with siderophores. Plos One. 11 (1), 0146926 (2016).
- Strandwitz, P., et al. GABA-modulating bacteria of the human gut microbiota. Nature Microbiology. 4 (3), 396-403 (2019).
- Hug, L. A., et al. A new view of the tree of life. Nature Microbiology. 1, 16048 (2016).
- Castelle, C. J., Banfield, J. F. Major new microbial groups expand diversity and alter our understanding of the tree of life. Cell. 172 (6), 1181-1197 (2018).
- He, X., et al. Cultivation of a human-associated TM7 phylotype reveals a reduced genome and epibiotic parasitic lifestyle. Proceedings of the National Academy of Sciences of the United States of America. 112 (1), 244-249 (2015).
- Hugenholtz, P., Tyson, G., Webb, R. I., Wagner, A. M., Blackall, L. L. Investigation of candidate division TM7, a recently recognized major lineage of the domain Bacteria with no known pure-culture representatives. Applied and Environmental Microbiology. 67 (1), 411-419 (2001).
- Brinig, M., Lepp, P. Prevalence of bacteria of division TM7 in human subgingival plaque and their association with disease. Applied and Environmental Microbiology. 69 (3), 1687-1694 (2003).
- Bor, B., et al. Insights obtained by culturing saccharibacteria with their bacterial hosts. Journal of Dental Research. , 689-694 (2020).
- Bor, B., et al. Phenotypic and physiological characterization of the epibiotic interaction between TM7x and its basibiont actinomyces. Microbial Ecology. 71 (1), 243-255 (2016).
- Skopek, R. J., Liljemark, W. F., Bloomquist, C. G., Rudney, J. D. Dental plaque development on defined streptococcal surfaces. Oral Microbiology and Immunology. 8 (1), 16-23 (1993).
- Murugkar, P. P., Collins, A. J., Chen, T., Dewhirst, F. E. Isolation and cultivation of candidate phyla radiation Saccharibacteria (TM7) bacteria in coculture with bacterial hosts. Journal of Oral Microbiology. 12 (1), 1814666 (2020).
- Cross, K. L., et al. Targeted isolation and cultivation of uncultivated bacteria by reverse genomics. Nature Biotechnology. 37 (11), 1314-1321 (2019).
- Kantor, R., et al. Small genomes and sparse metabolisms of sediment-associated bacteria from four candidate phyla. MBio. 4 (5), 00708-00713 (2013).
Nachdrucke und Genehmigungen
Genehmigung beantragen, um den Text oder die Abbildungen dieses JoVE-Artikels zu verwenden
Genehmigung beantragenThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Alle Rechte vorbehalten