Zum Anzeigen dieser Inhalte ist ein JoVE-Abonnement erforderlich. Melden Sie sich an oder starten Sie Ihre kostenlose Testversion.
Method Article
Ein reproduzierbares Knorpelimpaktmodell zur Erzeugung einer posttraumatischen Arthrose beim Kaninchen
* Diese Autoren haben gleichermaßen beigetragen
In diesem Artikel
Zusammenfassung
Das offene mediale femorale Kondylus-Impaktmodell bei Kaninchen ist zuverlässig für die Untersuchung der posttraumatischen Osteoarthritis (PTOA) und neuer therapeutischer Strategien zur Eindämmung der PTOA-Progression. Dieses Protokoll erzeugt einen isolierten Knorpeldefekt des hinteren medialen Femurkondylus bei Kaninchen unter Verwendung eines schlittenbasierten Fallturms mit einem Impaktorkopf.
Zusammenfassung
Posttraumatische Osteoarthritis (PTOA) ist für 12 % aller Arthrosefälle in den Vereinigten Staaten verantwortlich. Die PTOA kann durch ein einzelnes traumatisches Ereignis ausgelöst werden, z. B. durch eine starke Belastung des Gelenkknorpels, oder durch eine Gelenkinstabilität, wie sie bei einer Ruptur des vorderen Kreuzbandes auftritt. Derzeit gibt es keine wirksamen Therapeutika zur Vorbeugung von PTOA. Die Entwicklung eines zuverlässigen Tiermodells für PTOA ist notwendig, um die Mechanismen, durch die Knorpelschäden ablaufen, besser zu verstehen und neue Behandlungsstrategien zu untersuchen, um das Fortschreiten der PTOA zu lindern oder zu verhindern. Dieses Protokoll beschreibt ein offenes, auf einem Fallturm basierendes Stoßmodell für den Femurkondylus von Kaninchen, um Knorpelschäden zu induzieren. Dieses Modell lieferte Spitzenlasten von 579,1 ± 71,1 N und Spitzenspannungen von 81,9 ± 10,1 MPa bei einer Time-to-Peak-Last von 2,4 ± 0,5 ms. Gelenkknorpel von impaktierten medialen Femurkondylen (MFCs) wiesen höhere Raten an apoptotischen Zellen (p = 0,0058) auf und besaßen höhere Osteoarthritis Research Society International (OARSI)-Werte von 3,38 ± 1,43 im Vergleich zu den nicht impaktierten kontralateralen MFCs (0,56 ± 0,42) und anderen Knorpeloberflächen des retinierten Knies (p < 0,0001). Es wurden keine Unterschiede in den OARSI-Scores zwischen den nicht impaktierten Gelenkflächen festgestellt (p > 0,05).
Einleitung
Posttraumatische Osteoarthritis (PTOA) ist weltweit eine der Hauptursachen für Behinderungen und macht 12 % bis 16 % der symptomatischen Osteoarthritis (OA) aus1. Der derzeitige Goldstandard für die Behandlung von Arthrose im Endstadium ist die totale Knie- und Hüftendoprothetik2 oder die Arthrodese, wie im Fall der tibiotalaren oder subtalaren Arthritis im Endstadium. Obwohl die Endoprothetik weitgehend erfolgreich ist, kann sie kostspielige und krankhafte Komplikationen mit sich bringen3. Darüber hinaus ist eine Endoprothetik bei Patienten unter 50 Jahren weniger wünschenswert, da die Überlebensrate bei revisionsfreien Implantaten bei 77 % bis 83 % gering ist4,5. Derzeit gibt es keine von der FDA zugelassenen Behandlungen, um das Fortschreiten der PTOA zu verhindern oder zu mildern.
PTOA betrifft das gesamte Gelenk, einschließlich des Synovialgewebes, des subchondralen Knochens und des Gelenkknorpels. Sie ist gekennzeichnet durch Gelenkknorpeldegeneration, Synovialentzündung, subchondralen Knochenumbau und Osteophytenbildung 6,7. Der Phänotyp der PTOA entwickelt sich über einen komplexen Prozess des Zusammenspiels von Knorpel, Synovium und subchondralem Knochen. Nach derzeitigem Verständnis führt eine Knorpelverletzung zur Freisetzung von Komponenten der extrazellulären Matrix (EZM) wie Typ-2-Kollagen (COL2) und Aggrecan (ACAN). Diese EZM-Komponentenfragmente sind entzündungsfördernd und verursachen eine erhöhte Produktion von IL-6, IL-1β und reaktiven Sauerstoffspezies. Diese Mediatoren wirken auf Chondrozyten und verursachen eine Hochregulierung von Matrix-Metalloproteinasen (MMPs) wie MMP-13, die den Gelenkknorpel abbauen und gleichzeitig die Matrixsynthese verringern, was zu einem allgemeinen katabolen Milieu für den Gelenkknorpel führt8. Darüber hinaus gibt es Hinweise auf eine erhöhte Chondrozyten-Apoptose bei primärer Arthrose und PTOA 9,10. Eine mitochondriale Dysfunktion tritt nach supraphysiologischer Belastung des Knorpels auf 11,12,13,14, was zu einer erhöhten Apoptose der Chondrozyten führen kann 12,15. Eine verstärkte Chondrozyten-Apoptose wurde mit einer erhöhten Proteoglykan-Depletion und einem Knorpelkatabolismus in Verbindung gebracht und geht nachweislich Veränderungen des Knorpels und des subchondralen Knochenumbaus voraus16,17,18.
Wie bei den meisten menschlichen Krankheiten sind zuverlässige und translationale Modelle der PTOA erforderlich, um die Pathophysiologie der Krankheit besser zu verstehen und neue Therapeutika zu testen. Große Tiere wie Schweine und Hunde wurden in intraartikulären Fraktur- und Impaktmodellen von PTOA17,19 verwendet, aber sie sind kostspielig. Kleinere Tiermodelle wie Mäuse, Ratten und Kaninchen sind kostengünstiger und werden verwendet, um PTOA zu untersuchen, die durch Gelenkdestabilisierung entsteht, was typischerweise eine chirurgische Durchtrennung des vorderen Kreuzbandes (ACL) und/oder eine Störung des Innenmeniskusbeinhaltet 20,21,22,23,24,25. Obwohl ein Gelenktrauma zu verschiedenen Folgen führen kann, einschließlich Bandverletzungen26, kommt es in fast allen Fällen zu einer mechanischen Überlastung des Knorpels.
Es gibt immer mehr Hinweise darauf, dass die Pathologie hinter der Entwicklung von PTOA nach Bandinstabilität (wie bei einer VKB-Durchtrennung) und einer akuten chondralen Verletzung auf unterschiedliche Mechanismen zurückzuführen ist27. Daher ist es wichtig, Modelle für die direkte Schädigung des Knorpels zu entwickeln. Derzeit gibt es eine begrenzte Anzahl von Impaktmodellen, die osteochondrale oder chondrale Verletzungen bei Ratten und Mäusen hervorrufen28,29. Der murine Knorpel ist jedoch nicht gut geeignet, um isolierte chondrale Defekte zu erzeugen. Dies liegt daran, dass der murine Gelenkknorpel nur 3-5 Zellschichten dick ist und keine organisierten oberflächlichen, radialen und Übergangsknorpelzonen sowie die dicke verkalkte Knorpelschicht aufweist, die bei Menschen und größeren Tieren zu finden ist. Mausmodelle zeigen auch eine spontane Auflösung von partiellen Knorpeldefekten30,31. Daher haben wir uns für das Kaninchen für dieses Aufprallmodell entschieden, da seine Knorpeldicke und -organisation denen des Menschen ähneln und es das kleinste Tiermodell ist, das die Verabreichung eines konsistenten chondralen Aufpralls ermöglicht, der zu PTOA führt. Frühere offene chirurgische Modelle des Aufpralls des Femurkondylus beim Kaninchen verwendeten ein Pendel32, eine handgehaltene, federbelastete Knorpelimpaktionsvorrichtung33 und einen Fallturm, der die Erzeugung eines kaninchenspezifischen Impaktors34 ermöglichte. Diesen Studien fehlten jedoch In-vivo-Daten. Andere haben In-vivo-Daten mit pendelbasierten35, pneumatischen36 und federbelasteten37 Schlaggeräten10 berichtet, und diese Studien zeigen eine hohe Variabilität der Spitzenbelastung und der Belastungsraten zwischen den Methoden. Dennoch fehlt es an einem konsistenten Ansatz, um akute Knorpeltraumata in vivo zuverlässig zu modellieren.
Das derzeitige Protokoll verwendet ein Fallturm-basiertes System, um einen gleichmäßigen Aufprall auf den hinteren medialen Kondylus des Kaninchenknies zu erzielen. Ein posteriorer Zugang zum Knie wird verwendet, um den hinteren medialen Femurkondylus freizulegen. Ein Steinman-Stift wird dann quer über die Femurkondylen von medial nach lateral in einer Linie mit der Gelenkoberfläche platziert und an der Plattform befestigt. Nach der Sicherung wird eine Ladung an den hinteren medialen Femurkondylus abgegeben. Diese Methode ermöglicht es, eine gleichmäßige Knorpelschädigung auf die gewichtstragende Oberfläche des distalen Femurs des Kaninchens zu übertragen.
Protokoll
Das folgende Verfahren wurde mit Genehmigung des Institutional Animal Care and Use Committee (IACUC) der Indiana University School of Medicine durchgeführt. Alle Überlebensoperationen wurden unter sterilen Bedingungen durchgeführt, wie in den NIH-Richtlinien beschrieben. Schmerz- und Infektionsrisiken wurden mit geeigneten Analgetika und Antibiotika behandelt, um die erfolgreichen Ergebnisse zu optimieren. Für die vorliegende Studie wurden skelettreife männliche neuseeländische Weißkaninchen mit einem Gewicht von 3,0-4,0 kg verwendet.
1. Herstellung von Falltürmen
- Generieren Sie CAD-Zeichnungen für Komponenten des Fallturms, der Basisplattform und des Mechanismus zur Sicherung des Steinman-Stifts (Ergänzende Abbildungen 1-14).
- Erwerben Sie handelsübliche Komponenten (siehe Materialtabelle).
- Beschaffen Sie die Maschinenteile des Geräts oder geben Sie CAD-Zeichnungen an einen Maschinisten zur Fertigung.
HINWEIS: Für die Herstellung der Impaktorspitze mit einem Durchmesser von 3 mm ist ein hochpräziser Maschinist mit Werkzeugbaukenntnissen erforderlich (Ergänzende Abbildung 1, Teil 20 und Ergänzende Abbildungen 13,14). Die Aufprallfläche des Impaktorkopfes wies Krümmungen von 7,14 mm bzw. 5,56 mm in der sagittalen bzw. koronalen Ebene auf, um der Krümmung des medialen Kaninchenkondylus35 zu entsprechen (ergänzende Abbildungen 13,14). - Montieren Sie die Teile so, dass der Fallturm aus einem Schlitten besteht, der sich auf zwei vertikalen Stangen über Linearkugellager mit fester Ausrichtung bewegt, und die Basisplattform den Hasen stützt und den Steinman-Stift sichert (Abbildung 1 und Abbildung 2).
ANMERKUNG: Die Schlittentraverse dieser Konstruktion hat eine Biegesteifigkeit, die der eines früheren Fallturms38 mit einem akzeptablen Schwingungsniveau entspricht.
2. Zubereitung von Tieren
- Wiegen Sie das Kaninchen und betäuben Sie es mit 2,5 mg/kg Alfaxalone und 0,15 mg/kg Midazolam i.m. (siehe Materialtabelle). Tragen Sie nach der Induktion Augensalbe auf beide Augen auf. Halten Sie die Anästhesie mit ~2%-3% Isofluran aufrecht. Geben Sie Buprenorphin SR (0,1 mg/kg) SQ zur Analgesie und perioperatives Enrofloxacin (10 mg/kg) SQ. Anstelle von Buprenorphin können NSAIDs wie Carprofen, 4 mg/kg oder Meloxicam, 0,2 – 0,3 mg/kg oder Ketoprofen, 3 mg/kg als SQ-Injektionen verabreicht werden.
- Rasieren Sie die Hintergliedmaße des Kaninchens vom Knöchel bis zur Hinterhand. Bei der Haarentfernung von Kaninchen ist besondere Vorsicht geboten, um eine Kontamination des Einschnitts zu vermeiden. Die Verwendung einer speziellen, scharfen Kaninchenhaarschneidemaschine ist wichtig.
- Legen Sie den vorderen Beinblock aus Edelstahl (Ergänzende Abbildung 1, Teil Nr. 2 und Ergänzende Abbildung 4) unter das Ende der Aufprallplattform und decken Sie die Plattform mit einem Heizkissen ab. Legen Sie das Brustbein des Kaninchens (d. h. in Bauchlage) auf das Heizkissen. Platzieren Sie eine gepolsterte Beule unter der kontralateralen Hüfte.
- Stellen Sie sicher, dass das Knie der operativen Extremität zentriert ist und auf dem Polyethylenblock aufliegt (Abbildung 2A1). Verwenden Sie Seidenband, um den Schwanz oberhalb und kontralateral der operativen Extremität sanft zurückzuziehen.
- Wischen Sie die Operationsstelle mit Chlorhexidin und 70%iger steriler Gaze ab. Schrubben Sie die Operationsstelle, beginnend am hinteren Knie, mit einem kreisförmigen Schwung nach außen. Wiederholen Sie dies mindestens 3 Mal mit frischen Peelings, die mit 70% Alkohol enden.
- Legen Sie einen sterilen Handschuh über den OP-Fuß bis zum Knöchel und wickeln Sie ihn mit einem sterilen, kohäsiven Wickel um.
- Decken Sie die Operationsstelle steril mit drei Abdeckungen ab: eines direkt unter der operativen Extremität und die anderen beiden, um den Rest des Körpers zu bedecken. Befestigen Sie die Vorhänge mit Handtuchklemmen.
3. Chirurgische Exposition
HINWEIS: Vor der Operation und dem Aufprall sollten das Gewicht und die Fallhöhe, die zu sichtbaren Knorpelschäden ohne subchondralen Knochenbruch führen, empirisch für den spezifischen Stamm, das Alter und das Geschlecht des Kaninchens bestimmt werden.
- Abtasten Sie die Position der Kniescheibe anterior, um die Position des Kniegelenks abzuschätzen, das sich distal der Kniescheibe befindet. Machen Sie mit einer 15-Klinge einen 3-4 cm langen Schnitt entlang der hinteren Seite des gestreckten Knies auf Höhe des oberen Pols der Kniescheibe distal.
- Führe stumpfe und scharfe Präparationen durch die darunter liegende oberflächliche Faszie durch. Entwickeln Sie das Intervall zwischen der Haut medial und dem medialen Gastrocnemius lateral. Platzieren Sie einen selbsthaltenden Weitlaner-Retraktor in diesem Intervall (siehe Materialtabelle).
- Eine sekundäre Faszienschicht wird direkt über der Arteria saphena und Vene sichtbar. Sezieren Sie lateral des Saphenus und ziehen Sie das Gefäßsystem medial und den posterioren Gastrocsoleus-Komplex lateral zurück.
HINWEIS: Achten Sie darauf, dieses Gefäßsystem nicht zu durchtrennen. Wenn diese Arterie beschädigt ist, stellen Sie eine ordnungsgemäße Ligatur sicher, da es zu einem postoperativen hämorrhagischen Schock kommen kann.
- Eine sekundäre Faszienschicht wird direkt über der Arteria saphena und Vene sichtbar. Sezieren Sie lateral des Saphenus und ziehen Sie das Gefäßsystem medial und den posterioren Gastrocsoleus-Komplex lateral zurück.
- Distal sezieren, bis eine kleine bewegliche Fabella über dem hinteren medialen Femurkondylus identifiziert wird. Führen Sie eine Arthrotomie durch, um die Fabella superolateral zu mobilisieren und den darunter liegenden medialen Femurkondylus freizulegen. Entfernen Sie vorsichtig das Weichgewebe durch stumpfe und scharfe Dissektion, um den hinteren Teil des medialen Femurkondylus freizulegen. Verwenden Sie einen Freer- und Cricket-Selbsthalter (siehe Materialtabelle), um das Weichgewebe auf dieser Ebene zurückzuziehen.
- Während der Kondylus freiliegt, schieben Sie einen 0,062 Zoll langen Steinman-Stift (siehe Materialtabelle) über den distalen Femur, beginnend am oberen Aspekt des medialen Femurkondylus und zentriert in der anterior-posterioren Richtung des medialen Femurkondylus, etwa 5 mm vom hinteren Aspekt des Kondylus entfernt.
- Treiben Sie den Draht mit einem batteriebetriebenen Steinman-Stifttreiber seitlich durch den Knochen und die Außenhaut parallel zur Gelenkoberfläche. Die Palpation des lateralen Epicondylus stellt die richtige Trajektorie des Steinman-Pins sicher.
- Entfernen Sie die Retraktoren und verschließen Sie die Haut mit einem 3-0 Polysorb-Naht (siehe Materialtabelle) in laufender Weise. Decken Sie den Einschnitt mit steriler Gaze ab.
4. Einfluss des Femurkondylus
- Entfernen Sie das Tuch unter der operativen Gliedmaße und befestigen Sie den Steinman-Stift an einer anpassbaren und höhenverstellbaren Aufprallplattform. Platzieren Sie zunächst die höhenverstellbare, untere Seite der Steinman-Bolzensicherung unter dem Stift (Abbildung 2A2). Stellen Sie sicher, dass der Draht auf dieser Plattform parallel zum Boden ist, indem Sie die Schraubenhöhen nach Bedarf anpassen.
- Nachdem Sie sich vergewissert haben, dass der Steinman-Stift parallel zum Boden ist, platzieren Sie die obere schraubenbasierte Seite der sicheren Plattform (Abbildung 2A3) auf der unteren schraubenbasierten Seite des höhenverstellbaren Teils. Stellen Sie sicher, dass der Steinman-Stift fest befestigt ist, indem Sie die obere Stange in den unteren höhenverstellbaren Teil der Stifthalteplattform schrauben (Abbildung 2A2).
- Sobald der Steinman-Stift an der Plattform befestigt ist, entfernen Sie die Naht und öffnen Sie den Schnitt erneut. Legen Sie den medialen Femurkondylus mit selbsthaltenden Weitlaner- und Cricket-Retraktoren frei. Ein zusätzlicher Freer kann erforderlich sein, um zusätzliches Weichgewebe aus dem Weg der Impaktorspitze herauszuziehen (Abbildung 2B).
- Wischen Sie den Fallturm mit einem zugelassenen Desinfektionsmittel ab. Befestigen Sie den sterilen 3-mm-Impaktorkopf (Abbildung 2A4) am Fallturmschlitten. Bringen Sie den Fallturm über das operative Ende und platzieren Sie seine Basis (Abbildung 2A6) unter der aufprallenden Plattform (Abbildung 3A).
- Senken Sie den Impaktor (ergänzende Abbildung 2, Teil 20 und ergänzende Abbildung 13) vorsichtig auf die Mitte des hinteren medialen Femurkondylus ab. Stellen Sie sicher, dass sich kein weiches Gewebe im Weg des Impaktors befindet.
- Bewegen Sie das Kaninchen oder den Turm nach Bedarf, um sicherzustellen, dass der Impaktorkopf über dem hinteren medialen Femurkondylus zentriert ist (Abbildung 3B). Jedes Mal, wenn das Kaninchen bewegt oder neu positioniert wird, sollte diese Operationsstelle auf mögliche Unterbrechungen der Sterilität untersucht und der Bereich bei Bedarf erneut sterilisiert werden.
- Sobald die richtige Flugbahn sichergestellt ist, wird der Turm mit den Schnellspannern auf die Plattform geklemmt (Abbildung 2A5, siehe Materialtabelle).
- Verabreichen Sie eine Dosis intravenös verabreichtes Alfaxalone (0,5-0,7 mg/kg) 5-10 Minuten vor dem Aufprall für eine tiefere Anästhesie, ohne die Inhalationsanästhesie zu erhöhen.
HINWEIS: Ein Mangel an Lidreflex, Pedalrückzug und Ohrmuschelreflex deutet auf eine tiefere Anästhesie hin. Diese tiefere Anästhesie hilft, mögliche Reaktionen der Gliedmaßen während der Platzierung im Gerät und beim Aufprall zu verhindern.
VORSICHT: Bei zu schneller Verabreichung kann Alfaxalone bei Kaninchen vorübergehende Apnoe und Hypoxie verursachen und sollte langsam über 1-2 Minuten verabreicht werden. Wenn eine Hypoxie auftritt, stellen Sie eine ausreichende Sauerstoffversorgung und Wiederherstellung der Vitalfunktionen sicher, bevor Sie fortfahren. - Stellen Sie den Impaktor auf dem Fallturm auf die gewünschte Höhe über dem medialen Femurkondylus ein. Bei der aktuellen Schlittenbaugruppe inklusive Lager mit einer Masse von 1,41 kg ist dies eine Höhe von 7 cm.
ANMERKUNG: Die Fallturmhöhe wurde anhand von Pilotstudien an Leichengewebe bestimmt. Diese Höhe führte bei den Kaninchen in dieser Studie zu sichtbaren Knorpelschäden, aber nicht zu subchondralen Knochenbrüchen. - Klicken Sie auf die Schaltfläche Start in der Datenerfassungssoftware LabVIEW (Supplementary Coding File 1), kurz bevor Sie den Spindelanschlag freigeben (Ergänzende Abbildung 2, Pos. 14), um den Schlitten zu lösen und ihn unter der Schwerkraft fallen zu lassen.
HINWEIS: Die Datenerfassungssoftware sammelt die Daten von einer Wägezelle (Abbildung 1, 6), die zwischen dem Schlagkörper und dem Schlitten positioniert ist, und einem Beschleunigungsmesser (Abbildung 1, 7) während des Aufpralls bei 100 kHz mit einem Laptop, der an ein Datenerfassungsmodul angeschlossen ist. - Platzieren Sie die von der Datenerfassungssoftware generierte txt-Datei im selben Ordner wie den Matlab-Datenanalysecode (Supplementary Coding File 2) und führen Sie den Datenanalysecode aus, um Rohdaten zu filtern und Auswirkungsparameter zu berechnen.
- Stellen Sie sicher, dass die maximale Belastung ermittelt wird. Der zugehörige Zeitpunkt wird als Zeitpunkt der maximalen Verformung und der Nullgeschwindigkeit betrachtet.
Hinweis: Der Datenanalysecode analysiert alle TXT-Dateien im Ordner und meldet die Ergebnisse für jede Datei. Der Code bestimmt den Beginn und das Ende der Auswirkung basierend auf Änderungen in den Ladezeitdaten. Die Daten des Beschleunigungsmessers werden numerisch integriert, um die Geschwindigkeit zu berechnen, und wieder integriert, um die Verschiebung zu berechnen. Der Datenanalysecode berechnet numerisch den Impuls, die Arbeit und die kinetische Energie aus den folgenden Formeln:
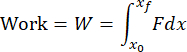

wobei F die vom Lastsensor gemessene Kraft, x 0 und t 0 die Verschiebung und Zeit zu Beginn des Aufpralls und x und tf die Verschiebung und Zeit am Ende des Aufpralls sind. Die Belastungsrate wird numerisch als Mittelwert von dσ/dt in der Belastungsphase des Aufpralls berechnet. Die Spitzenspannung wird berechnet, indem die Spitzenlast durch die Kontaktfläche des Schlagkörperkopfes dividiert wird. - Führen Sie eine Visualisierung der Knorpeloberfläche durch, um festzustellen, ob ein entsprechender Knorpelschaden aufgetreten ist (Abbildung 4A).
5. Verschluss der Operationsstelle
- Entferne den Fallturm über der operativen Extremität. Legen Sie alle gebrauchten chirurgischen Instrumente beiseite und ziehen Sie neue sterile Handschuhe an.
HINWEIS: Da der Fallturm nicht steril ist, sollten nun alle bis zum Aufprall verbrauchten Werkzeuge als kontaminiert betrachtet werden. - Legen Sie erneut ein steriles Tuch auf die untere Extremität und besorgen Sie sich unbenutzte sterile Selbstretraktoren.
- Legen Sie den medialen Femurkondylus wieder frei und spülen Sie die Operationsstelle gründlich mit 50-60 ml steriler Kochsalzlösung.
- Verschließen Sie die hintere Kapsel mit einer 5-0 Polysorb-Naht, gefolgt von einem Hautverschluss mit einer 4-0 Monosorb-Naht (siehe Materialtabelle).
- Injizieren Sie 2 ml Lidocain/Bupivacain zur lokalen Analgesie um den Einschnitt herum intradermal.
- Entfernen Sie den Steinman-Stift mit einem Power-Driver-Set (siehe Materialtabelle), indem Sie ihn oszillieren, um Weichteilverletzungen zu minimieren.
- Verbinden Sie die Wunde mit einem nicht klebenden Verband, gefolgt von Klebeband. Führen Sie eine Röntgenaufnahme der operativen Extremität durch, um sicherzustellen, dass keine Fraktur aufgetreten ist und der Stift richtig platziert wird (Abbildung 4B).
6. Postoperatives Management
- Bringen Sie das Kaninchen in seinen Käfig zurück und überwachen Sie es auf beheizten Decken, bis es sich von der Narkose erholt hat (~25 min).
- Beobachten Sie die Kaninchen noch einige Tage nach der Operation genau, um sicherzustellen, dass sie richtig heilen und ihre Mobilität wiedererlangen. Enrofloxacin (10 mg/kg) für 2 Tage postoperativ zur Infektionsprophylaxe verabreichen. Verabreichen Sie die Buprenorphin-SR-Analgesie (0,1 mg/kg) alle 2-3 Tage nach der Operation und nach Bedarf subkutan. Anstelle von Buprenorphin können NSAIDs wie Carprofen, 4 mg/kg SQ täglich, Meloxicam, 0,2 – 0,3 mg/kg SQ täglich bis zu 3 Tage oder Ketoprofen, 3 mg/kg SQ täglich 3-5 Tage nach der Operation und nach Bedarf verabreicht werden.
HINWEIS: Es ist uns gelungen, eine postoperative Wunddehiszenz durch Lecken oder Kauen von Kaninchen zu verhindern, indem wir menschliche Neugeborenenhosen über die Hintergliedmaßen gelegt haben39. Wenn das Kaninchen die Hose durchkaut, kann ein elisabethanisches Halsband (siehe Materialtabelle) angebracht werden, um das Kauen des Einschnitts zu verhindern.
7. Histologische Auswertung
- 16 Wochen nach der Verletzung entnehmen Sie die Knie von euthanasierten Kaninchen, fixieren sie 48 Stunden lang in 10% neutralem gepuffertem Formalin, gefolgt von Paraffineinbettung und Schneiden in 5 μm dicke Scheiben.
- Nach der Deparaffinisierung und Rehydratisierung färben Sie die Abschnitte mit Safranin O fast green gemäß den Standardprotokollen40,41.
- Führen Sie den terminalen Desoxynukleotidyltransferase-dUTP-Nick-End-Labeling-Assay (TUNEL) an den Abschnitten mit dem TUNEL Chromogenic Apoptosis Detection Kit gemäß den Anweisungen des Herstellers durch, das mit Hämatoxylin42 gegengefärbt ist (siehe Materialtabelle).
Ergebnisse
Der Erfolg dieses Eingriffs wurde unmittelbar nach dem Aufprall durch die Visualisierung des Kondylus durch den Chirurgen (Abbildung 4A) und durch Röntgenaufnahmen überwacht, um sicherzustellen, dass keine Fraktur auftrat (Abbildung 4B). Es besteht die Gefahr eines Stoßversagens, das zu einer intraoperativen Fraktur des Kondylus führt. Dies war in der Regel auf eine unsachgemäße Platzierung der Steinman-Stifte zurückzuführen (Abbildu...
Diskussion
Dieses chirurgische Verfahren zielt darauf ab, in einem Modell der PTOA eine konsistente Knorpelschädigung an der gewichtstragenden Oberfläche des medialen Femurkondylus des Kaninchens zu erzeugen. Ein Vorteil dieses Verfahrens besteht darin, dass der posteriore Zugang zum Knie eine direkte Visualisierung des kompletten posterioren medialen Femurkondylus ermöglicht und in ca. 37 min durchgeführt werden kann (Tabelle 2). Es sollte auch beachtet werden, dass es sich um ein offenes Verletzungsmodell han...
Offenlegungen
Roman Natoli hält Vorträge für AO Trauma North America, ist Redakteur für Current Osteoporosis Reports und erhielt Tantiemen für Lehrbücher von Morgan und Claypool. Todd McKinley erhält Tantiemen von Innomed. Die übrigen Autoren haben nichts offenzulegen.
Danksagungen
Diese Studie wurde unterstützt durch das DoD Peer Reviewed Medical Research Program - Investigator-Initiated Research Award W81XWH-20-1-0304 von der U.S. ARMY MEDICAL RESEARCH ACQUISITION ACTIVITY, durch NIH NIAMS R01AR076477 und ein umfassendes Musculoskeletal T32 Training Program der NIH (AR065971) und durch NIH NIAMS Grant R01 AR069657. Die Autoren danken Kevin Carr für die Bereitstellung seines Fachwissens in der Bearbeitung und Herstellung für dieses Projekt sowie Drew Brown und dem Indiana Center for Musculoskeletal Health Bone Histology Core für die Unterstützung bei der Histologie.
Materialien
| Name | Company | Catalog Number | Comments |
| Flat head screw | McMaster-Carr | 92210A194 | Stainless steel hex drive flat head screw, 8-32, 1/2" |
| #15 scalpel blades | McKesson | 1029066 | Scalpel McKesson No. 15 Stainless Steel / Plastic Classic Grip Handle Sterile Disposable |
| 1/2”-20 threaded rod | McMaster-Carr | 99065A120 | 1/2”-20 threaded rod |
| 10 mL syringe | McKesson | 1031801 | For irrigation; General Purpose Syringe McKesson 10 mL Blister Pack Luer Lock Tip Without Safety |
| 3 mL syringe | McKesson | 1031804 | For lidocaine/bupiviacaine injection; General Purpose Syringe McKesson 3 mL Blister Pack Luer Lock Tip Without Safety. |
| 3-0 polysorb | Ethicon | J332H | 3-0 Vircryl, CT-2, 1/2 circle, 26 mm, tapered |
| 4-0 monosorb | Ethicon | Z397H | 4-0 PDS 2, FS-2, 3/8 circle, 19mm, cutting edge |
| 5-0 polysorb | Med Vet International | NC9335902 | Med Vet International 5-0 ETHICON COATED VICRYL C-3 |
| Accelerometer | Kistler | 8743A5 | Accelerometer |
| Adson-Browns Forceps | World precision tools | 500177 | Adson-Brown Forceps, 12 cm, Straight, TC Jaws, 7 x 7 Teeth |
| Alfaxalone | Jurox | 49480-002-01 | Alfaxan Multidose by Jurox : 10 mg/mL |
| Buprenorphine | Par Pharmaceuticals | 42023-0179-05 | Buprenorphine HCL injection: 0.3 mg/mL |
| Butorphanol | Zoetis | 54771-2033 | Butorphanol tartrate 10mg/ml by Zoetis |
| Chlorhexidine Hand Scrub | BD | 371073 | BD E-Z Scrub 107 Surgical Scrub Brush/Sponge, 4% CHG, Red |
| Collet | STRYKER | 14023 | Stryker 4100-62 wire Collet 0.28-0.71'' |
| Cordless Driver handpiece | STRYKER | OR-S4300 | Stryker 4300 CD3 Cordless Driver 3 handpiece |
| Cricket Retractors | Novosurgical | G3510 21 | 2x Heiss (Holzheimer) Cross Action Retractor |
| Dissector Scissors | Jorvet labs | J0662 | Aesculap AG, Metzenbaum, Scissors, Straight 5 3/4″ |
| Elizabethian Collar | ElizaSoft | 62054 | ElizaSoft Elizabethan Recovery Collar |
| Enrofloxacin | Custom Meds | Enrofloxacin compounded by Custom Meds | |
| Eye Ointment | Pivetal | 46066-753-55 | Pivetal Articifical Tears- recently recalled |
| Face-mount shaft collar | McMaster-Carr | 5631T11 | Face-mount shaft collar |
| Fast green | Millipore Sigma | F7258 | Fast green |
| Freer | Jorvet labs | J0226Q | Freer elevator |
| Head screw -1 | McMaster-Carr | 91251A197 | Black-oxide alloy steel socket head screw, 8-32, 3/4" |
| Head screw -2 | McMaster-Carr | 92196A194 | Stainless steel socket head screw, 8-32, 1/2" |
| Head screw -3 | McMaster-Carr | 92196A146 | Stainless steel socket head screw, 8-32, 1/2" |
| Head screw -4 | McMaster-Carr | 92196A151 | Stainless steel socket head screw, 6-32, 3/4" |
| Hematoxylin Solution, Gill No. 1 | Millipore Sigma | GHS132-1L | Hematoxylin Solution, Gill No. 1 |
| Hex nut | McMaster-Carr | 91841A007 | Stainless steel hex nut, 6-32 |
| Hold-down toggle clamp | McMaster-Carr | 5126A71 | Hold-down toggle clamp |
| Impact device | n/a | n/a | custom made |
| Impact platform | n/a | n/a | custom made |
| K-wires | Jorvet Labs | J0250A | JorVet Intramedullary Steinman Pins, Trocar-Trocar 1/16" x 7" |
| Lab View | National Instruments | n/a | n/a |
| Load cell | Kistler | 9712B5000 | Load cell |
| MATLAB | The MathWorks Inc. | n/a | n/a |
| Microscope | Leica | DMi-8 | Leica DMi8 microscope with LAS-X software |
| Midazolam | Almaject | 72611-749-10 | Midazolam Hydrochloride injection: 5mg/ml by Almaject |
| milling machine depth stops | McMaster-Carr | 2949A71 | Clamp-on milling machine depth stops |
| Mobile C-arm | Philips | 718095 | BV Pulsera, Mobile C-arm |
| Mounted linear ball bearing | McMaster-Carr | 9338T7 | Mounted linear ball bearing |
| Needle Driver | A2Z Scilab | A2ZTCIN39 | TC Webster Needle Holder Smooth Jaws 5", Premium |
| Pentobarbital | Vortech | 0298-9373-68 | Pentobarbital 390 mg/mL by Vortech |
| Safranin O | Millipore Sigma | HT90432 | Safranin O |
| Small Battery pack | STRYKER | NS014036 | 6212 Small Battery pack- 9.6 V |
| Steel rod, 2’ | McMaster-Carr | 89535K25 | Steel rod, 2’ |
| Sterile Saline | ICU Medical | 6139-22 | AquaLite Solution Pour Bottles, 250 mL |
| Stryker 6110-120 System 6 Battery Charger | STRYKER | OR-S6110-120 | |
| Surgical gloves | McKesson | 1044729 | Surgical Glove McKesson Perry Size 6.5 Sterile Pair Latex Extended Cuff Length Smooth Brown Not Chemo Approved |
| Surgical gown | McKesson | 1104452 | Non-Reinforced Surgical Gown with Towel McKesson Large Blue Sterile AAMI Level 3 Disposable |
| Suture scissors | Jorvet Labs | J0910SA | Super Cut Scissors, Mayo, Straight, 5 1/2″ |
| TUNEL staining kit | ABP Bioscience | A049 | TUNEL Chromogenic Apoptosis Detection Kit |
| Weitlaner Retractors | Fine Science Tools | 17012-11 | 2x Weitlaner-Locktite Retractors |
Referenzen
- Thomas, A. C., Hubbard-Turner, T., Wikstrom, E. A., Palmieri-Smith, R. M. Epidemiology of posttraumatic osteoarthritis. Journal of Athletic Training. 52 (6), 491-496 (2017).
- Pasquale, M. K., et al. Healthcare Utilization and costs of knee or hip replacements versus pain-relief injections. American Health Drug Benefits. 8 (7), 384-394 (2015).
- Yao, J. J., et al. Direct Inpatient medical costs of operative treatment of periprosthetic hip and knee infections are twofold higher than those of aseptic revisions. Journal of Bone and Joint Surgery America. 103 (4), 312-318 (2021).
- Anatone, A. J., et al. Decreased implant survival is associated with younger patients undergoing total knee arthroplasty. HSS Journal. 18 (2), 290-296 (2022).
- Stone, B., Nugent, M., Young, S. W., Frampton, C., Hooper, G. J. The lifetime risk of revision following total knee arthroplasty : a New Zealand Joint Registry study. The Bone and Joint Journal. 104-B (2), 235-241 (2022).
- Chen, D., et al. Osteoarthritis: toward a comprehensive understanding of pathological mechanism. Bone Research. 5, 16044 (2017).
- Robinson, W. H., et al. Low-grade inflammation as a key mediator of the pathogenesis of osteoarthritis. Nature Review Rheumatology. 12 (10), 580-592 (2016).
- Perez-Garcia, S., et al. Profile of matrix-remodeling proteinases in osteoarthritis: impact of fibronectin. Cells. 9 (1), 40 (2019).
- Hashimoto, S., Ochs, R. L., Komiya, S., Lotz, M. Linkage of chondrocyte apoptosis and cartilage degradation in human osteoarthritis. Arthritis Rheumatology. 41 (9), 1632-1638 (1998).
- Natoli, R. M., Athanasiou, K. A. Traumatic loading of articular cartilage: Mechanical and biological responses and post-injury treatment. Biorheology. 46 (6), 451-485 (2009).
- Coleman, M. C., Brouillette, M. J., Andresen, N. S., Oberley-Deegan, R. E., Martin, J. M. Differential effects of superoxide dismutase mimetics after mechanical overload of articular cartilage. Antioxidants (Basel). 6 (4), 98 (2017).
- Goodwin, W., et al. Rotenone prevents impact-induced chondrocyte death. Journal of Orthopaedic Research. 28 (8), 1057-1063 (2010).
- Wolff, K. J., et al. Mechanical stress and ATP synthesis are coupled by mitochondrial oxidants in articular cartilage. Journal of Orthopaedic Research. 31 (2), 191-196 (2013).
- Delco, M. L., Bonnevie, E. D., Bonassar, L. J., Fortier, L. A. Mitochondrial dysfunction is an acute response of articular chondrocytes to mechanical injury. Journal of Orthopaedic Research. 36 (2), 739-750 (2018).
- Coleman, M. C., Ramakrishnan, P. S., Brouillette, M. J., Martin, J. A. Injurious loading of articular cartilage compromises chondrocyte respiratory function. Arthritis Rheumatology. 68 (3), 662-671 (2016).
- Bobinac, D., Spanjol, J., Zoricic, S., Maric, I. Changes in articular cartilage and subchondral bone histomorphometry in osteoarthritic knee joints in humans. Bone. 32 (3), 284-290 (2003).
- Coleman, M. C., et al. Targeting mitochondrial responses to intra-articular fracture to prevent posttraumatic osteoarthritis. Science Translational Medicine. 10 (427), eaan5372 (2018).
- Heraud, F., Heraud, A., Harmand, M. F. Apoptosis in normal and osteoarthritic human articular cartilage. Annals of Rheumatological Diseases. 59 (12), 959-965 (2000).
- Narez, G. E., Fischenich, K. M., Donahue, T. L. H. Experimental animal models of post-traumatic osteoarthritis of the knee. Orthopedic Reviews (Pavia). 12 (2), 8448 (2020).
- Fischenich, K. M., et al. Chronic changes in the articular cartilage and meniscus following traumatic impact to the lapine knee. Journal of Biomechanics. 48 (2), 246-253 (2015).
- Isaac, D. I., Meyer, E. G., Kopke, K. S., Haut, R. C. Chronic changes in the rabbit tibial plateau following blunt trauma to the tibiofemoral joint. Journal of Biomechanics. 43 (9), 1682-1688 (2010).
- Wei, F., et al. Post-traumatic osteoarthritis in rabbits following traumatic injury and surgical reconstruction of the knee. Annals of Biomedical Engineering. 50 (2), 169-182 (2022).
- Terracciano, R., et al. Quantitative high-resolution 7T MRI to assess longitudinal changes in articular cartilage after anterior cruciate ligament injury in a rabbit model of post-traumatic osteoarthritis. Osteoarthritis and Cartilage Open. 4 (2), 100259 (2022).
- Huang, K., Cai, H. L., Zhang, P. L., Wu, L. D. Comparison between two rabbit models of posttraumatic osteoarthritis: A longitudinal tear in the medial meniscus and anterior cruciate ligament transection. Journal of Orthopaedic Research. 38 (12), 2721-2730 (2020).
- Sun, Z. B., Peng, H. Experimental Study on the prevention of posttraumatic osteoarthritis in the rabbit knee using a hinged external fixator in combination with exercises. Journal of Investigative Surgery. 32 (6), 552-559 (2019).
- Gardner, M. J., et al. The incidence of soft tissue injury in operative tibial plateau fractures: a magnetic resonance imaging analysis of 103 patients. Journal of Orthopedic Trauma. 19 (2), 79-84 (2005).
- Dilley, J. E. B. . M. A., Roman, N., McKinley, T. O., Sankar, U. Post-traumatic osteoarthritis: A review of pathogenic mechanisms and novel targets for mitigation. Bone Reports. 18, 101658 (2023).
- Seol, D., et al. Effects of knockout of the receptor for advanced glycation end-products on bone mineral density and synovitis in mice with intra-articular fractures. Journal of Orthopedic Research. 36 (9), 2439-2449 (2018).
- Furman, B. D., et al. Joint degeneration following closed intraarticular fracture in the mouse knee: a model of posttraumatic arthritis. Journal of Orthopedic Research. 25 (5), 578-592 (2007).
- Glasson, S. S., Chambers, M. G., Van Den Berg, W. B., Little, C. B. The OARSI histopathology initiative - recommendations for histological assessments of osteoarthritis in the mouse. Osteoarthritis Cartilage. 18 Suppl 3, S17-S23 (2010).
- McCoy, A. M. Animal models of osteoarthritis: comparisons and key considerations. Veterinary Pathology. 52 (5), 803-818 (2015).
- Fening, S. D., Jones, M. H., Moutzouros, V., Downs, B., Miniaci, A. Method for Delivering a controlled impact to articular cartilage in the rabbit knee. Cartilage. 1 (3), 211-216 (2010).
- Leucht, F., et al. Development of a new biomechanically defined single impact rabbit cartilage trauma model for in vivo-studies. Journal of Investigative Surgery. 25 (4), 235-241 (2012).
- Vrahas, M. S., Smith, G. A., Rosler, D. M., Baratta, R. V. Method to impact in vivo rabbit femoral cartilage with blows of quantifiable stress. Journal of Orthopedic Research. 15 (2), 314-317 (1997).
- Borrelli, J., Burns, M. E., Ricci, W. M., Silva, M. J. A method for delivering variable impact stresses to the articular cartilage of rabbit knees. Journal of Orthopedic Trauma. 16 (3), 182-188 (2002).
- Milentijevic, D., Rubel, I. F., Liew, A. S., Helfet, D. L., Torzilli, P. A. An in vivo rabbit model for cartilage trauma: a preliminary study of the influence of impact stress magnitude on chondrocyte death and matrix damage. Journal of Orthopedic Trauma. 19 (7), 466-473 (2005).
- Alexander, P. G., et al. An In vivo lapine model for impact-induced injury and osteoarthritic degeneration of articular cartilage. Cartilage. 3 (4), 323-333 (2012).
- Bonitsky, C. M., et al. Genipin crosslinking decreases the mechanical wear and biochemical degradation of impacted cartilage in vitro. Journal of Orthopedic Research. 35 (3), 558-565 (2017).
- Bartley, K. A., Johnson, C. H. Human Infant pants for postoperative protection during social housing of new zealand white rabbits (Oryctolagus cuniculus). Journal of the American Association for Laboratory Animal Science. 58 (4), 510-516 (2019).
- Lillie, R. D., Fullmer, H. M. . Histopathologic technic and practical histochemistry. , (1976).
- Prophet, E., Mills, B., Arrington, J. B., Sobin, L. H. . Armed Forces Institute of Pathology: Laboratory Methods in Histotechnology. Washington DC: American Registry of Pathology. , (1992).
- Dilley, J. E., et al. CAMKK2 is upregulated in primary human osteoarthritis and its inhibition protects against chondrocyte apoptosis. Osteoarthritis and Cartilage. 31 (7), 908-918 (2023).
- Pritzker, K. P., et al. Osteoarthritis cartilage histopathology: grading and staging. Osteoarthritis Cartilage. 14 (1), 13-29 (2006).
- Christiansen, B. A., et al. Non-invasive mouse models of post-traumatic osteoarthritis. Osteoarthritis Cartilage. 23 (10), 1627-1638 (2015).
- Borrelli, J., Zaegel, M. A., Martinez, M. D., Silva, M. J. Diminished cartilage creep properties and increased trabecular bone density following a single, sub-fracture impact of the rabbit femoral condyle. Journal of Orthopaedic Research. 28 (10), 1307-1314 (2010).
- Borrelli, J., Silva, M. J., Zaegel, M. A., Franz, C., Sandell, L. J. Single high-energy impact load causes posttraumatic OA in young rabbits via a decrease in cellular metabolism. Journal of Orthopedic Research. 27 (3), 347-352 (2009).
- Borrelli, J., Zhu, Y., Burns, M., Sandell, L., Silva, M. J. Cartilage tolerates single impact loads of as much as half the joint fracture threshold. Clinical Orthopedics and Related Research. 426, 266-273 (2004).
- Karnik, S., et al. Decreased SIRT1 activity is involved in the acute injury response of chondrocytes to ex vivo injurious mechanical overload. International Journal of Molecular Sciences. 24 (7), 6521 (2023).
- Mevel, E., et al. Systemic inhibition or global deletion of CaMKK2 protects against post-traumatic osteoarthritis. Osteoarthritis Cartilage. 30 (1), 124-136 (2022).
Nachdrucke und Genehmigungen
Genehmigung beantragen, um den Text oder die Abbildungen dieses JoVE-Artikels zu verwenden
Genehmigung beantragenThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Alle Rechte vorbehalten