Se requiere una suscripción a JoVE para ver este contenido. Inicie sesión o comience su prueba gratuita.
Method Article
El aislamiento de la microglía Primaria cultivos mixtos de células gliales del tejido neonatal cerebro de rata
En este artículo
Resumen
Aislamiento de la microglía primaria a partir de la heterogeneidad celular del cerebro es esencial para investigar su papel en las dos condiciones fisiológicas y patológicas. Este protocolo describe un aislamiento mecánico y técnica mixta de cultivo celular que proporciona un alto rendimiento y alta pureza, viables células primarias microgliales para In vitro Estudio y aplicaciones posteriores.
Resumen
La microglía representan aproximadamente el 12% de la población celular total en el cerebro de los mamíferos. Mientras que las neuronas y astrocitos son considerados como los principales tipos de células del sistema nervioso, la microglía desempeñar un papel importante en la fisiología normal del cerebro mediante el control de los tejidos de los escombros y los agentes patógenos y el mantenimiento de la homeostasis en el parénquima a través de la actividad fagocítica 1,2. Microglia se activan durante una serie de condiciones lesiones y enfermedades, incluyendo enfermedad neurodegenerativa, lesión cerebral traumática, y la infección del sistema nervioso 3. Bajo estas condiciones de activación, la microglía aumentar su actividad fagocítica, sufren cambios morpohological y proliferativa, y secretan activamente las especies reactivas de oxígeno y nitrógeno, quimiocinas pro-inflamatorias y citoquinas, que a menudo la activación de un circuito paracrina o autocrina 4-6. A medida que estas respuestas microgliales contribuir a la patogénesis de la enfermedad en enfermedades neurológicas, la investigación se centró en microglia está garantizado.
Debido a la heterogeneidad celular del cerebro, es técnicamente difícil obtener suficiente material muestra microglial con alta pureza durante los experimentos in vivo. La investigación actual sobre las funciones neuroprotectoras y neurotóxica de la microglía requieren un método de rutina técnica para generar constantemente microglia pura y saludable con el rendimiento suficiente para su estudio. Se presentan, en texto y video, un protocolo para aislar microglia primaria pura a partir de cultivos gliales mixtos para una variedad de aplicaciones posteriores. Brevemente, esta técnica utiliza tejido cerebral disociada de crías de rata neonatal para producir cultivos mixtos de células gliales. Después de que los cultivos gliales mixtas alcanzar la confluencia, microglía primarios son mecánicamente aislado del cultivo mediante un breve duración de agitación. La microglia se siembran con alta pureza para el estudio experimental.
El principio y el protocolo de esta metodología han sidodescrito en la literatura 7,8. Además, las metodologías alternativas para aislar microglia primarias están bien descritos 9-12. Tejido cerebral homogeneizada puede ser separado por centrifugación en gradiente de densidad para producir primaria microglía 12. Sin embargo, la centrifugación es de longitud moderada (45 min) y puede causar daño celular y la activación, así como, causar enriquecido microglía y otras poblaciones celulares. Otro protocolo se ha utilizado para aislar microglía primaria en una variedad de organismos por prolongada (16 h) agitando mientras que en la cultura 9-11. Después de agitar, el sobrenadante se centrifuga medios para aislar microglía. Este método de aislamiento ya dos pasos también pueden perturbar la función microglial y la activación. Se utilizan principalmente el siguiente protocolo microglía aislamiento en nuestro laboratorio para un número de razones: (1) primaria microglía simular en la biología in vivo más fielmente que líneas celulares inmortalizadas roedores microglia, (2) Mecánico interrupción nominal minimiza disfunción potencial celular o activación, y (3) el rendimiento se puede obtener suficiente sin paso de los cultivos de células gliales mixtas.
Es importante señalar que este protocolo utiliza el tejido cerebral de crías de rata neonatal para aislar microglia y que el uso de las ratas viejas para aislar microglía puede afectar significativamente el rendimiento, estado de activación, y las propiedades funcionales de aislado microglía. Hay evidencia de que el envejecimiento está relacionado con la disfunción microglia, neuroinflamación aumentado y patologías neurodegenerativas, estudios previos han utilizado para ex vivo para adultos microglia para comprender mejor el papel de la microglía en las enfermedades neurodegenerativas, donde el envejecimiento es un parámetro importante. Sin embargo, ex vivo microglía no se pueden mantener en cultivo durante períodos prolongados de tiempo. Por lo tanto, mientras que este protocolo se extiende la vida de la microglía primaria en cultivo, se debe señalar que la microglía comportan differently de los adultos microglia y en estudios in vitro deben ser cuidadosamente considerados cuando se traduce a un ajuste en vivo.
Protocolo
1. La disección de los tejidos neonatal cerebro de rata
- 15 L-medios de comunicación acondicionado Chill Leibovitz (Leibowitz L-15 + BSA al 0,1% + 1% Pen / Strep) a 4 ° C. Medios calientes de cultivo (DMEM + 10% de SFB + 1% de penicilina / estreptomicina) a 37 ° C. Preparar 4 60x15 mm placas de Petri con 4-5 ml de los 15 L-acondicionado medios de comunicación sobre el hielo. Esterilice todos los instrumentos quirúrgicos con un 100% de etanol.
- Enjuague los cachorros recién nacidos P2 rap con el 70% de etanol. (Crías de rata neonatal edades comprendidas entre P1-P5 se puede utilizar en este protocolo.)
- Rápidamente decapitar a una cría de rata con tijeras estériles y colocar la cabeza de inmediato en etanol al 70%. Repetir para un total de 5 crías de rata luego transferir las cabezas en solución salina.
- Retire los cerebros enteros de los jefes y colocarlos en una placa de Petri con 4 - 5 ml de solución de L-15 (Leibowitz L-15 + BSA al 0,1% + 1% Pen / Strep) en el hielo.
- Repita los procedimientos de 1,2 - 1,4 para el resto de los cachorros en la camada.
- Retire las meninges del cerebro y transferir el destejido cerebral IRED (es decir, la corteza, el cerebelo, el cerebro entero, etc) en una nueva placa de Petri con 4-5 ml de solución de L-15 (Leibowitz L-15 + BSA al 0,1% + 1% Pen / Strep) en el hielo.
2. Preparación de la población mixta de células gliales
- Sin dañando los tejidos cerebrales con unas tijeras o una cuchilla, la transferencia del tejido con una pipeta de 10 ml a un estéril de 50 ml tubo cónico.
- Cónico de centrífuga a 2.500 RCF durante 5 min a 4 ° C.
- Aspirar el sobrenadante. Añadir 4-5 ml de frescos 15 L-medios de comunicación (Leibowitz L-15 + BSA al 0,1% + 1% Pen / Strep).
- Pipetear tejido hacia arriba y hacia abajo 10 veces con una pipeta estéril de 10 ml.
- Colocar un filtro de células (100 poros micras) en un tubo cónico fresco 50 ml. Tejido pipeta arriba y hacia abajo una vez con una pipeta estéril de 5 ml y con la pipeta a ras de la filtro de células, dispensar el material a través del filtro de células en el tubo cónico.
- Limpie el filtro de células con 4-5 ml de frescos 15 L-medios de comunicación (Leibowitz L-15 + 0,1% BSUna pluma + 1% / Strep).
- Centrífuga cónico con células tensas a 2.500 RCF durante 5 min a 4 ° C.
3. Revestimiento y mantenimiento de cultivos mixtos de células gliales
- Para cada cerebro procesa las crías de rata, preparar 1 T-75 frascos estériles mediante la adición de 12 ml de medio de cultivo (DMEM + 10% de SFB + 1% de penicilina / estreptomicina) en cada frasco.
- Aspirar el sobrenadante de las células sedimentadas y añadir 5-6 ml de medio de cultivo para el pellet celular. Pipetear arriba y hacia abajo 10 veces con una pipeta de 10 ml.
- Transferir un volumen igual de suspensión de células en cada matraz T-75.
- Incubar los frascos en un 5% de CO 2 incubadora a 37 ° C durante un total de 1-3 semanas.
- Los matraces se incubaron primero durante 5 días, y el quinto día, reemplazar los medios de cultivo en cada matraz con 12 ml de medio fresco y volver a la incubadora. Luego, cada 3 días, vuelva a colocar los medios de comunicación acondicionado en cada frasco con 12 ml de medio fresco para lograr la confluencia. Esto se debe hacerne muy cuidadosamente sin tocar el fondo de los frascos donde las células se adhieren.
4. El aislamiento y forro de Primaria microglía
- Después de cultivos mixtos gliales son completamente confluente, eliminar matraces de la incubadora y cubrir las tapas matraz con parafilm para impedir el intercambio de gases con el aire ambiental.
- Agitar frascos a 100 rps (compañero de laboratorio SI-600, Jeio Tech) durante 1 hora a 37 ° C.
- Recoger los medios de comunicación de todos los frascos con una pipeta de 10 ml sin alterar la capa de los astrocitos en la superficie del frasco. Coloque el material en tubos de 50 ml cónicos. Añadir medio fresco a los frascos y frascos de retorno a la incubadora.
- Centrifugar los tubos cónicos a 2.500 RCF durante 5 min a 4 ° C.
- Aspirar el sobrenadante de todos los tubos cónicos. Gránulos de las células son células de la microglia alta pureza. Volver a suspender las pastillas en 1 ml de revestimiento microglia los medios de comunicación (DMEM + FES 10% + 1% de penicilina / estreptomicina).
- Cuente con la densidad celular en los medios de comunicación que utilizan resuspendidasun hemocitómetro.
- Añadir un volumen apropiado de los medios de comunicación de enchapado microglia para lograr un 2 x 10E5 células por ml de densidad. Placa como adecuado para el análisis experimental.
- Permita que la microglia para unir toda la noche.
5. Los resultados representativos
El protocolo descrito anteriormente resultados en cultivos primarios de alta pureza microglía. Según lo determinado por inmunohistoquímica para un marcador celular de macrófagos / microglia específico (Iba1), enchapados en culturas microglia son> 90% de pureza (Figura 2). Además, la tinción de los marcadores de células de astrocitos, oligodendrocitos y neuronas específicas demuestra la mínima contaminación (Figura 2). Después de establecer cultivos mixtos de células gliales, la microglía puede ser aislado por agitación hasta 4 veces sucesivas. El primer aislamiento de microglia rendirá aproximadamente 2.2 x 106 células / ml o aproximadamente 9 millones de células por cada 10 frascos y el rendimiento esperado disminuye con cada sucesiva shake. Microglia aisló por este método se han utilizado con éxito para investigar la capacidad de fagocitosis, funciones tales como la producción de óxido nítrico, y la toxicidad neuronal (Figura 3) 13-14.
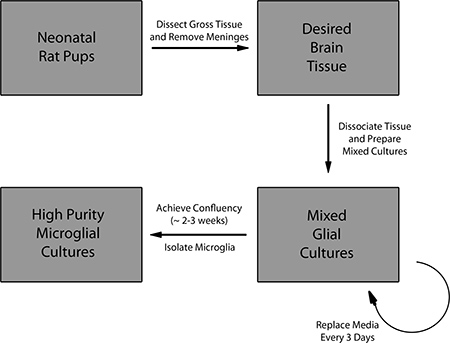
Figura 1. Visión general del protocolo para la preparación de cultivos mixtos de células gliales y el aislamiento de la microglía primaria.
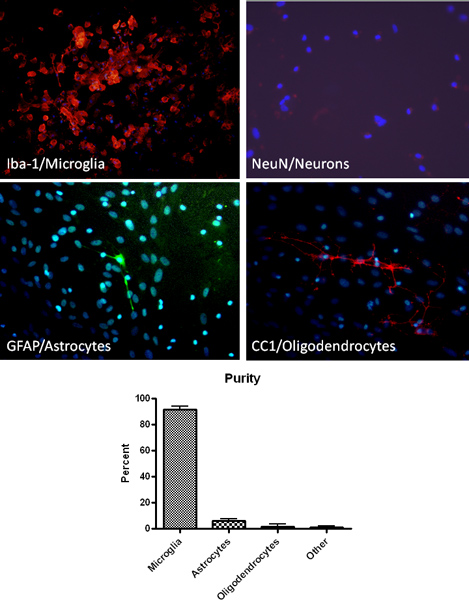
Figura 2. El aislamiento de la microglía de alta pureza que se han verificado mediante análisis de inmunohistoquímica con la microglía (IBA-1, roja), astrocitos (GFAP, verde), las neuronas (NeuN, rojo) y oligodendrocitos (CC1, rojo) de marcadores específicos. La tinción de ADN de las células en cultivo por DAPI (azul) también se muestra.
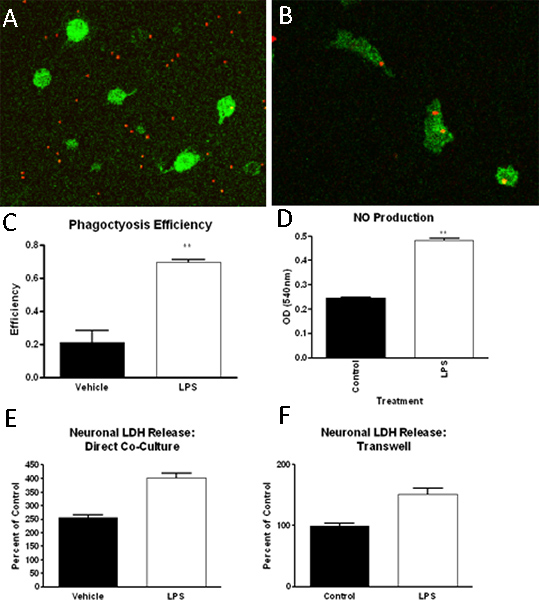
Figura 3. Microglia aislado en el método descricama se han utilizado en una serie de ensayos, incluyendo, pero no se limitan a, los ensayos de fagocitosis, ensayos de la función y los estudios de neurotoxicidad. En estos estudios, se ha encontrado que la microglía (IBA-1 positivo, verde), cuando se expone a controlar (A) o LPS (B) medios tratados, aumentar su fagocitosis de marcadas fluorescentemente perlas de látex (rojo), que pueden ser cuantificados ( C). Además, el LPS (1ng/ml) el tratamiento puede aumentar la producción de óxido nítrico en la microglía (D). Por último, tanto a través de transwell inserto separado o directa culturas microglia-neuronas, hemos encontrado que la microglia incubadas con LPS puede inducir la muerte celular neuronal, medido por la lactato deshidrogenasa (LDH) liberación (E, F).
Discusión
Si bien este protocolo se utiliza rutinariamente para producir la microglía pura y saludable para los experimentos de investigación, la consideración cuidadosa de los aspectos técnicos durante las partes críticas del procedimiento minimizar la variabilidad en la microglia aislado. En primer lugar, durante la disección del tejido cerebral de crías de ratas neonatales, trabajando en el momento oportuno es necesario para minimizar el daño hipóxico isquémica, y en el tejido. Sin embargo, también es importante eli...
Divulgaciones
No hay conflictos de interés declarado.
Agradecimientos
Financiado por el programa intramuros de la Universidad de Servicios Uniformados.
Materiales
| Name | Company | Catalog Number | Comments |
| Nombre del reactivo | Empresa | Número de catálogo | Comentarios |
| 60 mm x 15 mm placas de Petri | Fisher de la marca | 0875713A | |
| Afiladas tijeras de disección | Herramientas de Bellas Ciencia | 14094-11 | |
| Dumont # 7b fórceps estándar consejos, curvas, 11cm | Herramientas de Bellas Ciencia | 11270-20 | |
| Dumont # 5 fórceps estándar consejos, rectas, 11 cm | Herramientas de Bellas Ciencia | 11251-10 | |
| 50 ml tubos de centrífuga cónicos | VWR | 89039-656 | |
| 5 ml pipetas serológicas | Grenier Bio One | 606180 | |
| 10 ml serológicas pipetas | Grenier Bio One | 607180 | |
| 100 micras de nylon estéril filtro de células | Halcón | 35-2360 | |
| 75 cm 2 frascos de cultivo de tejidos | Corning | 430641 | |
| Medio esencial mínimo de Dulbecco (DMEM) | Gibco (Invitrogen) | 31053-028 | |
| Leibovitz medio L-15 | Gibco (Invitrogen) | 11415064 | |
| Suero bovino fetal | Gibco (Invitrogen) | 16000-036 | |
| Fetal suero equino | Pescador | SH3007402 | |
| La penicilina-estreptomicina | Gibco (Invitrogen) | 15140163 | |
| 100% de etanol | La Compañía Warner Graham | 64-17-5 | |
| Solución salina tamponada con fosfato, 10X, pH 7,4 | De calidad biológica, inc. | 119-069-131 | 1X en agua destilada estéril |
| Bolsas de bioseguridad | VWR | 14220-028 | |
| Hemocitómetro | Hausser Científico | 1492 | |
| 6-y las placas de cultivo celular con superficie Cellbind | Corning | 3335 |
Referencias
- Ransohoff, R. M., Perry, V. H. Microglial physiology: unique stimuli, specialized responses. Annu. Rev. Immunol. 27, 119-145 (2009).
- Raivich, G., Bohatschek, M., Kloss, C. U., Werner, A., Jones, L. L., Kreutzberg, G. W. Neuroglial activation repertoire in the injured brain: graded response, molecular mechanisms and cues to physiological function. Brain Res. Brain Res. Rev. 30, 77-105 (1999).
- Loane, D. J., Byrnes, K. R. Role of microglia in neurotrauma. Neurotherapeutics. 7, 245-265 (2010).
- Glass, C. K., Saijo, K., Winner, B., Marchetto, M. C., Gage, F. H. Mechanisms underlying inflammation in neurodegeneration. Cell. 140, 918-934 (2010).
- Pocock, J. M., Liddle, A. C. Microglial signalling cascades in neurodegenerative disease. Prog. Brain Res. 132, 555-565 (2001).
- Block, M. L., Hong, J. S. Chronic microglial activation and progressive dopaminergic neurotoxicity. Biochem. Soc. Trans. 35, 1127-1132 (2007).
- Barger, S. W., Basile, A. S. Activation of microglia by secreted amyloid percursor protein evokes release of glutamate by cystine exchange and attenuates synpatic function. J. Neurochem. 76, 846-854 (2001).
- Ni, M., Aschner, M. Neonatal rat primary microglia: isolation, culturing, and selected applications. Curr. Protoc. Toxicol. Chapter 12, Unit 12.17 (2010).
- Hassan, N. F., Rifat, S., Campbell, D. E., McCawley, L. J., Douglas, S. D. Isolation and flow cytometric characterization of newborn mouse brain-derived microglia maintained in vitro. J. Leukoc. Biol. 50, 86-92 (1991).
- Hassan, N. F., Prakash, K., Chehimi, J., McCawley, L. J., Douglas, S. D. Isolation and characterization of newborn rabbit brain-derived microglia. Clin. Immunol. Immunopathol. 59, 426-435 (1991).
- Hassan, N. F., Campbell, D. E., Rifat, S., Douglas, S. D. Isolation and characterization of human fetal brain-derived microglia in in vitro culture. Neuroscience. 41, 149-158 (1991).
- Frank, M. G., Wieseler-Frank, J. L., Watkins, L. R., Maier, S. F. Rapid isolation of highly enriched and quiescent microglia from adult rat hippocampus: immunophenotypic and functional characteristics. J. Neurosci. Methods. 151, 121-130 (2006).
- Byrnes, K. R., Stoica, B., Loane, D. J., Riccio, A., Davis, M. I., Faden, A. I. Metabotropic glutamate receptor 5 activation inhibits microglial associated inflammation and neurotoxicity. Glia. 57, 550-560 (2009).
- Loane, D. J., Stoica, B. A., Pajoohesh-Ganji, A., Byrnes, K. R., Faden, A. I. Activation of metabotropic glutamate receptor 5 modulates microglial reactivity and neurotoxicity by inhibiting NADPH oxidase. J. Biol. Chem. 284, 15629-15639 (2009).
Reimpresiones y Permisos
Solicitar permiso para reutilizar el texto o las figuras de este JoVE artículos
Solicitar permisoThis article has been published
Video Coming Soon
ACERCA DE JoVE
Copyright © 2025 MyJoVE Corporation. Todos los derechos reservados