Method Article
Irritación de los ojos de prueba (IET) para la identificación del peligro de los ojos: Irrita los productos químicos que utilizan Reconstruido humana Córnea-como epitelial (RHCE) Modelo de Tejidos
En este artículo
Resumen
Hemos desarrollado un ensayo de irritación ocular que utiliza un modelo de tejido tridimensional epitelial-córnea como humana reconstruida (RHCE). La prueba es capaz de discriminar entre irritante ocular y materiales corrosivos (SGA Categorías 1 y 2 combinados) y aquellos que no requieren etiquetado (GHS No Categoría).
Resumen
Para cumplir con la Enmienda Séptima a la legislación Directiva sobre cosméticos y de REACH de la UE de la UE, se necesitan métodos alternativos sin animales validados para la evaluación fiable y exacto de toxicidad ocular en el hombre. Para hacer frente a esta necesidad, hemos desarrollado un ensayo de irritación ocular (IET), que utiliza un modelo tridimensional reconstruida humano-como córnea epitelial (RHCE) tejido que se basa en las células humanas normales. El IET es capaz de separar los irritantes y corrosivos oculares (SGA Categorías 1 y 2 combinados) y aquellos que no requieren etiquetado (GHS No Categoría). La prueba utiliza dos protocolos separados, uno diseñado para productos químicos líquidos y un segundo protocolo, similar para artículos de prueba sólidos. El modelo de predicción EIT utiliza un único período de exposición (30 min para líquidos, 6 hr para los sólidos) y una sola viabilidad del tejido de corte (60,0% según se determina mediante el ensayo de MTT). Basado en los resultados para 83 productos químicos (44 líquidos y sólidos 39) IET logra 95,5 / 68,2 / 81,8% y sensitivity / especificidad y la precisión (SS & A) para líquidos, 100,0 / 68,4 / 84,6% y SS & A para sólidos y 97,6 / 68,3 / 83,1% y para el general de las SS & A. El EIT contribuirá significativamente a clasificar el potencial de irritación ocular de una amplia gama de productos químicos líquidos y sólidos sin el uso de animales para satisfacer los requisitos de ensayos reglamentarios. El método EpiOcular IET se implementó en 2015 en las Directrices de la OCDE como TG 492.
Introducción
Los productos de consumo tales como cosméticos, detergentes y productos de limpieza para el hogar incluyen una variedad de sustancias químicas que pueden provocar lesiones graves si entran en contacto con los ojos. Por lo tanto, las pruebas de estos agentes para la irritación de los ojos es requerido por las agencias reguladoras de Estados Unidos y de la UE para garantizar la seguridad de los consumidores 1. Una evaluación del potencial de irritación de los ojos de las mezclas y formulaciones es también un requisito para cumplir con REACH (Registro, Evaluación, Autorización y Restricción de Sustancias Químicas) legislación para el etiquetado de los ingredientes cosméticos bajo la Directiva sobre cosméticos de la UE para el transporte de productos químicos, y por el etiquetado de los pesticidas y productos para el hogar 2. Actualmente, las agencias reguladoras requieren la evaluación del peligro ocular mediante el Sistema Globalmente Armonizado de Clasificación y Etiquetado de Productos Químicos (GHS) 3. SGA se basa principalmente en la prueba de irritación ocular de Draize, el ensayo de irritación ocular más utilizado en las que las sustancias extrañas y mixtures se introducen directamente en el saco conjuntival del ojo del conejo 4. De acuerdo con la clasificación del SGA, SGA Categoría 1 (corrosivos oculares) se refiere a las sustancias que causan lesión inicial severo a los tejidos oculares o daño grave al ojo y la visión que no es totalmente reversible en los 21 días después de la exposición 3.5. GHS categoría 2 se refiere a las sustancias que producen cambios significativos en el ojo que son totalmente reversibles en los 21 días de exposición. Las sustancias de ensayo que no son corrosivos o irritantes se conocen como GHS Sin categoría.
Durante más de 40 años, la prueba del ojo del conejo de Draize ha sido criticado por su falta de reproducibilidad, la sobreestimación de las respuestas humanas, y el uso de animales vivos 5-8. Estas preocupaciones han alentado a muchas propuestas de refinamiento, reducción y sustitución de la prueba in vivo 9. La necesidad de alternativas sin animales validados se fortaleció aún máspor la adopción de la Séptima Enmienda de la Directiva sobre cosméticos, que prohibió el uso de animales en la evaluación de la seguridad de los productos cosméticos (en 2005) y los ingredientes (en 2009) 2.
Desde 1996, el modelo de tejido-córnea como reconstruido ha sido ampliamente utilizado por la industria cosmética para evaluar el potencial de irritación de las materias primas, formulaciones a base de tensioactivos y mezclas que están diseñados para su uso en compuesto, o en las proximidades de, el ojo 10-13. El uso del modelo de tejido RHCE permite la aplicación tópica directa del material de prueba sobre la superficie del tejido en su forma nativa, sin diluir. De esta manera, las formulaciones no solubles en agua pueden ser probados sin diluir con disolventes. En respuesta a la EURL de CEVMA (Centro Europeo Laboratorio de Referencia de la Unión Europea para la Validación de Métodos Alternativos) solicitud de un método ampliamente aplicable, directa y económica del Test de irritación ocular (IET) que utiliza un single tiempo de exposición y es capaz de separar los irritantes oculares y corrosivos con materiales que no requieren etiquetado fue desarrollado (Figura 1) 14. Basándose en los resultados para 83 productos químicos (44 líquidos y 39 de sólidos), el EIT logra 95,5 / 68,2 / y 81,8% de sensibilidad / especificidad y exactitud (SS & A) para líquidos, 100,0 / 68,4 / y 84,6% SS & A para sólidos, y 97,6 / 68,3 / y 83,1% para el general de las SS & A.
En 2007, un multi-laboratorio de estudio de pre-validación patrocinado por Cosméticos Europa (anteriormente Colipa) bajo los auspicios de la CEVMA EURL evaluó la relevancia y fiabilidad del IET con el objetivo de llevar a validación formal 15. En este estudio, se realizaron 298 ensayos independientes en siete laboratorios independientes. Los resultados del estudio demostraron acuerdo de 99,7% en la predicción con bajos coeficientes de variación en todos los laboratorios participantes 15. Como resultado, en 2010 el protocolo EIT entró en una EURL formales CEVMAprograma de validación. El estudio de validación utilizado 104 sustancias químicas de prueba codificadas, incluidas las sustancias individuales y mezclas químicas, para lo cual en vivo los datos de referencia (Draize datos irritación de los ojos) estaban disponibles. Basado en el éxito de este trabajo, una guía de proyecto de ensayo de la OCDE se presentó en 2014. Se prevé que el IET contribuirá de manera significativa a la clasificación del potencial de irritación ocular de una amplia gama de materiales de acuerdo con la clasificación y el etiquetado del sistema SGA de la ONU.
Protocolo
1. Preparación de RHCE Tejidos para Tratamiento - Día 0
- Una vez recibido el kit epitelial-córnea como humana comercial (RHCE), compruebe que todos los componentes del kit para la integridad (para detalles del kit ver Standard Kit de ensayo Componentes (Tabla 1) y los equipos y materiales necesarios para realizar el ensayo EIT (Tabla 2). En la fecha de recepción, equilibre los tejidos (en su envase de 24 pocillos de envío) a la temperatura ambiente durante 15 min.
| Cantidad | Reactivo | Condiciones | Fuente | Descripción | Fecha de caducidad |
| 1 | Sellado placa de 24 pocillos de tejidos EpiOcular (OCL-200) | 2.8 ° C | MatTek | Contiene 24 tissues de cultivo celular inserta, paquete en agarosa | 72 horas |
| 1 botella, 200 ml | EpiOcular Medio de Ensayo (OCL-200-ASY) | 2.8 ° C | MatTek | Medio basado en DMEM | 21 días |
| 1 botella, 100 ml | Ca ++ Mg ++ -Free Dulbecco-PBS (DPBS) | RT | Sigma-Aldrich, D5652, o equiv. | Se utiliza para el lavado insertos | 1 año |
| 4 | 6 pocillos | RT | Halcón | Se utiliza para el mantenimiento de los tejidos durante el protocolo de ensayo | N / A |
| 2 | 12 pocillos | RT | Halcón | Se usa durante protocolo de ensayo | N / A |
| 2 | 24 pocillos | RT | Halcón | Se utiliza para realizar el ensayo de MTT | N / A |
| 1 vial, 0,5 ml | Acetato de metilo (CAS # 79-20-9) | RT | Sigma-Aldrich, Cat # 186325 | Se utiliza como PC en el ensayo | 1 mes |
Tabla 1: estándar de ensayo Componentes del kit.
| / Material | Necesario para: |
| Incubador humidificado (37 ± 1 ° C, 5 ± 1% de CO 2, 90 ± 10% de humedad) | La incubación de los tejidos antes y durante los ensayos |
| Campana de flujo laminar | Trabajo seguro en condiciones estériles |
| Bomba de vacío (opcional) | Aspiración de las soluciones de mediano y |
| Lector de placas fotómetro (para placas de 96 pocillos) | Lectura OD |
| Agitador de placas | Extractoion de formazán |
| Pinzas estériles, con bordes romos | Manejo de inserciones de tejido |
| Cronómetros | Calendario de aplicación de materiales de prueba y otras medidas cronometradas en el protocolo |
| Baño de agua (37 ± 1 ° C) | Medios de calentamiento y solución de MTT |
| Mortero y maja | Molienda sólidos granulares |
| Pipeta de desplazamiento positivo (50 l) | Aplicación de materiales y suspensiones viscosas y semi-sólidas |
| Pipetas ajustables (200 l-2 ml) | Aplicación de materiales líquidos, medio de ensayo MTT y |
| Consejos esterilizados previamente (200 ly 20 l), Rainin Cat # HR-200F y HR-20F (o equivalente) | Aplicación de materiales líquidos, medio de ensayo MTT y |
| Consejos de orificio ancho pre-esterilizados (250 l), Rainin Cat # HR-250WS (o equivvalente) | Aplicación de materiales y suspensiones viscosas y semi-sólidas |
| 8 oz / 220 ml espécimen contenedores, Falcon Cat # 3540200 (o equivalente) | Enjuague tejidos |
| Jeringas estériles de un solo uso (por ejemplo, 1 ml tuberkulin jeringa Omnifix-F, B. Braun Melsungen AG, Cat. No. 9161406V) | Entrega de ~ 50 mg materiales sólidos (opcional) |
| Ted Pella micro espátula / cuchara, Ted Pella Inc., Cat # 13504 (o equivalente, agudo cuchara o hueso cureta, por ejemplo, Aesculap, No: FK 623) | Entrega de ~ 50 mg materiales sólidos |
| Ca ++ y Mg ++ salina tamponada con fosfato de Dulbecco libre (Ca ++ Mg ++ Free-DPBS): Sigma-Aldrich, Cat # D5652 (o equivalente) | Enjuague tejidos durante el ensayo |
| Estéril grado cultura del agua desionizada, el tejido (calidad biológica o equivalente) | Usar como NC |
| Placas de 96 pocillos de fondo plano, Falcon (o equivalente) | Para la lectura de OD |
| Swaps de punta de algodón (estéril) | Para el secado de la superficie del tejido (opcional) |
| Cinta adhesiva o Parafilm | Cubrir las placas durante la extracción de formazán |
| Kit de ensayo de MTT-100 | Contiene extracto MTT-tetrazolio azul de tiazolilo Bromuro de reactivo (Sigma # M-5655) e isopropanol. |
Tabla 2: Equipamiento y materiales necesarios para realizar el IET.
- En condiciones estériles, abrir la bolsa de plástico que contiene la placa de 24 pocillos con los tejidos RHCE y retire la gasa estéril. Inspeccione todos los tejidos de las burbujas de aire entre el gel de agarosa y se inserte. No utilice las culturas con las burbujas de aire bajo la cobertura de inserción> 50% del área de inserción, tejidos defectuosos o tejidos whi ch están completamente cubiertos de líquido.
- Etiquetar las placas de 6 pocillos con el artículo de prueba o códigos de control y los tiempos de exposición. Alícuotas de 1,0 ml de medio de ensayo (suministradas con el kit), pre-calentado a aproximadamente 37 ° C, en los pocillos de placas de 6 pocillos pre-etiquetados.
- Utilice pinzas estériles para eliminar cada inserto que contiene el tejido RHCE y colocar el inserto en la placa de 6 pocillos etiquetados. Durante este paso, eliminar cualquier envío de agarosa restante que se adhiere a los lados exteriores de la pieza de inserción mediante transferencia suave sobre papel de filtro estéril. Suelte las burbujas de aire atrapadas debajo de las inserciones.
- Preincubarlos los tejidos RHCE en las placas de 6 pocillos a las condiciones de cultivo estándar (SCC, atmósfera húmeda con 5 ± 1% de CO 2 a 37 ± 1 ° C) durante 1 hora.
- Después de 1 hora, sustituya el medio de ensayo con 1,0 ml de medio de ensayo fresco precalentado a 37 ° C e incubar los tejidos RHCE en condiciones de SCC (durante la noche = O / N) (16-24 h).
- Después de la O / N de incubación, se aplican 20 l de Ca 2 + 2 + Mg salina tamponada con fosfato de Dulbecco exento-(DPBS, siempre) utilizando un dispositivo de pipeta apropiada. Si el DPBS no se propaga a través de los tejidos, golpee suavemente el inserto en la placa para asegurar que los DPBS moja toda la superficie del tejido.
- Incubar los tejidos RHCE en SCC de 30 ± 2 min.
Nota: Este paso es necesario para la hidratación del tejido y para imitar las condiciones in vivo.
3. material de ensayo Procedimientos de Exposición
- Aplicar cada artículo de prueba y los controles de duplicar tejidos RHCE (n = 2). El procedimiento de ensayo artículo de dosificación es diferente para líquidos y sólidos. Tópicamente aplicar 50 l de artículos de prueba líquidos utilizando una pipeta. El tiempo de exposición para los líquidos es de 30 min. Aplicar 50 mg de artículos de prueba sólidos usando una cucharada nivelado (calibrado para contener 50 mg de cloruro de sodio). El extiempo de exposición para los sólidos es de 6 horas.
Nota: Los líquidos se definen como sustancias fluidas (por ejemplo, líquidos, geles y cremas) que pueden ser aplicados utilizando un dispositivo de pipeta. Los sólidos se definen como sustancias no fluido (por ejemplo, polvos, materiales resinosos o cerosa) que no se pueden aplicar utilizando una pipeta.- Si el estado físico de los artículos de prueba no es fácil de determinar, coloque los viales con artículo de prueba en un baño de agua durante 15 minutos (37 ° C). Siga el protocolo IET para líquidos para esos artículos de prueba que licuan a 37 ° C.
- Utilice una pipeta de desplazamiento positivo para materiales particularmente viscosos.
- Dosis el control negativo y el control positivo primero y luego dosificar los artículos de prueba.
- Aplicar 50 l de control negativo (NC) y el control positivo (PC) a los tejidos RHCE utilizando una pipeta estándar. La NC es agua desionizada estéril; la PC es el acetato de metilo (CAS # 79-20-9). Aplique la NC y PC durante 30 minutos cuando la pruebaing artículos de prueba líquidos y durante 6 horas al probar artículos de prueba sólidos.
4. Pruebe el artículo Exposición - Día 1
- Para el tratamiento de artículos de prueba líquidos, seguir el horario de tiempo dado en la Tabla 3. Deja intervalos de 1 min entre aplicaciones de cada artículo de prueba para garantizar la igualdad de exposición para todos los tejidos.
- Después de que el 30 ± 2 min DPBS pre-tratamiento, aplicar tópicamente 50 l de NC y PC, y cada artículo de prueba líquido por vía tópica en los tejidos RHCE utilizando un dispositivo de pipeteo apropiado.
- Aplicar 50 l de artículo de prueba líquido directamente sobre el tejido para cubrir la superficie superior. Cortar el punto de la punta de pipeta estrecha para ensanchar el orificio para materiales viscosos. Para los materiales muy viscosos, aplicar el artículo de prueba a un dispositivo de dosificación (un cilindro de cabeza plana de diámetro ligeramente menor que el diámetro interior del inserto de tejido o un marcador de plástico), invertir la dosificación device y colóquelo sobre el tejido para que el artículo de ensayo uniformemente contacto con la superficie del tejido.
- Si artículo de prueba no se propaga a través del tejido, golpee suavemente el inserto para asegurarse de que se extiende sobre toda la superficie del tejido. Difusión mecánica de los artículos de prueba (por ejemplo, con una punta de pipeta), no se recomienda ya que puede dañar los tejidos.
- Incubar los tejidos en SCC de 30 ± 2 min.
- Para el tratamiento de artículos de prueba maciza - Día 1, seguir el horario de tiempo dado en la Tabla 4 Deja intervalos de 2 min entre aplicaciones de cada artículo de prueba para garantizar la igualdad de exposición para todos los tejidos..
- Después de que el 30 ± 2 min DPBS pre-tratamiento, aplicar 50 l de NC y PC tópicamente sobre los tejidos RHCE utilizando un dispositivo de pipeteo apropiado.
- Para la aplicación del artículo de prueba sólido, quite los insertos (n = 2) desde el pozo y colocarlos sobre una superficie estéril (por ejemplo, la tapa de la mañanaplaca ultiwell) para evitar un artículo de prueba se derrame en el medio.
- Con una cuchara nivelada, aplique tópicamente aproximadamente 50 mg del artículo de prueba en la superficie del tejido; asegurarse de que la superficie del tejido está completamente cubierta por el artículo de prueba. Si el artículo de prueba no se propaga a través del tejido, agitar el inserto suavemente de un lado a otro para asegurarse de que el tejido está completamente cubierta por el artículo de prueba. Difusión mecánica de los artículos de prueba (por ejemplo, con una punta de pipeta), no se recomienda ya que puede dañar los tejidos.
- Si es necesario, moler polvos cristalinos con un mortero y mano de mortero para garantizar un mejor contacto entre el artículo de prueba y el tejido.
- Como alternativa, coloque polvos directamente sobre el cultivo de tejidos dentro de la inserción mediante el uso de una jeringa de 1 ml con la cabeza cortada. Polvos cosas en la jeringa cuando el émbolo se dibuja hacia atrás y luego se aplican al presionar el émbolo hacia abajo.
- Si la pared exterior del inserto es contaminated por ejemplo, polvos, limpie las partículas con una gasa estéril.
- Después de la dosificación, devolver los tejidos a los 6 y placas que contienen medio de cultivo y se incuba a SCC durante 6 h ± 15 min.
5. Enjuague
- Preparar un conjunto de tres vasos limpios (150 ml de capacidad) por artículo de prueba y llenar cada uno de ellos con 100 ml de DPBS. Para cada artículo de prueba, utilizar un conjunto diferente de tres vasos de precipitados.
- Al final de la exposición min 30 ± 2 para materiales líquidos o 6 hr 15 min ± exposición para materiales sólidos, retirar y desechar el dispositivo de dosificación si se ha utilizado.
- Levantar los insertos que contienen el tejido RHCE fuera del medio agarrando el borde superior de la 'cuello' de plástico con unas pinzas finas. Utilice pinzas curvas para facilitar el manejo y decantación. Enjuague los tejidos dos a la vez mediante la celebración de las inserciones duplicadas entre sí por sus collares utilizando fórceps. Tenga cuidado de not dañar los tejidos con los fórceps.
- Decantar los artículos de prueba o controles de la superficie del tejido sobre un material absorbente limpio (toallas de papel, gasa, etc.)
- Sumerja los insertos en el primer vaso de DPBS, remolino en un movimiento circular en el DPBS durante aproximadamente 2 segundos, levante los insertos para que se llenan sobre todo con DPBS, y decantar el líquido de nuevo en el vaso de precipitados. Repita este proceso tres veces en el primer vaso de precipitados.
- Enjuagar los insertos en el segundo y tercer vasos de precipitados de DPBS tres veces cada uno de la misma manera.
- Decantar cualquier líquido residual en la pieza de inserción sobre el material absorbente. Gire la inserción a un ángulo de 45 ° aproximadamente (extremo abierto hacia abajo) y toque el labio superior con el material absorbente.
Nota: Si no es posible eliminar todo el material de prueba visible, no más lejos de enjuague se debe hacer para evitar el daño a los tejidos debido a una manipulación excesiva.
6. Post-remojo
- Después de enjuagar,sumerja inmediatamente tejidos en 5 ml de medio de ensayo previamente calentado a temperatura ambiente en una placa de 12 pocillos pre-etiquetados.
- Incubar los tejidos de 12 ± 2 min para materiales líquidos o 25 ± 2 min para materiales sólidos sumergidos en RT para facilitar la eliminación de cualquier artículo de prueba residual.
7. Post-incubación
- Al final de la Post-Soak periodo de inmersión, se decanta el medio de ensayo de los tejidos y secar los insertos en un material absorbente.
- La transferencia de los insertos en la placa de 6 pocillos pre-marcado que contiene 1 ml de calentamiento medio de ensayo.
- Incubar los tejidos de 120 ± 15 min a SCC de los materiales de ensayo líquidos.
- Incubar los tejidos de 18 ± 0,25 horas a SCC para materiales de prueba sólidos.
8. MTT ensayo de viabilidad - Día 1 (Protocolo de líquidos) y el Día 2 (Protocolo de sólidos)
- Realizar el ensayo MTT después de la post-incubación de 12077; 15 min para líquidos y 18 ± 0,25 h para sólidos, respectivamente.
- Preparar 1,0 mg / ml de solución de MTT y 0,3 ml de alícuota de la solución en cada pocillo de una placa de 24 pocillos pre-marcado.
- Utilice el kit MTT comercial (Tabla 5):
- 2 horas antes de su uso, descongele el concentrado MTT a RT. Combinar 2 ml del concentrado de MTT y 8 ml del diluyente MTT para producir ml de solución de 1,0 mg / MTT.
- Guarde la solución de MTT a 4 ° C en la oscuridad hasta su uso. No guarde la solución MTT durante más de 1 día.
- Al final de la incubación Post, retire cada inserción de la placa de 6 pocillos y seque suavemente sobre un material absorbente.
- Coloque los insertos en la placa de 24 pocillos que contenía 0,3 ml de solución de MTT. Suelte las burbujas de aire atrapadas debajo de las inserciones. Incubar la placa de 180 ± 10 min a SCC.
- Extracción de MTT
- Después de 180 ± 10 min de incubación en la solución de MTT, retire cada insertode la placa de 24 pocillos y se seque la parte inferior de la inserción en un material absorbente.
- Para los artículos de prueba líquido no colorantes (extracción sumergida): La transferencia de los insertos en una placa de 24 pocillos pre-marcado que contiene 2,0 ml de una solución de extracción (isopropanol) para que se sumerge la pieza de inserción.
- Para sólidos y colorantes líquidos (no sumergida de extracción para evitar la contaminación de la solución extractante): La transferencia de los insertos en una placa de 6 pocillos pre-marcado que contiene 1,0 ml de la solución de extracción (isopropanol) para que no se sumerge la pieza de inserción.
Nota: Realice la misma extracción no sumergida para los correspondientes controles negativos y positivos.
- Sellar las placas (por ejemplo, con parafilm entre la cubierta de la placa y el borde superior de los pocillos o con un sellador de placas estándar). Coloque las placas en una placa de agitación y agitar durante 2 a 3 horas a temperatura ambiente para extraer el MTT.
- Alternativamente, realice la extracción de O / N a 2-876; C en la oscuridad sin agitación.
- Para los artículos de prueba líquido no colorantes (extracción sumergida): Al final del periodo de extracción, decantar el líquido de cada inserte de nuevo en el pozo y descartar los insertos con los tejidos RHCE.
- Mezclar la solución de extracto y transferir dos 200 alícuotas en los pocillos apropiados de una placa de 96 pocillos pre-etiquetados de acuerdo con la configuración de la placa (Figura 2).
- Para sólidos y colorantes líquidos (extracción no sumergido): Al final del periodo de extracción, descartan los tejidos (asegúrese de no perforar los tejidos).
- Añadir 1,0 ml de la solución de extracción en cada pocillo de la placa de 24 pocillos que contenía la solución extraída de los tejidos. Mezclar la solución de extracción y traslado de dos 200 alícuotas en los pocillos apropiados de una placa de 96 pocillos pre-etiquetados de acuerdo con la configuración de la placa (Figura 2).
- Determinar tque la densidad óptica (DO) de las muestras extraídas a una sola longitud de onda entre 550 y 590 nm (debe ser coherente dentro de un laboratorio) en un lector de placa o un espectrofotómetro.
- En caso de soluciones de extracto turbias causados por los sólidos insolubles, de centrífuga de las soluciones antes de medir la OD (enfriar la centrífuga a 4 ° C para evitar la evaporación). En caso de que el enjuague no retire el artículo de prueba (TA) y la TA interfiere con la reducción del MTT, se deben utilizar controles adicionales. Por favor, consulte a un SOP detallada para corregir la reducción de MTT 16.
- En caso de que se muestra una TA de tener, o desarrollar el color que puede interactuar con la medición MTT, una prueba adicional debe realizarse para determinar la cantidad de color unido a, y posteriormente se extrae de los tejidos. Por favor, consulte a un SOP detallada para corregir artículos de prueba de color 16.
9. Cálculos para realizar la prueba la viabilidad del tejido (Tabla 6 y Figura 3) & #160;
- Cálculos generales
- Calcular el valor medio de DO de los pocillos de control en blanco (OD negro) para cada experimento.
- Restar OD Blk de cada valor de DO del mismo experimento (negro corregida de datos).
- Calcular el valor medio de las dos partes alícuotas para cada tejido (OD = corregido).
- Calcular el porcentaje de viabilidad de cada uno de los dos tejidos replicados para cada control y artículo de prueba en relación con el control negativo promedio (control 100%).
Viabilidad (%) = [corregido OD tejidos tratados / control negativo OD corregido] x 100% - Calcular la diferencia de la viabilidad (la diferencia entre la viabilidad dos tejidos replicados).
- Calcular la viabilidad artículo de prueba de medias (viabilidad TA) y clasificar el artículo de prueba de acuerdo con el modelo de predicción.
10. Predicción de modelo (Figura 3)
- Si la viabilidad del tejido tratado-TA es> 60.0 en relación con el tejido tratado-NC vESPONSABILIDAD, etiquetar el artículo de prueba como no irritante (NI) (GHS No Categoría).
- Si la viabilidad del tejido tratado con TA es ≤ 60.0 en relación con la viabilidad del tejido tratado con NC, etiquetar el artículo de prueba como irritante (I) (SGA Categorías 1 y 2).
Nota: Los resultados de las pruebas del IET se consideran cualificado si:- la DO IET NC> 0,8 y <2,5;
- la viabilidad del tejido EIT PC (%, en relación con NC) es ≤50.0%;
- la diferencia entre los dos tejidos replicadas (Carolina del Norte, PC, y el artículo de ensayo) es <20.0%.
Resultados
Resultados EIT representativos realizados con 10 artículos de prueba (TA) y controles negativos y positivos se presentan en la Tabla 6 y la Figura 3. La media OD = 1,31 para la NC corresponde a 100% la viabilidad del tejido, por lo tanto el PC (DO media = 0,41) tenían la viabilidad del tejido relativa de 31,2%. Cuando el protocolo IET se realizó en 15 experimentos independientes válidos en 7 laboratorios utilizando el protocolo de exposición líquida y en 8 experimentos válidos independientes en 4 laboratorios, utilizando el protocolo de exposición sólida, la viabilidad media de tejido para el PC utilizando el protocolo de líquido fue 36,4 ± 4,0 % y 32,3 ± 6,4% para el protocolo de sólidos. En todos los casos, los resultados de los controles positivos fueron por debajo del valor de corte de 60,0% 15.
Como se muestra en la Figura 3, TA1, TA2, TA4, TA7, y TA8 tenido viabilidades de tejidos> 60,0% y por lo tanto fueron clasificados como "NI". TA3, TA5, TA6, TA9 y TA10 tenía Viabilidades tejido X04; 60,0% y por lo tanto fueron clasificados como "I". La diferencia de la viabilidad del tejido entre los tejidos duplicados era <20,0% para todos los TA con una excepción de TA2. Por lo tanto, los resultados de todos los artículos de prueba, con la excepción de TA2, se consideraron "calificado", ya que cumplen todos los criterios de aceptación del IET (Sección 10.2). Debido a la alta variabilidad entre tejidos duplicados para TA2 en el experimento inicial, un segundo experimento era necesario para obtener resultados EIT calificados.
El método de prueba IET como se describe aquí utilizando el modelo de tejido RHCE se utilizó para la evaluación de la irritación ocular en varios estudios de validación multilaboratorio, incluyendo validación formal por el CEVMA EURL / Cosméticos Europa 15,17-19. En todos los estudios, el IET ha demostrado ser reproducible y fue capaz de identificar correctamente los productos químicos (ambas sustancias y mezclas) que no requieren de clasificación y etiquetado de la irritación ocular o lesiones oculares graves acacuerdo con la ONU GHS 15,17-19. El método de prueba IET cumple los criterios de aceptación del Grupo de Gestión de Validación (VMG) para la irritación de los ojos para la sensibilidad, especificidad y precisión global y en la actualidad está pendiente de aplicación formal a la renovación parcial de conejo en vivo Test Draize 19.
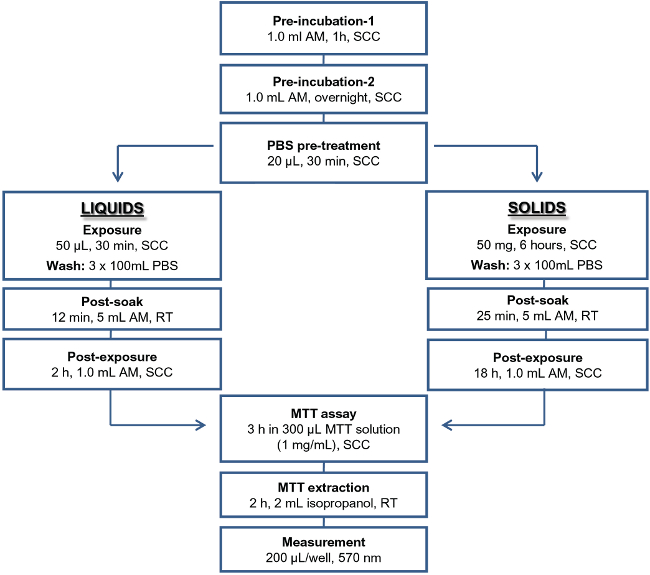
Figura 1: Esquema del protocolo IET para artículos de prueba líquidos y sólidos Abreviaturas utilizadas: AM, medio de ensayo;. SCC, condiciones de cultivo estándar; PBS, fosfato de Dulbecco solución salina tamponada; RT, la temperatura ambiente.
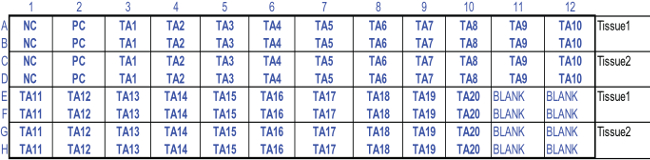
Figura 2:. La configuración de la placa de 96 pocillos estandarizado para la prueba de viabilidad del tejido MTT Dos 200 alícuotas son transferred a los pocillos apropiados de una placa de 96 pocillos pre-marcado. Abreviaturas utilizadas: NC, control negativo; PC, control positivo; TA1-TA20, artículos de prueba 1-20; Solución en blanco, de extracción. 96- configuración de placas MTT se utiliza con hoja de cálculo Excel diseñado para calcular la viabilidad del tejido RHCE y los resultados del IET.
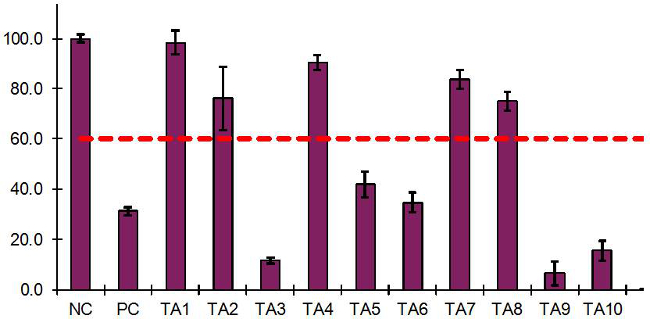
Figura 3: Resultados del IET obtuvieron de los artículos 10 de la prueba, Carolina del Norte y los controles de PC utilizando el modelo de tejido RHCE La gráfica se genera a partir de una hoja de cálculo de Excel diseñada para presentar los resultados del IET.. Las sustancias de ensayo que redujo la viabilidad del tejido ≤ 60,0% con respecto a Carolina del Norte se clasifican como irritantes ("I", TA3, TA5, TA6, TA9 y TA10) y los productos químicos de prueba que tenía la viabilidad del tejido> 60,0% son clasificados como no-irritantes (" NI ", TA1, TA2, TA4, TA7, y TA8).
| Hora de inicio de los pasos de trabajo de protocolo IET (un día de trabajo por un operador) | |||||||
| Cada línea corresponde a un par de tejidos | |||||||
| Orden de pasos: | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| Líquidos: | PBS | TA Exposición | Post- Remoje | Post- Incub. | MTT Reacción | MTT Extracción | Medida |
| 30 minutos | 30 minutos | 12 min | 120 min | 180 min | 120 min | Sobredosis | |
| NC | 09:00 | 09:30 | 10:00 | 10:12 | 12:12 | 15:12 | después |
| Ordenador personal | 09:01 | 9:31 | 10:01 | 10:13 | 12:13 | 15:13 | 17:30 |
| TA-1 | 09:02 | 09:32 | 10:02 | 10:14 | 12:14 | 15:14 | |
| TA-2 </ strong> | 09:03 | 09:33 | 10:03 | 10:15 | 12:15 | 15:15 | |
| TA-3 | 09:04 | 09:34 | 10:04 | 10:16 | 12:16 | 15:16 | |
| TA-4 | 09:05 | 09:35 | 10:05 | 10:17 | 12:17 | 15:17 | |
| TA-5 | 09:06 | 09:36 | 10:06 | 10:18 | 12:18 | 15:18 | |
| TA-6 | 09:07 | 09:37 | 10:07 | 10:19 | 12:19 | 15:19 | |
| TA-7 | 09:08 | 09:38 | 10:08 | 10:20 | 12:20 | 15:20 | |
| ng> TA-8 | 09:09 | 09:39 | 10:09 | Veintiuno después de las diez | Veintiún después de las doce de la noche | 15:21 | |
| TA-9 | 09:10 | 09:40 | 10:10 | 10:22 | 12:22 | 15:22 | |
| TA-10 | 09:11 | 09:41 | 10:11 | 10:23 | 12:23 | 15:23 | |
Tabla 3:. Horario Tiempo de la muestra para la prueba de los artículos de prueba líquidos pasos del protocolo, incluyendo pre-mojar los tejidos con DPBS, Aplicación de los artículos de prueba (TA), enjuague y Post-remojo, periodo post-incubación, ensayo MTT, Extracción de MTT, y medición de OD MTT se presentan en columnas. Los tiempos para los tejidos duplicados se organizan en filas. La totalidad de las pruebas de ensayo de 10 TA y controles se pueden acabar en un día.
e_content ">| Hora de inicio de los pasos del protocolo del IET (2 días de trabajo para un operador) | |||||||
| Cada línea corresponde a un par de tejidos | |||||||
| Día 1 | Día 2 (día siguiente) | ||||||
| Orden de pasos: | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| Sólidos: | PBS | TA Exposición | Post- Remoje | Post- Incubaction | MTT Reacción | MTT Extracción | Medida |
| 30 minutos | 6 hr | 26 min | 18 horas | 180 min | 120 min | Sobredosis | |
| NC | 09:00 | 09:30 | 15:30 | 15:56 | 09:56 | 12:56 | después |
| Ordenador personal | 09:02 | 09:32 | 15:32 | 15:58 | 09:58 | 12:58 | 15:30 |
| TA-1 | 09:04 | 09:34 | 15:34 | 16:00 | 10:00 | 13:00 | |
| TA-2 | 09:06 | 09:36 | 15:36 | 16:02 | 10:02 | 13:02 | |
| TA-3 | 09:08 | 09:38 | 15:38 | 16:04 | 10:04 | 13:04 | |
| TA-4 | 09:10 | 09:40 | 15:40 | 16:06 | 10:06 | 13:06 | |
| TA-5 | 09:12 | 09:42 | 15:42 | 16:08 | 10:08 | 13:08 | |
| TA-6 | 09:14 | 09:44 | 15:44 | 16:10 | 10:10 | 13:10 | |
| TA-7 | 09:16 | 09:46 | 15:46 | 16:12 | 10:12 | 13:12 | |
| TA-8 | 09:18 | 09:48 | 15:48 | 16:14 | 10:14 | 13:14 | |
| TA-9 | 09:20 | 09:50 | 15:50 | 16:16 | 10:16 | 13:16 | |
| TA-10 | 09:22 | 09:52 | 15:52 | 16:18 | 10:18 | 13:18 | |
Tabla 4: horario Tiempo de la muestra para la prueba de los artículos de prueba sólidos. Pasos del protocolo incluyendo pre-humectación de los tejidos con DPBS, Aplicación de los artículos de prueba, aclarado y Post-remojo, período post-incubación, el ensayo de MTT, Extracción de MTT, y medición de OD MTT se presentan en columnas. Los tiempos para los tejidos duplicados se organizan en filas. Todo el ensayo de prueba de 10 TA y controles se lleva a cabo durante un período de dos días.
| Cantidad | Reactivo | Condiciones de almacenamiento | Fuente | Descripción | Fecha de caducidad |
| 1 vial, 2 ml | MTT Concentrado (MTT-100-CON) | Protegido de la luz (-20ºC) | MatTek | Frozen MTT concentrado | 2 meses |
| 1 vial, 8 ml | MTT diluyente | 2-8 y# 186; C | MatTek | Para diluir el concentrado MTT antes de su uso en el ensayo de MTT | 2 meses |
| 1 botella, 60 ml | Isopropanol (CAS # 67-63-0) | RT | Sigma-Aldrich | Solución de extracción | N / A |
Tabla 5: MTT-100 Componentes del kit de ensayo.
| Código N ° | Tejidos | Los datos en bruto | Datos corregidos en blanco | media de OD | % De la viabilidad | ||
| n | Aliq. 1 | Aliq. 2 | Aliq. 1 | Aliq. 2 | |||
| NC | 1 | 1,316 | 1,352 | 1,316 | 1,352 | 1,334 | 101.6 |
| 2 | 1,277 | 1,309 | 1,277 | 1,309 | 1,293 | 98.4 | |
| Ordenador personal | 1 | 0,379 | 0,397 | 0,379 | 0,397 | 0,388 | 29.6 |
| 2 | 0,419 | 0,442 | 0,419 | 0,442 | 0,431 | 32.8 | |
| TA1 | 1 | 1,213 | 1,244 | 1,213 | 1,244 | 1,229 | 93.5 |
| 2 | 1,355 | 1,355 | 1,355 | 1,355 | 1,355 | 103.2 | |
| TA2 | 1 | 1,210 | 1,122 | 1,210 | 1,122 | 1,166 | 88.7 |
| 2 | 0,828 | 0,837 | 0,828 | 0,837 | 0,833 | 63.4 | |
| TA3 | 1 | 0,167 | 0,168 | 0,167 | 0,168 | 0,167 | 12.7 |
| 2 | 0,138 | 0,136 | 0,138 | 0,136 | 0,137 | 10.4 | |
| TA4 | 1 | 1,137 | 1,160 | 1,137 | 1,160 | 1,149 | 87.4 |
| 2 | 1,262 | 1,191 | 1,262 | 1,191 | 1,227 | 93.4 | |
| TA5 | 1 | 0,610 | 0,621 | 0,610 | 0,621 | 0,616 | 46.9 |
| 2 | 0,480 | 0,484 | 0,480 | 0,484 | 0,482 | 36.7 | |
| TA6 | 1 | 0,502 | 0,513 | 0,502 | 0,513 | 0,508 | 38.7 |
| 2 | 0,396 | 0,407 | 0,396 | 0,407 | 0,402 | 30.6 | |
| TA7 | 1 | 1,048 | 1,050 | 1,048 | 1,050 | 1,049 | 79.9 |
| 2 | 1,149 | 1,150 | 1,149 | 1,150 | 1,150 | 87.5 | |
| TA8 | 1 | 1,032 | 1,034 | 1,032 | 1,034 | 1,033 | 78.7 |
| 2 | 0,941 | 0,935 | 0,941 | 0,935 | 0,938 | 71.4 | |
| TA9 | 1 | 0,022 | 0,022 | 0,022 | 0,022 | 0,022 | 1.7 |
| 2 | 0,144 | 0,149 | 0,144 | 0,149 | 0,147 | 11.2 | |
| TA10 | 1 | 0,150 | 0,150 | 0,150 | 0,150 | 0,150 | 11.4 |
| 2 | 0,254 | 0,255 | 0,254 | 0,255 | 0,255 | 19.4 | |
| significar | Dif. | significado de | Dif. | Dif. / 2 | Clasificación | ||
| de OD | de OD | viabilidades [%] | de viabilidades | ||||
| NC | 1,314 | 0,041 | 100.0 | 3.12 | 1.56 | NI | calificado |
| Ordenador personal | 0,410 | 0,043 | 31.2 | 3.23 | 1.62 | YO | calificado |
| TA1 | 1,292 | 0,127 | 98.3 | 9.63 | 4.81 | NI | calificado |
| TA2 | 0,999 | 0,333 | 76.1 | 25.36 | 12.68 | NI | D> 20 |
| TA3 | 0,152 | 0,030 | 11.6 | 2.32 | 1.16 | YO | calificado |
| TA4 | 1,188 | 0,078 | 90.4 | 5.94 | 2.97 | NI | calificado |
| TA5 | 0,549 | 0,134 | 41.8 | 10.16 | 5.08 | YO | calificado |
| TA6 | 0,455 | 0,106 | 34.6 | 8.07 | 4.03 | YO | calificado |
| TA7 | 1,100 | 0,101 | 83.7 | 7.65 | 3.82 | NI | calificado |
| TA8 | 0,986 | 0,095 | 75.0 | 7.23 | 3.62 | NI | calificado |
| TA9 | 0,085 | 0,125 | 6.4 | 9.48 | 4.74 | YO | calificado |
| TA10 | 0,203 | 0,105 | 15.4 | 7.95 | 3.98 | YO | calificado |
Tabla 6:. Los resultados obtenidos del IET por 10 artículos de prueba, controles NC y PC Las mesas son produced por una hoja de cálculo de Excel diseñado para calcular la viabilidad del tejido y los resultados del IET. Las sustancias de ensayo que redujo la viabilidad del tejido ≤ 60,0% con respecto a Carolina del Norte se clasifican como irritantes ("I", TA3, TA5, TA6, TA9 y TA10) y los productos químicos de prueba que tenía la viabilidad del tejido> 60,0% son clasificados como no-irritantes (" NI ", TA1, TA2, TA4, TA7, y TA8).
Discusión
Hemos presentado la Prueba de irritación ocular (Figura 1) que fue desarrollado para el modelo de tejido EpiOcular. El IET es capaz de separar los irritantes oculares y corrosivos (GHS Categorías 1 y 2 combinados) a partir de materiales que no requieren etiquetado (GHS No Categoría) con alto grado de sensibilidad y especificidad 17. El IET como se presenta en este documento no discrimina entre SGA Categoría 1 de Categoría 2 productos químicos. El IET fue validado para la clasificación y el etiquetado de potencial de irritación ocular de una amplia gama de productos químicos, incluidos los ingredientes cosméticos y farmacéuticos. En conjunción con otros ensayos in vitro, el EIT servir como un reemplazo para el ensayo de irritación de ojo de conejo in vivo.
El IET utiliza dos protocolos similares pero distintos para materiales líquidos y sólidos, que varían en el tiempo de exposición y períodos de incubación después de la exposición (Figura 1). El criterio de valoración utilizado en el IETes la viabilidad del tejido, determinado por el ensayo MTT, que se ha utilizado previamente en modelos validados de tejidos epiteliales humanas 20,21. Para realizar este ensayo, no se necesita ningún equipo especial además de equipo de cultivo celular estándar. Debido al alto nivel de reproducibilidad de tejido-al tejido, n = 2 en lugar de los tejidos generalmente recomienda n = 3 se utilizan. La capacidad de utilizar n = 2 los tejidos es un aspecto crítico del protocolo, ya que permite a un operador con experiencia para procesar simultáneamente dos tejidos, reduciendo así al mínimo la variabilidad del ensayo que puede surgir debido a la diferente manejo de tejidos individuales 14. Además, mediante el uso de n = 2 tejidos por artículo de prueba, la irritación de las 10 sustancias de prueba del mismo estado físico (líquido o sólido), junto con los controles positivos y negativos, se puede evaluar utilizando un kit (24 tejidos).
Otros puntos clave que garantizan la clasificación fiable de materiales son las especificaciones para el control positivo Dobstance (viabilidad del tejido ≤50.0%), la reproducibilidad entre los tejidos duplicados (diferencia <20,0%), y las lecturas de DO de control negativo (> 0,8 y <2,5).
Al realizar la prueba de IET, es importante seguir el protocolo validado y para la dosificación sugerida y horarios de enjuague (Tablas 3 y 4), ya que la desviación del protocolo o los cambios en los períodos de incubación puede dar lugar a resultados alterados. Del mismo modo, las desviaciones del tiempo de 3 horas para la incubación MTT darán lugar a diferentes lecturas MTT y pueden afectar resultado del ensayo.
Ocasionalmente, una sustancia de ensayo puede tener propiedades ópticas o de otro tipo que puedan interferir con la viabilidad del tejido ensayo MTT o reducción causa de MTT. Por ejemplo, un compuesto químico de prueba puede reducir directamente MTT en un producto de reacción azul-púrpura, o puede ser una sustancia coloreada que absorbe la luz en el mismo rango que MTT formazán (~ 570 nm). Sin embargo, estos productos químicos de prueba se present un problema solamente, si en el momento del ensayo MTT, una cantidad suficiente del material todavía está presente en (o absorbida por) el tejido. Para evitar esta interferencia, los procedimientos extensos de enjuague se incorporan en el protocolo de EIT. Si el enjuague no quita el TA y TA interfiere con la reducción del MTT, controles adicionales deben ser utilizados para detectar y corregir para ello. En pocas palabras, si se sospecha de reducción de MTT directa de la sustancia de ensayo, 50 l (o 50 mg de sólidos) del producto químico en cuestión se incuba durante 3 horas con una solución de MTT de trabajo en SCC (NC, 50 l de agua desionizada estéril, debe ser ejecutar simultáneamente). Si la solución de MTT se vuelve azul-púrpura, el artículo de prueba se presume que han reducido el MTT. En este caso, una comprobación funcional utilizando los controles de tejido por congelación muerto se debe realizar para evaluar si el material de prueba es vinculante para el tejido y que conduce a una falsa señal de reducción de MTT. Si hay reducción de MTT apreciable en el control de tejido muerto expuesta-TA(en relación con la cantidad en el tejido viable sin tratar), la viabilidad del tejido media del artículo de prueba debe ser corregido restando la viabilidad media del control matado.
El IET yerra en el lado de la seguridad, como lo demuestra la baja incidencia de las clasificaciones negativas falsas 14,15,18. Es importante destacar que ninguno de los productos químicos SGA Categoría 1, que son corrosivos para el ojo y que representan el peligro ocular más grave, fueron clasificados como no irritante en este ensayo 14,15,18,19. Por último, una de las principales ventajas de la RHCE en el método de ensayo in vitro es la posibilidad de probar líquido puro y materiales sólidos (que no es posible con cultivos celulares bidimensionales, sumergidos).
El IET contribuirá de manera significativa en la determinación del potencial de irritación ocular de una amplia gama de materiales de acuerdo con la clasificación y el etiquetado del sistema SGA de la ONU. La sustitución de los animales para determinar oToxicidad cular ha sido un objetivo de la investigación toxicológica durante muchos años. El método de prueba IET ha completado un estudio formal de validación con el apoyo de EURL CEVMA en 2014 y de la EpiOcular IET fue implementado en las Directrices de ensayo de la OCDE TG 492 de la OCDE como en 2015.
Divulgaciones
Tasas de publicación para este artículo fueron pagados por MatTek Corporation.
Agradecimientos
Los autores desean agradecer al Dr. John Harbell por su apoyo y tiempo científica dedicada al proyecto IET. Los autores también desean agradecer a Beiersdorf AG (Alemania), los VII (EE.UU.), Mary Kay Inc. (EE.UU.), Avon Products Inc. (EE.UU.), Procter & Gamble / Cosmital (Suiza), Laboratoire Pierre Fabre (Francia), Harlan Laboratories (Reino Unido), y LVMH Parfume (Francia) para la participación en estudios de la Prueba de Irritación ocular 15 Multi-Centro Internacional de prevalidación y validación.
Referencias
- National Toxicology Program (NTP) Interagency Center for the Evaluation of Alternative Toxicological Methods (NICEATM). Request for Ocular Irritancy Test Data From Human, Rabbit, and In Vitro Studies Using Standardized Testing Methods. Federal Register. 72 (109), 31582-31583 (2007).
- . Regulation (EC) No 1907/2006 of the European Parliament and of the Council of 18 December 2006 concerning the Registration, Evaluation, Authorisation and Restriction of Chemicals (REACH), establishing a European Chemicals Agency, amending Directive 1999/45/EC and repealing Council Regulation (EEC) No 793/93 and Commission Regulation (EC) No 1488/94 as well as Council Directive 76/769/EEC and Commission Directives 91/155/EEC, 93/67/EEC, 93/105/EC and 2000/21/EC. OJ. L396 (49), 1-849 (2006).
- . . Globally Harmonized System of Classification and Labelling of Chemicals (GHS). , (2013).
- Draize, J. H., Woodard, G., Calvery, H. O. Methods for the Study of Irritation and Toxicity of Substances Applied Topically to the Skin and Mucous Membranes. J Pharmacol Exp Ther November. 82, 377-390 (1944).
- Adriaens, E. Retrospective analysis of the Draize test for serious eye damage/eye irritation: importance of understanding the in vivo endpoints under UN GHS/EU CLP for the development and evaluation of in vitro test methods. Arch tox. 88, 701-723 (2014).
- Balls, M., Botham, P. A., Bruner, L. H., Spielmann, H. The EC/HO international validation study on alternatives to the Draize eye irritation test. Toxicol in Vitro. 9, 871-929 (1995).
- Curren, R. D., Harbell, J. W. Ocular safety: a silent (in vitro) success story. Altern Lab Anim. 30, 69-74 (2002).
- Wilhelmus, K. R. The Draize Eye Test. Survey of Ophthalmology. 45, 493-515 (2001).
- Curren, R. D., Harbell, J. W. In vitro alternatives for ocular irritation. Environ health persp. 106, 485-492 (1998).
- McCain, N. E., Binetti, R. R., Gettings, S. D., Jones, B. C. Assessment of ocular irritation ranges of market-leading cosmetic and personal-care products using an in vitro tissue equivalent. Toxicologist. 66, 243 (2002).
- Niranjan, P., Dang, A. H., January, B. G., Gomez, C., Harbell, J. W. Use of the EpiOcular assay for preclinical qualification of formulas for human clinical studies. Toxicologist. 96, 249 (2007).
- Yin, X. J. Prediction of ocular irritation potential of surfactants-based formulations at different concentrations using the EpiOcular model. Toxicologist. 108, 378 (2009).
- Harbell, J., Curren, R. In vitro methods for the prediction of ocular and dermal toxicity. Handbook of Toxicology. , (2001).
- Kaluzhny, Y. Development of the EpiOcular(TM) eye irritation test for hazard identification and labelling of eye irritating chemicals in response to the requirements of the EU cosmetics directive and REACH legislation. Altern Lab Anim. 39, 339-364 (2011).
- Pfannenbecker, U. Cosmetics Europe Multi-Laboratory Pre-Validation of the EpiOcular Reconstituted Human Tissue Test Method for the Prediction of Eye Irritation. Toxicol in vitro. , (2013).
- MatTek Corporation. . EpiOcular™ Eye Irritation Test (OCL-200-EIT) for the prediction of acute ocular irritation of chemicals for use with Reconstructed Human EpiOcular Model (OCL-200-EIT). Protocol#MK-24-007-0055. , (2014).
- Kaluzhny, Y. EpiOcular Eye Irritation Test (EIT) for Hazard Identification and Labeling of Eye Irritating Chemicals: Protocol Optimization for Solid Materials and Extended Shipment Times. Altern Lab Anim. 43 (2), 101-127 (2015).
- Kolle, S. N., Kandarova, H., Wareing, B., van Ravenzwaay, B., Landsiedel, R. In-house validation of the EpiOcular(TM) eye irritation test and its combination with the bovine corneal opacity and permeability test for the assessment of ocular irritation. Altern Lab Anim. 39, 365-387 (2011).
- . Reconstructed Human Cornea-like Epithelium (RhCE) Test Method for Identifying Chemicals Not Requiring Classification and Labelling for Eye Irritation or Serious Eye Damage. Draft proposal for a new test guideline.. OECD Guideline for the Testing of Chemicals. , (2014).
- Blazka, M. E., Harbell, J. Evaluating the ocular irritation potential of 54 test articles using the EpiOcular Human tissue Construct Model. Toxicol. In Vitro. , (2003).
- Kandarova, H. The EpiDerm Test Protocol for the Upcoming ECVAM Validation Study on In Vitro Skin Irritation Tests — An Assessment of the Performance of the Optimised Test. Altern Lab Anim. 33, 351-367 (2005).
Reimpresiones y Permisos
Solicitar permiso para reutilizar el texto o las figuras de este JoVE artículos
Solicitar permisoThis article has been published
Video Coming Soon
ACERCA DE JoVE
Copyright © 2025 MyJoVE Corporation. Todos los derechos reservados