Method Article
Test auf Augenreizung (EIT) zur Kennzeichnung der Gefahr von Augen Reizt Chemicals mit rekonstruierter menschlicher Hornhaut-ähnlichen Epithelial (RhCE) Gewebemodell
In diesem Artikel
Zusammenfassung
Wir haben einen Test auf Augenreizung, die einen dreidimensionalen rekonstruierten menschlichen Hornhaut artigen Epithelzellen (RhCE) Gewebemodell nutzt entwickelt. Der Test ist in der Lage, zwischen den Augenreizstoffes und ätzende Stoffe (GHS Kategorien 1 und 2 kombiniert) und diejenigen, die nicht die Kennzeichnung (GHS Keine Kategorie) erfordern, zu unterscheiden.
Zusammenfassung
Um mit dem siebten Änderung der EU-Kosmetikrichtlinie und der EU-REACH-Verordnung zu erfüllen, sind validierte tierversuchsfreien Alternativmethoden für eine zuverlässige und genaue Bewertung der okulare Toxizität beim Menschen erforderlich. Um diesen Bedarf anzusprechen, haben wir eine Augenreizung (EIT), die ein dreidimensionales rekonstruiertes menschlichen Hornhaut artigen Epithelzellen (RhCE) Gewebemodells, die auf normalen menschlichen Zellen basiert, nutzt entwickelt. Das ETI ist in der Lage, die Augen reizenden und ätzenden Stoffen (GHS Kategorien 1 und 2 kombiniert) und jene, die keine Kennzeichnung (GHS Keine Kategorie) zu trennen. Der Test verwendet zwei getrennte Protokolle, eine für flüssige Chemikalien, und ein zweites, ähnliches Protokoll für feste Testartikel konzipiert. Das EIT Vorhersagemodell verwendet einen einzelnen Expositionszeit (30 min für Flüssigkeiten, 6 Stunden für Feststoffe) und eine einzelne Gewebelebensfähigkeit cut-off (60,0%, wie durch den MTT-Test bestimmt). Basierend auf den Ergebnissen für 83 Chemikalien (44 Flüssigkeiten und Feststoffen 39) EIT erreicht 95,5 / 68,2 / 81,8% sensitivity / Spezifität und Genauigkeit (SS & A) für Flüssigkeiten, 100,0 / 68,4 / 84,6% und SS & A für Feststoffe und 97,6 / 68,3 / 83,1% und für die gesamte SS & A. Das EIT wird wesentlich zur Klassifizierung des Augenreizungspotenzial von einer breiten Palette von flüssigen und festen Chemikalien, ohne die Verwendung von Tieren zu regulatorischen Testanforderungen gerecht zu leisten. Die EpiOcular EIT-Verfahren wurde im Jahr 2015 in den OECD-Prüfungsrichtlinien als TG 492 implementiert.
Einleitung
Consumer-Produkte wie Kosmetika, Wasch- und Reinigungsmitteln umfassen eine Vielzahl von Chemikalien, die schwere Schäden verursachen können, wenn sie Kontakt mit den Augen. Daher ist die Prüfung dieser Mittel zur Augenreizung durch die US- und EU-Aufsichtsbehörden erforderlich ist, um die Sicherheit der Verbraucher zu gewährleisten 1. Eine Bewertung der Augenreizung Potenzial der Mischungen und Formulierungen ist auch eine Voraussetzung für die Einhaltung der REACH (Registrierung, Bewertung, Zulassung und Beschränkung chemischer Stoffe) Rechtsvorschriften für die Etikettierung von kosmetischen Inhaltsstoffen im Rahmen der EU-Kosmetik-Richtlinie für den Transport von Chemikalien und für die Kennzeichnung von Pflanzenschutzmitteln und Haushaltsprodukte 2. Derzeit Aufsichtsbehörden verlangen, Augengefährdungsbeurteilung unter Verwendung des Global Harmonisierte System zur Einstufung und Kennzeichnung von Chemikalien (GHS) 3. GHS basiert hauptsächlich auf der Draize Augenreiztest basiert, die am weitesten verbreitete Augenreizung Assay, in dem Fremdstoffe und mixtures werden direkt in den Bindehautsack des Kaninchenauges 4 eingeleitet. Nach GHS-Einstufung, GHS-Kategorie 1 (augenverätzender) bezieht sich auf Chemikalien, die schwere anfänglichen Schädigung der Augengewebe oder schwere Schäden am Auge und Vision, die nicht innerhalb von 21 Tagen nach der Exposition 3,5 vollständig reversibel verursachen testen. GHS Kategorie 2 bezieht sich auf Chemikalien, die wesentlichen Änderungen des Auges, die innerhalb von 21 Tagen nach der Exposition vollständig reversibel sind produzieren zu testen. Testchemikalien, die keine korrosive oder Reizstoffe werden als GHS Keine Kategorie bezeichnet.
Seit mehr als 40 Jahren hat sich die Kaninchenaugentest Draize für seinen Mangel an Reproduzierbarkeit, Überschätzung der menschlichen Reaktionen, und der Einsatz von lebenden Tieren 08.05 kritisiert worden. Diese Bedenken wurden viele Vorschläge zur Verfeinerung, Verringerung und Ersetzung der in-vivo-Test 9 gefördert. Der Bedarf an validierten ohne Tier Alternativen weiter gestärktdurch die Annahme der siebten Änderung der Kosmetik-Richtlinie, die die Verwendung von Tieren in die Sicherheitsbewertung kosmetischer Mittel (2005) verboten und Zutaten (in 2009) 2.
Seit 1996 ist der rekonstruierte Cornea artigen Gewebemodell wurde in großem Umfang von der kosmetischen Industrie verwendet, um das Reizpotential der Rohstoffe, tensidhaltigen Formulierungen zu bewerten und compoundierten Mischungen, die zur Verwendung in ausgelegt sind, oder in der Nähe von, dem Auge 10-13. Die Nutzung der RhCE Gewebemodell ermöglicht die direkte topische Anwendung des Testmaterials auf die Gewebeoberfläche in seiner nativen, unverdünnt. Auf diese Weise können nicht-wasserlösliche Formulierungen, ohne sie mit Lösungsmitteln verdünnt getestet werden. Als Reaktion auf EURL ECVAM (EU-Referenzlabor Europäische Zentrum für die Validierung alternativer Methoden) Anforderung für eine breite Anwendung, einfache und wirtschaftliche Methode der Test auf Augenreizung (EIT), das eine singl nutzte Belichtungszeit und ist in der Lage, die Augen reizenden und ätzenden Stoffen aus Materialien, die nicht Kennzeichnung erfordern getrennt wurde (Abbildung 1) 14 entwickelt. Basierend auf den Ergebnissen für die 83 Chemikalien (44 Flüssigkeiten und 39 Feststoffe) erzielte das EIT 95.5 / 68.2 / und 81,8% Sensitivität / Spezifität und Genauigkeit (SS & A) für Flüssigkeiten, 100,0 / 68,4 / 84,6% SS & A für Feststoffe und 97,6 / 68,3 / 83,1% und für die gesamte SS & A.
Im Jahr 2007, ein Multi-Labor vor, eine Validierungsstudie durch Cosmetics Europe (ehemals Colipa) unter der Schirmherrschaft der EURL ECVAM gesponserte bewertet die Relevanz und Zuverlässigkeit des EIT mit dem Ziel, es zu formellen Validierung 15 bringen. In dieser Studie wurden 298 unabhängige Studien in sieben unabhängigen Labors durchgeführt. Die Ergebnisse der Studie zeigten 99,7% Zustimmung bei der Vorhersage mit niedrigen Variationskoeffizienten für alle teilnehmenden Laboratorien 15. Als Ergebnis im Jahr 2010 die EIT-Protokoll trat eine formelle EURL ECVAMValidierungsprogramm. Die Validierungsstudie verwendet 104 codierte Testchemikalien, einschließlich Einzelstoffe und Mischungen von Chemikalien, für die in-vivo-Referenzdaten (Draize-Augenreizungsdaten) zur Verfügung standen. Basierend auf dem Erfolg dieser Arbeit wurde ein OECD-Prüfrichtlinie Entwurf 2014 vorgelegt Es wird erwartet, dass das EIT wird wesentlich zur Einstufung von Augenreizungspotenzial von einer breiten Palette von Materialien gemäß der UN GHS Einstufung und Kennzeichnung Systems beitragen.
Protokoll
1. Herstellung von RhCE Gewebe für die Behandlung - Tag 0
- Nach Erhalt der kommerziellen menschlichen Hornhaut artigen Epithelzellen (RhCE) Kit, überprüfen Sie alle Komponenten des Kits für Integrität (für Kit Details Standard-Assay Kit Components (Tabelle 1) und die Ausrüstung und Materialien benötigt, um den EIT-Assay (Tabelle 2) durchzuführen. Auf der Tag des Zugangs, ins Gleichgewicht Geweben (in seinem 24-Loch-Transportbehälter) auf RT für 15 min.
| Höhe | Reagens | Bedingungen | Ursprung | Bezeichnung | Ablaufdatum |
| 1 | Sealed 24-Well-Platte von EpiOcular Geweben (OCL-200) | 2-8 ° C | MatTek | Enthält 24 tissues der Zellkultur-Einsätze, Paket auf Agarose | 72 Stunden |
| 1 Flasche, 200 ml | EpiOcular Assay-Medium (OCL-200-ASY) | 2-8 ° C | MatTek | DMEM Medium auf der Grundlage | 21 Tagen |
| 1 Flasche, 100 ml | Ca Mg ++ -Free Dulbecco PBS (DPBS) ++ | RT | Sigma-Aldrich, D5652, oder equiv. | Verwendet zum Spülen Einsätze | 1 Jahr |
| 4 | 6-Well-Platten | RT | Falcon | Verwendet für die Aufrechterhaltung der Gewebe während Testprotokoll | N / A |
| 2 | 12-Well-Platten | RT | Falcon | Während der Assay-Protokoll verwendet | N / A |
| 2 | 24-Well-Platten | RT | Falcon | Verwendet werden, um MTT-Test durchführen | N / A |
| 1 Flasche, 0,5 ml | Methyl Acetate (CAS # 79-20-9) | RT | Sigma-Aldrich, Cat # 186325 | Verwendet als PC im Assay | 1 Monat |
Tabelle 1: Standard Assay Kit Components.
| / Material | Benötigt für: |
| Befeuchteten Inkubator (37 ± 1 ° C, 5 ± 1% CO 2, 90 ± 10% Luftfeuchtigkeit) | Inkubieren Gewebe vor und während des Assays |
| Laminarströmungshaube | Sicheres Arbeiten unter sterilen Bedingungen |
| Vakuumpumpe (optional) | Absaugen von Medium und Lösungen |
| Plattenleser-Photometer (für 96-Well-Platten) | Lesen OD |
| Plattenschüttler | ExtraktIonen Formazan |
| Sterile, stumpfen Pinzette | Umgang mit Gewebeeinlagen |
| Die Stoppuhren | Zeitpunkt der Anwendung der Testmaterialien und andere zeitgesteuerte Schritte in dem Protokoll |
| Wasserbad (37 ± 1 ° C) | Warming Medien und MTT-Lösung |
| Mörser und Stößel | Schleifen körnigen Feststoffen |
| Verdrängerpipette (50 ul) | Anwendung des viskosen und halbfeste Materialien und Suspensionen |
| Einstellbare Pipetten (200 & mgr; l-2 ml) | Anwendung von flüssigen Materialien, Assay-Medium und MTT |
| Vorsterilisiert Spitzen (200 ul und 20 ul), Rainin Cat # HR-200F und HR-20F (oder gleichwertig) | Anwendung von flüssigen Materialien, Assay-Medium und MTT |
| Breite Öffnung vorsterilisierte Spitzen (250 ul), Rainin Cat # HR-250WS (oder equivalent) | Anwendung des viskosen und halbfeste Materialien und Suspensionen |
| 8 Unzen / 220 ml Probenbehälter, Falcon Cat # 3540200 (oder gleichwertig) | Spülen Geweben |
| Sterile Einmalspritzen (zB 1 ml Tuberkulin-Spritze Omnifix-F, B. Braun Melsungen AG, Kat. Nr 9161406V) | Lieferung von ~ 50 mg Feststoffe (optional) |
| Ted Pella Mikro Spatel / Löffel, Ted Pella Inc., Cat # 13504 (oder gleichwertig, scharfen Löffel oder Knochen Kürette, zB Aesculap, No: FK 623) | Lieferung von ~ 50 mg Feststoffe |
| Ca ++ und Mg ++ frei Dulbeccos phosphatgepufferter Salzlösung (Ca ++ Mg ++ Free-DPBS): Sigma-Aldrich, Cat # D5652 (oder gleichwertig) | Spülen Gewebe während Assay |
| Steriles entionisiertes Wasser, Gewebekultur-Grad (Qualitäts biologischen oder gleichwertig) | wie NC Verwenden |
| 96-Loch-Flachbodenplatten, Falcon (oder gleichwertig) | Zum Lesen OD |
| Wattestäbchen-Swaps (steril) | Zum Trocknen der Gewebeoberfläche (optional) |
| Klebeband oder Parafilm | Während Formazan Extraktion Abdeckplatten |
| MTT-100-Assay-Kit | Enthält MTT-Thiazolylblau tetrazoliumbromid Reagenz (Sigma # M-5655) und Isopropanol-Extrakt. |
Tabelle 2: Ausrüstung und Materialien benötigt, um das EIT durchzuführen.
- Unter sterilen Bedingungen, öffnen Sie den Plastikbeutel mit dem 24-Loch-Platte mit RHCE-Geweben und entfernen Sie den steriler Gaze. Überprüfen Sie alle Gewebe für Luftblasen zwischen dem Agarose-Gel und einfügen. Kulturen, die mit Luftblasen, nicht unter dem Deckeinsatz> 50% der Einsatzbereich, defekte Gewebe oder Gewebe whi ch sind vollständig mit Flüssigkeit bedeckt.
- Beschriften Sie die 6-Well-Platten mit dem Testartikel oder Steuercodes und Belichtungszeiten. Aliquots von 1,0 ml Assay-Medium (im Kit enthalten) auf ca. 37 ° C vorgewärmt, in die Vertiefungen der voretikettierten 6-well-Platten.
- Verwenden einer sterilen Pinzette, um jeden Einsatz mit dem RhCE Gewebe in das markierte 6-Well-Platte zu entfernen und den Einsatz. Während dieses Schritts zu entfernen jegliche verbleibenden Versand Agarose, die an den Außenseiten des Einsatzes von sanften Blotting auf sterilem Filterpapier haftet. Lassen Sie alle Luftblasen unter den Einsätzen gefangen.
- Vorge inkubieren RhCE Gewebe in den 6-Well-Platten zu Standardkulturbedingungen (SCC, befeuchteten Atmosphäre mit 5 ± 1% CO 2 bei 37 ± 1 ° C) für 1 Stunde.
- Nach 1 Stunde, ersetzen Sie die Assay-Medium mit 1,0 ml frischem Assay-Medium vorgewärmt auf 37 ° C und Inkubation RHCE Geweben bei SCC Bedingungen (Nacht = O / N) (16-24 h).
- Nach dem O / N Inkubation anzuwenden 20 ul Ca 2+ Mg 2+ -frei ist Dulbecco-phosphatgepufferter Salzlösung (DPBS, zur Verfügung gestellt) unter Verwendung eines geeigneten Pipettiervorrichtung. Wenn die DPBS nicht über das Gewebe verteilt, leicht auf den Einsatz auf der Platte, um sicherzustellen, dass die DPBS benetzt die gesamte Gewebeoberfläche.
- RHCE Geweben bei SCC Inkubieren für 30 ± 2 min.
Hinweis: Dieser Schritt zur Gewebehydration notwendig ist, und in-vivo-Bedingungen zu imitieren.
3. Testmaterial Belichtungsverfahren
- Sollten alle Testartikel und Kontrollen, um RhCE Geweben duplizieren (n = 2). Der Testgegen Dosiervorgang ist für Flüssigkeiten und Feststoffe. Topisch anzuwenden 50 ul flüssigen Testartikel mit einer Pipette. Die Belichtungszeit für Flüssigkeiten beträgt 30 min. Übernehmen 50 mg des festen Testartikel mit einem Löffel voll eingeebnet (kalibriert auf 50 mg Natriumchlorid zu halten). Die Ex-Belichtungszeit für feste Stoffe bis zu 6 Std.
Anmerkung: Die Flüssigkeiten werden als flüssige Substanzen (beispielsweise Flüssigkeiten, Gele und Cremes), die angewendet werden unter Verwendung einer Pipettiervorrichtung werden definiert. Feststoffe werden als nicht-flüssigen Substanzen (beispielsweise Pulver, harz- oder wachsartige Materialien), die mit einer Pipette nicht angewendet werden können definiert.- Wenn der physikalische Zustand der Testsubstanzen ist nicht leicht zu bestimmen, legen Sie die Durchstechflaschen mit Testartikel in einem Wasserbad für 15 min (37 ° C). Folgen EIT Protokoll für Flüssigkeiten für die Testsubstanzen, die bei 37 ° C verflüssigt.
- Verwenden Sie eine positive Verdrängungspipette für besonders viskose Materialien.
- Dosieren Sie die negative Kontrolle und positive Kontrollen erste und die Testartikel dann dosieren.
- Je 50 ul der negativen Kontrolle (NC) und der positiven Kontrolle (PC) an die RhCE Geweben unter Verwendung einer Standardpipette. Die NC ist steril entionisiertem Wasser; der PC Methylacetat (CAS # 79-20-9). Übernehmen Sie die NC und PC für 30 Minuten, wenn Testing flüssigen Test Artikel und für 6 Stunden bei der Prüfung von festen Testartikel.
4. Test Artikel Exposure - Tag 1
- Für die Behandlung von flüssigen Test Artikel, folgen dem Zeitplans in Tabelle 3 angegeben. Lassen Sie 1 min Intervalle zwischen den Anwendungen der jeweiligen Testartikel auf Gleich Exposition für alle Gewebe zu gewährleisten.
- Nachdem das 30 ± 2 min DPBS Vorbehandlung, topisch 50 ul NC und PC, und jeder Flüssigkeitstestartikel topisch anzuwenden auf die RhCE Geweben unter Verwendung eines geeigneten Pipettiervorrichtung.
- Je 50 ul der flüssigen Test Artikel direkt auf das Gewebe, um die obere Oberfläche zu bedecken. Entzieht der Engstelle der Pipettenspitze, um die Öffnung für viskose Materialien zu erweitern. Für sehr viskose Materialien, gelten die Testartikel auf eine Dosiereinrichtung (eine Flachkopfzylinder mit einem Durchmesser etwas kleiner als der Innendurchmesser der Gewebeeinlage oder einem Kunststoff PIN), drehen Sie die Dosierung device und legen Sie sie auf das Gewebe, so dass die Testartikel gleichmäßig Kontakte der Gewebeoberfläche.
- Wenn Testartikel nicht über das Gewebe verteilt, leicht auf den Einsatz, um sicherzustellen, dass es breitet sich auf der gesamten Gewebeoberfläche. Mechanische Verbreitung der Testsubstanzen (beispielsweise mit einer Pipettenspitze) wird nicht empfohlen, da es das Gewebe beschädigen.
- Das Gewebe bei SCC Inkubieren für 30 ± 2 min.
- Für die Behandlung von festen Testartikel - Tag 1, folgen Sie dem Zeitplans in Tabelle 4 angegeben Leave 2 min Intervalle zwischen den Anwendungen der jeweiligen Testartikel auf Gleich Exposition für alle Gewebe zu gewährleisten..
- Nachdem das 30 ± 2 min DPBS Vorbehandlung anzuwenden 50 ul NC und PC topisch auf die RhCE Geweben unter Verwendung eines geeigneten Pipettiervorrichtung.
- Für feste Testartikel Anwendung, entfernen Sie die Einsätze (n = 2) aus dem Brunnen und legen Sie sie auf eine sterile Oberfläche (zB der Deckel der Uhrultiwell Platte), um eine Testartikel Verschütten in das Medium zu vermeiden.
- Mit Hilfe eines nivellierten Löffel, topisch etwa 50 mg des Testartikels auf die Gewebeoberfläche anzuwenden; stellen Sie sicher, dass die Oberfläche des Gewebes vollständig von dem Testartikel bedeckt. Wenn der Test Artikel nicht über das Gewebe verteilt, schütteln Sie den Einsatz vorsichtig von einer Seite zur anderen, um sicherzustellen, dass das Gewebe vollständig von dem Testartikel bedeckt. Mechanische Verbreitung der Testsubstanzen (beispielsweise mit einer Pipettenspitze) wird nicht empfohlen, da es das Gewebe beschädigen.
- Falls erforderlich, zu mahlen kristalline Pulver mit Mörser und Pistill, einen besseren Kontakt zwischen dem Testgegenstand und dem Gewebe zu gewährleisten.
- Alternativ Ort Pulver direkt auf die Gewebekultur im Inneren des Einsatzes unter Verwendung einer 1 ml Spritze mit seinem Kopf abgeschnitten. Stuff Pulver in die Spritze, wenn der Kolben zurückgezogen wird und dann durch Drücken der Kolben nach unten anzuwenden.
- Wenn die äußere Wand des Einsatzes ist contaminated zB durch Pulver, wischen Sie die Partikel mit einem steriler Gaze.
- Nach der Dosierung, kehren die Gewebe auf die 6-well-Platten mit Kulturmedium und Inkubation bei SCC 6 h ± 15 min.
5. Spülen
- Bereiten Sie einen Satz von drei sauberen Becher (150 ml Kapazität) pro Testartikel und füllen jeweils mit 100 ml DPBS. Für jede Testartikel, nutzen, eine andere Gruppe von drei Bechern.
- Am Ende der 30 ± 2 min Belichtung für flüssige Materialien oder 6 h ± 15 min Belichtung für feste Materialien, entfernen und entsorgen Sie die Dosiereinrichtung, wenn es verwendet wurde.
- Heben Sie die Einsätze mit dem RhCE Gewebe aus dem Medium durch Ergreifen des oberen Rand des Kunststoff 'Kragen' mit feinen Pinzette. Verwenden einer gebogenen Pinzette, um die Handhabung und Dekantieren zu erleichtern. Spülen Sie das Gewebe zwei auf einmal, indem Sie die doppelten Einsätze miteinander durch ihre Kragen mit einer Pinzette. Seien Sie vorsichtig, not, um das Gewebe mit der Zange zu beschädigen.
- Dekantiert man die Testartikel oder Kontrollen von der Gewebeoberfläche auf ein sauberes saugfähigem Material (Papiertuch, Gaze, etc.)
- Tauchen Sie die Einsätze in den ersten Becher DPBS, Wirbel in einer Kreisbewegung in der DPBS für ca. 2 sec, heben Sie die Einsätze, so dass sie meist mit DPBS befüllt und dekantiert die Flüssigkeit zurück in das Becherglas. Wiederholen Sie diesen Vorgang drei Mal in der ersten Becherglas.
- Spülen der Einsätze in der zweiten und dritten Becher DPBS je dreimal in der gleichen Weise.
- Dekantieren Sie alle verbleibenden in dem Einsatz auf dem absorbierenden Material Flüssigkeit. Drehen Sie den Einsatz zu einem ungefähren Winkel von 45 ° (offenes Ende nach unten) und berühren Sie die Oberlippe zu dem absorbierenden Material.
Hinweis: Wenn es nicht möglich ist, alle sichtbaren Testmaterial zu entfernen, sollte keine weitere Spülung durchgeführt, um Gewebeschäden zu vermeiden, werden aufgrund einer übermäßigen Handhabung.
6. Post-einweichen
- Nach dem Spülen,unmittelbar einzutauchen Gewebe in 5 ml Testmedium vorher auf RT in einer vorher markierten 12-Well-Platte erwärmt.
- Inkubieren Sie das Gewebe für 12 ± 2 min für flüssige Materialien oder 25 ± 2 min für Feststoffe bei Raumtemperatur eingetaucht, um die Entfernung von Rückständen des Testartikel zu erleichtern.
7. Post-Inkubation
- Am Ende der Post-Soak Eintauchdauer, dekantiert die Assay-Medium aus dem Gewebe und tupfen Sie die Einsätze auf ein saugfähiges Material.
- Übertragen Sie die Einsätze in die Pre-markierte 6-Well-Platte mit 1 ml warmem Assay-Medium.
- Inkubieren Sie die Gewebe für 120 ± 15 min bei SCC für flüssige Testmaterialien.
- Das Gewebe Inkubieren für 18 ± 0,25 h bei SCC für feste Testmaterialien.
8. MTT Viability Assay - Tag 1 (Protokoll für Flüssigkeiten) und Tag 2 (Protokoll für Feststoffe)
- Führen Sie den MTT-Test nach dem Post-Inkubation von 12077; 15 min für Flüssigkeiten und 18 ± 0,25 h bei Feststoffen auf.
- Bereiten 1,0 mg / ml MTT-Lösung und 0,3 ml Aliquot der Lösung in jeder Vertiefung einer pre-markierten 24-Well-Platte.
- Verwenden Sie den kommerziellen MTT-Kit (Tabelle 5):
- 2 h vor der Verwendung aufgetaut des MTT-Konzentrat bei RT. Kombinieren 2 ml MTT-Konzentrat und 8 ml MTT-Verdünnungsmittel auf 1,0 mg / ml MTT-Lösung zu erzeugen.
- Bewahren Sie die MTT-Lösung bei 4 ° C im Dunkeln bis zur Verwendung. Haben die MTT-Lösung für mehr als 1 Tag lagern.
- Am Ende der Post Incubation, entfernen Sie jedes Einsatzes aus dem 6-Well-Platte und tupfen Sie leicht auf einem saugfähigen Material.
- Setzen Sie die Einsätze in der 24-Well-Platte mit 0,3 ml MTT-Lösung. Lassen Sie alle Luftblasen unter den Einsätzen gefangen. Die Platte für 180 ± 10 min bei SCC.
- MTT-Extraktion
- Nach 180 ± 10 min Inkubation in der MTT-Lösung Entfernen Sie jede Einsatzvon der Platte mit 24 Vertiefungen und klopfen Sie den Boden des Einsatzes auf einem saugfähigen Material.
- Für Nicht-Farbstoff flüssigen Testartikel (untergetaucht Extraktion): Übertragen Sie die Einsätze in eine vorge markierten 24-Well-Platte mit 2,0 ml Extraktionslösung (Isopropanol), so dass es den Einsatz eintaucht.
- Für Feststoffe und flüssige Farbstoffe (nicht gedeckte Extraktions um eine Kontamination der Extraktionsmittellösung zu vermeiden): Übertragen der Einsätze in eine vormarkierten Platte mit 6 Vertiefungen, die 1,0 ml der Extraktionslösung (Isopropanol), so dass sie nicht eintauchen des Einsatzes.
Hinweis: Führen Sie den gleichen nicht-untergetaucht Extraktion für die entsprechenden Negativ- und Positivkontrollen.
- Verschließen Sie die Platten (zB mit Parafilm zwischen der Plattenabdeckung und die obere Kante der Vertiefungen oder mit einem Standard-Plattenversiegelung). Legen Sie die Platten auf einem Rundplattenschüttler und schütteln Sie für 2 bis 3 Stunden bei Raumtemperatur, um das MTT zu extrahieren.
- Alternativ führen die Extraktion O / N bei 2-876; C im Dunkeln ohne Schütteln.
- Für Nicht-Farbstoff flüssigen Testartikel (untergetaucht Extraktion): Am Ende der Extraktionszeit, dekantieren die Flüssigkeit aus jeder Einsatz zurück in den Brunnen und entsorgen Sie die Einsätze mit RHCE-Gewebe.
- Mischen Sie die Extraktlösung und übertragen zwei 200 ul Aliquots in die entsprechenden Vertiefungen einer pre-markierten 96-Well-Platte nach der Plattenkonfiguration (Abbildung 2).
- Für Feststoffe und Flüssigfarben (nicht unter Wasser Extraktion): Am Ende der Extraktionszeit, entsorgen Sie die Gewebe (stellen Sie sicher nicht, um das Gewebe zu durchdringen).
- 1,0 ml des Extraktionslösung in jede Vertiefung der Platte mit 24 Vertiefungen, die die aus dem Gewebe extrahierten Lösung. Mischen Sie die Extraktionsmittellösung und übertragen zwei 200 ul Aliquots in die entsprechenden Vertiefungen einer pre-markierten 96-Well-Platte nach der Plattenkonfiguration (Abbildung 2).
- Bestimmen Sie ter die optische Dichte (OD) der extrahierten Proben bei einer einzelnen Wellenlänge zwischen 550 und 590 nm auf einem Plattenleser oder einem Spektrophotometer (sollte konsistent innerhalb eines Labors sein).
- Im Falle einer trüben Extraktlösungen von unlöslichen Feststoffen verursacht, Zentrifuge die Lösungen vor der Messung der OD (Abkühlung der Zentrifuge bis 4 ° C, um Verdunstung zu vermeiden). Bei Spülen nicht die Testartikel (TA) zu entfernen und die TA stört MTT-Reduktion, müssen zusätzliche Kontrollen verwendet werden. Bitte beziehen Sie sich auf eine detaillierte SOP für MTT-Reduktion 16 zu korrigieren.
- Falls ein TA gezeigt zu haben oder um Farbe, die mit dem MTT-Messung zusammenwirken können entwickeln, müssen ein zusätzlicher Test durchgeführt, um die Farbmenge zu bindenden bestimmen und anschließend aus dem Gewebe extrahiert. Bitte beziehen Sie sich auf eine detaillierte SOP für farbige Testartikel 16 zu korrigieren.
9. Berechnungen für Gewebeviabilität Test (Tabelle 6 und Abbildung 3) & #160;
- Allgemeine Berechnungen
- Berechnen Sie den mittleren OD-Wert der leere Kontrollvertiefungen (OD Blk) für jedes Experiment.
- Subtrahieren OD Blk von jedem OD-Wert der gleiche Experiment (Schwarzes korrigierten Daten).
- Der Mittelwert der beiden Aliquoten für jedes Gewebe (= korrigierte OD).
- Die prozentuale Lebensfähigkeit von jedem der zwei Wiederholungs Gewebe für jede Kontrolle und Testartikel relativ zu der Durchschnittsnegativkontrolle (100% Kontrolle).
Lebensfähigkeit (%) = [korrigierten OD behandelten Gewebe / korrigierten OD Negative Kontrolle] x 100% - Berechnen Sie die Differenz der Lebensfähigkeit (die Lebensfähigkeit Differenz zwischen zwei Replikat-Gewebe).
- Berechnen Sie die mittlere Testartikel Lebensfähigkeit (TA Lebensfähigkeit) und klassifizieren den Testartikel nach der Vorhersagemodell.
10. Prediction Modell (Abbildung 3)
- Wenn der TA-behandelten Gewebelebensfähigkeit von> 60,0, bezogen auf NC-behandelten Gewebe vAFTUNG, beschriften Sie die Testartikel nicht als reizend (NI) (GHS Keine Kategorie).
- Wenn der TA-behandelten Gewebelebensfähigkeit ist ≤ 60,0, bezogen auf NC-behandelten Gewebelebensfähigkeit, beschriften Sie die Testartikel als reizend (I) (GHS Kategorien 1 und 2).
Hinweis: Die EIT Testergebnisse gelten als qualifiziert, wenn:- das EIT NC OD> 0,8 und <2,5;
- das EIT PC Gewebelebensfähigkeit (%, bezogen auf NC) ist ≤50.0%;
- der Unterschied zwischen den beiden Geweben replizieren (NC, PC und Testartikel) ist <20,0%.
Ergebnisse
Repräsentative EIT Ergebnisse mit 10 Testartikel (TA) und Negativ- und Positivkontrollen durchgeführt, sind in Tabelle 6 und Abbildung 3 dargestellt. Der OD = 1,31 für die NC entspricht 100% Gewebelebensfähigkeit, damit der PC (mittlere OD = 0,41) hatten relativen Gewebelebensfähigkeit von 31,2%. Wenn das EIT-Protokoll wurde in 15 gültigen unabhängigen Experimenten in 7 Labors unter Verwendung des flüssigen Exposition Protokoll und in 8 unabhängige gültige Versuche in 4 Labors, unter Verwendung der festen Exposition Protokoll durchgeführt, die durchschnittliche Gewebelebensfähigkeit für den PC mit der Flüssigkeit Protokoll betrug 36,4 ± 4,0 % bzw. 32,3 ± 6,4% in der Feststoff Protokoll. In allen Fällen waren die positiven Kontrollergebnisse unterhalb des Cut off-Wert von 60,0% 15.
Wie in Figur 3, TA1, TA2, TA4, TA7 gezeigt und TA8 hatten Gewebelebensfähigkeiten> 60,0% und wurden daher als "NI" klassifiziert. TA3, TA5, TA6, hatte TA9 und TA10 Gewebe Bewohnbarkeit X04; 60,0% und damit als "I" klassifiziert. Die Differenz der Gewebelebensfähigkeit zwischen doppelte Gewebe war <20,0% für alle TAs mit Ausnahme von TA2. Daher Ergebnisse für alle Test Artikel, mit Ausnahme von TA2, wurden als "qualifiziert", da sie alle EIT Akzeptanzkriterien (Abschnitt 10.2) erfüllt. Wegen der hohen Variabilität zwischen doppelte Gewebe für TA2 in der anfänglichen Experiment wurde ein zweites Experiment notwendig, qualifizierte EIT Ergebnisse zu erhalten.
Das EIT Testverfahren wie hierin beschrieben, unter Verwendung der RhCE Gewebemodell wurde für die Bewertung der Augenreizung in mehreren multilaboratory Validierungsstudien, einschließlich der formellen Bestätigung durch EURL ECVAM / Cosmetics Europe 15,17-19 verwendet. In allen Studien wurde der EIT gezeigt reproduzierbar sein und konnte Chemikalien (beide Stoffe und Gemische) die Einstufung und Kennzeichnung für Augenreizungen oder schwere Augenschäden ac ohne eigenes korrekt zu identifizierenCording zu UN GHS 15,17-19. Das EIT Testverfahren erfüllt die Akzeptanzkriterien der Validation Management Group (VMG) für die Augenreizung für Sensitivität, Spezifität und Gesamtgenauigkeit und derzeit anhängig ist es formale Umsetzung als teilweiser Ersatz für die in vivo Kaninchen Draize-Test 19.
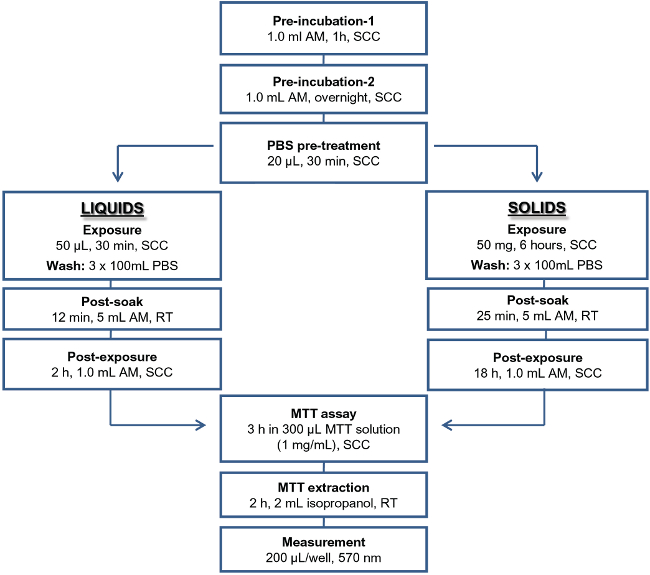
Abbildung 1: Überblick über die EIT-Protokoll für flüssige und feste Testartikel verwendete Abkürzungen: AM, Assay-Medium;. SCC, Standardkulturbedingungen; PBS Dulbecco Phosphat-gepufferter Saline; RT Raumtemperatur.
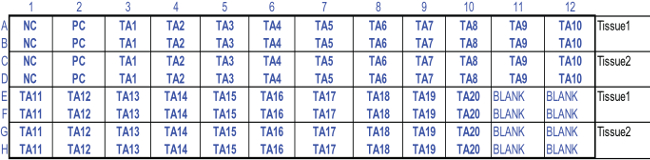
Abb. 2: Die standardisierte 96-Well-Platte-Konfiguration für das MTT Gewebeviabilität Test zwei 200 ul Aliquots sind train die entsprechenden Vertiefungen einer pre-markierten 96-Well-Platte nsferred. Verwendete Abkürzungen: NC, negative Kontrolle; PC, Positivkontrolle; TA1-TA20, Testartikel 20.01; Blank, Extraktionsmittellösung. 96- MTT Plattenkonfiguration ist mit Excel-Tabelle zur RhCE Gewebelebensfähigkeit und EIT Ergebnisse zu berechnen.
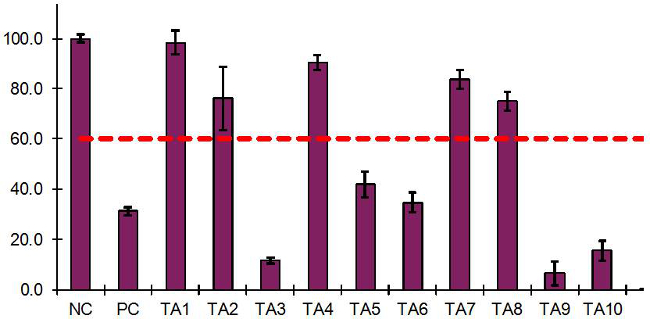
Abbildung 3: EIT-Ergebnisse für 10 Test Artikel, NC und PC-Steuerungen mit RHCE-Gewebemodell erhalten Die Grafik wird aus einer Excel-Tabelle zur EIT Ergebnisse zu präsentieren generiert.. Testchemikalien, die Lebensfähigkeit des Gewebes ≤ 60,0%, bezogen auf NC reduziert werden als Reizstoffe ("I", TA3, TA5, TA6, TA9 und TA10) und Testchemikalien, die Lebensfähigkeit des Gewebes> 60,0% werden als nicht-Reizstoffe eingestuft hatte (klassifiziert " NI ", TA1, TA2, TA4, TA7 und TA8).
| Startzeit für die EIT-Protokoll Arbeitsschritte (ein Tag der Arbeit für einen Operator) | |||||||
| Jede Zeile entspricht einem Paar von Geweben | |||||||
| Reihenfolge der Schritte: | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| Flüssigkeiten: | PBS | TA Belichtung | Post- Durchnässen | Post- Incub. | MTT Reaktion | MTT Extraktion | Maßnahme |
| 30 Minuten | 30 Minuten | 12 min | 120 min | 180 min | 120 min | OD | |
| NC | 9.00 | 9.30 | 10.00 | 10.12 | 0.12 | 15.12 | nach |
| PC | 9.01 | 9.31 | 10.01 | 10.13 | 0.13 | 15.13 | 17.30 |
| TA-1 | 9.02 | 9.32 | 10.02 | 10.14 | 0.14 | 15.14 | |
| TA-2 </ strong> | 9.03 | 9.33 | 10.03 | 10.15 | 0.15 | 15.15 | |
| TA-3 | 9.04 | 9.34 | 10.04 | 10.16 | 0.16 | 15.16 | |
| TA-4 | 9.05 | 9.35 | 10.05 | 10.17 | 0.17 | 15.17 | |
| TA-5 | 9.06 | 9.36 | 10.06 | 10.18 | 0.18 | 15.18 | |
| TA-6 | 9.07 | 9.37 | 10.07 | 10.19 | 0.19 | 15.19 | |
| TA-7 | 9.08 | 9.38 | 10.08 | 10.20 | 0.20 | 15.20 | |
| ng> TA-8 | 9.09 | 9.39 | 10.09 | 10.21 | 0.21 | 15.21 | |
| TA-9 | 9.10 | 9.40 | 10.10 | 10.22 | 0.22 | 15.22 | |
| TA-10 | 9.11 | 9.41 | 10.11 | 10.23 | 0.23 | 15.23 | |
Tabelle 3:. Beispiel Zeitplan für die Prüfung von flüssigen Testartikel Protocol Schritte einschließlich Vorbenetzung die Gewebe mit DPBS, Anwendung von Test-Artikel (TAS), Spülen und Post-tränken, Post-Inkubationszeit MTT-Test, Extraktion von MTT, und Messung der MTT OD in Spalten dargestellt. Zeiten für die Doppelgewebe in Reihen organisiert. Der gesamte Test Test 10 TAs und Kontrollen können in einem Tag abgeschlossen werden.
e_content ">| Startzeit für das EIT Protokollschritte (2 Tage arbeiten für einen Operator) | |||||||
| Jede Zeile entspricht einem Paar von Geweben | |||||||
| Tag 1 | Tag 2 (am nächsten Tag) | ||||||
| Reihenfolge der Schritte: | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| Festkörper: | PBS | TA Belichtung | Post- Durchnässen | Post- Incubaction | MTT Reaktion | MTT Extraktion | Maßnahme |
| 30 Minuten | 6 Stunden | 26 min | 18 Stunden | 180 min | 120 min | OD | |
| NC | 9.00 | 9.30 | 15.30 | 15.56 | 9.56 | 0.56 | nach |
| PC | 9.02 | 9.32 | 15.32 | 15.58 | 09.58 | 0.58 | 15.30 |
| TA-1 | 9.04 | 9.34 | 15.34 | 16.00 | 10.00 | 13.00 | |
| TA-2 | 9.06 | 9.36 | 15.36 | 16.02 | 10.02 | 13.02 | |
| TA-3 | 9.08 | 9.38 | 15.38 | 16.04 | 10.04 | 13.04 | |
| TA-4 | 9.10 | 9.40 | 15.40 | 16.06 | 10.06 | 13.06 | |
| TA-5 | 9.12 | 9.42 | 15.42 | 16.08 | 10.08 | 13.08 | |
| TA-6 | 9.14 | 9.44 | 15.44 | 16.10 | 10.10 | 13.10 | |
| TA-7 | 9.16 | 9.46 | 15.46 | 16.12 | 10.12 | 13.12 | |
| TA-8 | 9.18 | 9.48 | 15.48 | 16.14 | 10.14 | 13.14 | |
| TA-9 | 9.20 | 09.50 | 15.50 | 16.16 | 10.16 | 13.16 | |
| TA-10 | 9.22 | 9.52 | 15.52 | 16.18 | 10.18 | 13.18 | |
Tabelle 4: Beispiel-Zeitplan für die Prüfung von festen Testartikel. Protokoll Schritte einschließlich Vorbenetzung die Gewebe mit DPBS, Anwendung von Test-Artikel, Spülen und Post-tränken, Post-Inkubationszeit MTT-Test, Extraktion von MTT und Messung der MTT OD in Spalten dargestellt. Zeiten für die Doppelgewebe in Reihen organisiert. Der gesamte Test testet 10 TAs und Kontrollen über einen Zeitraum von zwei Tagen durchgeführt.
| Höhe | Reagens | Lagerbedingungen | Ursprung | Bezeichnung | Ablaufdatum |
| 1 Flasche, 2 ml | MTT-Konzentrat (MTT-100-CON) | Unter Lichtschutz (-20 ° C) | MatTek | Gefrorene MTT-Konzentrat | 2 Monate |
| 1 Flasche, 8 ml | MTT Verdünnungs | 2-8 &# 186; C | MatTek | Zum Verdünnen MTT Konzentrat vor der Verwendung in dem MTT-Assay verwenden | 2 Monate |
| 1 Flasche, 60 ml | Isopropanol (CAS # 67-63-0) | RT | Sigma-Aldrich | Extraktionslösung | N / A |
Tabelle 5: MTT-100 Assay Kit Components.
| Code N ° | Gewebe | Rohdaten | Blank korrigierten Daten | Mittelwert der OD | % Der Lebensfähigkeit | ||
| n | Aliq. 1 | Aliq. 2 | Aliq. 1 | Aliq. 2 | |||
| NC | 1 | 1,316 | 1,352 | 1,316 | 1,352 | 1,334 | 101,6 |
| 2 | 1,277 | 1,309 | 1,277 | 1,309 | 1,293 | 98,4 | |
| PC | 1 | 0,379 | 0,397 | 0,379 | 0,397 | 0,388 | 29,6 |
| 2 | 0,419 | 0,442 | 0,419 | 0,442 | 0,431 | 32,8 | |
| TA1 | 1 | 1,213 | 1,244 | 1,213 | 1,244 | 1,229 | 93,5 |
| 2 | 1,355 | 1,355 | 1,355 | 1,355 | 1,355 | 103,2 | |
| TA2 | 1 | 1,210 | 1,122 | 1,210 | 1,122 | 1,166 | 88,7 |
| 2 | 0,828 | 0,837 | 0,828 | 0,837 | 0,833 | 63,4 | |
| TA3 | 1 | 0,167 | 0,168 | 0,167 | 0,168 | 0,167 | 12,7 |
| 2 | 0,138 | 0,136 | 0,138 | 0,136 | 0,137 | 10.4 | |
| TA4 | 1 | 1,137 | 1,160 | 1,137 | 1,160 | 1,149 | 87,4 |
| 2 | 1,262 | 1,191 | 1,262 | 1,191 | 1,227 | 93,4 | |
| TA5 | 1 | 0,610 | 0,621 | 0,610 | 0,621 | 0,616 | 46,9 |
| 2 | 0,480 | 0,484 | 0,480 | 0,484 | 0,482 | 36,7 | |
| TA6 | 1 | 0,502 | 0,513 | 0,502 | 0,513 | 0,508 | 38,7 |
| 2 | 0,396 | 0,407 | 0,396 | 0,407 | 0,402 | 30,6 | |
| TA7 | 1 | 1,048 | 1.050 | 1,048 | 1.050 | 1,049 | 79,9 |
| 2 | 1,149 | 1.150 | 1,149 | 1.150 | 1.150 | 87,5 | |
| TA8 | 1 | 1,032 | 1,034 | 1,032 | 1,034 | 1,033 | 78,7 |
| 2 | 0,941 | 0,935 | 0,941 | 0,935 | 0,938 | 71,4 | |
| TA9 | 1 | 0,022 | 0,022 | 0,022 | 0,022 | 0,022 | 1.7 |
| 2 | 0,144 | 0,149 | 0,144 | 0,149 | 0,147 | 11.2 | |
| TA10 | 1 | 0,150 | 0,150 | 0,150 | 0,150 | 0,150 | 11.4 |
| 2 | 0,254 | 0,255 | 0,254 | 0,255 | 0,255 | 19,4 | |
| bedeuten | Dif. | Mittelwert | Dif. | Dif. / 2 | Klassifikation | ||
| der OD | der OD | Bewohnbarkeit [%] | der Bewohnbarkeit | ||||
| NC | 1,314 | 0,041 | 100,0 | 3.12 | 1.56 | NI | qualifiziert |
| PC | 0,410 | 0,043 | 31,2 | 3.23 | 1.62 | ICH | qualifiziert |
| TA1 | 1,292 | 0,127 | 98,3 | 9.63 | 4.81 | NI | qualifiziert |
| TA2 | 0,999 | 0,333 | 76,1 | 25,36 | 12.68 | NI | D> 20 |
| TA3 | 0,152 | 0,030 | 11,6 | 2.32 | 1.16 | ICH | qualifiziert |
| TA4 | 1,188 | 0,078 | 90,4 | 5.94 | 2.97 | NI | qualifiziert |
| TA5 | 0,549 | 0,134 | 41,8 | 10,16 | 5.08 | ICH | qualifiziert |
| TA6 | 0,455 | 0,106 | 34,6 | 8.07 | 4.03 | ICH | qualifiziert |
| TA7 | 1.100 | 0,101 | 83,7 | 7.65 | 3.82 | NI | qualifiziert |
| TA8 | 0,986 | 0,095 | 75,0 | 7.23 | 3.62 | NI | qualifiziert |
| TA9 | 0,085 | 0,125 | 6.4 | 9.48 | 4.74 | ICH | qualifiziert |
| TA10 | 0,203 | 0,105 | 15,4 | 7.95 | 3.98 | ICH | qualifiziert |
Tabelle 6:. Für 10 Testartikel erhalten EIT Ergebnisse, NC und PC-Steuerungen Die Tische sind proddurch eine Excel-Tabelle entworfen, um die Lebensfähigkeit des Gewebes und EIT Ergebnisse zu berechnen uced. Testchemikalien, die Lebensfähigkeit des Gewebes ≤ 60,0%, bezogen auf NC reduziert werden als Reizstoffe ("I", TA3, TA5, TA6, TA9 und TA10) und Test-Chemikalien, die Lebensfähigkeit des Gewebes> 60,0% werden als nicht-Reizstoffe eingestuft hatte (klassifiziert " NI ", TA1, TA2, TA4, TA7 und TA8).
Diskussion
Wir haben den Test auf Augenreizung (Abbildung 1), die für die EpiOcular Gewebemodell entwickelt wurde, vorgestellt. Das ETI ist in der Lage, die Augen reizenden und ätzenden Stoffen (GHS Kategorien 1 und 2 kombiniert) aus Materialien, die keine Kennzeichnung (GHS Keine Kategorie) mit hoher Sensitivität und Spezifität 17. Das EIT zu trennen, wie sie hier vorgestellt wird nicht zwischen GHS-Kategorie unterscheiden 1 von Kategorie 2 Chemikalien. Das EIT wurde für die Einstufung und Kennzeichnung von Augenreizungspotenzial von einer breiten Palette von Chemikalien, einschließlich kosmetischen und pharmazeutischen Inhaltsstoffen validiert. In Verbindung mit anderen in vitro-Tests wird das EIT als Ersatz für die in-vivo-Kaninchenaugenreiztest dienen.
Das EIT verwendet zwei ähnliche, aber unterschiedliche Protokolle für flüssige und feste Materialien, die in der Länge der Exposition und der Nachbelichtung Inkubationszeiten (Figur 1) variieren. Die in der EIT verwendet Endpunktist die Lebensfähigkeit des Gewebes, durch das MTT-Assay, der zuvor in validierten menschlichen Epithelgewebe Modelle 20,21 verwendet wurde bestimmt. Um diesen Test durchzuführen, wird keine spezielle Ausrüstung neben Standard-Zellkultur Ausrüstung benötigt. Aufgrund der hohen Gewebe zu Gewebe Reproduzierbarkeit, n = 2 Geweben anstelle der Regel empfohlen, n = 3 verwendet. Der Fähigkeit zur Nutzung n = 2 Geweben ist ein kritischer Aspekt des Protokolls, denn sie erlaubt es einem erfahrenen Bediener, zwei Gewebe gleichzeitig zu verarbeiten, wodurch die Variabilität des Assays, die entstehen, minimiert aufgrund der unterschiedlichen Handhabung von einzelnen Tissues 14. Auch durch Verwendung von n = 2 Geweben pro Testartikel, die Reizwirkung von 10 Testsubstanzen der gleichen physikalischen Zustand (flüssig oder fest), zusammen mit den positiven und negativen Kontrollen, unter Verwendung von einem Satz (24 Gewebe) ausgewertet werden.
Andere wichtige Punkte, die zuverlässige Klassifizierung von Materialien gewährleisten Spezifikationen für die positive Kontroll substance (Gewebeviabilität ≤50.0%), Reproduzierbarkeit zwischen doppelte Gewebe (Differenz <20,0%) und negative Kontrolle OD-Ablesungen (> 0,8 und <2,5).
Bei der Durchführung des EIT-Test, ist es wichtig, auf die validierten Protokoll und der vorgeschlagenen Dosierung und Spülen Pläne (Tabellen 3 und 4) zu halten, da Abweichung vom Protokoll oder Änderungen der Inkubationszeiten kann zu veränderten Ergebnissen führen. Ebenso werden Abweichungen von der 3 Stunden Zeit für MTT Inkubation in verschiedenen MTT Lesungen führen und Assay-Ergebnis auswirken.
Gelegentlich kann eine Testchemikalie müssen optische oder andere Eigenschaften, die mit MTT Gewebelebensfähigkeitstest oder verursachen Reduktion von MTT stören können. Zum Beispiel kann eine Testchemikalie direkt MTT in blau-lila-Reaktionsprodukt, oder sie kann eine gefärbte Substanz, die Licht in der gleichen Größenordnung wie MTT Formazan (~ 570 nm) absorbiert werden. Allerdings werden diese Testchemikalien prESENT nur ein Problem, wenn zum Zeitpunkt des MTT-Tests, ist immer noch eine ausreichende Menge des Materials auf den heutigen (oder absorbiert) des Gewebes. Um diese Störungen zu vermeiden, sind umfangreiche Spülvorgänge in den EIT-Protokoll einbezogen. Wenn Spülen nicht entfernen Sie die TA und die TA stört MTT-Reduktion, müssen zusätzliche Kontrollen verwendet werden, zu erkennen und zu korrigieren ist. Kurz gesagt, wenn eine direkte MTT-Reduktion der Prüfsubstanz wird vermutet, 50 ul (oder 50 mg für Feststoffe) der betreffenden Chemikalie wird 3 h mit Arbeits MTT-Lösung bei SCC (NC 50 ul sterilem, entionisiertem Wasser inkubiert wird, sollte gleichzeitig laufen). Wenn der MTT Lösung blau-violett, ist der Testgegen vermutlich das MTT reduziert. In diesem Fall ist eine Funktionsprüfung mit gefrier getötet Gewebekontrollen durchgeführt werden sollte, um zu bewerten, ob das Testmaterial auf die Gewebebindung und zu einer falschen MTT-Reduktionssignal. Wenn es nennens MTT-Reduktion in der TA-ausgesetzt, getötet Gewebekontrolle(relativ zu der Menge bei der unbehandelten lebensfähiges Gewebe), muß die mittlere Gewebelebensfähigkeit des Testgegenstands durch Subtrahieren der mittleren Überlebensfähigkeit des getötet Steuerung korrigiert werden.
Das EIT irrt auf der Seite der Sicherheit, wie durch die niedrige Inzidenz von falsch negativen Klassifikationen 14,15,18 gezeigt. Wichtig ist, dass keiner der GHS-Kategorie 1 Chemikalien, die ätzend auf die Augen sind und stellen den schwersten Augengefahr, wurden als nicht reizend in diesem Assay 14,15,18,19 klassifiziert. Schließlich ist einer der Hauptvorteile des RhCE in vitro-Testverfahren die Möglichkeit der Prüfung reine Flüssigkeit und festen Materialien (die nicht mit zweidimensionaler, untergetaucht Zellkulturen möglich ist).
Das EIT wird bei der Bestimmung des Augenreizungspotenzial von einer breiten Palette von Materialien gemäß der UN GHS Einstufung und Kennzeichnung System einen wichtigen Beitrag. Der Ersatz von Tieren o bestimmen,sondere Toxizität ist seit vielen Jahren ein Ziel der toxikologischen Forschung. Das EIT Testmethode hat eine formelle Validierungsstudie durch EURL ECVAM unterstützt im Jahr 2014 abgeschlossen und die EpiOcular EIT wurde im Jahr 2015 in den Testleitlinien der OECD OECD TG 492 implementiert.
Offenlegungen
Publikationskosten für diesen Artikel wurden von MatTek Corporation, bezahlt.
Danksagungen
Die Autoren bedanken sich bei Dr. John Harbell für seine wissenschaftliche Unterstützung und Zeit für das ETI-Projekt gewidmet danken. Die Autoren möchte auch danken, Beiersdorf AG (Deutschland), IIVS (USA), Mary Kay Inc. (USA), Avon Products Inc. (USA), Procter & Gamble / Cosmital (Schweiz), Laboratoire Pierre Fabre (Frankreich), Harlan Laboratories (Vereinigtes Königreich), und LVMH Parfume (Frankreich) für die Teilnahme an multizent Internationale Pre-und Validierungsstudien der Test auf Augenreizung 15.
Referenzen
- National Toxicology Program (NTP) Interagency Center for the Evaluation of Alternative Toxicological Methods (NICEATM). Request for Ocular Irritancy Test Data From Human, Rabbit, and In Vitro Studies Using Standardized Testing Methods. Federal Register. 72 (109), 31582-31583 (2007).
- . Regulation (EC) No 1907/2006 of the European Parliament and of the Council of 18 December 2006 concerning the Registration, Evaluation, Authorisation and Restriction of Chemicals (REACH), establishing a European Chemicals Agency, amending Directive 1999/45/EC and repealing Council Regulation (EEC) No 793/93 and Commission Regulation (EC) No 1488/94 as well as Council Directive 76/769/EEC and Commission Directives 91/155/EEC, 93/67/EEC, 93/105/EC and 2000/21/EC. OJ. L396 (49), 1-849 (2006).
- . . Globally Harmonized System of Classification and Labelling of Chemicals (GHS). , (2013).
- Draize, J. H., Woodard, G., Calvery, H. O. Methods for the Study of Irritation and Toxicity of Substances Applied Topically to the Skin and Mucous Membranes. J Pharmacol Exp Ther November. 82, 377-390 (1944).
- Adriaens, E. Retrospective analysis of the Draize test for serious eye damage/eye irritation: importance of understanding the in vivo endpoints under UN GHS/EU CLP for the development and evaluation of in vitro test methods. Arch tox. 88, 701-723 (2014).
- Balls, M., Botham, P. A., Bruner, L. H., Spielmann, H. The EC/HO international validation study on alternatives to the Draize eye irritation test. Toxicol in Vitro. 9, 871-929 (1995).
- Curren, R. D., Harbell, J. W. Ocular safety: a silent (in vitro) success story. Altern Lab Anim. 30, 69-74 (2002).
- Wilhelmus, K. R. The Draize Eye Test. Survey of Ophthalmology. 45, 493-515 (2001).
- Curren, R. D., Harbell, J. W. In vitro alternatives for ocular irritation. Environ health persp. 106, 485-492 (1998).
- McCain, N. E., Binetti, R. R., Gettings, S. D., Jones, B. C. Assessment of ocular irritation ranges of market-leading cosmetic and personal-care products using an in vitro tissue equivalent. Toxicologist. 66, 243 (2002).
- Niranjan, P., Dang, A. H., January, B. G., Gomez, C., Harbell, J. W. Use of the EpiOcular assay for preclinical qualification of formulas for human clinical studies. Toxicologist. 96, 249 (2007).
- Yin, X. J. Prediction of ocular irritation potential of surfactants-based formulations at different concentrations using the EpiOcular model. Toxicologist. 108, 378 (2009).
- Harbell, J., Curren, R. In vitro methods for the prediction of ocular and dermal toxicity. Handbook of Toxicology. , (2001).
- Kaluzhny, Y. Development of the EpiOcular(TM) eye irritation test for hazard identification and labelling of eye irritating chemicals in response to the requirements of the EU cosmetics directive and REACH legislation. Altern Lab Anim. 39, 339-364 (2011).
- Pfannenbecker, U. Cosmetics Europe Multi-Laboratory Pre-Validation of the EpiOcular Reconstituted Human Tissue Test Method for the Prediction of Eye Irritation. Toxicol in vitro. , (2013).
- MatTek Corporation. . EpiOcular™ Eye Irritation Test (OCL-200-EIT) for the prediction of acute ocular irritation of chemicals for use with Reconstructed Human EpiOcular Model (OCL-200-EIT). Protocol#MK-24-007-0055. , (2014).
- Kaluzhny, Y. EpiOcular Eye Irritation Test (EIT) for Hazard Identification and Labeling of Eye Irritating Chemicals: Protocol Optimization for Solid Materials and Extended Shipment Times. Altern Lab Anim. 43 (2), 101-127 (2015).
- Kolle, S. N., Kandarova, H., Wareing, B., van Ravenzwaay, B., Landsiedel, R. In-house validation of the EpiOcular(TM) eye irritation test and its combination with the bovine corneal opacity and permeability test for the assessment of ocular irritation. Altern Lab Anim. 39, 365-387 (2011).
- . Reconstructed Human Cornea-like Epithelium (RhCE) Test Method for Identifying Chemicals Not Requiring Classification and Labelling for Eye Irritation or Serious Eye Damage. Draft proposal for a new test guideline.. OECD Guideline for the Testing of Chemicals. , (2014).
- Blazka, M. E., Harbell, J. Evaluating the ocular irritation potential of 54 test articles using the EpiOcular Human tissue Construct Model. Toxicol. In Vitro. , (2003).
- Kandarova, H. The EpiDerm Test Protocol for the Upcoming ECVAM Validation Study on In Vitro Skin Irritation Tests — An Assessment of the Performance of the Optimised Test. Altern Lab Anim. 33, 351-367 (2005).
Nachdrucke und Genehmigungen
Genehmigung beantragen, um den Text oder die Abbildungen dieses JoVE-Artikels zu verwenden
Genehmigung beantragenThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Alle Rechte vorbehalten