Se requiere una suscripción a JoVE para ver este contenido. Inicie sesión o comience su prueba gratuita.
Method Article
Generación de hielo y la transferencia de calor y masa fenómenos de introducción de agua a un baño de agua fría de salmuera
En este artículo
Resumen
A continuación, se presenta un protocolo para demostrar la generación de hielo cuando el agua se introduce en un baño de agua fría de salmuera, como refrigerante secundario, en un rango de temperaturas muy por debajo del punto de congelación del agua. Se puede usar como una forma alternativa de producir hielo para la industria.
Resumen
Se demuestra un método para el estudio de la calor y transferencia de masa y de los fenómenos de congelación en un entorno de salmuera subenfriado. Nuestro experimento mostró que, en las condiciones adecuadas, el hielo se puede producir cuando el agua se introduce en un baño de salmuera fría. Para hacer que forma el hielo, además de tener la mezcla de salmuera y agua, la tasa de transferencia de calor debe pasar por alto que el de la transferencia de masa. Cuando se introduce agua en forma de pequeñas gotas a la superficie de la salmuera, el modo de transferencia de calor y masa es por difusión. La flotabilidad se detiene el agua se mezcle con la salmuera por debajo, pero a medida que el hielo se espesa, se ralentiza la velocidad de transferencia de calor, hacer hielo más difíciles de cultivar como resultado. Cuando se introduce agua en el interior de la salmuera en forma de un flujo, una serie de factores se encuentran para influir en la cantidad de hielo puede formar. la temperatura y la concentración de salmuera, que son las fuerzas impulsoras de la transferencia de calor y masa, respectivamente, pueden afectar a la ratificación de conversión de agua-hieloo; más bajas temperaturas del baño y las concentraciones de salmuera animan más hielo a la forma. La reología de flujo, que puede afectar directamente tanto el calor y coeficientes de transferencia de masa, es también un factor clave. Además, la reología de flujo cambia el área de contacto de la corriente con el fluido a granel.
Introducción
Lechadas de hielo se utilizan ampliamente en la industria, y una aplicación particularmente exitosa es la tecnología de rascado de hielo 1, 2. En comparación con la espuma convencional y cerdo sólido, el cerdo de hielo puede viajar a través de topologías complejas a larga distancia, debido al efecto de lubricación de la fase líquida y la elevación de su punto de congelación como algunos de los cristales de hielo se derriten 3, 4, 5 . Incluso si el cerdo se queda atascado, uno puede simplemente esperar a que las lechadas de hielo se derrita y reanudar el proceso de limpieza posterior. Este método de limpieza de tuberías es barato y fácil de usar.
La fracción de hielo juega un papel clave en el rendimiento del cerdo hielo. Para medir la fracción de hielo, se puede usar una cafetera de émbolo (prensa francesa) para determinar si la suspensión de hielo es lo suficientemente gruesa 6,"> 7. Una fracción de hielo de alta cafetera, típicamente 80%, se requiere en la realización de pigging hielo. La investigación reciente en la detección fracción de hielo en línea mostró que ambas ondas electromagnéticas y ultrasónicos son adecuados para el trabajo 8, 9, 10, 11.
El cerdo de hielo se hace generalmente por una máquina de hielo de superficie raspada de una solución de NaCl al 5% en peso (salmuera). También es la forma principal de hacer lechadas de hielo en la industria. Este tipo de máquina de hielo se congela el agua o salmuera sobre una superficie metálica fría, típicamente una superficie lisa de acero 316 y luego cizalla cíclicamente las partículas de hielo fuera. Las interfaces-líquido-metal son muy complejos y se ven afectados por una amplia gama de factores que son esenciales para la fabricación de hielo 12. La interfaz entre no metal y el agua pueden ser muy diferentes, y un ejemplo especialmente interesante es caolinita. el Kaolunión entre el agua Inite es especial porque no hay una estructura de hielo favorable adyacente a la superficie del sólido, sino más bien una capa de fluido sustrato anfótero que anima a los enlace de hidrógeno similares al hielo que se forman en la parte superior de la misma 13, 14. Otra forma de producir el cerdo de hielo requiere aplastar a los bloques de hielo prefabricados, mientras que se añadió salmuera de alta concentración de forma simultánea. Para este método, el sistema de refrigeración puede funcionar a una temperatura de evaporación mucho más alta porque no depresor del punto de congelación (FPD) se añade antes de la formación de hielo; por lo tanto, se considera más eficaz debido a la relación de compresión baja y energía reducido para un destino determinado de enfriamiento 15, 16, 17.
Hay otros dos métodos de producción de hielo: la producción de hielo de agua-enfriada y poniendo el refrigerante y el agua en contacto directo 18, 19. El método implica sobreenfriamiento perturbar el agua supercooled metaestable para generar la nucleación del hielo y el crecimiento. El mayor problema de este método es la formación de hielo no deseado que puede bloquear el sistema. El método de contacto directo es considerado no apto para limpieza con tacos de hielo debido a que ni el refrigerante ni aceite de lubricación se desean en el producto final de hielo.
La formación de hielo requiere calor y transferencia de masa debido al calor latente de fusión generado en el proceso. Fue descubierto por primera vez por Osborn Reynolds en 1874 que el transporte de calor y masa en los gases están fuertemente acoplados y se puede expresar en fórmulas matemáticas similares 20. Este trabajo formó el trabajo pionero sobre el tema del momento, el calor y transferencia de masa en los fluidos y fue reimpreso varias veces 21, 22. A continuación, este tema fue estudiado por unnúmero de otros, de ambos enfoques analíticos y empíricos, para los gases, líquidos y de metal fundido 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33. Aparte de la transferencia de calor y masa, el fluido necesita puntos de nucleación de hielo donde el crecimiento dendrítico puede desarrollar. Una visión moderna en el crecimiento de cristales de hielo utiliza Ley Constructal, desarrollado por Adrian Bejan, para explicar por qué el hielo crece de este modo 34, 35, 36.
La formación de hielo en salmuera es muy diferente de la de agua pura debido a la existencia de sal. Ante todo, sal cambia la termodinámica del fluido y deprime su punto de congelación. En segundo lugar, la sal no puede disolverse en la matriz de hielo (excepto para hydrohalite, que sólo puede formar cuando la temperatura alcanza el punto eutéctico), y se rechazó el líquido mayor cuando el hielo comienza a crecer. El rechazo de la sal fue descubierta en tanto el hielo marino y el hielo estudiado en el laboratorio 37, 38. Desde la salmuera de alta concentración rechazado está a una temperatura muy por debajo del punto de congelación del agua de mar, a medida que desciende, el hielo crece en la interfaz entre la salmuera que fluye y el fluido de mayor reposo. Estas estalactitas de hielo, también llamado brinicles, fueron descubiertos por primera vez en el estrecho de McMurdo, en la Antártida y se estudiaron experimentalmente 39, 40, 41, 42. En 2011, la BBC filmó la formación de brinicles en su serie Frozen Planet"xref"> 43, 44.
En nuestro laboratorio, se descubrió que mediante la inversión de los fluidos que fluyen y quiescentes cuando se introduce agua a un baño de salmuera fría, el agua puede transformarse en hielo bajo las condiciones correctas 45. Se encontró que la ubicación donde se introduce el agua, la reología de flujo y temperatura de la salmuera y la concentración son factores clave que influyen en la cantidad de hielo se puede producir. El objetivo general de este estudio es investigar si una máquina de hielo puede ser desarrollado a través de este mecanismo para generar lechadas de hielo, teniendo en cuenta que la temperatura del evaporador elevado y la alta tasa de transferencia de calor líquido-líquido pueden mejorar la eficiencia de uso de energía. Este artículo comparte aspectos clave del experimento.
Access restricted. Please log in or start a trial to view this content.
Protocolo
Precaución: Hay dos productos químicos tóxicos, metanol y etilenglicol, que se utilizan en estos experimentos. El metanol puede ser metabolizado en el cuerpo humano para generar formaldehído y luego en ácido fórmico o sal de formiato. Estas sustancias son venenosas para el sistema nervioso central y pueden incluso provocar la muerte. El etilenglicol se puede oxidar al ácido, que entonces se puede convertir en ácido oxálico glicólico. Esto puede causar insuficiencia renal y la muerte. No beber estos productos químicos. Consulte a un médico inmediatamente si se produce un accidente.
1. El Sistema de refrigeración
NOTA: Es muy difícil mantener la salmuera a -18 ° C o menos cuando la temperatura ambiente es más o menos a temperatura ambiente. Es importante que los tanques de almacenamiento de glicol de etileno y salmuera son bien aisladas y de un tamaño razonable para evitar el exceso de consumo de electricidad y para garantizar un rendimiento óptimo del sistema. Se recomienda que el tamaño del tanque no exceda de 30 L.
- Preparar el líquido de enfriamiento secundario
- Verter 1 litro de etilenglicol en el tanque de enfriamiento secundario, Tanque A (base: 400 mm x 200 mm, Altura: 350 mm). Añadir aproximadamente 0,6 a 0,65 L (600-650 g) de agua al tanque A.
- Repita el paso 1.1.1 varias veces hasta que haya suficiente líquido en el tanque A (25 L).
- Se agita el fluido de manera que el fluido es homogéneo.
- Encender las dos bombas en el tanque de la A a la creación de capacidad máxima (2.500 l / h). Asegúrese de que todas las burbujas atrapadas en los intercambiadores de calor y los tubos son liberados.
- Apagar la bomba para observar si todas las burbujas se liberan. Si no es así, repita el paso 1.1.4.
- Preparación de la salmuera
NOTA: En este ejemplo, se prepara 22% en peso de salmuera. Si se necesitan otras concentraciones, la masa de sal agregada también debería ser modificada en consecuencia. Los valores de concentración y densidad de la salmuera de referencia se pueden encontrar en la página D-257 de la 64ª edición (1983) de THCRC Handbook correo de Química y Física 46.- Añadir 4 kg de agua en un vaso de precipitados de plástico de 5 L.
- Medida 1 kg de sal de NaCl en una balanza electrónica y se vierte esta sal en el vaso con el agua.
- Se agita la mezcla hasta que la solución es transparente (es decir, no hay partículas de sal o burbujas de agua visible en la solución).
- Tomar una muestra, ~ 10 ml, de la solución usando una jeringa de 10 ml.
- Inyectar el líquido en el medidor de densidad de tubo en U.
- Compruebe si hay burbujas de aire en el tubo. Si los hay, inyectar más fluido para empujar hacia fuera.
- Presione "Configuración rápida" y seleccione "Densidad de temperatura." Tipo de 20 ° C y pulse "OK". El medidor de densidad ahora medir la densidad del fluido a esta temperatura.
- Pulse Iniciar y esperar el resultado.
- Compare la lectura de la densidad con 1164,00 kg / m3.
- Añadir más sal si la lectura está por debajo del COMPARACIÓNDensidad n. Añadir agua si es de otra manera.
- Repita los pasos 1.2.3-1.2.10 hasta que la densidad del fluido es correcto (1164.00 kg / m 3).
- Verter esta solución en un recipiente más grande, Container A.
- Siga los pasos para hacer 1.2.1-1.2.12 35-40 l de salmuera y poner Container A en un congelador a -40 ° C. Mantenga la salmuera allí durante 48-72 horas, hasta que su temperatura alcanza -19,18 ° C (punto de este 22% en peso de salmuera congeladora).
2. Preparación del hielo para el agua de lavado y Inyectar
- Preparar el hielo para la inyección de agua
- Verter 1 L de agua en un recipiente pequeño (200 × 200 × 50 mm).
- Repita el paso 2.1.1 con otro recipiente y coloque los dos contenedores en el congelador a -40 ° C.
- Mantener en el congelador durante 10 horas o más para asegurarse de que toda el agua se congela.
- Preparar capa de hielo de agua de lavado
- Llenar un 5-L vaso de precipitados con 5 L de agua.
- Llenar un 2-L vaso de precipitados con 2 L de agua.
- Coloque ambos vasos en el congelador a -40 ° C durante 8-10 h, de modo que hay una cáscara gruesa envoltura de hielo en torno al agua no congelada.
- Utilizar un chorro de agua a alta velocidad a una velocidad de 3-5 m / s de la llave para abrir un agujero de 3 cm de diámetro en la parte superior de la capa de hielo.
- Escurrir el agua dentro de la capa de hielo.
- Ponga los dos vasos de precipitados de nuevo en el congelador.
- Si la masa de la capa de hielo no llega a 3 kg y 1 kg para los dos vasos de precipitados, respectivamente, repita los pasos 2.2.1-2.2.5, pero mantener los vasos en el congelador ya en el paso 2.2.3. Los dos vasos de precipitados ahora deben ser capaces de contener 2 L y 1 L de agua, respectivamente.
3. El agua Introducción La posición y el experimento de control de reología
- Introducir agua en la superficie salmuera
- Decantar 2 L de 22% en peso de salmuera fría del recipiente A en elcubo de aluminio de la máquina para hacer helados y el interruptor de la unidad de refrigeración.
- Medir la temperatura de la salmuera con un termómetro / termopar (ya sea tipo K o de tipo T son adecuados). Continuar el experimento si la salmuera es de -15 ° C o menos.
- Llenar la jeringa de vidrio de 100 ml con agua del grifo a temperatura ambiente. Adjuntar un diámetro de 2 mm interno, de espesor 1 mm, y 1-m tubo largo de silicona a la punta de la jeringa.
- Coloque la jeringa en una posición específica de tal manera que hay una cabeza entre el agua en la jeringa y la salida del tubo de silicona. La presión hidrostática se apriete el agua fuera del tubo.
- Sumergir una cierta longitud del tubo de silicona, por lo general de 70 cm, en la salmuera.
- Ajustar la posición relativa entre la jeringa y la salida de tubo de modo que la presión hidrostática es suficientemente grande para permitir que el agua para salir de la jeringa. Si el tubo está bloqueado, aumentar la cabeza mediante la elevación de la jeringa a una posición vertical superior, until la presión hidrostática puede superar la tensión de corte dentro del tubo.
- Mantenga el tubo de salida de aproximadamente 1 cm o menos por encima de la superficie de la salmuera.
- Ajustar la longitud del tubo sumergido y de la altura de la jeringa para controlar la salida del agua deja la temperatura y la velocidad de flujo con el fin de determinar la cantidad de hielo puede ser producida o la cantidad de mezcla se produce en la superficie salmuera. El fenómeno de congelación ahora debe observarse en la superficie salmuera. Véase la referencia 45 para más instrucciones.
- Introducir agua a través de la salmuera
- Repita los pasos 3.1.1-3.1.6.
- Mantenga la salida del tubo dentro de la salmuera, de preferencia en la parte inferior del recipiente.
- Ajuste de la longitud del tubo sumergido y de la altura de la jeringa.
- Ajustar el ángulo de la salida del tubo para controlar la reología de la corriente.
- Repita los pasos 3.2.3-3.2.4 para encontrar la mejor reología de flujo acoplado y la velocidad que puede producir la mayor parte del hielo fluir.
4. Producción de hielo, Colección, y Medición
- hacer hielo
- Si hay burbujas en los tubos, encender las dos bombas en el interior del tanque de A a liberar las burbujas fuera del sistema de circulación de glicol, y luego apagar las bombas.
- Se encienden las tres unidades de refrigeración y dejar correr durante 10-16 h para enfriar las soluciones de glicol de etileno.
- Medir la solución de etilenglicol con un termómetro / termopar. La temperatura de glicol debe ser aproximadamente a -25 ° C.
- Medir la temperatura de la salmuera en el recipiente A para asegurarse de que está a -19 ° C antes de proceder al paso 4.1.5.
- Llenar el tanque de salmuera, Tanque B, con aproximadamente 30 l de salmuera del recipiente A y el interruptor de las dos bombas en el tanque A.
- Medir la temperatura del glicol en el Tanque A. Si es más frío que -19 ° C, apagar una o más unidades de refrigeración para evitar la precipitación de partículas de hielo fuera de los intercambiadores de calor in tanque B. Si la temperatura es más caliente que la temperatura de la salmuera se esperaba, a su vez en las tres unidades de refrigeración. Llevar a cabo el experimento a -17 ° C a -19 ° C.
- Coloque los dos bloques prefabricados de hielo desde el paso 2.1 en el aislamiento de 5 litros vaso de precipitados, de contenedores B, y vierta más o menos 3 litros de agua en el vaso de precipitados.
- Medir la temperatura del agua y la mantendrá a 2 ° C por agitación de la mezcla entre los experimentos si la temperatura sube.
- Llene la jeringa de vidrio con 100 ml de agua 2 ° C.
- Aplicar 5-10 ml de metanol a la ventana de cristal de tanque B para detener la condensación y la formación de hielo.
- Inyectar el agua en la salmuera mediante el ajuste de la posición relativa entre la jeringa y la salida del tubo de manera que existe una presión hidrostática constante y por lo tanto una velocidad de flujo constante. Cerca de 70 cm del tubo de silicona deben ser sumergidas en la salmuera. Ajustar el ángulo de inyección para 0 °, de modo que la velocidad inicial de agua en la extrema hacia arribacción es 0 m / s.
NOTA: La jeringa puede ser o sujeto a un soporte de mano. De mano es más apropiado cuando la temperatura de la salmuera es más frío, porque se necesita más tiempo para ajustar un soporte, y el hielo puede bloquear la trompa. Mantenga la reología flujo constante durante todo el experimento, garantizando una velocidad de flujo y la inyección de ángulo constante (0 °) y manteniendo la frontera de congelación de aproximadamente 3 cm por encima de la salida del tubo. No deje que el flujo de entrar en la región en la que comienza a girar turbulenta 47. Véase la referencia 45 para más instrucciones. - Recoger el hielo como se describe en los pasos 4.2 y 4.3. Repita los pasos 4.1.8 - 4.1.11 a diferentes temperaturas de salmuera.
- Recoger el hielo producido y estimar la cantidad de hielo se produce (colección seco)
- Coloque un recipiente (200 × 200 × 50 mm) en la escala de cero y la lectura pulsando el botón "Activar" botón.
- Utilizar el tamiz para recoger el hielo y quitarse de encimala salmuera.
- Ponga este hielo en el recipiente. Medir la masa del hielo usando la escala.
- Después de que se derrita el hielo, utilizar la jeringa de 10 ml para tomar una muestra. Inyectar esta muestra de líquido en el medidor de densidad.
- Realice los pasos 1.2.6-1.2.9.
- Registre la lectura de la densidad.
- Calcular la masa neta de agua de su densidad (es decir, la masa de agua convertida en hielo) utilizando la siguiente fórmula:
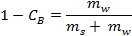
dónde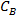 es la concentración de la salmuera en% en peso y
es la concentración de la salmuera en% en peso y 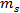 y
y 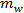 son las masas de sal y agua, respectivamente.
son las masas de sal y agua, respectivamente.
- Recoger el hielo producido y estimar la cantidad de hielo se produce (recogida en húmedo)
- Llenar el vaso de precipitados de 5-L con una capa de hielo (paso 2.2) a temperatura ambiente y el agua del grifo. Poner de nuevo en el congelador a -40 ° C.
- Decantar el agua con la capa de hielo de la 5-L en un vaso de precipitados de 2-L vaso de precipitados cuando su temperatura es de al 0 ° C. Llenar el vaso de precipitados de 5 l. Mantenga los dos vasos en el congelador.
- Saca la hielo producido en los pasos 4.1.8 y 4.1.9 y verter 200-500 ml de agua de la 2-L vaso de precipitados sobre el hielo para lavarlo. No agite el tamiz antes de aplicar el agua a 0 ° C.
- Sacudir el líquido en el tamiz.
- Repita los pasos 4.2.2-4.2.7.
Access restricted. Please log in or start a trial to view this content.
Resultados
La Figura 1 compara los efectos de agua introducida en la superficie de la salmuera con el agua inyectada a través de la salmuera. En el escenario de "capa de hielo", el hielo que se forma es sólida porque el agua no se mezclaba mucho con el fluido a granel. La diferencia de temperatura y la densidad entre los dos fluidos genera fuerza de flotabilidad en el agua e impide la mezcla. Ambos fluidos son estáticas (es decir, la transferencia de calor es ...
Access restricted. Please log in or start a trial to view this content.
Discusión
El proceso de la generación de hielo usando salmuera como refrigerante secundario consiste en la combinación de calor y transferencia de masa. Si la transferencia de calor es mayor, entonces se forma el hielo antes de que el agua tiene la oportunidad de mezclarse con el líquido a granel. Se observó que cuando hay un movimiento relativo entre el agua introducida y la salmuera mayor de reposo (es decir, la inyección de agua dentro de la salmuera), el flujo de ayuda a la transferencia de calor y alienta hielo...
Access restricted. Please log in or start a trial to view this content.
Divulgaciones
Los autores no tienen nada que revelar.
Agradecimientos
Los autores no tienen reconocimientos.
Access restricted. Please log in or start a trial to view this content.
Materiales
| Name | Company | Catalog Number | Comments |
| DMA 4500 M | Anton Paar | 81546022 | Density Metre |
| GELATO Chef 2200 | magimix | 0036500504R13 | Ice Cream Maker |
| 280D | FREEZE MASTER | 241-1441 | Pipe Freezer |
| M17.5X2 | BLUE ICE MACHINES | GK924 | Slushy Puppy Machine |
| HH68K | OMEGA | 140045 | Thermometer |
| OHAUS | TS4KW | 1324 | Scale |
| ZFC321WA/BNI225 | ZANUSSI | 920672574-00 | Freezer |
| EIS Heater Matrix | Vauxhall | 214720041 | Heat Exchanger |
| 2500LPH | JBA | AP-2500 | Pump |
| Glass syringe | FORTUNA Optima | 100 mL | |
| OAT concentrated coolant | wilko | P30409014 | Ethylene Glycol |
| pure dried vacuum salt | INEOS Enterprise | 1433324 | NaCl Salt |
| Methylated Spirits | Barrettine | 1170 | Methanol |
Referencias
- Cleaning and separation in conduits. UK patent. , GB2358229, WO0151224 (2001).
- Quarini, J. Ice-pigging to reduce and remove fouling and to achieve clean-in-place. Appl. Therm. Eng. 22, 747-753 (2002).
- Evans, T. S., Quarini, G. L., Shire, G. S. F. Investigation into the transportation and melting of thick ice slurries in pipes. Int. J. Refrig. 31, 145-151 (2008).
- Shire, G. S. F., Quarini, G. L., Rhys, T. D. L., Evans, T. S. The anomalous pressure drop behaviour of ice slurries flowing through constrictions. Int. J. Multiph. Flow. 34, 510-515 (2008).
- Shire, G. S. F., Quarini, G. L., Evans, T. S. Pressure drop of flowing ice slurries in industrial heat exchangers. Appl. Therm. Eng. 29, 1500-1506 (2009).
- Evans, T. S. Technical Aspects of Pipeline Pigging with Flowing Ice Slurries [dissertation]. , Department of Mechanical Engineering, University of Bristol. (2007).
- Shire, G. S. F. The behaviour of ice pigging slurries [dissertation]. , Department of Mechanical Engineering, University of Bristol. (2006).
- Hales, A., et al. Ice fraction measurement of ice slurries through electromagnetic attenuation. Int. J. Refrig. 47, 98-104 (2014).
- Hales, A., et al. The effect of salinity and temperature on electromagnetic wave attenuation in brine. Int. J. Refrig. 51, 161-168 (2015).
- Hales, A. Ice slurry diagnostics through electromagnetic wave attenuation and other techniques [dissertation]. , Department of Mechanical Engineering, University of Bristol. (2015).
- Lucas, E. J. K., Hales, A., McBryde, D., Yun, X., Quarini, G. L. Noninvasive Ultrasonic Monitoring of Ice Pigging in Pipes Containing Liquid Food Materials. J. Food Process. Eng. 40, e12306(2015).
- Carrasco, J., Hodgson, A., Michaelides, A. A molecular perspective of water at metal interfaces. Nat. Mater. 11, 667-674 (2012).
- Hu, X. L., Michaelides, A. Ice formation on kaolinite: Lattice match or amphoterism? Surf. Sci. 601, 5378-5381 (2007).
- Hu, X. L., Michaelides, A. The kaolinite (0 0 1) polar basal plane. Surf. Sci. 604, 111-117 (2010).
- Leiper, A. N., Ash, D. G., McBryde, D. J., Quarini, G. L. Improving the thermal efficiency of ice slurry production through comminution. Int. J. Refrig. 35, 1931-1939 (2012).
- Leiper, A. Carnot cycle optimisation of ice slurry production through comminution of bulk ice [dissertation]. , Department of Mechanical Engineering, University of Bristol. (2012).
- Leiper, A. N., Hammond, E. C., Ash, D. G., McBryde, D. J., Quarini, G. L. Energy conservation in ice slurry applications. Appl. Therm. Eng. 51, 1255-1262 (2013).
- Bédécarrats, J. -P., David, T., Castaing-Lasvignottes, J. Ice slurry production using supercooling phenomenon. Int. J. Refrig. 33, 196-204 (2010).
- Wijeysundera, N. E., Hawlader, M. N. A., Andy, C. W. B., Hossain, M. K. Ice-slurry production using direct contact heat transfer. Int. J. Refrig. 27, 511-519 (2004).
- Reynolds, O. On the extent and action of the heating surface of steam boilers. Proc. Lit. Philos. Soc. Manch. 14, 7-12 (1874).
- Reynolds, O. Papers on mechanical and physical subjects: reprinted from various transactions and journals. , Cambridge University Press. Vol. I, 1869-1882, Ch. 14. On the extent and action of the heating surface of steam boilers 81-85 (1900).
- Reynolds, O. Papers on mechanical and physical subjects. Int. J. Heat Mass Transfer. 12, 129-136 (1969).
- Prandtl, L. Eine Beziehung zwischen Wärmeaustausch und Strömungswiderstand der Flüssigkeiten (On the relation between heat exchange and stream resistance of fluid flow). Physik. Z. 11, 1072-1078 (1910).
- Prandtl, L. Bemerkung über den Wärmeübergang im Rohr (Note on heat transmission in pipes). Physik. Z. 29, 487-489 (1928).
- Taylor, G. I. Conditions at the surface of a hot body exposed to the wind. Rep. Memo. ACA. 272, (1916).
- Taylor, G. I. The Application of Osborne Reynolds' Theory of Heat Transfer to Flow through a Pipe. Proc. R. Soc. A. 129, 25-30 (1930).
- Kármán, T. v Proceedings of the Fourth International Congress for Applied Mechanics. , Cambridge, UK. 54-91 (1934).
- Kármán, T. v The analogy between fluid friction and heat transfer. Trans. Am. Soc. Mech. Eng. 61, 705-710 (1939).
- Martinelli, R. C. Heat transfer to molten metals. Trans. Am. Soc. Mech. Eng. 69, 947-959 (1947).
- Colburn, A. P. A method of correlating forced convection heat-transfer data and a comparison with fluid friction. Trans. Am. Inst. Chem. Eng. 29, 174-210 (1933).
- Colburn, A. P. A method of correlating forced convection heat-transfer data and a comparison with fluid friction. Int. J. Heat Mass Transfer. 7, 1359-1384 (1964).
- Chilton, T. H., Colburn, A. P. Mass Transfer (Absorption) Coefficients Prediction from Data on Heat Transfer and Fluid Friction. Ind. Eng. Chem. 26, 1183-1187 (1934).
- Friend, W. L., Metzner, A. B. Turbulent heat transfer inside tubes and the analogy among heat, mass, and momentum transfer. AIChE J. 4, 393-402 (1958).
- Bejan, A. Constructal-theory network of conducting paths for cooling a heat generating volume. Int. J. Heat Mass Transfer. 40, 799-816 (1997).
- Bejan, A., Lorente, S. Constructal theory of generation of configuration in nature and engineering. J. Appl. Phys. 100, 041301(2006).
- Bejan, A., Lorente, S., Yilbas, B. S., Sahin, A. Z. Why solidification has an S-shaped history. Sci. Rep. 3, 1711(2013).
- Lake, R. A., Lewis, E. L. Salt rejection by sea ice during growth. J. Geophys. Res. 75, 583-597 (1970).
- Wettlaufer, J. S., Worster, M. G., Huppert, H. E. Natural convection during solidification of an alloy from above with application to the evolution of sea ice. J. Fluid Mech. 344, 291-316 (1997).
- Paige, R. A. Stalactite Growth beneath Sea Ice. Science. 167, 171-172 (1970).
- Dayton, P. K., Martin, S. Observations of ice stalactites in McMurdo Sound, Antarctica. J. Geophys. Res. 76, 1595-1599 (1971).
- Eide, L. I., Martin, S. The formation of brine drainage features in young sea ice. J. Glaciol. 14, 137-154 (1975).
- Martin, S. Ice stalactites: comparison of a laminar flow theory with experiment. J. Fluid Mech. 63, 51-79 (1974).
- Jeffs, K., Attenborough, D. Frozen Planet: Episode 5 'Winter'. , BBC. (2011).
- Fothergill, A., Berlowitz, V., Attenborough, D. Ch. Winter: Life closes down. in Frozen Planet: A World Beyond Imagination. , BBC books. (2011).
- Yun, X., et al. Ice formation in the subcooled brine environment. Int. J. Heat Mass Transfer. 95, 198-205 (2016).
- Weast, R. C. CRC Handbook of Chemistry and Physics. 64, 64 edn, CRC Press. 257-258 (1983).
- Bejan, A., Lage, J. L. The Prandtl Number Effect on the Transition in Natural Convection Along a Vertical Surface. J. Heat Transfer. 112, 787-790 (1990).
Access restricted. Please log in or start a trial to view this content.
Reimpresiones y Permisos
Solicitar permiso para reutilizar el texto o las figuras de este JoVE artículos
Solicitar permisoThis article has been published
Video Coming Soon
ACERCA DE JoVE
Copyright © 2025 MyJoVE Corporation. Todos los derechos reservados