A subscription to JoVE is required to view this content. Sign in or start your free trial.
Method Article
דור קרח ואת מעבר החום ומסת התופעות של מי היכרות על אמבט קר של בריין
In This Article
Summary
כאן, אנו מציגים פרוטוקול כדי להדגים את הדור של קרח, כאשר מתערבים מים באמבט צונן של מי מלח, כמו קירור משני, בטווח של בטמפרטורות מתחת לנקודת הקיפאון של מים. זה יכול לשמש כדרך חלופית לייצר קרח לתעשייה.
Abstract
אנו להדגים שיטה לחקר העברת חום ומסה ושל התופעות הקפאת בסביבה מלח subcooled. הניסוי שלנו הראה כי, תחת התנאים המתאימים, קרח יכול להיות מיוצר כאשר מים הוא הציג באמבט של מלח קר. כדי להפוך טופס קרח, בנוסף בעל תמהיל מלח ומים, על קצב העברת החום חייב לעקוף את זה של העברת מסה. כאשר המים הציגו בצורה של טיפות זעירות על פני שטח המלח, במצב של חום ומסה הוא על ידי דיפוזיה. הציפה מפסיקה מים מן הערבוב עם המלח מתחת, אבל כמו הקרח מתעבה, זה מאט את קצב העברת חום, מה שהופך קרח קשה יותר לצמוח כתוצאה מכך. כאשר המים הוא הציג בתוך מלח בצורת זרימה, מספר גורמים נמצאים להשפיע כמה קרח יכול להיווצר. טמפרטורה וריכוז בריין, אשר הם הכוחות המניעים של חום ומסה, בהתאמה, יכולים להשפיע על רטי המרת מים אל הקרחo; טמפרטורות אמבטיה נמוכות וריכוזי התמלחות לעודד עוד קרח להיוצר. Rheology הזרימה, אשר יכול להשפיע באופן ישיר גם מן החום וגם מקדמי העברה המוניים, הוא גם גורם מפתח. בנוסף, rheology הזרימה משנה את שטח המגע של הזרימה עם הנוזל בכמות הגדול.
Introduction
Slurries הקרח נמצא בשימוש נרחב בתעשייה, ואת יישום אחד מוצלח במיוחד הוא הטכנולוגיה pigging קרח 1, 2. בהשוואת הקצף הקונבנציונלי החזיר מוצק, חזיר הקרח יכול לנסוע דרך טופולוגיות מורכבות לאורך מרחק גדול בגלל השפעת השימון של השלב הנוזלי ואת הגובה של נקודת הקיפאון שלה כמו חלק מקרח גבישים להמס 3, 4, 5 . גם אם החזיר נתקע, אפשר פשוט לחכות slurries הקרח כדי להמיס ולחדש את תהליך ניקוי מאוחר יותר. שיטה זו של ניקוי צינור היא זולה וקלה לשימוש.
שבר הקרח ממלא תפקיד מרכזי בביצוע של חזיר הקרח. כדי למדוד את השבר קרח, אפשר להשתמש CAFETIERE (בעיתונות הצרפתית) כדי לקבוע אם slurry קרח עבה מספיק 6,"> 7. שבריר קרח גבוהה CAFETIERE, בדרך כלל 80%, נדרש בעת ביצוע הצנרת נקראת קרח. מחקרים אחרונים על גילוי חלק קרח באינטרנט הראו כי הן גלים אלקטרומגנטיים ואולטרא סאונד מתאימים לתפקיד 8, 9, 10, 11.
חזיר קרח בדרך כלל נעשה על ידי יצרנית קרח מגורד-משטח מפתרון NaCl 5% WT (מלח). זוהי גם הדרך העיקרית של ביצוע slurries קרח בתעשייה. סוג זה של יצרנית קרח קופא מים או מלח על משטח מתכתי קר, בדרך כלל משטח 316 פלדה חלקה ולאחר מכן מחזור מזמרת חלקיקי הקרח off. ממשקי נוזלי אל מתכת הם מאוד מורכבים ומושפעים מגוון רחב של גורמים חיוניים קרח עושה 12. הממשק בין הלא-מתכת ומים יכול להיות שונה מאוד, ואחד במיוחד דוגמה מעניינת היא קאוליניט. Kaolממשק inite-מים הוא מיוחד כי אין מבנה קרח נוח סומך לפני השטח של מוצק, אלא שכבה של נוזל מצע amphoteric המעודדת אשכול מלוכדות המימן-הקרח כמו להיוצר על גבי זה 13, 14. דרך נוספת לייצר חזיר הקרח דורשת ריסוק אבני קרח premade בעוד מלח גבוה ריכוז מתווסף זמנית. בשיטה זו, מערכת הקירור יכולה לרוץ בטמפרטורה מתאדה הרבה יותר גבוהה כי אף דיכאון נקודת קיפאון (FPD) מתווסף לפני ההיווצרות של קרח; ולכן זה נחשב יעיל יותר בשל יחס דחיסת וריד וכוח פחתה עבור חובת קירור נתונה 15, 16, 17.
קיימות שתי שיטות ייצור קרח אחרות: ייצור קרח ממים בקירור לשים קירור ומים בקשר ישיר 18, 19. השיטה קירור-יתר כרוך בהפרות מים בקירור metastable ליצור נוקלאציה קרח וצמיחה. הבעיה הגדולה ביותר עבור שיטה זו היא היווצרות הקרח לא הרצויה שיכול לחסום את המערכת. שיטת הקשר הישירה נחשבת לא מתאימה צנרת נקרא קרח כי לא קירור ולא שמן סיכה הם רצו במוצר הקרח האחרון.
היווצרות קרח דורש חום ומסה עקב החום הכמוס של היתוך שנוצר בתהליך. זה התגלה לראשונה על ידי אוסבורן ריינולדס בשנת 1874 כי הובלת חום ומסה בגזים הם מצמידים חזק יכול לבוא לידי ביטוי נוסחאות מתמטיות דומה 20. עבודה זו יצרה את הנייר חלוצית בנושא מומנטום, חום, ומסה בנוזל ראתה אור מחדש מספר פעמים 21, 22. נושא זה ולאחר מכן נחקר על ידימספר היתר, שתי הגישות אנליטיים ואמפיריים, גזים, נוזלים, ואת מתכת מותכת 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33. מלבד העברת חום ומסה, הנוזל צריך אתרי התגרענות שצמיחת קרח הדנדריטים יכול לפתח. תובנה מודרנית לתוך הצמיחה של גבישי קרח משתמשת חוק Constructal, שפותח על ידי אדריאן Bejan, כדי להסביר מדוע קרח גדל בדרך זו 34, 35, 36.
היווצרות הקרח במי מלח שונה מאוד מזו מים טהורים בשל קיומו של מלח. ראשית כל, מלח משנה את התרמודינמיקה של נוזל ומדכא נקודת הקיפאון שלה. שנית, מלח אינו יכול להתמוסס המטריצה קרח (למעט hydrohalite, אשר יכול להיווצר רק כאשר הטמפרטורה מגיעה לנקודה eutectic), והוא דחה את נוזל בכמות גדולה כאשר הקרח מתחיל לצמוח. דחיית המלח התגלתה בשני קרח מים וקרח למד במעבדה 37, 38. מאז המלח גבוה ריכוז דחה הוא בטמפרטורה הרבה מתחת לנקודת הקיפאון של מי ים, ככל שיורד, קרח גדל על הממשק בין המלח זורם הנוזל בתפזורת השקט. נטיפי קרח אלה, גם בשם brinicles, התגלו לראשונה ב מקמורדו סאונד, אנטרקטיקה נחקרו 39 באופן ניסיוני, 40, 41, 42. בשנת 2011, ה- BBC צלמה את היווצרות brinicles בסדרת Planet הקפוא שלה"Xref"> 43, 44.
במעבדה שלנו, התגלה כי על ידי היפוך הנוזלים זורמים שקטים כאשר מים הוא הציג באמבט של מלח קר, המים עלולים להפוך קרח בתנאים הנכונים 45. נמצא כי המיקום שבו המים הוא הציג, לזרום rheology, וטמפרטורת מלח וריכוז הם כל הגורמים המרכזיים המשפיעים כיצד קרח הרבה יכול להיות מיוצר. המטרה הכללית של מחקר זה היא לחקור אם יצרנית קרח ניתן לפתח באמצעות מנגנון זה כדי ליצור slurries קרח, בהתחשב כי הטמפרטורה המאיידת הגבוהה והשיעור הגבוה של נוזל אל נוזל העברת חום יכולים לשפר את היעילות של שימוש באנרגיה. מניות מאמר זה היבטים מרכזיים של הניסוי.
Access restricted. Please log in or start a trial to view this content.
Protocol
זהירות: ישנם שני כימיקלים רעילים, מתנול אתילן גליקול, השתמשו בניסויים אלה. מתנול יכול להיות מפורק בגוף האדם כדי ליצור פורמלדהיד ולאחר מכן לחומצה פורמית או מלח formate. חומרים אלו רעילים למערכת העצבים המרכזית ואף עלול לגרום למוות. אתילן גליקול ניתן מתחמצן ל חומצה גליקולית, אז מה שיכול להפוך חומצה אוקסלית. זה יכול לגרום לכשל כליות ומוות. אל תשתו הכימיקלים האלה. להתייעץ עם רופא באופן מיידי אם מתרחשת תאונה.
1. מערכת הקירור
הערה: זה מאוד קשה לשמור על המלח ב -18 ° C או משהו כזה כאשר טמפרטורת הסביבה היא בערך בטמפרטורת חדר. חשוב כי טנקי אחסון אתילן גליקול ותמלחות הם מבודדים היטב ושל בגודל סביר, כדי למנוע צריכת חשמל עודפת ולהבטיח ביצועי מערכת מיטביים. מומלץ כי גודל המכל אינו עולה על 30 L.
- מכינים את נוזל הקירור משנית
- יוצקים 1 ליטר של אתילן גליקול לתוך הטנק קירור משני, טנק A (הבסיס: 400 מ"מ × 200 מ"מ, גובה: 350 מ"מ). להוסיף בערך 0.6-0.65 L (600-650 גרם) של מים כדי טנק א
- 1.1.1 חזור על שלב מספר פעמים עד שיש מספיק נוזלים טנק A (25 ליטר).
- מערבבים את הנוזלים כך הנוזל הוא הומוגני.
- הפעל שני משאבות טנק להגדרה מלאת הקיבולת (2,500 ליטר / שעה). ודא כי כל הבועות לכודות בתוך מחליפי חום צינורות משתחררים.
- כבה את המשאבה להתבונן אם כל הבועות משתחררות. אם לא, חזור על שלב 1.1.4.
- הכנת מי מלח
הערה: בדוגמא זו, 22% WT תמיסות מוכנות. אם ריכוזים אחרים נדרשים, המסה של תוספת מלח צריכה גם להיות שונה בהתאם. התמלחת התייחסות ערכי ריכוז וצפיפות ניתן למצוא באתר דף D-257 של מהדורת 64 th (1983) של הHandbook דואר CRC של כימיה ופיזיקה 46.- הוסף 4 ק"ג של מים לתוך כוס פלסטיק 5-L.
- מדוד 1 קילו של מלח NaCl בקנה מידה אלקטרוני לזרות מלח זה לתוך הכוס עם המים.
- מערבב את התערובת עד הפתרון הוא ברור (כלומר, אין חלקיקי מלח או בועות מים גלויות הפתרון).
- קחו לדוגמה, ~ 10 מ"ל, של הפתרון באמצעות מזרק 10 מ"ל.
- להזריק את הנוזל לתוך מטר צפיפות U-tube.
- בדקו אם בועות אוויר בצינור. אם יש כאלה, להזריק יותר נוזל כדי לדחוף אותם החוצה.
- לחץ "הגדרות מהירות" ובחר "טמפרטורה וצפיפות." הקלד 20 ° C ולחץ על "אישור". מד צפיפות חברה ימדוד את צפיפות הנוזל בטמפרטורה זו.
- לחץ להתחיל לחכות לתוצאות.
- השווה את הקריאה צפיפות עם 1164.00 ק"ג / מ '3.
- מוסיפים מלח יותר אם הקריאה היא מתחת comparisoצפיפות n. מוסיפים מים אם אחרת.
- חזור על שלבים 1.2.3-1.2.10 עד צפיפות הנוזל נכונה (1164.00 ק"ג / מ '3).
- יוצקים את הפתרון הזה לתוך מיכל גדול, מיכל א
- השתמש בשלבי 1.2.1-1.2.12 לעשות 35-40 ליטר של מלח ולשים מכולה לתוך מקפיא חזה ב -40 ° C. שמור התמלחת שם במשך 48-72 שעות, עד לטמפרטורה מגיעה -19.18 ° C (הקפאת נקודת 22 זה מלח wt%).
2. הכנת הקרח עבור ההזרקה ומי כביסה
- כן קרח המים הזרקה
- יוצקים 1 ליטר של מים לתוך מיכל קטן (200 × 200 × 50 מ"מ).
- חזור על שלב 2.1.1 עם מיכל אחר ומקום שני מיכלי במקפיא החזה ב -40 ° C.
- שמור אותם במקפיא למשך 10 שעות או יותר על מנת להבטיח כי כל המים הוא קפוא.
- מכין את מעטפת הקרח של שטיפת המים
- ממלאים כוס 5-L עם 5 ליטר מים.
- ממלאים כוס 2-L עם 2 ליטר מים.
- מניחים שתי כוסות למקפיא החזה ב -40 ° C במשך 8-10 שעות, כך שיש מעטפת דקה של גלישת קרח סביב מים מהקפאה.
- השתמש סילון מים במהירות גבוהה במהירות של 3-5 מ '/ s מהברז להיפתח חור בקוטר 3 סנטימטר בחלק העליון של קליפת הקרח.
- מסנן את המים בתוך קליפת הקרח.
- שים שתי כוסות להחזיר להקפאה.
- אם המסה של קליפת הקרח אינה מגיעה 3 קילו ו 1 קילו עבור שתי כוסות, בהתאמה, חזור על שלבי 2.2.1-2.2.5, אבל לשמור על הכוסות במקפיא כבר בשלב 2.2.3. שתי הכוסות אמורות להיות מסוגלים להכיל L 2 ו 1 ליטר של מים, בהתאמה.
3. תפקיד מבוא מים ואת ניסוי בקרת Rheology
- הצג מים על פני שטח המלח
- למזוג 2 ליטר של 22% WT מלח קר ממיכל לתוךדלי אלומיניום של מכונת גלידה ו לעבור על יחידת הקירור.
- מדדו את הטמפרטורה של מי מלח עם מדחום / תרמי (או-Type K או T-סוג מתאימים). להמשיך את הניסוי אם התמיסות -15 ° C או נמוך יותר.
- מלאו את המזרק זכוכית 100 מ"ל עם מי ברז בטמפרטורת החדר. צרף בקוטר פנימי 2 מ"מ, 1 מ"מ עבה, שפופרת סיליקון רב 1-מ 'קצה המזרק.
- יש להכניס את המזרק במיקום ספציפי כזה שיש ראש בין המים בתוך המזרק ואת היציאה של צינור סיליקון. הלחץ ההידרוסטטי יהיה לסחוט את המים מתוך הצינור.
- לצלול באורך מסוים של צינור סיליקון, בדרך כלל 70 ס"מ, לתוך מי המלח.
- התאם את המיקום היחסי בין מזרק יציאת הצינורית כך לחץ ההידרוסטטי הוא גדול מספיק כדי לאפשר למים לצאת המזרק. אם הצינור נחסם, להגדיל ראש על ידי הרמת את המזרק במצב אנכי גבוה, unt il הלחץ ההידרוסטטי יכול להתגבר על הלחץ גזירה בתוך הצינור.
- שמור את יציאת צינור בערך 1 סנטימטר או פחות מעל פני המלח.
- התאם את האורך של צינור שקוע וגובה המזרק לשלוט המשקע של המים ולתת טמפרטורה וספיקה כדי לקבוע כמה קרח יכול להתבצע או כמה ערבוב מתרחש על פני שטח המלח. תופעת ההקפאה יש לשים לב עכשיו על פני שטח המלח. ראה 45 הפניה להכוונה נוספת.
- הצג מים דרך המלח
- חזור על שלבים 3.1.1-3.1.6.
- שמור את יציאת הצינור בתוך המלח, רצויה בתחתית המכל.
- התאם את האורך של הצינור השקוע וגובה המזרק.
- התאם את הזווית של יציאת הצינור לשלוט rheology של הזרם.
- חזור על שלבי 3.2.3-3.2.4 כדי למצוא את rheology זרימת המצמידים הטובים וספיקה שיכול לייצר את הקרח ביותר.
התחת = "jove_title"> 4. ייצור קרח, אוסף, ומדידה
- הפוך קרח
- אם יש בועות בצינורות, לעבור על שתי המשאבות בתוך טנק לשחרר בועות מחוץ למערכת זרימת גליקול, ולאחר מכן לכבות את המשאבות.
- הפעל שלוש יחידות הקירור ולתת להם לרוץ 10-16 שעות להתקרר פתרונות אתילן גליקול.
- מדוד את פתרון אתילן גליקול עם מדחום / תרמי. טמפרטורת גליקול צריכה להיות בסביבות -25 ° C.
- מדדו את הטמפרטורה של מי מלח ב מכולה כדי לוודא שהוא נמצא -19 ° C לפני שתמשיך לשלב 4.1.5.
- מלאו את מיכל מלח, טנק B, עם בערך 30 ליטר של מלח ממכל A ו- מתג על שתי משאבות טנק א
- מדדו את הטמפרטורה של גליקול ב א טנק אם זה C קר יותר -19 °, לכבות יחידות קירור אחד או יותר כדי למנוע משקעים של חלקיקי קרח מחוץ מחליפי חום in הטנק B. אם הטמפרטורה הוא חם יותר מטמפרטורת המלח הצפוי, להפעיל את כל שלוש יחידות הקירור. לבצע את הניסוי ב- C -17 ° C עד -19 °.
- מניחים את שני רחובות התערובת של העוגיות של קרח משלב 2.1 לתוך כוס 5-L מבודדים, מיכל B, ויוצקים בערך 3 ליטר מים לתוך כוס.
- מדוד את טמפרטורת המים ולשמור על 2 מעלות צלזיוס על ידי ערבוב את התערובת בין ניסויים אם הטמפרטורה עולה.
- מלאו את המזרק זכוכית עם 100 מ"ל של מים C 2 °.
- החל 5-10 מ"ל של מתנול אל חלון הזכוכית של טנק B להפסיק עיבוי ואת היווצרות קרח.
- להזריק את המים לתוך המלח באמצעות התאמת המיקום היחסי בין המזרק ואת של יציאת הצינורית כך קיים לחץ הידרוסטטי קבוע ובכך בקצב זרימה מתמיד. כ -70 סנטימטרים של צינור סיליקון צריכים להיות שקועים התמלחות. התאם את הזווית של הזרקת 0 ° כך מהירויות מים הראשוניות כלפי מעלה נואשction הוא 0 m / s.
הערה: המזרק יכול להיות כף יד או הדק עמדה. ידניים מתאימים יותר כאשר טמפרטורת המלח היא קרה, כי זה לוקח יותר זמן להסתגל עמדה, וקרח עלול לחסום את הצינור. שמור על rheology הזרימה עקבי לאורך הניסוי על ידי הבטחת זווית שיעור הזרקת זרם בלתי פוסקת (0 °) ועל ידי שמירת הגבול הקפאה בערך 3 סנטימטרים מעל יציאת הצינור. אל תתנו את הזרימה להיכנס לאזור שבו הוא מתחיל להפוך סוער 47. ראה 45 הפניה להכוונה נוספת. - אסוף את הקרח כמתואר בשלבים 4.2 ו -4.3. חזור על שלבי 4.1.8 - 4.1.11 בטמפרטורות מלח שונות.
- אסוף את הקרח הפיק להעריך כמה קרח מופק (אוסף יבש)
- שים במיכל (200 × 200 × מ"מ 50) על המאזניים לאפס את הקריאה על ידי לחיצה על "הפעל" כפתור.
- השתמש מסננת כדי לגרוף את הקרח להתנערהתמלחות.
- שים קרח זה בתוך המיכל. למדוד את המסה של הקרח באמצעות סולם.
- אחרי שהקרח נמס, להשתמש במזרק 10 מ"ל לקחת דגימה. להזריק מדגם זה של נוזל לתוך מטר הצפיפות.
- בצע שלבים 1.2.6-1.2.9.
- רשום את קריאת הצפיפות.
- חשב את מסת המים נטו צפיפות שלה (כלומר, את המסה של מים שהוסב קרח) באמצעות הנוסחה הבאה:
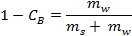
איפה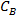 הוא ריכוז המלח באמצעות% WT ו
הוא ריכוז המלח באמצעות% WT ו 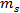 ו
ו 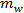 הם ההמונים של מלח ומים, בהתאמה.
הם ההמונים של מלח ומים, בהתאמה.
- אסוף את הקרח הפיק להעריך כמה קרח מופק (אוסף רטוב)
- מלאו את כוס 5-L עם פגז קרח (שלב 2.2) ו-בטמפרטורת החדר מי ברז. שים אותו בחזרה למקפיא ב -40 ° C.
- למזוג את המים עם קליפת הקרח מן הקנקן 5-L לתוך מבחנת 2-L כאשר הטמפרטורה שלו היא ב 0 מעלות צלזיוס. מלאו את כוס 5-L. יש להחזיק את הכוסות במקפיא.
- סקופ את הקרח המיוצר 4.1.8 צעדים 4.1.9 ויוצקים 200-500 מ"ל מים מקנקן 2-L אל הקרח כדי לשטוף אותו. אין לטלטל את המסננת לפני מריחת המים C ° 0.
- להתנער הנוזל במסננת.
- חזור על שלבים 4.2.2-4.2.7.
Access restricted. Please log in or start a trial to view this content.
תוצאות
איור 1 משווה את ההשפעות של מים הציגו בפני שטח המלח למים המוזרק דרך המלח. בתרחיש "קרח-קאפ", הקרח התגבש הוא מוצק כי המים לא לערבב הרבה עם נוזל בכמות גדולה. הבדל הטמפרטורה וצפיפות בין שני הנוזלים מייצר כוח ציפה על פני המים ומונע מהם הערבוב. נ...
Access restricted. Please log in or start a trial to view this content.
Discussion
התהליך של יצירת קרח באמצעות מלח כמו קירור משני כרוך בשילוב של חום ומסה. אם העברת חום גבוה, אז צורות קרח לפני המים יש את הסיכוי לערבב עם נוזל בכמות גדולה. היה נראה כי כאשר קיימת תנועה יחסית בין המים הציגו ואת המלח בתפזורת השקט (כלומר, הזרקת מים בתוך מי המלח), זרימת עו?...
Access restricted. Please log in or start a trial to view this content.
Disclosures
החוקרים אין לי מה לחשוף.
Acknowledgements
יש המחברים לא בתודות.
Access restricted. Please log in or start a trial to view this content.
Materials
| Name | Company | Catalog Number | Comments |
| DMA 4500 M | Anton Paar | 81546022 | Density Metre |
| GELATO Chef 2200 | magimix | 0036500504R13 | Ice Cream Maker |
| 280D | FREEZE MASTER | 241-1441 | Pipe Freezer |
| M17.5X2 | BLUE ICE MACHINES | GK924 | Slushy Puppy Machine |
| HH68K | OMEGA | 140045 | Thermometer |
| OHAUS | TS4KW | 1324 | Scale |
| ZFC321WA/BNI225 | ZANUSSI | 920672574-00 | Freezer |
| EIS Heater Matrix | Vauxhall | 214720041 | Heat Exchanger |
| 2500LPH | JBA | AP-2500 | Pump |
| Glass syringe | FORTUNA Optima | 100 mL | |
| OAT concentrated coolant | wilko | P30409014 | Ethylene Glycol |
| pure dried vacuum salt | INEOS Enterprise | 1433324 | NaCl Salt |
| Methylated Spirits | Barrettine | 1170 | Methanol |
References
- Cleaning and separation in conduits. UK patent. , GB2358229, WO0151224 (2001).
- Quarini, J. Ice-pigging to reduce and remove fouling and to achieve clean-in-place. Appl. Therm. Eng. 22, 747-753 (2002).
- Evans, T. S., Quarini, G. L., Shire, G. S. F. Investigation into the transportation and melting of thick ice slurries in pipes. Int. J. Refrig. 31, 145-151 (2008).
- Shire, G. S. F., Quarini, G. L., Rhys, T. D. L., Evans, T. S. The anomalous pressure drop behaviour of ice slurries flowing through constrictions. Int. J. Multiph. Flow. 34, 510-515 (2008).
- Shire, G. S. F., Quarini, G. L., Evans, T. S. Pressure drop of flowing ice slurries in industrial heat exchangers. Appl. Therm. Eng. 29, 1500-1506 (2009).
- Evans, T. S. Technical Aspects of Pipeline Pigging with Flowing Ice Slurries [dissertation]. , Department of Mechanical Engineering, University of Bristol. (2007).
- Shire, G. S. F. The behaviour of ice pigging slurries [dissertation]. , Department of Mechanical Engineering, University of Bristol. (2006).
- Hales, A., et al. Ice fraction measurement of ice slurries through electromagnetic attenuation. Int. J. Refrig. 47, 98-104 (2014).
- Hales, A., et al. The effect of salinity and temperature on electromagnetic wave attenuation in brine. Int. J. Refrig. 51, 161-168 (2015).
- Hales, A. Ice slurry diagnostics through electromagnetic wave attenuation and other techniques [dissertation]. , Department of Mechanical Engineering, University of Bristol. (2015).
- Lucas, E. J. K., Hales, A., McBryde, D., Yun, X., Quarini, G. L. Noninvasive Ultrasonic Monitoring of Ice Pigging in Pipes Containing Liquid Food Materials. J. Food Process. Eng. 40, e12306(2015).
- Carrasco, J., Hodgson, A., Michaelides, A. A molecular perspective of water at metal interfaces. Nat. Mater. 11, 667-674 (2012).
- Hu, X. L., Michaelides, A. Ice formation on kaolinite: Lattice match or amphoterism? Surf. Sci. 601, 5378-5381 (2007).
- Hu, X. L., Michaelides, A. The kaolinite (0 0 1) polar basal plane. Surf. Sci. 604, 111-117 (2010).
- Leiper, A. N., Ash, D. G., McBryde, D. J., Quarini, G. L. Improving the thermal efficiency of ice slurry production through comminution. Int. J. Refrig. 35, 1931-1939 (2012).
- Leiper, A. Carnot cycle optimisation of ice slurry production through comminution of bulk ice [dissertation]. , Department of Mechanical Engineering, University of Bristol. (2012).
- Leiper, A. N., Hammond, E. C., Ash, D. G., McBryde, D. J., Quarini, G. L. Energy conservation in ice slurry applications. Appl. Therm. Eng. 51, 1255-1262 (2013).
- Bédécarrats, J. -P., David, T., Castaing-Lasvignottes, J. Ice slurry production using supercooling phenomenon. Int. J. Refrig. 33, 196-204 (2010).
- Wijeysundera, N. E., Hawlader, M. N. A., Andy, C. W. B., Hossain, M. K. Ice-slurry production using direct contact heat transfer. Int. J. Refrig. 27, 511-519 (2004).
- Reynolds, O. On the extent and action of the heating surface of steam boilers. Proc. Lit. Philos. Soc. Manch. 14, 7-12 (1874).
- Reynolds, O. Papers on mechanical and physical subjects: reprinted from various transactions and journals. , Cambridge University Press. Vol. I, 1869-1882, Ch. 14. On the extent and action of the heating surface of steam boilers 81-85 (1900).
- Reynolds, O. Papers on mechanical and physical subjects. Int. J. Heat Mass Transfer. 12, 129-136 (1969).
- Prandtl, L. Eine Beziehung zwischen Wärmeaustausch und Strömungswiderstand der Flüssigkeiten (On the relation between heat exchange and stream resistance of fluid flow). Physik. Z. 11, 1072-1078 (1910).
- Prandtl, L. Bemerkung über den Wärmeübergang im Rohr (Note on heat transmission in pipes). Physik. Z. 29, 487-489 (1928).
- Taylor, G. I. Conditions at the surface of a hot body exposed to the wind. Rep. Memo. ACA. 272, (1916).
- Taylor, G. I. The Application of Osborne Reynolds' Theory of Heat Transfer to Flow through a Pipe. Proc. R. Soc. A. 129, 25-30 (1930).
- Kármán, T. v Proceedings of the Fourth International Congress for Applied Mechanics. , Cambridge, UK. 54-91 (1934).
- Kármán, T. v The analogy between fluid friction and heat transfer. Trans. Am. Soc. Mech. Eng. 61, 705-710 (1939).
- Martinelli, R. C. Heat transfer to molten metals. Trans. Am. Soc. Mech. Eng. 69, 947-959 (1947).
- Colburn, A. P. A method of correlating forced convection heat-transfer data and a comparison with fluid friction. Trans. Am. Inst. Chem. Eng. 29, 174-210 (1933).
- Colburn, A. P. A method of correlating forced convection heat-transfer data and a comparison with fluid friction. Int. J. Heat Mass Transfer. 7, 1359-1384 (1964).
- Chilton, T. H., Colburn, A. P. Mass Transfer (Absorption) Coefficients Prediction from Data on Heat Transfer and Fluid Friction. Ind. Eng. Chem. 26, 1183-1187 (1934).
- Friend, W. L., Metzner, A. B. Turbulent heat transfer inside tubes and the analogy among heat, mass, and momentum transfer. AIChE J. 4, 393-402 (1958).
- Bejan, A. Constructal-theory network of conducting paths for cooling a heat generating volume. Int. J. Heat Mass Transfer. 40, 799-816 (1997).
- Bejan, A., Lorente, S. Constructal theory of generation of configuration in nature and engineering. J. Appl. Phys. 100, 041301(2006).
- Bejan, A., Lorente, S., Yilbas, B. S., Sahin, A. Z. Why solidification has an S-shaped history. Sci. Rep. 3, 1711(2013).
- Lake, R. A., Lewis, E. L. Salt rejection by sea ice during growth. J. Geophys. Res. 75, 583-597 (1970).
- Wettlaufer, J. S., Worster, M. G., Huppert, H. E. Natural convection during solidification of an alloy from above with application to the evolution of sea ice. J. Fluid Mech. 344, 291-316 (1997).
- Paige, R. A. Stalactite Growth beneath Sea Ice. Science. 167, 171-172 (1970).
- Dayton, P. K., Martin, S. Observations of ice stalactites in McMurdo Sound, Antarctica. J. Geophys. Res. 76, 1595-1599 (1971).
- Eide, L. I., Martin, S. The formation of brine drainage features in young sea ice. J. Glaciol. 14, 137-154 (1975).
- Martin, S. Ice stalactites: comparison of a laminar flow theory with experiment. J. Fluid Mech. 63, 51-79 (1974).
- Jeffs, K., Attenborough, D. Frozen Planet: Episode 5 'Winter'. , BBC. (2011).
- Fothergill, A., Berlowitz, V., Attenborough, D. Ch. Winter: Life closes down. in Frozen Planet: A World Beyond Imagination. , BBC books. (2011).
- Yun, X., et al. Ice formation in the subcooled brine environment. Int. J. Heat Mass Transfer. 95, 198-205 (2016).
- Weast, R. C. CRC Handbook of Chemistry and Physics. 64, 64 edn, CRC Press. 257-258 (1983).
- Bejan, A., Lage, J. L. The Prandtl Number Effect on the Transition in Natural Convection Along a Vertical Surface. J. Heat Transfer. 112, 787-790 (1990).
Access restricted. Please log in or start a trial to view this content.
Reprints and Permissions
Request permission to reuse the text or figures of this JoVE article
Request PermissionThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. All rights reserved