Un abonnement à JoVE est nécessaire pour voir ce contenu. Connectez-vous ou commencez votre essai gratuit.
Method Article
À haut débit la synthèse des glucides et fonctionnalisation de nanoparticules polyanhydride
Dans cet article
Résumé
Dans cet article, une méthode à haut débit est présenté pour la synthèse d'oligosaccharides et de leur attachement à la surface de nanoparticules polyanhydrides pour une utilisation ultérieure dans le ciblage des récepteurs spécifiques sur les cellules présentatrices d'antigènes.
Résumé
Approches transdisciplinaires impliquant des domaines tels que la conception de matériel, les nanotechnologies, la chimie, et de l'immunologie doivent être utilisés pour concevoir rationnellement efficaces transporteurs de vaccins. À base de nanoparticules plates-formes peuvent prolonger la durée de la persistance d'antigènes vaccinaux, ce qui pourrait améliorer l'immunogénicité vaccin 1. Plusieurs polymères biodégradables ont été étudiés en tant que véhicules de livraison des vaccins 1, en particulier, les particules polyanhydride ont démontré la capacité de fournir à libération prolongée d'antigènes protéiques stables et à activer les cellules présentatrices d'antigènes et de moduler les réponses immunitaires 2-12.
La conception moléculaire de ces porte-vaccins se doit d'intégrer la sélection rationnelle des propriétés des polymères, ainsi que l'incorporation de appropriées des agents de ciblage. De fabrication à haut débit automatisé des ligands de ciblage et de particules fonctionnalisées est un outil puissant qui permettra d'améliorer la capacité d'étudier un large rAnge de propriétés et mènera à la conception de dispositifs reproductibles de livraison des vaccins.
L'ajout de ligands de ciblage susceptibles d'être reconnus par des récepteurs spécifiques sur les cellules immunitaires a été démontré pour moduler et adapter les réponses immunitaires 10,11,13 récepteurs lectine de type C (PLC) sont des récepteurs de reconnaissance des formes du porc (SDRP) qui reconnaissent les hydrates de carbone présents sur le surface de pathogènes. La stimulation des cellules immunitaires via PLC permet l'internalisation accrue de l'antigène et la présentation subséquente pour l'activation des lymphocytes T en outre 14,15. Par conséquent, les molécules d'hydrates de carbone jouent un rôle important dans l'étude des réponses immunitaires; cependant, l'utilisation de ces biomolécules souffre souvent du manque de disponibilité de la structure bien définie et des hydrates de carbone purs. Une plate-forme d'automatisation basée sur la solution itérative des réactions en phase peut permettre la synthèse rapide et contrôlée de ces molécules de synthèse difficiles en utilisant b significativement plus faibleonstruire quantités de blocs que les traditionnels en phase solide des méthodes 16,17.
Ici on signaler un protocole pour la solution automatisée en phase de synthèse d'oligosaccharides tels que le mannose à base fluorée avec des ligands de ciblage extraction en phase solide pour la purification intermédiaire. Après développement de procédés automatiques pour faire l'agent à base de carbohydrate ciblage, on décrit les méthodes pour leur fixation sur la surface de nanoparticules polyanhydride employant un ensemble robotique automatisé jusqu'à actionné par LabVIEW comme décrit précédemment 10. Fonctionnalisation de surface avec des hydrates de carbone a montré son efficacité dans le ciblage PLC 10,11 et augmenter le débit du procédé de fabrication pour déterrer les complexités associées à un système multi-paramétrique sera d'une grande valeur (Figure 1a).
Protocole
1. Synthèse des glucides à haut débit
- Avant la synthèse automatisée de dimannoside, un donneur de sucre convenablement protégé, généralement trichloroacétimidate, et l'accepteur, essentiellement d'un alcool fluoré alcényle, sont synthétisés sur le banc-dessus.
- Un programme est écrit pour la synthèse automatisée de dimannoside. Une représentation schématique de la procédure de base automatisé est présenté dans la Figure 2. Dans le programme, il est assuré que, avant l'addition du promoteur, le mélange de donneur et l'accepteur est agité pendant au moins 30 min.
- Solutions du donneur, accepteur synthétique et trimethylsilyltrifluoromethanesulfonate sont faites dans le dichlorométhane. Le toluène et le dichlorométhane sont le plus fréquemment utilisé pour les réactions de glycosylation.
- En outre, préparer des solutions de réactifs pour la déprotection des groupements protecteurs temporaires dans le méthanol et le méthanol de 80% à 100%.
- Avant le début du programme, veiller à ce que le RELAl'humidité ive dans la salle est de 30% ou moins dans la chambre de l'automatisation. Taux d'humidité élevé est préjudiciable pour les réactions de glycosylation.
- Une fois que le programme est lancé, le bras robotisé transfère les solutions de donneur et accepteur dans le flacon de réaction séquentielle. Ensuite, le mélange est agité pendant 30 min.
- Ensuite, le bras robotisé transfère de 0,2 à 0,3 équivalents de trimethylsilyltrifluoromethanesulfonate dans le mélange, généralement à la température ambiante, bien que des températures plus basses, comme -20 ° C peut être atteint. Le mélange réactionnel est agité pendant 30 min.
- Après 30 min, la réaction est arrêtée et une petite partie aliquote retiré de surveiller l'avancement de la réaction. Si ce n'est pas complet, la réaction peut être poursuivi et, finalement, le temps nécessaire peut être modifié.
- Une fois la réaction terminée, le mélange réactionnel est transféré dans les fluorés extraction en phase solide (FSPE) cartouches contenant C 8 F 17-gel de silice modifiée pour la purification.
- Le paniercrêtes sont d'abord lavées avec une participation de 80% mélange méthanol-eau (8 ml) de se débarrasser de la fraction non fluorée.
- Puis les cartouches sont lavées avec du méthanol à 100% pour obtenir le produit désiré fluorée-marqué. Si une purification supplémentaire est souhaitée, la machine peut être arrêtée et le produit de la réaction (s) enlevé pour purification par des moyens supplémentaires.
- Après le cycle de purification, le bras robotisé distribue le méthylate de sodium dans le flacon de réaction. La réaction est agitée pendant 2 heures. Si ce n'est pas complet, la réaction peut être à nouveau poursuivi pour une plus longue période et, finalement, le temps programmé nécessaire peut être modifié.
- Après l'achèvement de la réaction, le produit est purifié par FSPE et ensuite soumis à une dissolution dans du toluène anhydre suivie d'une évaporation pour éliminer l'eau résiduelle.
- Puis le cycle (à partir de l'étape 6 à 13) est répétée jusqu'à ce que la longueur de chaîne désirée est obtenue pour la molécule cible.
- Le produit protégé obtenu à partir de l'automatisation est een outre purifié et entièrement caractérisé par des techniques telles que de résonance nucléaire (RMN) magnétique. Déprotection complète (suppression de tous les groupes protecteurs restants) de la molécule cible finale est ensuite complété en dehors de la plate-forme d'automatisation comme une règle, car elle implique souvent des gaz d'hydrogène explosif et le palladium. L'étape de déprotection finale a été réalisée sur la paillasse en dehors de la plate-forme d'automatisation. La première étape est ozonolyse de la double liaison dans la balise fluorée suivie d'une oxydation de l'aldéhyde produit en un acide carboxylique. Le produit a été purifié par Chromatographie sur colonne. La dernière étape était la déprotection des groupes éther benzylique par hydrogénation catalysée par le palladium. Le produit a été passé sur célite pad pour se débarrasser de palladium pour obtenir pur produit final.
2. À haut débit Fonctionnalisation de surface des nanoparticules
- La synthèse de polymères à haut débit et la fabrication de nanoparticules est réalisée en suivant le même protocole et robotique mis en place décrit par Petersen et al 19. Les systèmes de copolymères utilisés pour la fabrication de particules sont à base d'acide sébacique (SA) et le 1,6-bis (para-carboxyphénoxy) hexane (CPH), et le 1,8-bis ( para-carboxyphénoxy) -3,6-dioxaoctane (CPTEG) et CPH. Une représentation schématique de l'appareil de dépôt robotisé utilisé est présenté dans la figure 1b.
- Après la fabrication des nanoparticules, le titulaire contenant les tubes avec la bibliothèque des nanoparticules est rattachée à l'étape actionneur linéaire.
- Pour la fixation d'hydrates de carbone à la surface des particules polyanhydride, une réaction amine-acide carboxylique couplage consistant en 20 deux réactions consécutives est effectuée.
- Pour la première réaction, la seringue dans la pompe à seringue programmable premier est rempli avec 10 équivalents (éq.) (équivalents de moyenne de concentration d'acide carboxylique molaire sur la surface des particules) de 1-éthyl-3-(3-diméthylaminopropyl)-bischlorhydrate rbodiimide (EDC) et 10 éq. d'éthylènediamine dans une solution aqueuse, lorsque la seringue dans la pompe à seringue programmable seconde est chargé avec 12 éq. de N-hydroxysuccinimide (NHS) en solution aqueuse.
- En utilisant le programme LabVIEW, les suspensions de réactifs sont déposés dans le * bibliothèque des nanoparticules.
- Suivante, chaque échantillon est traité par ultrasons (30 s à 40 Hz) et le tube de support est détaché de la plate-forme robotique.
- Suspensions de nanoparticules sont incubées pendant ** h 9 avec une rotation constante à 4 ° C.
- Après un temps de réaction est terminée, les tubes sont centrifugés (12000 xg pendant 5 min) et a renvoyé à la station de robotique pour effectuer deux étapes de lavage.
- Pour le lavage, une seringue reste vide et chargé dans le pousse-seringue programmable première pendant la seringue dans la deuxième pompe à seringue est remplie d'eau froide. Le surnageant dans chaque tube est retiré dans la seringue vide et les dépôts de pompe deuxièmes eau froide.
- Homogénéisation des nanosuspension de particules est réalisée comme décrit à l'étape 2.6. Les tubes sont ensuite centrifugés (12000 xg pendant 5 min) et une étape second lavage est effectué comme décrit à l'étape 2.9.
- Pour la seconde réaction, deux étapes de dépôt sont utilisés. Dans le première étape de dépôt, 12 éq. des EDC sont chargés avec une pompe et 12 éq. NHS sont chargés avec de la seconde pompe.
- La seconde étape de dépôt comprend 10 éq. d'un saccharide spécifique sur les première et seconde pompes (c.-à-galactose, le lactose ou di-mannose) *** et une troisième pompe à 10 éq. l'acide glycolique de (utilisé comme contrôle ****).
- Suspensions de nanoparticules est homogénéisé comme décrit à l'étape 2.6 et incubés pendant 9 heures avec de rotation constante à 4 ° C.
- Après le temps de réaction est terminée, une étape de lavage est effectué comme décrit dans les étapes 2.8, 2.9 et 2.10.
- La bibliothèque nanoparticule fonctionnalisée est ensuite placé dans une chambre à vide à sécher pendant au moins 2 h.
- Les nanoparticules fonctionnalisées sont alors caractèreIzed par spectroscopie des rayons X des photoélectrons et un criblage à haut débit débit phénol-acide sulfurique afin de déterminer la composition de la surface et la concentration du saccharide respectivement. Microscopie électronique à balayage et de diffusion dynamique de la lumière sont utilisés pour déterminer la taille des particules, distribution en taille, et la charge de surface.
Notes: * Dépôt volumes varient avec la masse de nanoparticules contenues dans chaque tube.
Temps de réaction ** pour les réactions des premier et second peut être changé pour ajuster la concentration finale de saccharide.
Chaque *** saccharide est déposé dans des tubes à essai en fonction du groupe désiré.
**** Pour la réaction spécifique utilisé dans cette étude pour la fixation des hydrates de carbone, l'acide glycolique est utilisé comme un contrôle de liaison depuis saccharides déprotégés déjà cette molécule liée de manière covalente, ce qui permet pour la fixation à la suite de surface des nanoparticules.
3. Les résultats représentatifs
Le utiledimannoside ment protégée montre la figure 2 a été synthétisé en utilisant la plate-forme d'automatisation. Le composé synthétisé a été caractérisé par RMN 1 H dans un spectromètre de 400 MHz VXR utilisant CDCl 3 comme solvant. Le spectre RMN est représenté sur la figure 3.
Utilisant la fabrication de nanoparticules à haut débit et la fonctionnalisation des nanoparticules polyanhydride décrit ci-après, l'attachement de dimannose, lactose et de galactose a été effectué avec succès 10, 11. En utilisant cette configuration, les conditions réactionnelles optimales (c.-à-la température de réaction et le temps) ont été identifiées pour atteindre la fonctionnalisation de nanoparticules et de la morphologie désirée. Lorsque la réaction a été réalisée à 4 ° C au lieu de la température ambiante, une diminution de l'agrégation des nanoparticules a été observée par MEB (données non présentées). Le tableau 1 montre des résultats représentatifs de la caractérisation des CPTEG 50:50 fonctionnalisé: des nanoparticules avec CPH soit di-mannose oule lactose, synthétisé à 4 ° C. Les données indiquent une légère augmentation du diamètre des nanoparticules moyenne en raison de la fonctionnalisation. Tandis que les nanoparticules non fonctionnalisés ont un potentiel zêta négatif d'env. -20 MV, les particules fonctionnalisées a montré une valeur zêta potentiel positif, démontrant la fonctionnalisation de succès de la surface des nanoparticules. Lactose et di-mannose sont à la fois les sucres neutres; cependant, des groupes aminés libres de l'éthylène-diamine-lieur utilisé pour fixer les saccharides peuvent être responsables du potentiel zêta positif.
Le temps de réaction est une autre variable qui pourrait affecter à la fois la morphologie finale des nanoparticules et le degré d'attachement à sucre atteint. En ajustant le temps de réaction, la concentration en sucre final rattaché à la surface des nanoparticules peut être contrôlée comme le montre la figure 4A. Comme prévu, la concentration de dimannose sur la surface de 50:50 CPTEG: CPH nanoparticules augmente avecle temps total de réaction et atteint un maximum après 18 heures. Nanoparticules fonctionnalisées avec le temps total de réaction de 24 heures ont été utilisées pour évaluer leur capacité à cibler PLC sur la souris de la moelle osseuse provenant cellules dendritiques (CD). La cytométrie en flux a été utilisée pour évaluer l'expression de deux récepteurs (c.-à-CL, le CIRE (CD209, DC-SIGN) et le récepteur du mannose (CD206)) après stimulation par la non-fonctionnalisé, et le lactose et le di-mannose nanoparticules fonctionnalisées (figure 4B). Un supérieur expression des deux récepteurs, qui est une indication de ciblage efficace, a été obtenue lorsque les cellules sont stimulées avec la fois du lactose et di-mannose nanoparticules fonctionnalisés. Cependant, di-mannose-fonctionnalisés particules ont un niveau plus élevé d'expression indiquant une spécificité de ce ligand pour les récepteurs qui ont été étudiés.
| Type de nanoparticules | Diamètre de particule moyen (nm) | Aveparticules rage ζ-potentiel (mV) |
| Non-fonctionnalisé | 162 ± 43 | -20 ± 0,6 |
| Lactose | 235 ± 34 | 26 ± 2,4 |
| Di-mannose | 243 ± 32 | 30 ± 4,2 |
Tableau 1. La caractérisation des nanoparticules. Non-fonctionnalisé et fonctionnalisé ont été caractérisées par diffusion de lumière quasi-élastique et mesures du potentiel zêta. Données sur la taille des particules représentent la valeur moyenne ± déviation standard (SD) de données dynamiques de diffusion de lumière collectées dans trois expériences indépendantes. Données Zeta potentiels représentent la valeur moyenne ± écart-type de trois lectures indépendantes. Changement dans le signe du potentiel zêta démontre que le sucre était efficace conjugué à la CPTEG 50:50: surface des nanoparticules CPH.
= "/ Files/ftp_upload/3967/3967fig1.jpg" />
Figure 1. (A) Représentation graphique de l'approche poursuivie avec la fonctionnalisation de nanoparticules glucides polyanhydride et un exemple des bibliothèques de nanoparticules fonctionnalisées qui pourraient être conçus avec le décrit à haut débit approche. (B) la représentation schématique de l'appareil de dépôt automatisé utilisé pour la fonctionnalisation de particules, qui consiste à i) trois pompes NE 1000, (ii) une étape robotique intégré par deux actionneurs (Zaber), un pour le mouvement dans la direction x et l'autre pour un mouvement dans la direction y, (iii) une deuxième étape de robot avec deux crémaillères voisines (correspondant pour tubes et les cuvettes) constitué de trois actionneurs, un pour chaque direction (x, y et z). Les pompes et un total de cinq actionneurs sont connectés en série. Actionneurs et les pompes sont actionnées par un ordinateur utilisant le logiciel LabVIEW. Ce schéma n'est pas à l'échelle.arge.jpg "target =" _blank "> Cliquez ici pour agrandir la figure.
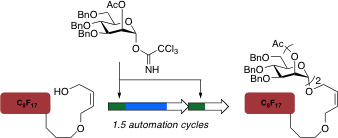
Figure 2. Représentation graphique de la automatisé itérative de synthèse des hydrates de carbone en utilisant le mannose comme un exemple.
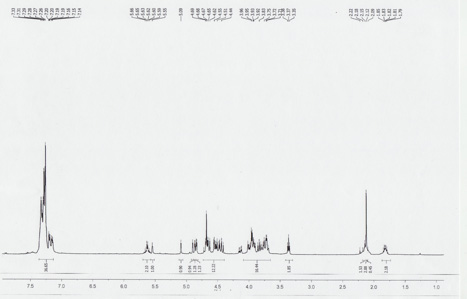
Figure 3. RMN 1 H de la dimannoside protégés.
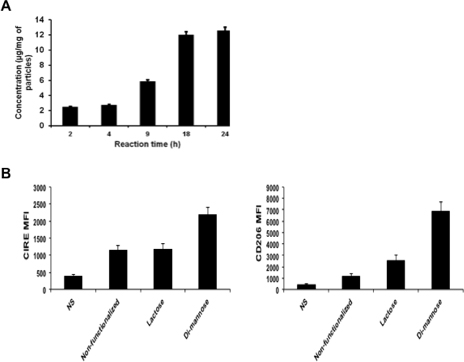
Figure 4. (A) Effet du temps de réaction sur la concentration de surface des nanoparticules de saccharide. Dans les données présentées, 50:50 CPTEG: nanoparticules CPH ont été fonctionnalisés avec dimannose à différents temps de réaction et la réaction a été réalisée à 4 ° C. L'erreur moyenne et le niveau de deux expériences indépendantes de fonctionnalisation est montré. (B) des nanoparticules de lactose et de di-mannose fonctionnalisésrécepteur cible efficacement DC-SIGN (CIRE, CD209) et le mannose (CD206) sur la moelle osseuse des cellules dendritiques dérivées comme l'a démontré par l'expression accrue de ces deux marqueurs après stimulation par CPTEG 50:50 fonctionnalisé: nanoparticules CPH en comparaison avec l'expression obtenue avec des particules non fonctionnalisés.
Discussion
L'efficacité des hydrates de carbone comme agents de ciblage à des interactions nanoparticules directs aux cellules immunitaires a été démontré précédemment 10, 11. Des recherches antérieures dans nos laboratoires ont montré que les sucres spécifiques attachés aux nanoparticules polyanhydrides sont en mesure de cibler PLC différents sur les cellules présentatrices d'antigènes (APC), améliorant ainsi l'activation des cellules immunitaires qui peut être important pour l'activati...
Déclarations de divulgation
NLBP est co-fondateur et titulaire d'équité dans la société glucides LuCella Biosciences, Inc
Remerciements
Les auteurs tiennent à remercier le US Army Medical Research et du matériel de commande (Grant # W81XWH-10-1-0806) et le National Institutes of Health (Grant # U19-01 AI091031 et Grant # 1R01GM090280) pour un soutien financier. BN reconnaît la chaire Balloun en génie chimique et biologique et NLBP reconnaît la chaire de génie Wilkinson interdisciplinaire. Nous remercions Julia Vela pour son aide dans l'exécution des expériences de fonctionnalisation des nanoparticules.
matériels
| Name | Company | Catalog Number | Comments |
| Nom | Entreprise | Le numéro de catalogue | |
| Motorisée XYZ scène: 3x T-LSM050A, 50 mm de débattement par axe | Technologies Zaber | T-XYZ-LSM050A-KT04 | |
| NE-1000 Pompe seringue à usage unique | Nouveaux systèmes de pompage Era | NE-1000 | |
| Pyrex * Vista * Monture réutilisables Tubes de culture en verre | Corning | 07-250-125 | |
| ASW 1000 | Technologies Chemspeed | ||
| LabVIEW | National Instruments | 776671-35 | |
| Seringues SGE étanches aux gaz, de Luer Loc | Sigma-Aldrich | 509507 | |
| XL-2000 Sonicator | Qsonica | Q55 | |
| Mini-tube à rotateurs | Fisher Scientific | 05-450-127 |
Références
- Zepp, F. Principles of vacine design-lessons from nature. Vaccine. 28, C14-C24 (2010).
- Ulery, B. D., Phanse, Y., Sinha, A., Wannemuehler, M. J., Narasimhan, B., Bellaire, B. H. Polymer chemistry influences monocytic uptake of polyanhydride nanospheres. Pharm. Res. 26, 683-690 (2009).
- Torres, M. P., Wilson-Welder, J. H., Lopac, S. K., Phanse, Y., Carrillo-Conde, B., Ramer-Tait, A. E. Polyanhydride microparticles enhance dendritic cell antigen presentation and activation. Acta Biomater. 7, 2857-2864 (2011).
- Torres, M. P., Determan, A. S., Anderson, G. L., Mallapragada, S. K., Narasimhan, B. Amphiphilic polyanhydrides for protein stabilization and release. Biomaterials. 28, 108-116 (2007).
- Petersen, L. K., Ramer-Tait, A. E., Broderick, S. R., Kong, C. S., Ulery, B. D., Rajan, K. Activation of innate immune responses in a pathogen-mimicking manner by amphiphilic polyanhydride nanoparticle adjuvants. Biomaterials. 32, 6815-6822 (2011).
- Petersen, L. K., Xue, L., Wannemuehler, M. J., Rajan, K., Narasimhan, B. The simultaneous effect of polymer chemistry and device geometry on the in vitro activation of murine dendritic cells. Biomaterials. 30, 5131-5142 (2009).
- Lopac, S. K., Torres, M. P., Wilson-Welder, J. H., Wannemuehler, M. J., Narasimhan, B. Effect of polymer chemistry and fabrication method on protein release and stability from polyanhydride microspheres. J. Biomed. Mater. Res. B. 91, 938-947 (2009).
- Determan, A. S., Wilson, J. H., Kipper, M. J., Wannemuehler, M. J., Narasimhan, B. Protein stability in the presence of polymer degradation products: Consequences for controlled release formulations. Biomaterials. 27, 3312-3320 (2006).
- Determan, A. S., Lin, V. S. Y., Nilsen-Hamilton, M., Narasimhan, B. Encapsulation, stabilization, and release of BSA-FITC from polyanhydride microspheres. J. Controlled Release. 100, 97-109 (2004).
- Chavez-Santoscoy, A., Roychoudhury, R., Ramer-Tait, A. E., Pohl, N. L. B., Wannemuehler, M. J., Narasimhan, B. Tailoring the immune response of alveolar macrophages by targeting different C-type lectin receptors using "pathogen-like" amphiphilic polyanhydride nanoparticles. Biomaterials. , (2011).
- Carrillo-Conde, B., Song, E. -. H., Chavez-Santoscoy, A., Phanse, Y., Ramer-Tait, A., Pohl, N. L. Mannose-functionalized "pathogen-like" polyanhydride nanoparticles target C-type lectin receptors on dendritic cells. Mol. Pharmaceutics. 8, 1877-1886 (2011).
- Carrillo-Conde, B., Schiltz, E., Torres, M. P., Yu, J., Phillips, G., Minion, C. Amphipilic polyanhydrides for stabilization of Yersinia pestis antigens. Acta. Biomater. 6, 3110-3119 (2010).
- Reddy, S. T., Swartz, M. A., Hubbell, J. A. Targeting dendritic cells with biomaterials: developing the next generation of vaccines. Trends Immunol. 27, 573-580 (2006).
- Higashi, N., Fujioka, K., Denda-Nagai, K., Hashimoto, S., Nagai, S., Sato, T. The macrophage C-type lectin specific for galactose/N-acetylgalactosamine is an endocytic receptor expressed on monocyte-derived immature dendritic cells. J. Biol. Chem. 277, 20686 (2002).
- Geijtenbeek, T. B. Signalling through C-type lectin receptors: shaping immune responses. Nat. Rev. Immunol. 9, 465-479 (2009).
- Seeberger, P. H. Automated oligosaccharide synthesis. Chem. Soc. Rev. 37, 19-28 (2008).
- Seeberger, P. H. Automated Carbohydrate Synthesis as Platform to Address Fundamental Aspects of Glycobiology-Current Status and Future Challenges. Carb. Res. 343, 1889-1896 (2008).
- Jaipuri, F. A., Pohl, N. L. Toward solution-phase automated iterative synthesis: fluorous-tag assisted solution-phase synthesis of linear and branched mannose oligomers. Org. Biomol. Chem. 6, 2686-2691 (2008).
- Petersen, L. K., Chavez-Santoscoy, A., Narasimhan, B. Combinatorial synthesis of and high-throughput protein release from polymer film and nanoparticle libraries. J. Vis. Exp. , (2011).
- Song, E. -. H., Osanya, A. O., Petersen, C. A., Pohl, N. L. B. Synthesis of multivalent tuberculosis and Leishmania-associated capping carbohydrates reveals structure-dependent responses allowing immune evasion. J. Am. Chem. Soc. 132, 11428-11430 (2010).
- Hakamori, S. Aberrant glycosylation in tumor and tumor associated carbohydrate antigens. Adv. Cancer Res. 59, 257-331 (1989).
- Atherton, T., Sheppard, R. C. . Solid-phase peptide synthesis: a practical approach. , (1999).
- Caruthers, M. H. Gene synthesis machines: DNA chemistry and the uses. Science. 230, 281-285 (1985).
- Plante, O. J., Palmacci, E. R., Seeberger, P. H. Automated solid- phase synthesis of oligosaccharides. Science. 291, 1523-1527 (2001).
- Ko, K. -. S., Park, G., Yu, Y., Pohl, N. L. Protecting group-based colorimetric monitoring of fluorous-phase and solid-phase synthesis of oligoglucosamines. Org. Lett. 10, 5381-5384 (2008).
- Pohl, N. L., Chen, X. H. R., Wang, G. P. Automated solution-phase oligosaccharide synthesis and carbohydrate microarrays: development of fluorous-based tools for glycomics. Chemical Glycobiology. , 272-287 (2008).
Réimpressions et Autorisations
Demande d’autorisation pour utiliser le texte ou les figures de cet article JoVE
Demande d’autorisationThis article has been published
Video Coming Soon