Un abonnement à JoVE est nécessaire pour voir ce contenu. Connectez-vous ou commencez votre essai gratuit.
Method Article
Identification de la Kinase cycline-dépendante 1 Sites de Phosphorylation spécifique par une Kinase In Vitro d’analyse
* Ces auteurs ont contribué à parts égales
Dans cet article
Résumé
Kinase cycline-dépendante 1 (Cdk1) intervient dans la phase G2 du cycle cellulaire et régule les nombreuses voies cellulaires. Ici, nous présentons un protocole de test in vitro kinase Cdk1, qui permet l’identification des sites de phosphorylation de Cdk1 spécifiques pour l’établissement de cibles cellulaires de cette kinase importante.
Résumé
Kinase cycline-dépendante 1 (Cdk1) est un contrôleur maître du cycle cellulaire chez tous les eucaryotes et phosphoryle environ 8 à 13 % du protéome ; Toutefois, le nombre de cibles identifiées pour Cdk1, particulièrement dans les cellules humaines est encore faible. L’identification des sites de phosphorylation de Cdk1 spécifique est importante, car elles donnent des indications mécanistes sur comment Cdk1 contrôle du cycle cellulaire. Régulation du cycle cellulaire est cruciale pour la ségrégation des chromosomes fidèle, et défauts dans ce complexe processus conduisent à des aberrations chromosomiques et le cancer.
Nous décrivons ici une analyse de kinase in vitro qui est utilisée pour identifier les sites de phosphorylation de Cdk1 spécifiques. Dans ce test, une protéine purifiée est phosphorylée in vitro par disponibles dans le commerce humain Successful Cdk1/cycline B. phosphorylation est confirmée par SDS-PAGE et sites de phosphorylation sont par la suite identifiés par spectrométrie de masse. Nous décrivons également les protocoles de purification qui donnent des préparations de protéines très pure et homogène qui conviennent à l’analyse de la kinase et un essai de liaison pour la vérification fonctionnelle des sites de phosphorylation identifiés, qui sonde l’interaction entre un signal de localisation nucléaire classique (cNLS) et son récepteur de transport nucléaire IMPORTINE α. Pour vous aider avec le plan expérimental, nous passons en revue les approches pour la prédiction des sites de phosphorylation de Cdk1 spécifique de séquences protéiques. Ces protocoles présentent ensemble une approche très puissante qui donne des sites de phosphorylation de Cdk1 spécifiques et permet des études mécanistes dans Comment Cdk1 contrôle du cycle cellulaire. Étant donné que cette méthode s’appuie sur les protéines purifiées, il peut être appliqué à n’importe quel modèle organisme et rendements des résultats fiables, surtout lorsqu’il est combiné avec des études fonctionnelles cellulaire.
Introduction
Kinases sont des enzymes transfer groupements phosphate de l’ATP sur des substrats et de réguler les nombreux processus cellulaires. Cette phosphorylation est réversible, rapide, ajoute deux charges négatives et emmagasine l’énergie libre et est l’une des modifications post-traductionnelles couramment utilisées par les cellules. CDK1, qui est également connu sous le nom homologue de protéine 2 cycle de division cellulaire (cdc2) est un contrôleur maître du cycle cellulaire dans tous les eucaryotes1,2,3,4,5et phosphoryle une environ 8 à 13 % du protéome6,7.
Alors que les récentes études protéomiques ont identifié de nombreux sites de phosphorylation de protéines, dans la plupart des cas, la kinase responsable de ces modifications est inconnue. Le nombre de cibles Cdk1 connues, en particulier dans les cellules humaines est faible7. L’identification des sites de phosphorylation de Cdk1 spécifique est importante, car elle permet des études mécanistes qui établissent comment Cdk1 contrôle du cycle cellulaire. Régulation du cycle cellulaire est importante pour la ségrégation des chromosomes fidèle et la division cellulaire, et une myriade de processus cellulaires doivent se produire à l’appui de cette importante fonction physiologique. Cela inclut les enrayer la transcription et la traduction avant le début de la mitose, ainsi qu’une réorganisation dramatique dans la structure cellulaire et l’organisation, comme le démontage de l’enveloppe nucléaire, condensation des chromosomes et assemblage du fuseau mitotique. Déréglementation et erreurs dans ces processus causent cancer, malformations congénitales ou mort cellulaire mitotique. Inhibiteurs spécifiques de Cdk1 tels que RO-3306 ont été développés8, qui fournissent des outils puissants pour des études fonctionnelles, et certains de ces inhibiteurs sont actuellement en essais cliniques pour le traitement du cancer (voir9 pour examen).
Nous décrivons ici une analyse de kinase in vitro qui permet l’identification de sites de phosphorylation de Cdk1 spécifiques. Dans ce test, disponible dans le commerce humain Cdk1/cycline B sert de phosphoryler une cible purifiée protéines in vitro. La phosphorylation du substrat augmente sa masse et ajoute deux charges négatives ; par conséquent, phosphorylation réussie est confirmée par un déplacement vers le haut de la bande de protéine gel SDS-page. Sites de phosphorylation de CDK1 spécifiques sont par la suite identifiés par analyse de spectrométrie de masse des protéines in vitro phosphorylée. Pour vous aider avec le plan expérimental, nous passons en revue également d’outils informatiques et de références pour la prédiction des sites de phosphorylation de Cdk1 spécifique de la séquence protéique. En outre, nous décrivons également les protocoles de purification qui donnent des préparations de protéines très pure et homogène pour l’analyse de la kinase. Enfin, les sites de phosphorylation identifiés doivent être vérifiées par des études fonctionnelles et un essai de liaison simple est décrit ici à cet effet. Combiné, c’est une approche très puissante qui donne des sites de phosphorylation de Cdk1 spécifiques et permet des études mécanistes dans Comment Cdk1 contrôle du cycle cellulaire7,10,11. Étant donné que cette méthode s’appuie sur les protéines purifiées, il peut être appliqué à n’importe quel modèle organisme et rendements des résultats fiables. Toutefois, la vérification fonctionnelle de la phosphorylation obtenus sites in vitro est conseillée, car les cellules ont des mécanismes réglementaires supplémentaires mis en place, comme des modifications post-traductionnelles, partenaires d’interaction ou localisation cellulaire qui peut rendre les sites de phosphorylation accessibles ou inaccessibles pour la reconnaissance de Cdk1.
CDK1 reconnaît un site de phosphorylation de consensus qui consiste (Ser/Thr-Pro-X-Lys/Arg), où X est n’importe quel résidu et une sérine ou thréonine est le site de phosphorylation. Particulièrement importante pour la reconnaissance est la présence de la proline en position + 1. En outre, les résidus basiques sont préférés dans les positions + 2 ou + 3, avec la plupart sites de phosphorylation de Cdk1 spécifique contenant un Lys ou Arg à la + 3 position6,12.
Activation de Cdk1 est étroitement contrôlée et conduit à l’apparition de la mitose1,2,3,4,5. L’activité des kinases cycline-dépendantes dépend en général de leur association avec les cyclines distinctes (cycline A, B, C, D et E chez les humains), qui sont expriment au oscillant niveaux tout au long du cycle cellulaire13. Expression de CDK1 est constante à travers le cycle cellulaire et la régulation de son activité s’appuie sur son association avec les sous-unités régulatrices cycline A et cycline B5,13,14,15, comme ainsi que les modifications post-traductionnelles. Formation du complexe Cdk1/cycline B est nécessaire pour la kinase activation5,14,15,16,17,18. Dans la phase G2, cycline B est traduit dans le cytosol et importée dans le noyau où il se lie à la Cdk15,14,15,16,17,18; Cependant, la Cdk1/cycline B se tient inactivé par phosphorylation aux résidus Thr14 et Tyr15 par les kinases Cdk1-inhibiteur humains Myt1 (kinase cdc2-inhibitrice associées aux membranes tyrosine et thréonine-spécifique) et Wee1, respectivement19, 20,21. Dans la dernière phase G2, déphosphorylation de Thr14 et Tyr15 par la phosphatase de 25 de cycle de division cellulaire (cdc25) permet d’activer l’activité kinasique du complexe Cdk1/cycline B et déclenche l’ouverture de la mitose12,14, 18 , 20 , 22 , 23. la phosphorylation de Thr161 est également requise pour l’activation de Cdk1/cycline B et est véhiculé par Cdk7, le Cdk-activating kinase (CAK)18. Dégradation de la cycline B en anaphase inactive Cdk1, permettant la sortie de la mitose24,25. Activation de Cdk1/cycline B est donc un processus complexe. Le protocole présenté ici est exécuté avec commercialement disponible Cdk1/cycline B. Pendant l’expression recombinante de ce complexe dans des cellules d’insectes, il est activé en vivo par des kinases endogènes14,20 et reste actif à l’État purifié. La résultante active, recombinant humain Cdk1/cycline B convient à des essais in vitro kinase.
Nous décrivons ici un protocole pour l’identification des sites de phosphorylation de Cdk1 spécifique dans le centromère humaine protéines F (CENP-F)10. CENP-F est une protéine du kinétochore qui réside dans le noyau pendant la majeure partie de l’interphase (G1 et phase S) et qui est exportée vers le cytosol dans le G2 phase26,27,28 à un Cdk1-dépendante manière10, 11. localisation nucléaire est conférée par une bipartite cNLS26. cNLSs sont reconnus par le facteur de transport nucléaire IMPORTINE α, qui facilite, ainsi que l’IMPORTINE β et RanGDP, l’importation du cNLS-cargo, dans le noyau29. Les exportations nucléaires lors de la phase G2 sont facilitée via une exportation inconnu voie10. Une fois CENP-F se trouve dans le cytosol, il est recruté à l’enveloppe nucléaire et recrute à son tour la protéine motrice complexe dynéine30,31. Cette voie est importante de placer le noyau respectif à centrosome pendant les étapes initiales de l’assemblage du fuseau mitotique de manière dynéine-dépendante, ce qui est importante pour le bon timing d’entrée mitotique et un processus fondamental dans le cerveau développement30,31,32. À partir de la phase G2, CENP-F est aussi rassemblé dans le kinétochore où il a un rôle important pour les fidèles de chromosome ségrégation27,28,33,34,35 . Une étape clé de réglementation de ces voies est l’exportation nucléaire du CENP-F dans la phase G2, qui dépend de la Cdk110,11. Nous décrivons ici un protocole pour l’identification des sites de phosphorylation de Cdk1 spécifique dans le cNLS du CENP-F. Phosphomimetic mutations de ces sites ralentissent import nucléaire du CENP-F, ce qui suggère que la Cdk1/cycline B régule directement localisation cellulaire de CENP-F par la phosphorylation de la cNLS10.
Dans l’ensemble, cette analyse de kinase in vitro permet l’identification des substrats spécifiques pour les protéines cibles de kinase Cdk1. purifiée sont phosphorylées in vitro par Cdk1/cycline B complexe disponible dans le commerce et les sites de phosphorylation sont identifiés par la suite par spectrométrie de masse. L’identification des sites de phosphorylation de Cdk1 spécifique prend en charge les études mécanistiques qui révèlent comment Cdk1 contrôle du cycle cellulaire.
Protocole
1. la prévision des Sites de Phosphorylation de Cdk1 spécifique de la séquence protéique
- Avant de commencer l’analyse de la kinase, analyser la séquence protéique pour sites de phosphorylation de Cdk1 spécifiques prévus et rechercher la littérature pour les sites de phosphorylation établie expérimentalement avec une spécificité kinase inconnu. Utilisez les outils suivants, bases de données et références qui sont résumées.
- Les circuits graphiques intégrés 3.0 logiciel36,37 (http://gps.biocuckoo.org/online_full.php) permet de prédire les sites de phosphorylation de Cdk1 spécifique dans la séquence de protéine cible. Utilisez le lien ici pour une prévision globale qui inclut les annotations de structure secondaire et accessibilité surface.
- Dans le logiciel, saisissez la séquence de la protéine au format FASTA. Pour la spécificité de la kinase, vérifier la sérine/thréonine kinase, CDK, CDC2, DCEG CDK1et décochez toutes les autres spécificités. Sélectionnez moyenne comme seuil et cliquez sur le bouton soumettre .
- Comparer les sites prédites obtenus avec le site de phosphorylation du consensus Cdk1 (Ser/Thr-Pro-X-Lys/Arg).
- Vérifiez le site prévu pour la proline à côté le résidu phosphorylée (certains substrats Cdk1 sont phosphorylés à un site minimal (Ser/Thr-Pro)6,12). En outre, recherchez les résidus basiques, qui sont préférées dans les positions + 2 ou + 3, avec la plupart sites de phosphorylation de Cdk1 spécifique contenant un Lys ou Arg à la position + 36,12.
- Assurez-vous également que le site est accessible pour la reconnaissance, comme la présence d’un site de consensus complet n’est pas suffisante pour la phosphorylation de Cdk1.
- Inspectez la surface accessibilité et annotation de prédiction de structure secondaire dans la sortie de circuits graphiques intégrés, qui précise que le site devrait pour être accessible ; N - et C-terminus des protéines sont souvent flexibles et accessibles pour la phosphorylation.
- Si une structure aux rayons x de la protéine cible est disponible, vérifiez l’accessibilité des sites de phosphorylation putatif en inspectant leur emplacement dans la structure.
- Rechercher la documentation pour les sites de phosphorylation expérimentalement établi avec spécificité kinase inconnu à l’aide de la UniProtKB/Swiss-Prot de base de données38 (http://www.uniprot.org).
- Entrez le nom de la protéine dans la zone Rechercher et cliquez sur le bouton Rechercher . Sélectionnez l’entrée de la séquence correcte. Sites de phosphorylation sont annotées et référencés dans la section modifications des acides aminés .
- Recherche pour l’étude de la protéomique des extraits mitotiques des cellules humaines lignes7,39,40, qui sont particulièrement utiles car Cdk1 devient actif lors de la phase G2 du cycle cellulaire.
- Identifier le cNLS bipartite de NLSmapper (facultatif).
Remarque : Pour les protéines qui transportent entre le cytosol et le noyau, un mécanisme commun pour le règlement de la localisation cellulaire est la phosphorylation d’un cNLS bipartite en position du motif majeur de Cdk1-1. La phosphorylation abolit la localisation nucléaire le G2 phase10,41,42,43.- Pour ces protéines navette, identifier le cNLS dans la séquence de la protéine en NLSmapper43 (http://nls-mapper.iab.keio.ac.jp/cgi-bin/NLS_Mapper_form.cgi). Coller la séquence des protéines sous forme de texte dans la case de la séquence, sélectionnez un point de coupure de 5.0 et choisir de chercher la NLS dans l' ensemble de la région. Cliquez sur le bouton de Prédire NLS .
- Comparer le cNLS prédit obtenu contre la séquence consensus d’un cNLS bipartite, qui comprend le motif mineur (Lys-Arg), un éditeur de liens d’au moins 10 résidus et le motif majeur (Lys-Lys/Arg-X-Lys/Arg), où X est n’importe quel résidu qui n’est pas chargé négativement .
- Vérifier si le site de phosphorylation de Cdk1 prédit (*) est adjacent au motif majeur en position de-1 de l’éditeur de liens : Ser/Thr*-Pro/X-X-Lys-Lys/Arg-X-Lys/Arg.
Remarque : La phosphorylation d’un cNLS bipartite en position de Cdk1-1 a été établie comme un mécanisme de réglementation pour la localisation cellulaire pour plusieurs navette protéines10,41,42, 43.
2. l’expression de protéines recombinantes dans Escherichia Coli
- Utiliser les plasmides d’expression de mesures 2.1.1-2.1.2 pour l’expression de protéines recombinantes dans e. coli.
- Pour créer l' expression humaine de CENP-F (résidus de 2 987-3 065) construire, générer insertions en amplifiant les fragments d’ADN par polymerase chain reaction (PCR) à partir d’une construction CENP-F pleine longueur (GenBank accession : U19769.1). Utiliser les amorces suivantes : AGTCGGGGATCCCAGCAATCTAAACAAGATTCCCG et AGTCGGCTCGAGTCATTATTCTGCAGGGTGAATACCACTCATG.
Remarque : Le plasmide de CENP-F humain pleine longueur a été généreusement fourni par Dr X. Zhu, instituts des Sciences biologiques, Académie chinoise des Sciences, Shanghai, Chine.- Cloner l’insert dans le vecteur pGEX6p1 avec les sites de restriction BamHI et XhoI. Ce plasmide permet d’exprimer les protéines de fusion N-terminal glutathion S-transférase (GST) de CENP-F (résidus de 2 987-3 065).
NOTE : La balise GST peut être clivée au large par la protéase précède (désormais dénommée protéase PS).
- Cloner l’insert dans le vecteur pGEX6p1 avec les sites de restriction BamHI et XhoI. Ce plasmide permet d’exprimer les protéines de fusion N-terminal glutathion S-transférase (GST) de CENP-F (résidus de 2 987-3 065).
- Pour l' humain expression d’IMPORTINE α construire, générer des insertions en amplifiant les fragments d’ADN par PCR d’une matrice d’ADNc pleine longueur IMPORTINE α2 (adhésion de séquence NM_002264.3 ; amorces : GCACTACATATGTCCACCAACGAGAATGCTAATA et TCACGCCTCGAGTTATCAAAAGTTAAAGGTCCCAGGAGCC).
Remarque : En raison de la similitude des isoformes, cette construction de α2 IMPORTINE est appelée dans le texte de subséquent IMPORTINE α.- Cloner l’insert dans le vecteur pET28a-pres avec les sites de restriction Ndel et XhoI.
NOTE : Il s’agit d’un vecteur mis à jour le pET28a dans lequel la séquence codant pour le site de clivage de la thrombine a été remplacé par une séquence codant pour un site de clivage de protéase PS. Ce plasmide permet d’exprimer une protéine de fusion d’IMPORTINE α d’un N-terminal son6-tag, où le son6-tag peut être clivé au large de protéase de PS.
- Cloner l’insert dans le vecteur pET28a-pres avec les sites de restriction Ndel et XhoI.
- Pour créer l' expression humaine de CENP-F (résidus de 2 987-3 065) construire, générer insertions en amplifiant les fragments d’ADN par polymerase chain reaction (PCR) à partir d’une construction CENP-F pleine longueur (GenBank accession : U19769.1). Utiliser les amorces suivantes : AGTCGGGGATCCCAGCAATCTAAACAAGATTCCCG et AGTCGGCTCGAGTCATTATTCTGCAGGGTGAATACCACTCATG.
- Pour créer des mutations ponctuelles d’une protéine cible, effectuez la mutagénèse dirigée avec un kit.
- Exprimer les protéines recombinantes chez e. coli pour purification ultérieure.
- Faire des stocks suivants : kanamycine 50 mg/mL (1:1, 000 solution mère), chloramphénicol 35 mg/mL dans 70 % éthanol (1:1, 000), ampicilline 100 mg/mL (1 / 1, 000) et 1 M isopropyl β-D-1-thiogalactopyranoside (IPTG ; 1:5 000).
- STERILE filtrer les stocks et conserver à-20 ° C. Éviter les cycles de gel-dégel répétés d’IPTG.
- Transformer 1 µL de plasmide expression dans 50 µL de cellules capables de la souche e. coli de pLysS Rosetta 2 (DE3), selon les instructions du fabricant.
- Plaque de la culture sur gélose Luria-Bertani (LB) avec le chloramphénicol (35 µg/mL LB) et ampicilline (100 µg/mL LB) pour la construction de CENP-F, ou le chloramphénicol et la kanamycine (culture de 50 µg/mL) pour l’IMPORTINE α construct. Incuber les boîtes pendant 12 à 20 h à 37 ° C.
- Prélever une colonie unique et l’inoculer dans 50 mL de LB additionné d’antibiotiques (voir étape 2.3.4). Incuber la préculture et en agitant à 160-180 tr/min pendant 12 à 20 h à 37 ° C.
- Préparer 1 L de LB moyen dans un 2 800 mL dérouté Fernbach fiole. Faire deux flacons pour chaque préculture et autoclave eux. Pour permettre l’aération, ne pas remplir les fioles à plus de deux tiers la fiole volume. Erlenmeyers peuvent être utilisés aussi bien.
- Ajouter des antibiotiques (étape 2.3.4) et 10 mL d’une solution de glucose 40 % (p/v) stérile filtré par 1 L de refroidi lb ajouter 20 mL de préculture par 1 L de milieu LB.
Remarque : L’absorbance à 600 nm d’un 01:10 dilution de la préculture devrait se situer entre 0,15 à 0,2. - Incuber les flacons et en agitant à 160-180 tr/min à 37 ° C. Mesurer l’absorbance à 600 nm de la culture de bactéries régulièrement. Si l’absorbance atteint 0,5 à 0,6, induisent l’expression de la protéine en ajoutant 0,2 mM IPTG (200 µL de stock de 1 M par 1 L de milieu LB).
Remarque : Il est important que les cellules sont induites à l’absorption correcte. Habituellement, cela prend 3-4 h pour arriver à ce stade. - Incuber les flacons et en agitant pendant 3 h à 37 ° C. Récolter les cellules par centrifugation (15 min, 4 100 x g, 4 ° C, rotor à balancier). Jeter le surnageant. Remettre en suspension les granules cellulaires dans 20 mL de tampon de liaison GST (CENP-F) ou son6-tampon de liaison (IMPORTINE α) par 1 L de la culture. Stocker les cellules à-80 ° C.
- Préparer le tampon de la GST-liaison (10 mM Tris pH 8.0 à 25 ° C, 150 mM NaCl, 1 mM le dithiothréitol (DTT), EDTA de 0,5 mM) et son6-liaison tampon (10 mM Tris pH 8.0 à 25 ° C, 250 mM NaCl, 5 mM Imidazole pH 8,0, 5 mM β-mercaptoéthanol (BME)) à l’avance.
3. purification de protéine recombinante par chromatographie d’affinité-glutathion et Filtration sur Gel
- Effectuer les actions suivantes : 1 M DTT (1:1, 000 actions, stérile filtrée avec taille de pore 0,2 µM et dégazé) ; 250 mM le fluorure de phénylméthylsulfonyle (PMSF ; 1 : 1 000 actions en diméthylsulfoxyde). Conserver à-20 ° C. Éviter les cycles de gel-dégel répétés.
- Faire les tampons suivants et refroidir à 4 ° C.
- Préparer le tampon de GST-liaison à l’aide de 10 mM Tris pH 8.0 à 25 ° C, 150 mM NaCl, 1 millimètre DTT, EDTA de 0,5 mM.
- Préparer le tampon d’élution GST utilisant 10 mM réduit de glutathion (0,15 g/50 mL) dissoute dans un tampon de 50 mM Tris pH 8.0 à 25 ° C, 150 mM NaCl, 1 millimètre DTT. Confirmer que le pH de la dernière mémoire tampon est 8.0 et utiliser le même jour, qu'elle a été faite.
- Préparer le tampon de Gel-filtration utilisant 20 mM Tris pH 7,5 à 25 ° C, 60 mM NaCl, 2 mM TNT. STERILE filtrer le tampon avec un filtre de bouteille-top (taille des pores 0,2 µM). Dégazer le tampon tout en agitant sous vide (-6 lb/po2) pendant 15 min.
- Ajouter TNT à tous au-dessus des tampons sur la journée d’utilisation.
- Décongeler les cellules de l’article 2 qui contiennent la construction CENP-F. Réglez le volume à 40 mL avec le tampon de GST-liaison. Ajouter 1 millimètre DTT, 0,25 mM PMSF, 0,5 mM EDTA (solution mère de 0,5 M, pH 8,0), 7 mg de chlorhydrate de benzamidine (1 mM) et la méthionine de 40 mg D/L.
Remarque : Afin de réduire la dégradation protéolytique, exécutez toutes les étapes à 4 ° C, de préférence dans une pièce froide, sauf indication contraire. Garder les cellules, lysats et fractions de protéine purifiée sur glace à tout moment et ajouter des inhibiteurs de la protéase. Pour éviter l’oxydation des résidus cystéine et méthionine, ajouter des agents réducteurs comme TNT et méthionine le jour de l’expérience. Pour réduire la dégradation protéolytique, travailler à travers les étapes rapidement. - Lyse des cellules dans un sonicateur comme suit. Remplissez une carafe en verre avec le lysat et le plonger dans un bain d’eau glacée. Laisser agir la culture (1 min 40 s, à 100 W (50 %) / amplitude de sortie, avec 10 impulsions s et 10 s cycles de repos). Ajouter 250 µM PMSF après sonication. Inspecter le lysat cellulaire, qui devrait regarder plus transparent et plus visqueux.
- Claire le lysat par centrifugation à 12 000-40 000 x g, 25 min, 4 ° C. Utilisez des tubes à centrifuger de fond rond et un rotor à angle fixe.
- Effectuer l’équilibration en ajoutant 2 mL de glutathion d’agarose lisier de 1:1 pour une colonne de chromatographie jetable. La colonne résultante aura un volume de 1 mL. Laver la colonne avec 25 mL d’eau ultrapure et 25 mL de tampon de GST-liaison.
- Exécuter la liaison comme suit. Travaillant dans une chambre froide ou une zone froide, décanter le lysat de boulettes. Filtrer la lysat (taille des pores de 0,2 µm) et versez-la sur la colonne bouchée. Cap de la colonne et il incuber tout doucement oscillant pendant 30 min à 4 ° C.
- Pour laver la colonne, mettez-le sur une grille, laisser le reposer et recueillir le flux à travers la résine. Laver la colonne avec 25 mL de tampon de GST-liaison.
-
Éluer par clivage protéolytique.
- Branchez la colonne. Ajouter 400 µL de tampon de GST-liaison et 250 µL de protéase PS (2 mg/mL de bouillon avec une activité de 1 000 U/mg, soit purifiée en laboratoire ou acheté ; voir Table des matières).
- Boucher de la colonne et agiter doucement pour remettre en suspension dans la résine dans la mémoire tampon. Incuber les colonnes pendant 16 à 20 h à 4 ° C. Puis ajouter 4 mL de tampon de GST-liaison pour éluer le fragment CENP-F clivé clivage protéolytique de la colonne.
-
Élution de glutathion
- Branchez la colonne, ajouter 4 mL de tampon d’élution GST (4 volumes de colonne) et incuber pendant 10 min Éluer la balise GST liée. Recueillir l’éluat. Régénérer les colonnes avant réutilisation comme indiqué par le fabricant.
- Analyser la fraction d’élution de protéase PS et la fraction d’élution de glutathion par SDS-PAGE sur gels d’acrylamide de 16 %. Effectuer l’électrophorèse à 25 V/cm pour 45 min. tache les gels de bleu de Coomassie. La fraction de protéase PS contiendra le fragment purifié de CENP-F, alors que la fraction de glutathion contiendra la balise GST clivée. Inspecter le gel afin d’évaluer l’efficacité de clivage protéolytique.
- Concentrer le PS éluat de protéase à 0,5 mL à l’aide d’unités de filtration centrifuge avec un poids moléculaire de 3 kDa coupure (voir Table des matières). Ajoutez l’éluat dans le compartiment supérieur du filtre et centrifuger il par incréments de 10-15 min à 4 100 x g, 4 ° C (rotor à balancier) à concentrer l’échantillon. La composition de pipetage après chaque incrément.
- Connecter un approprié gel colonne de filtration (voir Table des matières pour infos achat) à un système de chromatographie en phase liquide (FPLC) protéine rapide et il équilibrer avec volume de 1 colonne de gel filtration tampon.
- Centrifuger le fragment CENP-F concentré dans une micro-centrifugeuse (20 min, 21 700 x g, 4 ° C). Injecter l’échantillon sur la colonne et il éluer avec volume de 1 colonne de gel filtration tampon. Recueillir des fractions de 0,6 mL.
Remarque : Le tampon de gel filtration est optimisé pour assurer la compatibilité avec l’analyse de la kinase ultérieures. Vérifier si la protéine cible est stable dans cette mémoire tampon. Si elle n’est pas stable, essayez d’ajouter plus de chlorure de sodium. - Analyser les fractions de pic par SDS-PAGE (étape 3.11). Mettre en commun les fractions de pic qui contiennent des fragments de CENP-F pures. Concentrer les fragments CENP-F purifiées à 3,3 mg/mL (étape 3.12). Analyser les fragments de CENP-F purifiées par SDS-PAGE (étape 3.11).
-
Détermination de concentration des protéines
- Diluer l’échantillon 1/100 dans l’eau ultrapure et placez-le dans une micro-cuvette de quartz. Spectres Records à une gamme de longueur d’onde de 220-300 nm dans un spectrophotomètre.
Remarque : La concentration de protéine c (mg/mL) est dérivée de l’équation suivante :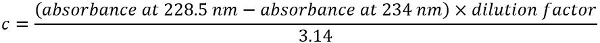
- Diluer l’échantillon 1/100 dans l’eau ultrapure et placez-le dans une micro-cuvette de quartz. Spectres Records à une gamme de longueur d’onde de 220-300 nm dans un spectrophotomètre.
- Faire 50 µL d’extraits de la protéine purifiée dans des microtubes 0,5 mL et gel des flash dans l’azote liquide. Stocker les aliquotes à-80 ° C.
4. purification de protéine recombinante par chromatographie d’affinité Ni-NTA
- Faire les tampons suivants et laisser refroidir à 4 ° C.
- Préparer le son6-tampon de liaison à l’aide de 10 mM Tris pH 8.0 à 25 ° C, 250 mM NaCl, 5 mM Imidazole pH 8,0, 5 mM BME. Ajouter BME à tous les tampons sur le jour d’utilisation.
- Préparer le son6-tampon de lavage de la même manière que le son6-liaison tampon mais en utilisant 20 mM Imidazole.
- Préparer le son6-tampon d’élution de la même façon que le tampon de liaison mais en utilisant 150 mM Imidazole.
-
Décongeler les cellules de l’article 2 qui contiennent l’IMPORTINE α construire et réglez le volume à 40 mL avec le son6 -tampon de liaison. Ajouter 5 mM BME, PMSF 0,250 mM, 7 mg de chlorhydrate de benzamidine (1 mM) et la méthionine 40 mg D/L.
- Procéder comme décrit dans les étapes 3,4-3,8 avec les variations suivantes : utiliser son6-tampon de liaison au lieu de tampon de GST-liaison pour toutes les étapes. Au lieu de glutathion d’agarose, utiliser 4 mL de l’affinité de Nickel pour créer la colonne, ce qui aura un volume de colonne de 2 mL de gel (voir Table des matières).
NOTE : Colonnes d’affinité de Nickel sont incompatibles avec la TNT et d’EDTA. Au lieu du gel d’affinité de Nickel, Ni2 +- nitrilotriacétique, acide (NTA) agarose peut être utilisé, si la concentration de l’imidazole dans la mémoire tampon d’élution est augmentée à 250 mM (voir Table des matières).
- Procéder comme décrit dans les étapes 3,4-3,8 avec les variations suivantes : utiliser son6-tampon de liaison au lieu de tampon de GST-liaison pour toutes les étapes. Au lieu de glutathion d’agarose, utiliser 4 mL de l’affinité de Nickel pour créer la colonne, ce qui aura un volume de colonne de 2 mL de gel (voir Table des matières).
- Laver les colonnes avec 8 mL de son6-tampon de lavage.
- Élution l’IMPORTINE α avec 12 mL de son6-élution de tampon et analyser l’éluat par SDS-PAGE (étape 3.11).
- Ajouter 250 µL de protéase PS (étape 3,9) de l’éluat et incuber pendant 16 à 20 heures à 4 ° C. Dans l’intervalle, dialyser l’éluat deux fois contre 1 L de son6-tampon de liaison pour 2-20 h, à l’aide d’une membrane de dialyse avec un poids moléculaire 6-8 kDa coupure.
- Régénérer la colonne de gel d’affinité Nickel tel que décrit par le fabricant. Équilibrer la colonne avec 25 mL de son6-tampon de liaison. Ajoute la colonne de la protéine dialysée et effectuez l' étape de liaison , comme indiqué au point 3.7.
- Recueillir le débit à travers, qui contient la purifiée IMPORTINE α (avec le son6-tag clivé au large) et Éluer la protéine reste avec une autre 4 mL de son6-tampon de liaison. Mettre en commun ces fractions. Éluer ensuite les colonnes avec 12 mL de son6-tampon d’élution. Cette fraction contient des impuretés.
- Analyser clivés et clivés IMPORTINE α des étapes 4.4-4.5 et les deux fractions d’élution de cette étape de SDS-PAGE (étape 3.11) pour évaluer l’efficacité de son6-marquer le clivage et la pureté.
- Concentrer l’IMPORTINE α à 8 mg/mL et flash-congélation dans l’azote liquide (étapes 3.15-3.17).
5. analyse in Vitro de Kinase Cdk1/cycline b
-
Analyse in vitro de kinase
Remarque : À l’arrivée de la kinase, faire des petites parties aliquotes, flash-congélation dans l’azote liquide et les stocker à-80 ° C. Utiliser dans les 6 mois. Alors que le poids moléculaire est de 34 kDa pour Cdk1 et 48 kDa pour la cycline B, le poids moléculaire apparent de la cycline B à SDS-PAGE est environ 60 kDa.- Préparer le 10 x à l’aide du tampon (fourni avec la kinase) PK 0,5 M Tris-HCl 0,1 M MgCl2, 1 mM EDTA, 20 mM DTT, 0,1 % Brij 35, pH de 7,5 à 25 ° C.
- Préparer les 10 de stock d’ATP : préparer une solution de 4 mM ATP dans 1 x tampon de PK et vérifier le pH final du stock. Stocker dans de petites parties aliquotes à-20 ° C et éviter les cycles de gel-dégel.
- Fragment de Mix 40 µL de CENP-F (à une concentration de 3,3 mg/mL, ou 400 µM), 6 µL 10 x PK tampon, 3 µL d’eau ultrapure, stock de 10 x 6 µL ATP et humain 5 µL Cdk1/cycline B (1 µg, 100 U) dans un microtube 0,5 mL.
Remarque : Le fragment CENP-F a une masse molaire de 8,6 kDa et quatre sites de phosphorylation de Cdk1 spécifiques. Pour un nouveau substrat, ajuster la concentration de kinase dans le dosage selon la concentration molaire de la protéine et selon le nombre de sites de phosphorylation. L’activité du stock Cdk1/cycline B humain recombinant est 20 000 U/mL et l’activité spécifique est de 1 000 000 U / mg. 1 U est définie comme la quantité de Cdk1/cycline B nécessaire pour catalyser le transfert de 1 pmol de phosphate au substrat de peptide de Cdk1 PKTPKKAKKL-NH2 (50 µM) en 1 min à 30 ° C (voir Table des matières). - Préparer une réaction de contrôle sans Cdk1/cycline B. Incuber les réactions dans un bain d’eau pour 1 à 16 h à 30 ° C.
- Analyser les 2,5 µL de la réaction de dosage kinase et 2,5 µL du contrôle par SDS-PAGE (étape 3.11), en utilisant un gel avec 16 % d’acrylamide. Pour augmenter la résolution, prolonger le temps d’exécution.
- Ajouter un volume égal de solution de chlorhydrate de guanidine 6 M dans la réaction de dosage kinase restants (et au contrôle). La concentration de chlorhydrate de guanidine final sera de 3 M. analyser ces échantillons par spectrométrie de masse (Section 6) pour identifier les sites de phosphorylation ou envoyer les échantillons à une installation de spectrométrie de masse pour l’analyse et effectuez ensuite la fonction vérification ( Article 7).
Remarque : Pour l’analyse de spectrométrie de masse ultérieures, il est très important que l’efficacité de la phosphorylation des sites individuels est aussi haute que possible, préférence 100 %, sinon les sites de phosphorylation ne peut pas être mappées. Grandement améliorer l’efficacité de la phosphorylation, ajouter de plus grandes quantités de Cdk1/cycline B et augmenter le temps d’incubation à 16 h. La concentration d’ATP peut également être doublée. - Pour le dépannage, effectuer un dosage de kinase in vitro du CENP-F (résidus de 2 987-3 065) comme témoin positif. Utiliser des lots frais de Cdk1/cycline B avec une activité élevée.
6. l’identification des Sites de Phosphorylation de Cdk1 spécifiques par spectrométrie de masse
- Pour dénaturer et dessalement des échantillons de la protéine, effectuer micrométrique de chromatographie en phase inverse avec une colonne PLRP300.
- Pour obtenir le nombre de sites de phosphorylation dans le fragment de CENP-F, analyser l’intacts in vitro phosphorylée CENP-F 84-mer par spectrométrie de masse piège ionique électrospray (ESI-ITMS)44,45.
- Pour déterminer l’emplacement du site acide phosphoamino du CENP-F, préparer les condensés de la trypsine du in vitro phosphorylée échantillons de protéines CENP-F. Dessalement la digestion trypsique avec embouts de dessalage.
- Analyser les condensés tryptiques de CENP-F par ionisation par électronébulisation Fourier transform ion cyclotron resonance la spectrométrie de masse (ESI-FTICR MS). Effectuer une analyse sur un spectromètre de masse FTICR-ESI avec un temps d’accumulation de 169 µs.
NOTE : La précision des masses déterminée par ESI-FTICR MS se trouve amu 0,005. Afin de quantifier le taux de chaque espèce phosphorylé respectif à la quantité de protéines totales, déterminer les hauteurs des pics des spectres de masse.
7. fonctionnelle Verification : Tester les effets des Mutations Phosphomimetic sur les Interactions protéine-protéine par analyse chromatographie d’Exclusion
Remarque : pour vérification fonctionnelle des sites de phosphorylation Cdk1 spécifiques identifiés, des mutants de phosphomimetic des fragments CENP-F ont été créés en remplaçant les sites de phosphorylation identifiés par aspartates. La charge négative de l’aspartate imite les effets de la phosphorylation. Un mutant S3048D du fragment CENP-F (résidus de 2 987-3 065) a été créé.
- Pour une vérification fonctionnelle, comparer la liaison de type sauvage et des fragments de phosphomimetic CENP-F à IMPORTINE α. utilisent une filtration sur gel analytique comme l’essai de liaison. Pour la filtration sur gel analytique, purifier des fragments CENP-F par chromatographie d’affinité de glutathion (étapes 3.1-3.12) et sauter l’étape de filtration de gel.
- Concentrer la protéine à 5-6 mg/mL. Flash-gel aliquotes de protéine dans l’azote liquide (étapes 3.15-3.17).
- Fragments de Mix le CENP-F purifié (0,1 mg, soit sauvage ou la variante S3048D) et purifié IMPORTINE α (0,7 mg) dans un rapport molaire de 1:1. Ajuster le volume de l’échantillon à 200 µL avec tampon de gel filtration. Incuber l’échantillon pendant 30 minutes sur la glace, filtrer l’échantillon (taille des pores 0,2 µm) et désactivez l’échantillon par centrifugation (25 min, 21 700 x g, 4 ° C)
- Séparer l’échantillon par chromatographie d’exclusion (étapes 3.13-3.14). Utilisez un tampon de gel filtration consistant en 20 mM HEPES, pH 7.5, NaCl, 150 mM et 2 mM TNT. Réaliser les expériences de filtration de gel analytiques dans des conditions identiques pour tous les échantillons.
- Calibrer la colonne de filtration gel analytique avec les normes de poids moléculaire de masse molaire connue telle que décrite par le fabricant.
- Analyser les fractions d’élution par 16 % SDS-PAGE (étape 3.11).
Résultats
Nous avons récemment utilisé un dosage in vitro kinase (Figure 1) pour identifier les sites de phosphorylation de Cdk1 spécifiques dans un fragment de CENP-F qui contenait un cNLS10. Ce signal confère une localisation nucléaire de CENP-F pendant la majeure partie de l’interphase. Dans la phase G2, CENP-F est exporté du noyau vers le cytosol de manière Cdk1-dépendante. Pour obtenir des perspicacités mécanistes sur c...
Discussion
Notre analyse de kinase in vitro est une méthode très puissante pour identifier des cibles moléculaires pour la kinase Cdk1, qui est un contrôleur maître du cycle cellulaire et régule les nombreux processus cellulaires importants. La méthode détermine si une protéine purifiée est un substrat pour la Cdk1 et permet l’identification de sites de phosphorylation spécifiques. Ceci facilite les études mécanistiques pour régulation de processus cellulaires par phosphorylation par l’intermédiaire de C...
Déclarations de divulgation
Les auteurs n’ont rien à divulguer.
Remerciements
Nous remercions le Dr David King, Howard Hughes Medical Institute, Université de Californie à Berkeley pour analyse par spectrométrie de masse et des commentaires utiles. Nous remercions m. Xuelian Zhu, Shanghai, instituts des Sciences biologiques, Académie chinoise des Sciences, Shanghai, en Chine, pour fournir une construction CENP-F pleine longueur. Enfin, nous remercions le Dr Susan Bane, Dr. Brian Callahan et Dr Christof Grewer à l’Université de Binghamton pour l’accès à l’équipement. Cette recherche a été financée par la Fondation de recherche pour la State University of New York et du département de chimie, State University of New York à Binghamton.
matériels
| Name | Company | Catalog Number | Comments |
| 2800 ml baffled Fernbach flask | Corning | 44232XL | |
| ampicillin | Gold Biotechnology | A-301-25 | |
| ATP | Fisher Scientfiic | BP413-25 | |
| benzamidine hydrochloride | Millipore Sigma | B6506-25 | |
| bottletop filter | Corning | 431161 | |
| Cdk1/cyclin B recombinant, human 20,000 U/mL | New England Biolabs | P6020 | |
| Cdk1/cyclin B (alternate source) | EMD Millipore | 14-450 | |
| Cdk1/cyclin B (alternate source) | Invitrogen | PV3292 | |
| Cdk1/cyclin B + 10x PK buffer | New England Biolabs | P6020 | |
| CENP-F (residues 2987 – 3065) pGEX6P1 plasmid | Available upon request. | ||
| centrifuge: Heraeus Multifuge X3R, cooled, with TX-1000 swing-out rotor | Thermo Scientific | 10033-778 | |
| centrifugal filter units: Amicon Ultra-15 centrifugal filter units, 3 kDa cutoff, Ultracel-PL membranes | EMD Millipore | UFC900324 | |
| chlorampenicol | Gold Biotechnology | C-105-100 | |
| D/L methionine | Agros Organics / Fisher | 125650010 | |
| desalting pipet tips: Zip tips | Millipore Sigma | ZTC18S008 | |
| disposable chromatography columns, Econo-Pac 1.5 x 12 cm | Biorad | 7321010 | |
| dithiothreitol | Gold Biotechnology | DTT50 | |
| E. coli Rosetta 2(DE3)pLysS strain | EMD Millipore | 71403 | |
| electrospray ionization Fourier transform ion | Bruker Amazon | Apex III | |
| cyclotron resonance mass spectrometer | |||
| electrospray ionization ion trap mass spectrometer | Bruker Amazon | custom | |
| fixed angle rotor: Fiberlite F15-8x-50cy | Thermo Scientific | 97040-276 | |
| FPLC system: Äkta Pure FPLC | GE Healthcare | 29032697 | |
| Gel filtration column: Superdex 200 Increase 10/300 GL | GE Healthcare | 28990944 | |
| glutathione agarose | Pierce | 16101 | |
| glutathione, reduced | Millipore Sigma | G4251-50g | |
| incubation shaker: multitron shaker | Infors | I10102 | |
| isopropyl β-D-1-thiogalactopyranoside | Gold Biotechnology | I2481C50 | |
| kanamycin | Gold Biotechnology | K-120-25 | |
| karyopherin α pet-28a pres plasmid | Available upon request. | ||
| Luria Bertani medium | Fisher Scientfiic | BP1426-2 | |
| microcentrifuge 5418R, refrigerated | Eppendorf | 5401000013 | |
| microtubes (0.5 ml) | Eppendorf | 30121023 | |
| microtubes (1.5 ml) | Eppendorf | 30120086 | |
| Nickel affinity gel: His-Select Nickel affinity gel | Millipore Sigma | P6611-100ml | |
| pGEX-6P-1 plasmid | Millipore Sigma | GE28-9546-48 | |
| phenylmethylsulfonyl fluoride | Gold Biotechnology | P470-10 | |
| PS protease: PreScission protease | GE Healthcare | 27084301 | |
| Phos-tag acrylamide | Wako Pure Chem. Ind. | 304-93521 | |
| reduced gluthathione | Millipore Sigma | G4251-50g | |
| roundbottom centrifuge tubes (Oakridge tubes) | Fisher Scientfiic | 055291D | |
| site-directed mutagenesis kit: QuikChange Lightning | Agilent | 210518 | |
| Site-Directed Mutagenesis Kit | |||
| sonifier: Branson S-250D sonifier | Branson | 15 338 125 | |
| Spectra/Por 1RC dialysis membrane (6-8 kDa cutoff) | Spectrum Labs | 08 670B | |
| swing out rotor TX-1000 | Thermo Scientific | 10033-778 |
Références
- Nurse, P. Cyclin dependent kinases and cell cycle control (Nobel Lecture). ChemBioChem. 3 (7), 596-603 (2002).
- Lee, M. G., Nurse, P. Complementation used to clone a human homologue of the fission yeast cell cycle control gene cdc2. Nature. 327, 31 (1987).
- Lohka, M. J., Hayes, M. K., Maller, J. L. Purification of maturation-promoting factor, an intracellular regulator of early mitotic events. Proc Natl Acad of Sci U S A. 85 (9), 3009-3013 (1988).
- Gautier, J., Norbury, C., Lohka, M., Nurse, P., Maller, J. Purified maturation-promoting factor contains the product of a Xenopus homolog of the fission yeast cell cycle control gene. Cell. 54 (3), 433-439 (1988).
- Gautier, J., Minshull, J., Lohka, M., Glotzer, M., Hunt, T., Maller, J. L. Cyclin is a component of maturation-promoting factor from Xenopus. Cell. 60 (3), 487-494 (1990).
- Ubersax, J. A., Woodbury, E. L., Quang, P. N., Paraz, M., Blethrow, J. D., Shah, K., Shokat, K. M., Morgan, D. O. Targets of the cyclin-dependent kinase Cdk1. Nature. 425 (6960), 859-864 (2003).
- Petrone, A., Adamo, M. E., Cheng, C., Kettenbach, A. N. Identification of Candidate Cyclin-dependent kinase 1 (Cdk1) Substrates in Mitosis by Quantitative Phosphoproteomics. Mol Cell Proteomics. 15 (7), 2448-2461 (2016).
- Vassilev, L. T., Tovar, C., Chen, S., Knezevic, D., Zhao, X., Sun, H., Heimbrook, D. C., Chen, L. Selective small-molecule inhibitor reveals critical mitotic functions of human CDK1. Proc Natl Acad of Sci U S A. 103 (28), 10660-10665 (2006).
- Balakrishnan, A., Vyas, A., Deshpande, K., Vyas, D. Pharmacological cyclin dependent kinase inhibitors: Implications for colorectal cancer. World J Gastroenterol. 22 (7), 2159-2164 (2016).
- Loftus, K. M., Coutavas, E., Cui, H., King, D., Ceravolo, A., Pereiras, D., Solmaz, S. Mechanism for G2 phase-specific nuclear export of the kinetochore protein CENP-F. Cell Cycle. 16 (15), 1414-1429 (2017).
- Baffet, A. D., Hu, D. J., Vallee, R. B. Cdk1 activates pre-mitotic nuclear envelope dynein recruitment and apical nuclear migration in neural stem cells. Dev Cell. 33 (6), 703-716 (2015).
- Songyang, Z., Blechner, S., Hoagland, N., Hoekstra, M. F., Piwnica-Worms, H., Cantley, L. C. Use of an oriented peptide library to determine the optimal substrates of protein kinases. Curr Biol. 4 (11), 973-982 (1994).
- Malumbres, M. Cyclin-dependent kinases. Genome Biol. 15 (6), 122 (2014).
- Peeper, D. S., Parker, L. L., Ewen, M. E., Toebes, M., Hall, F. L., Xu, M., Zantema, A., van der Eb, A. J., Piwnica-Worms, H. A- and B-type cyclins differentially modulate substrate specificity of cyclin-cdk complexes. EMBO J. 12 (5), 1947-1954 (1993).
- Trembley, J., Ebbert, J., Kren, B., Steer, C. Differential regulation of cyclin B1 RNA and protein expression during hepatocyte growth in vivo. Cell Growth Differ. 7 (7), 903-916 (1996).
- Pines, J., Hunter, T. The differential localization of human cyclins A and B is due to a cytoplasmic retention signal in cyclin B. EMBO J. 13 (16), 3772-3781 (1994).
- Morgan, D. O. Principles of CDK regulation. Nature. 374, 131 (1995).
- Larochelle, S., Merrick, K. A., Terret, M. -. E., Wohlbold, L., Barboza, N. M., Zhang, C., Shokat, K. M., Jallepalli, P. V., Fisher, R. P. Requirements for Cdk7 in the assembly of Cdk1/cyclin B and activation of Cdk2 revealed by chemical genetics in human cells. Mol cell. 25 (6), 839-850 (2007).
- Parker, L. L., Sylvestre, P. J., Byrnes, M. J., Liu, F., Piwnica-Worms, H. Identification of a 95-kDa WEE1-like tyrosine kinase in HeLa cells. Proc Natl Acad of Sci U S A. 92 (21), 9638-9642 (1995).
- Atherton-Fessler, S., Parker, L. L., Geahlen, R. L., Piwnica-Worms, H. Mechanisms of p34cdc2 regulation. Mol Cell Biol. 13 (3), 1675-1685 (1993).
- Liu, F., Stanton, J. J., Wu, Z., Piwnica-Worms, H. The human Myt1 kinase preferentially phosphorylates Cdc2 on threonine 14 and localizes to the endoplasmic reticulum and Golgi complex. Mol Cell Biol. 17 (2), 571-583 (1997).
- McGowan, C. H., Russell, P. Human Wee1 kinase inhibits cell division by phosphorylating p34cdc2 exclusively on Tyr15. EMBO J. 12 (1), 75-85 (1993).
- Strausfeld, U., Labbé, J. C., Fesquet, D., Cavadore, J. C., Picard, A., Sadhu, K., Russell, P., Dorée, M. Dephosphorylation and activation of a p34cdc2/cyclin B complex in vitro by human CDC25 protein. Nature. 351, 242 (1991).
- Leuken, R., Clijsters, L., Wolthuis, R. To cell cycle, swing the APC/C. Biochim Biophys Acta. 1786 (1), 49-59 (2008).
- Acquaviva, C., Pines, J. The anaphase-promoting complex/cyclosome: APC/C. J Cell Sci. 119 (12), 2401-2404 (2006).
- Zhu, X., Chang, K. -. H., He, D., Mancini, M. A., Brinkley, W. R., Lee, W. -. H. The C-terminus of mitosin is essential for its nuclear localization, centromere/kinetochore targeting, and dimerization. J Biol Chem. 270 (33), 19545-19550 (1995).
- Liao, H., Winkfein, R. J., Mack, G., Rattner, J. B., Yen, T. J. CENP-F is a protein of the nuclear matrix that assembles onto kinetochores at late G2 and is rapidly degraded after mitosis. J Cell Biol. 130 (3), 507-518 (1995).
- Rattner, J. B., Rao, A., Fritzler, M. J., Valencia, D. W., Yen, T. J. CENP-F is a ca 400 kDa kinetochore protein that exhibits a cell-cycle dependent localization. Cell Motil Cytoskeleton. 26 (3), 214-226 (1993).
- Christie, M., Chang, C. -. W., Rona, G., Smith, K. M., Stewart, A. G., Takeda, A. A. S., Fontes, M. R. M., Stewart, M., Vertessy, B. G., Forwood, J. K., Kobe, B. Structural biology and regulation of protein import into the nucleus. J Mol Biol. 428 (10A), 2060-2090 (2016).
- Zuccolo, M., Alves, A., Galy, V., Bolhy, S., Formstecher, E., Racine, V., Sibarita, J. B., Fukagawa, T., Shiekhattar, R., Yen, T., Doye, V. The human Nup107/160 nuclear pore subcomplex contributes to proper kinetochore functions. EMBO J. 26, 1853-1864 (2007).
- Bolhy, S., Bouhlel, I., Dultz, E., Nayak, T., Zuccolo, M., Gatti, X., Vallee, R., Ellenberg, J., Doye, V. A Nup133-dependent NPC-anchored network tethers centrosomes to the nuclear envelope in prophase. J Cell Biol. 192 (5), 855-871 (2011).
- Hu, D. J., Baffet, A. D., Nayak, T., Akhmanova, A., Doye, V., Vallee, R. B. Dynein recruitment to nuclear pores activates apical nuclear migration and mitotic entry in brain progenitor cells. Cell. 154 (6), 1300-1313 (2013).
- Vergnolle, M. S., Taylor, S. S. Cenp-F links kinetochores to Ndel1/Nde1/Lis1/Dynein microtubule motor complexes. Curr Biol. 17 (13), 1173-1179 (2007).
- Yang, Z. Y., Guo, J., Li, N., Qian, M., Wang, S. N., Zhu, X. L. Mitosin/CENP-F is a conserved kinetochore protein subjected to cytoplasmic dynein-mediated poleward transport. Cell Res. 13 (4), 275-283 (2003).
- Yang, Z., Guo, J., Chen, Q., Ding, C., Du, J., Zhu, X. Silencing mitosin induces misaligned chromosomes, premature chromosome decondensation before anaphase onset, and mitotic cell death. Mol Cell Biol. 25 (10), 4062-4074 (2005).
- Xue, Y., Ren, J., Gao, X., Jin, C., Wen, L., Yao, X. GPS 2.0, a tool to predict kinase-specific phosphorylation sites in hierarchy. Mol Cell Proteomics. 7 (9), 1598-1608 (2008).
- Song, C., Ye, M., Liu, Z., Cheng, H., Jiang, X., Han, G., Songyang, Z., Tan, Y., Wang, H., Ren, J., Xue, Y., Zou, H. Systematic analysis of protein phosphorylation networks from phosphoproteomic data. Mol Cell Proteomics. 11 (10), 1070-1083 (2012).
- UniProt-Consortium. UniProt: the universal protein knowledgebase. Nucleic Acids Res. 45 (D1), D158-D169 (2017).
- Olsen, J. V., Vermeulen, M., Santamaria, A., Kumar, C., Miller, M. L., Jensen, L. J., Gnad, F., Cox, J., Jensen, T. S., Nigg, E. A., Brunak, S., Mann, M. Quantitative phosphoproteomics reveals widespread full phosphorylation site occupancy during mitosis. Science Signal. 3 (104), ra3 (2010).
- Dephoure, N., Zhou, C., Villén, J., Beausoleil, S. A., Bakalarski, C. E., Elledge, S. J., Gygi, S. P. A quantitative atlas of mitotic phosphorylation. Proc Natl Acad of Sci U S A. 105 (31), 10762-10767 (2008).
- Rona, G., Marfori, M., Borsos, M., Scheer, I., Takacs, E., Toth, J., Babos, F., Magyar, A., Erdei, A., Bozoky, Z., Buday, L., Kobe, B., Vertessy, B. G. Phosphorylation adjacent to the nuclear localization signal of human dUTPase abolishes nuclear import: structural and mechanistic insights. Acta Cryst D. 69 (12), 2495-2505 (2013).
- Harreman, M. T., Kline, T. M., Milford, H. G., Harben, M. B., Hodel, A. E., Corbett, A. H. Regulation of nuclear import by phosphorylation adjacent to nuclear localization signals. J Biol Chem. 279 (20), 20613-20621 (2004).
- Kosugi, S., Hasebe, M., Tomita, M., Yanagawa, H. Systematic identification of cell cycle-dependent yeast nucleocytoplasmic shuttling proteins by prediction of composite motifs. Proc Natl Acad Sci U S A. 106 (25), 10171-10176 (2009).
- McLachlin, D. T., Chait, B. T. Analysis of phosphorylated proteins and peptides by mass spectrometry. Curr Opin Chem Biol. 5 (5), 591-602 (2001).
- Van Berkel, G. J., Glish, G. L., McLuckey, S. A. Electrospray ionization combined with ion trap mass spectrometry. Anal Chem. 62 (13), 1284-1295 (1990).
- Hodel, A. E., Harreman, M. T., Pulliam, K. F., Harben, M. E., Holmes, J. S., Hodel, M. R., Berland, K. M., Corbett, A. H. Nuclear localization signal receptor affinity correlates with in vivo localization in Saccharomyces cerevisiae. J Biol Chem. 281 (33), 23545-23556 (2006).
- Hong, K. U., Kim, H. -. J., Kim, H. -. S., Seong, Y. -. S., Hong, K. -. M., Bae, C. -. D., Park, J. Cdk1-Cyclin B1-mediated Phosphorylation of Tumor-associated Microtubule-associated Protein/Cytoskeleton-associated Protein 2 in Mitosis. J Biol Chem. 284 (24), 16501-16512 (2009).
- Meraldi, P., Lukas, J., Fry, A. M., Bartek, J., Nigg, E. A. Centrosome duplication in mammalian somatic cells requires E2F and Cdk2–Cyclin A. Nature Cell Biol. 1, 88 (1999).
- Heuvel, S., Harlow, E. Distinct roles for cyclin-dependent kinases in cell cycle control. Science. 262 (5142), 2050-2054 (1993).
- Kinoshita, E., Kinoshita-Kikuta, E., Takiyama, K., Koike, T. Phosphate-binding Tag, a New Tool to Visualize Phosphorylated Proteins. Mol Cell Proteomics. 5 (4), 749-757 (2006).
- Takeda, H., Kawasaki, A., Takahashi, M., Yamada, A., Koike, T. Matrix-assisted laser desorption/ionization time-of-flight mass spectrometry of phosphorylated compounds using a novel phosphate capture molecule. Rapid Commun Mass Spectrom. 17 (18), 2075-2081 (2003).
- Linder, M. I., Köhler, M., Boersema, P., Weberruss, M., Wandke, C., Marino, J., Ashiono, C., Picotti, P., Antonin, W., Kutay, U. Mitotic Disassembly of Nuclear Pore Complexes Involves CDK1- and PLK1-Mediated Phosphorylation of Key Interconnecting Nucleoporins. Dev Cell. 43 (2), (2017).
- Arai, T., Haze, K., Iimura-Morita, Y., Machida, T., Iida, M., Tanaka, K., Komatani, H. Identification of β-catenin as a novel substrate of polo-like kinase 1. Cell Cycle. 7 (22), 3556-3563 (2008).
- Hansen, D. V., Tung, J. J., Jackson, P. K. CaMKII and Polo-like kinase 1 sequentially phosphorylate the cytostatic factor Emi2/XErp1 to trigger its destruction and meiotic exit. Proc Natl Acad of Sci U S A. 103 (3), 608-613 (2006).
- Zhang, Y., Dong, Z., Nomura, M., Zhong, S., Chen, N., Bode, A. M., Dong, Z. Signal Transduction Pathways Involved in Phosphorylation and Activation of p70S6K Following Exposure to UVA Irradiation. J Biol Chem. 276 (24), 20913-20923 (2001).
- Richard, D. E., Berra, E., Gothié, E., Roux, D., Pouysségur, J. p42/p44 Mitogen-activated Protein Kinases Phosphorylate Hypoxia-inducible Factor 1α (HIF-1α) and Enhance the Transcriptional Activity of HIF-1. J Biol Chem. 274 (46), 32631-32637 (1999).
Réimpressions et Autorisations
Demande d’autorisation pour utiliser le texte ou les figures de cet article JoVE
Demande d’autorisationThis article has been published
Video Coming Soon