Un abonnement à JoVE est nécessaire pour voir ce contenu. Connectez-vous ou commencez votre essai gratuit.
Method Article
Monitoring Pedogenic Inorganic Carbon Accumulation Due to Weathering of Amended Silicate Minerals in Agricultural Soils.
* Ces auteurs ont contribué à parts égales
Dans cet article
Résumé
La méthode de vérification décrite ici est adaptable pour surveiller la séquestration du carbone inorganique pédogène dans divers sols agricoles amendés avec des roches contenant du silicate métallique alcalino-terreux, telles que la wollastonite, le basalte et l’olivine. Ce type de validation est essentiel pour les programmes de crédits de carbone, qui peuvent bénéficier aux agriculteurs qui séquestrent le carbone dans leurs champs.
Résumé
La présente étude vise à démontrer une procédure systématique de surveillance du carbone inorganique induit par l’altération accrue des roches comminutées dans les sols agricoles. À cette fin, les échantillons de sol de carotte prélevés à différentes profondeurs (y compris des profils de 0 à 15 cm, 15 à 30 cm et de 30 à 60 cm) sont prélevés dans un champ agricole dont la couche arable a déjà été enrichie d’un silicate métallique alcalino-terreux contenant un minéral (comme la wollastonite). Après le transport au laboratoire, les échantillons de sol sont séchés à l’air et tamisés. Ensuite, la teneur en carbone inorganique des échantillons est déterminée par une méthode volumétrique appelée calcimétrie. Les résultats représentatifs présentés ici ont montré cinq incréments de carbone inorganique dans les sols amendés avec le ca-silicate par rapport aux sols témoins. Ce changement de composition s’est accompagné de plus de 1 unité d’augmentation du pH dans les sols amendés, ce qui implique une dissolution élevée du silicate. Les analyses minéralogiques et morphologiques, ainsi que la composition élémentaire, corroborent davantage l’augmentation de la teneur en carbone inorganique des sols amendés par silicate. Les méthodes d’échantillonnage et d’analyse présentées dans cette étude peuvent être adoptées par les chercheurs et les professionnels qui cherchent à retracer les changements de carbone inorganique pédogène dans les sols et les sous-sols, y compris ceux modifiés avec d’autres roches silicatées appropriées telles que le basalte et l’olivine. Ces méthodes peuvent également être exploitées comme outils de vérification de la séquestration du carbone inorganique dans le sol par des entités privées et gouvernementales afin de certifier et d’attribuer des crédits de carbone.
Introduction
Le CO2 est un gaz à effet de serre (GES) majeur et sa concentration dans l’atmosphère ne cesse d’augmenter. La moyenne mondiale préindustrielle du CO2 était d’environ 315 parties par million (ppm), et en avril 2020, la concentration atmosphérique de CO2 a augmenté à plus de 416 ppm, provoquant ainsi un réchauffement climatique1. Par conséquent, il est essentiel de réduire la concentration de ce GES qui emprisonne la chaleur dans l’atmosphère. Socolow2 a suggéré que pour stabiliser la concentration de CO2 atmosphérique à 500 ppm d’ici 2070, neuf « coins de stabilisation » seront nécessaires, où chaque coin de stabilisation est une approche d’atténuation individuelle, dimensionnée pour atteindre 3,67 Gt d’équivalent CO2 par an en réduction des émissions.
Le captage et le stockage du carbone (CSC) est la principale technologie permettant de réduire le CO2 de l’atmosphère, comme le recommande l’initiative Mission Innovation, lancée lors de la Conférence des Nations Unies sur les changements climatiques 20153. Pour capter le CO2atmosphérique, les trois principales options de stockage disponibles sont le stockage en mer, le stockage géologique et la carbonatation minérale4. En se concentrant sur la carbonatation minérale, le CO2 est stocké en convertissant les métaux alcalino-terreux, principalement les silicates riches en calcium et en magnésium, en carbonates thermodynamiquement stables pour des périodes géologiques (sur des millions d’années)5. Par exemple, les minéraux de l’olivine, du pyroxène et du groupe serpentin ont le potentiel de subir une carbonatation minérale6; cependant, dans des conditions normales, ces réactions sont limitées par la cinétique de réaction lente. Par conséquent, pour accélérer le procédé dans des conditions ambiantes, des formes finement broyées (broyées/broyées) de ces silicates peuvent être appliquées sur les sols agricoles, procédé appelé altération terrestre améliorée7. Le sol est un puits naturel pour stocker le CO2,étant actuellement un réservoir pour 2500 Gt de carbone, ce qui est trois fois le réservoir atmosphérique (800 Gt de carbone)8. Les processus pédogènes dans les sols et les sous-sols régulent le CO2 atmosphérique par deux voies naturelles majeures, à savoir le cycle de la matière organique et l’altération des minéraux métalliques alcalino-terreux, affectant respectivement les réservoirs de carbone organique et inorganique9.
On estime que près de 1,1 Gt de CO2 atmosphérique est minéralisé par altération chimique des roches chaque année10. Les roches silicatées riches en calcium et en magnésium (p. ex. basalte) sont considérées comme les principales matières premières pour l’altération améliorée9,11,12. Une fois que les minéraux broyés contenant du silicate sont appliqués sur les champs agricoles, ils commencent à réagir avec leCO2 dissous dans l’eau intersyaire du sol, se terminant par la précipitation minérale de carbonates stables11,13. L’olivine14,15,la wollastonite (CaSiO3)13,la dolérite et le basalte16 font partie des minéraux qui ont démontré un potentiel de séquestration du carbone grâce à une altération accrue dans des études antérieures. Malgré la plus grande disponibilité, et donc peut-être une plus grande capacité de séquestration du CO2, des silicates de magnésium, on s’inquiète de leur application pour une altération accrue dans les terres cultivées en raison de leur impact environnemental potentiel résultant de la lixiviation du Cr et du Ni et de la présence possible de particules asbestiformes11,15,17,18. En tant que silicate calcique, la wollastonite est ici mise en évidence comme un candidat de choix pour ce processus en raison de sa grande réactivité, de sa structure chimique simple, étant respectueuse de l’environnement ainsi que facilitant la production de carbonates en raison de la liaison plus faible des ions Ca à sa matrice de silice12,19,20,21. La wollastonite qui est extraite à Kingston, en Ontario, au Canada, et qui est actuellement commercialisée par la wollastonite canadienne pour des applications agricoles, ne contient pas de concentrations élevées de métaux dangereux. Les réserves mondiales de wollastonite sont estimées à plus de 100 Mt, la Chine, l’Inde, les États-Unis, le Mexique, le Canada et la Finlande étant les pays les plus productifs22.
L’altération accrue des minéraux silicatés est censée favoriser la santé des sols, notamment l’augmentation du rendement des cultures et l’amélioration de la croissance des plantes, conduisant à la réduction potentielle de l’application d’engrais synthétiques, ce qui peut contribuer davantage à la réduction des émissions de GES11,18,19. Des études antérieures ont rapporté que l’application de minéraux silicatés riches en Ca sur les sols fournit une basicité pour neutraliser l’acidité dans le milieu du sol, favorisant la production végétale23,24,25. Cela entrave également la mobilisation des métaux toxiques, sensibles aux conditions acides, et une altération accrue pourrait être utile pour retarder l’érosion par l’incrément de matière organique du sol11.
Les équations 1 à 3 montrent comment la séquestration du carbone pédogène sous forme de carbonates inorganiques est possible en amendant les sols avec de la wollastonite. Le CO2 ambiant pénètre dans le sol par l’eau de pluie ou est produit dans le sol par l’activité microbienne dégradant les composés organiques. Une fois en contact avec l’eau intersyrique du sol, de l’acide carbonique se forme, qui se dissocie pour former du bicarbonate et du proton (équation 1). En présence de plantes, des exsudats racinaires, tels que l’acide citrique et l’acide maléique, sont libérés, qui fournissent également des protons dans le système. Ces protons facilitent la dissolution de la wollastonite dans le sol en libérant des ions Ca et en laissant derrière eux de la silice amorphe (équation 2). Les ions Ca libérés réagissent finalement avec le bicarbonate pour précipiter sous forme de carbonates (calcite cristalline ou autres variétés, selon les conditions géochimiques) (équation 3). Ce carbonate de calcium formé fait partie de la fraction de carbone inorganique (SIC) du sol26.
Solvaation ambiante de CO2:
2CO2(g) + 2H2O(l) ↔ 2H2CO3(aq) ↔2HCO3- + 2H+ (1)
Dissolution de la wollastonite (H+ de la dissociation de l’acide carbonique et des exsudats racinaires):
CaSiO3(s) + 2 H+ → Ca2+ +H2O(l) + SiO2(s) (2)
Précipitation de carbonates inorganiques pédogènes :
Ca2+ + 2HCO3- → CaCO3(s)↓ +H2O(l) + CO2(g) (3)
Dans nos travaux récents, l’amélioration des intempéries par l’application de la wollastonite sur les sols agricoles, en tant qu’amendement de remplacement du calcaire, s’est avérée efficace pour les précipitations de CaCO3 dans la couche arable, à l’échelle des laboratoires et des champs, et sur des termes courts (quelques mois) et longs (3 ans). Dans les études sur le terrain, des évaluations chimiques et minéralogiques ont révélé que la teneur en CSIC augmente proportionnellement à la dose d’application de wollastonite (tonne·hectare-1)13. Dans les études de laboratoire, l’analyse minéralogique a montré la présence de carbonate pédogène dû à la séquestration du carbone19. La formation de carbonates pédogènes dans le sol dépend de plusieurs facteurs, notamment: la topographie, le climat, la végétation de surface, les processus biotiques du sol et les propriétés physicochimiques du sol27. Notre étude précédente23 a déterminé le rôle des plantes (une plante légumineuse (haricot vert) et une plante non légumineuse (maïs)) sur l’altération de la wollastonite et la formation de carbonates inorganiques dans le sol. Nos recherches en cours sur la formation et la migration pédogènes du carbone dans les sols et les sous-sols comprennent l’étude du devenir des carbonates de sol dans les sols agricoles, d’abord formés dans les couches arables en raison de l’altération minérale à diverses profondeurs et au fil du temps. Selon Zamanian et al.27, l’horizon des carbonates pédogènes naturels se trouve plus loin de la surface à mesure que le taux de précipitations locales augmente, le sommet de cet horizon apparaissant généralement entre quelques centimètres et 300 cm sous la surface. D’autres paramètres ambiants et pédologiques, tels que l’équilibre de l’eau du sol, la dynamique saisonnière, la teneur initiale en carbonates dans le matériau parent, les propriétés physiques du sol, ont également une incidence sur la profondeur de cette occurrence27. Il est donc important d’échantillonner les sols à une profondeur suffisante à toutes les occasions d’obtenir une compréhension précise des niveaux originaux et différentiels de CTI résultant de l’altération accrue des silicates.
À l’échelle du champ, une limite importante est l’utilisation de faibles taux d’application d’amendements au sol de silicate. Comme les connaissances sur l’effet de nombreux silicates (comme la wollastonite et l’olivine) sur la santé du sol et des végétaux sont limitées, les producteurs commerciaux évitent d’appliquer des doses d’application plus élevées qui pourraient entraîner une séquestration importante du carbone. En raison de ces faibles taux d’application, ainsi que de la grande superficie des champs de culture, un défi de recherche auquel il est généralement confronté consiste à déterminer les changements dans la CSIC lorsque les valeurs sont relativement faibles, et à récupérer et isoler les grains de silicate et les produits d’altération du sol pour étudier les changements morphologiques et minéralogiques. Dans nos travaux antérieurs, nous avons fait état de la façon dont le fractionnement physique du sol amendé par la wollastonite (à l’aide du tamisage) a permis de mieux comprendre le processus d’altération, en particulier la formation et l’accumulation de carbonates pédogènes28. En conséquence, les teneurs plus élevées en wollastonite et en produits d’altération ont été détectées dans la fraction la plus fine du sol, ce qui a fourni des valeurs raisonnablement élevées lors des analyses, garantissant des résultats plus précis et plus fiables. Les résultats soulignent l’importance d’utiliser le fractionnement physique, par tamisage ou d’autres moyens de ségrégation, pour une estimation fiable de l’accumulation de carbone séquestré dans les sols amendés au silicate. Cependant, le degré de fractionnement peut varier d’un sol à l’autre et d’un silicate à l’autre, il convient donc de le rechercher davantage.
La mesure précise de la CSIC est essentielle à l’établissement d’une norme et d’une procédure scientifique qui peuvent être adoptées par divers chercheurs intéressés à analyser l’évolution de la CSIC et (et du carbone organique) au fil du temps et de la profondeur du sol. Une telle méthodologie permet aux agriculteurs de demander un crédit de carbone à la suite de la formation de SIC dans leurs sols de champ. Le protocole suivant décrit en détail : (1) une méthode d’échantillonnage du sol à utiliser à la suite de l’amendement du silicate du sol, qui tient compte de la signification statistique des données sur le sol analysées; (2) une méthode de fractionnement du sol qui améliore l’exactitude de la quantification des changements dans le pool de carbonates inorganiques pédogènes résultant de l’altération accrue du silicate, et (3) les étapes de calcul utilisées pour déterminer le taux de séquestration SIC à la suite de l’amendement du silicate du sol. Aux fins de cette démonstration, on présume que la wollastonite, provenant de la wollastonite canadienne, est le minéral silicaté épandu sur les sols agricoles, et les sols agricoles sont considérés comme semblables à ceux que l’on trouve dans les terres agricoles du Sud de l’Ontario.
La procédure consistant à modifier le sol agricole avec de la wollastonite (par exemple, déterminer la quantité de wollastonite à appliquer par hectare et la méthode pour l’épandre sur le sol) a été décrite dans notre étude précédente13. La zone d’étude dans nos travaux antérieurs et actuels est des parcelles rectangulaires; par conséquent, la méthode d’échantillonnage aléatoire direct est appropriée pour de telles études. Il s’agit d’une méthode couramment utilisée en raison de son faible coût, de son temps réduit et de sa capacité à fournir une incertitude statistique adéquate. De même, selon les diverses conditions sur le terrain et le niveau de signification statistique souhaité, des méthodes d’échantillonnage zonal ou par grille peuvent également être utilisées. L’exactitude de l’échantillonnage du sol est essentielle pour réduire l’incertitude statistique résultant du biais d’échantillonnage. Lorsque des statistiques sont utilisées, l’atteinte d’un niveau de confiance inférieur à 95 % (c.-à-d. p < 0,05) n’est pas considérée comme « statistiquement significative ». Toutefois, pour certaines études de sol, le niveau de confiance peut être assoupli à 90 % (c.-à-d. p < 0,10) en raison du nombre de paramètres non contrôlés (c.-à-d. variant naturellement) dans les conditions de terrain qui influent sur la précision générale des mesures. Dans ce protocole, deux ensembles d’échantillons sont prélevés afin d’étudier la teneur en CTI et d’autres propriétés chimiques, minérales et morphologiques du sol dans l’ensemble de son profil vertical.
Access restricted. Please log in or start a trial to view this content.
Protocole
1. Méthode d’échantillonnage du sol et collecte des carottes
- Divisez la zone d’intérêt des terres agricoles cartographiées et délimitées en différentes parcelles en fonction de l’altitude des terres, du rendement historique des cultures et/ou de la stratégie de gestion des terres. Déterminer le nivellement de chaque placette à l’aide d’un récepteur GPS, classer le rendement des cultures en fonction des enregistrements agricoles historiques (inférieur à la moyenne, moyen, supérieur à la moyenne) et de la stratégie de gestion des terres utilisée pour chaque parcelle (types d’amendements du sol utilisés, le cas échéant). Placez les drapeaux aux limites de chaque placette pour faciliter l’échantillonnage ultérieur.
NOTA: La figure 1 montre le coupement de la zone rectangulaire à l’étude en quatre placettes (A, B, C, D). Un tel plan expérimental et des informations seront utiles pour vérifier la signification statistique des données analysées. De plus, il peut être approprié pour les terres agricoles irrégulières et être pratique pour aligner l’échantillonnage en fonction d’un paramètre jugé nécessaire, de l’orientation des rangées de cultures à la direction du terrain, du ruissellement, du vent dominant, de la trajectoire du soleil, etc. Ces quatre intrigues ont été envisagées afin de faciliter une campagne de tournage sur le terrain. - Utiliser la méthode d’échantillonnage aléatoire dirigé pour recueillir les carottes dans chaque placette. Subdiviser chaque placette selon un quadrillage en 25 sous-placettes(figure 2). La collecte de 25 cœurs est supérieure au nombre minimum de cœurs traditionnellement recommandé (15-20).
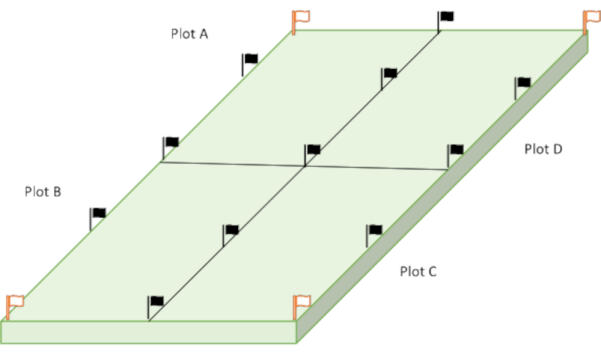
Figure 1: Représentation des placettes utilisées pour le prélèvement d’échantillons (chaque placette représente une superficie de 5 m × 10 m (au total quatre x 50 m2). Les drapeaux noirs délimitent chaque limite de parcelle pour faciliter l’échantillonnage, et les drapeaux blancs marquent les emplacements pour l’échantillonnage en profondeur. Veuillez cliquer ici pour voir une version plus grande de cette figure.

Figure 2: Sous-sectionnement de chaque placette pour le prélèvement d’échantillons de carottes (chaque sous-section représente une superficie de 1 m x 2 m), selon la méthode d’échantillonnage aléatoire dirigé. Veuillez cliquer ici pour voir une version plus grande de cette figure.
- Prélever des échantillons de carottes à partir de points aléatoires dans chaque sous-diagramme, un par sous-diagramme. Utilisez une sonde de sol ou un échantillonneur de carotte de sol pour recueillir la carotte de sol jusqu’à trois zones de profondeur de 0 à 15 cm, 15 à 30 cm et 30 à 60 cm afin de tenir compte de la variation de la CSS avec la profondeur due à l’amendement du sol par le silicate.
NOTA : Selon le type de sol et la sonde ou l’échantillonneur utilisé, un échantillonneur différent peut être nécessaire pour prélever l’échantillon de 30 à 60 cm. - Utilisez une tarière extensible (ou un échantillonneur de capacité similaire) pour prélever des échantillons de sol profond aux emplacements des drapeaux blancs de la figure 1,jusqu’à trois zones de profondeur supplémentaires de 60 à 100 cm, 100 à 175 cm et 175 à 250 cm. Ces échantillons tiennent compte de la variation de la caractérisation du sol à l’intérieur de ces profondeurs et évaluent le niveau de fond de la CSIC dans la zone terrestre étudiée, jusqu’à la profondeur supérieure de l’horizon de carbonates pédogènes naturels.
NOTA : D’après les propriétés locales du site (p. ex. profondeur de la nappe phréatique), la zone la plus profonde peut être modifiée à différents endroits. - Transporter les échantillons de sol dans des seaux, un pour chaque profondeur échantillonnée sur chaque placette. Mélangez soigneusement les sols dans chaque seau. Placez le testeur d’humidité portatif dans l’échantillon de sol mélangé. Attendez que la teneur en humidité se fixe à un point stable de la jauge de l’appareil. Appuyez sur le bouton du support et enregistrez la valeur en tant que teneur en humidité en temps réel des sols mélangés.
- Conservez les échantillons composites dans des sacs scellés. Étiquetez correctement les sacs avec des informations sur les parcelles (A, B, C ou D), la profondeur du sol (0-15 cm, 15-30 cm, 30-60 cm, 60-100 cm, 100-175cm, 175-250 cm) et la date d’échantillonnage.
2. Fractionnement du sol avant l’analyse chimique
- Sécher à l’air les échantillons de sol dès que possible après l’échantillonnage afin de minimiser l’oxydation du carbone du sol. Pour cela, placez les échantillons de sol dans des boîtes en carton (2,5 « x 3 » x 3 ») et placez les boîtes dans une armoire de séchage à 50 °C pendant 24-48 h, jusqu’à ce que le sol soit sec. Entreposer les échantillons séchés à l’air dans des sacs d’échantillons jusqu’à une analyse plus approfondie.
- Avant le fractionnement du sol, faire passer les échantillons de sol à travers un tamis de 2 mm pour éliminer les gros fragments de roches et les restes de plantes.
- Sécher au four les sols tamisés en plaçant les échantillons dans un four à moufle maintenu à 105 ± 2 °C pendant au moins 15 h.
- Pour le fractionnement du sol, placer 1 kg de l’échantillon séché au four sur la maille supérieure du tamis shaker composée de différents maillages (710 à 50 μm). Agiter les tamis à 60 tr/min pendant 15 min. Des fractions pan <50 μm sont de préférence utilisées pour les analyses, car il s’agit de la fraction pédogène du sol enrichie en carbonates.
NOTA : D’autres fractions du sol peuvent également être testées pour fournir des données supplémentaires pour la vérification de l’accumulation de CSIC en raison de l’altération accrue des silicates amendés.
3. Détermination de la séquestration du carbone inorganique pédogène
- Pour déterminer la teneur en carbone inorganique des échantillons de sol à l’aide d’une analyse calcimétrique, placer 5 g d’un échantillon de sol tamisé dans une fiole Erlenmeyer appropriée. Suspendre l’échantillon dans 20 mL d’eau ultrapure. Ajouter 7 mL de HCl 4 M à un petit tube à essai en verre à fond plat, puis placer ce tube debout à l’intérieur du ballon à l’aide d’une pince à épiler.
- Fixer soigneusement le ballon au calcimètre en apposant le bouchon en caoutchouc. Les niveaux d’eau de burette sur le calcimètre auraient dû être préalablement ajustés au besoin, et les blancs et les étalons CaCO3 auraient dû être exécutés une fois sur le calcimètre au besoin.
- Agiter le ballon, renversant ainsi le tube acide, jusqu’à ce que le niveau d’eau dans la burette atteigne une valeur constante et qu’aucun bouillonnement ne soit observé dans la solution (cela prend environ 5 min).
- Calculer la teneur en caCO3équivalente (CaCO3(eqv))de l’échantillon (g,CaCO3(eqv)·( kg,sol)-1) sur la base du changement de volume observé dans la burette, et des valeurs d’étalonnage à blanc et CaCO3, en utilisant la formule de calcimétrie appropriée. La teneur en SIC est obtenue en convertissant le g,CaCO3(eqv)· (kg,sol) -1 valeur enkg,CO2· (tonne,sol) -1 ou kg,C· (tonne,sol) -1.
- Calculer la teneur en CaCO3(eqv) de l’échantillon à l’aide de la formule ci-dessous :
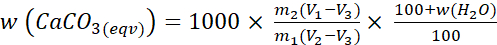 (4)
(4)
où:
w (CaCO3(eqv)) = teneur en carbonates du sol séché au four
m1 = masse de la portion d’essai
m2 = masse moyenne des étalons de carbonate de calcium
V1 = le volume de dioxyde de carbone produit par la réaction de la phase d’essai
V2 = le volume moyen de dioxyde de carbone produit par les étalons de carbonate de calcium
V3 = variation de volume dans les déterminations à blanc
w(H2O) = la teneur en eau de l’échantillon séché
REMARQUE: les étapes 3.1 à 3.4 sont effectuées sur la base d’un protocole standard29.
- Calculer la teneur en CaCO3(eqv) de l’échantillon à l’aide de la formule ci-dessous :
- Pour mesurer la densité apparente (BD) du sol ((tonne,sol)·m−3),placer une partie aliquote suffisamment importante de l’échantillon de sol séché au four dans un récipient dont le volume est connu. Peser l’échantillon à l’aide d’une balance. Le rapport entre le poids séché et le volume de l’échantillon est considéré comme BD.
NOTA: Les autres dispositifs de calcul de la « masse volumique apparente non perturbée » sont présentés dans la discussion. - Calculer le SIC sur lesont (kg,CO2 ·( hectare)−1) en utilisant la formule suivante:
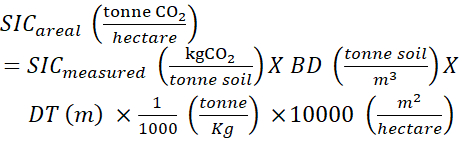 (5)
(5)
où:
A = la surface
DT = épaisseur de profondeur - Calculer le CSIC total (CSD 0-60 cm, kg,CO2·( hectare)−1) pour chaque placette, en utilisant les valeurs SIC suralaires obtenues pour chaque profondeur, comme suit:
SIC Plot A = SIC0-60 cm = SIC0-15 cm + SIC15-30 cm + SIC30-60 cm (6) - Ajouter le SIC total sural (CS 0-60 cm,kg,CO2·( hectare)−1) pour chaque placette (A, B, C, D) étudiée et obtenir la moyenne comme suit:
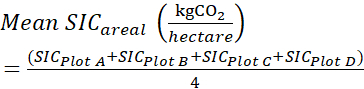 (7)
(7) - Diviser la SIC moyenne suramétale (kg,CO2 ·( hectare)−1) obtenu à partir de Eq. 7 par la vitesse d’application de silicate minéral/roche utilisé pour l’amendement du sol ((tonne, silicate)·( hectare)−1).
NOTA: Cela fournira la quantité de carbone inorganique pédogène séquestré en termes de kg de CO2 par tonne de silicate appliquée (kg, CO2·( tonne, silicate)−1). Si une enquête pluriannuelle est effectuée ou si une placette témoin sans modification du silicate est présente, cette étape doit être modifiée pour tenir compte de la séquestration totale et de l’amendement total sur une valeur à plus long terme, ou d’une année à l’autre, ou de la séquestration nette du carbone pédogène.
Access restricted. Please log in or start a trial to view this content.
Résultats
La teneur en CSIC des sols peut être déterminée à l’aide de diverses méthodes, y compris un analyseur de carbone automatisé ou un calcimètre. L’analyseur automatisé de carbone pour la détermination du carbone total du sol mesure la pression de CO2 accumulée dans un récipient fermé30. En calcimétrie, le volume évolué de CO2 libéré après acidification, généralement par l’ajout d’acide HCl concentré, de l’échantill...
Access restricted. Please log in or start a trial to view this content.
Discussion
Étant donné qu’il est habituellement difficile de prélever des échantillons dans des champs agricoles fertilisés, il est suggéré de prélever des échantillons avant l’épatée d’éléments nutritifs. Il est également conseillé d’éviter de prélever des échantillons dans des champs gelés. La profondeur d’échantillonnage peut varier selon les zones en fonction de la facilité d’échantillonnage sur le profil vertical et de la profondeur de la nappe phréatique. Le dispositif d’échantillonnage d...
Access restricted. Please log in or start a trial to view this content.
Déclarations de divulgation
Les auteurs n’ont pas de conflit d’intérêts.
Remerciements
Ce travail a été appuyé par une subvention de commercialisation des aliments de la pensée, qui est financée par le Fonds d’excellence en recherche Apogée Canada. La wollastonite canadienne a fourni un soutien financier industriel dans le cadre de cette subvention.
Access restricted. Please log in or start a trial to view this content.
matériels
| Name | Company | Catalog Number | Comments |
| Analytical scale | Sartorius | Quintix 224-S1 | Four decimals. |
| Calcimeter | Eijkelkamp | Model 08.53 | To determine the wt% CaCO3-equivalent in the sample. |
| Drying cabinet/muffle furnace | Thermo Scientific | F48055-60 | 50°C or 103 ± 2°C. |
| HCl | Fisher Scientific | A144S-500 | Reagent grade (36.5%-38.0%). |
| HNO3 | Fisher Scientific | T003090500 | Trace metal analysis grade (69.0%-70.0%) |
| Inductively Coupled Plasma Mass Spectrometer (ICP-MS) | PerkinElmer | NexION | To determine the concentration of Ca in the microwave-digested soil. |
| Microwave digester | PerkinElmer | Titan | To digest soils in concentrated HNO3. |
| pH meter | Oakton | 700 | Calibrated with standard solutions before each set of measurements; temperature corrected to 25 °C. |
| Scanning Electron Microscope -Energy Dispersive Spectroscope (SEM-EDS) | Oxford | X-Max20 SSD | To determine the morphology of soil particulates. |
| Sieve shaker | Retsch | AS-200 | For soil fractionation. |
| Soil auger sampler | Eijkelkamp | 01-16 | Depths down to 700 cm. |
| Soil Dakota probe sampler | JMC | PN139 | Depths down to 100 cm. |
| Soil probe sampler | JMC | PN031 | Depths down to 30 cm. |
| Soil moisture meter | Extech | MO750 | Measure moisture content up to 50% |
| Wavelength Dispersive X-ray Fluorescence spectroscope (WDXRF) | Malvern Panalytical | Zetium | To characterize elemental composition of soil. |
| X-ray Diffraction analyzer (XRD) | Panalytical | Empyrean | To characterize mineralogicalbproperties of soil. |
Références
- NOAA. Trends in atmospheric carbon dioxide. NOAA. , Available from: https://www.esrl.noaa.gov/gmd/ccgg/trends/ (2020).
- Socolow, R. Wedges reaffirmed. Bulletin of the Atomic Scientists. 2011 (9), (2011).
- Mission Innovation. Joint launch statement. Mission Innovation. , Mission Innovation Countries. Paris. (2015).
- Lackner, K. S., Brennan, S. Envisioning carbon capture and storage: Expanded possibilities due to air capture, leakage insurance, and C-14 monitoring. Climatic Change. 96 (3), 357-378 (2009).
- Lackner, K. S. A guide to CO2 sequestration. Science. 300 (5626), 1677-1678 (2003).
- Kwon, S., Fan, M., DaCosta, H. F. M., Russell, A. G. Factors affecting the direct mineralization of CO2 with olivine. Journal of Environmental Sciences. 23 (8), 1233-1239 (2011).
- Hartmann, J., et al. Enhanced chemical weathering as a geoengineering strategy to reduce atmospheric carbon dioxide, supply nutrients, and mitigate ocean acidification. Reviews of Geophysics. 51 (2), 113-149 (2013).
- Batjes, N. H. Total carbon and nitrogen in the soils of the world. European Journal of Soil Science. 47 (2), 151-163 (1996).
- Haque, F., Chiang, Y. W., Santos, R. M. Alkaline mineral soil amendment: A climate change stabilization wedge. Energies. 12 (12), 2299(2019).
- Strefler, J., Amann, T., Bauer, N., Kriegler, E., Hartmann, J. Potential and costs of carbon dioxide removal by enhanced weathering of rocks. Environmental Research Letters. 13 (3), 34010(2018).
- Beerling, D. J., et al. Farming with crops and rocks to address global climate, food and soil security. Nature Plants. 4 (3), 138-147 (2018).
- Lefebvre, D., et al. Assessing the potential of soil carbonation and enhanced weathering through Life Cycle Assessment: A case study for Sao Paulo State, Brazil. Journal of Cleaner Production. 233, 468-481 (2019).
- Haque, F., Santos, R. M., Chiang, Y. W. CO2 sequestration by wollastonite-amended agricultural soils-An Ontario field study. International Journal of Greenhouse Gas Control. 97, 103017(2020).
- Ten Berge, H. F. M., et al. Olivine weathering in soil, and its effects on growth and nutrient uptake in ryegrass (Lolium perenne L.): a pot experiment. PloS One. 7 (8), 42098(2012).
- Amann, T., et al. Enhanced weathering and related element fluxes-A cropland mesocosm approach. Biogeosciences. 17 (1), 103-119 (2020).
- Manning, D. A. C., Renforth, P., Lopez-Capel, E., Robertson, S., Ghazireh, N. Carbonate precipitation in artificial soils produced from basaltic quarry fines and composts: An opportunity for passive carbon sequestration. International Journal of Greenhouse Gas Control. 17, 309-317 (2013).
- Frazell, J., Elkins, R., O'Geen, A. T., Reynolds, R., Meyers, J. Facts about serpentine rock and soil containing asbestos in California. ANR Publication: University of California. , 8399(2009).
- Kelland, M. E., et al. Increased yield and CO2 sequestration potential with the C4 cereal Sorghum bicolor cultivated in basaltic rock dust-amended agricultural soil. Global Change Biology. 26 (6), 3658-3676 (2020).
- Haque, F., Santos, R. M., Chiang, Y. W. Optimizing inorganic carbon sequestration and crop yield with wollastonite soil amendment in a microplot study. Frontiers in Plant Science. 11, 1012(2020).
- Palandri, J. L., Kharaka, Y. K. A compilation of rate parameters of water-mineral interaction kinetics for application to geochemical modeling. National Energy Technology Laboratory-United States Department of Energy. , Menlo Park, California. USGS Open File report 2004-1068 (2004).
- Schott, J., et al. Formation, growth and transformation of leached layers during silicate minerals dissolution: The example of wollastonite. Geochimica et Cosmochimica Acta. 98, 259-281 (2012).
- Brioche, A. S. Mineral commodity summaries-Wollastonite. US Geological Survey. , (2018).
- Haque, F., Santos, R. M., Dutta, A., Thimmanagari, M., Chiang, Y. W. Co-benefits of wollastonite weathering in agriculture: CO2 sequestration and promoted plant growth. ACS Omega. 4 (1), 1425-1433 (2019).
- Li, Y., Both, A. -J., Wyenandt, C. A., Durner, E. F., Heckman, J. R. Applying Wollastonite to Soil to Adjust pH and Suppress Powdery Mildew on Pumpkin. HortTechnology. 29 (6), 811-820 (2019).
- Mao, P., et al. Phosphate addition diminishes the efficacy of wollastonite in decreasing Cd uptake by rice (Oryza sativa L.) in paddy soil. Science of the Total Environment. 687, 441-450 (2019).
- Hangx, S. J. T., Spiers, C. J. Coastal spreading of olivine to control atmospheric CO2 concentrations: A critical analysis of viability. International Journal of Greenhouse Gas Control. 3 (6), 757-767 (2009).
- Zamanian, K., Pustovoytov, K., Kuzyakov, Y. Pedogenic carbonates: Forms and formation processes. Earth-Science Reviews. 157, 1-17 (2016).
- Dudhaiya, A., Haque, F., Fantucci, H., Santos, R. M. Characterization of physically fractionated wollastonite-amended agricultural soils. Minerals. 9 (10), 635(2019).
- Calcimeter manual. Eijlelkamp Soil & Water. , Available from: https://www.eijkelkamp.com/download.php?file=M0853e_Calcimeter_b21b.pdf (2020).
- ASTM. ASTM D4373 - Standard test method for rapid determination of carbonate content of soils. American Society of Testing of Materials. , (2014).
- Schönenberger, J., Momose, T., Wagner, B., Leong, W. H., Tarnawski, V. R. Canadian field soils I. Mineral composition by XRD/XRF measurements. International Journal of Thermophysics. 33 (2), 342-362 (2012).
- Versteegh, E. A. A., Black, S., Hodson, M. E. Carbon isotope fractionation between amorphous calcium carbonate and calcite in earthworm-produced calcium carbonate. Applied Geochemistry. 78, 351-356 (2017).
- Soil Sampling. LSADPROC-300-R4. EPA. , Available from: https://www.epa.gov/sites/production/files/2015-06/documents/Soil-Sampling.pdf (2020).
- Smith, P., et al. How to measure, report and verify soil carbon change to realize the potential of soil carbon sequestration for atmospheric greenhouse gas removal. Global Change Biology. 26 (1), 219-241 (2020).
- Donovan, P. Measuring soil carbon change: A flexible, practical, local method. , Retrieved on January 19, https://soilcarboncoalition.org/measuring-soil-carbon-change-flexible-practical-local-method/ (2021).
- Haque, F., Santos, R. M., Chiang, Y. W. Using nondestructive techniques in mineral carbonation for understanding reaction fundamentals. Powder Technology. 357, 134-148 (2019).
- Han, X., et al. Understanding soil carbon sequestration following the afforestation of former arable land by physical fractionation. Catena. 150, 317-327 (2017).
- Jagadamma, S., Lal, R. Distribution of organic carbon in physical fractions of soils as affected by agricultural management. Biology and Fertility of Soils. 46 (6), 543-554 (2010).
- Walter, K., Don, A., Tiemeyer, B., Freibauer, A. Determining soil bulk density for carbon stock calculations: a systematic method comparison. Soil Science Society of America Journal. 80 (3), 579-591 (2016).
- Huijgen, W. J. J., Witkamp, G. -J., Comans, R. N. J. Mechanisms of aqueous wollastonite carbonation as a possible CO2 sequestration process. Chemical Engineering Science. 61 (13), 4242-4251 (2006).
- Bughio, M. A., et al. Neoformation of pedogenic carbonates by irrigation and fertilization and their contribution to carbon sequestration in soil. Geoderma. 262, 12-19 (2016).
- Carmi, I., Kronfeld, J., Moinester, M. Sequestration of atmospheric carbon dioxide as inorganic carbon in the unsaturated zone under semi-arid forests. Catena. 173, 93-98 (2019).
- Washbourne, C. L., Lopez-Capel, E., Renforth, P., Ascough, P. L., Manning, D. A. C. Rapid removal of atmospheric CO2 by urban soils. Environmental Science and Technology. 49 (9), 5434-5440 (2015).
Access restricted. Please log in or start a trial to view this content.
Réimpressions et Autorisations
Demande d’autorisation pour utiliser le texte ou les figures de cet article JoVE
Demande d’autorisationThis article has been published
Video Coming Soon