Un abonnement à JoVE est nécessaire pour voir ce contenu. Connectez-vous ou commencez votre essai gratuit.
Method Article
Microdissection en couche des feuillets de valve tricuspide pour la caractérisation mécanique biaxiale et la quantification microstructurale
Dans cet article
Résumé
Ce protocole décrit la caractérisation mécanique biaxiale, la quantification du collagène basée sur l’imagerie du domaine de fréquence spatiale polarisée et la microdissection des feuillets de valve tricuspide. La méthode fournie explique comment les couches de la foliole contribuent aux comportements holistiques de la feuille.
Résumé
La valve tricuspide (TV) régule le flux unidirectionnel de sang non oxygéné de l’oreillette droite vers le ventricule droit. Le téléviseur se compose de trois dépliants, chacun avec des comportements mécaniques uniques. Ces variations entre les trois feuillets de télévision peuvent être mieux comprises en examinant leurs quatre couches anatomiques, qui sont l’atrialis (A), le spongiosa (S), la fibrose (F) et le ventriculaire (V). Bien que ces couches soient présentes dans les trois feuillets de télévision, il existe des différences dans leurs épaisseurs et leurs constituants microstructuraux qui influencent davantage leurs comportements mécaniques respectifs.
Ce protocole comprend quatre étapes pour élucider les différences spécifiques à la couche: (i) caractériser les comportements architecturaux mécaniques et des fibres de collagène de la feuille de télévision intacte, (ii) séparer les couches composites (A / S et F / V) de la feuille de télévision, (iii) effectuer les mêmes caractérisations pour les couches composites et (iv) effectuer des couches post-hoc évaluation histologique. Ce cadre expérimental permet de manière unique la comparaison directe du tissu TV intact à chacune de ses couches composites. En conséquence, des informations détaillées concernant la microstructure et la fonction biomécanique des feuillets de télévision peuvent être collectées avec ce protocole. Ces informations peuvent potentiellement être utilisées pour développer des modèles informatiques de télévision qui cherchent à fournir des conseils pour le traitement clinique de la maladie de la télévision.
Introduction
Le téléviseur est situé entre l’oreillette droite et le ventricule droit du cœur. Tout au long du cycle cardiaque, le téléviseur régule le flux sanguin unidirectionnel par l’ouverture et la fermeture cycliques de la feuillet antérieure de la télévision (TVAL), de la feuillet postérieure de la télévision (TVPL) et de la feuillet septale de la télévision (TVSL). Ces folioles sont complexes et ont quatre couches anatomiques distinctes – l’atrialis (A), le spongiosa (S), le fibrosa (F) et le ventricularis (V) – avec des constituants microstructuraux uniques. Les fibres d’élastine dans l’atrialis et le ventriculaire aident à restaurer le tissu à sa géométrie non déformée après charge mécanique1. En revanche, la fibrose contient un réseau dense de fibres de collagène ondulées qui contribuent à la capacité portante des feuillets2. Principalement constitué de glycosaminoglycanes, le spongiosa a été supposé permettre le cisaillement entre les couches de la foliole pendant la fonction valvulaire cardiaque3. Bien que les trois types de feuillets aient les mêmes couches anatomiques, il existe des variations dans les épaisseurs des couches et les rapports constitutifs qui ont des implications pour les comportements mécaniques spécifiques aux feuillets.
Les chercheurs ont exploré les propriétés des feuillets de télévision à l’aide de caractérisations mécaniques planes, d’évaluations histomorphologiques et de caractérisations optiques de l’architecture des fibres de collagène. Par exemple, les caractérisations mécaniques biaxiales planes cherchent à imiter la charge physiologique en appliquant des déplacements perpendiculaires au tissu et en enregistrant les forces associées. Les observations de déplacement de force (ou d’étirement de contrainte) qui en ont résulté ont révélé que les trois feuillets de télévision présentent des comportements mécaniques non linéaires et spécifiques à la direction avec des réponses plus apparentes spécifiques à la feuillet dans la direction du tissu radial 4,5,6. On pense que ces comportements spécifiques aux feuillets proviennent de différences dans les propriétés microstructurelles observées à l’aide de techniques histologiques standard 6,7. En outre, l’imagerie de deuxième génération harmonique6, la diffusion de lumière à petit angle8 et l’imagerie du domaine de fréquence spatiale polarisée7 (pSFDI) visent à comprendre ces propriétés microstructurelles et ont montré des différences spécifiques à la feuillet dans l’orientation de la fibre de collagène et le sertissage de la fibre qui ont des implications pour les comportements mécaniques observés au niveau des tissus. Ces études ont considérablement fait progresser notre compréhension de la microstructure tissulaire et de son rôle dans les comportements au niveau des tissus. Cependant, il reste encore beaucoup à faire pour relier expérimentalement la mécanique tissulaire et la microstructure sous-jacente.
Récemment, ce laboratoire a réalisé des caractérisations mécaniques des couches de feuillet TV séparées en deux couches composites (A/S et F/V) à l’aide d’une technique de microdissection9. Ces travaux antérieurs ont mis en évidence les différences dans les propriétés mécaniques des couches et ont permis de mieux comprendre comment la microstructure en couches contribue aux comportements mécaniques des tissus. Bien que cette enquête ait amélioré notre compréhension de la microstructure des feuillets de télévision, la technique présentait plusieurs limites. Premièrement, les propriétés des couches composites n’ont pas été directement comparées au tissu intact, ce qui a conduit à un manque de compréhension complète de la relation mécanique-microstructure. Deuxièmement, l’architecture des fibres de collagène des couches composites n’a pas été examinée. Troisièmement, seules les couches du TVAL ont été étudiées en raison de difficultés à collecter les couches composites des deux autres dépliants télévisés. La méthode décrite ici fournit un cadre de caractérisation holistique qui surmonte ces limitations et fournit des caractérisations complètes des dépliants TV et de leurs couches composites.
Cet article décrit la technique de microdissection qui sépare les trois feuillets TV en leurs couches composites (A/S et F/V) pour les caractérisations mécaniques et microstructurelles biaxiales 10,11,12. Ce protocole itératif comprend (i) des essais mécaniques biaxiaux et la caractérisation pSFDI de la notice intacte, (ii) une technique de microdissection nouvelle et reproductible pour obtenir de manière fiable les couches TV composites, et (iii) des tests mécaniques biaxiaux et la caractérisation pSFDI des couches TV composites. Le tissu a été exposé à une charge de traction biaxiale avec différents rapports de force pour les essais mécaniques. Ensuite, pSFDI a été utilisé pour déterminer l’orientation et l’alignement des fibres de collagène dans diverses configurations chargées. pSFDI préserve l’architecture native des fibres de collagène, permet une analyse dépendante de la charge et contourne le besoin typique de fixer ou de nettoyer les tissus pour l’analyse de l’architecture des fibres de collagène, comme dans l’imagerie de deuxième génération harmonique ou la diffusion de la lumière à petit angle. Enfin, les tissus ont été préparés à l’aide de techniques d’histologie standard pour visualiser la microstructure tissulaire. Ce cadre itératif et holistique permet de comparer directement les propriétés mécaniques et microstructurelles de la feuille de télévision à ses couches composites.
Access restricted. Please log in or start a trial to view this content.
Protocole
Toutes les méthodes décrites dans le présent document ont été approuvées par le Comité institutionnel de soins et d’utilisation des animaux de l’Université de l’Oklahoma. Les tissus animaux ont été acquis dans un abattoir approuvé par l’USDA.
1. Caractérisation mécanique biaxiale
- Préparation des tissus
- Récupérez un dépliant TV du congélateur, des lames de rasoir, un stylo chirurgical, une pince, une pipette avec de l’eau désionisée (DI) et un tapis de coupe. Décongelez le dépliant tv en utilisant 2-3 gouttes d’eau DI à température ambiante.
REMARQUE: L’eau DI est utilisée à la place de la solution saline tamponnée au phosphate (PBS) pour éviter toute difficulté induite par le PBS pour la microdissection de la couche. - Déposer l’échantillon à plat sur le tapis de coupe avec la couche de ventriculaire (c’est-à-dire la surface avec les insertions de chordes) tournée vers le haut. Positionnez l’échantillon de manière à ce que la direction radiale s’aligne sur la direction Y et la direction circonférentielle s’aligne sur la direction X.
REMARQUE: La direction circonférentielle est orientée le long de la circonférence de la valve. - Examinez les emplacements d’insertion des chordes du tissu. Déterminez une zone, idéalement ~12 x 12 mm, avec le moins d’insertions de grandes chordes tout en évitant les zones extrêmement minces (c.-à-d. transparentes) (Figure 1).
- Retournez l’échantillon de sorte que la surface auriculaire (c.-à-d. la surface sans insertion de chordes) soit orientée vers le haut. Assurez-vous que les directions circonférentielle et radiale de la feuillette restent alignées avec les axes X et Y, respectivement.
- Découpez un échantillon carré de 12 x 12 mm dans le tissu de la feuillet qui évite les grandes insertions de chordes ou les zones minces identifiées à l’étape 1.1.3. Retirez les parties coupées du tissu de la feuillet avec les pinces et placez-les dans un conteneur à déchets.
- S’il n’est pas possible d’éviter complètement les grandes insertions de chordes, coupez les tissus de manière à ce qu’ils soient le long du bord du spécimen carré. Éviter les insertions de chordes est important car cela aide à prévenir les problèmes pour la microdissection ultérieure.
- Utilisez un stylo chirurgical pour placer un petit point dans le coin supérieur droit afin de suivre l’orientation de l’échantillon. Laissez sécher l’encre pendant environ 30 s.
- Retournez l’échantillon avec la surface ventriculaire (c.-à-d. la surface avec des insertions chordales) tournée vers le haut. Coupez les attaches chordales à l’arrière du tissu en étirant les cordes de la feuillet et en utilisant une lame de rasoir pour couper près de son emplacement d’insertion. Retournez l’échantillon pour que la surface auriculaire (c.-à-d. la surface lisse) soit orientée vers le haut.
- Récupérez un dépliant TV du congélateur, des lames de rasoir, un stylo chirurgical, une pince, une pipette avec de l’eau désionisée (DI) et un tapis de coupe. Décongelez le dépliant tv en utilisant 2-3 gouttes d’eau DI à température ambiante.
- Mesure d’épaisseur
- Récupérez un capteur de déplacement laser sans contact. Mettez à zéro le capteur de déplacement sur une section plate du tapis de coupe près du tissu coupé.
ATTENTION : Ne faites pas briller directement le laser dans les yeux. - Placez le laser sur la région centrale de l’échantillon. Retirez l’air emprisonné sous la surface de la feuillette car il peut provoquer des erreurs de mesure. Pour libérer l’air emprisonné, utilisez une pince à épiler pour pousser la bulle vers le bord du tissu ou soulevez un coin du tissu.
- Enregistrez l’épaisseur indiquée sur l’écran du capteur de déplacement. Répétez deux autres mesures à d’autres endroits de l’échantillon.
- Calculez l’épaisseur moyenne de la feuille à l’aide des trois mesures enregistrées à l’étape précédente. Utilisez cette valeur lors de la création des protocoles de caractérisation mécanique biaxiale.
- Récupérez un capteur de déplacement laser sans contact. Mettez à zéro le capteur de déplacement sur une section plate du tapis de coupe près du tissu coupé.
- Configuration du testeur biaxial et montage des tissus
- Préparez un bain-marie DI à 37 °C, en suivant les directives du système d’essai, pour assurer la température dans des conditions physiologiques in vivo .
- Récupérez les pinces, l’échantillon de tissu, le matériel de montage, un outil à pointe fine, de la colle cyanoacrylate liquide et des perles de verre peintes en noir (diamètre: 300-500 μm).
REMARQUE: Le matériel de montage comprend les tiges, le pont de montage et le caoutchouc de montage. - Montez l’échantillon de tissu sur le système d’essai. Assurez-vous que la direction circonférentielle du tissu s’aligne sur la direction X, qui peut être assistée par le point précédemment placé à l’étape 1.1.6.
REMARQUE: Les tiges utilisées ici doivent être espacées uniformément sur toute la longueur du bord du tissu. La longueur effective du bord est fixée à 10 mm pour le tissu intact et à >3,3 mm pour les couches composites.
- Placement des marqueurs fiducial
- Identifiez la région centrale d’un tiers carré du tissu monté. Utilisez les coins approximatifs de cette zone pour le placement du marqueur fiducial.
- Placez des perles de verre dans un bateau de pesage à face ouverte et créez un petit bassin de colle cyanoacrylate liquide dans un bateau de pesage séparé. Enduisez le dessus de l’outil à pointe fine avec une petite quantité de colle. Tamponnez l’excès de colle sur le côté du bateau de pesage.
- Créez un coin du tableau central d’un tiers carré en appuyant doucement sur la pointe enduite de colle sur le tissu. À l’aide d’une pince, saisissez une perle de verre et placez-la soigneusement sur le point de colle. Utilisez la caméra de l’appareil de test biaxial pour vous aider à placer les perles.
- Répétez les étapes 1.4.2 et 1.4.3 pour trois perles supplémentaires jusqu’à ce que le tableau carré soit terminé. Assurez-vous que les perles sont solidement attachées et que leurs points de colle respectifs ne se touchent pas ou ne collent pas ensemble. Séchez la colle avant d’abaisser le tissu dans le bain-marie.
- Si les perles sont collées ensemble, attendez que la colle sèche, puis utilisez la pince pour saisir doucement la perle ou la colle et retirez-la du tissu.
REMARQUE: La colle et les perles doivent se détacher, ce qui permet de réessayer le placement des perles.
- Si les perles sont collées ensemble, attendez que la colle sèche, puis utilisez la pince pour saisir doucement la perle ou la colle et retirez-la du tissu.
- Préconditionnement
- Créer un protocole de préconditionnement contrôlé par la force, dans lequel le tissu avec la longueur et l’épaisseur du bord subira six répétitions de charge équiaxiale jusqu’à un pic de tension membranaire T de 40 N/m avec une précharge de 3% × Tpic10 et des temps d’étirement et de récupération de 30 s chacun.
- Construisez un répertoire de test arbitraire qui stockera temporairement les données pour les calculs futurs. Réglez le taux de chargement sur 4,42 N/m.
- Construisez un nouveau jeu de paramètres de test portant le nom Preconditioning0. Réglez les modes de contrôle de l’axe X et de l’axe Y pour forcer et réglez les fonctions de contrôle sur pas. Définissez l’amplitude de la charge comme étant la force associée au pic T, c’est-à-dire fpic = T pic · L. Définissez l’amplitude de précharge comme 3 % du pic f pour la première répétition seulement et définissez à la fois la durée de l’étirement et la durée de récupération comme 30 s. Définissez le nombre de répétitions comme étant 10.
REMARQUE: Le pic calculé de la première contrainte de Piola-Kirchhoff, c’est-à-dire le pic P = pic T / t, peut dépasser 200 kPa pour les tissus plus minces, ce qui pourrait entraîner une déchirure des tissus pendant les tests. Dans ces scénarios, la tension maximale de la membrane a été ajustée à une première contrainte maximale de Piola-Kirchhoff de 200 kPa.
- Exécutez le protocole de préconditionnement. Après le préconditionnement, enregistrez les dimensions X et Y actuelles de l’échantillon pour les utiliser dans les protocoles d’essai biaxiaux.
- Créer un protocole de préconditionnement contrôlé par la force, dans lequel le tissu avec la longueur et l’épaisseur du bord subira six répétitions de charge équiaxiale jusqu’à un pic de tension membranaire T de 40 N/m avec une précharge de 3% × Tpic10 et des temps d’étirement et de récupération de 30 s chacun.
- Création et exécution de protocoles de test biaxiaux
- Déterminez le temps nécessaire pour obtenir la configuration équbiaxiale de crête à partir de la configuration post-préconditionnée avec le taux de déplacement souhaité. En tenant compte d’un taux de déplacement constant, calculez les temps de chargement pour les rapports de charge restants (c.-à-d. TXX:TYY = 1:0,5 et TXX:TYY = 0,5:1).
- Effectuez manuellement le jogging des actionneurs linéaires pour qu’ils correspondent aux forces cibles pour un rapport de charge donné. Répétez ce processus et enregistrez les dimensions de la feuille pour tous les rapports de chargement.
- Préparez un protocole d’essai contrôlé par déplacement qui déplace biaxialement le tissu de la configuration post-préconditionnée vers les configurations enregistrées à l’étape 1.6.2 (c.-à-d. TXX:TYY = 1:1, 1:0.5, 0.5:1) dans les délais déterminés à l’étape 1.6.1. Assurez-vous que chaque protocole comporte trois cycles de chargement/déchargement pour la répétabilité du comportement mécanique.
- Construisez un répertoire de test qui stockera les données pour les calculs futurs. Assurez-vous que le nom du répertoire correspond à l’échantillon actuel.
- Construisez un nouveau jeu de paramètres de test portant le nom 1:1, définissez les modes de contrôle de l’axe X et de l’axe Y sur déplacement et définissez les fonctions de contrôle sur rampe. Définissez l’amplitude d’étirement comme étant la configuration enregistrée à l’étape 1.6.1. Définissez l’amplitude de précharge comme 3 % du pic f pour la première répétition seulement, et définissez à la fois la durée d’étirement et la durée de récupération comme le temps enregistré à l’étape 1.6.1. Définissez le nombre de répétitions comme 3.
- Répétez l’étape 1.6.3.2 pour les rapports de charge restants (c.-à-d. TXX:TYY = 1:0,5 et TXX:TYY = 0,5:1), sauf définir l’amplitude de précharge comme non appliquée. Assurez-vous que l’amplitude de l’étirement, la durée de l’étirement et la durée de récupération correspondent à celles enregistrées à l’étape 1.6.2.
REMARQUE : Seules les données du dernier (troisième) cycle seront utilisées pour les analyses de contrainte et de déformation.
- Exécutez les protocoles contrôlés par déplacement. Une fois le test biaxial terminé, ramener le tissu à ses dimensions post-préconditionnées.
REMARQUE: Le test doit être immédiatement avorté si le tissu commence à se déchirer.
- Autres caractérisations
- Laissez le tissu immergé dans l’eau DI et monté sur le système de test biaxial. Effectuez l’imagerie pSFDI comme décrit aux étapes 2.1 à 2.3.
- Démontez le tissu. S’il s’agit d’un tissu intact, passez à la microdissection décrite aux étapes 3.1-3.7. Si ce n’est pas le cas, collectez l’histologie après l’étape 3.7.
REMARQUE: Le bain-marie DI peut être utilisé pour des caractérisations ultérieures dans la même journée. - Répétez les étapes 1.2 à 1.7 avec les couches A/S et F/V acquises après la microdissection (étapes 3.1 à 3.6).
REMARQUE: La répétition du protocole d’essai pour les couches permet une comparaison directe du tissu intact à ses propres couches.
- Procédures de post-traitement des données de test biaxiaux
- Effectuez une corrélation d’image numérique des images de test biaxiales acquises pour déterminer les positions des marqueurs dépendant du temps. Calculez les déplacements des marqueurs fiducial via Eq (1). 5
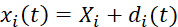 (1)
(1)
Ici, xi(t), Xi et di(t) sont l’emplacement dépendant du temps, l’emplacement initial (référence) et le déplacement du marqueur i. - Calculer le gradient de déformation F en considérant les marqueurs fiducaux comme un élément fini bilinéaire à quatre nœuds, comme indiqué dans Eq (2)5
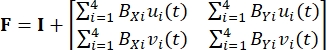 (2)
(2)
Où BXi et BYi sont les dérivées des fonctions de forme pour le nœud i dans les directions X et Y, respectivement, et ui(t) et vi(t) sont les composants de di(t): di(t) = [ui(t), vi(t)]T. - Calculer la première contrainte de Piola-Kirchhoff appliquée P en utilisant les forces enregistrées, comme dans Eq (3)5
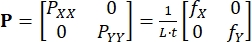 (3)
(3)
PXX et PYY sont les composantes X et Y de P; L et t sont la longueur et l’épaisseur du bord du tissu; fX et fY sont les forces enregistrées dans les directions X et Y. - Déterminer d’autres mesures de déformation et de contrainte au besoin,13 qui comprennent la déformation de Cauchy-Green droite C = FT/F, la déformation de Green-Lagrange E = (C - I)/2, la contrainte de Cauchy σ = J-1PFT et la deuxième contrainte de Piola-Kirchhoff S = F-1P.
REMARQUE: Ici, I est un tenseur d’identité de second ordre, et J = det(F) est le jacobin du gradient de déformation F.
- Effectuez une corrélation d’image numérique des images de test biaxiales acquises pour déterminer les positions des marqueurs dépendant du temps. Calculez les déplacements des marqueurs fiducial via Eq (1). 5
2. Imagerie du domaine de fréquence spatiale polarisée
- Préparation du système
REMARQUE: Si vous le souhaitez, les marqueurs fiducial peuvent être retirés du tissu avant les étapes suivantes.- Centrez le dispositif pSFDI sur l’échantillon (Figure 2). Allumez le projecteur et éclairez l’échantillon avec une lumière de 490 nm (cyan).
- Ouvrez le logiciel de la caméra et inspectez le champ de vision de la caméra. Assurez-vous que l’échantillon est centré dans le cadre et qu’il est complètement contenu dans le champ de vision.
- Si l’échantillon monté est un dépliant intact, ajustez la luminosité du projecteur de traitement numérique de la lumière (DLP) pour vous assurer que le tissu est entièrement éclairé sans éblouissement sur la surface du tissu. N’ajustez pas la luminosité si l’échantillon est l’une des couches composites.
- Faites pivoter le polariseur sur toute son amplitude de mouvement pour détecter d’éventuels éblouissements ou saletés sur la lentille polarisante. Nettoyez soigneusement la lentille polarisante avec un chiffon en microfibre si nécessaire.
- Collecte de données
REMARQUE : La collecte de données suivante peut être automatisée à l’aide de logiciels, tels que LabVIEW ou Python.- Déplacez le polariseur vers sa position d’origine, idéalement alignée sur l’un des axes de test biaxiaux. Capturez une image en niveaux de gris et enregistrez-la sur l’ordinateur avec l’emplacement du polariseur (c’est-à-dire 0°).
- Faites pivoter le polariseur de 5° et capturez une autre image en niveaux de gris. Répétez ce processus pour acquérir 37 images allant de 0° à 180° avec un incrément de 5°.
REMARQUE: Les images de la première séquence d’imagerie pSFDI peuvent être analysées au préalable pour assurer la réponse optique souhaitée du tissu. Reportez-vous à l’étape 2.3 pour obtenir des instructions. - Répétez la séquence d’imagerie pSFDI pour d’autres configurations tissulaires souhaitées, par exemple, les configurations de crête des protocoles de charge pris en compte pour les tests mécaniques biaxiaux.
- Procédures de post-traitement des données pSFDI
REMARQUE : La méthode suivante inclut des étapes pour le langage du programme MATLAB. Cependant, n’importe quel langage préféré (par exemple, Python, C ++) peut être utilisé à la place.- Utilisez la fonction MATLAB imread() pour construire des tableaux contenant les intensités en pixels des 37 images acquises. Pour plus de commodité, disposez-les comme un n × m × tableau tridimensionnel 37, où n et m sont les nombres de pixels le long des deux axes.
- Définissez la région tissulaire d’intérêt (ROI) à l’aide de la fonction grabit() définie par l’utilisateur.
- Ajuster les données d’intensité par rapport à l’angle du polariseur pour chaque pixel ROI à l’aide d’une série de Fourier à 3 termes, comme dans Eq (4) :
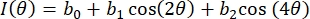 (4)
(4)
Ici, I(θ) est l’intensité par pixel en fonction de l’angle du polariseur, et bi sont les constantes de Fourier. Utilisez la régression linéaire standard des moindres carrés pour déterminer bi. - Déterminez l’orientation de la fibre en pixels comme l’angle de polarisation associé à la valeur maximale de I(θ). Calculer le degré d’anisotropie optique (DOA) via Eq (5).
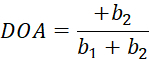 (5)
(5) - Utilisez plot() et histogram() pour visualiser l’orientation de la fibre acquise et les valeurs DOA. Enregistrez les résultats traités pour une utilisation ultérieure.
3. Microdissection des couches composites de feuillet de valve tricuspide
- Fixation tissulaire au panneau de cire
- Rassemblez les matériaux requis: planche de cire, eau DI, pipette, scalpel, micro ciseaux, pinces minces, pinces incurvées, pinces épaisses et épingles.
REMARQUE: N’utilisez que des pinces à épiler sans dents ni poignées, car les pinces de ce type peuvent très facilement déchirer le tissu mince de la couche A / S lors de la dissection. - Démontez le tissu du testeur biaxial et mesurez son épaisseur à l’aide du capteur de déplacement laser décrit à l’étape 1.2. Placez le tissu sur le panneau de cire.
- Examinez le côté ventriculaire du tissu pour les insertions de grandes chordes. Notez la position de ces insertions pour les éviter pendant la dissection (Figure supplémentaire S1). Prenez une photo pour référence.
- Étalez le tissu à plat sur la planche de cire avec l’atriaalis vers le haut. Apposez le tissu sur la planche à l’aide des broches:
- Dans chaque coin du tissu, placez une broche qui est inclinée loin du tissu (pour une meilleure visualisation) et qui tire légèrement le tissu tendu (Figure 3A). Faites-le dans le sens des aiguilles d’une montre ou dans le sens inverse des aiguilles d’une montre. Assurez-vous que les broches sont à l’extérieur des trous créés par les tiges lors du montage du tissu.
- Ajustez légèrement le placement de la broche pour vous assurer que le tissu est tendu et dans une configuration carrée (Figure 3B) de sorte que le tissu reste à plat et ne se déplace pas pendant la micro-dissection de la couche.
- Si nécessaire, placez des épingles le long du côté du tissu pendant la dissection pour étirer davantage le tissu. Gardez à l’esprit lorsque vous placez et inclinez des broches supplémentaires qu’elles doivent être contournées pendant la dissection.
- Retirez les marqueurs fiduciaires des billes de verre.
REMARQUE : L’étape suivante est facultative. L’eau DI ajoutée aide à maintenir l’hydratation des tissus et empêche le tissu de coller à lui-même tout au long de la microdissection. - À l’aide d’une pipette, placez de l’eau DI à la surface du tissu afin qu’elle recouvre complètement le tissu d’une manière semblable à une bulle. Reconstituez l’eau DI au besoin tout au long de la dissection.
- Rassemblez les matériaux requis: planche de cire, eau DI, pipette, scalpel, micro ciseaux, pinces minces, pinces incurvées, pinces épaisses et épingles.
- Faites le coin initial.
- Sélectionnez un coin de l’échantillon épinglé pour commencer la dissection. Évitez les grandes insertions de chordes et les zones extrêmement minces.
- Faites une coupe dans la couche A/S en faisant glisser légèrement le scalpel sur la surface du tissu le long des trous de montage des essais mécaniques (Figure 3C). Assurez-vous que la coupe mesure au moins 5 mm de long et que les bords de la coupe commencent à se séparer, révélant la couche F/V en dessous.
- Utilisez les pinces minces (sans pointe pointue) pour frotter fermement le long de la coupe et écarter les bords de la coupe (figure supplémentaire S2).
- Si la coupe dans la couche A / S ne commence pas à se séparer, tracez légèrement la même coupe à nouveau avec le scalpel jusqu’à ce qu’il commence à le faire. Veillez à ne pas couper trop profondément dans le tissu (au-delà de la couche composite A / S) car il est plus difficile de séparer proprement les couches.
- Répétez les étapes 3.2 et 3.2.3 pour effectuer une deuxième coupe perpendiculaire à la première coupe (Figure 3D). Assurez-vous que les deux coupes sont connectées et forment un coin.
- Si les deux coupes ne sont pas connectées, passez la pince à épiler fine sous la petite zone de tissu séparant les deux coupes (figure supplémentaire S3). Ensuite, utilisez soigneusement les ciseaux pour couper le tissu.
- Pelez le tissu du coin.
- Frottez le long des coupes à l’aide de la pince mince jusqu’à ce que le tissu commence à se séparer de la couche F / V. Dès qu’un petit morceau de tissu est séparé, saisissez-le avec la pince à épiler et tirez-le doucement pour séparer davantage les couches composites.
REMARQUE: Placez toujours la pointe de la pince à épiler mince au-delà du bord du tissu lors de la préhension. Sinon, ils pourraient accidentellement percer un trou dans la couche composite A / S. - Continuez à peler le tissu et frottez la couture jusqu’à ce qu’elle atteigne la fin des deux coupes faites pour le coin. Tout au long de ce processus, passez à une pince à épiler plus grande pour saisir le tissu pour le processus de pelage afin d’éviter la déchirure et la déchirure indésirables de la couche composite A / S.
- Si le premier virage tenté présente des problèmes majeurs de séparation, essayez un autre virage comme point de départ (revenez à l’étape 3.2).
- Frottez le long des coupes à l’aide de la pince mince jusqu’à ce que le tissu commence à se séparer de la couche F / V. Dès qu’un petit morceau de tissu est séparé, saisissez-le avec la pince à épiler et tirez-le doucement pour séparer davantage les couches composites.
- Étendez les coupures, pelez le tissu et faites un deuxième coin.
- Étendez les deux coupes faites pour le premier coin en plaçant la pointe du scalpel au bas de chaque coupe et en la faisant légèrement glisser le long de la surface du tissu (Figure 4A). Assurez-vous que toutes les coupes d’extension mesurent au moins 5 mm et que les extensions de coupe se connectent aux coupes d’origine et continuent de suivre les trous de tige ou de suture.
REMARQUE: Si la coupe d’extension est trop profonde, le peeling à venir doit être surveillé de près pour s’assurer que des sections de la fibrose ne sont pas séparées par la couche composite A / S (Figure 5A). - Continuez à étendre les coupes et à décoller la couche supérieure de composite A / S tout en frottant la couture jusqu’à ce qu’un côté soit terminé. Observez que le tissu sera complètement séparé le long d’une coupe; s’assurer que la couture entre les couches composites A/S et F/V est droite (Figure 4B).
- Répétez les instructions des étapes 3.2 et 3.3 pour créer un deuxième coin perpendiculaire à l’extrémité du côté entièrement pelé (Figure 4C).
- Étendez les deux coupes faites pour le premier coin en plaçant la pointe du scalpel au bas de chaque coupe et en la faisant légèrement glisser le long de la surface du tissu (Figure 4A). Assurez-vous que toutes les coupes d’extension mesurent au moins 5 mm et que les extensions de coupe se connectent aux coupes d’origine et continuent de suivre les trous de tige ou de suture.
- Séparez complètement la couche A/S.
- Prolongez les coupes restantes tout en évitant les grandes insertions de chordes. Continuez à séparer les couches A/S et F/V en utilisant les techniques de frottement et de traction utilisées pour le premier virage. Prenez note de plusieurs considérations ou problèmes qui peuvent survenir au cours de ce processus :
- Exclure les insertions de chordes de la zone de séparation A/S (figure 5B) uniquement lorsque cette exclusion permet d’obtenir un échantillon A/S suffisamment grand pour les caractérisations expérimentales (>3,3 mm).
- Si le tissu se déchire ou si un trou se forme, arrêtez immédiatement de séparer le tissu. Pour éviter que la pince à épiler ne se coince, placez les ciseaux dans n’importe quel trou qui se forme et coupez le tissu loin du centre. Si le défaut se forme le long de la couture de séparation, commencez à séparer le tissu le long d’un autre bord pour éviter toute déchirure supplémentaire (Figure 5C).
- Recherchez les connexions intercalaires qui peuvent apparaître lors de la séparation du tissu et empêchez une séparation ultérieure du tissu sans risque élevé de déchirure (figure 5D). Observez que ce sont des brins minces mais solides qui doivent être soigneusement coupés à l’aide de ciseaux. Évitez de créer un trou dans la couche A/S ou de couper vers le bas dans la couche F/V, car cela entraînerait une séparation inégale.
- Poursuivez ce processus jusqu’à ce que le plus grand échantillon possible de la couche A/S ait été séparé. Marquez l’orientation de l’échantillon à l’aide du stylo chirurgical (Figure 6A).
- Prolongez les coupes restantes tout en évitant les grandes insertions de chordes. Continuez à séparer les couches A/S et F/V en utilisant les techniques de frottement et de traction utilisées pour le premier virage. Prenez note de plusieurs considérations ou problèmes qui peuvent survenir au cours de ce processus :
- Dissection finale.
- Utilisez les ciseaux pour couper le long de la couture de séparation pour le bord du tissu restant (Figure 6B). Assurez-vous que cette coupe est aussi proche que possible de la couture de séparation.
- Placez la couche composite A/S séparée à plat sur le tapis de coupe. Si nécessaire, utilisez le scalpel pour redresser les bords du tissu et créer une forme de tissu carrée adaptée aux tests mécaniques biaxiaux. Placez la couche A/S dans de l’eau DI jusqu’à ce qu’elle soit prête à être testée.
- Marquez l’orientation de la couche F/V qui reste sur le panneau de cire. Découpez le plus grand carré possible dans la zone où la couche A/S a été retirée (Figure 6C), puis placez-la dans de l’eau DI.
- Histologie
- Excisez deux bandes de tissu – alignées avec les directions circonférentielle et radiale – pour une utilisation en histologie. Utilisez différents protocoles pour les couches intactes et composites (c.-à-d. A/S et F/V).
- Pour la couche intacte, prélevez les spécimens du tissu qui reste épinglé à la planche de cire. Utilisez le tissu à l’extérieur des trous de suture, car cette partie du tissu n’a pas été disséquée et représentera la feuillette intacte.
- Pour les couches composites A/S et F/V, ne prélevez des échantillons d’histologie qu’après avoir terminé leurs tests et leur imagerie. Démontez l’échantillon du système de test biaxial, posez le tissu à plat sur un tapis de coupe et excisez les bandes circonférentielles et radiales à l’aide d’une lame de rasoir.
- Placez les bandes excisées dans des cassettes de tissu et immergez les cassettes dans 10% de formol.
- Jetez le tissu restant. Nettoyez les outils de dissection à l’aide d’un composé nettoyant (voir le tableau des matériaux).
- Après 24-48 h de fixation, transférer les cassettes à l’éthanol, où elles peuvent être stockées indéfiniment jusqu’au traitement histologique et à la coloration.
REMARQUE: Cette analyse histologique peut confirmer que la microdissection est réussie. ATTENTION: 10% de formol provoque une irritation de la peau et de graves lésions oculaires. Il peut également provoquer une réaction allergique ou un cancer par inhalation. Lors de la manipulation, portez un équipement de protection individuelle approprié, comme des gants, des lunettes et un manteau de laboratoire, et n’utilisez que dans des espaces bien ventilés, comme dans une hotte aspirante. Lorsqu’il n’est pas utilisé, assurez-vous que le récipient de stockage est bien fermé.
- Excisez deux bandes de tissu – alignées avec les directions circonférentielle et radiale – pour une utilisation en histologie. Utilisez différents protocoles pour les couches intactes et composites (c.-à-d. A/S et F/V).
Access restricted. Please log in or start a trial to view this content.
Résultats
La microdissection produira des échantillons A/S et F/V d’épaisseurs relativement uniformes pouvant être montés sur un dispositif d’essai biaxial (commercial). L’analyse histologique de la feuillette intacte et des deux couches disséquées permettra de vérifier si le tissu a été correctement séparé le long de la frontière entre la spongiose et la fibrose (Figure 7). De plus, les micrographies histologiques peuvent être utilisées pour déterminer l’épaisseur de la couche...
Access restricted. Please log in or start a trial to view this content.
Discussion
Les étapes critiques du protocole comprennent : (i) la microdissection de la couche, (ii) le montage tissulaire, (iii) le placement du marqueur fiducial et (iv) la configuration de l’IDSP. La microdissection de couche appropriée est l’aspect le plus important et le plus difficile de la méthode décrite ici. Avant de lancer une enquête utilisant cette technique, le ou les dissecteurs devraient avoir une pratique à long terme avec la technique de microdissection et les trois dépliants télévisés. Le dissecteur ...
Access restricted. Please log in or start a trial to view this content.
Déclarations de divulgation
Les auteurs n’ont aucun conflit d’intérêts à divulguer.
Remerciements
Ce travail a été soutenu par l’American Heart Association Scientist Development Grant (16SDG27760143) et la Presbyterian Health Foundation. KMC a été soutenu en partie par le programme d’opportunités de recherche de premier cycle de l’Université de l’Oklahoma (OU) et le programme d’apprentissage en recherche spécialisé. DWL a été soutenu en partie par la National Science Foundation Graduate Research Fellowship (GRF 2019254233) et l’American Heart Association/Children’s Heart Foundation Predoctoral Fellowship (prix #821298). Tout ce soutien est reconnu avec gratitude.
Access restricted. Please log in or start a trial to view this content.
matériels
| Name | Company | Catalog Number | Comments |
| 10% Formalin Solution, Neutral Buffered | Sigma-Aldrich | HT501128-4L | |
| Alconox Detergent | Alconox | cleaning compound | |
| BioTester - Biaxial Tester | CellScale Biomaterials Testing | 1.5 N Load Cell Capacity | |
| Cutting Mat | Dahle | B0027RS8DU | |
| Deionized Water | N/A | ||
| Fine-Tipped Tool | HTI INSTRUMENTS | NSPLS-12 | |
| Forceps - Curved | Scientific Labwares | 16122 | |
| Forceps - Thick | Scientific Labwares | 161001078 | |
| Forceps - Thin | Scientific Labwares | 16127 | |
| LabJoy | CellScale Biomaterials Testing | Version 10.66 | |
| Laser Displacement Sensor | Keyence | IL-030 | |
| Liquid Cyanoacrylate Glue | Loctite | 2436365 | |
| MATLAB | MathWorks | Version 2020a | |
| Micro Scissors | HTI Instruments | CAS55C | |
| Pipette | Belmaks | 360758081051Y4 | |
| Polarized Spatial Frequency Domain Imaging Device | N/A | Made in-house using a digital light projector, linear polarizer, rotating polarizer mount, and charge-coupled device camera. See doi.org/10.1016/j.actbio.2019.11.028 (PMCID: PMC8101699) for more details. | |
| Scalpel | THINKPRICE | TP-SCALPEL-3010 | |
| Single Edge Industrial Razor Blades (Surgical Carbon Steel) | VWR International | H3515541105024 | |
| Surgical Pen | LabAider | LAB-Skin-6 | |
| T-Pins | Business Source | BSN32351 | |
| Wax Board | N/A | Made in-house using modeling wax and baking tray | |
| Weigh Boat | Pure Ponta | mdo-azoc-1030 |
Références
- Vesely, I. The role of elastin in aortic valve mechanics. Journal of Biomechanics. 31 (2), 115-123 (1998).
- Zhang, W., Ayoub, S., Liao, J., Sacks, M. S. A meso-scale layer-specific structural constitutive model of the mitral heart valve leaflets. Acta Biomaterialia. 32, 238-255 (2016).
- Stella, J. A., Sacks, M. S. On the biaxial mechanical properties of the layers of the aortic valve leaflet. Journal of Biomechanical Engineering. 129 (5), 757-766 (2007).
- Khoiy, K. A., Amini, R. On the biaxial mechanical response of porcine tricuspid valve leaflets. Journal of Biomechanical Engineering. 138 (10), 104504(2016).
- Jett, S. V., et al. An investigation of the anisotropic mechanical properties and anatomical structure of porcine atrioventricular heart valves. Journal of the Mechanical Behavior of Biomedical Materials. 87, 155-171 (2018).
- Meador, W. D., et al. A detailed mechanical and microstructural analysis of ovine tricuspid valve leaflets. Acta Biomaterialia. 102, 100-113 (2020).
- Hudson, L. T., et al. A pilot study on linking tissue mechanics with load-dependent collagen microstructures in porcine tricuspid valve leaflets. Bioengineering. 7 (2), 60(2020).
- Pant, A. D., et al. Pressure-induced microstructural changes in porcine tricuspid valve leaflets. Acta Biomaterialia. 67, 248-258 (2018).
- Kramer, K. E., et al. An investigation of layer-specific tissue biomechanics of porcine atrioventricular heart valve leaflets. Acta Biomaterialia. 96, 368-384 (2019).
- Ross, C. J., Laurence, D. W., Wu, Y., Lee, C. -H. Biaxial mechanical characterizations of atrioventricular heart valves. Journal of Visualized Experiments: JoVE. (146), e59170(2019).
- Goth, W., Lesicko, J., Sacks, M. S., Tunnell, J. W. Optical-based analysis of soft tissue structures. Annual Review of Biomedical Engineering. 18, 357-385 (2016).
- Jett, S. V., et al. Integration of polarized spatial frequency domain imaging (pSFDI) with a biaxial mechanical testing system for quantification of load-dependent collagen architecture in soft collagenous tissues. Acta Biomaterialia. 102, 149-168 (2020).
- Reddy, J. N. An Introduction to Continuum Mechanics. , Cambridge University Press. (2013).
- Duginski, G. A., Ross, C. J., Laurence, D. W., Johns, C. H., Lee, C. -H. An investigation of the effect of freezing storage on the biaxial mechanical properties of excised porcine tricuspid valve anterior leaflets. Journal of the Mechanical Behavior of Biomedical Materials. 101, 103438(2020).
- Salinas, S. D., Clark, M. M., Amini, R. Mechanical response changes in porcine tricuspid valve anterior leaflet under osmotic-induced swelling. Bioengineering. 6 (3), 70(2019).
- Pokutta-Paskaleva, A., Sulejmani, F., DelRocini, M., Sun, W. Comparative mechanical, morphological, and microstructural characterization of porcine mitral and tricuspid leaflets and chordae tendineae. Acta Biomaterialia. 85, 241-252 (2019).
- Ross, C. J., et al. An investigation of the glycosaminoglycan contribution to biaxial mechanical behaviors of porcine atrioventricular heart valve leaflets. Journal of the Royal Society Interface. 16 (156), 0069(2019).
- Sommer, G., Regitnig, P., Költringer, L., Holzapfel, G. A. Biaxial mechanical properties of intact and layer-dissected human carotid arteries at physiological and supraphysiological loadings. American Journal of Physiology-Heart and Circulatory Physiology. 298 (3), 898-912 (2009).
- Holzapfel, G. A., Sommer, G., Gasser, C., Regitnig, P. Determination of the layer-specific mechanical properties ofhuman coronary arteries with intimal thickening, and related constitutive modelling. American Journal of Physiology-Heart and Circulatory Physiology. 289 (5), 2048-2058 (2005).
- Sommer, G., et al. Multiaxial mechanical response and constitutive modeling of esophageal tissues: Impact on esophageal tissue engineering. Acta Biomaterialia. 9 (12), 9379-9391 (2013).
Access restricted. Please log in or start a trial to view this content.
Réimpressions et Autorisations
Demande d’autorisation pour utiliser le texte ou les figures de cet article JoVE
Demande d’autorisationExplorer plus d’articles
This article has been published
Video Coming Soon