Method Article
Mise en place d’un modèle de dressage animal de duodénoscopie, de cholédochoscopie et de laparoscopie pour la cholélithiase
* Ces auteurs ont contribué à parts égales
Dans cet article
Résumé
Ici, nous présentons un protocole pour l’établissement d’un modèle d’entraînement animal combiné multi-scopies afin d’améliorer la compétence et la compréhension des jeunes médecins dans la technologie combinée multi-scopies.
Résumé
La cholélithiase est une affection caractérisée par la formation de calculs dans la vésicule biliaire et/ou les voies biliaires. L’utilisation efficace des techniques de duodénoscopie, de laparoscopie et de cholédochoscopie joue un rôle central dans la prise en charge de la cholélithiase. Afin d’améliorer les compétences des jeunes médecins dans l’application de la technologie des multiendoscopes, un modèle de formation pour la duodénoscopie, la cholédochoscopie et la laparoscopie a été établi à l’aide d’un modèle de porc vivant. Initialement, le duodénoscope était utilisé pour accéder au duodénum par le passage par la bouche, l’œsophage et l’estomac afin d’observer la papille duodénale. Par la suite, le tube a été inséré dans le canal cholédoque, suivi de la mise en place du fil guide. Des trocarts ont ensuite été insérés pour établir le pneumopéritoine et faciliter la réalisation de la cholécystectomie laparoscopique. Le canal cholédoque a été exploré et ouvert en récupérant le fil-guide qui s’y trouvait. Le cholédochoscope a ensuite été utilisé pour explorer à la fois le canal cholédoque distal et les canaux biliaires intrahépatiques. Enfin, sous guidage duodénoscopie, la mise en place d’une sonde nasobiliaire ou d’une endoprothèse biliaire en plastique a eu lieu avant la fermeture de la suture primaire du canal cholédoque. L’établissement d’un modèle animal combiné multi-scopies peut encore améliorer les compétences des jeunes médecins dans la technologie combinée multi-scopies grâce à l’expérience pratique.
Introduction
La cholélithiase est une maladie courante du système digestif, caractérisée par la formation de calculs dans la vésicule biliaire et/ou les voies biliaires. L’incidence des calculs biliaires chez l’adulte est estimée entre 10 % et 20 %1,2, avec environ 5 à 15 % des patients présentant également une cholédocholithiase ou une hépatolithiase. La cholédocholithiase peut entraîner de graves complications telles qu’une cholangite aiguë ou une pancréatite biliaire.
Les calculs cholédoques (CBDS) sont souvent dus à la migration de la vésicule biliaire, bien que quelques-uns puissent se développer directement dans le canal biliaire. Des calculs cholédoques coexistants sont trouvés chez 3 % à 16 % des patients atteints de calculs symptomatiques de la vésicule biliaire 3,4. Selon les directives de pratique clinique fondées sur des preuves pour la cholélithiase 2021, l’ablation endoscopique du CBDS associée à une cholécystectomie chirurgicale et l’ablation chirurgicale du CBDS associée à une cholécystectomie sont recommandées pour les CBDS avec calculs de la vésicule biliaire 5,6. Pour une récupération mini-invasive et rapide, la cholangiographie rétrograde endoscopique (CPRE) associée à la cholécystectomie laparoscopique (LC) ou la cholédochotomie en tube T d’exploration laparoscopique du cholédoque (LCBDE) associée à la LC constituent la prise en charge habituelle en clinique. Ces traitements nécessitent l’utilisation de techniques combinées à plusieurs scopies telles que la technique CPRE associée à la technique laparoscopique ou la technique laparoscopique associée à la technique cholédoscopique. Ces techniques sont aujourd’hui principalement des procédures thérapeutiques, et le manque d’expérience entraîne un risque plus élevé d’événements indésirables 7,8. Ainsi, la formation et l’enseignement des techniques combinées de multi-scopie ont gagné en importance9. Cependant, il n’existe actuellement aucun bon modèle de formation et d’enseignement des techniques combinées de multiscopie.
Ici, nous présentons un protocole d’entraînement pour les techniques combinées de multi-scopie impliquant la duodénoscopie, la cholédochoscopie et la laparoscopie à l’aide d’un modèle de porc vivant. La mise en place d’un modèle animal combiné multi-scopies peut améliorer les compétences et la compréhension des jeunes médecins dans la technologie combinée multi-scopies grâce à une expérience pratique. Cela contribuera au développement de leurs compétences globales et à leur compréhension dans ce domaine.
Protocole
La procédure d’expérimentation sur des porcs vivants a été réalisée conformément aux règles internationales et a été approuvée par le Comité de protection des animaux (WebLab020-FY202403).
1. Préparation du modèle
- Soumettez le mini-porc à une période de jeûne de 12 h et privez-lui l’accès à l’eau potable le matin de l’intervention.
- Effectuer une intubation endotrachéale et administrer de l’isoflurane de 0,5 à 2 % dans un rapport de 1:1 avec de l’oxygène à un débit de 5 à 10 mL/kg/min pour amorcer l’anesthésie générale. Gardez les yeux du porc fermés avec un pansement film.
REMARQUE : La réponse somatocinétique est utilisée pour évaluer la profondeur de l’anesthésie. Cette évaluation est jugée appropriée lorsque le porc ne répond pas alors que la fréquence cardiaque et la respiration restent stables pendant l’opération. - Placez le porc sur une table d’opération en position couchée pour les expériences.
- Surveillez la fréquence cardiaque et la saturation en oxygène à l’aide d’un électrocardiogramme.
- Stérilisez la peau abdominale avec de l’iodophore, puis couvrez-la de serviettes stériles.
2. Procédure de CPRE (figure 1)
- Vérifiez le duodénoscope en conjonction avec le système d’imagerie et ses fonctionnalités, y compris la consommation d’eau, l’absorption deCO2 et les capacités d’aspiration.
- Tenez le duodénoscope et insérez-le dans la bouche, passez-le dans l’œsophage et dans la cavité gastrique (Figure 1A, B).
- Naviguez à travers le pylore (figure 1C) et dans le duodénum pour observer la papille duodénale (figure 1D).
REMARQUE : Habituellement, le passage à travers le pylore est difficile et facile à glisser vers l’arrière car le muscle pylorique est hypertrophique et la position de la papille duodénale est près du pylore. La personne qui tient et contrôle le duodénoscope doit être bien formée à cette procédure. - À l’aide d’un sphinctérotome muni d’un fil-guide biliaire, c’est la canule de la papille duodénale (figure 1E).
- Canulez le canal cholédoque (CBD) à l’aide d’un fil-guide et conservez-le dans le CBD (Figure 1F).
3. Etablissement du pneumopéritoine
- Incisez la peau au-dessus de l’ombilic avec 10 mm, puis utilisez deux pinces à serviette pour clamper et soulever la peau des deux côtés de l’incision. Insérez l’aiguille Veress dans la cavité abdominale par l’incision.
- En cas d’échec, incisez la paroi abdominale couche par couche jusqu’à la profondeur pour atteindre la cavité abdominale.
- Injectez du dioxyde de carbone à travers l’aiguille de Veress (reliée à une pompe à gaz de dioxyde de carbone) et maintenez une pression de pneumopéritoine de 12 mmHg.
4. Placement du trocart
- Positionnez le port d’observation à proximité de l’ombilic pour faciliter une exploration complète de la cavité abdominale.
- Insérez un trocart de 12 mm à environ 2 cm sous l’apophyse xiphoïde après avoir incisé la peau.
- Insérez un trocart de 5 mm à environ 2 cm sous le bord costal de la ligne médio-claviculaire droite après avoir incisé la peau.
- Insérez un trocart de 5 mm à 2 cm sous le bord costal de la ligne axillaire antérieure droite après avoir incisé la peau.
REMARQUE : Des précautions doivent être prises pour éviter d’endommager les intestins qui peuvent adhérer à la paroi abdominale.
5. Procédure LC (Figure 2)
- Retenez le lobe du foie pour exposer la vésicule biliaire à l’aide d’une pince gastrique.
- Saisissez l’ampoule de la vésicule biliaire pour exposer le triangle de la vésicule biliaire à l’aide d’une pince séparée.
- Disséquez soigneusement le canal cystique et l’artère kystique. Ensuite, ligaturez-les et déconnectez-les (Figure 2B).
- Détachez doucement la vésicule biliaire de l’arrière du foie jusqu’à ce qu’elle soit complètement retirée (Figure 2A).
6. Procédure LCBDE (Figure 3)
- Retenez le lobe du foie pour exposer la position du CBD à l’aide d’une pince gastrique.
- Séparez le CBD jusqu’à la dissociation complète à l’aide d’un crochet électrique (Figure 3A).
- Disséquez le CBD longitudinalement pour exposer le fil-guide dans le CBD (Figure 3B).
- À l’aide d’un cholédochoscope, explorez la partie inférieure du CBD et de la papille duodénale vers le bas (figures 3C, E), et le canal hépatique commun et le canal biliaire intrahépatique vers le haut (figures 3D, F).
REMARQUE : Dans les cas où des calculs résiduels sont présents, une extraction endoscopique du panier peut être effectuée. Envisagez soit une fermeture primaire, soit la mise en place d’un tube en T pour une gestion optimale, en fonction du diamètre du CBD.
7. Post-opération
- Suturez les incisions abdominales et euthanasiez le porc avec 20 ml d’injection de chlorure de potassium sous anesthésie.
Résultats
Le protocole d’entraînement pour les techniques combinées de multi-scopie a été réalisé avec une femelle mini-porc domestiquée de 35 kg. Après que le porc ait été anesthésié et surveillé, la peau de l’abdomen a été stérilisée et recouverte de serviettes. Le duodénoscope a été inséré dans la bouche, passé à travers l’œsophage et dans la cavité gastrique (figures1A, B), guidé à travers le pylore (figure 1C) et dans le duodénum, où la papille duodénale (figure 1D) a pu être observée. Le CBD a été canulé sélectivement à l’aide d’un sphinctérotome et d’un fil-guide (figure 1E), qui a ensuite été maintenu en place (figure 1F). Après l’établissement d’un pneumopéritoine et la mise en place de trocarts, une cholécystectomie laparoscopique a été réalisée (Figure 2). Le CBD a été séparé à l’aide d’un crochet électrique (figure 3A) et disséqué longitudinalement avec le fil-guide exposé (figure 3B). L’ensemble du CBD et du canal biliaire intrahépatique a été exploré à l’aide d’un cholédochoscope (Figure 3C-F). Une fermeture primaire a ensuite été effectuée avant le retrait de l’équipement et la suture des incisions. Enfin, sous anesthésie, l’euthanasie du porc a eu lieu.
Nous avons effectué cette procédure sur cinq porcs. Au départ, nous avons appliqué la procédure à un seul porc, ce qui a donné des résultats positifs. Ensuite, nous avons réuni 20 stagiaires pour présenter le protocole et les vidéos de procédure, en dispensant une formation à quatre porcs supplémentaires. Parmi ces stagiaires, quatre praticiens expérimentés de la CPRE ont terminé avec succès la procédure de CPRE en 30 minutes. En revanche, huit stagiaires ayant peu ou pas d’expérience préalable en CPRE ont rencontré des difficultés dans le délai initial de 30 minutes ; cependant, quatre d’entre eux ont été en mesure de terminer la procédure de CPRE après deux ou trois essais avec l’aide de tuteurs dans les 30 minutes suivantes. De plus, quatre stagiaires ont exécuté avec succès la procédure LC tandis que quatre autres stagiaires ont accompli la procédure LCBDE en 30 minutes. Ainsi, un total de quatre groupes de stagiaires ont terminé avec succès le protocole (tableau 1).
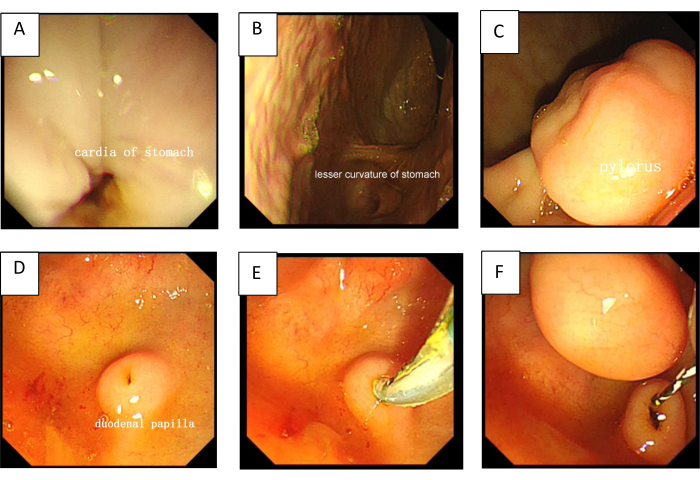
Figure 1 : Le déroulement de la CPRE. (A) Le cardia de l’estomac. (B) La moindre courbure de l’estomac. (C) Le pylore. (D) La papille duodénale. (E) Un sphinctérotome avec un fil-guide biliaire pour canuler la papille duodénale. (F) Après une canulation sélective du canal cholédoque (CBD), le fil-guide a été retenu dans le canal cholédoque. Veuillez cliquer ici pour voir une version agrandie de cette figure.
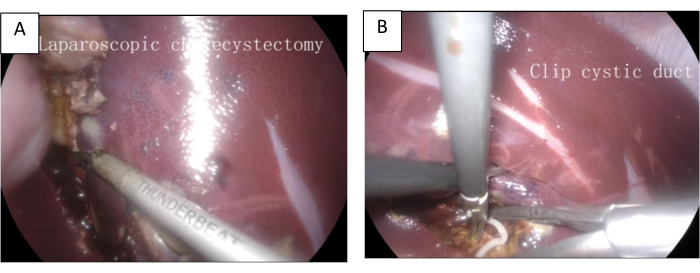
Figure 2 : La procédure de LC. (A) La vésicule biliaire est séparée de l’arrière du foie. (B) Coupez le canal cystique. Veuillez cliquer ici pour voir une version agrandie de cette figure.
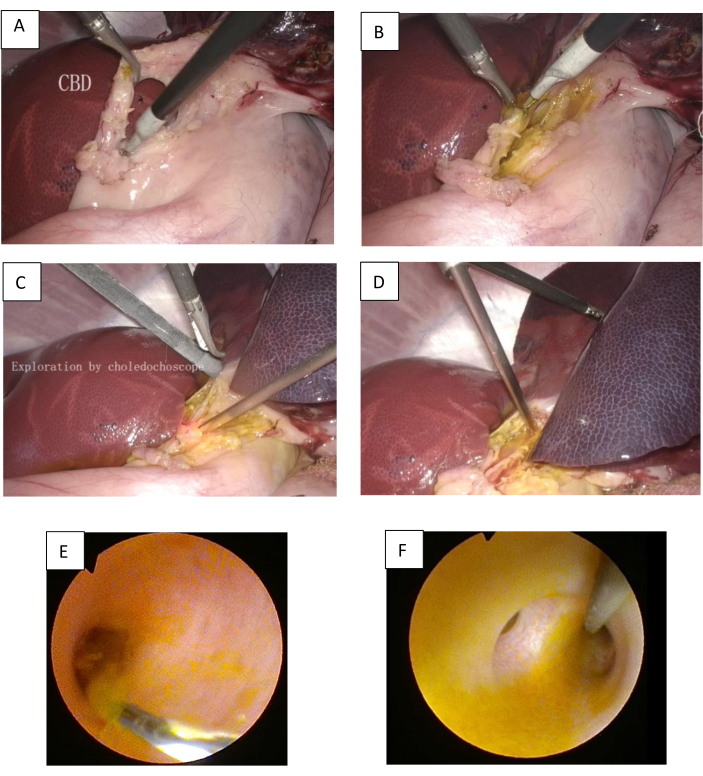
Figure 3 : La procédure de LCBDE : (a) Séparer le CBD. (B) Le CBD a été disséqué longitudinalement pour exposer le fil-guide. (C) Un cholédochoscope a été utilisé pour explorer la partie inférieure du CBD et la papille duodénale vers le bas. (D) Un cholédochoscope a été utilisé pour explorer le canal hépatique commun et le canal biliaire intrahépatique vers le haut. (E) La partie inférieure du CBD. (F) Le canal biliaire hilaire. Veuillez cliquer ici pour voir une version agrandie de cette figure.
| Description | Nombre de stagiaires | Procédure | |
| Réalisation réussie de la procédure de CPRE en 30 min | 4 | CPRE | |
| Stagiaires non expérimentés avec des difficultés dans les 30 premières minutes | CPRE | ||
| Non expérimenté avec des difficultés après 2-3 essais avec l’aide de tuteurs dans les 30 minutes suivantes | 4 | CPRE | |
| Non expérimenté avec réussite après 2-3 essais avec l’aide de tuteurs dans les 30 minutes suivantes | 4 | CPRE | |
| Réalisation réussie de la procédure LC en 30 min | 4 | LC | |
| Réalisation réussie de la procédure LCBDE en 30 min | 4 | LCBDE | |
| Nombre total de stagiaires | 20 | ||
Tableau 1 : Données représentatives du programme de formation.
Discussion
La cholélithiase est une maladie courante et récurrente qui présente des défis dans la prise en charge. Avec les progrès de la technologie, les techniques mini-invasives, en particulier la technique combinée à plusieurs scopies, ont été de plus en plus utilisées dans le traitement de la cholélithiase. Selon la taille et la répartition des calculs, les modèles de traitement des calculs peuvent être classés comme suit : (1) Pour les CBD inférieurs à 1 cm, avec ou sans calculs de la vésicule biliaire, il est suggéré d’enlever le calcul à l’aide d’une CPRE à expansion lente du ballonnet pour préserver la fonction du mamelon, avec ou sans LC. (2) Pour les CBDS de plus de 1 cm, avec ou sans calculs de la vésicule biliaire, il est recommandé d’éliminer les calculs à l’aide d’une lithotripsie électrohydraulique ou d’un panier de lithotripsie après dilatation lente par ballonnet sous CPRE préservant le mamelon, avec ou sans LC. Alternativement, les pierres peuvent être éliminées par LCBDE avec ou sans LC. La mise en place d’une endoprothèse biliaire sous CPRE combinée à une LC et une LCBDE sans tube T est également une option viable. (3) En cas de calculs biliaires intrahépatiques, l’approche thérapeutique peut impliquer une hépatectomie laparoscopique ou une cholangioscopie transhépatique percutanée, en fonction de la situation et de la distribution des calculs. Un seul traitement utilisant la laparoscopie ou la duodénoscopie ne permet souvent pas d’obtenir une efficacité optimale pour les patients atteints de vésicule biliaire et de calculs de CBD. L’application combinée de la multi-scopie a apporté des changements révolutionnaires dans le traitement mini-invasif de la cholélithiase10. Lv et al.11 ont démontré que l’approche tri-endoscopique pour la cholécystolithiase et la cholédocholithiase concomitantes est à la fois sûre et efficace, ce qui permet de raccourcir les séjours à l’hôpital et de réduire les coûts. Il est évident que des compétences maîtrisées dans les techniques de duodénoscopie, de laparoscopie et de cholédochoscopie jouent un rôle crucial dans le traitement de la cholélithiase. Parce que le manque d’expérience pourrait entraîner un risque plus élevé d’événements indésirables, la formation et l’enseignement semblent avoir gagné en importance. Traditionnellement, les techniques de CPRE ont été entraînées à l’aide de simulateurs informatisés12 ou de modèles d’entraînement ex vivo13, tandis que les compétences laparoscopique ont été développées à l’aide de méthodes de boîtesèche 14 ou de boîte15 ex vivo. Cependant, ces modèles de formation ne parviennent souvent pas à intégrer efficacement les avantages de la CPRE et des techniques laparoscopique. Par conséquent, il est urgent de disposer d’un nouveau modèle d’entraînement qui facilite les techniques combinées pour l’entraînement multi-scopies.
Nous avons développé un modèle de porc vivant pour l’entraînement aux techniques de multi-scopie combinées. Les résultats représentatifs indiquent que ce modèle est efficace (tableau 1). Des techniques telles que la CPRE, la chirurgie laparoscopique et la cholédochoscopie peuvent toutes être entraînées efficacement à l’aide de ce modèle. Ce modèle présente plusieurs avantages uniques. Tout d’abord, il est bénéfique pour simuler les structures physiologiques et anatomiques humaines. Par exemple, il fournit une simulation réaliste du tube digestif physiologique pour l’entraînement au contrôle de la duodénoscopie, ainsi que des opportunités de pratiquer la gestion des saignements et la suture des voies biliaires à l’aide de techniques laparoscopique16. Le modèle porcin offre un environnement de formation précieux pour les médecins débutants. Deuxièmement, ce modèle porcin facilite l’entraînement aux techniques hybrides. Dans les cas où la duodénoscopie s’avère infructueuse, le gastroscope peut être inséré dans le duodénum à la place. Un fil-guide laparoscopique peut ensuite être introduit dans le canal cholédoque via le canal cystique, puis avancé dans le duodénum par la papille. Après une observation sous guidage gastroscopique, des pinces peuvent être utilisées pour saisir et manœuvrer le fil-guide hors de la bouche avant de revenir à un duodénoscope pour faire naviguer le fil le long de son chemin prévu dans le duodénum. De plus, ce modèle met l’accent sur le travail d’équipe lors des sessions de formation en nécessitant une collaboration étroite entre les membres de l’équipe. Cette approche favorise l’esprit d’équipe et améliore les compétences de communication chez les jeunes médecins. Enfin, ce modèle de formation incarne les caractéristiques de la chirurgie mini-invasive en privilégiant la réduction des traumatismes. Il vise à améliorer la compréhension et la compétence des jeunes médecins dans les pratiques chirurgicales mini-invasives.
Pour des raisons éthiques, nous avons choisi un porc vivant comme modèle d’entraînement en raison de sa taille et de ses structures anatomiques qui ressemblent beaucoup à celles des humains17. Sa taille substantielle permet l’utilisation de tous les équipements et appareils conçus pour des applications humaines. De plus, ses caractéristiques anatomiques offrent aux jeunes médecins de précieuses opportunités pour pratiquer le contrôle de la duodénoscopie. Parmi les modèles animaux existants, les porcs sont particulièrement adaptés à l’entraînement aux techniques de multi-scopie. Pendant l’opération, aucune stratégie de gestion de la douleur n’a été utilisée ; Par conséquent, le porc n’a montré aucune réactivité tandis que la fréquence cardiaque et la respiration sont restées stables tout au long de la procédure. Le processus d’euthanasie a été mené rapidement et efficacement à l’aide d’une injection de 20 ml de chlorure de potassium sous anesthésie.
Cependant, ce modèle de porc présente plusieurs limitations. Tout d’abord, les coûts associés sont élevés. Les principales dépenses de ce modèle proviennent de l’achat de porcs, ainsi que de l’équipement et des appareils nécessaires, ce qui peut entraver son adoption généralisée. Deuxièmement, le porc est destiné à un usage unique. En raison des expériences in vivo menées dans des conditions physiologiques et des dommages opérationnels infligés au système biliaire, il est difficile d’utiliser des porcs pour des études ultérieures. Par conséquent, cela contribue également à l’augmentation des coûts expérimentaux. De plus, ce modèle de porc ne représente pas fidèlement un modèle de cholélithiase. La localisation d’un porc atteint de cholélithiase d’origine naturelle pose des difficultés importantes ; De plus, la création d’un modèle de porc artificiel de cholélithiase peut ne pas être autorisée selon les règlements du comité de protection des animaux. Néanmoins, il reste le modèle idéal pour l’entraînement en multi-scopie pour la cholélithiase en raison de sa taille appropriée et de sa similitude avec les structures physiologiques et anatomiques humaines. Même en l’absence de calculs dans le canal biliaire, la procédure de traitement d’entraînement pour la cholélithiase peut toujours être effectuée efficacement.
Le modèle pourrait être amélioré à l’avenir en utilisant des organes abdominaux entiers provenant d’abattoirs, soutenus par des systèmes de circulation artificielle à l’intérieur d’une boîte humide pour simuler des conditions physiologiques et anatomiques. On s’attend à ce que cette approche soit plus rentable. Grâce aux progrès de la technologie et de l’intelligence artificielle18, il est possible de créer un simulateur artificiel de formation à la multi-endoscopie à l’aide de la réalité virtuelle ou augmentée19,20. Cette évolution transforme fondamentalement la question de la non-réutilisabilité associée au modèle actuel.
Le modèle de formation aux techniques combinées de multi-scopie dans le traitement de la cholélithiase est une méthode d’enseignement innovante et pratique. Il est utile pour améliorer les compétences des jeunes médecins et la capacité d’application de la technologie combinée multi-scopie. Cette méthode fournit une expérience pratique précieuse aux professionnels de la santé pour améliorer leurs compétences dans le traitement de la cholélithiase.
Déclarations de divulgation
Les auteurs n’ont aucun conflit d’intérêts ou lien financier à divulguer.
Remerciements
Nous remercions le Centre d’éducation technique OLYMPUS China (Guangzhou) pour son aide dans le cadre de l’étude.
matériels
| Name | Company | Catalog Number | Comments |
| Anesthesia machine | Mindray | WATO EX-20 | |
| Choledochoscope | OLMPLUS | CHF-V2 | |
| Duodenoscopy | OLMPLUS | TJF-260V | |
| Electric hook | OLMPLUS | A6292 | |
| Electrocardiogram monitor | Mindray | iMEC12 | |
| Electrocoagulation system | OLMPLUS | ESG-400/USG-400 | |
| Guidewire | OLMPLUS | G-240-3527A | |
| Laparoscopic gastric forceps | OLMPLUS | WA64130L | |
| Laparoscopic needle holder | OLMPLUS | WA64700A | |
| Laparoscopic separation forceps | OLMPLUS | WA64320A | |
| Laparoscopy | OLMPLUS | OTV-S400 | |
| Sphincterotome | OLMPLUS | KD-V431M-0720 | |
| Trocar (5.5 mm, 12 mm) | OLMPLUS | 5.5-A5809/12-A5859 | |
| Ultrasonic scalpel and equipment | OLMPLUS | TB-0520FCS/TD-TB400 | |
| Veress needle | OLMPLUS | SD-301 | |
| Vicryl Plus 5-0 | ETHICON | VCP433H | |
| Video recording system | OLMPLUS | IMH-20 |
Références
- Lammert, F., et al. Gallstones. Nat Rev Dis Primers. 2, 16024 (2016).
- Lammert, F., Wittenburg, H. Gallstones: Prevention, diagnosis and treatment. Semin Liver Dis. 44 (3), 394-404 (2024).
- Collins, C., Maguire, D., Ireland, A., Fitzgerald, E., O'sullivan, G. C. A prospective study of common bile duct calculi in patients undergoing laparoscopic cholecystectomy: Natural history of choledocholithiasis revisited. Ann Surg. 239 (1), 28-33 (2004).
- Caddy, G. R., Tham, T. C. Gallstone disease: Symptoms, diagnosis and endoscopic management of common bile duct stones. Best Pract Res Clin Gastroenterol. 20 (6), 1085-1101 (2006).
- Fujita, N., et al. Evidence-based clinical practice guidelines for cholelithiasis 2021. J Gastroenterol. 58 (9), 801-833 (2023).
- Dahiya, D. S., et al. Understanding evidence-based clinical practice guidelines for cholelithiasis 2021. Hepatobiliary Surg Nutr. 13 (2), 352-355 (2024).
- Fried, G. M. Lessons from the surgical experience with simulators: Incorporation into training and utilization in determining competency. Gastrointest Endosc Clin N Am. 16 (3), 425-434 (2006).
- Kachaamy, T. A., Faigel, D. O. Improving ERCP quality and decreasing risk to patients and providers. Expert Rev Gastroenterol Hepatol. 7 (6), 531-540 (2013).
- Loganathan, P., et al. Trainee involvement and ERCP complications: A systematic review and meta-analysis. Dig Dis Sci. 69 (7), 2363-2369 (2024).
- Zhang, Z., et al. Strategies of minimally invasive treatment for intrahepatic and extrahepatic bile duct stones. Front Med. 11 (4), 576-589 (2017).
- Lv, F., et al. Single-stage management with combined tri-endoscopic approach for concomitant cholecystolithiasis and choledocholithiasis. Surg Endosc. 30 (12), 5615-5620 (2016).
- Sahakian, A. B., et al. Can a computerized simulator assess skill level and improvement in performance of ERCP. Dig Dis Sci. 61 (3), 722-730 (2016).
- Velazquez-Avina, J., Sobrino-Cossio, S., Chavez-Vargas, C., Sulbaran, M., Monkemuller, K. Development of a novel and simple ex vivo biologic ERCP training model. Gastrointest Endosc. 80 (6), 1161-1167 (2014).
- Deie, K., et al. Evaluation of minimally invasive surgical skills training: Comparing a neonatal esophageal atresia/tracheoesophageal fistula model with a dry box. Surg Endosc. 36 (8), 6035-6048 (2022).
- Zhang, H., et al. Development of a continuously perfused ex vivo kidney training model for laparoscopic partial nephrectomy: Validity and efficiency. Int J Surg. 109 (12), 3919-3928 (2023).
- Phillips, M. S., Marks, J. M. Overview of methods for flexible endoscopic training and description of a simple explant model. Asian J Endosc Surg. 4 (2), 45-52 (2011).
- Jeong, S., Park, J. S., Lee, D. H. Large animal models in pancreas and biliary disease. Korean J Gastroenterol. 77 (3), 99-103 (2021).
- Ryder, C. Y., et al. Using artificial intelligence to gauge competency on a novel laparoscopic training system. J Surg Educ. 81 (2), 267-274 (2024).
- Bogar, P. Z., et al. Validation of a novel, low-fidelity virtual reality simulator and an artificial intelligence assessment approach for peg transfer laparoscopic training. Sci Rep. 14 (1), 16702 (2024).
- Koch, K., et al. Development and evaluation of artificial organ models for ERCP training in patients with surgically altered anatomies. Sci Rep. 13 (1), 22920 (2023).
Réimpressions et Autorisations
Demande d’autorisation pour utiliser le texte ou les figures de cet article JoVE
Demande d’autorisationExplorer plus d’articles
This article has been published
Video Coming Soon