Quadruples clusters métalliques
Vue d'ensemble
Source : Corey Burns, Tamara M. Powers, département de chimie, Texas A & M University
Roue à aubes complexes sont une classe de composés composé deux ions métalliques (1st, 2èmeou 3rd row les métaux de transition) qui s’est tenues à proximité de quatre ligands pontants (plus communément formamidinates ou carboxylates) (Figure 1). Variant de l’identité de l’ion métallique et le ligand passerelle donne accès aux grandes familles de roue à aubes complexes. La structure des complexes de la roue à aubes permet la liaison métal-métal, qui joue un rôle essentiel dans la structure et la réactivité de ces complexes. En raison de la diversité des structures électroniques qui sont disponibles à la roue à aubes complexes - et les différences correspondantes dans M-M liaison affichée par ces structures - roue à aubes complexes ont trouvé application dans divers domaines, tels que dans homogène catalyse et comme blocs de construction pour cadres métallo-organiques (MOF). Comprendre la structure électronique des liaisons M-M dans les complexes de la roue à aubes est essentielle à la compréhension de leurs structures et donc à l’application de ces complexes en chimie de coordination et de la catalyse.
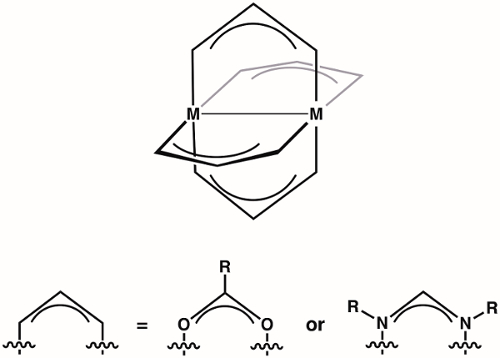
Figure 1. Structure générale des complexes de roue à aubes, où M peut être un 1st, 2èmeou 3rd row métal de transition.
Quand deux métaux de transition ont lieu à proximité de la d-recouvrement d’orbitales, qui peut entraîner la formation de liaisons M-M. Chevauchement des d -orbitales peut former trois types de liaisons - σ et π δ - selon la symétrie des orbitales impliquées. Si nous attribuons l’axe des z moléculaire pour être coplanaire avec le lien de M-M, une liaison σ est formée par la superposition des orbitales dz2 et liaisons π sont formées par le recouvrement des orbitales dyz dxz . Obligations δ sont générées par superposition des d-orbitales disposant de deux nœuds planaires (dxy et dx2-y2). En conséquence, tous les quatre lobes de la d-recouvrement d’orbitales et la liaison δ correspondant a deux nœuds planes (Figure 2). En théorie, avec l’ajout d’obligations δ, roue à aubes complexes sont capables de supporter des obligations quintuples, ou cinq liaisons entre atomes métalliques. 1 dans la plupart des complexes, le dx2-y2 forme des liaisons métal-ligand fortes et ne contribuent pas utilement au collage de M-M. Ainsi, les liaisons quadruples sont l’ordre de liaison maximale dans les nombreux complexes.
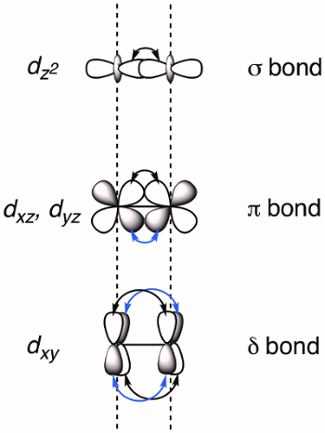
Figure 2. Représentation visuelle de σ et π δ collage MOs résultant de la combinaison linéaire de métal d-orbitales. Les orbitales atomiques dz2 ont le meilleur chevauchement spatial, suivi du dxz et les orbitales dyz . Les orbitales atomiques dxy ont le moins de chevauchement spatial.
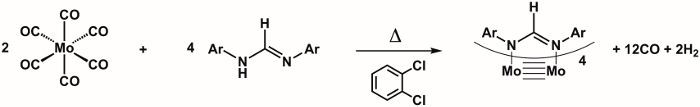
Dans cette vidéo, nous résumera la roue à aubes dimolybdenum Mo complexe2(ArNC(H)NAr)4, où Ar = p-(MeO) C6H4, qui dispose d’une liaison quadruple. Nous caractériser le composé par spectroscopie RMN et cristallographie aux rayons x permet d’étudier le lien M-M.
Procédure
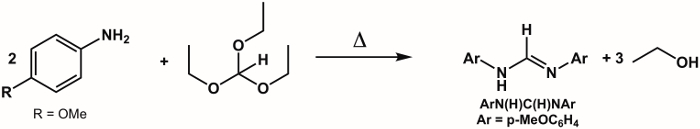
1. synthèse du Ligand ArN (H) C (H) NAr, où Ar = p-(MeO) C6H4 (Figure 5)2
- Combiner les 6,0 g (0,050 mol) de p -anisidine et 4,2 mL (0,025 mol) de triethylorthoformate dans un 100 mL ballon à fond rond avec une barre d’agitation magnétique.
- Fixez une tête de distillation sur le ballon à réaction.
- En remuant, faites chauffer la réaction dans un bain d’huile à reflux (120 ° C). Une fois que le reflux e
Résultats
Ligand ArN (H) C (H) NAr
Rendement : 3,25 g (53 %). 1 H RMN (chloroforme -d, 500 MHz, δ, ppm) : 8.06 (s, 1 H, NHC -HN), 6.99 (d, 4 H, aromatiques C -H, J = 8,7 Hz), 6,86 (d, 4 H, aromatiques C -H, J = 9,0 Hz), 3,80 (s, 6 H, - OCH3).
Mo Mo complexe2(ArNC(H)NAr)-4
Rendement?...
Applications et Résumé
Dans cette vidéo, nous avons appris sur la liaison de M-M. Nous avons synthétisé un molybdène dinuclear complexe comportant une liaison quadruple. Les liaisons quadruples se composent de trois types d’obligations différentes, y compris les liaisons σ et π δ. Nous avons recueilli des données de diffraction des rayons x sur un cristal unique et observé une courte longueur de la liaison Mo-Mo compatible avec un composé quadruply servile.
Roue à aubes complexes, tels que le Mo2<...
References
- Nguyen, T., Sutton, A. D., Brynda, M., Fettinger, J. C., Long, G. J., Power, P. P. Synthesis of a stable compound with fivefold bonding between two chromium(I) centers. Science. 310(5749), 844-847 (2005).
- Lin, C., Protasiewicz, J. D., Smith, E. T., Ren, T. Linear free energy relationship in dinuclear compounds. 2. Inductive redox tuning via remote substituents in quadruply bonded dimolybdenum compounds. Inorg Chem. 35(22), 6422-6428 (1996).
- Cotton, F. A., Murillo, C. A., Walton, R. A. Eds. Multiple Bonds Between Metal Atoms, 3rd ed. Springer. New York, NY. (2005).
- Nakamura, E., Yoshikai, N., Yamanaka, M. Mechanism of C−H Bond Activation/C−C Bond Formation Reaction between Diazo Compound and Alkane Catalyzed by Dirhodium Tetracarboxylate. J Am Chem Soc. 124 (24), 7181-7192 (2002).
Passer à...
Vidéos de cette collection:

Now Playing
Quadruples clusters métalliques
Inorganic Chemistry
15.3K Vues

Synthèse d'un métallocène de Ti(III) avec une ligne Schlenk
Inorganic Chemistry
31.6K Vues

Boîte à gants et capteurs d'impuretés
Inorganic Chemistry
18.6K Vues

Purification du Ferrocène par sublimation
Inorganic Chemistry
54.7K Vues

La méthode Evans
Inorganic Chemistry
68.6K Vues

Diffraction par rayons X : cristal vs poudre
Inorganic Chemistry
104.7K Vues

Spectroscopie par résonance paramagnétique électronique (RPE)
Inorganic Chemistry
25.5K Vues

Spectroscopie Mössbauer
Inorganic Chemistry
22.0K Vues

Interaction des acides et bases de Lewis au sein du complexe Ph3P-BH3
Inorganic Chemistry
38.9K Vues

Structure du ferrocène
Inorganic Chemistry
79.6K Vues

Application de la théorie des groupes à la spectroscopie IR
Inorganic Chemistry
45.5K Vues

Théorie de l’orbital moléculaire (OM)
Inorganic Chemistry
35.4K Vues

Capteurs solaires teintés
Inorganic Chemistry
15.8K Vues

Synthèse d'un complexe de cobalt(II) porteur d'oxygène
Inorganic Chemistry
51.7K Vues

Initiation photochimique des réactions de polymérisation radicalaire
Inorganic Chemistry
16.8K Vues