Method Article
אופטימיזציה של צמיחת קריסטל עבור קריסטלוגרפיה מקרומולקולרית נויטרון
In This Article
Summary
מחקרים מבניים של ביומקרומולקולים על ידי קריסטלוגרפיה דורשים גבישים באיכות גבוהה. כאן אנו מדגימים פרוטוקול שיכול לשמש את OptiCrys (מכשיר אוטומטי לחלוטין שפותח במעבדה שלנו) ו/או כפתורי מיקרו-דיאליזה לגידול גבישים גדולים ואיכותיים המבוססים על ידע בדיאגרמת שלב ההתגבשות.
Abstract
השימוש בקריסטלוגרפיה מקרומולקולרית נויטרונית (NMX) מתרחב במהירות עם רוב המבנים שנקבעו בעשור האחרון הודות לקורות NMX חדשות שנבנו וזמינות מוגברת של תוכנה לעידון מבנים. עם זאת, מקורות הנויטרונים הזמינים כיום עבור NMX חלשים משמעותית ממקורות מקבילים עבור קריסטלוגרפיה של קרני רנטגן. למרות ההתקדמות בתחום זה, גבישים גדולים משמעותית תמיד יידרשו למחקרי עקיפת נויטרונים, במיוחד עם הנטייה ללמוד מקרומולקולות ומורכבויות גדולות יותר ויותר. שיפורים נוספים בשיטות ומכשור המתאימים לגידול גבישים גדולים יותר נחוצים אפוא לשימוש ב- NMX כדי להתרחב.
בעבודה זו, אנו מציגים אסטרטגיות רציונליות וספסל צמיחת קריסטל (OptiCrys) שפותח במעבדה שלנו המשלב תצפית בזמן אמת באמצעות מצלמת וידאו המותקנת על מיקרוסקופ עם שליטה אוטומטית מדויקת בפתרונות התגבשות (למשל, ריכוז משקעים, pH, תוסף, טמפרטורה). לאחר מכן אנו מדגימים כיצד שליטה זו בטמפרטורה ובהרכב הכימי מקלה על החיפוש אחר תנאי התגבשות אופטימליים באמצעות חלבונים מסיסים במודל. ידע מעמיק בדיאגרמת שלב ההתגבשות חיוני לבחירת מיקום ההתחלה והנתיב הקינטי לכל ניסוי התגבשות. אנו מראים כיצד גישה רציונלית יכולה לשלוט בגודל ובמספר הגבישים הנוצרים בהתבסס על ידע בדיאגרמות פאזה רב-ממדיות.
Introduction
הבנת הקשר המבני-פונקציה של חלבונים ואת המנגנון של מסלולים פיזיולוגיים לעתים קרובות מסתמך על לדעת את העמדות של אטומי מימן (H) וכיצד תשלום מועבר בתוך חלבון1,2. מאז אטומי מימן לפזר קרני רנטגן חלש, עמדותיהם ניתן לקבוע רק עם נתוני עקיפת רנטגן ברזולוציה גבוהה מאוד (>1 Å)3,4. לעומת זאת, ניתן להשתמש בקריסטלוגרפיה של נויטרונים כדי להשיג מיקום מדויק של אטומי מימן במקרומולקולות ביולוגיות כמימן ודיטריום (H2, איזוטופ של מימן) אטומי פיזור בסדר גודל שווה בערך כמו חמצן, חנקן ופחמן5. עם זאת, שטף נויטרונים ממקורות נויטרונים זמינים חלש יותר מזה של קרני רנטגן, ולכן זה חייב להיות מתוגמל לעתים קרובות עבור2,3. זה יכול להיות מושגת על ידי החלפת H עם H2 ו / או הגדלת נפח הגבישים כדי להפחית את פיזור לא קוהרנטי של מימן ולהגדיל את יחס אות לרעש של תמונות עקיפה.
ישנן גישות התגבשות שונות (דיאגרמת הפאזה הסכימטית המתאימה מוצגת באיור 1) להשגת גבישים גדולים ואיכותיים הן עבור רנטגן והן עבור גבישים ביו-מקרומולקולריים נויטרונים6. ב דיפוזיה אדים, טיפה שהוכנה מתערובת של חלבון ותמיסת התגבשות משתווה לאורך זמן, באמצעות אידוי של מים או מינים נדיפים אחרים, כנגד מאגר המכיל ריכוז גבוה יותר של משקעים של אותו פתרון התגבשות. העלייה בריכוז החלבון והמשקעים בטיפה מובילה לתרופה הנדרשת לגרעין ספונטני ואחריו צמיחת גביש בגרעינים אלה6,7. למרות דיפוזיה אדים היא הטכניקה הנפוצה ביותר לגידול גבישים 4 ,תהליךהתגבשות לא ניתן לשלוט במדויק8. בשיטת דיפוזיה ממשק חינם, פתרון התגבשות מתפזר לתוך פתרון חלבון מרוכז, לאט מאוד מכוון את המערכת לכיוון רוויה. שיטה זו יכולה להיחשב כשיטת אצווה עם קצב ערבוב איטי6,9,10,11,12. בשיטת האצווה, החלבון מעורבב במהירות עם פתרון התגבשות המוביל רוויה מהירה בתורו התגרענות אחידה עם גבישים רבים3,7. שיטה זו מהווה כשליש מכלל המבנים המופקדים כיום בבנק נתוני החלבון. שיטת הדיאליזה משמשת גם לגידול גבישי חלבון איכותיים ומפזרים היטב. בשיטת הדיאליזה, מולקולות של משקעים מפוזרות ממאגר דרך קרום חדיר למחצה לתא נפרד עם תמיסת החלבון. הקינטיקה של שיווי משקל תלויה בגורמים שונים, כגון טמפרטורה, גודל נקבוביות קרום, ואת נפח וריכוז של דגימות חלבון וסוכני התגבשות6.
דיאגרמות שלב התגבשות ניתן להשתמש כדי לתאר מצבים שונים של חלבון כפונקציה של משתנה פיזי או כימישונה 3. כפי שמודגם באיור 1, ניתן לדמיין כל טכניקת התגבשות כשימוש במסלול קינטי שונה כדי להגיע לאזורי התגרענות והמטא-נתונים שלדיאגרמה 6,10,13. זה מספק מידע על מסיסות חלבון וריכוז החלבון שבו שיווי משקל תרמודינמי בין גביש ותמיסה הוא ציין, ובכך למצוא את התנאים האופטימליים עבור התגרענות וצמיחה3,14. בדיאגרמת פאזה דו מימדית, ריכוז החלבון מותווה כפונקציה של משתנה אחד והמשתנים האחרים נשמריםקבועים 15. בתרשים פאזה כזה, כאשר ריכוז החלבון נמצא מתחת לעקומת המסיסות, הפתרון נמצא באזור התת-רווי ולא מתרחשת גרעין או צמיחת גביש. מעל עקומה זו נמצא אזור רוויה-העל שבו ריכוז החלבון גבוה ממגבלת המסיסות3,14. זה מחולק עוד יותר לשלושה אזורים: האזור metastable, אזור הגרעין הספונטני, ואת אזור המשקעים. באזור metastable, רוויה אינה מספיקה עבור התגרענות להתרחש בתוך זמן סביר אבל צמיחה של גבישים זרע יכול להתרחש. צבירה ומשקעים מועדפים באזור המשקעים, שבו רוויה גבוהה מדי14,15.
כאשר מספיק רוויה לגרעין ספונטני מושגת, הגרעינים הראשונים יופיעו10. צמיחת הגבישים מובילה לירידה בריכוז החלבון עד להגבלת המסיסות. כל עוד רוויה-על נשארת בקרבת עקומת המסיסות, לא יהיה שינוי משמעותי בגודל הגבישים. עם זאת, הוכח כי וריאציות בטמפרטורה ובהרכב הכימי של פתרון התגבשות (לדוגמה, ריכוז המשקעים) ישפיעו על מסיסות החלבון ועלולות להוביל ליזום צמיחת גביש נוספת8,13,16.
מכיוון שהדיאליזה מועילה לצמיחת קריסטל באיכות טובה, ספסל התגבשות OptiCrys המאויר באיור 2, תוכנן ופותח במעבדה שלנו כדי לשלוט בהתגבשות באופן אוטומטי לחלוטין8. לשם כך נכתבה תוכנה עם LabVIEW המאפשרת בקרה וניטור של הטמפרטורה של מערך דיאליזה של מאגר זורם במגע עם אלמנטים פלטייה, באמצעות בקר אלקטרוני וצ'ילר. אותה תוכנה גם מסדירה באופן אוטומטי את ההרכב הכימי של פתרון התגבשות (למשל חילופי סוכני התגבשות) באמצעות מערכת נוזלית רב ערוצית. בנוסף, מצלמה דיגיטלית ומיקרוסקופ הפוך משמשים כדי לדמיין ולתעד את תהליך ההתגבשות. שני תאי התגבשות עם 15 μL ו 250 נפחי μL זמינים לגידול גבישים למטרות שונות. כמו תהליך התגבשות הוא הפיך, הקרנה עבור תנאים שונים אפשרי עם רק כמה microliters של פתרון החלבון כל עוד המדגם אינו פגום8. כתוצאה מכך, שימוש בשיטה זו ממזער את כמות חומר החלבון המשמש.
מעבודהקודמת 8, ברור כי במהלך תהליך צמיחת הגביש, תצפיות situ צריך להתבצע במרווחי זמן קבועים. אלה יכולים לנוע בין כמה שניות למספר ימים, בהתאם לאירוע תחת השגחה (משקעים, התגרען או צמיחת גביש).
האופטימיזציה של צמיחת גביש עם OptiCrys מבוססת על דיאגרמות שלב ריכוז משקעים בטמפרטורה. במקרה של חלבונים עם מסיסות כתפקוד ישיר של הטמפרטורה, ניתן לעשות שימוש במשטר המלחה החוצה18. זה המקום שבו הגדלת הכוח היוני של הפתרון, אשר ניתן לדמיין באמצעות דיאגרמות שלב משקעים חלבון, מקטין את המסיסות של החלבון. כמו כן, חלבונים עם מסיסות הפוכה יכולים לעשות שימוש במשטרהמלחה 18. התגרענות מתרחשת באזור התגרענות, בקרבת האזור metastable, וצמיחת גביש ואז מתרחשת באזור metastable של דיאגרמת השלב עד ריכוז החלבון מגיע לגבול המסיסות. כפי שמוצג באיור 3A, ניתן להקטין את טמפרטורת ההרכב הכימי המתמדת כדי לשמור על פתרון ההתגבשות באזור המטה-שולחן כדי למנוע התגרענות חדשה. גבישים לגדול עד שיווי המשקל הגביש השני / פתרון מושגת ולאחר מכן, אין עלייה נוספת בגודל של גבישים נצפתה. הטמפרטורה יורדת מספר פעמים עד שהקריסטלים מגיעים לגודל הרצוי. באיור 3B, בטמפרטורה קבועה, הגדלת ריכוז המשקעים שומרת על הפתרון באזור המטא-שולחן. לאחר מכן ניתן לחזור על תהליך זה מספר פעמים כדי להשיג גבישים גדולים. שינוי הטמפרטורה ומניפולציה של תנאי פתרון התגבשות, על ידי שליטה על רמות רוויה, הם שני כלים רביעוצמהלהפרדת התגרענות וצמיחה של גבישים הנשלטים באופן מדויק וא אוטומטי על ידי OptiCrys 5,8,14.
דוגמאות של גבישי חלבון הגדלים על ידי התגבשות מבוקרת טמפרטורה, או טמפרטורה ומשקעים מבוקר ריכוז, כמו גם נתוני עקיפה יחסית המתקבלים זמינים בספרות וב- PDB. ביניהם הם אדם γ גבישי E, PA-IIL לקטין, שמרים פירופוספטאז אנאורגניים, אורט אוקסידאז, אנהידראז פחמני אנושי II, YchB קינאז, לקטט דהידרוגנאז5,14,17,18.
למרות OptiCrys היה ממוסחר על ידי NatX-ray, ישנן מעבדות רבות שאין להם גישה למכשיר זה או לגישה הסדרתית שהיא מציעה. החלופה לטכניקה זו היא להשתמש בכפתורי מיקרו-דיאליזה פלסטיים זמינים מסחרית עם נפחים שונים. באמצעות אלה, טמפרטורה והרכב כימי ניתן להתאים ומגוון באופן ידני. בדיקה של כפתורי מיקרודיאליזה לא יכולה להיעשות באתרו ובמקום זאת יש לעשות זאת באופן ידני עם מיקרוסקופ אופטי. בקרת טמפרטורה יכולה להיות מושגת על ידי שמירה על המדגם באינקובטור מבוקר טמפרטורה ללא רטט. זה חיוני כדי לשמור על הטמפרטורה קבועה כדי להבטיח כי ניסויים התגבשות הם לשחזור. שינוי משמעותי בטמפרטורה עלול גם להוביל לנזק או הרס של גבישים5.
כאן אנו מספקים פרוטוקול מפורט המתאר הכנת מדגם ושימוש בתוכנת בקרה לצמיחה של גבישים גדולים ואיכותיים המתאימים לקריסטלוגרפיה של חלבון נויטרונים. הליך שלב אחר שלב זה נועד לנצל את דיאגרמת שלב ההתגבשות על מנת לבחור מיקום התחלתי ונתיב קינטי כדי לשלוט בגודל ובאיכות הגבישים הנוצרים. בנוסף, מוצג פרוטוקול מפורט לגידול גבישים עם כפתורי מיקרו-דיאליזה המשתמש באותו רציונל להשגת גבישים גדולים ואיכותיים.
Protocol
1. שיטת דיאליזה עם כפתורי מיקרו-דיאליזה
- הכנה לדוגמה
- הכן את פתרון החלבון על ידי המסת 30 מ"ג ליזוזים לבנים ביצה עוף כמו אבקה lyophilized ב 1 מ"ל של CH3מאגר COONa (100 מ"מ נתרן אצטט, pH 4) על מנת להשיג פתרון עם ריכוז סופי של 30 מ"ג·mL-1.
- צנטריפוגה המדגם ב 13,000 × גרם במשך 10 דקות ב 277 K. תהליך זה מסייע להסיר אגרגטים כלשהם לפני תחילת תהליך ההתגבשות.
- בדוק את ספיגת המדגם ב 280 ננומטר ולחשב את ריכוז החלבון באמצעות משוואת בירה למברט (A = εcl).
הערה: על פי משוואת באר למברט, ספיגה אלקטרונית (A) היא פרופורציונלית ישירות לריכוז (c,mg·mL-1)של מין סופג בהינתן אורך אופטי קבוע (l, cm). השיפוע של מערכת יחסים ליניארית זו הוא מקדם ההכחדה הטוחנת (ε, עבור lysozyme ב 280 ננומטר הוא 2.64 מ"ל·מ"ג-1·ס"מ-1)19. sidechains של חומצות אמינו ארומטיות (טירוזין, טריפטופן, פנילאלנין) וקשרים disulfide בין שאריות ציסטאין יש ספיגה חזקה ב ~ 280 ננומטר הנובעים π מותר ספקטרוסקופית – π * מעברים. כמו רוב החלבונים מכילים שאריות אלה, ריכוז החלבון בדרך כלל ניתן לחשב בקלות על ידי מדידת הספיגה ב 280 ננומטר, בהתחשב בידע של מקדם ההכחדה. - הכינו פתרונות התגבשות כפי שמוצג באיור 4. לסנן את כל פתרונות המלאי עם מסנני 0.22 מיקרומטר מיליפור לפני הכנת פתרון התגבשות.
- צמיחת קריסטל
- חותכים קרום דיאליזה תאית עם חיתוך משקל מולקולרי מתאים (6-8 kDa) ולהשרות אותו במים מזוקקים.
הערה: דיסקים קרום דיאליזה זמינים מסחרית עבור כפתורי מיקרודיאליזה, אבל אם צינורות דיאליזה משמש, לא לשכוח לחתוך את הקצוות על מנת להפריד את שתי שכבות של קרום מן הצינור יש רק קרום שכבה אחת. - מלאו בארות של מגש של 24 בארות עם 2 מ"ל של פתרון התגבשות באותו סדר כפי שמוצג באיור 4.
הערה: אם נעשה שימוש בלחצנים עם אמצעי אחסון גדולים יותר (למשל, 200 μL), מלא צינורות 50 מ"ל במינימום של פתרון התגבשות של 5 מ"ל על מנת להבטיח החלפה יעילה. - הוסף/פיפטה 35 μL של פתרון lysozyme לתא של כפתור המיקרו-דיאליזה כפי שמודגם באיור 5A.
הערה: כדי למנוע היווצרות של בועות אוויר בלחצן דיאליזה μL 30 כאשר הוא סגור, נפח נוסף (נפח מת) של 5 μL של חלבון נוסף יש להוסיף, כלומר סך של 35 μL של דגימת חלבון. דגימת חלבון נוספת זו יוצרת צורה מעט כיפת על גבי התא, כפי שמוצג באיור 5B, המונע היווצרות של בועות אוויר. - קחו מוליך בגודל המתאים והניחו את ה-O-ring האלסטי בקצהו (איור 5C). לאחר מכן הניחו את הממברנה, שבעבר ניגבה /רוקנה קלות באמצעות פיסת נייר נטולת סיבים, על גבי התא של כפתור הדיאליזה. היזהר לא לשים אבק בתא בעת החלת הנייר. הגדר את קרום הדיאליזה במקומו על-ידי העברת ה- O-ring האלסטי מהמוליך לגרוב של לחצן הדיאליזה (איור 5C).
הערה: הרגע הקריטי של הטיפול הוא תיקון קרום הדיאליזה על גבי התא על ידי העברת O-ring אלסטי מן המוליך לתוך החריץ של כפתור הדיאליזה. כל התנועות חייבות להיות מסונכרנות בצורה מושלמת כדי למנוע צירוף בועות אוויר עם המדגם בתא החלבון. כדאי לתרגל מתיחת O-ring אלסטי לפני היישום שלה כדי לדעת את קשיחותה, להשתמש פינצטה להחזיק חלק הממברנה במהלך היישום שלה ולבצע את הניסויים הבדיקה הראשונה עם חלבון מודל. - מעבירים את הלחצן לבאר או לצינור של 50 מ"ל באמצעות פינצטה(איור 5D).
- מכסים את הבאר בעזרת כיסוי ולוחצים עליה בעדינות על השומן כדי לאטום את הבאר(איור 5E).
הערה: אם אין גריז על גבי בארות, הקפד להוסיף את זה לפני תחילת הניסוי או להשתמש חתיכת קלטת במקום כיסוי זכוכית. העיקרון של התגבשות חלבונים באמצעות כפתורי מיקרו-דיאליזה מאויר באיור 5. - שמור את הדגימה ב 293 K באינקובטור תרמורגולטי. טמפרטורות שונות עשויות להיות נחוצות בהתאם לתנאי החלבון וההתגבשות המשמשים.
הערה: ניתן לסנן את אותה רשת של תנאי התגבשות המוצגים באיור 4 (המאפשרת את המגוון של המשקעים) כפונקציה של טמפרטורה. במקרה כזה, יש לשכפל את אותה צלחת התגבשות ויש למקם כל עותק באינקובטור המוסדר בטמפרטורה שונה. זה דורש שיש כמה אינקובטורים תרמורגולציה ללא רטט זמין. - בדקו אם יש גבישים במגש או בצינורות (איור 4)ורשמו הערות על בסיס קבוע, בדרך כלל מדי יום, כדי להבחין מה יש בכל מגש. הערות טובות חיוניות כדי למנוע תוצאות חיוביות שגויות להפלות אבק מגבישים.
- חותכים קרום דיאליזה תאית עם חיתוך משקל מולקולרי מתאים (6-8 kDa) ולהשרות אותו במים מזוקקים.
2. תהליך צמיחת קריסטל באמצעות OptiCrys
- הכנה לדוגמה
- הכינו תמיסת חלבון וקרום דיאליזה כמתואר בסעיף 1.1.
- הכן פתרונות מלאי של NaCl (4 M) ושל CH3COONa pH 4 (1 M) וסנן אותם לתוך צינורות 50 מ"ל.
- הוסיפו את תמיסת החלבון (15 μL של lysozyme עם 30 מ"ג מ"ל-1)לתא הדיאליזה של מערך דיאליזה מאגר זורם מבוקר טמפרטורה. עיין באיור 6 לקבלת פרטים על הגדרת דיאליזה של מאגר זורם מבוקר טמפרטורה. OptiCrys יש שני תאי דיאליזה, נפח המינימום הוא 15 μL ואת הנפח המרבי הוא 250 μL.
- מכסים את הישפן עם קרום דיאליזה ולתקן את הממברנה עם O-ring אלסטי (איור 6B).
הערה: התקנה זו שונה מכפתורי מיקרו-דיאליזה שבהם כל תא אטום ישירות על ידי קרום דיאליזה. בתא הזרימה, קרום הדיאליזה קבוע במקום זאת לשיפוע המאפשר הרכבה של גבישים ללא הסרתו. לשם כך, overchamber יכול פשוט להיות מופץ מהמאגר. - הופכים את הישן ומניחים אותו על תא הדיאליזה. לחץ עליו באיטיות ובעדינות כדי להסיר את כל האוויר הלכוד בין שני החלקים ולהימנע מבועות בתא(איור 6C). תרגול עם חלבון מודל יכול להיות יתרון בעת אימון כדי למנוע בועות אוויר ואובדן מדגם.
- לתקן את המאגר במקומו על ידי בעדינות דופק אותו על גבי overchamber, שוב להיות מודע כדי למנוע לכידת בועות אוויר. הידוק יתר של המאגר יכול גם ליצור בועות בתא ההתגבשות(איור 6D).
- מוסיפים את תמיסת ההתגבשות ומכסים את תא המאגר בכובע אטום. (איור6G). הנפח המרבי של המאגר הוא 1 מ"ל.
- העבר הרכבה זו והכנס אותה לתמיכת הפליז. תמיכה זו נמצאת במגע עם אלמנטים Peltier המשמשים כדי לשלוט על הטמפרטורה.
- כפי שמודגם באיור 6, המכסה האטום מצויד בחלון אופטי כדי לאפשר תאורה עליונה של תא הדיאליזה. הנח את מקור האור (איור 2) על החלון כדי לאפשר לאור לעבור דרך התא.
- תא המאגר יכול להיות מחובר למשאבה כדי לאפשר לו לתפקד כתא זרימה רציף. חברו את הצינור מעל צינורות ה-50 מ"ל המכילים את פתרונות המלאי והמים המזוקקים לשסתום הסיבובי כפי שמודגם באיור 7.
הערה: אם הכנה אוטומטית ושינוי של פתרונות התגבשות אינם רצויים במהלך הניסוי, השמט את שלב 2.1.10. במקרה כזה, יש להכין את פתרון ההתגבשות ולמלא את המאגר באופן ידני.
- תוכנה
- הפעל את המחשב ולהפעיל את התוכנה קרואסון קריסטלין [צמיחת קריסטל]. תוכנת בקרה זו נכתבת עם LabVIEW (http://www.ni.com/labview/) ומציעה ממשק גרפי ידידותי למשתמש. הוא כולל 4 ממשקים גרפיים שונים(Accueil [ברוכים הבאים], פרמטראז' [הגדרה], אסאי [בדיקה] ותחזוקה [תחזוקה]) (איור 8).
הערה: תרגומים מצרפתית נמצאים בסוגריים מרובעים. - בחרו בתצוגת 'תחזוקה' בלחיצה על הלחצן כפי שמודגם באיור 8. תצוגה זו היא כיום הנפוצה ביותר ומאפשרת למשתמשים לשלוט ברוב הפרמטרים במהלך הניסוי.
הערה: לאחר לחיצה על תצוגת תחזוקה, יופיע חלון חדש עם מקטעים שונים לשליטה בפרמטרים כגון טמפרטורה או אור. באיור 8 חלקים שונים של תצוגה זו מוצגים עם חצים ומסגרות. בשלבים הבאים, אנו מדגימים כיצד כל פרמטר נשלט באמצעות התוכנה. - סעיף Régulateur de température [בקר טמפרטורה] מאפשר שליטה וניטור של הטמפרטורה. לחצו על הכפתור, מספר אחד (1) באיור 8, כדי להפעיל אותו.
הערה: טווח הטמפרטורות ב OptiCrys הוא 233.0 – 353.0 ± 0.1 K. - קבעו את הטמפרטורה במקטע [setpoint] והקישו enter (איור 8(2). מתחת ללחצן זה, יש גרף עם 2 עקבות (אדום וצהוב). העקבות האדומות מראות את הטמפרטורה הסופית (מסודרת) והעקבות הצהובות מראות את הטמפרטורה הנוכחית. כפי שמוצג באיור 8(2),הטמפרטורה נקבעת על 20 °C (69 °F).
הערה: על מנת לגדל גביש, כפי שמוסבר בחלק צמיחת הגביש, יהיה צורך לבחור טמפרטורות רבות. כדי לשנות את הטמפרטורה, הוסף כל טמפרטורה חדשה במקטע [setpoint] ולחץ על לחצן Enter בלוח המקשים. - הדליקו את האור על ידי הגברת הזוהר מהסעיף Lumières [אורות] באיור 8. בהירות נעה בין 0 ל 100, "0" מציין כי האור כבוי ב "100" האור מוגדר למקסימום של עוצמה ובהירות. על ידי הגדלת האור, בחלק מיקרוסקופ, אפשר לראות בתוך תא הדיאליזה. במהלך הניסוי, הבהירות בתא עשויה להשתנות; להתאים את הפרמטרים כדי לדמיין בבירור בתוך תא הדיאליזה. הגדלה ניתן גם להגדיל או להקטין באמצעות + ו - כפתורים מול "זום" לצפייה טובה יותר.
- בצד ימין של סעיף המיקרוסקופ, ישנם מספר חלקים לאחסון מידע רלוונטי עבור כל ניסוי התגבשות. כל משתמש יכול ליצור תיקיה לאחסון מידע על תנאי התגבשות, שמות חלבונים וחיתוך המשקל המולקולרי של קרום הדיאליזה המשמש (איור 8(3).
- המשתמש יכול להגדיר שם לניסוי פשוט על ידי הקלדתו בתיק Nom [שם התיקיה]. לחיצה על התיק [לחצן תיקיה] (מוצג עם מסגרת ירוקה באיור 8)פותחת חלון חדש. בחלון זה, יהיה קובץ טקסט המכיל את כל המידע המוגדר עבור הניסוי. בנוסף, תמונות עם חותמת זמן נשמרות בתיקיה זו לעיבוד עתידי.
- מהמקטע תמונות NB , בחר את מספר התמונות שיש לצלם במהלך הניסוי. ציין את מספר התמונות בחלונית השמאלית יחד עם מרווח הזמן הרצוי בין אלה (למשל, מינימום, שעה, יום). איור 8 מציג את כיוונון התוכנה כדי להקליט אפס תמונות בדקה.
הערה: השתמש בסעיף פומפה [משאבה] לערבוב פתרונות מלאי והזרקת פתרון התגבשות לתא המאגר. ראו סעיף 2.1.10 ואיור 7 לקבלת הסבר על העיקרון של מערכת ערבוב הנוזלים. - ריכוזי קלט של פתרונות המניות באטאפה 1 [שלב 1]: מניות פתרונות. לניסוי התגבשות בחלק הבא, NaCl 4 M ו CH3COONa 1 M pH 4 ישמש.
הערה: ריכוזי פתרונות המלאי נמצאים ביחידות טוחנות. - הגדר את הריכוז הסופי של כל פתרון. לדוגמה, 0.75 M עבור NaCl ו- 0.1 M עבור CH3COONa pH 4. הזן אותם בסעיף הריכוז הסופי (איור 8) ב- Etape 2 [שלב 2]: פתרון à préparer [פתרון להכנה]. לחצו על הלחצן Calcul [Compute], המוצג עם מסגרת אדומה באיור 8. הנפח הסופי של כל פתרון מלאי שישמש בערבוב יוצג בלוח עוצמת הקול מול כל לוח ריכוז.
- לחץ על כפתור ההכנה לנסר [הכנת שיגור] (איור 8). כפי שמודגם באיור 7, השסתום הסיבובי לוקח כל תמיסת מלאי ומזריק אותם לצינור הערבוב באמצעות מתג.
- לאחר הכנת פתרון ההתגבשות, לחצו על כפתור פתרון המנה [ערך פתרון] באטאפה 3 [שלב 3]: שטף מקטע המשאבה (מסגרת צהובה באיור 8). המתג משתנה כדי להזריק את פתרון ההתגבשות החדש מערבוב הצינור לתוך תא המאגר. כדי להפסיק את תהליך ההחלפה, לחץ על לחצן הפצת Arrêt [עצירת הפצה].
הערה: שים לב לתהליך ההתגבשות במהלך הניסוי ושנה פרמטרים כגון טמפרטורה, פתרון התגבשות וזום, בממשק הגרפי המתאים של תוכנת הפיקוח. על ידי שימוש בתוכנה אין צורך להסיר את המכסה האטום או את תא הזרימה במהלך הניסוי כך שהמשתנה היחיד יהיה זה שהמשתמש משתנה באמצעות התוכנה.
- הפעל את המחשב ולהפעיל את התוכנה קרואסון קריסטלין [צמיחת קריסטל]. תוכנת בקרה זו נכתבת עם LabVIEW (http://www.ni.com/labview/) ומציעה ממשק גרפי ידידותי למשתמש. הוא כולל 4 ממשקים גרפיים שונים(Accueil [ברוכים הבאים], פרמטראז' [הגדרה], אסאי [בדיקה] ותחזוקה [תחזוקה]) (איור 8).
- צמיחת גביש גדולה
- הוסף 15 μL של lysozyme עם ריכוז של 30 מ"ג מ"ל-1 לתא הדיאליזה (איור 6A).
הערה: הכינו את דגימת החלבון כמתואר בסעיף 1.1. - אספו את מערך הדיאליזה של המאגר הזורם מבוקר הטמפרטורה כמתואר בסעיף 2.1 ובאיור 6.
- הכינו את פתרון ההתגבשות. אל תשכח לסנן את כל פתרונות המלאי לפני הכנת מדגם עם מסנני 0.22 מיקרומטר. עבור ניסוי זה, פתרון התגבשות מכיל 0.75 M NaCl ו 0.1 M CH3COONa pH 4. ניתן להוסיף זאת באופן ידני או באמצעות תא המאגר ומערכת השאיבה כמתואר בסעיפים 2.2.10 עד 2.2.12.
- הגדר את הטמפרטורה ל- 295 K כפי שמוסבר בסעיפים 2.2.3 ו- 2.2.4 והוצג בתמונה 8. בתנאים ראשוניים, שיווי המשקל בין תא הדיאליזה למאגר יושג לאחר כ-90 דקות והגרעין הנראה הראשון יופיע לאחר 22 שעות.
- אפשרו לקריסטלים לצמוח עד שלא יתבוננו עוד שינויים גלויים בגודל הגבישים(איור 9, לוח 1).
הערה: כדי לקבוע את זמן הגרעין ולמדוד את השונות בגודל הגבישים, הקלט תמונות כל 15 או 20 דקות, שזה בהתאמה 4 או 3 תמונות לשעה במקטע תמונות NB. עבור במקום תצפית של denaturation חלבון, הצטברות ומשקעים או פירוק גביש או גרעינים, בדרך כלל בין כמה שניות לכמה עשרות דקות נדרשים. עם זאת, עבור צמיחת גביש, טווח זה הוא בין כמה דקות לכמה שעות. - לאחר שלושה ימים, להוריד את הטמפרטורה ל 291 K כדי להתחיל מחדש את צמיחת הגביש. שמרו על הטמפרטורה קבועה ותנו לקריסטל להתפתח(איור 9, פאנל 2). בשלב זה של הניסוי, זה יהיה מספיק כדי להקליט תמונות כל 2 שעות ולבדוק כל 10 עד 12 שעות עבור כל שינוי בגודל של הגבישים. ניתן להמשיך בניסוי אם לא נצפה שינוי בגודל הגבישים.
הערה: בהתאם לריכוזי החלבון והמשקעים בתמיסת ההתגבשות ולנפחי החלבון המשמשים, הזמן הדרוש כדי להגיע לשיווי המשקל עבור כל שלב עשוי להשתנות. - להקטין את הטמפרטורה ל 288 K כדי להתחיל מחדש את צמיחת הגביש. במצב הניסיוני של המקרה המוצג כאן, יום אחד מספיק כדי להגיע לשיווי משקל(איור 9, פאנל 3).
- בדוק את גודל הגבישים ולשמור על טמפרטורה קבועה כל עוד הגביש ממשיך לגדול.
- לאחר 4 ימים, הפחיתו את הטמפרטורה ל-275 K כדי להתחיל מחדש את צמיחת הגבישים (איור 9, פאנל 4).
– בתנאי הניסוי של המקרה המוצג, לאחר כ-10 ימים יתקבל גביש בעל 500 מיקרומטר בממד אחד (איור 9).
- הוסף 15 μL של lysozyme עם ריכוז של 30 מ"ג מ"ל-1 לתא הדיאליזה (איור 6A).
- שליטה בגודל הגביש
- הכינו תמיסת חלבון ואת דיאליזה מאגר זורם מבוקר טמפרטורה להגדיר כמתואר בסעיפים 2.3.1 ו 2.3.2.
- הכן פתרונות התגבשות עם 0.9 M NaCl ו- 0.1 M CH3COONa pH 4.
- הגדר את הטמפרטורה ל 291 K ולאפשר גבישים לגדול. בתנאים ראשוניים, אירוע הגרעין הראשון יתחיל לאחר כשעה וקריסטלים רבים יגדלו בתא הדיאליזה למשך שלוש שעות(איור 10, צעדים: 1 ו-2). הקלט תמונות כל 20 דקות כדי לבדוק את גודל הגבישים במהלך תהליך הגדילה.
הערה: אופטימיזציה של תנאי התגבשות היא חיונית בשליטה על רוב המאפיינים הסופיים של גבישים שנוצרו. ניתן לשנות את הטמפרטורה וההרכב הכימי של פתרונות התגבשות כדי להתמוסס ולגדל מחדש גבישים בגודל אחיד. יש לציין גם כי דגימת חלבון אינה נצרכת בניסוי כזה, שכן ניתן להפוך את התנאים כדי להמיס מחדש את המדגם כל עוד הוא לא denatured. בעת המסת גבישים על ידי שינוי הטמפרטורה ושמירה על הרכב כימי קבוע, להמשיך את הניסוי כדלקמן: - לאחר שהקריסטלים גדלו ב-291 קיי, ניתן להמיס אותם כדי לגדל מחדש פחות גבישים גדולים יותר. הגדל את הטמפרטורה בהדרגה מעל 20 דקות כדי להגיע 313 K. לוקח כשעה להמיס את כל הגבישים בתוך תא הדיאליזה(איור 10, צעדים: 3-5). הקלט תמונות כל 5 עד 15 דקות כדי לפקח על תהליך הפירוק.
הערה: חלבונים רבים רגישים לטמפרטורות גבוהות. הקפד לעבוד בטווח הטמפרטורות שבו החלבון יציב כדי למנוע נזק / denaturation. בנוסף מסיסות החלבון, הטמפרטורה משפיעה גם על פתרון החיץ. לדוגמה, רמת ה- pH של המאגר יכולה להשתנות עם הטמפרטורה, במיוחד במאגר Tris. במקרה כזה, חיוני להגדיר את ה- pH על פי הטמפרטורה שבה הניסוי מבוצע18. כמו כן יש לציין כי פירוק חלבון לוקח באופן משמעותי פחות זמן (מכמה דקות עד כמה שעות) לעומת צמיחת גביש חלבון (מכמה שעות עד כמה ימים). באופן כללי, במהלך פירוק הגבישים, הטמפרטורה עולה בהדרגה ובאיטיות (תוך כיבוד זמן הפירוק הכולל הקצר), בעיקר במקרה של פירוק חלקי של הגבישים כדי למנוע את עליית פסיפס הגבישים. כאשר הגבישים גדלים, הטמפרטורה יכולה לרדת במהירות (בפחות מדקה) לטמפרטורה שנקבעה (תוך כיבוד זמן הגדילה הכולל הארוך). ניטור קבוע של תא התגבשות על ידי הקלטת תמונות מומלץ למנוע נזק לחלבון ולעזור להגדיר את הזמן האופטימלי לפירוק או צמיחה של גבישים עבור כל חלבון למד. - אחרי שכל הגבישים התמוססו, קבעו את הטמפרטורה ל-295 K כדי ליזום אירוע התגרענות שני(איור 10, צעדים: 6,7). הקלט תמונות כל 5 דקות כדי לפקח על תהליך הגרעין השני. בשלב זה, הגרעינים הראשונים מופיעים לאחר כ -18 דקות.
הערה: בטמפרטורה זו, הפתרון יהיה באזור הגרעין, בקרבת האזור metastable. כתוצאה מכך, רק גרעינים מעטים יופיעו בתא ההתגבשות. - המשך בניסוי שחוזר על זרימת העבודה של המיטוב המתוארת בסעיף 2.3 לגידול גבישים גדולים יותר. משך הניסוי הכולל באיור 10 הוא ימים ספורים בלבד.
הערה: אם במהלך שלב הגרעין הגבישים מופיעים בזמנים שונים, גבישים בגדלים שונים מתקבלים בתא ההתגבשות. במקרה כזה, עליית הטמפרטורה (במקרה של חלבונים עם מסיסות ישירה) תגרום לפירוק מהיר יותר של הגבישים הקטנים יותר. בהתאם לאפקט ההבשלה הקינטית, החלבון הנוסף (שנרכש מפירוק) יכול לשמש לצמיחת הגבישים הגדולים יותר.
בעת המסת גבישים בטמפרטורה קבועה על ידי שינוי ההרכב הכימי של פתרון ההתגבשות, המשך בניסוי כדלקמן:
ניתן גם להמיס גבישים שגודלו בעבר על ידי שינוי ההרכב הכימי של פתרון התגבשות במהלך הניסוי לגדל מחדש אוכלוסייה של גבישים בגודל אחיד בתנאים חדשים. - הכינו את תמיסת החלבון (2.3.1), את מערך הדיאליזה של מאגר הזורם מבוקר הטמפרטורה (2.1) ואת פתרון ההתגבשות (2.4.2) כמתואר לעיל. בתנאים ראשוניים באזור הגרעין הרחק מהאזור המגושה, גבישים קטנים רבים יופיעו בתא ההתגבשות ויתחילו לגדול (איור 11, צעדים: 1,2).
- לאחר שלוש שעות, כאשר גבישים בינוניים רבים נראים בתא ההתגבשות(איור 11, שלב: 3), הקטן את ריכוז NaCl (0.9 M) בהדרגה כדי להגיע לאפס. בשביל זה, להכין פתרון התגבשות חדש המכיל רק פתרון חיץ עם 0.1 M CH3COONa pH 4. השתמש במערכת השאיבה כדי להחליף אותו עם פתרון התגבשות בתא המאגר. בצעו את שלבים 2.2.10 עד 2.2.12 להכנה והזרקה של פתרון חדש לתא המאגר. עם פתרון חדש זה, כאשר פתרונות מוחלפים ריכוז NaCl פוחתת בתא עד הפתרון הסופי בתא המאגר מכיל לא יותר מ 0.1 M של CH3COONa pH 4 ולא NaCl. לכוד תמונות כל 10 דקות כדי לתעד את תהליך הפירוק.
- אפשרו לקריסטלים להתמוסס לחלוטין(איור 11, צעדים: 4,5). זמן הפירוק הוא כשעתיים לניסוי הזה. כאמור, זמן הפירוק תלוי במערכת החלבון, בתנאי ההתגבשות ובנפח תא הדיאליזה בו נעשה שימוש. התבוננות קבועה בתא ההתגבשות (ראה סעיף מיקרוסקופ) והקלטת תמונות ופתקים במהלך הניסוי הם חיוניים.
- כאשר כל הגבישים בתוך התא מומסים(איור 11, שלב: 5), השתמש שוב במערכת השאיבה כדי להכין פתרון התגבשות חדש על ידי הזרקת NaCl בריכוז נמוך יותר מהקודם (0.75 M NaCl ב- 0.1 M CH3COONa pH 4).
- הזריקו את הפתרון החדש לתא המאגר (איור 11, שלבים: 6,7) וחזרו על זרימת העבודה של אופטימיזציית הצמיחה המתגבשת כמתואר בסעיף 2.3. אוכלוסייה אחידה של גבישים גדולים יותר תיווצר. התוצאות המוצגות באיור 11 התקבלו לאחר מספר ימים.
תוצאות
בסעיפים 2.3 ו-2.4 מוצגות שלוש דוגמאות לצמיחת גבישים ממוטבת, המציגות שימוש במכשיר ועיצוב ניסיוני לגידול גבישים גדולים. להדגמה זו, השתמשנו lysozyme כמו חלבון מודל, למרות ניסויים צמיחת גביש בוצעו בהצלחה עם מערכות חלבון רבות אחרות בשיטה זו (ראה לעיל). על ידי שימוש ושליטה בפרוטוקול המוצג כאן ניתן להתאים אותו למועמדים אחרים לחלבון.
בסעיף 2.3 הוכחנו כי אסטרטגיות התגבשות רציונליות מבוססות יכולות להועיל בגידול גבישים עם נפחי פיזור מספיקים לקריסטלוגרפיה של חלבון נויטרונים. כאן, אנו מראים כי אסטרטגיות האופטימיזציה הרציונליות המוצעות מאפשרות גם יצירת אוכלוסייה אחידה של גבישים בכל גודל ספציפי הנדרש לגישות קביעת מבנה במורד הזרם.
שני ניסויים אלה נועדו להדגיש את החשיבות של דיאגרמות פאזה בשליטה על התגרענות גביש וצמיחה. כאן, השליטה על הטמפרטורה וההרכב הכימי של פתרונות התגבשות בשילוב עם ניטור תהליך ההתגבשות בזמן אמת משמשים לחקר דיאגרמת הפאזה האיכותית. באמצעות שיטה זו, ניתן לייעל את הגרעין וצמיחת הגביש באופן רציונלי באופן הפיך. שימוש בגישה סדרתית כזו גם מקטין את כמות החלבון ואת הזמן הנדרש כדי לשלוט בגודל ובאיכות של הגבישים.
בשיטת הדיאליזה, פתרון חלבון מופרד מתמיסת התגבשות על ידי קרום חדיר למחצה6 (איור 5). קרום דיאליזה זה מאפשר למולקולות קטנות כגון תוספים, חיץ ויונים לעבור דרך הממברנה אך לא מקרומולקולות כגון חלבונים6,20. תכונה זו מאפשרת לשנות את פתרון התגבשות במהלך הניסוי6. חילופי הפתרון יכולים להיעשות באופן ידני, למשל בלחצני מיקרו-דיאליזה, או באופן אוטומטי באמצעות מכשיר שפותח למטרה זו, OptiCrys8.
בסט הניסויים הראשון, כפתורי מיקרו-דיאליזה שימשו להתגבשות lysozyme לבן ביצה עוף. כפתורי מיקרו-דיאליזה היו שקועים בפתרונות התגבשות עם ריכוזי מלח שונים. בניסוי רשת התגבשות פשוט זה, המשתנה היחיד הוא ריכוז משקעים בעוד הטמפרטורה נשמרת קבועה (293 K). כפי שמוצג באיור 4, שינויים קלים בריכוז המלח גורם לשינוי בגודל ובמספר הגבישים שנצפו, ומאפשרים חקירה של תרשים שלב ההתגבשות. באיור 4, פאנל 1, תמיסת ההתגבשות מכילה 0.7 M NaCl ומספר מצומצם של גבישים גדולים יותר הופיעו בלחצנים. על ידי הגדלת ריכוז המלח מ-0.7 ל-1.2 מ', רוויית-העל גדלה והפתרון באזור הגרעין מתרחק מהאזור המגנטי(איור 4,לוחות 1 עד 6). כתוצאה מכך, מספר הגבישים גדל וגודלם פוחת.
בניסוי הראשון עם מכשיר אוטומטי לחלוטין המאפשר התגבשות דיאליזה מבוקרת טמפרטורה, OptiCrys (איור 9),ניסוי צמיחת הגבישים הותאם ליצירת צמיחת גבישים גדולה. הניסוי הושק בטמפרטורה ראשונית של 295 K עם פתרון התגבשות המכיל 0.75 M NaCl ו 0.1 M Na אצטט חיץ pH 4. בתנאי ניסוי אלה, פתרון ההתגבשות הגיע לאזור הגרעין בקרבת האזור המטא-יציב של תרשים הפאזה(איור 9, חץ 1). כתוצאה מכך, רק גרעינים בודדים נוצרו בשלב הראשון של הניסוי. כדי לגדל גבישים נבחרים עוד יותר (מוצג באיור 9),זרימת העבודה של אופטימיזציית צמיחת הגבישים הונעה לכיוון האזור המגנטי על ידי טמפרטורה משתנה ברגע שהגיעו לשיווי המשקל של פתרון הגביש.
בכל פעם שהושג שיווי משקל בין גביש לפתרון, הטמפרטורה הופחתה, תחילה ל 291 K, לאחר מכן ל 288 K ולבסוף ל 275 K, כדי לשמור על פתרון התגבשות באזור metastable. התוצאה של ניסוי זה היא גביש גדול אחד המתאים הן לרנטגן מקרומולקולרי והן לקריסטלוגרפיה של נויטרונים.
עבור רוב החלבונים, דיאגרמת הפאזה הכמותית המדויקת (או סתם דיאגרמה איכותית) עדיין לא הושגה בשל היעדר התקנים ניסיוניים המסוגלים למדוד במדויק את ריכוז החלבון (או סתם התבוננות/גילוי תהליך ההתגבשות בזמן אמת) במהלך ניסויי התגבשות18. כתוצאה מכך, לעתים קרובות לא ניתן לתכנן את הניסוי באופן כזה שהתגבשות מתחילה באזור האופטימלי של דיאגרמת הפאזה, בקרבת האזור המגושה.
לכן, מחקר אופטימיזציה התגבשות חייב להתקיים לפני הניסוי המוקדש לצמיחה של גביש נפח גדול מתבצע. במחקר זה, באמצעות וריאציות טמפרטורה (בהרכב כימי מתמיד) מצד אחד וריאציות בהרכב כימי (בטמפרטורה קבועה) מצד שני, יש צורך לזהות את האזור metastable ולתוות את התנאים האופטימליים להתחלת ניסוי צמיחת גביש גדול.
למטרה זו, שני ניסויים אחרים מוצגים אשר הותאמו כדי להדגים את ההפיכה של ניסויי התגבשות דיאליזה מבוקרת טמפרטורה עם OptiCrys עבור התגרענות, צמיחת גביש, פירוק וצמיחה מחדש. זרימת העבודה אופטימיזציה צמיחת גביש נשלטה כך אוכלוסייה אחידה של פחות, גבישי lysozyme גדול גדל, באמצעות וריאציה של טמפרטורה או ריכוז משקעים.
בניסוי השני עם OptiCrys, ההרכב הכימי של פתרון התגבשות נשמר קבוע לאורך כל הניסוי (0.9 M NaCl ב 0.1 M CH3COONa pH 4) עם טמפרטורה משתנה. הטמפרטורה הראשונית נקבעה על 291 K. תוצאות הניסוי מסוכמות באיור 10. בשל רוויית-על גבוהה, מספר רב של גבישים קטנים הופיעו בתא ההתגבשות(איור 10, לוחות 1 ו-2). בהתאם למושג מסיסות חלבון ישירה, על ידי הגדלה הדרגתית של הטמפרטורה ל-313 K, כל הגבישים התמוססו (איור 10, לוחות 3, 4 ו-5). לבסוף, על ידי הורדת הטמפרטורה ל 295 K, הגרעין השני היה יזם בקרבת האזור metastable ואיפשר היווצרות מבוקרת של מספר נמוך יותר של גרעינים. גידול גביש נוסף הביא לדור אחיד של אוכלוסייה של גבישים גדולים יותר(איור 10, פאנל 7).
כפי שמוצג באיור 11, וריאציה של ההרכב הכימי של פתרון ההתגבשות, בטמפרטורה קבועה של 291 K, יכולה לשמש גם להשגת אוכלוסייה אחידה של גבישים גדולים יותר. בדומה לניסוי הקודם, המצב הראשוני היה 0.9 M NaCl ב 0.1 M CH3COONa pH 4. ריכוז NaCl הונמך בהדרגה מ-0.9 מ' לאפס כדי להמיס את הגבישים(איור 11, לוחות 4 ו-5). בשלב זה, NaCl הוחלף לחלוטין על ידי פתרון חיץ של 0.1 M CH3COONa pH 4. הפחתת ריכוז המלח שומרת על הפתרון באזור התת-רווי של דיאגרמת הפאזה, מה שמוביל לפירוק הגבישים. לאחר מכן, פתרון התגבשות חדש עם חוזק יוני נמוך יותר, ב 0.75 M NaCl ב 0.1 M CH3COONa pH 4, הוזרק לתוך תא המאגר. בריכוז משקעים זה הופיע הגרעין הראשון (איור 11, פאנל 6) לאחר 90 דקות. מספר הגבישים שנוצרו היה נמוך יותר והקריסטלים מגיעים לנפח גדול יותר (איור 11, פאנל 7) מבעבר.
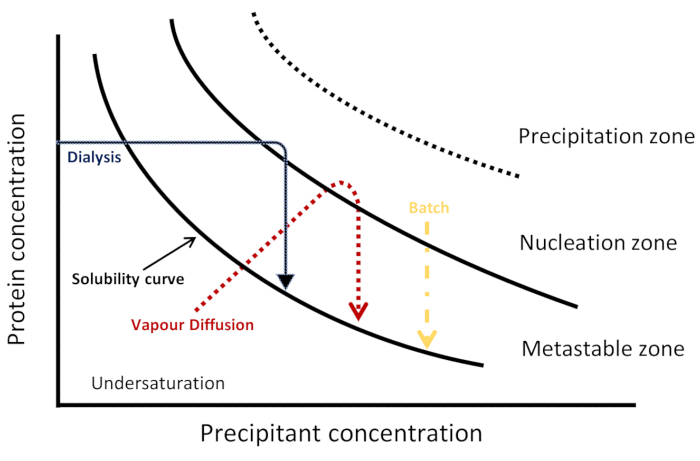
איור 1: דיאגרמת פאזה סכמטית. מסלולים קינטיים לשלוש טכניקות התגבשות מיוצגים במשטר מלח החוצה. כל שיטה משיגה התגרענות והתגבשות באופן שונה, דמיינה על ידי מסלול קינטי שונה דרך דיאגרמת הפאזה כדי להגיע לאזורי הגרעין והמטא-חומר. עקומת המסיסות מפרידה בין אזורי ת-רוויה ותת-רוויה. רוויית-על מחולקת לשלושה אזורים: מטא-חומר, התגרענות ומשקעים. באזור התגרענות, התגרענות ספונטנית מתרחשת בעוד באזור metastable צמיחת גביש מתרחשת. נתון זה מותאם מ- Junius et al. 8אנא לחץ כאן כדי להציג גרסה גדולה יותר של איור זה.
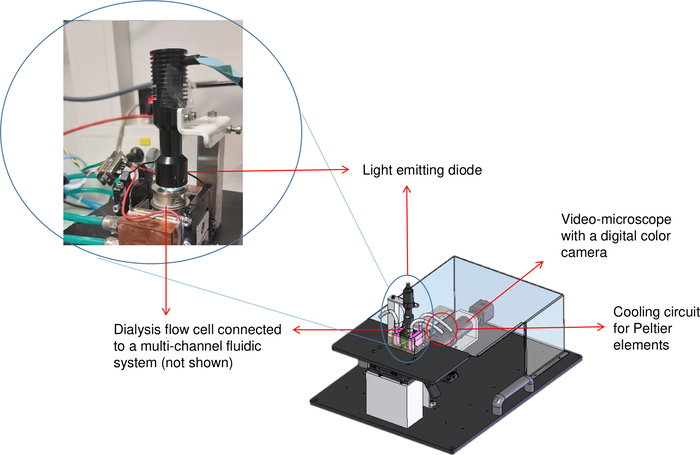
איור 2: ייצוג סכמטי של ספסל ההתגבשות (OptiCrys). מקור אור ה-LED ממוקם על גבי תא זרימת הדיאליזה מבוקר הטמפרטורה. מיקרוסקופ הפוך והמצלמה הדיגיטלית מוצגים בקצה השמאלי העליון של התמונה עם החץ האדום. העיגול האדום מייצג את מיקום צינורות הצ'ילר. לחץ כאן כדי להציג גירסה גדולה יותר של איור זה.

איור 3: דיאגרמת שלב התגבשות חלבונים דו-ממדית סכמטית כפונקציה של טמפרטורה (A) וריכוז משקעים (B). (א) במקרה של חלבון עם מסיסות ישירה, הפחתת הטמפרטורה שומרת על פתרון ההתגבשות באזור metastable. וריאציה טמפרטורה ניתן לחזור מספר פעמים כדי לשלוט על תהליך צמיחת הגביש עד גבישים עם הנפח הרצוי מתקבלים. (ב) שינוי הריכוז של הפתרון המשקעים יכול לשמש גם כדי לשמור על פתרון התגבשות באזור metastable עבור גבישים גדל. נתון זה מותאם מ- Junius et al. 8אנא לחץ כאן כדי להציג גרסה גדולה יותר של איור זה.

איור 4: גבישי lysozyme המתקבלים בשיטת הדיאליזה. ניסוי זה בוצע בטמפרטורה קבועה של 293 K ב 0.1 M נתרן אצטט חיץ pH 4. הגדלת ריכוז NaCl מ 0.7 M ל 1.2 M מגביר את קצב התגרענות ותוצאות מספר גדול יותר של גבישים. לחץ כאן כדי להציג גירסה גדולה יותר של איור זה.
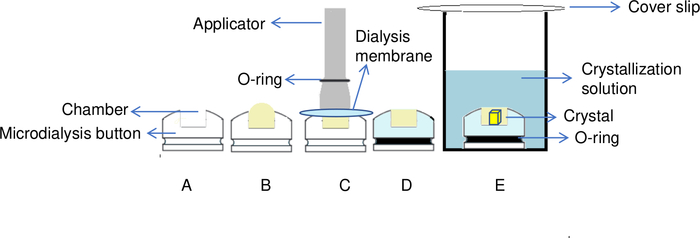
איור 5: סקירה כללית של תהליך התגבשות החלבון בשיטת הדיאליזה. (א) על ידי הוספת החלבון לתא של כפתור הדיאליזה, (B) צורת כיפה נוצרת בחלק העליון של התא. (ג) אפליקטור משמש להעברת O-ring לגרוב של כפתור הדיאליזה על מנת לתקן את קרום הדיאליזה במקום. (ד) כפתור הדיאליזה מוכן לטבילה בפתרון המאגר. (ה) תמיסת התגבשות עוברת דרך הממברנה החצי-חדירה והקריסטלים מתחילים להיווצר בתוך התא. לחץ כאן כדי להציג גירסה גדולה יותר של איור זה.
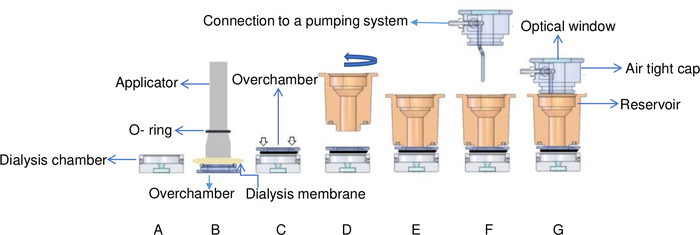
איור 6: תצוגה סכמטית של הגדרת הדיאליזה הזורמת מבוקרת הטמפרטורה. (א) דגימת החלבון מתווספת לתא הדיאליזה. (ב) קרום הדיאליזה קבוע על הישפן עם O-ring באמצעות אפליקטור. (ג) הישדון הופך ומתוקן על החלק העליון של תא הדיאליזה. חצים לבנים מציינים היכן בורגים ממוקמים על הישבן. (ד) תא המאגר מופנה בכיוון השעון (E) ומתוקן על גבי חדר ה-overchamber. (ו) תא המאגר מכוסה בכובע אטום עם מחברים למערכת שאיבה ו-(G) תא הזרימה ממוקם בתמיכת הפליז. נתון זה מותאם מ- Junius et al. 8אנא לחץ כאן כדי להציג גרסה גדולה יותר של איור זה.
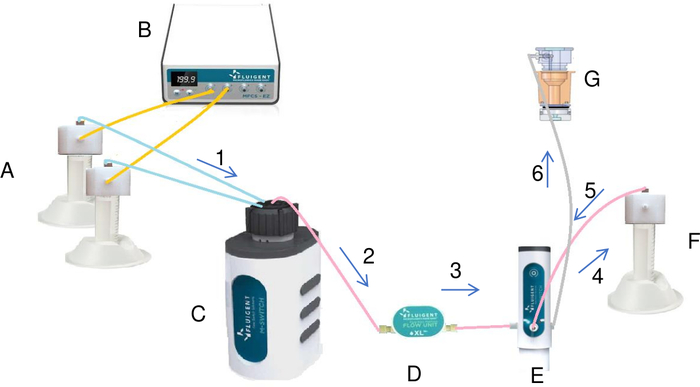
איור 7: הכנה והזרקה של פתרון ההתגבשות במאגר על ידי המערכת הנוזלית (A). שפופרות המכילות מלח ומים מחוברות לבקר הלחץ/ואקום (B) ולשסתום הסיבובי (C). באמצעות הלחץ, בקר לחץ / ואקום יוצר זרימה מתמדת של הנוזלים מהצינורות לשסתום הסיבובי. כל נוזל העובר דרך מד הזרימה (D) והמתג מוזרק לצינור הערבוב (F). לאחר שכל הנוזלים נוספו לצינור הערבוב, המתג על ידי כמה שינויים מזריק את הפתרון הסופי מצינור הערבוב לתוך המאגר (G). הנוזל זורם דרך המערכת בכיוון החצים בדיאגרמה המסומנים בסדר עולה (מ- 1 עד 6). לחץ כאן כדי להציג גירסה גדולה יותר של איור זה.

איור 8: תצוגת תחזוקה של תוכנת הפיקוח. תצוגה זו משמשת לשליטה בפרמטרים שונים כמו טמפרטורה, אור, פתרון התגבשות וזום. לחץ כאן כדי להציג גירסה גדולה יותר של איור זה.
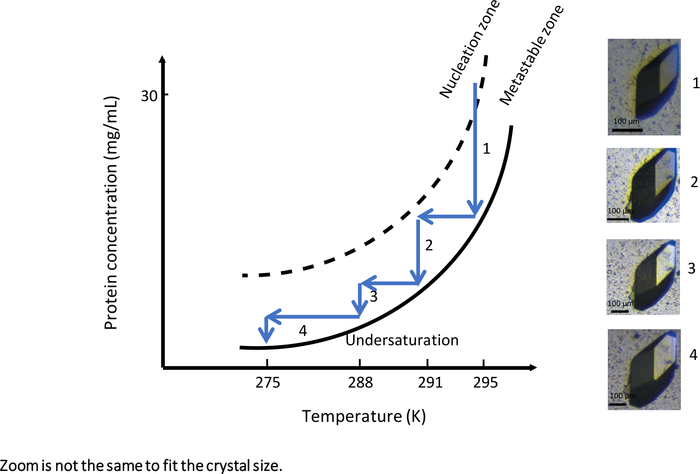
איור 9: דיאגרמת הפאזה כפונקציה של הטמפרטורה (יש לעקוב אחר תמונות נבחרות בסדר עולה). גביש lysozyme גדול יחיד מתקבל על ידי שינוי שיטתי של הטמפרטורה מ 295 K ל 275 K. בכל שלב, צמיחת הגביש נעצרת עם ההגעה לעקומת המסיסות. הפחתת הטמפרטורה על ידי שמירה על הפתרון באזור metastable מחדש את צמיחת הגביש. התמונות כוללות רמות שונות של הגדלה. נתון זה מותאם מ- Junius et al. 8,18אנא לחץ כאן כדי להציג גירסה גדולה יותר של איור זה.
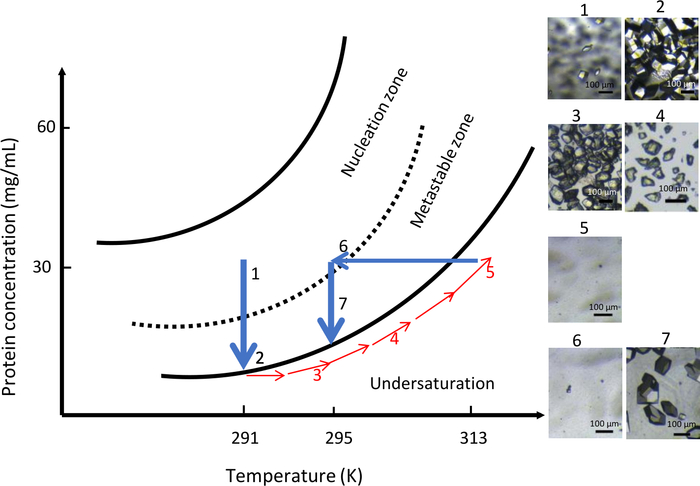
איור 10: אופטימיזציה של צמיחת גביש בהרכב כימי קבוע באמצעות בקרת טמפרטורה (יש לעקוב אחר תמונות נבחרות בסדר עולה). התחלת תהליך הגרעין באזור הגרעין ב 291 K, רחוק מהאזור metastable, תוצאות היווצרות של גבישים רבים. הגדלת הטמפרטורה ל 313 K ואז ממיס את הגבישים עד שלא נראים גרעינים גלויים בתא הדיאליזה. לבסוף, הפחתת הטמפרטורה ל 295 K מפעילה מחדש את תהליך הגרעין בפעם השנייה המוביל למספר מוגבל של גבישים גדולים יותר. נתון זה מותאם מ- Junius et al. 8,18אנא לחץ כאן כדי להציג גירסה גדולה יותר של איור זה.
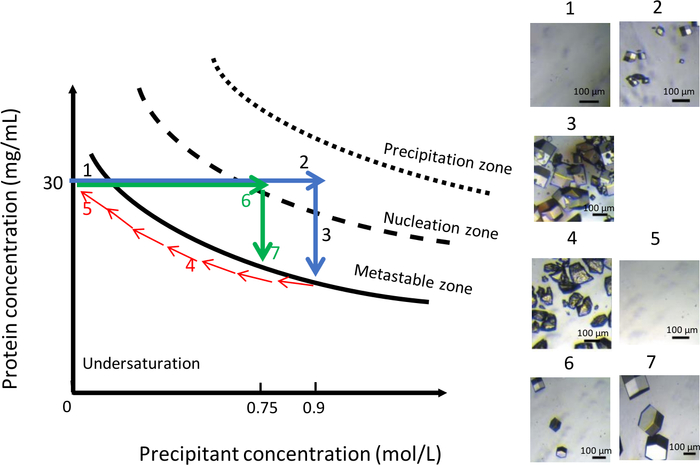
איור 11: אופטימיזציה של צמיחת גביש בטמפרטורה קבועה באמצעות וריאציות בריכוז משקעים (יש לעקוב אחר תמונות נבחרות בסדר עולה). הפחתת ריכוז המשקעים מ-0.9 מ' ל-0 מ' ממיסה את הגבישים שהושגו במהלך אירוע הגרעין הראשון. תהליך ההתגבשות מופעל מחדש על ידי הזרקה של אותו משקע אך בעוצמה יונית נמוכה יותר, 0.75 M, מה שמוביל להיווצרות של כמה גבישים גדולים יותר. נתון זה מותאם מ- Junius et al. 8,18אנא לחץ כאן כדי להציג גירסה גדולה יותר של איור זה.
Discussion
משתנים פיזיקליים, כימיים וביולוגיים שונים משפיעים על התגבשות החלבון על ידי השפעה על מסיסות החלבון21. בין משתנים אלה, טמפרטורה והרכב כימי של פתרון התגבשות משמשים כאן בשילוב עם טכניקת דיאליזה כדי לשפר ולגדל גבישים גדולים באיכות גבוהה של biomacromolecules למחקרי עקיפה נויטרונים. על ידי שימוש בידע של דיאגרמות פאזה, התגבשות נעשית צפויה יותר. למרות סינון של תנאי התגבשות שונים בגישה סדרתית אפשרית גם, המטרה העיקרית של שימוש בגישות רציונליות המוצגות היא להפריד ולשלוט בקינטיקה של התגרענות גביש וצמיחה.
בדומה לכל מחקרי ההתגבשות, דגימות חלבון טהורות והומוגניות באיכות גבוהה ופתרונות התגבשות נטולי אבק מגדילים את שיעור ההצלחה של הניסוי. סינון וצנטריפוגה של פתרונות הם צעדים חיוניים בפרוטוקולים המתוארים. הכרת התכונות הפיזיוכימיות של החלבונים שנחקרו כגון המשקל המולקולרי (לבחירת קרום הדיאליזה המתאים), הנקודה האיזואלקטרית ומסיסות החלבון חיוניים לתכנון ניסוי צמיחת גביש אופטימלי. כמו כן, יש לשקול את יציבות החלבון בטמפרטורות שונות או עם כימיקלים שונים כדי למנוע אובדן מדגם ולהגדיל את הסבירות להצלחה. בהתחשב בטווח הטמפרטורות של OptiCrys (233.0–353.0 ± 0.1 K), ניתן לגבש מגוון רחב של חלבונים באמצעותו. אבל כדאי להדגיש כי חלבונים כי הם בעיקר תרמו יציב, כגון חלבונים ממקורות תרמופיליים, יועיל ביותר בטמפרטורה מבוקרת ניסויים צמיחת גביש בנפח גדול המוצעים על ידי מכשיר זה.
באמצעות תא דיאליזה בנפח נמוך (בעת שימוש בלחצני OptiCrys) או מיקרו-דיאליזה וסינון מספר טמפרטורות ותנאי התגבשות (למשל, רשתות של ריכוז משקעים או pH), ניתן לקבל מידע על מיקום הגבול של האזור metastable (שיווי משקל קינטי בין גרעינים ואזורים metastable). זה לא יסולא בפז בעת עיצוב ניסוי מוצלח צמיחת גביש במיוחד עבור מועמדים חדשים חלבון התגבשות. ללא מידע זה ניסויים יכולים להתחיל מאזור של דיאגרמת פאזה עם רוויה גבוהה, רחוק מדי מהגבול של האזור metastable לשלוט בקלות התגרענות גביש. למרות פירוק של משקע החלבון ניתן לנסות, למשל על ידי הגדלת הטמפרטורה במקרה של מסיסות ישירה, עבור חלבונים עם תרמוביות מופחתת, שמירה על המדגם בטמפרטורה גבוהה במשך תקופה ארוכה יותר של זמן עשוי להפוך את משקע החלבון בלתי הפיך. לכן, האסטרטגיה הטובה ביותר מורכבת משימוש במצב ראשוני עם רוויית-על נמוכה יותר הממוקמת בסמוך לגבול המטא-יציבות, שם ניתן לשלוט בגרעין ולהימנע ממשקעי חלבון. בקנה אחד עם זה, התגבשות prescreening מקטין את הסיכוי שיש משקע חלבון בתא הדיאליזה ומגביר את שיעור ההצלחה של הניסוי.
לאחר תכנון ניסוי, הכנת תאי דיאליזה (OptiCrys) או כפתורי מיקרו-דיאליזה היא צעד חשוב נוסף. מניעת היווצרות בועת אוויר בתא/כפתור הדיאליזה מגדילה את הסיכוי להתגבשות מוצלחת במיוחד כאשר משתמשים בנפחים קטנים. נוכחותן של בועות אוויר בתא הדיאליזה עשויה גם לשנות את הקינטיקה של תהליך ההתגבשות ולהפחית את השחזור של הניסוי (מכיוון שמשטח המגע של החלבון/פתרון שונה). לא רק חלבון אלא גם פתרון התגבשות יכול להשפיע על ההצלחה של הניסוי. שימוש בצינורות חדשים של 50 מ"ל למערכת השאיבה בכל פעם שרוצים להתחיל ניסוי חדש וצינורות כביסה לאחר כל ניסוי מקטין את הסיכוי לזיהום ומונע יצירת גבישי מלח במנגנון.
השימוש בלחצני מיקרו-דיאליזה הוא חלופה כאשר OptiCrys אינו זמין. האסטרטגיות לאופטימיזציה של התגבשות וניטור צמיחת הגביש שהוזכרו לעיל, חייבות להתבצע באופן ידני. בדרך כלל זה מחייב להיות מחוץ לחממה תרמורגולטית, אשר יכול להיות בעייתי כאשר ויסות הטמפרטורה הוא צעד קריטי במתודולוגיה המתוארת. זה לא מקל על שינוי ההרכב הכימי של פתרונות התגבשות, או ניטור צמיחת גביש על ידי הדמיה, ולכן תהליך צמיחת הגביש לא ניתן לשלוט בזמן אמת.
הידע של תרשים הפאזה הוא הבסיס לשימוש בספסל ההתגבשות, OptiCrys, כדי לגדל באופן שיטתי גבישים גדולים ואיכותיים באופן אוטומטי. שליטה בפרמטרים פיזיוכימיים כמו טמפרטורה, ריכוז משקעים ו- pH במהלך התגבשות מעבירה את שיווי המשקל של תמיסת החלבון במסלול קינטי מוגדר היטב לאורך דיאגרמת הפאזה. זה משלים את השימוש בקרום דיאליזה כדי להתאים הובלת המונים וליצור שיפוע מבוקר בתא התגבשות המשפיע על הגודל והאיכות של הגבישים. לכן, שימוש הן בנתונים תרמודינמיים והן במסלולים קינטיים חיוני כדי לשלוט בתהליך ההתגבשות על מנת לגדל גבישים באיכות גבוהה. הודות OptiCrys, דיאגרמות שלב שיטתי במרחב רב ממדי ניתן ללמוד עם גישה סדרתית באמצעות חומר פחות באופן משמעותי מבעבר. כדי להדגים מתודולוגיה זו, אנו מספקים כאן מקרה מבחן עם חלבון מודל, ליזוזים לבנים ביצה עוף. על ידי שימוש ושליטה בפרוטוקול המוצג כאן ניתן להתאים אותו למערכות חלבון אמיתיות5,14,17,18.
Disclosures
למחברים אין מה לחשוף.
Acknowledgements
MBS מאשרת את התמיכה של LABEX VALO GRAL במסגרת החוזה 2015. ניו ג'רזי מכירה בתוכנית הבינלאומית לחקר הדוקטורט (Irtelis) של CEA עבור מלגת הדוקטורט. המחברים מאשרים מימון מתוכנית המחקר והחדשנות Horizon 2020 של האיחוד האירופי במסגרת הסכם המענק מארי סקלודובסקי-קירי מספר 722687. המחברים גם אסירי תודה לד"ר אסקו אוקסנן (ESS, לונד) וד"ר ז'אן לוק פרר (IBS, גרנובל) על שיחות ותובנות מועילות. IBS מכיר בהשתלבות במכון המחקר הבינתחומי של גרנובל (IRIG, CEA).
Materials
| Name | Company | Catalog Number | Comments |
| 200 µl Dialysis Button | Hampton Research | HR3-330 | Dialysis button |
| 24 well plates | Jena Bioscience | CPL-132 | Crystallization plate |
| 2-Switch | FLUIGENT | 2SW001 | Switch |
| 30 μl Dialysis Button | Hampton Research | HR3-324 | Dialysis button |
| 50 mL Corning Centrifuge tubes | Sigma-Aldrich | CLS430828-500EA | Centrifuge tubes |
| Acetic acid | Sigma-Aldrich | S2889 | Chemical |
| Chicken Egg White Lysozyme | Sigma-Aldrich | L6876 | Lyophilized protein powder |
| Dialysis Membrane Discs 6-8 kDa MWCO | Spectrum | 132478 | Dialysis membrane |
| Dialysis Membrane Tubing 6-8 kDa MWCO | Spectrum | 132650T | Dialysis membrane |
| Microcentrifuge | Eppendorf | Minispin | Bench-top centrifuge |
| Flow Unit | FLUIGENT | FLU-XL | Flow meter |
| Flowboard | FLUIGENT | FLB | Flowboard |
| Microfluidic Flow Control System EZ | FLUIGENT | EZ-01000002 | Pressure/vacuum controller |
| MilliporeSigma 0.22 µm syringe Filters | Millipore | GSWP04700 | 0.22 μm pore size filter |
| M-Switch | FLUIGENT | MSW002 | Rotary valve |
| Opticrys | NatX-ray | PRT008 | Crystallization bench |
| Siliconized circle cover slides | Hampton Research | HR3-231 | Glass slides |
| Sodium Chloride ≥ 99% | Sigma-Aldrich | 746398 | Chemical |
| Switchboard | FLUIGENT | SWB002 | Switchboard |
| Thermoregulated incubator | Memmert | IPP30 | Thermoregulated incubator |
References
- Blakeley, M. P., Langan, P., Niimura, N., Podjarny, A. Neutron crystallography: opportunities, challenges, and limitations. Current Opinion in Structural Biology. 18 (5), 593-600 (2008).
- Snell, E. H., Van Der Woerd, M. J., Damon, M., Judge, R. A., Myles, D. A. A., Meilleur, F. Optimizing crystal volume for neutron diffraction: D-xylose isomerase. European Biophysics Journal. 35 (7), 621-632 (2006).
- Ng, J. D., Baird, J. K., Coates, L., Garcia-Ruiz, J. M., Hodge, T. A., Huang, S. Large-volume protein crystal growth for neutron macromolecular crystallography. Acta Crystallographica Section F:Structural Biology Communications. 71, 358-370 (2015).
- O'Dell, W. B., Bodenheimer, A. M., Meilleur, F. Neutron protein crystallography: A complementary tool for locating hydrogens in proteins. Archives of Biochemistry and Biophysics. 602, 48-60 (2016).
- Oksanen, E., Blakeley, M. P., Bonneté, F., Dauvergne, M. T., Dauvergne, F., Budayova-Spano, M. Large crystal growth by thermal control allows combined X-ray and neutron crystallographic studies to elucidate the protonation states in Aspergillus flavus urate oxidase. Journal of the Royal Society Interface. 6, (2009).
- Krauss, I. R., Merlino, A., Vergara, A., Sica, F. An overview of biological macromolecule crystallization. International Journal of Molecular Sciences. 14 (6), 11643-11691 (2013).
- Chayen, N. E. Comparative Studies of Protein Crystallization by Vapour-Diffusion and Microbatch Techniques. REVIEW Acta Cryst. , (1998).
- Junius, N., Oksanen, E., Terrien, M., Berzin, C., Ferrer, J. L., Budayova-Spano, M. A crystallization apparatus for temperaturecontrolled flow-cell dialysis with real-time visualization. Journal of Applied Crystallography. 49, 806-813 (2016).
- Salemme, F. R. A free interface diffusion technique for the crystallization of proteins for X-ray crystallography. Archives of Biochemistry and Biophysics. 151 (2), 533-539 (1972).
- Chayen, N. E., Saridakis, E. Protein crystallization: From purified protein to diffraction-quality crystal. Nature Methods. 5 (2), 147-153 (2008).
- Otálora, F., Gavira, J. A., Ng, J. D., García-Ruiz, J. M. Counterdiffusion methods applied to protein crystallization. Progress in Biophysics and Molecular Biology. 101 (1-3), 26-37 (2009).
- Garciá-Ruiz, J. M. Counterdiffusion Methods for Macromolecular Crystallization. Methods in Enzymology. 368, 130-154 (2003).
- Budayova-Spano, M., Koruza, K., Fisher, Z. Large crystal growth for neutron protein crystallography. Methods in Enzymology. 634, 21-46 (2020).
- Budayova-Spano, M., Dauvergne, F., Audiffren, M., Bactivelane, T., Cusack, S. A methodology and an instrument for the temperature-controlled optimization of crystal growth. Acta Crystallographica Section D: Biological Crystallography. 63 (3), 339-347 (2007).
- Asherie, N. Protein crystallization and phase diagrams. Methods. 34 (3), 266-272 (2004).
- Astier, J. P., Veesler, S. Using temperature to crystallize proteins: A mini-review. Crystal Growth and Design. 8 (12), 4215-4219 (2008).
- Budayova-Spano, M., et al. A preliminary neutron diffraction study of rasburicase, a recombinant urate oxidase enzyme, complexed with 8-azaxanthin. Acta Crystallographica Section F: Structural Biology and Crystallization Communications. 62 (3), 306-309 (2006).
- Junius, N., Vahdatahar, E., Oksanen, E., Ferrer, J. L., Budayova-Spano, M. Optimization of crystallization of biological macromolecules using dialysis combined with temperature control. Journal of Applied Crystallography. 53 (3), (2020).
- Grimsley, G. R., Pace, C. N. Spectrophotometric Determination of Protein Concentration. Current Protocols in Protein Science. 33 (1), 1-9 (2003).
- McPherson, A., Gavira, J. A. Introduction to protein crystallization. Acta Crystallographica Section F:Structural Biology Communications. 70 (1), 2-20 (2014).
- McPherson, A. Introduction to protein crystallization. Methods. 34 (3), 254-265 (2004).
Reprints and Permissions
Request permission to reuse the text or figures of this JoVE article
Request PermissionThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. All rights reserved