Method Article
Istituzione e Propagazione dei Tumori retinoblastoma umani in topi privi di sistema immunitario
* Questi autori hanno contribuito in egual misura
In questo articolo
Riepilogo
Un metodo è descritto per propagare i tumori retinoblastoma umano nei topi. Le cellule tumorali sono direttamente iniettate negli occhi di topi privi di sistema immunitario. Tumori secondari sono state stabilite con successo utilizzando sia le cellule raccolte direttamente da tumori umani e tumorspheres colta.
Abstract
Coltura di cellule tumorali retinoblastoma nei media di cellule staminali definite dà luogo a tumorspheres primario che può essere coltivata e mantenuta solo per un tempo limitato. Queste tumorspheres colta possono presentare fenotipi cellulari notevolmente diverso rispetto al tumore originale. Dimostrazione che le cellule in coltura hanno la capacità di formare nuovi tumori è importante assicurarsi che il modello di una coltura di cellule la biologia del tumore originale.
Qui vi presentiamo un protocollo per la propagazione dei tumori retinoblastoma umano in vivo utilizzando RAG2 - / - immune topi deficienti. Colta tumorspheres retinoblastoma umano di passaggio basso o cellule ottenute da appena raccolte tumori retinoblastoma umano iniettato direttamente in camera vitreale di occhi murino formare tumori entro 2-4 settimane. Questi tumori possono essere raccolte e sia ulteriori diversi passaggi negli occhi di topo in vivo o coltivate come tumorspheres in vitro. Propagazione è stato svolto con successo per almeno tre passaggi stabilendo così una continua fonte di tessuto retinoblastoma umano per ulteriori sperimentazioni.
Wesley S. Bond e Lalita Wadhwa sono co-primi autori.
Protocollo
1. Preparazione del tumorspheres retinoblastoma
- Ottenere tumore campione retinoblastoma sotto un IRB-approvato il protocollo.
- Preparare fresca di supporto definito di cellule staminali (Neurobasal-A media, 1X B-27 integratore meno vitamina A, 1X non essenziali della soluzione di amminoacidi, L-glutamina 1X, 20 ng / mL di EGF, 10 ng / ml bFGF).
- Meccanicamente disaggregare il tessuto tumorale con un bisturi con una trasversale tecnica in una sterile, il tessuto della cultura trattati con 6-pozzetti. Immediatamente aggiungere 100 ml di mezzi di comunicazione definite cellule staminali del tessuto e delicatamente diffondere il tessuto tritata con il bisturi. Aggiungere 5 ml di mezzi di comunicazione di cellule staminali definite al pozzo.
- Incubare a 37 ° C, 5% di CO 2 in un incubatore umidificato e controllare tutti i giorni. Alcuni tumorspheres dovrebbe derivare dal tessuto tumorale interrotto quasi subito, con un numero sempre crescente nel corso di 2-4 giorni.
- Settimanale, tumorspheres centrifugare a 300xg per 5 minuti, risospendere nei media staminali preparati al momento definito di cellule, e seminare su e giù per 10 volte per interrompere più grandi, sfere centrale necrotica e consentire nuove sfere sano di forma.
2. La preparazione delle cellule tumorali per iniezione
- Se l'iniezione tumorspheres colta, dolcemente sfere in una pipetta da 15 ml tubo conico. Pipettare delicatamente su e giù con una pipetta sierologica 10-15 volte per distruggere le sfere.
- Contare le cellule da iniettare utilizzando un emocitometro, e aliquota almeno 50.000 cellule per iniezione in un nuovo tubo. Prepararsi per le iniezioni maggior numero possibile in base al numero di cellule disponibili.
- Centrifugare a 300xg per 5 minuti. Con attenzione aspirare il surnatante e risospendere in 5 ml di PBS. Ripetere centrifugazione e aspirazione e risospendere in 10 L PBS per iniezione.
3. Preparazione degli animali
- Utilizzando una siringa per insulina, somministrare un'iniezione intraperitoneale di cocktail roditori anestesia (ketamina 37,6 mg / ml, xilazina 1,92 mg / ml, acepromazina 0,38 mg / ml) a 1 ml per grammo di peso corporeo (GBW). Attendere 5 minuti per l'animale a diventare sedato. Controllare il battito cardiaco e posizionare l'animale su un blocco riscaldato. Mantenere gli animali su un blocco riscaldato in ogni momento fino al recupero.
- Dopo la sedazione, somministrare 1 goccia di HCl proparacaina per l'occhio destro. Sostituire animali sul pad riscaldato e attendere 1 minuto.
- Somministrare 1 goccia di fenilefrina HCl per l'occhio destro. Sostituire l'animale sul pad riscaldato e attendere 5 minuti. Se la dilatazione della pupilla non si è verificato, ri-somministrare 1 goccia e attendere altri 5 minuti.
- Monitorare gli animali per i segni di movimento o spasmi, che può verificarsi in> 30 minuti dopo la sedazione. Al primi segni di movimento, somministrare 1 ml / GBW di ketamina HCl (diluito a 10 mg / ml in PBS) e attendere 5 minuti.
4. Iniezione di cellule tumorali
- Posizionare l'animale anestetizzato sotto il microscopio su un lato, con l'occhio destro rivolto verso l'alto e con la testa appoggiata su garza e centrato per ottenere un riflesso rosso dell'occhio destro fondo (pupilla dilatata dovrebbe essere in questo momento) quando osservata attraverso il microscopio .
- Puntellare il globo destra spingendo delicatamente verso il basso contemporaneamente con due dita sulle palpebre e mantenere questa posizione costante per il resto della procedura.
- Usando una sterile da 30 gauge collegato a una siringa Luer-Lock, perforare il globo lateralmente attraverso la congiuntiva e la sclera adiacente al limbus corneale nella zona della pars plana (figura 1) e solo attraverso la coroide in camera vitreale. Rimuovere l'ago dalla apertura.
- Sterilizzare l'ago Hamilton con un batuffolo di cotone imbevuto di alcool. Disegnare la sospensione cellulare nella siringa Hamilton e inserire l'ago nel foro fino a quando l'ago viene visualizzato attraverso il microscopio dietro l'obiettivo nel vitreo vicino alla retina. Con l'aiuto di una seconda persona mentre si tiene l'ago stabilmente in questa posizione, spingere il pistone lentamente. Rimuovere l'ago. Se necessario, utilizzare un batuffolo di cotone per assorbire qualsiasi liquido dall'apertura.
- Delicatamente rilasciare la pressione delle palpebre per chiudere le palpebre del mouse.
- Somministrare 1 goccia di ipromellosa per ciascun occhio e tornare animale pad riscaldato per il recupero.
5. Monitoraggio di topi iniettati e la raccolta dei tumori
- Ogni giorno, esaminare l'occhio iniettato per leucocoria (bianco riflesso papillare) e / o perioculare distensione che di solito si manifesta 2-4 settimane dopo l'iniezione.
- Una volta che la crescita del tumore viene rilevato, l'eutanasia degli animali secondo le linee guida istituzionali.
- Se l'occhio e tumore sono coperti dalla palpebre, utilizzare il bisturi per fare due incisioni ortogonali alla fessura palpebrale e sollevare i lembi della pelle.
- Sotto la visualizzazione utilizzando il microscopio stereoscopico, fare una incisione circonferenziale al limbus, eliminando la cornea e la lente, e con attenzione sezionare la maggior parte della massa tumorale da altri tessuti utilizzando tweezers. Posizionare il tumore in sterili RPMI-1640 media.
- Utilizzare le pinzette per estrarre lentamente il globo aperto da presa. Per assicurare un nervo ottico collegato in modo invasione tumorale possono essere visualizzati, tirare il globo fino a quando il nervo è esposto e usare le forbici per tagliare il nervo più a lungo possibile. Posto in formalina al 10% per l'elaborazione normale di esame istologico.
6. Rappresentante dei risultati:
Tumorspheres retinoblastoma inizierà ad apparire dal tessuto disaggregati quasi immediatamente come sono liberate dalla massa tumorale. Entro 2-4 giorni, più tumorspheres inizierà a formare e aumento delle dimensioni. Le sfere tendono ad essere regolari e mostrano una ben definita, la membrana che circonda l'aggregato secondaria (Figura 2).
L'animale si presenta tipicamente con leucocoria entro 4 settimane post-iniezione (figura 3b), seguita dall'ampliamento del globo e la distensione dei tessuti circostanti 5-8 settimane dopo l'iniezione come il tumore cresce (Figura 3c).
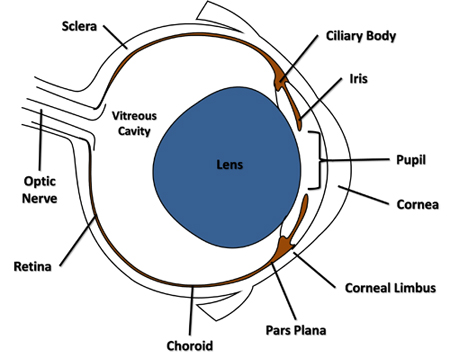
Figura 1. Sezione trasversale dell'occhio del mouse mettendo in evidenza le caratteristiche si fa riferimento nel protocollo.
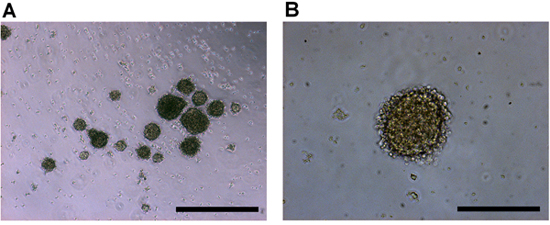
Figura 2. Retinoblastoma cultura di cellule umane in vitro ripreso a) 4x, e b) ingrandimento obiettivo 10x. Cellule del tumore primario retinoblastoma produrre tumorspheres con una forma regolare sferoidale e una membrana esterna croccante. Barre rappresentano una scala) 500 micron, e b) 200 micron.
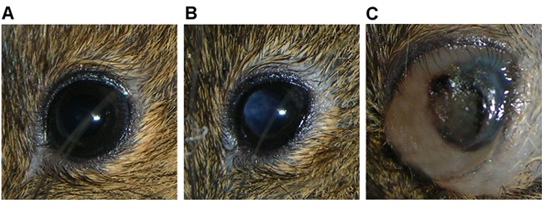
Figura 3 Eye of RAG2 -. / - Topo mostrando a) funzioni di normale, b) indicativi di una massa tumorale nella cavità vitrea leucocoria, e c) una massa tumorale grande riempiendo il mondo con distensione perioculare associati, emorragia intraoculare.
Discussione
La tecnica qui descritta favorisce i tumori nel loro propagazione retinoblastoma intraoculare, ambiente intravitreale. La tecnica di iniezione intraoculare è stata utilizzata in passato per creare i tumori da retinoblastoma derivate linee cellulari 1, nonché per fornire vettori virali per la terapia genica intraoculare 2,3. Questa tecnica è stata utilizzata con successo per la produzione di tumori retinoblastoma umano mediante iniezione diretta di cellule dal tumore primario e l'iniezione di tumorspheres, nonché la riproduzione seriale di tumori trapiantati. La prova visibile della formazione del tumore (di solito leucocoria) di solito è notata la prima volta entro 4 settimane, dopo di che emorragia intraoculare e distensione del / mondo e tessuti circostanti o l'orbita sviluppano entro 5-8 settimane. Una minoranza di topi iniettati ferire l'occhio iniettato, con conseguente chiusura permanente delle palpebre. In questi casi, la distensione è l'unico segno della formazione di tumori.
Istituzione di tumori murini trapiantati non ha avuto successo con tutti i tumori retinoblastoma umano, anche se la propagazione dei tumori trapiantati stabilito è di grande successo. Questa osservazione suggerisce che alcune caratteristiche del tumore primario, come l'invasività e il livello di differenziazione o di qualche altro fattore sconosciuto, può influenzare la capacità di questi tumori a persistere nell'ambiente oculare murino.
La quantità di tessuto che può essere acquisito da un tumore retinoblastoma umano è abbastanza piccola, e ci sono significative limitazioni sulla capacità di cellule di retinoblastoma cultura umana in vitro ad esempio come span durata limitata, perdita di istologia tumore solido e cambiamenti nel fenotipo cellulare. Questo protocollo fornisce un modo relativamente semplice per propagare il tumore umano e stabilire un modello murino della malattia umana. Questo permette inoltre in vitro e in vivo la sperimentazione della biologia di retinoblastoma e più manutenzione del tumore al di fuori del paziente.
Divulgazioni
Gli esperimenti sugli animali sono stati eseguiti in conformità con le linee guida e dei regolamenti previsti dal Baylor College of Medicine IACUC Comitato.
Riconoscimenti
Il finanziamento per questo progetto è fornito dalla Fondazione Clayton per la Ricerca e la Fondazione di Ricerca Retina.
Materiali
| Name | Company | Catalog Number | Comments |
| Nome | Azienda | Catalogo | Commenti |
|---|---|---|---|
| Fenilefrina HCl 2,5% | Bausch & Lomb | 053-11 | Soluzione oftalmica |
| 30-Ago ga | BD | 305128 | Conica regolare |
| 10-ml Luer-Lock siringa | BD | 309604 | |
| 3/10-cc insulina siringa | BD | 328431 | |
| Tamponi imbevuti di alcool | BD | 326895 | |
| 6-pozzetti, Tissue Culture-trattati | BD | 353046 | |
| Proparacaina HCl 0,5% | Maggiordomo AHS | 017239 | Soluzione oftalmica |
| Ketamina HCl 100mg/ml | Fort Dodge | 4402A | |
| 10-microlitri Hamilton siringa | Hamilton Azienda | 7648-01 | |
| 32-Ago ga Hamilton | Hamilton Azienda | 7803-04 | Personalizzati lunghezza - 0,5 " |
| Neurobasal-A Media | Invitrogen | 10888-022 | |
| B-27 Minus supplemento di vitamina A, 50X | Invitrogen | 12587-010 | |
| RPMI-1640 media | Mediatech | 10-040-CV | |
| Non essenziali soluzione di aminoacidi, 100X | Mediatech | 25-025-CI | |
| L-Glutammina, 100X | Mediatech | 25-005-CI | |
| Disposable Scalpel # 11 | Miltex | 4-411 | |
| Roditori Anestesia Combo | n / a | n / a | In-house formulazione farmacia (ketamina 37,6 mg / ml, xilazina 1,92 mg / ml, acepromazina 0,38 mg / ml) |
| Fattore umano ricombinante crescita epidermico (EGF) | StemCell Technologies | 02633 | Ricostituire a 10 mg / mL di soluzione di magazzino |
| Ricombinante umano di base fattore di crescita dei fibroblasti (bFGF) | StemCell Technologies | 02634 | Ricostituire a 10 mg / mL di soluzione di magazzino |
| OMS-75 Microscopio di funzionamento | Topcon Medical Systems | OMS-75 | Questo modello è stato interrotto |
| Formalina 10% | VWR | 95042-908 |
Riferimenti
- Chèvez-Barrios, P. Metastatic and Nonmetastatic Models of Retinoblastoma. Am. J. Pathol. 157, 1405-1412 (2000).
- Suber, M. L., Hurwitz, M. Y., Chèvez-Barrios, P., Hurwitz, R. L. Immune consequences of intraocular administration of modified adenoviral vectors. Hum. Gene Ther. 12, 833-838 (2001).
- Mallam, J. N., Hurwitz, M. Y., Mahoney, T., Chèvez-Barrios, P., Hurwitz, R. L. Efficient Gene Transfer into Retinal Cells Using Adenoviral Vectors: Dependence on Receptor Expression. Invest. Ophthalmol. Vis. Sci. 45, 1680-1687 (2004).
Ristampe e Autorizzazioni
Richiedi autorizzazione per utilizzare il testo o le figure di questo articolo JoVE
Richiedi AutorizzazioneThis article has been published
Video Coming Soon