È necessario avere un abbonamento a JoVE per visualizzare questo. Accedi o inizia la tua prova gratuita.
Method Article
Isolamento dei Nuclei Cardiomyocyte dal post-mortem del tessuto
In questo articolo
Riepilogo
Nuclei cardiaca sono isolati tramite sedimentazione densità e immunolabeled con anticorpi contro materiale pericentriolar 1 (PCM-1) per identificare e ordinare nuclei cardiomiociti mediante citometria a flusso.
Abstract
Identificazione dei nuclei cardiomiociti è stato impegnativo in sezioni di tessuto, come la maggior parte delle strategie di contare solo su proteine marker citoplasmatici 1. Eventi rari in miociti cardiaci quali la proliferazione e l'apoptosi richiedono una identificazione accurata dei miociti cardiaci nuclei di analizzare il rinnovamento cellulare in omeostasi e in condizioni patologiche 2. Qui, forniamo un metodo per isolare nuclei cardiomyocyte dal tessuto post mortem di sedimentazione densità e immunomarcatura con anticorpi contro materiale pericentriolar 1 (PCM-1) e la successiva selezione citometria a flusso. Questa strategia permette una analisi un elevato throughput e l'isolamento con il vantaggio di lavorare altrettanto bene su tessuti freschi e congelati materiale d'archivio. Ciò rende possibile studiare materiale già raccolto in biobanche. Questa tecnica è applicabile e testato in una vasta gamma di specie e adatto a molteplici applicazioni a valle, come il carbonio-14 datazione 3, cell-cyCLE analisi 4, la visualizzazione di analoghi della timidina (ad esempio BrdU e IDU) 4, l'analisi del trascrittoma ed epigenetici.
Protocollo
1. Isolamento dei Nuclei Cardiac
- Coat tubi ultracentrifuga (Tubi centrifuga Beckman # 363664) con 10 ml di 1% BSA / PBS soluzione di rivestimento. Coprire le provette e farli ruotare per 30 minuti in un rotatore tubo. Rimuovere la soluzione di rivestimento e lasciare la centrifuga tubi aria secca (un tubo per il cuore di topo è richiesto per l'analisi di cuore di topo singoli, alternativamente fino a 5 cuore di topo o 1 g di tessuto cardiaco da una specie diversa (ad esempio umano) può essere elaborato in un tubo).
- Tutti i passaggi seguenti devono essere eseguiti sul ghiaccio. Sezionare il ventricolo sinistro del mouse dal cuore fresco o snap-frozen con un bisturi. Attenzione, questo protocollo è ottimizzato per il cuore del mouse, ma può anche essere adattato per ratto o cuore umano. In alternativa, utilizzare fino a 1 g di tessuto cardiaco da una specie diversa.
- Tagliare il campione in cubicoli di piccole dimensioni con un bisturi.
- Trasferire i pezzi di tessuto in un tubo Falcon da 50 ml riempito con 15 ml di tampone di lisi.
- Omogeneizzare latessuto cardiaco con un T-25 Ultra-Turrax sonda omogeneizzatore (IKA) a 24.000 rpm per 10 sec.
- Diluire l'omogeneizzato con un volume uguale di tampone di lisi a 30 ml.
- Utilizzare un bicchiere douncer (40 ml) per omogeneizzare ulteriormente il tessuto e il libero nuclei. Eseguire otto colpi con un pestello gioco di grandi dimensioni.
- Passare il greggio isolare nuclei attraverso un 100 micron e 70 micron nylon mesh cellulare filtro (BD Biosciences), consecutivamente.
- Centrifugare la nuclei grezzo isolato in una centrifuga refrigerata (4 ° C) a 700 xg per 10 min.
- Rimuovere il surnatante attentamente invertendo i tubi e pulire l'interno del tubo con carta assorbente. Fare attenzione a non disturbare il pellet nuclei.
- Sciogliere il nuclei grezzo isolato in 5 ml di tampone saccarosio pipettando la soluzione più volte su e giù. Aggiungi un ulteriore 25 ml di tampone saccarosio alla disciolta pellet.
- Aggiungere 10 ml di tampone saccarosio appena preparato al tubo rivestito ultracentrifuga (vedi punto 1.1).
- Accuratamente sovrapporre il aggiunti 10 ml di tampone saccarosio con i nuclei pellet risospeso sciolto in tampone saccarosio dal passaggio 1,9.
- Bilanciare le provette prima di metterli in un rotore JS13.1 libera oscillazione e posizionare il rotore in una centrifuga ad alta velocità (Beckman Avanti S-25).
- Spin il campione nuclei a 13.000 xga 4 ° C per 60 min.
- Quando la rotazione è stata completata, rimuovere i tubi accuratamente dal rotore e scartare il supernatante invertendo i tubi e pulire i detriti restante dall'interno dei tubi con carta assorbente.
- Sciogliere i nuclei pellet in 1 ml di tampone nuclei di stoccaggio (NSB più buffer). Nota: NSB più contiene 1,5 mM spermina come stabilizzante DNA.
- Procedere con il punto 2.1, immunocolorazione dei nuclei cardiomiociti.
2. Immunoenzimatica per Citometria a Flusso
- Preparare il controllo negativo per immunocolorazione. Prelevare un 'aliquota di 20 microlitri di fuori del campione nuclei edd 980 pl di tampone NSB più.
- Aggiungi anti-pericentriolar materiale 1 anticorpi (di coniglio anti-PCM-1, anticorpi Atlas) al campione nuclei in una diluizione di 1:500 per nuclei immunolabel cardiomiociti. Aggiungere l'anticorpo isotipo nella stessa diluizione come l'anti-anticorpo PCM-1 per il controllo negativo, preparato nella fase 2,1.
- Incubare controllo negativo e la provetta a 4 ° C per una notte.
- Lavare controllo negativo e campione almeno una volta con NSB più tampone (spin down tubi in una centrifuga refrigerata (4 ° C) a 700 xg per 10 min. Eliminare il surnatante e sciogliere il nuclei pellet in 1 ml di tampone più NSB).
- Aggiungi anti-coniglio immunofluorescenza secondario (FITC o APC) al controllo negativo e la provetta in una diluizione di 1:1000.
- Incubare controllo negativo e la provetta a 4 ° C per 1 h.
- Lavare controllo negativo e campione almeno una volta con NSB più tampone (spin down tubi in una centrifuga refrigerata (4 ° C) a 700 xg per 10 min. Gettare il surnatante e sciogliere i nuclei pellet in 1 ml di NSB più buffer).
- Procedere con l'analisi di citometria di flusso e di smistamento.
3. Citometria a Flusso
- Coat nuclei provette Falcon (15 ml) con 1% BSA / PBS soluzione prima di iniziare la citometria a flusso di smistamento come descritto al punto 1,1.
- Filtrare il campione e il controllo negativo tramite un setaccio cella 30 um e caricare il primo controllo negativo al citofluorimetro (Influx BD). Definire il primo cancello e la seconda per definire nuclei e canottiere (nuclei singola), sulla base di forward scatter (FSC), larghezza di impulso in avanti scatter (FS larghezza d'impulso) e Side Scatter (SSC) (Fig. 2a e b). Aggiunta di un DNA macchia (DRAQ5 (1:500)) per il campione può aiutare a identificare la popolazione nuclei inizialmente.
- Caricare il campione immunolabeled e definire la terza porta per isolare nuclei cardiomiociti (PCM-1-positve) da non-cardiomiociti nuclei (PCM-1-negativo). Avviare l'ordinamento(Fig. 2c e d).
Optional: Al fine di analizzare il contenuto nucleare di DNA (ploidia) e di eseguire l'analisi del ciclo cellulare aggiungere un DNA adeguato macchia per i nuclei (ad esempio, Hoechst 33342 o DRAQ5) (Fig. 2e).
- Dopo cernita citometria di flusso, posizionare i nuclei su ghiaccio e ri-analisi per determinare la purezza di smistamento (Fig. 3a e b).
- Centrifugare la nuclei ordinato nei tubi di raccolta a 1500 xg in una centrifuga refrigerata per 15 min.
- Sciogliere il nuclei pellet in un buffer compatibile con l'applicazione a valle.
4. Risultati rappresentativi
Nuclei morfologia e l'integrità può essere valutata attraverso macchie di DNA e visualizzati al microscopio (Fig. 1). Successo PCM-1 di etichettatura può essere valutata mediante microscopia in epifluorescenza e mediante citometria a flusso (Fig. 1 e Fig. 2c e d). PCM-1-positiVE e popolazioni negativi devono essere ben separati uno dall'altro (Fig. 2c e d). In murino ventricolo sinistro circa il 30% di tutti i nuclei dovrebbe essere nuclei cardiomiociti (Fig. 2d). Ordinamento purezza può essere valutata da ri-analizzando i nuclei ordinati (Fig. 3a e b). Entrambe le popolazioni nuclei dovrebbe avere una purezza superiore al 95% di smistamento.
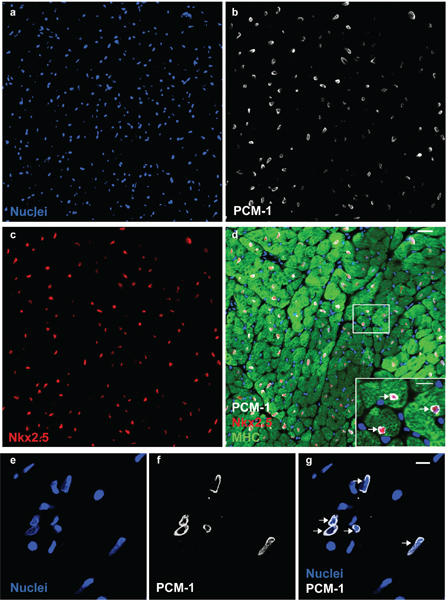
Figura 1. PCM-1 identifica nuclei cardiomiociti. Nuclei cardiaca (a) vengono colorate con anticorpi anti PCM-1 (b) e per Nkx2.5 (c) in un cuore topo adulto. (D) PCM-1-marcato nuclei sono circondati da citoplasma cardiomiociti (catena pesante della miosina (MHC)) ed esprimere il fattore di trascrizione Nkx2.5, che documenta l'identificazione accurata dei nuclei cardiomiociti da PCM-1 colorazione (scala di 20 bar e 10 micron micron (d, inserto)). (E) isolati nuclei cardiache visualizzati con il DNA macchia DRAQ5. (F e G) Cardiomyocnuclei yte sono etichettati con anticorpi contro il PCM-1 (scala bar 10 micron). Nota, il pattern di colorazione epinuclear PCM-1 in nuclei muscolari in sezione del tessuto e in nuclei isolati (frecce).
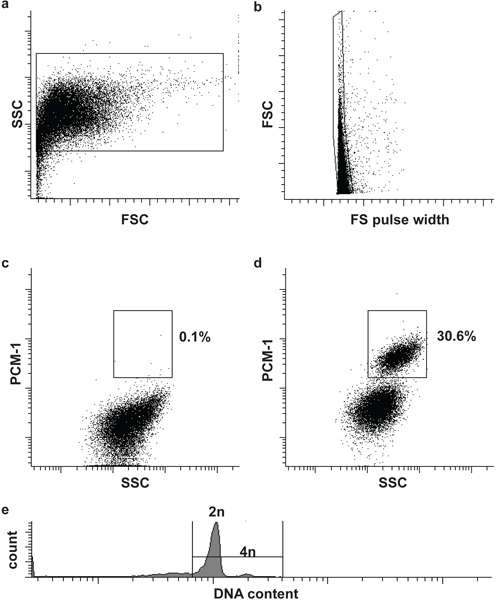
Figura 2. Citometria a flusso ordinamento dei nuclei cardiomiociti. (A) nuclei Cardiac sono identificati dalla forward scatter (FSC) e lato scatter (SSC). (B) Una seconda porta identifica i singoli nuclei da FSC e FS larghezza di impulso 5. (C, d) gating fluorescente permette la separazione dei nuclei cardiomiociti (PCM-1-positive) e non-cardiomiociti (PCM-1-negativi) nuclei di tessuto cardiaco. (E) cardiomiociti mouse sono in gran parte (> 80%) diploide (2n), solo un piccolo sottoinsieme è tetraploide (4n) 6. Nota, cardiomiociti umani contengono una maggiore frequenza di nuclei poliploidia (> 2n) 7,8.

Figura 3. Analisi di purezza ordinati nuclei cardiomiocita e non cardiomiociti. Re-analisi di ordinato nuclei non cardiomiociti (a) e cardiomiociti (b). Entrambe le popolazioni mostrano una purezza superiore al 99% di smistamento.
Access restricted. Please log in or start a trial to view this content.
Discussione
Identificazione accurata di nuclei cardiomiocita è cruciale per l'analisi dei processi rigenerativi nel miocardio 2,3. Le tecniche convenzionali per isolare cardiomiociti di tessuto fresco si basa principalmente sulla digestione enzimatica delle proteine della matrice extracellulare e la successiva purificazione dalle cellule interstiziali mediante centrifugazione a bassa velocità. Ulteriore purificazione di cardiomiociti viventi di cellule staminali embrionali (ESC) può essere eseguita da immuno...
Access restricted. Please log in or start a trial to view this content.
Divulgazioni
Non ci sono conflitti di interesse dichiarati.
Riconoscimenti
Ci piace riconoscere Marcelo Toro per l'assistenza con la citometria a flusso. Questo studio è stato sostenuto dalla svedese Heart-Lung Foundation e, Commissione UE FP7 "CardioCell", Consiglio svedese della ricerca, AFA assicurazioni e ALF. OB è stato sostenuto da Deutsche Forschungsgemeinschaft.
Access restricted. Please log in or start a trial to view this content.
Materiali
| Name | Company | Catalog Number | Comments |
| 1. Lysis Buffer | |||
| Nome del reattivo | |||
| 0,32 M di saccarosio | |||
| 10 mM Tris-HCl (pH = 8) | |||
| 5 mM CaCl 2 | |||
| 5 mM acetato di magnesio | |||
| 2,0 mM EDTA | |||
| 0,5 mM EGTA | |||
| 1 mM DTT |
| 2. Saccarosio tampone |
| Nome del reattivo |
| 2,1 M saccarosio |
| 10 mM Tris-HCl (pH = 8) |
| 5 mM acetato di magnesio |
| 1 mM DTT |
| 3. Nuclei soluzione per la conservazione (NSB plus) |
| Nome del reattivo |
| 0,44 M di saccarosio |
| 10 mM Tris-HCl (pH = 7,2) |
| 70 mM KCl |
| 10 mM MgCl 2 |
| 1,5 mM spermina |
| Reagenti e materiale | Azienda |
| Isotipo IgG di coniglio ChIP-Grade, # ab37415 | Abcam |
| Coniglio anti-PCM-1 anticorpo, # HPA023374 | Atlas Anticorpi |
| Donkey sec. anticorpo anti-coniglio Alexa Fluor 488, # A-21.206 o equivalente sec. immunofluorescenza | Life Technologies |
| DRAQ5 | Biostatus |
| filtri cella 30 micron, 70 micron e 100 micron | BD Biosciences |
| Douncer vetro (40 ml) epestello "L" | VWR (Wheaton Industries Inc.) |
| T-25 Ultra-Turrax | IKA Germania |
| Disperdente strumento S25 N-18 G | IKA Germania |
| Centrifuga Beckman Avanti | Beckman Coulter |
| Provette Falcon da 15 ml e 50 ml | VWR |
| Tubi centrifuga Beckman # 363664 | Beckman Coulter |
| JS13.1 rotore oscillante libero | Beckman Coulter |
| Influx citometro | Beckman Coulter |
| Tubo Rotator | VWR |
Riferimenti
- Ang, K. L. Limitations of conventional approaches to identify myocyte nuclei in histologic sections of the heart. American journal of physiology. Cell physiology. , 298-1603 (2010).
- Bergmann, O. Identification of cardiomyocyte nuclei and assessment of ploidy for the analysis of cell turnover. Experimental cell research. 327, 188-194 (2011).
- Bergmann, O. Evidence for Cardiomyocyte Renewal in Humans. Science. 324, 98-102 (1126).
- Walsh, S. Cardiomyocyte cell cycle control and growth estimation. Cardiovascular Research. , 1-31 (2010).
- Spalding, K., Bhardwaj, R. D., Buchholz, B., Druid, H., Frisén, J. Retrospective birth dating of cells in humans. Cell. 122, 133-143 (2005).
- Adler, C. P., Friedburg, H., Herget, G. W., Neuburger, M., Schwalb, H. Variability of cardiomyocyte DNA content, ploidy level and nuclear number in mammalian hearts. Virchows Arch. 429, 159-164 (1996).
- Herget, G. W., Neuburger, M., Plagwitz, R., Adler, C. P. DNA content, ploidy level and number of nuclei in the human heart after myocardial infarction. Cardiovascular Research. 36, 45-51 (1997).
- Adler, C. P., Friedburg, H. Myocardial DNA content. ploidy level and cell number in geriatric hearts: postmortem examinations of human myocardium in old age. Mol. Cell Cardiol. 18, 3953-39 (1986).
- Dubois, N. C. SIRPA is a specific cell-surface marker for isolating cardiomyocytes derived from human pluripotent stem cells. Nature. 29, 1011-1018 (2011).
- Hattori, F. Nongenetic method for purifying stem cell-derived cardiomyocytes. Nature Methods. 7, 61-66 (2010).
- Fransioli, J. Evolution of the c-kit-Positive Cell Response to Pathological Challenge in the Myocardium. Stem Cells. 26, 1315-1324 (2008).
- Elliott, D. A. NKX2-5(eGFP/w) hESCs for isolation of human cardiac progenitors and cardiomyocytes. Nature Methods. 8, 1037-1040 (2011).
- Laflamme, M. A. Evidence for Cardiomyocyte Repopulation by Extracardiac Progenitors in Transplanted Human Hearts. Circulation Research. 90, 634-640 (2002).
- Srsen, V., Fant, X., Heald, R., Rabouille, C., Merdes, A. Centrosome proteins form an insoluble perinuclear matrix during muscle cell differentiation. BMC cell biology. 10, 28(2009).
- Spoelgen, R. A novel flow cytometry-based technique to measure adult neurogenesis in the brain. Journal of neurochemistry. 119, 165-175 (2011).
- Soonpaa, M. H., Kim, K. K., Pajak, L., Franklin, M., Field, L. J. Cardiomyocyte DNA synthesis and binucleation during murine development. The American journal of physiology. 271, H2183-H2189 (1996).
- Olivetti, G. Aging, cardiac hypertrophy and ischemic cardiomyopathy do not affect the proportion of mononucleated and multinucleated myocytes in the human heart. J Mol Cell Cardiol. 28, 1463-1477 (1996).
- Okada, S. Flow cytometric sorting of neuronal and glial nuclei from central nervous system tissue. Journal of cellular physiology. 226, 552-558 (2011).
- Matevossian, A., Akbarian, S. Neuronal Nuclei Isolation from Human Postmortem Brain Tissue. J. Vis. Exp. (20), e914(2008).
Access restricted. Please log in or start a trial to view this content.
Ristampe e Autorizzazioni
Richiedi autorizzazione per utilizzare il testo o le figure di questo articolo JoVE
Richiedi AutorizzazioneThis article has been published
Video Coming Soon