È necessario avere un abbonamento a JoVE per visualizzare questo. Accedi o inizia la tua prova gratuita.
Method Article
Tirando nanotubi di membrana da vescicole unilamellari gigante
* Questi autori hanno contribuito in egual misura
In questo articolo
Riepilogo
Molte proteine nella cellula senso e inducono la curvatura della membrana. Descriviamo un metodo per tirare nanotubi di membrana da vescicole lipidiche per studiare l'interazione delle proteine o qualsiasi molecola di curvatura-attivo con membrane curvo in vitro.
Abstract
Il rimodellamento della membrana cellulare è parte integrante di molti fenomeni cellulari, come ad esempio endocitosi, traffici illeciti, la formazione di filopodi, ecc. Molte proteine diverse associano con membrane curve a causa della loro capacità di percepire o indurre la curvatura della membrana. In genere, questi processi comportano una moltitudine di proteine che li rende troppo complessa per studiare quantitativamente nella cella. Descriviamo un protocollo per ricostituire una membrana curvilinea in vitro, che imita una struttura cellulare curva, come il collo di endocitosi. Delle vescicole unilamellari gigante (GUV) viene utilizzata come modello di una membrana cellulare, in cui pressione interna e la tensione superficiale sono controllato con l'aspirazione di una micropipetta. L'applicazione di una forza di trazione di punto su GUV utilizzando pinzette ottiche crea un nanotubo ad alta curvatura collegato ad una membrana piatta. Questo metodo è stato utilizzato tradizionalmente per misurare le proprietà meccaniche fondamentali delle membrane lipidiche, quali rigidità di piegamento. Negli ultimi anni, esso è stato ampliato per studiare come le proteine interagiscono con curvatura della membrana e il modo che interessano la forma e la meccanica delle membrane. Un sistema che unisce la micromanipolazione, microiniezione, Pinzetta ottica e microscopia confocale permette la misura della curvatura della membrana, tensione nelle membrane e la densità di superficie delle proteine, contemporaneamente. Da queste misurazioni, si può dedurre molte importanti proprietà meccaniche e morfologiche del sistema proteina-membrana. Inoltre, abbiamo stendere un protocollo di creazione GUV in presenza di concentrazione salina fisiologica e un metodo per quantificare la densità superficiale delle proteine sulla membrana da intensità di fluorescenza di etichettato proteine e lipidi.
Introduzione
Molti processi cellulari, come endocitosi, traffici illeciti, la formazione di filopodi, infezione, ecc., sono accompagnati da un drammatico cambiamento nella forma di membrane cellulari1,2. Nella cella, un numero di proteine partecipa a questi processi legandosi alla membrana e alterare la loro forma. Gli esempi più notevoli sono membri della famiglia di proteine Bin/anfifisina/Rvs (BAR), contenente una caratteristica intrinsecamente curvata BAR dominio3,4,5,6,7. In genere, essi interagiscono con la membrana aderendo il dominio di BAR alla superficie e, in molti casi, anche superficialmente inserimento eliche amphipathic in doppio strato. La forma, la dimensione e la carica del dominio BAR insieme al numero delle eliche amphipathic determina: (1) la direzione della curvatura della membrana (cioè, se inducono i invaginations o sporgenze) e (2) l'entità della membrana curvatura5,8. Di nota, qui curvatura positiva è definito come il lato convesso della membrana curvilinea, vale a dire, il rigonfiamento verso la particella interagente e negativa altrimenti. Inoltre, gli studi quantitativi di BAR proteine ha rivelato che il loro effetto sulla membrana dipende un set di parametri fisici: densità di proteine, tensione nelle membrane e forma di membrana (piatto contro tubolare contro sferica di superficie forma)7. In base a questi parametri BAR proteine può: (1) fungono da sensori di curvatura della membrana, (2) piegare membrane o (3) indurre membrana scissione7.
Dovuto il numero di componenti coinvolti nella membrana rimodellamento nella cella, studiando gli aspetti quantitativi dei fenomeni, quali endocitosi, in vivo è estremamente impegnativo. In vitro la ricostituzione del numero minimo di componenti che imita curve membrane nella cella fornisce mezzi per acquisire una comprensione meccanicistica di proteine di membrana-curvatura come operare. Questo articolo descrive un protocollo per ricostituire una membrana nanotubi in vitro mediante micromanipolazione, microscopia confocale e pinzette ottiche. L'approccio può essere utilizzato per studiare in modo quantitativo, come proteine, lipidi o piccole molecole interagiscono con le membrane curve. GUV del lipido sono utilizzati come modelli di una membrana cellulare, cui curvatura è trascurabile rispetto alle dimensioni delle molecole interagenti curvatura a membrana. Essi sono preparati utilizzando il metodo di electroformation9 in cui le vescicole sono formate da idratante un film lipidico e gonfiore in GUV sotto una corrente alternata (AC)10. Sono più comuni substrati su cui sono coltivati GUV o semi-conduttori piatti ricoperti di ossido della latta dell'indio (ITO) o fili di platino (Pt-fili)11. In questo lavoro, GUV sono coltivate su Pt-fili come questo metodo ha dimostrato di funzionare molto meglio rispetto all'alternativa nel rendere GUV in presenza di sali nei buffer12. Anche se il protocollo di electroformation è qui descritto in dettaglio sufficiente per riprodurlo, rimandiamo il lettore ad articoli precedenti in cui simili e altri metodi di fare GUV sono stati descritti in dettaglio13,14. Nelle nostre mani, electroformation il Pt-fili ha correttamente dato GUV da un mix di lipidi sintetici o da lipidiche naturali estratti in un tampone contenente ~ 100 mM NaCl. Inoltre, era anche possibile incapsulare GUV contiene proteine durante la crescita. Una camera di electroformation esempio è mostrata in Figura 1A; si compone di due ~ 10 cm-lunghezza Pt-fili inserite in un supporto effettuato in politetrafluoroetilene (PTFE) che può essere sigillato su entrambi i lati con lamelle di vetro ~ 1-2 cm di distanza (Figura 1A).

Figura 1: messa a punto sperimentale. (A) il GUV electroformation camera con connettori elettrici collegati ai fili di Pt. Sinistra (B): il sistema sperimentale mostrando il microscopio, la camera sperimentale sopra l'obiettivo e due Micropipette (sinistra e destra) associati ad i micromanipolatori e inseriti nella camera sperimentale per tubo tirando e proteina iniezione. A destra: una vista ravvicinata della camera sperimentale montato sopra l'obiettivo mostrando le punte di aspirazione e le micropipette di iniezione inserite. (C) A siringa dotata di un erogatore sottile inserito in una micropipetta a suo back-end. Il fondo è una vista ravvicinata del dispenser all'interno la micropipetta con la linea tratteggiata blu che delinea la micropipetta. Questo sistema è utilizzato per riempire la micropipetta con caseina per passivare la superficie di vetro e anche per eseguire il riempimento con olio minerale quando necessario. (D) A sistema utilizzato per aspirare quantità µ l della soluzione della proteina. L'ago è collegato ad una siringa e al tubo che è collegato alla micropipetta di iniezione. La punta della micropipetta è accuratamente immerso nella soluzione della proteina e aspirata così per riempire la punta della micropipetta. La micropipetta indietro viene poi riempita con olio minerale, utilizzando il sistema mostrato nel pannello di C. Clicca qui per visualizzare una versione più grande di questa figura.
Un nanotubo di membrana, che vanno nel raggio da 7 a diverse centinaia nm, può essere tirato da un capo da una forza esterna. Questo metodo è stato inizialmente progettato per misurare le proprietà elastiche delle membrane cellulari e vescicole, ad esempio il piegamento rigidità15,16. Nelle opere più recenti, il metodo è stato esteso per studiare l'interazione delle proteine con membrane curve di microinjecting le proteine vicino il nanotubo tirato7,17. Altri metodi sono stati sviluppati per lo studio delle proteine di membrana-curvatura. In un unico metodo, proteine vengono incubate con diverse dimensioni liposomi legati ad una superficie passivata. La microscopia confocale è utilizzata per misurare il legame con le proteine in funzione del diametro di liposomi, che può indicare indotta da curvatura ordinamento18,19. In un altro metodo, proteine vengono iniettate nei pressi di un micro-aspirato GUV per misurare la loro capacità di indurre spontaneamente tubuli20,21. Il metodo descritto in questo protocollo è in grado di studiare la curvatura a membrana proteine coinvolte nell'endocitosi, dove la maggior parte delle proteine in genere incontrano nanotubi di membrana preformata collegando l'invaginazione della membrana contenenti merci con il fondo piatto della membrana plasmatica. Inoltre, in questo metodo, a differenza nell'analisi con liposomi piccoli tethered, i nanotubi di membrana sono continuamente collegato alla membrana; Pertanto, è in equilibrio meccanico con il capo, una situazione previsto in vivo. Quindi, fisica fondamentale della membrana si applica e si può dedurre una pletora di proprietà meccaniche da nostre misure22,23,24.
Per una piena attuazione di questo metodo, l'attrezzatura comprende un microscopio confocale, pinzette ottiche e uno o due Micropipette collegate ad un serbatoio di acqua (Figura 1B). Combinando tutti e tre, è possibile misurare la tensione della membrana, membrana della curvatura, densità di superficie delle proteine, e contemporaneamente forza25del tubo. Micropipetta aspirazione è essenziale e facilmente è costruito mediante l'inserimento di una micropipetta di vetro in un supporto collegato ad un serbatoio di acqua, che, tramite pressione idrostatica, controlla la pressione di aspirazione26. La micropipetta e il titolare sono controllati da un micromanipolatore e, idealmente, in una direzione da un attuatore piezoelettrico per il movimento di precisione. Per tirare un nanotubo, la microaspirated GUV brevemente è attaccato ad una perlina micron imprese poi tirata via creando un nanotubo. In questa implementazione, il tallone è detenuto da Pinzetta ottica, che può essere costruita seguendo un protocollo pubblicato27. È possibile fare a meno delle pinzette ottiche e nanotubi di tirare in modi diversi, anche se a costo di misure di forza accurata. Se è troppo difficile da costruire un'ottica trap o se misure di forza sono non essenziali, come se uno vuole semplicemente verificare la preferenza delle proteine per membrane curve, un tubo può essere estratto utilizzando una perlina aspirata all'estremità di una micropipetta secondo28. È anche possibile tirare tubi mediante forza gravitazionale29 o30,31di flusso. Inoltre, la microscopia confocale è non è essenziale; Tuttavia, si è preferito così per misurare la densità di superficie delle proteine. Permette inoltre di misurare il raggio di nanotubi da intensità di fluorescenza dei lipidi nel tubo, così indipendentemente dalla forza della membrana e la tensione. Raggio del tubo deduzione da fluorescenza è particolarmente importante se il rapporto tra queste quantità si discosta dalle equazioni ben consolidate a causa della presenza di proteine di membrana-aderito25. Cosa importante, uno non può erogare della trappola ottica e microscopia confocale, poichè non è possibile misurare la curvatura del tubo.
Il metodo descritto in questo protocollo è stato utilizzato per studiare l'ordinamento di curvatura-indotta di varie proteine di membrana periferici su nanotubi, soprattutto quelli dalla famiglia25,BAR32,33,34 . Inoltre è stato indicato che il canale del potassio del transmembrane conicamente sagomato che KvAP si arricchisce il curvo nanotubi nello stesso modo come BAR proteine35. Grazie all'ottimizzazione del metodo per incapsulare GUV contiene proteine, l'interazione delle proteine con curvatura negativa è stato recentemente studiato come ben36. Inoltre, questo metodo è stato usato per delucidare la formazione di proteina scaffold25,37 e per studiare il meccanismo di scissione di membrana da entrambi linea tensione38, proteina dinamina39, o da BAR proteine40,41. Oltre alle proteine, piccole molecole o ioni possono anche indurre la curvatura. Utilizzando questo metodo, gli ioni di calcio sono stati indicati per indurre la curvatura positiva sotto condizioni senza sale42. Interessante, ha anche dimostrato che i lipidi possono subire curvatura differenziata, anche se solo per le composizioni che sono vicino a un demixing punto43,44. In sintesi, il metodo può essere utilizzato dai ricercatori interessati a indagare come entrambi componenti integrali di membrana (ad es., lipidi o proteine transmembrana) o marginalmente associazione molecole (sia all'interno o all'esterno di GUV) interagire con membrane cilindricamente curve, dal punto di vista meccanico e quantitativa. Inoltre è inteso per coloro che sono interessati a misurare le proprietà meccaniche della membrana stessa22,23,45.
Protocollo
1. preparazione del Guv da Electroformation su Pt-fili
- Pulire la camera di electroformation (Vedi Introduzione e Figura 1A) e i Pt-fili con un solvente organico come etanolo o acetone per lavare via i lipidi e con acqua per lavare via i sali.
Nota: Consigliamo di lasciare asciugandosi il residuo con tessuto imbevuto di etanolo prima sonicating in acetone, etanolo, quindi acqua, ciascuno per 5 min. - Preparare una miscela di lipidi di una composizione lipidica desiderata a 1 mg/mL in cloroformio. Il mix deve contenere ~ 0.05% frazione molare di un lipide coniugato con biotina (ad es., 1,2-distearoyl-sn-glycero-3-phosphoethanolamine-N-[biotinyl(polyethyleneglycol)-2000]) e ~ 0,5% frazione molare di un lipide coniugato con un fluoroforo ( ad esempio, BODIPY-TR-C5-ceramide).
Nota: Nella nostra esperienza, era difficile produrre GUV a un alto rendimento contenente più del 30% addebitato i lipidi.
Attenzione: Cloroformio deve essere gestita all'interno di una cappa chimica indossare guanti appropriati. - Inserire una coppia di Pt-fili nella camera electroformation. Depositare il mix del lipido su Pt-fili in gocce separate da ~ 2-3 mm (totale ~ 4 µ l della miscela).
- Asciugare i fili sotto vuoto per 30 – 60 min a temperatura ambiente.
- Sigillare il fondo della camera aderendo il coprioggetto sopra la camera utilizzando grasso al silicone. Riempire la camera con una soluzione tamponata contenente NaCl, saccarosio e un agente tampone (ad es., 70 mM NaCl, saccarosio 100 mM e 10 mM Tris, pH 7.4). Questo mezzo sarà dentro il GUV nell'esperimento. È essenziale che l'osmolarità di questo mezzo corrisponda l'osmolarità del mezzo sperimentale all'interno di ~ 10%. Utilizzare saccarosio per regolare l'osmolarità. Se l'obiettivo è quello di incapsularlo nel Guv, aggiungere proteine alla soluzione ad una concentrazione desiderata.
Attenzione: Vari sali e zuccheri nel buffer possono influenzare la rigidità di piegamento e la curvatura spontanea delle membrane24,42,46,47. - Sigillare la parte superiore della camera di aderendo un vetrino coprioggetto con grasso al silicone garantire aria minima all'interno della camera. Applicare una corrente sinusoidale AC attraverso i Pt-fili a 500 Hz e 280 mV.
Nota: Il tempo di crescita e la temperatura devono essere ottimizzati a seconda della composizione lipidica e la sensibilità della proteina. Quando si utilizza estratti naturali del lipido e anche quando si incapsula proteine in Guv, il migliore rendimento è stato raggiunto da una crescente GUV a 4 ° C durante la notte. In assenza di proteine e per le composizioni dei lipidi sintetici, crescita a temperatura ambiente per ~ 2 ore era sufficiente.
2. preparazione della sezione sperimentale e le micropipette
- Per preparare le micropipette, tirare un capillare di vetro utilizzando un estrattore di pipetta. Si consiglia di utilizzare un capillare di vetro con raggi interni ed esterni di, rispettivamente, 0,7 mm e 1 mm. Quindi, affinare la punta della micropipetta affinché suo diametro interno è 5–7 µm, utilizzando un microforge. Se proteine o altre molecole saranno iniettati nell'esperimento, tirare un'altra micropipetta e raffinare la sua punta ad un diametro interno di 8–15 µm.
- Costruire una camera sperimentale posizionando due vetrini coprioggetto microscopia rettangolare su una base metallica, come illustrato nella Figura 1. Le lamelle devono essere separate da ~ 1 mm. La camera dovrebbe avere aperture lungo i bordi lunghi (Vedi Figura 1). I lati aperti dovrebbero andare bene la punta della micropipetta dove la punta dovrebbe raggiungere almeno il centro della camera.
- Preparare il tampone sperimentale cui osmolarità non deve differire di oltre il 10% dal buffer utilizzato per crescere GUV. Regolare l'osmolarità con glucosio. Un esempio di un buffer sperimentale che è stato usato nello studiare l'interazione di endophilin con nanotubi è NaCl 100 mM, 40 millimetri di glucosio, tamponata con Tris pH 7,4. Una combinazione di saccarosio all'interno / glucosio all'esterno garantisce: (a) sufficiente contrasto di fase per osservare GUV con microscopia luminosa del campo e (b) alta densità all'interno il GUV che li induce a depositarsi sul fondo della camera. Regolare la concentrazione di sale sulla base del requisito sperimentale.
Nota: Oltre a influire sulle proprietà meccaniche della membrana, nella nostra esperienza, alta concentrazione nel glucosio (> 300 mM) influisce negativamente l'istituzione di legami di streptavidina-biotina, necessaria per tirare un nanotubo. Inoltre, troppo poco sale inibisce la streptavidina-biotina obbligazioni, mentre troppo alto di una concentrazione schermi interazioni proteina-membrana. In caso di incapsulamento di proteina, utilizzando molto alta concentrazione di sale nel buffer esterno (ad es., > 200 mM NaCl) può essere utilizzato come un trucco per staccare le proteine dal volantino esterno36. È necessario sperimentare con una gamma di concentrazione salina di trovare le condizioni ottimali di legame della molecola di interesse. -
30 – 60 min prima di raccogliere GUV per l'esperimento, passivare le superfici di vetro, riempiendo la camera sperimentale e la micropipetta di aspirazione con una soluzione di 5 mg/mL di un β-caseina altamente puro (ad es., dissolto nel buffer sperimentale). Β-caseina crea uno strato protettivo sulle superfici di vetro, prevenendo GUV per aderire troppo fortemente, che potrebbe causare loro di scoppiare. Incubare con β-caseina per 30 – 60 min.
Nota: non ci dovrebbe essere nessun bolle all'interno della micropipetta che potrebbero interferire con il controllo di tensione della membrana.- Per costruire un dispenser per il riempimento di micropipette, rompere un ago di siringa vicino il connettore di plastica e colla in esso un capillare di silice sottile (come quelli usati per cromatografia in fase liquida) (Figura 1).
- Durante l'incubazione con β-caseina, montare la camera sul microscopio e centrarla sopra l'obiettivo. Inserire la punta della micropipetta di aspirazione attraverso l'apertura sul bordo lungo e portare la punta sopra l'obiettivo del microscopio. Regolare il livello del serbatoio dell'acqua in modo che la pressione di aspirazione è vicino a zero (non ci dovrebbe essere nessun flusso pesante dentro o fuori la pipetta, che può essere visto al microscopio).
-
Nel caso in cui le proteine o altre molecole verranno iniettati durante l'esperimento, riempire la micropipetta di iniezione con la molecola desiderata dissolta nel buffer sperimentale ad una concentrazione di scelta, montare la micropipetta all'interno di un micromanipolatore, e Inserire attraverso il lato opposto della camera sperimentale.
- Per utilizzare una minima quantità di proteine, riempire solo la punta di una micropipetta con la proteina dall'aspirazione. Per farlo, avvolgere l'estremità di un ago collegato ad una siringa con tubazione di plastica. Inserire il tubo nella parte posteriore della micropipetta iniezione.
- Molto attentamente immergere la punta della micropipetta nella soluzione della proteina ed aspirare per riempire la punta della micropipetta.
Nota: Questa semplice configurazione è mostrata in Figura 1 e, nella nostra esperienza, permette di aspirare da appena pochi µ l della soluzione della proteina. - Recupero informazioni il resto della micropipetta di iniezione con olio minerale per evitare la miscelazione della soluzione della proteina e l'acqua dal serbatoio dell'acqua (utilizzando il programma di installazione in Figura 1).
- Fare attenzione a non introdurre bolle d'aria la pipetta di iniezione, come il suo agire può indurre la pressione di iniezione instabile. In alternativa, se la quantità di proteina è sufficiente, riempire la micropipetta con le proteine alla stregua di riempimento con β-caseina come descritto al punto 2.4. Regolare il livello del serbatoio di acqua per ridurre al minimo la pressione di aspirazione nella pipetta di iniezione.
Nota: La concentrazione del iniettato molecola o ione vicino il nanotubo sta per essere inferiore a causa della diluizione e può essere valutato misurando la diminuzione di intensità di fluorescenza in funzione della distanza dalla pipetta uscita42. È tuttavia più importante conoscere la densità associato a doppio strato della molecola iniettata, che può essere misurata con precisione (Vedi sezione 4).
- Dopo incubazione con β-caseina, rimuovere la soluzione dalla camera e risciacquare con il buffer sperimentale diverse volte. Riempire con il buffer di sperimentale.
- Smettere di electroformation di GUV e ritirarli direttamente i fili di Pt. Aggiungere pochi µ l della soluzione GUV alla camera sperimentale. Utilizzare solo preparata GUV.
- Aggiungere pochi µ l di perline rivestite con streptavidina alla camera sperimentale per una concentrazione finale di perline nella camera a circa 0,1 x 10− 3% (p/v) o meno. Perle di polistirolo ~ 3 µm di diametro sono raccomandati (perle di polistirolo in acqua hanno un contrasto di indice di rifrazione quasi ottimali per quanto riguarda massimizzando la forza di gradiente per quanto riguarda la forza di dispersione nella trappola ottico). La concentrazione della perla può essere regolata basata sull'esperimento: una concentrazione molto bassa rende difficile trovarli in aula, e una concentrazione troppo alta corre il rischio di cadere le pinzette ottiche più di perline.
3. tirando un nanotubo di membrana da un GUV
- Lasciate che il GUV e le perle si depositano alla parte inferiore della camera. Sgonfiare il GUV lasciando un po' del buffer sperimentale evaporare, per circa ~ 15 min sgonfiando il GUV è essenziale per produrre qualche zona in eccesso che può essere aspirato con la micropipetta. GUV dovrebbe visibilmente ondeggiano (cioè, appaiono floppy) sotto il microscopio chiaro. Se appaiono tese, consentono più tempo di evaporazione.
Nota: Il tasso di cambiamento di osmolarità dipende la superficie di evaporazione, la temperatura, ecc.e deve essere attentamente monitorato. In linea di principio, la differenza di osmolarità potrebbe essere impostata dall'inizio regolando la concentrazione di saccarosio e glucosio, tuttavia, si dovrebbe prestare attenzione non per indurre un shock osmotico. - Trovare un disco floppy GUV ed esso aspirare nella pipetta. La lunghezza della linguetta aspirazione (la parte della membrana all'interno della pipetta) deve essere uguale o maggiore del raggio di pipetta per l'analisi teorica di essere applicabile15,16,22,(23 Figura 2). Provare diversi GUV. Se nessuno del Guv può essere aspirato per produrre una lingua abbastanza a lungo, attendere qualche minuto. Se GUV sono abbastanza floppy, procedere al passaggio successivo.
- Tenuta la camera con olio minerale, per impedire ulteriore evaporazione del buffer. Farlo pipettando accuratamente l'olio lungo i bordi aperti della camera sperimentale.
- Per impostare la posizione zero della pressione di aspirazione, in primo luogo, cercare una perlina in aula e posizionare l'uscita di pipetta di aspirazione vicino il tallone. Regolare l'altezza del serbatoio dell'acqua in modo che il tallone non viene aspirato né spazzato via dalla pipetta di aspirazione. Anche se l'olio minerale evita l'evaporazione e conseguenza maggiori cambiamenti di pressione all'interno della camera, è possibile azzerare la pressione di aspirazione prima di misurare ogni GUV.
- Trovare un GUV ed aspirare esso. Spostare la micropipetta e fuori fuoco (per mantenere il GUV lontano dalla superficie dove si potrebbe essere tirato fuori la pipetta da shear stress quando la camera viene spostata).
- Cercare una perlina spostando attentamente intorno alla camera. Movimenti bruschi possono espellere il GUV. Intrappolarlo con pinzette ottiche a distanza ~ 20 µm dalla parte inferiore della camera. Assicurarsi che l'area di interesse viene pulito con nessun altro perline o membrane in vista. Tutto ciò che cade nella Pinzetta ottica tranne il tallone altererà la misurazione.
- Riportare il GUV a fuoco e lontano il tallone con la micropipetta allineata con la trappola ottica (Figura 2).
- Registrare il movimento del tallone per 1 – 2 min misurare la posizione di equilibrio (necessaria per misure di forza).
- Ridurre la pressione all'interno della micropipetta per quanto possibile senza perdere il GUV così per diminuire la tensione della membrana. Con attenzione portare il GUV a contatto con il tallone per circa un secondo, stabilire legami streptavidina-biotina, quindi tirare delicatamente indietro creando un nanotubo. Il movimento del GUV avvicinandolo o allontanandolo il tallone idealmente dovrebbe essere fatto con un attuatore piezoelettrico per disturbare minimamente il tallone nella Pinzetta ottica.
Nota: Se i nanotubi non formano, potrebbe essere dovuto povera streptavidina rivestimento del tallone, una quantità insufficiente di biotinylated lipidi nel GUV, insufficiente concentrazione di sale o eccessiva concentrazione di glucosio nel buffer sperimentale, o la membrana tensione nel GUV è troppo alta48. - Aumentare la pressione di aspirazione così per ricreare la linguetta di aspirazione. Allineare il tubo per sdraiarsi sull'asse della pipetta di aspirazione e al massimo lo stato attivo sul tubo (Figura 2).
- Assicurarsi che il tubo e l'equatore GUV siano a fuoco. Registrare il movimento del tallone con microscopia del campo luminoso per qualche minuto (qui, la velocità di acquisizione di fotocamera è 30 Hz). Registrare l'altezza, h, del serbatoio dell'acqua rispetto alla posizione zero. Prendere un paio di immagini confocal del sistema (Figura 2).
- Ripetere il passaggio precedente alle pressioni di aspirazione diversi, in modo implicito le tensioni di membrana. Gamma tensione tipica è 0,015 – 0.2 mN/m, con un passo di circa 0.02 mN/m.
- Se l'iniezione di proteine o molecole vicino il sistema, portare la micropipetta iniezione vicino il nanotubo, assicurandosi che il tallone nella trappola ottico non è perturbato. Iniettare delicatamente ad una pressione di circa 1 – 2 PA.
-
Dopo il legame proteico è equilibrata (l'intensità di fluorescenza della proteina iniettata sulla membrana resti costante sul GUV), ripetere le misurazioni graduale come con la membrana nuda (passaggi 3.11 e 3.12).
Nota: Poiché le misurazioni vengono effettuate durante l'iniezione di proteine vicino GUV a pressione costante, la concentrazione di massa della proteina rimane più o meno invariata vicino GUV; così, il desorbimento di proteine deve essere trascurabile durante la misurazione.- In alternativa, è possibile incubare il GUV insieme con le proteine prima di eseguire esperimenti tubo-tirando per garantire una concentrazione di massa di proteine costante. Dato che la frazione relativa membrana di proteine sul tubo e sul GUV è misurata, il modo proteine vengono consegnate non influenza il calcolo curvatura-ordinamento (Vedi sezione 4).
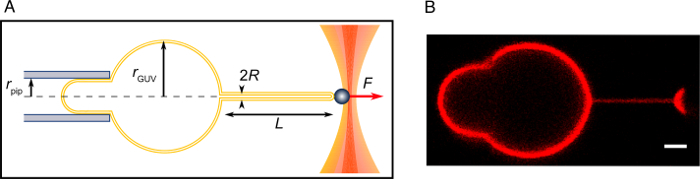
Figura 2: tubo-tirando esperimento. (A) schemi dell'esperimento. (B) un immagine confocale di un tubo tirato come descritto in questo protocollo. Barra della scala = 2 µm. Clicca qui per visualizzare una versione più grande di questa figura.
4. misurazioni e analisi dei dati
- Misurazione di tensione della membrana
- Calcolare la pressione idrostatica per ogni passaggio a pressione di aspirazione costante:
ΔP = pgh
dove p è la densità dell'acqua, accelerazione di gravità g e h l'altezza del serbatoio dell'acqua dal punto 3.11. - Da immagini confocal, misurare il raggio del GUV, rGUVe il raggio della pipetta aspirazione, rpip (Figura 2).
- Calcolare la tensione di membrana, σ, utilizzando di equazione di Laplace49:
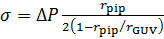
- Calcolare la pressione idrostatica per ogni passaggio a pressione di aspirazione costante:
- Misurazione della forza di membrana
- Determinare la rigidezza della Pinzetta ottica, k, utilizzando uno dei diversi metodi di calibrazione27. In questa configurazione, è necessario misurare k utilizzando il metodo di trascinamento viscoso27.
- Calcolare la posizione di equilibrio del tallone, un0, mediamente da una misurazione prima di tirare il tubo (punto 3.8).
- Per ogni misura di tensione costante, calcolare la forza di membrana equilibrio, F, da legge di Hooke:
F = k(un - 0)
dove un è la posizione media del tallone durante tale misurazione.
- Misura raggio del tubo
- Nel caso di una membrana nudo (senza curvatura a membrana aggiunto molecole), calcolare il raggio del tubo, R, dalla forza come:
R = F/(4πσ)
(fa riferimento22,23). - Per misurare il raggio del tubo in presenza di molecole di membrana-curvatura ed indipendentemente dal punto 4.3.1, in primo luogo, registrare l'intensità di fluorescenza del lipido lungo la lunghezza del tubo, holavascae lungo il contorno GUV, hoGUV. Misurare l'intensità di fluorescenza media di un fluoroforo in o associata alla membrana come un'intensità media lungo la linea più brillante di un tubo o un contorno GUV. Selezionare una scatola rettangolare contenente una sezione orizzontale di contorno GUV o il tubo e calcolare la somma delle intensità di fluorescenza di ogni riga orizzontale nella casella.
- Dividere ogni somma per il numero di pixel della linea orizzontale (cioè, la larghezza della casella). Si noti che nella casella selezionata, non ci dovrebbe essere nessun altre membrane presenti. Il profilo di intensità di fluorescenza lungo la lunghezza della casella selezionata è ottenuto.
- Dopo aver sottratto l'intensità di sfondo, prendere l'intensità di fluorescenza pixel medi dalla riga più brillante. Il raggio del tubo è linearmente relativo al rapporto di fluorescenza lungo il contorno del tubo e del GUV come:
R = Kvascahovasca/hoGUV
dove Kidromassaggio è un fattore di taratura25.
Nota: Questo metodo può essere utilizzato per misurare il raggio del tubo nell'intervallo 10-80 nm (quando il tubo è abbastanza stretto per trovarsi all'interno di un voxel confocale larghezza) e con una maggiore incertezza nel 80 nm e gamma più alta. La sensibilità della misurazione dipende dall'impostazione.
- Determinare Kvasca eseguendo misurazioni indipendenti raggio nei passaggi 4.3.1 e 4.3.2 su una composizione di membrana semplice utilizzando i lipidi uncharged. Tale composizione semplice membrana assicura che il raggio e la forza la semplice relazione fornita al punto 4.3.1. Ripetere l'esperimento più volte e trama R, dedotto dalla forza (punto 4.3.1) contro iovasca/hoGUV (punto 4.3.2). Calcolare Kidromassaggio dal fit. In questa configurazione, Kvasca = 200 ± 50 nm utilizzando uovo membrana L-α-fosfatidilcolina (uovo-PC) e un lipide fluorescente cui fluorescenza come minimo dipende dalla polarizzazione25.
Nota: Kvasca deve essere misurato per diversi obiettivi, a causa di loro volumi diversi confocale voxel. Il fluoroforo lipidica non dovrebbe interagire con le molecole di proteine/iniettate. Il lipido fluorescente consigliato qui, ceramide BODIPY TR, non dovrebbe avere tutte le interazioni con le proteine. Questa ipotesi è stata confermata con gli studi precedenti di BAR e -BAR domini25,36,37, che hanno dimostrato che a copertura della superficie ad alta percentuale proteica, il raggio del tubo è fissato dalle proteine, indipendentemente dal fatto il tensione nel GUV. Se le proteine interagiscono con il fluoroforo lipidica, una deplezione o l'arricchimento del fluoroforo sarà osservato nel tubo alle frazioni di superficie varia ad alta percentuale proteica.
- Nel caso di una membrana nudo (senza curvatura a membrana aggiunto molecole), calcolare il raggio del tubo, R, dalla forza come:
- Misurare la densità superficiale delle proteine
- Preparare miscele del lipido utilizzando un semplice lipido uncharged (ad es., uovo-PC) completato con circa cinque frazioni diverse mole di un lipide fluorescente (della lunghezza d'onda stessa come il colorante usato per etichettare la proteina, per esempio, BODIPY-FLC5-hexadecanoyl-phosphatidylcholine (HPC *) per es., la proteina Alexa488-labeled) nella gamma: XHPC * = 0,01 – 1%. Preparare GUV in saccarosio di 100 mM di electroformation su ITO piastre (seguire il passaggio 1 di una precedente pubblicazione13).
- GUV di raccogliere e trasferire in una camera sperimentale passivata con β-caseina. Utilizzare ad esempio, 100 millimetri di glucosio per la soluzione sperimentale. Attendere qualche minuto per il GUV a stabilirsi.
- Prendere le immagini di fluorescenza confocale di GUV e registrare l'intensità di fluorescenza media lungo il GUV contorni come una funzione della frazione molare del lipido fluorescente (Vedi punto 4.3.2). Per ogni composizione, calcolare la densità di zona del lipido fluorescente, φHPC*. Ad esempio, assumendo che l'area a lipido è 0,7 nm2, φHPC* = 1,43 x 106 XHPC * al foglio illustrativo. Trama HPC * intensità di fluorescenza in GUV, hoHPC *, GUV, contro φHPC*. Misura dà la costante di taratura, A, dato da φHPC* = AIHPC *, GUV. A dipende le impostazioni di microscopia, come la potenza del laser e la sensibilità del rivelatore (cioè, guadagno), quindi record A per varie impostazioni di microscopia (Vedi esempio nella Figura 3) comunemente utilizzate.
- Preparare diverse soluzioni di HPC * sciolto nel detersivo, per esempio, laurilsolfato di sodio (SDS), alle concentrazioni differenti nella gamma da ~ 1 per 10-50 µM. registrare l'intensità di fluorescenza di ogni soluzione alla rinfusa e calcolare la pendenza di intensità contro concentrazione (Figura 3). Ripetere la misurazione con il fluoroforo che verrà coniugato alla proteina in una gamma di concentrazione simile (vedere l'esempio con Alexa488 nella Figura 3). Questa misura è necessaria per correlare le intensità di fluorescenza dell'etichetta della proteina e l'etichetta del lipido, hoA488, massa / hoHPC *, alla rinfusa, come essi non possono necessariamente emettono nello stesso modo alla stessa concentrazione di massa.
- Misurare il numero di fluorofori per molecola di proteina usando un fluorospectrometer. Ad esempio, per il caso di Alexa488, il numero di molecole Alexa488 della proteina, nA488, può essere calcolato utilizzando la seguente relazione:
n A488 = (A494/εA488) / ((A280 - 0,11A494) / εprot)
dove A494 e A280 sono i valori di assorbanza per unità di lunghezza a 494 nm e 280 nm, rispettivamente, e εA488 e εprot sono i coefficienti di assorbimento molecolare di Alexa488 e la proteina, rispettivamente. - Calcolare la densità di superficie della proteina il GUV, φprot, GUV, secondo la seguente formula:
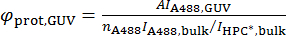
Tenere presente lo stato di polimerizzazione della proteina. Ad esempio, BAR proteine dimerizzano, pertanto la densità calcolata sarà quello del monomero BAR per superficie se utilizzando il coefficiente di estinzione della forma monomerica.

Figura 3: esempio di taratura della densità superficiale di proteina. Misurati sono la fluorescenza intensità del lipido HPC * alla rinfusa (a sinistra) e in GUV (centro). Inoltre, misurati sono l'intensità di fluorescenza di massa di Alexa488 (associato a un dominio di BAR) (a destra). L'intensità di fluorescenza scala linearmente con la concentrazione. Misure indicate sono per rilevamento specifico guadagno e potenza di uscita del laser. Trame generato basato sui dati di riferimento37. Clicca qui per visualizzare una versione più grande di questa figura.
Risultati
L'esperimento di tubo-tirando può dare informazioni vitali meccaniche su membrana. In assenza di proteine o altre molecole che forza la coppia con curvatura della membrana, la membrana e raggio del tubo può essere correlato con tensione nelle membrane applicando l'Hamiltoniana di carnevali-Helfrich equazione ad un tubo tirato da un GUV50,51
Discussione
Il metodo di tirare tubi da GUV dà ricco di informazioni sul sistema proteina di membrana, come non è solo il mezzo per misurare le proprietà meccaniche fondamentali della membrana, ma aiuta a far luce sull'accoppiamento tra membrana e proteine curvatura. Come discusso nell'introduzione, esistono altre tecniche per misurare gli effetti delle proteine di membrana-curvatura, o incubando le proteine con liposomi di sub-micron legati a una superficie passivata18,19
Divulgazioni
Gli autori non hanno nulla a rivelare.
Riconoscimenti
Gli autori ringraziano Benoit Sorre, Damien Cuvelier, Pierre Nassoy, François Quémeneur e Gil Toombes per i loro contributi essenziali per stabilire il metodo di nanotubi nel gruppo. Il gruppo di P.B. appartiene al Consorzio CNRS CellTiss, il Labex CelTisPhyBio (ANR-11-LABX0038) e di Scienze di Parigi et Lettres (ANR-10-IDEX-0001-02). F.-C. Tsai è stato finanziato dal EMBO fellowship a lungo termine (ALTF 1527-2014) e Marie Curie actions (H2020-MSCA-IF-2014, progetto membrana-ezrin-actina). M.S. è un Junior Fellow della Society of Fellows Simons.
Materiali
| Name | Company | Catalog Number | Comments |
| 1,2-Dioleoyl-sn-glycero-3-phosphatidylcholine (DOPC) | Avanti | 850375 | Example lipid used in data for Figure 3 |
| 1,2-distearoyl-sn-glycero-3-phosphoethanolamine-N-[biotinyl(polyethyleneglycol)-2000] [DSPE-PEG(2000)-biotin] | Avanti | 880129 | biotinylated lipid |
| BODIPY-TR-C5-ceramide | Molecular Probes (ThermoFisher) | D7540 | fluorescent lipid |
| BODIPY- FLC5-hexadecanoyl phosphatidylcholine (HPC*) | Molecular Probes (ThermoFisher) | fluorescent lipid for protein density calibration | |
| egg L-α-phosphatidylcholine (eggPC) | Avanti | 840051 | used for calibrating the tube radius constant |
| β-casein from bovine milk (>99%) | Sigma Aldrich | C6905 | used for passivating the micropipette and the experimental chamber |
| Sucrose | Sigma Aldrich | S7903 | |
| D(+) glucose | Sigma Aldrich | G7021 | |
| NaCl | Sigma Aldrich | S7653 | |
| Tris | Sigma Aldrich | 10708976001 | |
| osmometer | Loser | n/a | |
| Pt-wires, 0.5 mm diameter, 99.99% pure | Goodfellow USA | PT005139 | used for GUV electroformation |
| function generator | n/a | used to create current for GUV electroformation | |
| putty sealant | Vitrex (from CML France) | CRIT 140013 | used to seal the electroformation chamber |
| bath sonicator | n/a | useful to clean the electroformation chamber, but not crucial | |
| Nikon TE2000 inverted microscope, eC1 confocal system (Nikon), with two laser lines (λ = 488 nm and 543 nm); optical tweezers induced by a 5 W ytterbium fiber continuous wave laser (λ > 1070 nm; IPG GmBH Germany) | an example of a confocal microscopy system equipped with optical tweezers | ||
| micromanipulators | n/a | ||
| borosilicate capillaries (with internal and external radii of 0.78 mm and 1 mm, respectively) | Harvard apparatus | 30-0036 | |
| micropipette puller | Sutter Instrument | P-2100 | |
| microforge | Narishige | MF-800 | |
| piezoelectric actuator | Physik Instrumente | n/a | |
| polystyrene streptavidin coated beads (diameter 3.2 µm) | Spherotech | SVP-30-5 |
Riferimenti
- McMahon, H. T., Gallop, J. L. Membrane curvature and mechanisms of dynamic cell membrane remodelling. Nature. 438 (7068), 590-596 (2005).
- Johannes, L., Wunder, C., Bassereau, P. Bending "on the rocks"--a cocktail of biophysical modules to build endocytic pathways. Cold Spring Harb Perspect Biol. 6 (1), (2014).
- Dawson, J. C., Legg, J. A., Machesky, L. M. Bar domain proteins: a role in tubulation, scission and actin assembly in clathrin-mediated endocytosis. Trends Cell Biol. 16 (10), 493-498 (2006).
- Mim, C., Unger, V. M. Membrane curvature and its generation by BAR proteins. Trends Biochem Sci. 37 (12), 526-533 (2012).
- Qualmann, B., Koch, D., Kessels, M. M. Let's go bananas: revisiting the endocytic BAR code. EMBO J. 30 (17), 3501-3515 (2011).
- Rao, Y., Haucke, V. Membrane shaping by the Bin/amphiphysin/Rvs (BAR) domain protein superfamily. Cell Mol Life Sci. 68 (24), 3983-3993 (2011).
- Simunovic, M., Voth, G. A., Callan-Jones, A., Bassereau, P. When Physics Takes Over: BAR Proteins and Membrane Curvature. Trends Cell Biol. 25 (12), 780-792 (2015).
- Safari, F., Suetsugu, S. The BAR Domain Superfamily Proteins from Subcellular Structures to Human Diseases. Membranes (Basel). 2 (1), 91-117 (2012).
- Angelova, M. I., Soléau, S., Méléard, P., Faucon, F., Bothorel, P., Helm, C., Lösche, M., Möhwald, H. . Progress in Colloid and Polymer Science Vol. 89: Trends in Colloid and Interface Science VI. 89, 127-131 (1992).
- Meleard, P., Bagatolli, L. A., Pott, T. Giant unilamellar vesicle electroformation from lipid mixtures to native membranes under physiological conditions. Methods Enzymol. 465, 161-176 (2009).
- Montes, L. R., Alonso, A., Goni, F. M., Bagatolli, L. A. Giant unilamellar vesicles electroformed from native membranes and organic lipid mixtures under physiological conditions. Biophys J. 93 (10), 3548-3554 (2007).
- Mathivet, L., Cribier, S., Devaux, P. F. Shape change and physical properties of giant phospholipid vesicles prepared in the presence of an AC electric field. Biophys J. 70 (3), 1112-1121 (1996).
- Collins, M. D., Gordon, S. E. Giant liposome preparation for imaging and patch-clamp electrophysiology. J Vis Exp. (76), (2013).
- Garten, M., Aimon, S., Bassereau, P., Toombes, G. E. Reconstitution of a transmembrane protein, the voltage-gated ion channel, KvAP, into giant unilamellar vesicles for microscopy and patch clamp studies. J Vis Exp. (95), e52281 (2015).
- Hochmuth, R. M., Evans, E. A. Extensional flow of erythrocyte membrane from cell body to elastic tether. I. Analysis. Biophys J. 39 (1), 71-81 (1982).
- Hochmuth, R. M., Wiles, H. C., Evans, E. A., McCown, J. T. Extensional flow of erythrocyte membrane from cell body to elastic tether. II. Experiment. Biophys J. 39 (1), 83-89 (1982).
- Bassereau, P., Sorre, B., Levy, A. Bending lipid membranes: experiments after W. Helfrich's model. Adv Colloid Interface Sci. 208, 47-57 (2014).
- Hatzakis, N. S., et al. How curved membranes recruit amphipathic helices and protein anchoring motifs. Nature chemical biology. 5 (11), 835-841 (2009).
- Bhatia, V. K., et al. Amphipathic motifs in BAR domains are essential for membrane curvature sensing. EMBO J. 28 (21), 3303-3314 (2009).
- Shi, Z., Baumgart, T. Membrane tension and peripheral protein density mediate membrane shape transitions. Nat Commun. 6, 5974 (2015).
- Chen, Z., Shi, Z., Baumgart, T. Regulation of membrane-shape transitions induced by I-BAR domains. Biophys J. 109 (2), 298-307 (2015).
- Cuvelier, D., Derenyi, I., Bassereau, P., Nassoy, P. Coalescence of membrane tethers: experiments, theory, and applications. Biophys J. 88 (4), 2714-2726 (2005).
- Derenyi, I., Julicher, F., Prost, J. Formation and interaction of membrane tubes. Phys Rev Lett. 88 (23), 238101 (2002).
- Dimova, R. Recent developments in the field of bending rigidity measurements on membranes. Adv Colloid Interface Sci. 208, 225-234 (2014).
- Sorre, B., et al. Nature of curvature coupling of amphiphysin with membranes depends on its bound density. Proc Natl Acad Sci U S A. 109 (1), 173-178 (2012).
- Evans, E., Rawicz, W. Entropy-driven tension and bending elasticity in condensed-fluid membranes. Phys Rev Lett. 64 (17), 2094-2097 (1990).
- Neuman, K. C., Nagy, A. Single-molecule force spectroscopy: optical tweezers, magnetic tweezers and atomic force microscopy. Nat Methods. 5 (6), 491-505 (2008).
- Capraro, B. R., Yoon, Y., Cho, W., Baumgart, T. Curvature sensing by the epsin N-terminal homology domain measured on cylindrical lipid membrane tethers. J Am Chem Soc. 132 (4), 1200-1201 (2010).
- Bo, L., Waugh, R. E. Determination of bilayer membrane bending stiffness by tether formation from giant, thin-walled vesicles. Biophys J. 55 (3), 509-517 (1989).
- Rossier, O., et al. Giant Vesicles under Flows: Extrusion and Retraction of Tubes. Langmuir. 19 (3), 575-584 (2003).
- Borghi, N., Rossier, O., Brochard-Wyart, F. Hydrodynamic extrusion of tubes from giant vesicles. EPL (Europhysics Letters). 64 (6), 837 (2003).
- Zhu, C., Das, S. L., Baumgart, T. Nonlinear sorting, curvature generation, and crowding of endophilin N-BAR on tubular membranes. Biophys J. 102 (8), 1837-1845 (2012).
- Ramesh, P., et al. FBAR syndapin 1 recognizes and stabilizes highly curved tubular membranes in a concentration dependent manner. Sci Rep. 3, 1565 (2013).
- Knorr, R. L., et al. Membrane morphology is actively transformed by covalent binding of the protein Atg8 to PE-lipids. PLoS One. 9 (12), e115357 (2014).
- Aimon, S., et al. Membrane shape modulates transmembrane protein distribution. Dev Cell. 28 (2), 212-218 (2014).
- Prévost, C., et al. IRSp53 senses negative membrane curvature and phase separates along membrane tubules. Nat Commun. , (2015).
- Simunovic, M., et al. How curvature-generating proteins build scaffolds on membrane nanotubes. Proc Natl Acad Sci U S A. 113 (40), 11226-11231 (2016).
- Allain, J. M., Storm, C., Roux, A., Ben Amar, M., Joanny, J. F. Fission of a multiphase membrane tube. Phys Rev Lett. 93 (15), 158104 (2004).
- Morlot, S., et al. Membrane shape at the edge of the dynamin helix sets location and duration of the fission reaction. Cell. 151 (3), 619-629 (2012).
- Renard, H. F., et al. Endophilin-A2 functions in membrane scission in clathrin-independent endocytosis. Nature. 517 (7535), 493-496 (2015).
- Simunovic, M., et al. Friction Mediates Scission of Tubular Membranes Scaffolded by BAR Proteins. Cell. 170 (1), 172-184 (2017).
- Simunovic, M., Lee, K. Y., Bassereau, P. Celebrating Soft Matter's 10th anniversary: screening of the calcium-induced spontaneous curvature of lipid membranes. Soft Matter. 11 (25), 5030-5036 (2015).
- Sorre, B., et al. Curvature-driven lipid sorting needs proximity to a demixing point and is aided by proteins. Proc Natl Acad Sci U S A. 106 (14), 5622-5626 (2009).
- Heinrich, M., Tian, A., Esposito, C., Baumgart, T. Dynamic sorting of lipids and proteins in membrane tubes with a moving phase boundary. Proc Natl Acad Sci U S A. 107 (16), 7208-7213 (2010).
- Dasgupta, R., Dimova, R. Inward and outward membrane tubes pulled from giant vesicles. Journal of Physics D: Applied Physics. 47 (28), 282001 (2014).
- Vitkova, V., Genova, J., Mitov, M. D., Bivas, I. Sugars in the aqueous phase change the mechanical properties of lipid mono- and bilayers. Molecular Crystals and Liquid Crystals. 449, 95-106 (2006).
- Bouvrais, H. . Mechanical properties of giant vesicle membranes investigated by flickering technique. , (2011).
- Koster, G., Cacciuto, A., Derenyi, I., Frenkel, D., Dogterom, M. Force barriers for membrane tube formation. Phys Rev Lett. 94 (6), 068101 (2005).
- Kwok, R., Evans, E. Thermoelasticity of large lecithin bilayer vesicles. Biophys J. 35 (3), 637-652 (1981).
- Helfrich, W. Elastic properties of lipid bilayers: theory and possible experiments. Z Naturforsch C. 28 (11), 693-703 (1973).
- Canham, P. B. The minimum energy of bending as a possible explanation of the biconcave shape of the human red blood cell. J Theor Biol. 26 (1), 61-81 (1970).
- Marcerou, J. P., Prost, J., Gruler, H. Elastic Model of Protein-Protein Interaction. Nuovo Cimento Della Societa Italiana Di Fisica D-Condensed Matter Atomic Molecular and Chemical Physics Fluids Plasmas Biophysics. 3 (1), 204-210 (1984).
- Leibler, S. Curvature Instability in Membranes. J Phys-Paris. 47 (3), 507-516 (1986).
Ristampe e Autorizzazioni
Richiedi autorizzazione per utilizzare il testo o le figure di questo articolo JoVE
Richiedi AutorizzazioneThis article has been published
Video Coming Soon