Case Report
胃がん治療のためのシングル切開と 1 ポート腹腔鏡下近位胃切除術 ダブルチャネル吻合術
要約
シングル切開と 1 ポート腹腔鏡下近位胃切除術とダブル チャネル吻合は、当初、近位胃がんの根治的切除に採用されました。この研究は、手順の実現可能性を実証し、さらなる研究の基礎を築きました。
要約
シングル切開と 1 ポート腹腔鏡下近位胃切除術とダブル チャネル 吻合 (SILT-DT) は、近位胃がんを治療するための低侵襲手術アプローチです。この技術には、近位胃の包括的な腹腔鏡下切除、リンパ節郭清、および二重路吻合が含まれます。SILT-DTは、シングルポート腹腔鏡手術と補助手術穴を統合することで、手術の困難さを軽減し、腹部ドレナージチューブの留置を容易にします。従来の5ポート腹腔鏡下胃切除術と比較して、SILT-DTは必要なポートが少なくて済み、切開長が短いため、術後の痛みが軽減され、回復が早くなります。手術の成功を確実にするために、腫瘍の大きさ、病期、位置、患者のBMIなどの要素を慎重に検討し、徹底的な術前評価が実施されました。この包括的な評価により、最適な患者選択と手術計画が可能になりました。術後のフォローアップでは重大な合併症は示されず、SILT-DTの安全性と有効性が強調されています。この革新的な技術は、優れた臨床転帰を維持しながら近位胃がんを管理するための有望な低侵襲代替手段を提供します。
概要
腹腔鏡技術は、最近、胃がんの外科的治療の主要な方向性の1つになっています1,2。胃がんの通常の腹腔鏡手術は、主に5穴法を使用して行われます。外科技術の進歩と医療機器の継続的な改善により、縮小ポート腹腔鏡下胃がん手術は、外科的外傷をさらに減らし、腹腔への障害を最小限に抑え、術後の回復を加速するために徐々に発展してきました3,4,5,6。
大森7は、2011年に初めてシングルポート腹腔鏡下遠位胃がん手術を報告しました。胃がんに対する純粋なシングルポート腹腔鏡下根治的胃切除術は、従来の5ポート腹腔鏡下胃切除術よりも困難です。これに対処するために、補助手術穴がシングルポート腹腔鏡手術に追加され、これにより手術の困難さが軽減され、腹部ドレナージチューブ8,9の配置が容易になります。胃がん患者向けの低侵襲技術である単切開腹腔鏡下手術プラス1ポート(SILS+1)は、ポート数が少なく、切開長さが短いため、近年人気を集めています。
現在、シングルポート腹腔鏡下またはSILS+1胃がん手術は、遠位胃切除術では比較的一般的ですが、胃全摘術への適用はまれです。さらに、腹腔鏡下二重トラクト胃がん全吻合の使用は報告されていません。
これに基づいて、最初にシングルポートとワンポートの腹腔鏡下全位胃切除術とダブルトラクト吻合(SILT-DT)を試みました。経臍術ポートをメイン操作ポートとして、左上腹部ドレナージポートを補助操作ポートとして使用しました。この技術は、近位胃切除術、D2リンパ節郭清、および消化管再建のための二重管吻合を行うために採用されました。
ケースプレゼンテーション:
患者は63歳の男性で、胃内視鏡検査中に食道胃接合部に腫瘍が発見された後、病院に入院しました(図1)。胃鏡からの生検結果は、中分化型腺癌を示唆しました(図2)。術前の胸部および腹部増強CTスキャンでは、遠隔転移の証拠は示されませんでした(図3)。患者は以前に健康であり、腹部手術の既往歴はありませんでした。
患者様の選択
患者は、組織学的にSiewertII型またはIII型の胃食道接合部腺がんが確認され、術前の腹部CTで胃周囲のリンパ節の肥大や遠隔転移が認められない場合、参加資格がありました。腫瘍の最大直径は3cm未満である必要があり、腫瘍の下極と胃の角度との間の距離は5cmを超えなければなりませんでした。除外基準には、以前に腹部手術を受けた患者、術前の腫瘍直径が3cmを超える患者、および/または多臓器切除が必要な患者、ネオアジュバント化学放射線療法に関する集学的チーム(MDT)のディスカッションを受けた患者、またはネオアジュバント化学放射線療法を受けた患者、および腹腔鏡手術に不耐性の患者が含まれていました。
プロトコル
手術は標準的な手順に従い、倫理的な承認を受けました。この研究は、湖北省芸術科学大学と提携している襄陽中央病院の倫理委員会によって許可されました。インフォームド ペーパー コンセントは患者から得られました。研究内容と方法は、医療倫理の規範と要件を遵守しています。この試験で使用された試薬および機器は、 材料表に記載されています。
1. 術前のステップ
- 患者は、手術の1日前に腸の準備のために経口リン酸ナトリウム塩を服用するように指示されました。患者は8時間絶食し、手術の2時間前まで水分摂取が許可されました。手術室に入る前に上部胃管が挿入されました。
- 患者は仰臥位のスプリットレッグポジションに配置され、頭が上昇し、わずかに右に傾いていました。
- 気管内挿管が行われ、全身麻酔は施設で承認されたプロトコルに従って投与されました。
2.外科的処置
- へその周囲に3.0〜3.5cmの横切開が作成され、4つの内蔵トロカールを備えたSILSポートが挿入されました(図4A)。さらに 12 mm のトロカールが左上象限に挿入され、超音波せん断、内視鏡用リニア ステープラー、術後ドレナージ チューブなどの手術器具の手術ポートとして機能しました。
- 超音波ナイフを使用して、グループ1、2、3、4、7、8a、9、および11pの脂肪リンパ組織を解剖しました(図5A、B)。食道セグメントの長さが約5〜7cm低く抑えられ(図5C)、胃の曲率の大小の自由度が維持されました。
注: SILT-DT の手順を 図 5 に示します。胃・リンパ節郭清は、胃がん腹腔鏡手術ガイドライン(2023年版)10に則り実施しました。D2リンパ節郭清と近位胃切除術が完了しました。 - 食道-空腸(EJ)吻合が確立されました。EJ吻合部位は、Treitzの靭帯から20 cm遠位、下部食道付近の空腸で同定されました。EJ吻合は、60mmの内視鏡用リニアステープラーを使用して、左上象限の12mmポートを介して行われました(図5D)。
注:消化管の再建を示す概略図を 図4Bに示します。 - 60 mm の内視鏡用リニア ステープラーを使用して、食道の標本を切除し、空腸と食道の間の吻合口を閉じました (図 5E)。
- 胃空腸(GJ)吻合が作成され、その部位はEJ吻合から遠位の空腸に8〜15cm、残りの胃のより大きな湾曲の後壁にマークされました(図5F)。
- 空腸空腸吻合が確立されました。空腸吻合は、GJ吻合部位から遠位5cmの60mmの内視鏡的直線ステープラーを使用して、へその3.5cmの切開を通じて行われました(図5G)。
- 個々の吻合部は閉鎖され、強化されました。GJ吻合と空腸吻合の一般的な開口部は、3-0マイクロジョースレッドを使用して閉じました。中脳裂孔は連続縫合糸で閉じられました。
- ドレナージチューブをEJ吻合の後ろに配置し、左上腹部から出ました(図5H)。
3. 術後管理
- 術後水絶食を実施し、胃管を留置袋で排出しました。
- 胃管は48時間の観察後に抜かれ、血まみれのドレナージ液が明らかに存在していないことが確認されました。
- 水分、電解質、酸塩基バランスを維持するとともに、酸の抑制のために輸液が投与されました。予防的抗生物質の期間は最大48時間に制限されました。
- 早期の動員は、術後6〜24時間以内に積極的に推進されました。回復期に2〜3日間、流動食を開始しました。
- 吻合部の漏出が評価され、7日目の上部消化管X線撮影を通じて残存胃の発達が評価されました。
- 腹腔ドレナージチューブは退院後5〜7日以内に抜去されました。
結果
手術は150分以内に完了し、術中出血は5mLと最小限でした。短期的な合併症はなく、術後の回復は成功しました。合計24のリンパ節を採取し、リンパ節転移は認められませんでした。手術時間は150分で、推定失血量は5mLでした。患者は2日間ベッドに留まりました。最初の放屁までの時間は70時間で、患者は3日後に流動食と飲料を摂取し始めました。胃管は4日目 に抜管し、ドレナージチューブは7日以内に抜管しました。造影剤は、食道に逆流することなく、30〜50分間残りの胃に持続しました(図6)。術後の腹部切開の美容的結果は満足のいくものでした(図4C)。疼痛は、11 段階の数値評価尺度 (NRS) によって評価され、0 は疼痛なし、10 は想像できる最悪の疼痛11 です。患者の詳細なデータは 、Table 1 に示されています。
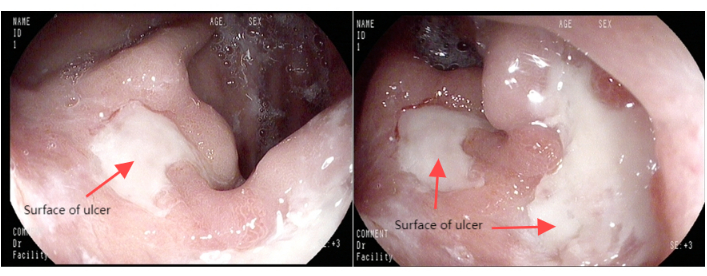
図1:胃鏡画像。 この図の拡大版を表示するには、ここをクリックしてください。
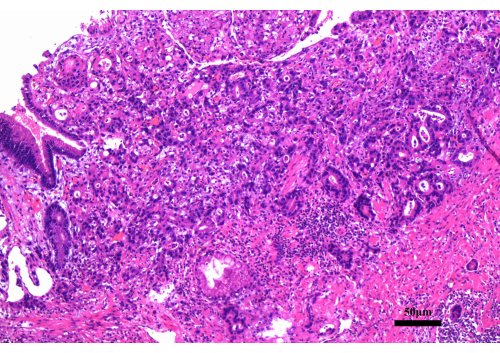
図2:胃鏡生検の結果。 胃鏡生検により、中分化型の腺癌が明らかになりました。スケールバー:50μm;倍率:200倍。 この図の拡大版を表示するには、ここをクリックしてください。
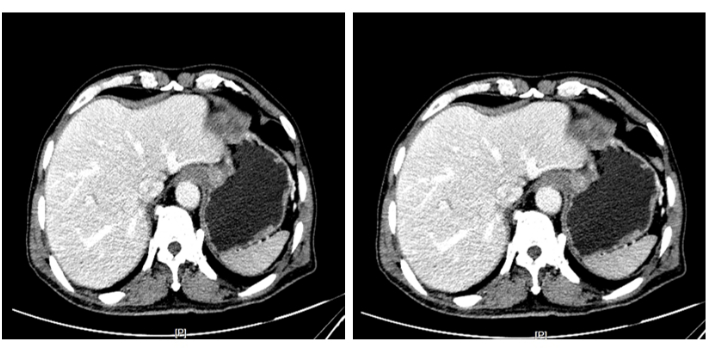
図3:腹部増強CTスキャン。 腫瘍性病変と考えられていた噴門に不均一な増強がみられ、腫瘍は筋肉層に浸潤しなかった。 この図の拡大版を表示するには、ここをクリックしてください。
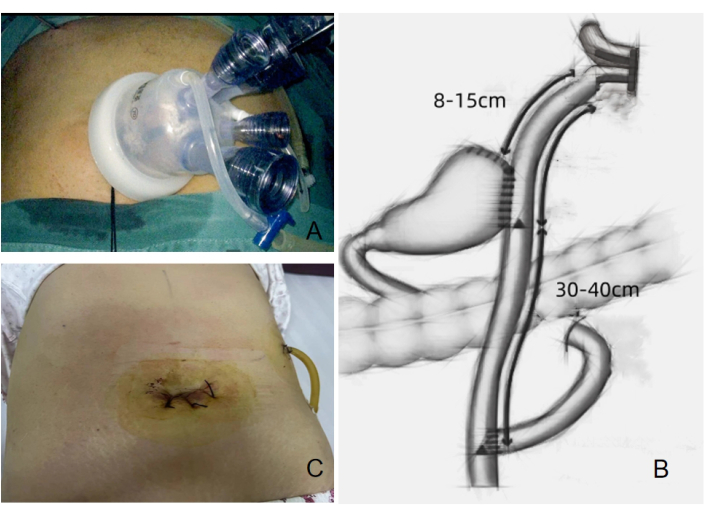
図4:手術のセットアップと術後の創傷の状態。 (A)手順で使用される4つの内蔵トロカール。(B)手術中に行われるダブルトラクト吻合。(C)処置後に示された術後創傷の状態。 この図の拡大版を表示するには、ここをクリックしてください。
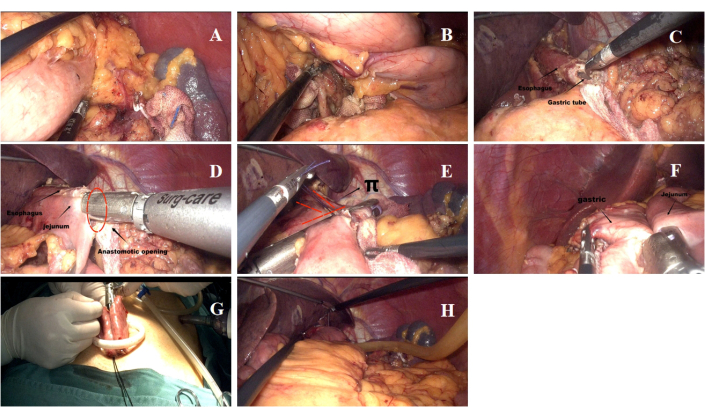
図5:手術手順の詳細 (A,B) 手術中にリンパ節を洗浄するプロセス。(C)食道の切断と下部食道端の開口部。(D) 吻合の一部として行われる左右の食道空腸吻合術。(E)食道空腸吻合部位の共通開口部の閉鎖。(F) 残存胃空腸吻合術が完了しました。(G) 臍帯切開を通じて行われる左右の腸腸管吻合。(H)ドレナージチューブの位置。 この図の拡大版を表示するには、ここをクリックしてください。
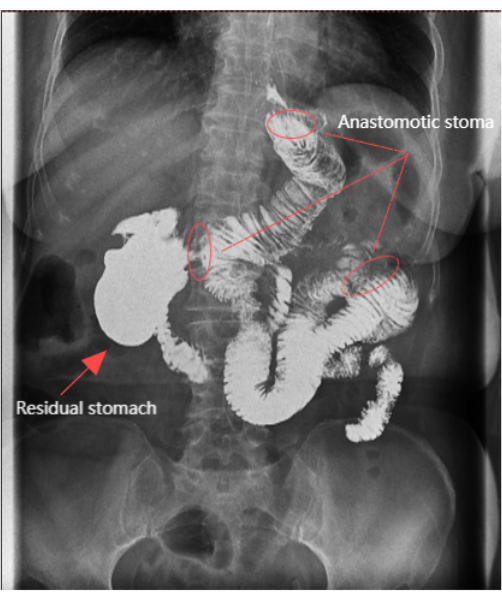
図6:上部消化管X線撮影。 上部消化管X線撮影では、吻合が開いており、残りの胃がはっきりと見えることが示されました。 この図の拡大版を表示するには、ここをクリックしてください。
| 項目 | 結果 |
| ジェンダー | 男性 |
| 年 | 63 |
| BMI (kg/m2) | 23.5 |
| 麻酔グレード | III. |
| 術前TNM病期分類 | cT1N0M0 |
| 動作時間(分) | 150 |
| 切開長さ(cm) | 2.8 |
| 術中出血量 (mL) | 5 |
| 病理学 | 中分化型腺がん |
| 近位縁の距離(cm) | 3.4 |
| 遠位縁の距離(cm) | 5.5 |
| 腫瘍サイズ(cm) | 1.5*2*1.2 |
| 取得されたリンパ節の数 | 24 |
| TNM病期分類 | pT2N0M0 |
| 手術後の胃管摘出の期間(d) | 4 |
| 最初の食事までの期間 | 3 |
| ベッド活動の期間 | 2 |
| flatusまでの期間(h) | 70 |
| 排便の時間(d) | 6 |
| ドレナージチューブの持続時間(d) | 7 |
| 手術後1日目の痛みスコア | 2 |
| 術後入院期間(日) | 8 |
| 合併症 | 何一つ |
表 1: 患者の周術期データ。 主要な測定値と結果を含む、患者の周術期データに関する詳細。
ディスカッション
シングルポートおよび縮小ポート腹腔鏡下根治的胃切除術は、胃がんを治療するための革新的なアプローチとなり、着実に受け入れられつつあります。これらの技術は、美容転帰の改善、術後の痛みの軽減、手術部位感染のリスクの低下、回復時間の短縮など、その利点から注目を集めています。
343例を対象とした12件の研究の結果から、遠位胃がんの治療にはシングルポートおよび縮小ポート腹腔鏡手術が有効であることが示され、症例の大部分を占めている3,4,12,13,14,15,16,17,18,19,20,21 .しかし、胃全摘術に焦点を当てた研究は4件のみであった22,23,24,25。これらの知見は、シングルポート胃がん手術、特に胃全摘術の臨床研究と応用は、手術の難易度が高いこと、広範な解剖とリンパ節切除が必要、および内視鏡的消化管再建の複雑な技術のために限られていることを示唆しています。
近位胃がんの治療のために、1つの切開と1つのポートを使用したダブルトラクト吻合を伴う最初の腹腔鏡下近位胃切除術を成功裏に実施しました。従来の外科的方法と比較して、シングル切開とワンポート手術はより低侵襲です。シングルポート技術と比較して、左上腹部ポートの追加は、手術中の利便性を高め、左上腹部の切開部を通じてドレナージチューブを合理的に配置することを可能にする。
Lee et al.26 は、2016 年に早期胃がんに対するシングルポート腹腔鏡下近位胃切除術と二重路再建術の最初の症例を報告しました。SILSと比較して、シングル切開とワンポート手術には左上腹部ポートが追加され、臍帯、左上腹部、手術領域からなる三角形の構造を作り出します。この革新的なアプローチは、不十分な抗牽引力や直線的な視覚化など、純粋な単一切開手術の限界に効果的に対処します。さらに、外科医の右手の器具の柔軟性を高め、手術効率の大幅な改善と、腹腔鏡検査下の各吻合中の複雑さの軽減につながります。
さらに、いくつかの戦略により、運用効率を向上させ、手順の期間を短縮できます。外科医は、リンパ節郭清および消化管再建中に、患者の左側または患者の脚の間に自分自身を配置するなど、自分の位置を変更して、手術領域の露出を最適化することを検討できます。食道空腸吻合術や胃空腸吻合術などの処置では、1人の助手または主任外科医が安定した位置を維持し、別の助手がドッキングを行うことで、吻合効率を向上させ、組織剥離のリスクを最小限に抑えることが推奨されます。さらに、光ファイバーと他の機器との間の干渉を最小限に抑えるために、統合された腹腔鏡器具を使用することをお勧めします。
要約すると、単切開と 1 ポート腹腔鏡下近位胃切除術とダブルチャネル吻合は、近位胃がんの治療に実行可能です。この場合、患者は成功した回復を経験しました。手術は低侵襲で、回復が早くなります。ただし、このプロトコルの制限には、早期の胃がんまたは良性胃腫瘍の必要性が含まれ、患者のBMIが過度に高くありません。このプロトコルの適用は、腫瘍の縁が陽性で手術の複雑さが増す潜在的なリスクがあるため、局所進行性疾患または高 BMI の患者には推奨されません。このプロトコルはまだ技術的な検討の段階にあり、確立されたガイドラインはなく、その長期的な有効性を完全に検証するための臨床データも不十分です。このプロトコールの開発には、医療機関からの倫理的承認と外科的適応の厳守が必要です。SILT-DT技術の臨床適用性を判断するには、さらなる臨床研究と調査が必要です。
開示事項
著者には、開示すべき利益相反や金銭的なつながりはありません。
謝辞
この研究は、湖北省衛生委員会の科学研究プロジェクトと、医療および健康分野における科学技術の襄陽主要プロジェクト(2021YL15)からの助成金によって支援されました。
資料
| Name | Company | Catalog Number | Comments |
| 3D laparoscope | KARL STORZ SE & Co. KG | 26605BA | |
| Absorbability surgical sutures | Johnson & Johnson | TLBJXZ | |
| Absorbable ligature clip | Hangzhou KANGJI Medical Instrument co., LTD | KJ-JZJ02ML | |
| Disposable puncture device | Hangzhou KANGJI Medical Instrument co., LTD | Type IV sets F | |
| Disposable step type endoscopic cutting stapler and nail bin | Nanjing Maidixin Medical Device Co.,Ltd | MLCR-Mb,MLCNC-60b-purple, MLCNC-45b-white | |
| laparoscopic instruments | Hangzhou KANGJI Medical Instrument co., LTD | ||
| Ultrasound knife | INNOLCON, Medical Science and Technology (suzhou) co., LTD |
参考文献
- Bray, F., et al. Global cancer statistics 2018: Globocan estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA Cancer J Clin. 68 (6), 394-424 (2018).
- Chevallay, M., et al. Cancer of the gastroesophageal junction: A diagnosis, classification, and management review. Ann N Y Acad Sci. 1434 (1), 132-138 (2018).
- Omori, T., et al. A randomized controlled trial of single-port versus multi-port laparoscopic distal gastrectomy for gastric cancer. Surg Endosc. 35 (8), 4485-4493 (2021).
- Kang, S. H., et al. Postoperative pain and quality of life after single-incision distal gastrectomy versus multiport laparoscopic distal gastrectomy for early gastric cancer - a randomized controlled trial. Surg Endosc. 37 (3), 2095-2103 (2023).
- Teng, W., et al. Short-term outcomes of reduced-port laparoscopic surgery versus conventional laparoscopic surgery for total gastrectomy: A single-institute experience. BMC Surg. 23 (1), 75 (2023).
- Podda, M., Saba, A., Porru, F., Pisanu, A. Systematic review with meta-analysis of studies comparing single-incision laparoscopic colectomy and multiport laparoscopic colectomy. Surg Endosc. 30 (11), 4697-4720 (2016).
- Omori, T., et al. Transumbilical single-incision laparoscopic distal gastrectomy for early gastric cancer. Surg Endosc. 25 (7), 2400-2404 (2011).
- Teng, W., et al. Comparison of short-term outcomes between single-incision plus one-port laparoscopic surgery and conventional laparoscopic surgery for distal gastric cancer: A randomized controlled trial. Transl Cancer Res. 11 (2), 358-366 (2022).
- Du, G. S., et al. Single-incision plus one-port laparoscopic gastrectomy versus conventional multi-port laparoscopy-assisted gastrectomy for gastric cancer: A retrospective study. Surg Endosc. 36 (5), 3298-3307 (2022).
- Chinese Society of Laparoscopic and Endoscopic Surgery, C. S. S., Chinese Medical Association, Association, R. a. L. S. C. O. C. R. H., Endoscopic and Robotic Surgical Society, C. a.-C. A., Endoscopy and Minimally Invasive Technology Society, C. a. O. M. E. Guideline for laparoscopic gastrectomy for gastric cancer (2023 edition). Chinese J Digest Surg. 22 (4), 425-436 (2023).
- Hjermstad, M. J., et al. Studies comparing numerical rating scales, verbal rating scales, and visual analogue scales for assessment of pain intensity in adults: A systematic literature review. J Pain Symptom Manage. 41 (6), 1073-1093 (2011).
- Park, D. J., Lee, J. H., Ahn, S. H., Eng, A. K., Kim, H. H. Single-port laparoscopic distal gastrectomy with d1+β lymph node dissection for gastric cancers: Report of 2 cases. Surg Laparosc Endosc Percutan Tech. 22 (4), e214-e216 (2012).
- Ahn, S. H., Jung, D. H., Son, S. Y., Park, D. J., Kim, H. H. Pure single-incision laparoscopic d2 lymphadenectomy for gastric cancer: A novel approach to 11p lymph node dissection (midpancreas mobilization). Ann Surg Treat Res. 87 (5), 279-283 (2014).
- Ahn, S. H., Son, S. Y., Jung, D. H., Park, D. J., Kim, H. H. Pure single-port laparoscopic distal gastrectomy for early gastric cancer: Comparative study with multi-port laparoscopic distal gastrectomy. J Am Coll Surg. 219 (5), 933-943 (2014).
- Kim, S. M., et al. Techniques of the single-port totally laparoscopic distal gastrectomy. Ann Surg Oncol. 22 (Suppl 3), S341 (2015).
- Jeong, O., Park, Y. K., Ryu, S. Y. Early experience of duet laparoscopic distal gastrectomy (duet-ldg) using three abdominal ports for gastric carcinoma: Surgical technique and comparison with conventional laparoscopic distal gastrectomy. Surg Endosc. 30 (8), 3559-3566 (2016).
- Kim, S. M., et al. Comparison of single-port and reduced-port totally laparoscopic distal gastrectomy for patients with early gastric cancer. Surg Endosc. 30 (9), 3950-3957 (2016).
- Lee, B., et al. Learning curve of pure single-port laparoscopic distal gastrectomy for gastric cancer. J Gastric Cancer. 18 (2), 182-188 (2018).
- Omori, T., et al. The safety and feasibility of single-port laparoscopic gastrectomy for advanced gastric cancer. J Gastrointest Surg. 23 (7), 1329-1339 (2019).
- Kang, S. H., et al. Long-term outcomes of single-incision distal gastrectomy compared with conventional laparoscopic distal gastrectomy: A propensity score-matched analysis. J Am Coll Surg. 234 (3), 340-351 (2022).
- Lee, S., et al. Intracorporeal modified delta-shaped gastroduodenostomy during 2-port distal gastrectomy: Technical aspects and short-term outcomes. Ann Surg Treat Res. 105 (3), 172-177 (2023).
- Ahn, S. H., Park, D. J., Son, S. Y., Lee, C. M., Kim, H. H. Single-incision laparoscopic total gastrectomy with d1+beta lymph node dissection for proximal early gastric cancer. Gastric Cancer. 17 (2), 392-396 (2014).
- Ertem, M., Ozveri, E., Gok, H., Ozben, V. Single incision laparoscopic total gastrectomy and d2 lymph node dissection for gastric cancer using a four-access single port: The first experience. Case Rep Surg. 2013, 504549 (2013).
- Lee, I. Y., Lee, D., Lee, C. M. Case report: Single-port laparoscopic total gastrectomy for gastric cancer in patient with situs inversus totalis. Front Oncol. 13, 1094053 (2023).
- Luo, Y., et al. A novel single-port robot for total gastrectomy to treat gastric cancer: A case report (with video). Asian J Endosc Surg. 17 (2), e13292 (2024).
- Lee, C. M., et al. Single-port laparoscopic proximal gastrectomy with double tract reconstruction for early gastric cancer: Report of a case. J Gastric Cancer. 16 (3), 200-206 (2016).
転載および許可
このJoVE論文のテキスト又は図を再利用するための許可を申請します
許可を申請さらに記事を探す
This article has been published
Video Coming Soon
Copyright © 2023 MyJoVE Corporation. All rights reserved