Case Report
Одиночный разрез плюс один порт Лапароскопическая проксимальная гастрэктомия с двухканальным анастомозом для лечения рака желудка
В этой статье
Резюме
Лапароскопическая проксимальная гастрэктомия с одним разрезом и одним портом и двухканальным анастомозом первоначально применялась для радикальной резекции проксимального рака желудка. Это исследование продемонстрировало осуществимость процедуры и заложило основу для дальнейших исследований.
Аннотация
Лапароскопическая проксимальная гастрэктомия с одним разрезом и одним портом с двухканальным анастомозом (SILT-DT) является минимально инвазивным хирургическим подходом для лечения проксимального рака желудка. Эта методика включает в себя комплексную лапароскопическую резекцию проксимального отдела желудка, диссекцию лимфатических узлов и двухтрактовый анастомоз. Благодаря интеграции однопортовой лапароскопической хирургии со вспомогательным операционным отверстием, SILT-DT снижает сложность процедуры и облегчает установку дренажной трубки брюшной полости. По сравнению с традиционной пятипортовой лапароскопической гастрэктомией, SILT-DT требует меньшего количества портов и приводит к более короткой длине разрезов, что способствует уменьшению послеоперационной боли и более быстрому восстановлению. Для обеспечения успеха процедуры была проведена тщательная предоперационная оценка, при этом были тщательно учтены такие факторы, как размер опухоли, стадия, расположение и ИМТ пациента. Эта всесторонняя оценка позволила оптимально выбрать пациента и спланировать хирургическое вмешательство. Послеоперационное наблюдение не показало существенных осложнений, что подчеркивает безопасность и эффективность SILT-DT. Этот инновационный метод предлагает многообещающую минимально инвазивную альтернативу для лечения проксимального рака желудка при сохранении отличных клинических результатов.
Введение
Лапароскопические методики в последнее время стали одним из основных направлений хирургического лечения рака желудка 1,2. Рутинная лапароскопическая хирургия при раке желудка в основном проводится методом 5 отверстий. С развитием хирургических методов и постоянным совершенствованием медицинского оборудования, лапароскопическая хирургия рака желудка с уменьшенным портом постепенно развивалась для дальнейшего снижения хирургической травмы, минимизации нарушений брюшной полости и ускорения послеоперационного восстановления 3,4,5,6.
Омори7 впервые сообщил об однопортовой лапароскопической хирургии дистального отдела рака желудка в 2011 году. Чисто однопортовая лапароскопическая радикальная гастрэктомия при раке желудка сложнее, чем традиционная пятипортовая лапароскопическая гастрэктомия. Для решения этой проблемы к однопортовой лапароскопической процедуре добавляется вспомогательное операционное отверстие, что снижает сложность операции и облегчает установку брюшной дренажной трубки 8,9. Лапароскопическая хирургия с одним разрезом и одним портом (SILS+1), минимально инвазивная техника для пациентов с раком желудка, приобрела популярность в последние годы благодаря меньшему количеству портов и более короткой длине разрезов.
В настоящее время однопортовая лапароскопическая хирургия или хирургия рака желудка SILS+1 относительно распространена при дистальной гастрэктомии, в то время как ее применение при тотальной гастрэктомии встречается редко. Кроме того, не сообщалось об использовании тотального лапароскопического двухтрактового анастомоза рака желудка.
Исходя из этого, мы впервые попытались провести однопортовую и однопортовую тотальную лапароскопическую проксимальную гастрэктомию с двухтрактовым анастомозом (SILT-DT). Транспумбильный порт использовался в качестве основного операционного порта, а левый верхний дренажный порт брюшной полости служил вспомогательным операционным портом. Эта техника была использована для выполнения проксимальной гастрэктомии, диссекции лимфатических узлов D2 и двухтрактового анастомоза для реконструкции пищеварительного тракта.
ПРЕЗЕНТАЦИЯ КЛИНИЧЕСКОГО СЛУЧАЯ:
Пациент, 63-летний мужчина, был госпитализирован после того, как во время гастроскопии в пищеводно-желудочном переходе была обнаружена опухоль (рис. 1). Результаты биопсии гастроскопа показали умеренно дифференцированную аденокарциному (рис. 2). Предоперационная КТ органов грудной клетки и брюшной полости не выявила признаков отдаленного метастазирования (Рисунок 3). Пациентка ранее была здорова и не имела в анамнезе операций на брюшной полости.
Отбор пациентов
Пациенты имели право на участие, если у них была гистологически подтвержденная аденокарцинома гастроэзофагеального перехода II или III типа по Зиверту, при этом предоперационная КТ брюшной полости не показала увеличения лимфатических узлов вокруг желудка или отдаленных метастазов. Максимальный диаметр опухоли должен был быть менее 3 см, а расстояние между нижним полюсом опухоли и желудочным углом должно было превышать 5 см. Критериями исключения были пациенты, которым ранее была проведена абдоминальная операция, пациенты с предоперационным диаметром опухоли более 3 см и/или требованием множественной висцеральной резекции, пациенты, которым были проведены обсуждения в мультидисциплинарной команде (МДТ) по поводу неоадъювантной химиолучевой терапии, или те, кто получил неоадъювантную химиолучевую терапию, а также пациенты с непереносимостью лапароскопической хирургии.
протокол
Операция проходила в соответствии со стандартными процедурами и получила этическое одобрение. Это исследование было разрешено Комитетом по этике Центральной больницы Сянъян, аффилированной с Хубэйским университетом искусств и наук. От пациента было получено информированное письменное согласие. Содержание и методы исследования соответствовали нормам и требованиям медицинской этики. Реагенты и оборудование, использованные в исследовании, перечислены в Таблице материалов.
1. Предоперационные этапы
- Пациенту было рекомендовано принимать пероральную натрий-фосфатную соль для подготовки кишечника за день до операции. Пациент голодал в течение 8 ч и ему разрешалось принимать воду за 2 ч до операции. Верхний желудочный зонд был установлен перед входом в операционную.
- Пациент был расположен в положении лежа на спине с разделенными ногами, голова была поднята и слегка наклонена вправо.
- Была проведена эндотрахеальная интубация, а также введена общая анестезия в соответствии с утвержденными в учреждении протоколами.
2. Хирургическое вмешательство
- Вокруг пупка был сделан поперечный разрез размером 3,0-3,5 см для введения порта SILS, оснащенного четырьмя встроенными троакарами (рис. 4A). Дополнительный 12-миллиметровый троакар был вставлен в левый верхний квадрант, чтобы служить операционным портом для хирургических инструментов, включая ультразвуковые ножницы, эндоскопический линейный степлер и послеоперационную дренажную трубку.
- Ультразвуковой нож был использован для рассечения жировой лимфоидной ткани групп 1, 2, 3, 4, 7, 8a, 9 и 11p (рис. 5A, B). Была обеспечена длина нижнего сегмента пищевода примерно 5-7 см (рис. 5В), а также была сохранена свобода большей кривизны и меньшей кривизны желудка.
ПРИМЕЧАНИЕ: Процедура SILT-DT показана на рисунке 5. Диссекция желудка и лимфатических узлов выполнена в соответствии с Рекомендациями по лапароскопической хирургии при раке желудка (издание 2023 года)10. Была завершена лимфаденэктомия D2 и проксимальная гастрэктомия. - Установлен пищеводно-тощий анастомоз (ЭЖ). Место анастомоза EJ было идентифицировано на тощей кишке, на расстоянии 20 см дистальнее связки Трейца и вблизи нижнего отдела пищевода. Анастомоз EJ осуществляли через 12-мм порт в левом верхнем квадранте с помощью 60-миллиметрового эндоскопического линейного степлера (рис. 5D).
ПРИМЕЧАНИЕ: Принципиальная схема, иллюстрирующая реконструкцию пищеварительного тракта, показана на рисунке 4B. - Эндоскопический линейный степлер диаметром 60 мм был использован для резекции образцов пищевода и закрытия отверстия анастомоза между тощей кишкой и пищеводом (рис. 5E).
- Был создан гастроеюнальный (GJ) анастомоз, участок которого отмечен на тощей кишке на 8-15 см дистальнее анастомоза EJ и на задней стенке большего искривления оставшегося желудка (рис. 5F).
- Установлен тоеюнальный анастомоз. Тоеюнный анастомоз проводили через разрез 3,5 см в области пупка с помощью эндоскопического линейного степлера диаметром 60 мм, размечая на расстоянии 5 см дистальнее места анастомоза GJ (рис. 5G).
- Отдельные анастомозы были закрыты и укреплены. Оба общих отверстия анастомоза GJ и ядеюнального анастомоза были закрыты с помощью нити 3-0 микро Джо. Мезангиальное отверстие закрывалось непрерывным швом.
- Дренажная трубка была помещена за анастомозом EJ и выведена из левой верхней части брюшной полости (Рисунок 5H).
3. Послеоперационное ведение
- Было проведено послеоперационное водное голодание, а желудочный зонд дренирован с помощью постоянного мешка.
- Желудочный зонд был удален через 48 ч наблюдения, что не обеспечило явного наличия кровянистой дренажной жидкости.
- Инфузию жидкости вводили для поддержания водно-электролитного и кислотно-щелочного баланса, а также для подавления кислотности. Продолжительность профилактического приема антибиотиков была ограничена максимум 48 ч.
- Ранняя мобилизация активно пропагандировалась в течение 6-24 ч после операции. Во время восстановления была начата жидкая диета на 2-3 дня.
- Оценивали утечку анастомоза, а на 7-й день оценивали развитие остаточного желудка с помощью рентгенографии верхних отделов желудочно-кишечного тракта.
- Дренажная трубка брюшной полости была удалена в течение 5-7 дней после выписки из больницы.
Результаты
Операция была завершена в течение 150 мин, с минимальным интраоперационным кровотечением 5 мл. Краткосрочных осложнений не было, послеоперационное восстановление пациента прошло успешно. В общей сложности было извлечено 24 лимфатических узла, метастазирование в лимфатические узлы не было обнаружено. Время операции составило 150 мин, а расчетная кровопотеря – 5 мл. Пациент оставался в постели в течение 2 дней. Время до первого метеоризма составило 70 ч, а употребление жидкой пищи и напитков пациент начал уже через 3 дня. Желудочный зонд был удален на4-е сутки, а дренажная трубка была удалена в течение 7 дней. Контрастное вещество сохранялось в остаточном желудке в течение 30-50 мин без рефлюкса в пищевод (рис. 6). Косметический исход послеоперационных разрезов брюшной полости был удовлетворительным (Рисунок 4В). Боль оценивалась по 11-балльной числовой шкале (NRS), где 0 — отсутствие боли, а 10 — самая сильная боль, которую только можно представить:11. Подробные данные по пациенту представлены в Table 1.
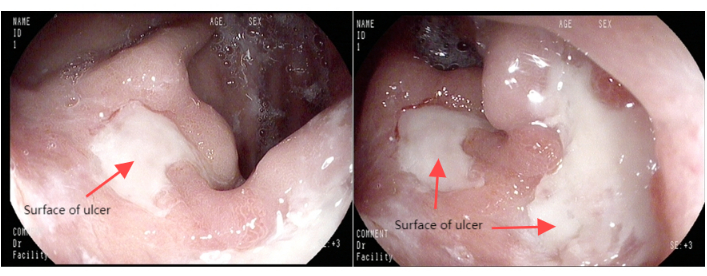
Рисунок 1: Гастроскопические изображения. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этой цифры.
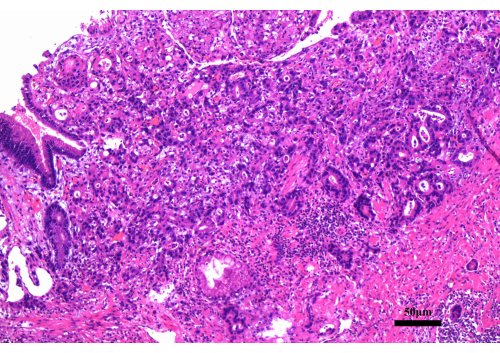
Рисунок 2: Результаты гастроскопической биопсии. При гастроскопической биопсии выявлена умеренно дифференцированная аденокарцинома. Масштабная линейка: 50 μм; увеличение: 200x. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этой цифры.
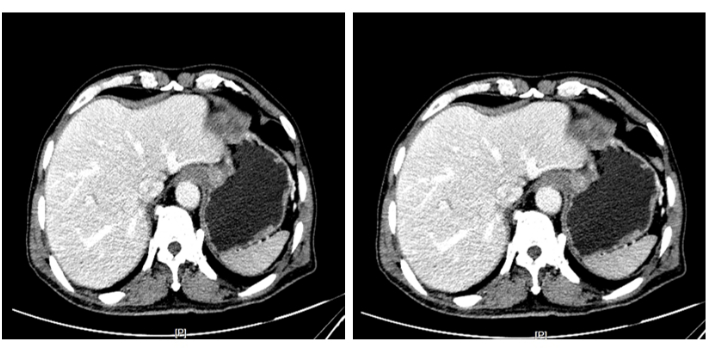
Рисунок 3: Усиленная компьютерная томография брюшной полости. Гетерогенное усиление наблюдалось в кардии, которая рассматривалась как опухолевое поражение, и опухоль не проникала в мышечный слой. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этой цифры.
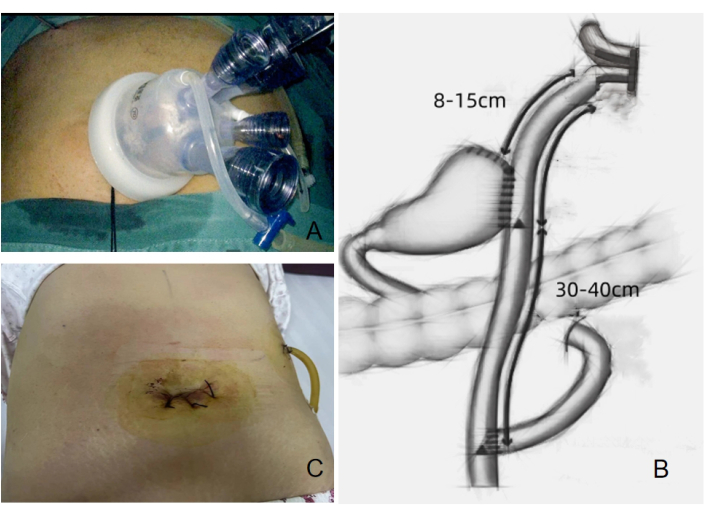
Рисунок 4: Хирургическая подготовка и состояние послеоперационной раны. (А) Четыре встроенных троакара, используемых в процедуре. (Б) Двухтрактовый анастомоз, выполняемый во время операции. (В) Состояние послеоперационной раны, показанное после процедуры. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этой цифры.
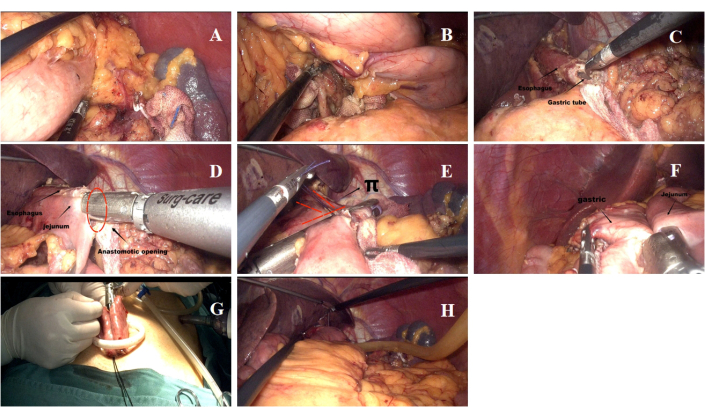
Рисунок 5: Детали хирургической процедуры. (A,B) Процесс очищения лимфатических узлов во время операции. (В) Пересечение пищевода и открытие нижнего конца пищевода. (D) Эзофагоеюностомия из стороны в сторону, выполняемая как часть анастомоза. (E) Закрытие общего отверстия в месте пищеводного анастомоза. (F) Завершена остаточная гастроеюностомия. (G) Энтерокишечный анастомоз из стороны в сторону через пупочный разрез. (H) Положение дренажной трубки. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этой цифры.
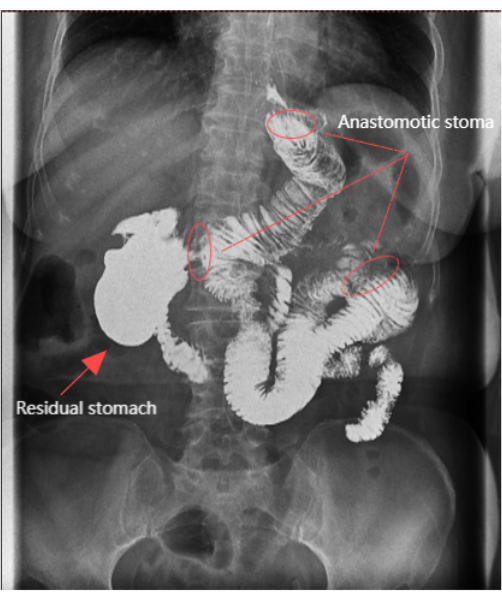
Рисунок 6: Рентгенография верхних отделов желудочно-кишечного тракта. Рентгенография верхних отделов желудочно-кишечного тракта показала, что анастомоз был открыт и оставшийся желудок был хорошо виден. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этой цифры.
| Элементы | Результат |
| Род | Мужской |
| Год | 63 |
| ИМТ (кг/м2) | 23.5 |
| Степень анестезии | Глава III |
| Предоперационная TNM-стадия | КТ1Н0М0 |
| Время работы (мин) | 150 |
| Длина разреза (см) | 2.8 |
| Объем интраоперационного кровотечения (мл) | 5 |
| Патология | умеренно дифференцированная аденокарцинома |
| Расстояние до проксимального края (см) | 3.4 |
| Расстояние до дистального края (см) | 5.5 |
| Размер опухоли (см) | 1.5*2*1.2 |
| Количество восстановленных лимфатических узлов | 24 |
| TNM-постановка | пТ2Н0М0 |
| Продолжительность удаления желудочного зонда после операции (d) | 4 |
| Продолжительность до первого приема пищи | 3 |
| Продолжительность активности постели | 2 |
| Продолжительность до метеоризма (ч) | 70 |
| Время для опорожнения кишечника (d) | 6 |
| Продолжительность дренажной трубки (d) | 7 |
| Оценка боли в первые сутки после операции | 2 |
| Послеоперационное пребывание в стационаре (сутки) | 8 |
| Осложнений | Никакой |
Таблица 1: Периоперационные данные пациента. Подробная информация о периоперационных данных пациента, включая ключевые измерения и результаты.
Обсуждение
Однопортовая и уменьшенно-портовая лапароскопическая радикальная гастрэктомия стали инновационными подходами к лечению рака желудка и неуклонно завоевывают признание. Эти методы привлекают повышенное внимание из-за их преимуществ, включая улучшение косметических результатов, уменьшение послеоперационной боли, снижение риска инфекций в области хирургического вмешательства и более быстрое время восстановления.
Результаты 12 исследований с участием 343 случаев показали, что однопортовая и уменьшенно-портовая лапароскопическая хирургия была эффективна в лечении дистального отдела рака желудка, составляя большинство случаев 3,4,12,13,14,15,16,17,18,19,20,21 . Тем не менее, только четыре исследования были сосредоточены на тотальной резекции желудка 22,23,24,25. Эти данные свидетельствуют о том, что клинические исследования и применение хирургии однопортового рака желудка, в частности тотальной гастрэктомии, ограничены из-за высокой хирургической сложности, необходимой обширной диссекции и удаления лимфатических узлов, а также сложной техники эндоскопической реконструкции пищеварительного тракта.
Мы успешно провели первую лапароскопическую проксимальную гастрэктомию с двухтрактовым анастомозом с использованием одного разреза и одного порта для лечения проксимального рака желудка. По сравнению с традиционными хирургическими методами, операция с одним разрезом и одним портом является менее инвазивной. По сравнению с однопортовой техникой, добавление левого верхнего брюшного порта повышает удобство во время операции и позволяет рационально разместить дренажную трубку через разрез в верхней левой части живота.
Lee et al.26 сообщили о первом случае однопортовой лапароскопической проксимальной гастрэктомии с двухтрактовой реконструкцией при раннем раке желудка в 2016 году. По сравнению с SILS, операция с одним разрезом и одним портом включает в себя дополнительный левый верхний брюшной порт, создавая треугольную структуру, состоящую из пупочной области, левой верхней части живота и хирургической области. Этот инновационный подход эффективно устраняет ограничения чистой хирургии с одним разрезом, такие как недостаточная антитракционная и линейная визуализация. Кроме того, он повышает гибкость правого инструмента хирурга, что приводит к значительному повышению эффективности операции и снижению сложности во время каждого анастомоза при тотальной лапароскопии.
Кроме того, несколько стратегий могут повысить операционную эффективность и сократить продолжительность процедуры. Хирург может рассмотреть возможность изменения их положения во время диссекции лимфатических узлов и реконструкции пищеварительного тракта, например, расположиться слева от пациента или между ног пациента, чтобы оптимизировать воздействие на операционную область. Для таких процедур, как эзофагоеюностомия и гастроеюностомия, рекомендуется, чтобы один ассистент или главный хирург сохранял стабильное положение, в то время как другой выполнял стыковку, тем самым повышая эффективность анастомоза и сводя к минимуму риск отрыва тканей. Кроме того, рекомендуется использовать встроенные лапароскопические инструменты для минимизации помех между оптическими волокнами и другими инструментами.
Таким образом, лапароскопическая проксимальная гастрэктомия с одним разрезом и одним портом с двухканальным анастомозом возможна для лечения проксимального рака желудка. В этом случае у пациента наблюдалось успешное выздоровление. Операция является малоинвазивной, а восстановление проходит быстрее. Тем не менее, ограничения этого протокола включают необходимость ранней стадии рака желудка или доброкачественных опухолей желудка, при этом ИМТ пациента не является чрезмерно высоким. Применение данного протокола не рекомендуется пациентам с местнораспространенным заболеванием или высоким ИМТ из-за потенциального риска положительных краев опухоли и повышенной сложности хирургического вмешательства. Этот протокол все еще находится на стадии технического исследования, без установленных рекомендаций и с недостаточными клиническими данными для полной проверки его долгосрочной эффективности. Разработка данного протокола требует этического одобрения со стороны медицинских учреждений и строгого соблюдения хирургических показаний. Необходимы дальнейшие клинические исследования и исследования для определения клинической применимости методики SILT-DT.
Раскрытие информации
Авторы не имеют конфликта интересов или финансовых связей, которые можно было бы раскрыть.
Благодарности
Эта работа была поддержана грантами Научно-исследовательского проекта Комиссии по здравоохранению провинции Хубэй и Ключевого проекта Сянъян по науке и технологиям в области медицины и здравоохранения (2021YL15).
Материалы
| Name | Company | Catalog Number | Comments |
| 3D laparoscope | KARL STORZ SE & Co. KG | 26605BA | |
| Absorbability surgical sutures | Johnson & Johnson | TLBJXZ | |
| Absorbable ligature clip | Hangzhou KANGJI Medical Instrument co., LTD | KJ-JZJ02ML | |
| Disposable puncture device | Hangzhou KANGJI Medical Instrument co., LTD | Type IV sets F | |
| Disposable step type endoscopic cutting stapler and nail bin | Nanjing Maidixin Medical Device Co.,Ltd | MLCR-Mb,MLCNC-60b-purple, MLCNC-45b-white | |
| laparoscopic instruments | Hangzhou KANGJI Medical Instrument co., LTD | ||
| Ultrasound knife | INNOLCON, Medical Science and Technology (suzhou) co., LTD |
Ссылки
- Bray, F., et al. Global cancer statistics 2018: Globocan estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA Cancer J Clin. 68 (6), 394-424 (2018).
- Chevallay, M., et al. Cancer of the gastroesophageal junction: A diagnosis, classification, and management review. Ann N Y Acad Sci. 1434 (1), 132-138 (2018).
- Omori, T., et al. A randomized controlled trial of single-port versus multi-port laparoscopic distal gastrectomy for gastric cancer. Surg Endosc. 35 (8), 4485-4493 (2021).
- Kang, S. H., et al. Postoperative pain and quality of life after single-incision distal gastrectomy versus multiport laparoscopic distal gastrectomy for early gastric cancer - a randomized controlled trial. Surg Endosc. 37 (3), 2095-2103 (2023).
- Teng, W., et al. Short-term outcomes of reduced-port laparoscopic surgery versus conventional laparoscopic surgery for total gastrectomy: A single-institute experience. BMC Surg. 23 (1), 75 (2023).
- Podda, M., Saba, A., Porru, F., Pisanu, A. Systematic review with meta-analysis of studies comparing single-incision laparoscopic colectomy and multiport laparoscopic colectomy. Surg Endosc. 30 (11), 4697-4720 (2016).
- Omori, T., et al. Transumbilical single-incision laparoscopic distal gastrectomy for early gastric cancer. Surg Endosc. 25 (7), 2400-2404 (2011).
- Teng, W., et al. Comparison of short-term outcomes between single-incision plus one-port laparoscopic surgery and conventional laparoscopic surgery for distal gastric cancer: A randomized controlled trial. Transl Cancer Res. 11 (2), 358-366 (2022).
- Du, G. S., et al. Single-incision plus one-port laparoscopic gastrectomy versus conventional multi-port laparoscopy-assisted gastrectomy for gastric cancer: A retrospective study. Surg Endosc. 36 (5), 3298-3307 (2022).
- Chinese Society of Laparoscopic and Endoscopic Surgery, C. S. S., Chinese Medical Association, Association, R. a. L. S. C. O. C. R. H., Endoscopic and Robotic Surgical Society, C. a.-C. A., Endoscopy and Minimally Invasive Technology Society, C. a. O. M. E. Guideline for laparoscopic gastrectomy for gastric cancer (2023 edition). Chinese J Digest Surg. 22 (4), 425-436 (2023).
- Hjermstad, M. J., et al. Studies comparing numerical rating scales, verbal rating scales, and visual analogue scales for assessment of pain intensity in adults: A systematic literature review. J Pain Symptom Manage. 41 (6), 1073-1093 (2011).
- Park, D. J., Lee, J. H., Ahn, S. H., Eng, A. K., Kim, H. H. Single-port laparoscopic distal gastrectomy with d1+β lymph node dissection for gastric cancers: Report of 2 cases. Surg Laparosc Endosc Percutan Tech. 22 (4), e214-e216 (2012).
- Ahn, S. H., Jung, D. H., Son, S. Y., Park, D. J., Kim, H. H. Pure single-incision laparoscopic d2 lymphadenectomy for gastric cancer: A novel approach to 11p lymph node dissection (midpancreas mobilization). Ann Surg Treat Res. 87 (5), 279-283 (2014).
- Ahn, S. H., Son, S. Y., Jung, D. H., Park, D. J., Kim, H. H. Pure single-port laparoscopic distal gastrectomy for early gastric cancer: Comparative study with multi-port laparoscopic distal gastrectomy. J Am Coll Surg. 219 (5), 933-943 (2014).
- Kim, S. M., et al. Techniques of the single-port totally laparoscopic distal gastrectomy. Ann Surg Oncol. 22 (Suppl 3), S341 (2015).
- Jeong, O., Park, Y. K., Ryu, S. Y. Early experience of duet laparoscopic distal gastrectomy (duet-ldg) using three abdominal ports for gastric carcinoma: Surgical technique and comparison with conventional laparoscopic distal gastrectomy. Surg Endosc. 30 (8), 3559-3566 (2016).
- Kim, S. M., et al. Comparison of single-port and reduced-port totally laparoscopic distal gastrectomy for patients with early gastric cancer. Surg Endosc. 30 (9), 3950-3957 (2016).
- Lee, B., et al. Learning curve of pure single-port laparoscopic distal gastrectomy for gastric cancer. J Gastric Cancer. 18 (2), 182-188 (2018).
- Omori, T., et al. The safety and feasibility of single-port laparoscopic gastrectomy for advanced gastric cancer. J Gastrointest Surg. 23 (7), 1329-1339 (2019).
- Kang, S. H., et al. Long-term outcomes of single-incision distal gastrectomy compared with conventional laparoscopic distal gastrectomy: A propensity score-matched analysis. J Am Coll Surg. 234 (3), 340-351 (2022).
- Lee, S., et al. Intracorporeal modified delta-shaped gastroduodenostomy during 2-port distal gastrectomy: Technical aspects and short-term outcomes. Ann Surg Treat Res. 105 (3), 172-177 (2023).
- Ahn, S. H., Park, D. J., Son, S. Y., Lee, C. M., Kim, H. H. Single-incision laparoscopic total gastrectomy with d1+beta lymph node dissection for proximal early gastric cancer. Gastric Cancer. 17 (2), 392-396 (2014).
- Ertem, M., Ozveri, E., Gok, H., Ozben, V. Single incision laparoscopic total gastrectomy and d2 lymph node dissection for gastric cancer using a four-access single port: The first experience. Case Rep Surg. 2013, 504549 (2013).
- Lee, I. Y., Lee, D., Lee, C. M. Case report: Single-port laparoscopic total gastrectomy for gastric cancer in patient with situs inversus totalis. Front Oncol. 13, 1094053 (2023).
- Luo, Y., et al. A novel single-port robot for total gastrectomy to treat gastric cancer: A case report (with video). Asian J Endosc Surg. 17 (2), e13292 (2024).
- Lee, C. M., et al. Single-port laparoscopic proximal gastrectomy with double tract reconstruction for early gastric cancer: Report of a case. J Gastric Cancer. 16 (3), 200-206 (2016).
Перепечатки и разрешения
Запросить разрешение на использование текста или рисунков этого JoVE статьи
Запросить разрешениеСмотреть дополнительные статьи
This article has been published
Video Coming Soon
Авторские права © 2025 MyJoVE Corporation. Все права защищены