Method Article
차단 혈액 시스템을 사용하여 준비 및 더블 복용 버피 코트의 혈소판 제품의 병원체 불 활성화
요약
이 문서는 전체 혈액 기부에서 준비 병원체 불 활성화에 대한 요격 피 시스템과 치료를 두 번 복용 버피 코트의 혈소판 중점을 생산 외 레브로 대학 병원에서 사용하는 프로세스를 설명합니다. 체외에서 품질 스토리지의 7 일 동안 평가하고 있습니다.
초록
혈액 센터는 극대화 생산에 발생하는 혈액 제품 기부 수율뿐만 아니라, 수혈 전송 질병으로부터 보호 등의 수혈 환자에 대한 안전성 가능한 가장 높은 수준을 보장하는 등 많은 도전에 직면하고 있습니다. 이것은 소모품, 장비, 폐기물 등 중 개인 비용 등의 운영 비용을 최소화 fiscally 책임 방식으로 수행해야합니다.
몇 가지 방법은 혈소판이 수혈에 중점을 생산 할 수 있습니다. 가장 일반적인 중 하나는 하나의 치료 혈소판 단위 (단위 당 또는 현지 규정에 따라 ≥ 2.0 X10 11 혈소판) 반년 혈액 기부까지에서 버피 코트 층을 풀링하여 준비되어있는 버피 코트 방식입니다. "더블 복용량"전체 혈액 유래 혈소판을 생산하기위한 절차는 최근에 개발되었습니다.
준비하기위한 새로운 방법입니다 여기에 제시된이중 복용량 전체 혈액 유래 혈소판은 7 버피 코트와 이후 병원체 불 활성화에 대한 요격 피 시스템과 이중 복용량 단위를 치료 수영장에서 중점을두고 있습니다. 차단은 바이러스, 박테리아, 기생충 및 기증 혈액에 존재 할 수 있습니다 오염 기증자 화이트 셀을 비활성화하기 위해 개발되었습니다. , 듀얼 저장 용기 (이하 "DS 세트")로 설정 절편 처리를 이용하여 두 번 복용 버피 코트 방식을 차단 페어링하면함으로써 환자 안전을 극대화, 혈액 센터는 단일 병원체 불 활성화 처리 세트에서의 이중 복용량 단위의 각을 치료 할 수 있습니다 비용을 최소화하면서. 이중 복용량 버피 코트 방법은 적은 버피 코트가 필요하며 단일 복용 버피 코트 혈소판 단위의 준비 및 치료에 비해 50 % (예를 들면 풀링 세트, 필터 세트, 혈소판 첨가제 솔루션 및 멸균 연결 웨이퍼)까지하여 소모품의 사용을 감소 . 기타 비용 절감 적은 폐기물, 적은 장비 maintenan을 포함CE, 낮은 전력 요구 사항, 인사 시간을 단축하고, 낮은 수집 비용은 apheresis 기술에 비해.
프로토콜
1. 전체 혈액 수집
- 450 ML의 상단에있는 자원 봉사 기증자로부터 온 혈액을 수집 / 하단의 컬렉션은 지역 혈액 수집 가이드 라인에 따라 설정합니다.
- 전체 피를 원심 분리 및 분리하기 전에 냉각 판에 2 시간의 최소 저장됩니다.
2. 버피 코트 준비
- 적혈구, 버피 코트, 그리고 플라즈마 : 3 층에 혈액을 분리하는 하드 스핀을 사용하여 전체 혈액을 원심 분리기. 사용 원심 분리기 매개 변수 ± 2 ° C. 22 11 분에 4,880 RCF했다
- 수집 용기에 버피 코트를 떠나지, 상단 위성 가방과 바닥 위성 가방에 적혈구 (RBC)에 플라즈마를 표현하기 위해 자동화 된 혈액 분리기를 사용하십시오. 버피 코트는 각각 약 48 ML 37 %입니다에 대한 볼륨 및 혈소판 범위를 의미 타겟팅 할 수 있습니다.
- 버피 - 코트 22 ± 2 ° C.에서 혈소판 교반기에 하루 아침에 저장됩니다
3. 버피 코트 풀링
- 멸균 연결 7 버피 코트 및 병렬 라인 열차 구성에서 SSP + 혈소판 첨가제 솔루션 (PAS) 300 ML은 기차 길이를 감소, PAS는 열차의 맨 위에 있어야합니다. PAS 및 제 버피 코트 사이에 선을 고정.
- 버피 코트 단위 사이의 무균 연결을 열고 버피 코트가 마지막 용기에 배출 할 수 있습니다.
- 용접 및 PAS 및 제 버피 코트 사이의 클램프를 엽니 다. 첨가제 솔루션의 삼분의이 순차적으로 버피 코트 컨테이너의 각을 씻어 할 수 있습니다. 두 번 이상 남아있는 PAS의 절반을 사용하여 각 시간을 반복합니다.
- 평균 버피 코트 풀 볼륨 약 600 ML해야합니다. 각 버피 코트의 대상 볼륨과 혈소판이 충족되면 플라즈마 비율은 32 수 - 47% 나중에 그 과정에서 가로 챌 병원체 불 활성화 처리를 위해 필요에 따라.
- 빈 SSP +와 버피을 삭제 하시겠습니까코트 용기.
- 최적의 혈소판 복구를 들어, 원심 분리하기 전에 1 시간 동안 교반에 수영장을 유지.
- 멸균은 버피 코트 수영장에 통합 leukoreduction 필터와 혈소판 스토리지 컨테이너를 연결합니다.
- 정지 혈소판 (9 분 20 초에 462 RCF)에서 적혈구를 분리 할 수있는 버피 코트 수영장의 "부드러운 스핀"을 수행합니다. 혈소판 저장 용기에 leukoreduction 필터를 통해 자동으로 혈액 분리기를 사용하여 혈소판 현탁액을 표현한다.
- 420 ML 볼륨, 2.5-7.0 X 10 11 혈소판 복용하고, ≤ 4 X 10 6 / ML 붉은 세포 - 이전에 설명 된 처리 요구 사항은 혈소판 정지가 차단 300 ML 처리 사양을 충족하는지 확인합니다.
4. 치료를 차단
- 수집 후 1 일의 끝 (하루 0 수거의 날입니다) 전에 차단 치료를 수행합니다.
- 차단 처리 세트 포장을 푸는투명한 플라스틱 주머니에서 듀얼 저장 용기가있는.
- 멸균은 도청 처리 세트에 amotosalen 컨테이너의 튜브에 혈소판 정지 컨테이너를 연결합니다.
- 지역 요구 사항에 따라 적절한 혈액 제품 식별을 차단 처리 설정 저장 용기 라벨을 지정합니다.
- 혈소판을 잡아와 조명 컨테이너에 흐름에 amotosalen 솔루션을 수 있도록 먼저 amotosalen 컨테이너에 하단의 캐뉼라을 깰. 혈소판은 조명 컨테이너에 amotosalen 컨테이너를 통해 흐를 수 있도록 amotosalen 컨테이너의 상단 캐뉼라를 해봐.
- 부드럽게 혈소판과 amotosalen 혼합물을 혼합 amotosalen 컨테이너에 조명 컨테이너에서 공기를 표현한다.
- 튜브의 4cm에 대해 작성, 튜브에 혈소판 혼합물의 작은 금액을 표현한다. 이 튜브와 조명 컨테이너 모두에서 혈소판이 병원체 inactivati을 받다 보장치료.
- 조명 컨테이너와 amotosalen 컨테이너 사이의 튜브를 밀봉합니다. 조명 컨테이너에서 연장 튜브의 약 4cm보다 더를 남겨 없습니다. 제거하고 폐기 빈 혈소판과 amotosalen 용기를하고 샘플링 파우치에 클램프를 닫습니다.
- 왼쪽에있는 큰 칸에있는 조명 컨테이너와 오른쪽에있는 작은 구획의 주최자와 조명기로 처리 세트를 놓습니다.
- 조명기에 기부 ID, 제품 코드, 및 가공 세트 로트 번호를 입력 휴대용 바코드 장치를 사용합니다. 금속 커버를 닫고 조명기 그래픽 인터페이스에 메시지가 표시되면, 서랍을 닫습니다. 조명을 시작하려면 "시작"을 누르십시오.
- 조명 후, 조명기에서 처리 세트를 제거합니다. 조명기가 자동으로 처리 혈소판 장치 (들)에 대한 치료 보고서를 인쇄합니다.
- 주최자의 용기 포장을 푸는와 P에 목을 매latelets 및 가공 세트, 조명 컨테이너의 출구에서 캐뉼라을 아프게하고, 혈소판은 화합물 흡착 장치 (CAD) 용기에 흐를 수 있습니다.
- 플라즈마 추출기를 사용하여 조명 컨테이너에 CAD 컨테이너에서 공기를 표현, CAD 웨이퍼를 구부리 않도록주의를 즐길 수도 있습니다.
- CAD 컨테이너의 입구 포트에 근처에있는 튜브를 밀봉합니다. 제거하고 빈 조명 컨테이너를 폐기하십시오.
- 최소 6 시간의 혈소판 교반기에 첨부 된 저장 용기와 CAD 컨테이너,하지만 이상 16 시간을 놓으십시오. 이 ≤ 2 μm의 농도에 잔류 amotosalen의 감소가 발생합니다.
- CAD 치료 후 교반기에서 혈소판 단위를 제거합니다. 혈소판을 잡아. 캐뉼라을 해제하고 혈소판의 저장 용기로 유동 할 수 있습니다.
- CAD 컨테이너에 저장 용기에서 공기를 표현한다. 잔여 혈소판 농축 흐름 다시 저장 용기에 의한하자중력. Y-피팅 위의 튜브를 밀봉하고 빈 CAD 컨테이너를 제거합니다.
- 필요에 따라 저장 용기 사이 재배포 볼륨입니다. 볼륨 조정은 저장 용기의 무게에 의해 만들어집니다. 몇 센티미터에 저장 용기의 입구 위의 각 스토리지 컨테이너에 튜브를 밀봉, 5.2에 설명 된대로이 최종 제품에서 멸균 샘플을 확보 용이하게한다.
5. 제품 샘플링
- 일상적인 QC 테스트의 경우 최종 저장 용기는 저장 용기의 샘플링 주머니를 사용하여 한 번에 맛보실 수 있습니다. 이렇게하려면 혈소판 장치가 잘 혼합되도록 한 후 주머니에 클램프를 열고 여러 번 당겨 요. 주머니는 혈소판이 가득 한 후 튜브를 밀봉합니다. 적절한 실험실 튜브에 혈소판 샘플을 전송하고 즉시 assays을 수행합니다.
- 이러한 검증 연구로, 저장의 과정을 통해 여러 시간 지점에서 샘플을 구하려면 무균 연결혈소판 저장 용기의 튜브에 새로운 샘플링 컨테이너. 혈소판이 잘 샘플링 컨테이너에 전송하기 전에 혼합되어 있는지 확인합니다.
6.에서 체외 기능 평가
- 이 검증 연구를 들어, 체외 평가에서 CAD 처리 (1 일 또는 2 일, CAD 기간에 따라 다름) 후 다시 4 일에 수행 된 (또는 5 일)과 일 7. 체외 측정에서 볼륨, 혈소판 수, pH를, 포함 혈액 가스 (PO 2, PCO 2), 포도당, 젖산, 그리고 회전.
- 볼륨 첨가제 솔루션에서 혈소판의 비중으로 1.01 g / ML을 사용하여 무게에 의해 결정되었다.
- 헤모글로빈 오염은 색상 차트로 비교를 사용하여 시각적으로 평가되었습니다.
- 회전은 시각적으로 산출 된 것입니다.
- 다른 assays의 방법론에 대해 "장비의 표"를 참조하십시오.
7. 대표 결과
d를 생산하는 과정ouble 복용 버피 코트 혈소판은 볼륨과 혈소판에 대한 목표 사양을 충족 개별 버피 코트의 생산을 시작합니다. 이 최종 공정에서는 정품 확인을 통해 개별 버피 코트의 혈소판을 측정 할 실질적인하지 않습니다, 우리는 우리가 지속적으로 대상 볼륨과 혈소판을 충족 할 수 있도록하기 위해 버피 코트를 최적화하기 위해 별도의 노력을 사업으로 시작했다. 표 1에 도시 된 바와 같이, 우리의 최적화 된 버피 코트 46에서 볼륨 및 혈소판 모두 ± 2 ML 37 ± 3 %, 각각의 대상 값으로 호의를 비교했다.
풀링 후, 버피 코트 풀의 볼륨과 혈소판은 각각 부드러운 회전 원심 분리하기 전에 약 600 ML 20 %해야합니다. 표 2에 도시 된 바와 같이, 우리의 버피 코트의 수영장 615 평균 ± 5 ML을, 혈소판 수치가 19 평균 ± 1 %입니다.
더블 선량 혈소판의 conc의 부드러운 회전 원심 분리 결과차단 혈액 시스템 DS 처리 설정을 사용 병원체 불 활성화에 대한 입력 요구 사항을 충족합니다 entrate. 차단 치료를 위해 주요 입력 매개 변수는 볼륨, 혈소판 수, 플라즈마 비율 및 RBC 내용이 포함되어 있습니다. 또한, 우리는 버피 코트 수영장에 비해 혈소판 농축액에있는 혈소판의 ≥ 75 %를 복구하는 것을 목표로하고 있습니다. 지역 요구 사항에 따라, 백혈구 (WBC) 오염은 <1x10 6 / 단위 수 있어야합니다. 혈소판의 검증에 집중이 가로 치료뿐만 아니라 백혈구 오염 및 표 3에 도시 된 바와 같이 혈소판 복구 목표에 대한 주요 매개 변수를 만났다.
병원체 불 활성화에 대한 요격 과정은 하나의 가로 채기 처리 설정을 사용하여 두 번 복용 혈소판 농축액에 수행됩니다. 처리 세트는 처리 장치가 경로의 완성에 두 개인의 치료 혈소판 투여로 분할 할 수 있도록이 통합 저장 용기를 포함ogen의 불 활성화 과정. 유럽 가이드 라인은 테스트 단위의 75 %가 ≥ 200x10 9 혈소판을 포함 할 것을 요구 당 치료 dose1, 스웨덴 지역의 요구 사항이 테스트 단위의 75 %가 포함> 복용량 당 240x10 9 혈소판이 필요합니다. 차단 치료 후 평균 혈소판 내용은 265이었다 ± 22 X10 9 (n은 = 24). 또한, 단위의 88 %가 만족 또는 치료 복용량 당 240x10 9 혈소판을 초과,이은 유럽 지침 및 스웨덴어로 규정 모두에서 잘 수 있습니다. 이중 복용량 버피 코트의 준비와 각각 차단 처리 프로세스의 그림을위한 그림 1 & 2를 참조하십시오.
이 확인을 위해, 우리는 혈소판의 체외 특성의이 차단 처리 (개별 저장 용기에 분할 한 후 예를 들면) 이후에 중점을 측정, 매개 변수는 저장 용량이 7 일 동안 측정 하였다. 평균과 표준 편차는에 수집 된혈소판 투여 량, 산도, PO 2, PCO 2, 젖산 생산과 포도당 소비.
그림 3은 저장 후 7 일 이상 차단 치료 후 분할 제품의 각 차단 치료와 평균 혈소판 복용하기 전에 두 번 복용 혈소판 농축액의 혈소판 투여를 시작하는 의미를 보여줍니다. 저장 중 혈소판 손실은 약 9 %이다. 이 감소는 기존 혈소판의 저장 기간 동안 혈소판의 예상 손실의 차이가 있습니다.이
표 4는 하나의 단위로 처리 및 분할 후 차단 혈소판의에서 체외 특성을 요약 한 것입니다.
유럽 요구 사항에 따라, 혈소판의 pH는 유통 기한의 끝 부분을 통해 6.4 이상 남아 있어야합니다. 처리 과정에서 혈소판의 pH가 약간 혈소판 농도, 양, 그리고 혈소판 스토의 가스 투과성을 기반으로 떨어 집중분노의 컨테이너. 그림 4는 저장 7 일에 걸쳐 분할 혈소판 제품의 pH를 보여줍니다. 저장하는 동안 pH는 안정적이고 잘 처리 요구 사항 내에서 유지.
으로 인물 5A 및 5B, 혈소판 O이 소비와 CO 2 생산에 표시된 저장 후 7 일 동안 PL2410 컨테이너에서 차단 혈소판에 의해 계속 호흡을 나타냅니다. 숫자는 6A 및 6B 스토리지 7 일 동안 젖산과 포도당 수준을 보여 . 혈소판 포도당 소비와 젖산 생산은 스토리지의 7 일 동안 서로 일치합니다. 5 단위는 포도당 수준 이하 1.11 mmol / L을 (포도당 분석에 대한 낮은 제한)했다.
특히, 볼륨, 혈소판 수, 플라즈마 비율, 빨간색 파, 버피 코트의 준비와 풀링을 검증 제작 혈소판 그런 일이 도청 치료에 대한 입력 기준을 충족 집중ood 세포 오염. 최종 단위는 혈소판 복용과 산도 등의 스토리지를 7 일 동안 유효성 검사 기준을 만났습니다.
| 매개 변수 | 대상 범위 | 결과 ± SD 평균 |
| 볼륨 (ML) | ~ 48 | 46 ± 2 |
| 혈소판 (%) | ~ 37 | 37 ± 3 |
| 풀링하기 전에 시간을 잡아 | 교반기에서 숙박 | 교반기에서 숙박 |
개인 버피 코트 (N = 19)의 표 1. 특성.
| 매개 변수 | 대상 범위 | 결과 ± SD 평균 |
| 볼륨 (ML) | ~ 600 | 615 ± 5 |
| Hematocrit (%) | ~ 20 | 19 ± 1 |
| 원심 분리하기 전에 시간을 잡아 | 교반기에서 1 시간 | 교반기에서 1 시간 |
버피 코트 풀 (N = 12)의 표 2. 특성.
| 매개 변수 | 목표 | 결과 ± SD 평균 |
| 볼륨 (ML) | 370-420 | 404 ± 8 |
| 혈소판 수 (X10 9 / 단위) | 250-700 | 577 ± 62 |
| 혈소판 복구 (%)를 평균 | ≥ 75 | 75 ± 4 |
| 플라즈마 비율 (%) | 32-47 | 38 ± 1 |
| RBC (X10 6 / ML) | ≤ 4 | 1.2 ± 0.4 |
| WBC (X10 6 / 단위 이상) | ≤ 1 | 0.11 ± 0.1 |
| 차단 (시간) 전에 시간을 잡아 | 일 1 ≤ 끝 | 일 1 ≤ 끝 |
두 번 복용 혈소판의 표 3. 특성 (n은 = 12)을 중점을두고 있습니다.
| 평균 ± SD | 최소 | 최대 | |
| 볼륨 (ML) | 199 ± 16 | 182 | 236 |
| 혈소판 수 (X10 9 / 단위) | 265 ± 22 | 225 | 292 |
| 산도 (22 ° C) | 6.9 ± 0.1 | 6.8 | 7.0 |
| PO 2 (kPa) | 21.4 ± 4.8 | 12.8 | 27.3 |
| PCO 2 (kPa) | 4.3 및 PLusmn, 0.4 | 3.3 | 4.9 |
| 락트산 (mmol / L) | 9.1 ± 1.7 | 6.8 | 12.4 |
| 포도당 (mmol / L) | 5.3 ± 0.9 | 3.7 | 6.5 |
차단 치료 혈소판의 1 일 / 2 (싱글 단위, N = 24)의 표 4. 특성.
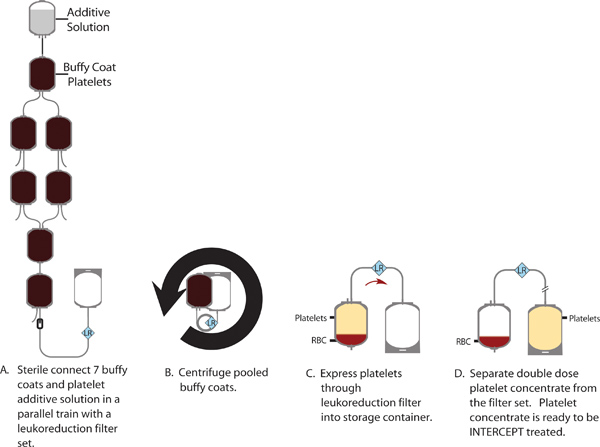
그림 1. 7 버피 코트의 수영장에서 더블 선량 혈소판 농축 생산.
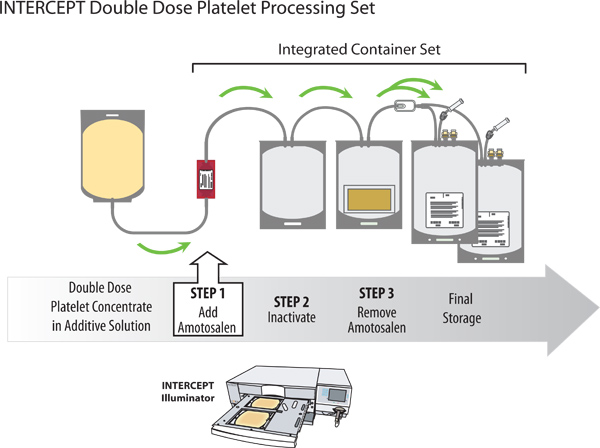
그림 2. 차단 혈액 시스템과 더블 선량 혈소판 농축액의 병원체 불 활성화.
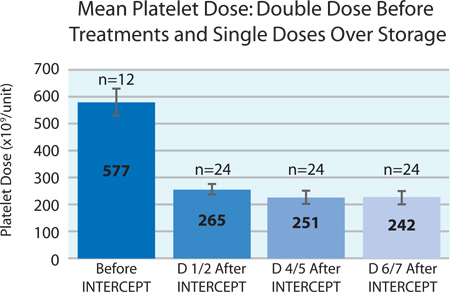
그림 3. 전과에 대한 혈소판 투여 량을 평균차단 치료 후 7 일 (N 도청 이전 = 12; 차단 한 후 N = 24).
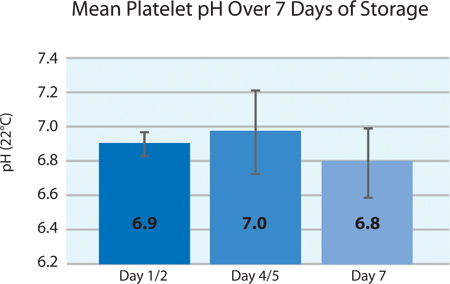
그림 4. 도청 처리 (N = 24) 이후에 혈소판 산도 ± SD를 의미합니다.
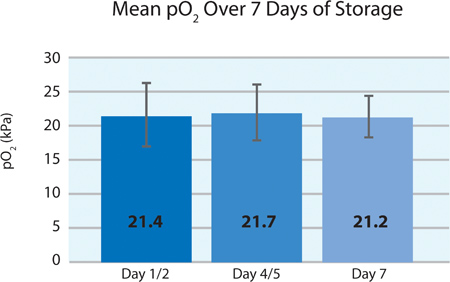
그림 5A는. 도청 처리 (N = 24) 이후 PO 2 ± SD를 의미합니다.
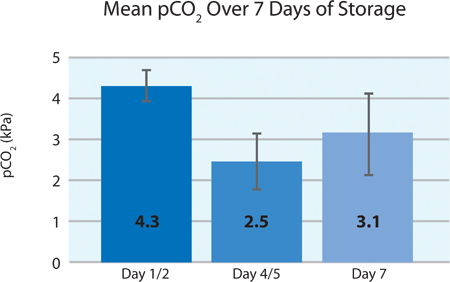
도 5B는. 도청 처리 (N = 24) 이후 PO 2 ± SD를 의미합니다.
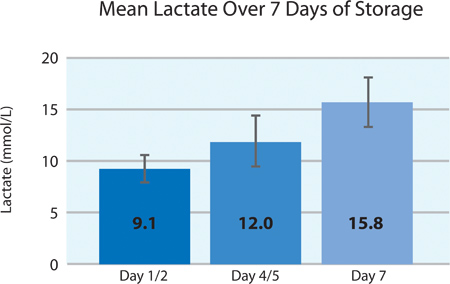
그림 6A는. 도청 처리 (N = 24) 이후 젖산 수준의 ± SD를 의미합니다.
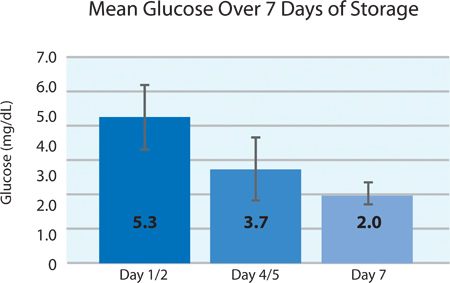
그림 6B는. 및 포도당 수준을 의미plusmn, SD 차단 처리 후 (N = 24).
토론
버피 코트의 혈소판은 여러 처리 단계를 필요로하는 혈소판 단위를 생산 전체 비용에 반영해야합니다 인사 시간, 소모품, 장비 및 폐기물 등의 사후 수집 비용에 따른 모든 책임은 사용자에게 있습니다. 각 버피 코트에서 혈소판 수율을 (버피 코트 볼륨 이랑 혈소판을 최적화를 통해) 개선하면 일곱 버피 코트의 수영장에서 두 번 복용 버피 코트 혈소판 단위의 생산이 가능합니다. 이 최적화가 수행 될 때, 버피 코트의 수는 혈소판 투여의 고정 번호를 생산하는 데 필요한 감소 될 수있다,이를 버피 코트의 전반적인 활용도를 개선하고 추가 혈소판의 생산 (PCS) 중점을 가능하게한다. 인사 시간뿐만 아니라 풀링 세트, 혈소판 첨가제 솔루션, 살균 연결 웨이퍼, 필터 세트, 및 원심 분리 절차 등의 소모품 및 장비 비용은 최대 50 %까지 감소된다. 혈소판 생산을 최적화하고, 생을 관련 비용을 절감 할뿐만 아니라S 풀링 방식은 우리뿐만 아니라 우리의 수혈을받는 사람에게 향상된 보호 기능을 제공 할 수 있도록 차단 듀얼 스토리지 컨테이너 처리 세트와 함께 사용하기위한 입력 요구 사항을 충족 혈소판 농축액 (PC)를 생성 할 수 있습니다.
병원체 불 활성화에 대한 도청 피 시스템은 핵산 복제 및 질병을 일으킬 수없는 렌더링 병원균을 방지 covalently 상호 링크 DNA와 RNA에 amotosalen와 자외선 A (UVA) 빛을 사용합니다. 3 그것은 효과적으로 바이러스, 세균 등의 병원균의 광범위한 스펙트럼을 inactivates , 기생충 및 오염 기증자 백혈구. 4-6 도청은 새로운 테스트가 개발하고 궁극적으로 구현하는 상당한 재정적 투자를 필요로하는 동안 역사적으로 상당한 지연을 포함 신흥 병원균에 대한 현재 테스트 패러다임에 대한 대안을 제공하는 경우 테스트 사용할 수 있습니다. 7,8는 또한 중복 안전 measu에 대한 대안을 제공 할 수 있습니다이러한 세균 검출 9 감마 방사선으로 고해상도. 또한 10-12, 도청은 우리가 두 번 투여 혈소판 단위를 취급 할 수있는 우리의 생산 효율성을 장점과 우리가 예산을 준수하는 데 도움이됩니다.
가로 더블 복용 버피 코트 방법은 혈액 센터 워크 플로우의 다양한 적용 할 수 있습니다. 예로서, 전체 혈액 컬렉션 500 ML로 증가 될 수있다; 컬렉션은 22 밤새 저장 될 수 있습니다 ° C 분리하기 전에. 또한, 다른 버피 코트 풀링 방법이 가능합니다 (예를 들어 문어 방법 대신 기차 방법) 및 / 또는 자동 장치 (예 TACSI) 남아있는 붉은 세포에서 두 번째 원심 분리하여 혈소판 정지의 분리에 활용 될 수있다 .
증가 혈소판 내용이 필요한 경우, 여러 기술 혈소판 수, 전체 혈액의 하룻밤 배양, adjus에 따라 기증자의 사전 선택 등의 이용이 가능합니다원심 분리 설정 tment, 또는 7 대신 8 버피 코트의 풀을 활용.
풀링의 제한으로 인해 현재 사용할 수 있고 원심 분리기의 버킷 용량 설정, 버피 코트 수영장의 총 볼륨은 약 600 ML해야합니다. 이 프로토콜에 설명 원심 분리 과정과 설정은 7 버피 코트의 수영장에 대한 차단 매개 변수를 충족하는 제품을 얻을 수 있도록 최적화되었습니다. 수영장에서 버피 코트의 숫자가 수정되는 경우 원심 분리 설정을 수정해야합니다.
일부 국가에서는 최소 혈소판 복용은 높은 있으며, QC 요구 사항은 스웨덴에 비해 더 엄격한 수 있습니다. 따라서, 우리의 결과는 보편적 적용되지 않을 수 있습니다. 이러한 국가에서는 사전에 차단 치료에 두 번 복용 PC는 가로 채서 처리 및 분할 후 지역의 요구 사항을 충족하기 위해 혈소판의 큰 숫자를 포함해야합니다. 때문에 최대 혈소판 콘텐츠 및 치료 볼륨 구경R 도청는 각각 7x10 11 혈소판과 420 ML이며, 차단 처리 요구 사항을 초과 또는 두 치료 복용으로 분할 할 충분한 혈소판 콘텐츠를 단위의 비율은, 이러한 혈소판 복용, QC 기준에 대한 로컬 요구 사항 등의 요소에 따라 달라집니다 버피 코트 최적화 결과, 생산의 안정성.
더블 선량 PC는 차단 처리 요구 사항을 초과하는 경우에는 수동으로 요구 사항을 충족하도록 조정하고 이후 처리 될 수 있습니다. 7 버피 코트 수영장이 차단 후 두 번 복용 제품에 부족한 혈소판을 산출에 몇 차례에서, 우리는 도청 치료를 수행 할 수 없습니다 선출한다. 또는 다른 혈액 센터는이를 통해 모든 단위에 병원체 불 활성화를 수행, 단일 선량 차단 처리 세트 (대형 볼륨 세트를 IE)로 PC를 취급하고 하나의 큰 치료 용량으로 PC를 저장하도록 선택할 수 있습니다. 우리가 만날 수 있도록 우리QC 요구하고 병원체 가능한 한 우리의 혈소판 단위의 많은, 우리가 풀링 할 때, 수영장에서 5.6x10 11 혈소판의 최소 혈소판 내용에 발생합니다, 기증자 혈소판 수치에 따라 버피 코트를 선택 비활성화. 이 도청 치료 후이 치료 용량을 생산하기에 충분한 혈소판 내용을 보장합니다.
Google의 확인은 7 전체 혈액 파생 된 버피 코트 단위가 성공적으로 풀링 및 혈소판에 대한 차단 프로세스를 처리, 제조 (스웨덴어 요구 사항과 유럽 지침) 및 환자 지원을위한 허용 기준을 충족 2 병원체 inactivated 혈소판 제품에 발생 될 수 있다는 설명 임상 실습 가이드 라인과 스웨덴의 표준 혈소판 주입 방법에 따라 혈소판 수혈을 필요로하는.
공개
이 기사에 생산 및 무료 액세스 Cerus의 후원을받습니다.
감사의 말
출판 기금은 Cerus 사, 가로 채기 피 시스템 제조업체가 제공됩니다.
자료
| Name | Company | Catalog Number | Comments |
| Whole blood donation, primary separation, and platelet production | |||
| Blood collection pack | Fenwal | R6485 | Top/Bottom set |
| Automated component extractor | Fenwal | Optipress-II | |
| Blood mixer and balance system | Baxter | Easymix V3 | |
| Platelet leukocyte filtration set | Fenwal | K4R7042 | |
| Centrifuge | Hettich | Roto Silenta 63 RS | Version 5.5 |
| Platelet additive solution - SSP+ | MacoPharma | SSP2030U | 300 ml |
| Sterile tubing welder | Terumo | T-SCD | |
| INTERCEPT treatment & storage | |||
| INTERCEPT processing set |  Cerus Cerus | INT2503 | Dual Storage (DS) set |
| INTERCEPT Illuminator |  Cerus Cerus | INT100 | |
| PC sample pack | Fenwal | FTX 1122 | |
| Incubator | Helmer | PC2200/PC3200 | |
| Agitator | Helmer | PF48H/PF96H | |
| Evaluation of in vitro Platelet Function | |||
| Blood gas analyzer | Radiometer | ABL 735 | Used for pH, blood gases, and lactate measurement |
| Chemistry system | Ortho Clinical Diagnostic | Vitros 5.1 | Used for glucose measurement |
| Hematology analyzer | Boule Medical AB | Medonic CA620-Cellguard | Used for platelet count measurement |
| Flow cytometer | BD | FACSCanto | Used for white blood cell measurement |
참고문헌
- . . Guide to the preparation, use and quality assurance of blood components. , (2010).
- Van Rhenen, D. J., Vermeij, J., Mayaudon, V., et al. Functional characteristics of S-59 photochemically treated platelet concentrates derived from buffy coats. Vox Sang. 79, 206-214 (2000).
- Wollowitz, S. Targeting DNA and RNA in pathogens: mode of action of amotosalen HCl. Transfus. Med. Rev. 31, 11-16 (2004).
- Irsch, J., Lin, L. Pathogen Inactivation of Platelet and Plasma Blood Components for Transfusion Using the INTERCEPT Blood SystemTM. Transfus. Med. Hemother. 38, (2011).
- Lin, L., Dikeman, R., Molini, B., et al. Photochemical treatment of platelet concentrates with amotosalen and long-wavelength ultraviolet light inactivates a broad spectrum of pathogenic bacteria. Transfusion. 44, 1496-1504 (2004).
- Lin, L., Hanson, C., Alter, H., et al. Inactivation of viruses in platelet concentrates by photochemical treatment with amotosalen and long-wavelength ultraviolet light. Transfusion. 45, 580-590 (2005).
- Allain, J. P., Cianco, C., Blajchman, A., et al. Protecting the blood supply from emerging pathogens: the role of pathogen inactivation. Transfus. Med. Rev. 19, 110-126 (2005).
- Stramer, S., Hollinger, F., Katz, L., et al. Emerging infectious disease agents and their potential threat to transfusion safety. Transfusion. 49, 1S-29S (2009).
- Nussbaumer, W., Allesdorfer, D., Grabmer, C., et al. Prevention of transfusion of platelet components contaminated with low levels of bacteria: a comparison of bacteria culture and pathogen inactivation methods. Transfusion. 47, 1125-1133 (2007).
- Schlenke, P. Protection against Transfusion-Associated Graft-versus-Host Disease in Blood transfusion: Is Gamma-Irradiation the Only Answer? Transfus. Med. Hemother. 31, 24-31 (2004).
- Lin, L., Corash, L., Osselear, J. C. Protection Against TA-GVHD Due to Platelet Transfusion By Using Pathogen Inactivation with the INTERCEPT Blood SystemTM - Gamma Irradiation is Not the Only Answer. Haematologica. 95 (Extra 1), 230-237 (2010).
- Corash, L., Lin, L. Novel processes for inactivation of leukocytes to prevent transfusion-associated graft-verus-host disease. Bone Marrow Transplant. 33, 1-7 (2004).
재인쇄 및 허가
JoVE'article의 텍스트 или 그림을 다시 사용하시려면 허가 살펴보기
허가 살펴보기더 많은 기사 탐색
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. 판권 소유