JoVE 비디오를 활용하시려면 도서관을 통한 기관 구독이 필요합니다. 전체 비디오를 보시려면 로그인하거나 무료 트라이얼을 시작하세요.
Method Article
트라이 전단지 폴리머 밸브의 상대 유체 역학 평가를위한 프로토콜
요약
폴리머 밸브 개발에 관심이 갱신되었습니다. 여기서 목적은 트라이 전단지 형상을 수용하고 가까운 동일한 조건에서 수집 된 네이티브 및 인공 밸브 데이터에 비해 폴리머 밸브 유체 역학적 데이터를 제시하는 프로토콜을 정의하는 상업 펄스 복제기를 수정의 타당성을 입증하는 것입니다.
초록
현재 인공 밸브, 이종 이식, 그리고 homografts의 한계 트라이 전단지 폴리머 밸브 보철물의 지역 발전의 최근 부활을하라는 메시지가있다. 그러나 폴리머 밸브 유체 역학적 기능의 초기 평가를위한 프로토콜의 식별은 디자인 프로세스의 초기 단계에서 가장 중요합니다. 체외 펄스 복제기 시스템의 전통이 유연 트라이 전단지 자료를 수용하도록 구성되지 않은,뿐만 아니라, 폴리머 밸브 기능의 평가는 동일한 시험 조건 하에서 네이티브 및 인공 심장 밸브에 대한 상대 맥락에서 이루어져야 할 필요가 있도록 다른에서 측정의 변화 악기를 피할 수 있습니다. 따라서, 우리는)) 네이티브 (N = 4, 평균 직경, D = 20 ㎜), ⅱ) 이중 전단 기계 (N = 2, D = 23 ㎜)와 III를 전의 유체 역학적 평가를 실시 폴리머 밸브 (N = 5, D 시판 펄스 복제기 시스템의 사용을 통해 = 22 ㎜) (ViVitro 연구소INC, 빅토리아, BC은)는이 세 배 전단 밸브 형상을 수용 할 수 있도록 수정되었습니다. 플로리다 대학에서 개발 된 트라이 전단지 실리콘 밸브는 폴리머 밸브 그룹을 구성. 물 35:65 글리세린의 비율 혼합물은 혈액 물리적 특성을 모방하는 데 사용되었다. 압력이 심실과 대동맥 위치에 기록하는 동안 순간 유량은 좌심실과 대동맥 단위의 인터페이스를 측정 하였다. 양방향 전단지와 문학에서 네이티브 밸브 데이터 흐름 및 압력 측정 값의 유효성을 검사하는 데 사용되었다. 다음과 같은 유체의 측정이보고되었다 : 앞으로 유동 압력 강하, 대동맥 사각형 앞으로 유량, 대동맥 폐쇄, 누설 및 역류 볼륨 transaortic 폐쇄, 누출, 총 에너지 손실을 의미합니다. 대표 결과는 세 개의 밸브 그룹의 유체 측정이 성공적으로 시판 펄스 복제기 시스템과 subsequentl에 맞춤식 어셈블리를 통합하여 얻을 수있는 표시Y 객관적으로 폴리머 밸브 설계의 기능적 측면에 대한 통찰력을 제공하기 위해 비교했다.
서문
심장 판막 질환은 흔히 퇴행성 판막 석회화 1, 류마티스 열이, 심내막염 3,4 또는 선천성 기형아 출산의 결과. 밸브의 손상이 협착 및 / 또는 역류 밸브 탈출증 및 수술 복구 할 수없는 원인이 발생하면, 기본 밸브는 일반적으로 인공 밸브로 대체됩니다. 현재 사용 가능한 옵션은 기계적 밸브 (케이지 볼 밸브, 틸팅 디스크 밸브, 등.), 동종 및 bioprosthetic 밸브 (돼지와 소 밸브를) 이용하실 수 있습니다. 기계적 밸브는 종종 자신의 내구성에 따라 젊은 환자에 권장되지만 환자는 혈전 합병증에게 5을 방지하기 위해 항응고제 치료에 남아 있어야합니다. 동종 및 생물 학적 인공 밸브는 혈액 희석제 치료를 피하기 위해 효과적인 선택했습니다, 그러나, 이러한 밸브는 섬유증에 대한 높은 위험, 석회화 변성 및 밸브 고장 6로 이어지는 면역 합병증이. 조직 공학 밸브는 새로운 기술 7-9로 조사하지만 아직도 많은 작업이 남아 발견 할 유지되고있다. 대안 내구성, 생체 적합성, 보철 밸브는 심장 판막 질환 환자의 삶의 질을 개선하기 위해 필요합니다. 다시 말하지만,이 밸브 설계는 심장 판막 질환 10을 선택한 환자의 치료를 변형의 가능성을 보여주는 경피적 접근법으로, 경피적 밸브 기술에 사용되는 판막을 대체 할 수 있습니다.
현재 표준에 의해 명시된 성공적인 심장 밸브 교체는 다음과 같은 성능 특성이 있어야합니다 "1) 수용 가능한 작은 평균 압력 차이 드롭 흐름을 기대 할 수 있습니다 2) 수용 가능한 작은 역류와 역류 방지 3) 색전술을 저항; 4) 저항 용혈, 5) 혈전 형성을 저항, 6) 생체 적합성, 7) 생체 진단 기술의 호환이다 8) 타겟 결과물 및 이식입니다인구, 10) 허용 소음 수준이; 9) 번 위치 고정이 남아있다 11) 재생 기능을 가지고, 12), 합리적인 평생의 기능을 유지 자사의 제네릭 클래스와 일치, 13) 합리적인 선반을위한 그것의 기능과 불임을 유지 이전의 이식에 생명. "11. 기존 밸브 보철물의 단점 중 일부는 잠재적 폴리머 밸브에 의해 극복 될 수있다. 생체 적합성 고분자 biostability, 반대로 가수 분해, 산화 방지와 같은 유리한 기계적 특성에 따라 최고의 후보로 간주되어 , 높은 강도와 탄성이. 특히, 탄성 중합체는 탄성 중합체는 부드러운 조직의 특성을 모방 조정할 수 있습니다. 기본 밸브 역학을 닮은 재료의 변형을 제공 할 수 있습니다, 그들은 바이오 관대하고 그 결합을 견딜 수있는 사용할 수있는 유일한 인공 재료가 될 수있다 생체 내에서 유체 유발, 휨 및 인장 응력, 아직, 건강 유사한 방식으로 이동기본 밸브의 움직임. 또한, 엘라스토머는 대량 생산 쉽게 저장 크기의 다양한 비용 효과적인 장치가 될 것으로 예상된다 구조적 섬유 보강 보강 할 수있다 할 수 있습니다.
트라이 전단지 밸브를 조립 고분자 재료의 사용의 개념은 새로운 것이 아니다 제한된 밸브 내구성으로 인해 주로 포기 된 지난 50 년 12 일 동안 여러 연구 조사의 대상이되고있다. 그러나 새로운 제조 방법 13,14의 도래와 함께, 고분자 재료 15,16 및 경피적 밸브 기술과 폴리머 밸브 대체의 가능성이 원활한 통합의 강화는 최근 잠재적으로 폴리머 밸브 개발에 새롭게 관심과 활동이있다 현재 상용 밸브 대안. 이 관점에서, 유체 기능을 평가하기 위해 이러한 밸브의 테스트를 가능하게하는 프로토콜은 첫 번째 단계입니다평가 과정에서, 아직 상업적으로 이용 가능한 펄스 시뮬레이터 시스템은 일반적으로 트라이 전단지 밸브 디자인을 수용 할 수 있도록되어 와서 시중 심장 판막 (예를 들어, 틸팅 디스크, 양방향 전단지 기계 심장 판막)를 삽입하는 고리 모양의 간격을 포함하지 않습니다. 둘째, 폴리머 밸브는 그의 유체 역학 만 상대 맥락에서 평가 될 수있는 새로운 기술입니다. 기본 심장 밸브의 압력 및 유량 데이터를 사용할 수 있더라도, 그것은에 대한 계정 않도록 폴리머 밸브를 평가하는 데 사용되는 것과 같은 맥박 시뮬레이터를 사용하여, 인간의 밸브 생물학적으로 유사하다 네이티브 대동맥 돼지 밸브의 테스트를 수행하는 것이 중요합니다 시스템에 따라있을 수 있습니다 측정의 차이. 따라서, 본 연구의 목적은 상업적으로 이용 가능한 펄스 시뮬레이터 트라이 전단지 밸브 구조를 수용하고 체계적으로 상대 연속 중합체 밸브 유체 역학적 지표를 평가하는 어셈블리를 장착 할 수있는 방법을 설명했다내선 기계 및 원시 돼지 심장 밸브 대응 비교합니다. 우리의 경우, 새로운 트라이 전단지 실리콘 폴리머 밸브는 이전 폴리머 밸브 그룹을 구성 플로리다 13 대학에서 개발.
프로토콜
1. 준비하기
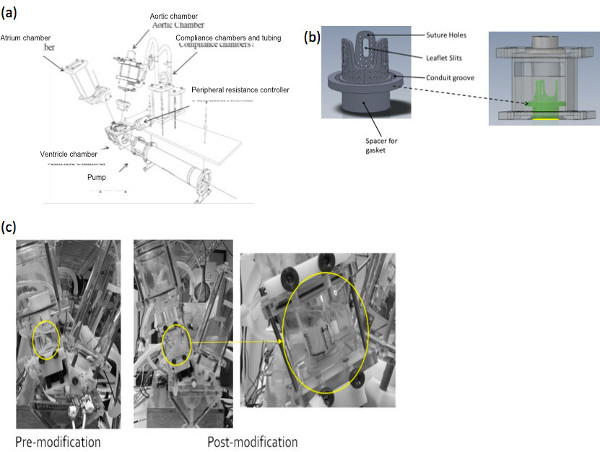
- 디자인과 트라이 전단지 밸브 형상을 수용하기 위해 어셈블리를 제조. 이 최소한 밸브 전단지 봉합 -에 밸브 홀더 및 펄스 복제기 시스템에 어셈블리를 고정하는 밸브 홀더 및 주변 액세서리를 수용 할 수있는 튜브를 포함합니다. 우리의 경우, 우리는 ViVitro 연구소 주식 회사 (빅토리아, BC)에서 사용할 수있는 상업적으로 이용 가능한 펄스 복제기 시스템을 활용. 밸브 홀더 디자인뿐만 아니라 사전 및 사후 조립 구성은 그림 1에 묘사되어 있습니다.
- 전체 루프는 이전의 사용으로 끝났다해야합니다. 이 두 단계를 포함한다 : ⅰ) 사용하기 전에 모든 분해 튜브 교체 및 II) 루프에 연결된 장비의 교정, 즉 펌프가 사용중인 흐름 조사 등의 비누 용액과 물을 사용하여 전체 루프 시스템을 클렌징하고, 압력 트랜스 듀서 (일반적으로 심방, 대동맥과 심실 위치에서 측정). 교정 초기화 할 수 있습니다ially 1 % 생리 식염수를 사용하여 수행 할 수 및 이전의 혈액 아날로그 글리세린 용액을 사용하여 반복해야합니다.
2. 네이티브 대동맥 밸브 해부
- USDA 승인 학살 하우스 (기관 애니멀 케어 및 사용위원회 (IACUC)의 승인이 필요할 수 있음)에서 그대로 대동맥으로 4 신선한 돼지의 마음을 얻을 수 있습니다. 우리의 경우, 우리의 해부 프로토콜은 플로리다 국제 대학교 (: 11-020 프로토콜 승인 번호)에서 IACUC에 의해 승인되었습니다. 탈 이온수로 마음을 씻어 유체 역학 시험 기관에 얼음에 식염수 (PBS) 용액 및 전송 버퍼 1 % 항생제 / 항진균 및 멸균 인산으로 채워진 용기에 넣습니다.
- 해부 냄비에 마음을 놓고 조심 심낭을 제거합니다. 복부 쪽을 향 그런 마음을 놓습니다. 육안 검사와 심장의 네 개의 챔버를 식별하고 그대로 대동맥에 대동맥 궁을 찾습니다.
- TW에 마음을 분리O를 고리를 아래에서 약 825에서 수평으로 가로 질러 절단하여 반으로, 대동맥과 좌심실 사이의 접합 즉. 조심스럽게 여전히 심실 조직 세그먼트에 연결된 그대로 대동맥을 분리.
- 손상 또는 석회화의 흔적이 없다는 것을 보장 대동맥, 대동맥 및 하부 원주 사이의 지역에있는 대동맥 밸브를 검사합니다.
- 환형 위에서 ~ 1시 대동맥을 분리하고 대동맥 밸브 (그림 2A)를 분리하는 환형 아래 왼쪽 심실 조직의 세그먼트를 구분합니다.
3. 고분자 및 기본 밸브 봉합 과정
- 각 밸브의 기본이 게시물 홀더의 기본과 정렬되도록 밸브 홀더 내부의 심장 밸브를 놓습니다. 종이 클립 일시적으로 각 게시물에 장소에 밸브를 확보하지만, commissures 또는 교두가 손상되지 않도록주의하십시오.
- 의 봉합을 삽입바늘. 외부에서 바늘이 쉽게 바닥에서 가져온 될 수 있다는 내부 등으로, 첫 번째 구멍을 통해 바늘을 통과하여 밸브 홀더의 하단에 봉합 시작합니다. 루프 방식으로, 수직 밸브 홀더의 게시물쪽으로 밸브를 봉합 시작합니다.
- 홀더 및 홀더 게시물의 끝의 주위에 추가 봉합사 보안의 원주를 따라 봉합 (그림 2B)와 함께 진행. 밸브가 완전히 3 게시물과 밸브 홀더 (그림 2D 및 2E)의 둘레에 봉합사를 사용하여 보호 할 때 종이 클립 (그림 2C)를 제거 할 수 있습니다.
4. 유체 역학적 평가
참고 : 실제 프로토콜을 사용하는 특정 펄스 복제기 시스템에 따라 달라집니다. 여기에 포함 된 모든 정보는 ViVitro 펄스 복제기 병 Sysytem을 (ViVitro 연구소, 주식 회사, 밴쿠버, BC)를 사용 caontained.
- 이중 전단 VALVE
- 70 비트 / 분에 펄스 복제기 시스템의 심장 박동을 설정합니다.
- 펌프 (ViVitro 시스템의 경우 S35 파형이 모든 유체 역학적 시험을 위해 선택되었다) 운전 유량 파형을 선택합니다. 우리의 실험에서 이용 된 특정 파형이 임 하였다. (2001) 17에 의해 설명된다.
- 앰프와 피스톤 펌프를 켭니다. 15 분 동안 워밍업.
- 대동맥 위치에 장소는 양방향 전단 밸브 (그림 2F).
- 누수가 발생할 수있는 장치의 접속점에 얼룩 진공 그리스.
- 심방 구획 글리세린 / 식염수 액을 붓는다. 35 % / 0.7 L 글리세린과 생리 식염수 65 % / 1.3 L를 : 타악기 복제기 시스템과 액체의 2 L에서 실행합니다. 생리 식염수는 9의 농도로 증류수에 잘 용해 일반 소금을 사용하여 준비가되어 밀리그램 / ML (중량 / 부피).
- 대동맥 위치에 배치 된 유량 센서의 전원을 켭니다.
- 일을 보정전자 펌프.
- 압력 트랜스 듀서 뒤에 유량 센서 교정을 진행합니다. 마찬가지로 펌프, 간단하게 보정 탭에서 각각의 유량과 압력 ViVitest 소프트웨어 (ViVitro 연구소 주식 회사)에 의해 주어진 지시 사항을 따르십시오.
- 보정이 완료되면 유체가 대동맥 함을 채울 때까지, 낮은 rpm에서 펌프를 시작합니다. 누출을 확인합니다. 추가 진공 그리스 필요한 경우 사용합니다.
- 두 스톱 콕 (대동맥과 심실 트랜스 듀서) 위치를 열십시오.
- 뇌졸중 볼륨 80 ML / 비트에 도달 할 때까지 펌프의 회전 수를 늘립니다.
- 흐름이 안정 될 때까지 시스템이 10 분 동안 실행할 수 있습니다. 흐름 안정화는 파형이 화면에 표시되는 유량과 압력을 관찰하여 확인할 수 있습니다. 주기 사이의 낮은 없음 변화는 시스템 안정화의 좋은 지표입니다.
- ViVitest 소프트웨어 모드를 취득 선택합니다.
- 10주기를 수집를 클릭합니다.
- 분석 모드, C에서테이블에 핥아하고 파일을 저장합니다. 또한 ViVitest에서 사진 스냅 옵션을 사용하여 파형의 이미지를 저장합니다.
- 네이티브 및 폴리머 밸브
- 3.1.3 양방향 전단지 밸브 지침에서 - 폴리머 동물 밸브, 동일한 단계 3.1.1를 따르십시오.
- 사용자 정의 만든 어셈블리에서 유리관 내부 봉합 밸브 밸브 홀더를 놓습니다. 상단과 하단 조각 및 측면 나사와 너트의 장소에 안전 샌드위치 튜브를.
- 대동맥 챔버와 원래의 대동맥 밸브 홀더 사이에 조립.
- 3.1.16 이중 전단 밸브 지침에서 - 단계 3.1.5을 계속합니다.
5. 후 처리
- 유량 및 압력 파형
- 평균 파형 수집, 즉 대동맥 압력 (AP), 심실 압력 (VP) 및 유량 (Q) 각각에 대해 수집 된 데이터.
- 밸브의 각 그룹 (고분자, 돼지 n에ative 대동맥 밸브와 이중 전단지), 해당 AP, VP 및 Q 대 같은 플롯 시간의 관계를 플롯.
- AP를 들어, 표준, 기본 대동맥 밸브 (18) 및 검증을 위해 문헌 양방향 전단지 인공 밸브 (19) 플롯을 중첩.
- 유체 측정
- 각 시험 밸브의 경우, 다음과 같은 유체 메트릭이 계산되어야한다) 앞으로 유동 압력 강하 및 최대 transvalvular 압력 (TVP), B)를 대동맥 대동맥 앞으로 흐름, 결산, 누설 광장 (RMS) 앞으로 유량, C)를 의미 총 역류 볼륨 D) 밸브 끝 오리피스 면적 (EOA), E) transaortic 앞으로 흐름, 마감, 누수 및 총 에너지 손실.
- 앞으로 유동 압력 강하 TVP 측정 값에서 계산되고, 3 시간 간격, P로 분류 될 수있다 : 앞으로 흐름과 H와 간격 : 간격 0 TVP로 시작하고 0 플로우로 끝나는 0 TVP, F로 시작하고 끝 간격입니다. 최대 TVP는 엄마입니다ximum 압력 구배는 대동맥과 심실 압력 수치에서 밸브를 통한 기록했다.
- RMS 앞으로 유량 (Q RMS)는 다음과 같이 순방향 유량의 크기를 정량화하기위한 유용한 통계를 제공합니다 :

'n'은 시점의 총 수입니다 순서대로 '나'를 수집 순간 유량 측정은 'Q 나는 수집. - 앞으로 대동맥, 폐쇄 및 누설 볼륨은 앞으로 다음 시간 간격에 따라 계산됩니다 : 앞으로 흐름 (T 1)의 끝 부분에 밸브 (T O)를 통해 앞으로 흐름의 시작, 마감 : T 1에서 인스턴스까지 밸브 폐쇄 (T 2)의, 누설 전류 : t 2의 심장주기 (T 3)의 끝까지. 총 역류 볼륨은 단순히 클의 합이다ING 누출 볼륨.
- 혈액 속성에 따라 EOA는 20로이 기간 동안 매년 평균 TVP에서 3 간격, P, F와 H에 대해 계산 될 수있다 :
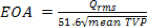
- 에너지 손실은 다음 21로 정의된다 :
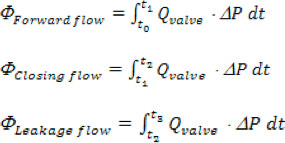
- 각 시험 밸브의 경우, 다음과 같은 유체 메트릭이 계산되어야한다) 앞으로 유동 압력 강하 및 최대 transvalvular 압력 (TVP), B)를 대동맥 대동맥 앞으로 흐름, 결산, 누설 광장 (RMS) 앞으로 유량, C)를 의미 총 역류 볼륨 D) 밸브 끝 오리피스 면적 (EOA), E) transaortic 앞으로 흐름, 마감, 누수 및 총 에너지 손실.
결과
대표 유량 및 압력 파형은 그림 3, 4와 5에 표시됩니다. 플롯 된 각 그룹에 대해 시험 밸브의 샘플 크기에 평균했다, n은 각각 = 5, 4, 폴리머, 원시 돼지와 양 전단 그룹 밸브 2. 평균 유체 측정 및 이러한 샘플 크기에 대한 평균의 표준 오차는 표 1에 제시되어있다.
?...
토론
본 연구에서는 고분자 고유의 돼지 밸브의 유체 테스트를 수행 할 수 있도록 트라이 전단지 밸브 형상을 수용하기 위해 상업적으로 이용 가능한 박동 복제기 장치를 수정하는 유틸리티를 증명하고있다. 특히 우리의 경우, 시스템 수정은 ViVitro 왼쪽의 마음과 ViViTest 데이터 수집 시스템 (ViVitro 시스템, Inc의 빅토리아, BC, 캐나다)를 통해 제어 전신 시뮬레이터 시스템 (그림 1a)이었다. 그...
공개
저자는 공개 아무것도 없어.
감사의 말
플로리다 대학에서 종자 부여 - 대학 의학은 기꺼이 인정 받고 있습니다. NIH / NIGMS R25 GM061347 : 과학 강화 (MBR에-RISE) 교제에 대한 연구 이니셔티브 - 졸업 연구 (마누엘 설리) 생물 의학 연구 프로그램의 소수 기회를 통해 지원되었다. 플로리다 국제 대학의를 통해 월러스 헤 보습 바로 앞에 달린 풀 베는 재단의 재정 지원은 생명 공학과도 기꺼이 인정 받고 있습니다. 카마 우 부두, 말라기 Suttle, 켄달 암스트롱 아브라함 알폰소 : 마지막으로, 저자는 실험 과정의 여러 단계에서 자신의 도움에 대해 다음과 같은 학생들에게 감사드립니다.
자료
| Name | Company | Catalog Number | Comments |
| Pump | ViVitro Labs | http://vivitrolabs.com/products/superpump/ | |
| Flow Meter and Probe | Carolina Medical | Model 501D | http://www.carolinamedicalelectronics.com/documents/FM501.pdf |
| Pressure Transducer | ViVitro Labs | HCM018 | |
| ViVitro Pressure Measuring Assembly | ViVitro Labs | 6186 | |
| Valve holder | WB Engineering | Designed by Florida International University. Manufactured by WB Engineering | |
| Pulse Duplicator | ViVitro Labs | PD2010 | http://vivitrolabs.com/wp-content/uploads/Pulse-Duplicator-Accessories1.pdf |
| Pulse Duplicator Data Acquisition and Control System, including ViViTest Software | ViVitro Labs | PDA2010 | http://vivitrolabs.com/products/software-daq |
| Porcine Hearts and Native Aortic Valves | Mary's Ranch Inc | ||
| Bi-leaflet Mechanical Valves | Saint Jude Medical | http://www.sjm.com/ | |
| High Vacuum Grease | Dow Corning Corporation | http://www1.dowcorning.com/DataFiles/090007b281afed0e.pdf | |
| Glycerin | McMaster-Carr | 3190K293 | 99% Natural 5 gal |
| Phosphate Buffered Saline (PBS) | Fisher Scientific | MT21031CV | 100 ml/heart |
| Antimycotic/Antibiotic Solution | Fisher Scientific | SV3007901 | 1 ml in 100 ml of PBS/heart; 20 ml for ViVitro System |
| NaCl | Sigma-Aldrich | S3014-500G | 9 g/L of deionized water |
| Deionized Water | EMD Millipore Chemicals | Millipore Deionized Purification System. 1.3 L for ViVitro System, 200 ml for heart valve dissection process |
참고문헌
- Rajamannan, N. M., et al. Calcific aortic valve disease: not simply a degenerative process: A review and agenda for research from the National Heart and Lung and Blood Institute Aortic Stenosis Working Group. Executive summary: Calcific aortic valve disease-2011 update. Circulation. 124, 1783-1791 (2011).
- Marijon, E., Mirabel, M., Celermajer, D. S., Jouven, X. Rheumatic heart disease. Lancet. 379, 953-964 (2012).
- Karaci, A. R., et al. Surgical treatment of infective valve endocarditis in children with congenital heart disease. J. Card. Surg. 27, 93-98 (2012).
- Knirsch, W., Nadal, D. Infective endocarditis in congenital heart disease. Eur. J. Pediatr. 170, 1111-1127 (2011).
- Korossis, S. A., Fisher, J., Ingham, E. Cardiac valve replacement: a bioengineering approach. Biomed. Mater. Eng. 10, 83-124 (2000).
- Ghanbari, H., et al. Polymeric heart valves: new materials, emerging hopes. Trends Biotechnol. 27, 359-367 (2009).
- Mol, A., Smits, A. I., Bouten, C. V., Baaijens, F. P. Tissue engineering of heart valves: advances and current challenges. Expert Rev. Med. Devices. 6, 259-275 (2009).
- Ramaswamy, S., et al. The role of organ level conditioning on the promotion of engineered heart valve tissue development in using mesenchymal stem cells. Biomaterials. 31, 1114-1125 (2010).
- Sacks, M. S., Schoen, F. J., Mayer, J. E. Bioengineering challenges for heart valve tissue engineering. Annu. Rev. Biomed. Eng. 11, 289-313 (2009).
- Zamorano, J. L., et al. EAE/ASE recommendations for the use of echocardiography in new transcatheter interventions for valvular heart disease. J. Am. Soc. Echocardiogr. 24, 937-965 (2011).
- ANSI/AAMI/ISO. Cardiovascular Implants - Cardiac Valve Prostheses. Assoc. Adv. Med. Instrum. 71, (2005).
- Gallocher, S. L. . Durability Assessment of Polymer Trileaflet Heart Valves PhD thesis. , 313 (2007).
- Carroll, R., Boggs, T., Yamaguchi, H., Al-Mously, F., DeGroff, C., Tran-Son-Tay, R. Blood Cell Adhesion on Polymeric Heart Valves. , (2012).
- Pierre, K. K., Salinas, M., Carroll, R., Landaburo, K., Yamaguchi, H., DeGroff, C., Al-Mousily, F., Bleiweis, M., Ramaswamy, S. Hydrodynamic Evaluation of a Novel Tri-Leaflet Silicone Heart Valve Prosthesis. , (2012).
- Cacciola, G., Peters, G. W., Schreurs, P. J. A three-dimensional mechanical analysis of a stentless fibre-reinforced aortic valve prosthesis. J. Biomech. 33, 521-530 (2000).
- De Hart, J., Cacciola, G., Schreurs, P. J., Peters, G. W. A three-dimensional analysis of a fibre-reinforced aortic valve prosthesis. J. Biomech. 31, 629-638 (1998).
- Lim, W. L., Chew, Y. T., Chew, T. C., Low, H. T. Pulsatile flow studies of a porcine bioprosthetic aortic valve in vitro: PIV measurements and shear-induced blood damage. J. Biomech. 34, 1417-1427 (2001).
- Gutierrez, C., Blanchard, D. G. Diastolic heart failure: challenges of diagnosis and treatment. Am. Fam. Physician. 69, 2609-2616 (2004).
- Shi, Y., Yeo, T. J., Zhao, Y., Hwang, N. H. Particle image velocimetry study of pulsatile flow in bi-leaflet mechanical heart valves with image compensation method. J. Biol. Phys. 32, 531-551 (2006).
- Chandran, K. B., Yoganathan, A. P., Rittgers, S. E. . Biofluid Mechanics: The Human Circulation. , 277-314 (2007).
- Akins, C. W., Travis, B., Yoganathan, A. P. Energy loss for evaluating heart valve performance. J. Thorac. Cardiovasc. Surg. 136, 820-833 (2008).
- Fung, Y. C. . Biomechanics: Circulation. , (1997).
- Keener, J., Sneyd, J. . Mathematical Physiology, II: Systems Physiology. , (1998).
- Quick, C. M., Berger, D. S., Noordergraaf, A. Apparent arterial compliance. Am. J. Physiol. 274, H1393-H1403 (1998).
- Wang, Q., Jaramillo, F., Kato, Y., Pinchuk, L., Schoephoerster, R. T. Hydrodynamic Evaluation of a Minimally Invasive Heart Valve in an Isolated Aortic Root Using a Modified In Vitro Model. J. Med. Devices. 3, 011002.1-011002.6 (2009).
- Baldwin, J. T., Campbell, A., Luck, C., Ogilvie, W., Sauter, J. Fluid dynamics of the CarboMedics kinetic bileaflet prosthetic heart valve. Eur. J. Cardiothorac. Surg. 11, 287-292 (1997).
재인쇄 및 허가
JoVE'article의 텍스트 или 그림을 다시 사용하시려면 허가 살펴보기
허가 살펴보기더 많은 기사 탐색
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. 판권 소유