Для просмотра этого контента требуется подписка на Jove Войдите в систему или начните бесплатную пробную версию.
Method Article
Протокол Относительная оценка гидродинамических трехстворчатый клапан полимеров
В этой статье
Резюме
Там был возобновлен интерес к разработке полимера клапанов. Здесь целью является продемонстрировать возможность изменения коммерческих копировальных импульсом для размещения трехстворчатый геометрии и определить протокол представить полимера данных гидродинамического клапана по сравнению с отечественными и протезов клапанов данные, собранные в условиях близких к идентичных условиях.
Аннотация
Ограничения в настоящее время протезов клапанов, ксенотрансплантаты и гомотрансплантатов вызвали недавнее возрождение событиях в области трехстворчатый клапан полимера протезов. Тем не менее, идентификация протокола для первоначальной оценки функциональных полимеров гидродинамического клапана имеет первостепенное значение на ранних этапах процесса проектирования. Традиционные в пробирке импульсных систем дубликатор не настроены для размещения гибких трехстворчатый материалы, кроме того, оценка функциональности клапана полимера должно быть сделано в относительном контексте отечественной и протезов клапанов сердца при одинаковых условиях испытаний, так что изменчивость в разных измерениях инструментов можно избежать. Соответственно, мы провели оценку гидродинамических I) родной (N = 4, средний диаметр, D = 20 мм), II) би-листовку механический (N = 2, D = 23 мм) и III) полимера клапанов (N = 5, D = 22 мм) через использование коммерчески доступных системе копировальный импульса (ViVitro LabsInc, Виктория, Британская Колумбия), которая была модифицирована для трехстворчатый клапан геометрии. Трехстворчатый клапан силиконовый разработанная в Университете Флориды составили группу полимеров клапана. Смеси в соотношении от 35:65 до глицерин вода использовалась для имитации крови физические свойства. Мгновенный расход был измерен на границе левого желудочка и аорты единиц в то время как давление было записано в желудочка и аорты позиций. Би-листовки и родных данные клапана из литературы был использован для проверки потока и давления. Следующие показатели гидродинамического сообщалось: прямое падение давления потока, аортальный среднеквадратичной вперед расхода, закрытие аортального, утечки и объем регургитации, трансаортальный закрытия, утечки, и общие потери энергии. Представитель Результаты показали, что гидродинамические метрик из трех групп клапана может быть успешно получены путем включения заказ сборки в коммерчески доступных импульсная система дубликатор и subsequentlу, по сравнению с объективно дать представление о функциональных аспектах дизайна полимера клапана.
Введение
Заболевания клапанов сердца чаще возникает в результате дегенеративных кальцификации клапана 1, ревматизм 2, эндокардит 3,4 или врожденными дефектами. Когда клапан ущерб, вызывая стеноз и / или пролапс клапана регургитация и не могут быть устранены хирургическим путем, родной клапан обычно заменяется искусственный клапан. В настоящее время доступны варианты включают механические клапаны (клетки-шаровые краны, клапаны наклона диска и т.д.)., Гомографт и биопротезных клапаны (свиной и бычий клапанов). Механические клапаны часто рекомендуются для молодых пациентов на основе их прочность, однако пациент должен оставаться на антикоагулянтной терапии для предотвращения тромботических осложнений 5. Гомографт и биологические протезы клапанов были эффективные выборы, чтобы избежать крови, тоньше, терапии, однако эти клапаны имеют повышенный риск фиброза, кальцификации, дегенерация и иммуногенных осложнений, ведущих к отказу крана 6. Тканевой инженерии клапаны находятся под следствием в качестве новой технологии 7-9, но многое еще предстоит раскрыться. Альтернативные прочный, биосовместимые, искусственные клапаны, необходимые для улучшения качества жизни пациентов с заболеваниями сердца клапанов сердца. Опять же, эта конструкция клапана может заменить биопротеза используется в технологии транскатетерных клапана, с транскатетерных подходов показывает потенциал для преобразования обработка отдельных пациентов с сердечной болезнью клапана 10.
Как заявил действующими стандартами, успешную замену сердечного клапана должна иметь следующие характеристики: "1) позволяет прямого потока с приемлемо малой среднее снижение перепада давления, 2) предотвращает обратный поток с приемлемо малой срыгивания, 3) сопротивляется эмболизации, 4) сопротивляется гемолиз, 5) противостоит образование тромба, 6) является биосовместимым, 7) совместим с в естественных условиях диагностических методов; 8) доставке и имплантируемые в целевойнаселения; 9) остается неизменным после размещения; 10) имеет приемлемый уровень шума; 11) имеет воспроизводимую функцию; 12) сохраняет свою функциональность за разумную жизнь, в соответствии со своим универсальным классом; 13) сохраняет свою функциональность и стерильности для разумного полку жизни до имплантации ". 11. Некоторые недостатки существующих протезов клапанов потенциально могут быть преодолены с помощью клапана полимера. биосовместимые полимеры были рассмотрены верхний кандидатов на основе биостойкость, анти-гидролиза, антиокислительные, и выгодные механические свойства, такие как высокая прочность и вязкоупругости. В частности, эластомерных полимеров может обеспечить деформацию материала напоминающего родной динамику клапана. эластомеры могут быть приспособлены, чтобы имитировать свойства мягких тканей, и они могут быть только искусственные материалы, которые являются био-терпимыми и которые могут выдержать току, в живом организме, жидкость-индуцированной, изгиб и растягивающих напряжений, тем не менее, двигаться таким образом, напоминающие здоровым,родного движения клапана. Кроме того, эластомеры могут выпускаться серийно в различных размерах, с легкостью хранить, как ожидается, быть экономически эффективными устройствами и могут быть конструктивно дополнены волокнистой арматуры.
Понятие использованием полимерных материалов, чтобы собрать три-листовку клапан не нова и была предметом нескольких исследований исследований в течение последних 50 лет, 12, которые были оставлены в значительной степени из-за ограниченной прочностью клапана. Тем не менее, с появлением новых методик производства 13,14, укрепление полимерных материалов 15,16 и потенциально бесшовной интеграции полимера клапана заменителей транскатетерных технологии клапана, в последнее время отмечается повышенный интерес и активность в развивающихся полимера клапаны как потенциально жизнеспособная альтернатива в настоящее время коммерческие клапанов. В свете этого протокола для включения тестировании этих клапанов для оценки гидродинамической функциональность является первым шагомв процессе оценки, однако коммерчески доступные системы импульса симулятор как правило, не приходят оборудованные для размещения трехстворчатый клапан конструкции и содержат кольцевой расстояние вставить коммерчески доступных клапанов сердца (например, наклона диска, би-листовку механических клапанов сердца). Во-вторых, полимерные клапаны новой технологии гидродинамики которого может быть оценена только в относительном контексте. Даже при том, родной клапан сердца и поток данные доступны, важно проводить тестирование родной аорты свиньи клапаны, которые являются биологически похожи на человеческие клапаны, используя тот же пульсирующий тренажер, который используется для оценки полимера клапана таким образом, чтобы учесть измерение различия, которые могут быть в зависимости от системы. Таким образом, цель данного исследования было продемонстрировать, как коммерчески доступные импульса Тренажер может быть оснащен сборки для размещения трехстворчатый клапан конструкции и систематически оценивать полимера клапана гидродинамической метрик в относительной продолжениедоб по сравнению с механическими и родной свиного коллегами клапан сердца. В нашем случае, роман трехстворчатый клапан силиконовый полимер ранее разработанный в Университете штата Флорида 13 составили группу полимеров клапана.
протокол
1. Подготовка
- Спроектировать и изготовить сборки для размещения трехстворчатый клапан геометрии. Это будет включать в себя как минимум клапана держатель шва в створок клапана и трубки для размещения держателя клапана и окружающих аксессуаров чтобы закрепить в систему дубликатор импульса. В нашем случае, мы использовали коммерчески доступные системы импульса дубликатор можно получить ViVitro Labs Инк (Виктория, Британская Колумбия). Клапан конструкция держателя, а также до и после конфигурации сборки изображены на рисунке 1.
- Весь цикл должны быть загрунтованы до использования. Это включает в себя два этапа: I) очищение всего система обратной связи с использованием мыльного раствора и воды, в том числе замена поврежденной трубы перед использованием и II) калибровка приборов подключены к петле, а именно насос используется, поток зонда, а преобразователи давления (как правило, оцениваются по предсердия, желудочка и аорты местах). Калибровка может инициализацииially быть выполнены с использованием 1% солевом растворе и должна быть повторена перед использованием крови аналоговый раствор глицерина.
2. Родные Вскрытие аортального клапана
- Получить 4 свежих сердца свиньи с аортой нетронутыми от USDA утвержденных бойню (Институциональные уходу и использованию животных комитета (IACUC) утверждение может потребоваться). В нашем случае, наши вскрытия протокол был одобрен IACUC Флоридского международного университета (протокол номер свидетельства: 11-020). Промойте сердца деионизированной водой и поместите его в сосуд, наполненный 1% противогрибковым / стерильных антибиотиков и фосфатным буферным раствором (PBS) и решения на лед к гидродинамической лаборатории тестирования.
- Поместите в сердцах рассекает весов и осторожно удалите перикарда. Расположите сердце так, что брюшная сторона обращена к вам. Осмотрите и определить четыре камеры сердца и найдите дуги аорты на интактной аорты.
- Отделите сердце в TWо половинки путем разрезания через горизонтально примерно 0,75 ниже в кольцевом пространстве, т.е. соединение между аортой и левого желудочка. Тщательно изолировать нетронутыми аорты еще привязаны к левому сегменту ткани желудочка.
- Изучить аортальный клапан, расположенный в корня аорты, область между восходящую часть дуги аорты и нижняя кольцо, гарантируя, что нет никаких повреждений или каких-либо признаков кальцификации.
- Сплит аорты на ~ 1 в выше кольца и отделить левые сегмента ткани желудочка ниже кольца, чтобы изолировать аортального клапана (рис. 2а).
3. Полимеров и собственный процесс наложения швов клапана
- Поместите сердечного клапана внутри клапана держатель таким образом, что основание каждого клапана совпадала с базой сообщение держателя. Закрепите клапан на месте в каждой должности временно с скрепки, но будьте осторожны, чтобы не повредить спайки или острые выступы.
- Вставьте шов виглы. Начать сшивания в нижней части клапана держатель пропусканием игла через первое отверстие, извне внутрь так, что игла может быть легко извлекается из нижней части. В циклически повторяется, начать ушивание клапан вертикально вверх должности клапана держателя.
- Прогресс с наложением швов (рис. 2б) по окружности держателя и безопасную дополнительный шов вокруг кончиков держатель сообщения. Скрепки (фиг. 2в) могут быть удалены, когда клапан полностью защищены с помощью швов на три сообщения и по окружности клапан держатель (фиг. 2d и 2е).
4. Оценка гидродинамических
Примечание: Фактическая протокол будет меняться в зависимости от конкретной системы дубликатор импульсов используется. Вся информация caontained здесь использован импульсный ViVitro Дубликатор Sysytem (ViVitro Labs, Inc, Ванкувер, Британская Колумбия).
- Би-ва листовкиLve
- Установите частоту сердечных сокращений импульса дубликатор системы до 70 уд / мин.
- Выбор потока сигнала для приведения в действие насоса (в случае системы ViVitro S35 сигнала был выбран для всех гидродинамических испытаний). Конкретная форма волны используемых в наших экспериментах проиллюстрировано Lim и соавт. (2001) 17.
- Включите усилитель и поршневого насоса. Прогреться в течение 15 мин.
- Место би-листовку клапана (рис. 2F) в аортальной позиции.
- Мазок вакуумной смазки на всех узлах устройства, на котором может произойти утечка.
- Налейте глицерин / солевой жидкости в предсердии отсека. Следует отметить, что пульсирующий система копировальный аппарат работает на 2 л жидкости с 35% / 0,7 л глицерина и 65% / 1,3 л солевого раствора. Солевой раствор получают с использованием обычной соли и растворяют в деионизированной воде при концентрации 9 мг / мл (масса / объем).
- Включите датчик расхода, который был помещен в аортальной позиции.
- Калибровка йэлектронной насоса.
- Продолжайте калибровку датчика расхода последующим датчиков давления. Как и в насосе, просто следуйте инструкциям ViVitest программное обеспечение (ViVitro Labs Инк) для каждого потока и давления под калибровку вкладку.
- После завершения калибровки, запустить насос на низких оборотах, пока жидкость не заполняет аорты отсека. Убедитесь в отсутствии утечек. Используйте дополнительную смазку вакуума в случае необходимости.
- Поверните два стоп-краны (аортальный и желудочковой преобразователей), чтобы открыть позицию.
- Увеличение числа оборотов насоса, пока объем хода не достигнет 80 мл / бит.
- Позвольте системе работать в течение 10 мин, пока поток не стабилизируется. Поток стабилизация может быть проверена путем наблюдения расхода и давления сигналы отображаются на экране. Слабый до нулевого изменения между циклами является хорошим индикатором системы стабилизации.
- В ViVitest приобрести программное обеспечение выбрать режим.
- Нажмите на сбор 10 циклов.
- Из режим анализа, Cлизать на столе и сохранить файл. Также сохранять изображения из сигналов с помощью фото-SNAP вариант в ViVitest.
- Родные и полимеров клапаны
- Полимеров и животных клапаны, выполните те же шаги 3.1.1 - 3.1.3 от би-листовку инструкции клапана.
- Поместите держатель клапана с зашивается клапан внутри стеклянной трубки от сборки на заказ. Сэндвич трубки с верхней и нижней части и безопасный на месте с боковыми винты и гайки.
- Место сборки между камерой аорты и оригинальный держатель аортального клапана.
- Продолжить с шага 3.1.5 - 3.1.16 от би-листовку инструкции клапана.
5. Постобработки
- Давления и осциллограмм
- Средний данных, собранных для каждого сигнала собирают, то есть давление в аорте (AP), давление в желудочке (VP) и расход (Q).
- Для каждой группы клапан (полимер, свиной нAtive аортального клапана и би-брошюра), участок соответствующего AP, вице-президент и Q в зависимости от времени отношения на том же участке.
- Для AP, накладывать нормальные, родные аортального клапана 18, и би-листовку протезов клапанов 19 сюжетов из литературы для целей проверки.
- Гидродинамические метрик
- Для каждого испытания клапана, следующие показатели гидродинамического должна исчисляться: а) прямое падение давления потока и максимальной трансклапанный давления (TVP), б) аорты среднеквадратичной (RMS) вперед расхода, в) аорты прямого потока, закрытие, утечки и общий объем регургитации, D) клапана конце площади отверстия (ОВД), д) трансаортальный прямого потока, закрытие, утечки и полных потерь энергии.
- Прямой поток перепад давления вычисляется из TVP чтения и могут быть разделены на 3 временных интервалов, P: интервал, который начинается и заканчивается 0 TVP, F: интервал с прямого потока и H: интервал, начиная с 0 TVP и заканчивая 0 потоком. Максимальная TVP является маximum градиент давления записал на клапане аорты от показаний и давление в желудочке.
- Поток RMS форвардный курс (Q RMS) обеспечивает полезную метрическую для количественного определения величины расхода вперед следующим образом:

Где 'N' является общее количество очков, набранных время, 'Q Я "мгновенного измерения расхода собираться для« я ». - Аорты вперед, закрытия и объемы утечки рассчитываются на основе следующих интервалах Время, вперед: начало прямого потока через клапан (Т о), до конца прямого потока (Т 1); Окончание: от 1 т до экземпляра о закрытии клапана (т 2); утечки: от т 2 до конца сердечного цикла (т 3). Общий объем регургитации является простой суммой КлосаIng и утечка томов.
- ОВД на основе свойств крови может быть вычислена по 3 интервала, P, F и Н от среднего ТВП в течение каждого из этих периодов, как 20:
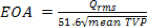
- Потери энергии определяются следующим образом 21:
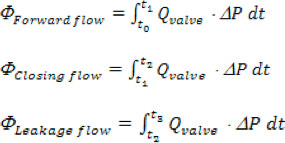
- Для каждого испытания клапана, следующие показатели гидродинамического должна исчисляться: а) прямое падение давления потока и максимальной трансклапанный давления (TVP), б) аорты среднеквадратичной (RMS) вперед расхода, в) аорты прямого потока, закрытие, утечки и общий объем регургитации, D) клапана конце площади отверстия (ОВД), д) трансаортальный прямого потока, закрытие, утечки и полных потерь энергии.
Результаты
Представитель потока и давления колебаний приведены на рисунках 3, 4 и 5. Эти участки были усредненные по образцу размер клапанов, состояние которых для каждой группы, который был, N = 5, 4 и 2 клапана для полимеров, родные свиньи и би-листовку, соответственно. Средний гидро?...
Обсуждение
В этом исследовании мы показали полезность изменения коммерчески доступных пульсирующей блока дубликатор для размещения трехстворчатый клапан геометрии так, что гидродинамические испытания полимера и естественных клапанов свиней может быть выполнена. В частности, в нашем случае, с?...
Раскрытие информации
Авторы не имеют ничего раскрывать.
Благодарности
Семян грант от университета Флориды - медицинский колледж выражает искреннюю признательность. Аспирантура (Мануэль Салинас) была оказана помощь меньшинство возможности программы в области биомедицинских исследований - исследовательская инициатива для повышения научного (MBRS-RISE) общения: NIH / NIGMS R25 GM061347. Финансовая поддержка со стороны Уоллес H. Coulter через Фонд Международного университета Флориды, в биомедицинской инженерии Департамент также с благодарностью. Наконец, авторы выражают благодарность следующим студентам за их помощь на различных этапах экспериментального процесса: Kamau Pier, Малахия Suttle, Кендалл Армстронг и Авраама Альфонсо.
Материалы
| Name | Company | Catalog Number | Comments |
| Pump | ViVitro Labs | http://vivitrolabs.com/products/superpump/ | |
| Flow Meter and Probe | Carolina Medical | Model 501D | http://www.carolinamedicalelectronics.com/documents/FM501.pdf |
| Pressure Transducer | ViVitro Labs | HCM018 | |
| ViVitro Pressure Measuring Assembly | ViVitro Labs | 6186 | |
| Valve holder | WB Engineering | Designed by Florida International University. Manufactured by WB Engineering | |
| Pulse Duplicator | ViVitro Labs | PD2010 | http://vivitrolabs.com/wp-content/uploads/Pulse-Duplicator-Accessories1.pdf |
| Pulse Duplicator Data Acquisition and Control System, including ViViTest Software | ViVitro Labs | PDA2010 | http://vivitrolabs.com/products/software-daq |
| Porcine Hearts and Native Aortic Valves | Mary's Ranch Inc | ||
| Bi-leaflet Mechanical Valves | Saint Jude Medical | http://www.sjm.com/ | |
| High Vacuum Grease | Dow Corning Corporation | http://www1.dowcorning.com/DataFiles/090007b281afed0e.pdf | |
| Glycerin | McMaster-Carr | 3190K293 | 99% Natural 5 gal |
| Phosphate Buffered Saline (PBS) | Fisher Scientific | MT21031CV | 100 ml/heart |
| Antimycotic/Antibiotic Solution | Fisher Scientific | SV3007901 | 1 ml in 100 ml of PBS/heart; 20 ml for ViVitro System |
| NaCl | Sigma-Aldrich | S3014-500G | 9 g/L of deionized water |
| Deionized Water | EMD Millipore Chemicals | Millipore Deionized Purification System. 1.3 L for ViVitro System, 200 ml for heart valve dissection process |
Ссылки
- Rajamannan, N. M., et al. Calcific aortic valve disease: not simply a degenerative process: A review and agenda for research from the National Heart and Lung and Blood Institute Aortic Stenosis Working Group. Executive summary: Calcific aortic valve disease-2011 update. Circulation. 124, 1783-1791 (2011).
- Marijon, E., Mirabel, M., Celermajer, D. S., Jouven, X. Rheumatic heart disease. Lancet. 379, 953-964 (2012).
- Karaci, A. R., et al. Surgical treatment of infective valve endocarditis in children with congenital heart disease. J. Card. Surg. 27, 93-98 (2012).
- Knirsch, W., Nadal, D. Infective endocarditis in congenital heart disease. Eur. J. Pediatr. 170, 1111-1127 (2011).
- Korossis, S. A., Fisher, J., Ingham, E. Cardiac valve replacement: a bioengineering approach. Biomed. Mater. Eng. 10, 83-124 (2000).
- Ghanbari, H., et al. Polymeric heart valves: new materials, emerging hopes. Trends Biotechnol. 27, 359-367 (2009).
- Mol, A., Smits, A. I., Bouten, C. V., Baaijens, F. P. Tissue engineering of heart valves: advances and current challenges. Expert Rev. Med. Devices. 6, 259-275 (2009).
- Ramaswamy, S., et al. The role of organ level conditioning on the promotion of engineered heart valve tissue development in using mesenchymal stem cells. Biomaterials. 31, 1114-1125 (2010).
- Sacks, M. S., Schoen, F. J., Mayer, J. E. Bioengineering challenges for heart valve tissue engineering. Annu. Rev. Biomed. Eng. 11, 289-313 (2009).
- Zamorano, J. L., et al. EAE/ASE recommendations for the use of echocardiography in new transcatheter interventions for valvular heart disease. J. Am. Soc. Echocardiogr. 24, 937-965 (2011).
- ANSI/AAMI/ISO. Cardiovascular Implants - Cardiac Valve Prostheses. Assoc. Adv. Med. Instrum. 71, (2005).
- Gallocher, S. L. . Durability Assessment of Polymer Trileaflet Heart Valves PhD thesis. , 313 (2007).
- Carroll, R., Boggs, T., Yamaguchi, H., Al-Mously, F., DeGroff, C., Tran-Son-Tay, R. Blood Cell Adhesion on Polymeric Heart Valves. , (2012).
- Pierre, K. K., Salinas, M., Carroll, R., Landaburo, K., Yamaguchi, H., DeGroff, C., Al-Mousily, F., Bleiweis, M., Ramaswamy, S. Hydrodynamic Evaluation of a Novel Tri-Leaflet Silicone Heart Valve Prosthesis. , (2012).
- Cacciola, G., Peters, G. W., Schreurs, P. J. A three-dimensional mechanical analysis of a stentless fibre-reinforced aortic valve prosthesis. J. Biomech. 33, 521-530 (2000).
- De Hart, J., Cacciola, G., Schreurs, P. J., Peters, G. W. A three-dimensional analysis of a fibre-reinforced aortic valve prosthesis. J. Biomech. 31, 629-638 (1998).
- Lim, W. L., Chew, Y. T., Chew, T. C., Low, H. T. Pulsatile flow studies of a porcine bioprosthetic aortic valve in vitro: PIV measurements and shear-induced blood damage. J. Biomech. 34, 1417-1427 (2001).
- Gutierrez, C., Blanchard, D. G. Diastolic heart failure: challenges of diagnosis and treatment. Am. Fam. Physician. 69, 2609-2616 (2004).
- Shi, Y., Yeo, T. J., Zhao, Y., Hwang, N. H. Particle image velocimetry study of pulsatile flow in bi-leaflet mechanical heart valves with image compensation method. J. Biol. Phys. 32, 531-551 (2006).
- Chandran, K. B., Yoganathan, A. P., Rittgers, S. E. . Biofluid Mechanics: The Human Circulation. , 277-314 (2007).
- Akins, C. W., Travis, B., Yoganathan, A. P. Energy loss for evaluating heart valve performance. J. Thorac. Cardiovasc. Surg. 136, 820-833 (2008).
- Fung, Y. C. . Biomechanics: Circulation. , (1997).
- Keener, J., Sneyd, J. . Mathematical Physiology, II: Systems Physiology. , (1998).
- Quick, C. M., Berger, D. S., Noordergraaf, A. Apparent arterial compliance. Am. J. Physiol. 274, H1393-H1403 (1998).
- Wang, Q., Jaramillo, F., Kato, Y., Pinchuk, L., Schoephoerster, R. T. Hydrodynamic Evaluation of a Minimally Invasive Heart Valve in an Isolated Aortic Root Using a Modified In Vitro Model. J. Med. Devices. 3, 011002.1-011002.6 (2009).
- Baldwin, J. T., Campbell, A., Luck, C., Ogilvie, W., Sauter, J. Fluid dynamics of the CarboMedics kinetic bileaflet prosthetic heart valve. Eur. J. Cardiothorac. Surg. 11, 287-292 (1997).
Перепечатки и разрешения
Запросить разрешение на использование текста или рисунков этого JoVE статьи
Запросить разрешениеСмотреть дополнительные статьи
This article has been published
Video Coming Soon
Авторские права © 2025 MyJoVE Corporation. Все права защищены