JoVE 비디오를 활용하시려면 도서관을 통한 기관 구독이 필요합니다. 전체 비디오를 보시려면 로그인하거나 무료 트라이얼을 시작하세요.
Method Article
접합 효율 모니터링을 위한 기자 기반 셀룰러 분석
요약
이 프로토콜은 5'splice 사이트 돌연변이가 접합에 미치는 영향을 모니터링하기 위한 미니유전자 기자 분석체를 설명하고 돌연변이 유발 접합 억제를 위한 억제기 U1 snRNA를 개발한다. 리포터 및 억제기 U1 snRNA 구조는 HeLa 세포에서 발현되고, 접합은 프라이머 확장 또는 RT-PCR에 의해 분석된다.
초록
유전자 발현 동안, pre-mRNA 접합의 중요한 단계는 성숙한 mRNA의 세포질 수출 의 앞에 엑손에 합류하고 인트론을 제거하기 위하여 스플라이스 사이트의 정확한 인식 및 pliceosomal 복합체의 능률적인 조립을 관련시킵니다. 접합 효율은 스플라이스 부위의 돌연변이 존재, 트랜스 작용 접합 인자의 영향 또는 치료제의 활동에 의해 변경될 수 있다. 여기에서는 주어진 exon의 접합 효율을 모니터링하기 위해 적용할 수 있는 셀룰러 분석프로토콜을 설명합니다. 분석법은 적응형 플라스미드 인코딩된 3-엑손/2-intron 미니진 리포터를 사용하며, 이는 일시적인 과도 경질에 의해 포유류 세포에서 발현될 수 있다. 전염 후, 총 세포 RNA는 단리되고, 기자 mRNA에서 결합하는 엑슨의 효율은 프라이머 확장 또는 반정량 역전사-폴리머라제 연쇄 반응(RT-PCR)에 의해 결정된다. 우리는 어떻게 관련된 질병의 충격을 설명합니다 5′ 스플라이스 사이트 돌연변이는 기자에 그(것)들을 소개하여 결정될 수 있습니다; 그리고 이러한 돌연변이의 억제는 U1 작은 핵 RNA (snRNA)와 의 결합에 의해 달성 될 수있는 방법 5′ 지역에서 보상 돌연변이를 운반 하는 구성 은 사전 mRNAs에 있는 엑손 인 트론 접합부에서 5′splice 사이트와 기질. 따라서, 리포터는 돌연변이 5′ 스플라이스 사이트의 인식을 향상시키기 위해 치료 U1 입자의 설계에 사용될 수 있다. 인핸서 또는 소음기 시퀀스를 접합하는 것과 같은 시스 작용 규제 사이트를 리포터에 삽입하여 특정 대체 접합 계자에 의해 중재된 규제에서 U1 snRNP의 역할을 검사하는 데도 사용할 수 있습니다. 마지막으로, 세포를 발현하는 기자는 소분자로 배양하여 구성적인 사전 mRNA 접합 또는 돌연변이 5′ 스플라이스 부위를 운반하는 엑슨에 잠재적 인 치료법의 효과를 결정할 수 있습니다. 전반적으로, 리포터 분석은 기본적인 접합 기계장치 및 접합 관련 질병을 연구하기 위하여 다양한 조건에서 접합 효율을 감시하기 위하여 적용될 수 있습니다.
서문
pre-mRNA 접합은 비코딩 인트론을 제거하고 코딩 엑손을 정확하게 리게이트하여 성숙한 mRNA를 형성하는 필수적인 처리 단계입니다. 5′-스플라이스 사이트 및 3′-스플라이스 사이트라고 하는 엑손 인트론 교차로에서 컨센서스 시퀀스를 인식하는 것은 접합 기계의 구성 요소에 의해 접합 과정을 시작합니다. U1 소형 핵리보뉴클레오프로틴(snRNP)은 U1 snRNA를 사전 mRNA1에 기본 페어링하여 5′-스플라이스 부위를 인식합니다. 5′-스플라이스 사이트 서열을 변경하는 유전적으로 승계한 돌연변이는 많은 질병2,3와 연관됩니다. U1 snRNA의 염기 페어링을 돌연변이 5′-스플라이스 사이트로 손상하면 비정상적인 접합이 발생하여 영향을 받는 성적증명서의 번역을 손상시킬 수 있습니다. 접합 결함을 해결하기 위한 잠재적인 치료 접근법은 5′-splice 사이트와 기초가 되는 5′-지구에 있는 보상 뉴클레오티드 변경을 운반하는 수정된 U1 snRNA에 의하여 돌연변이의 억제를 관련시킵니다. 이러한 수정된 U1 snRNAs는 exon 특정 U1 snRNAs라고도 하며, 접합 결함을 반전시키는 데 효과적인 것으로 밝혀졌으며, 그 결과 구조된 mRNA4,5,6,7,8에서 단백질 발현이 증가되는 것으로 나타났다.
여기에서, 우리는 U1 snRNP 보완 분석, 엑슨의 접합에 5′ss 돌연변이의 효과의 평가를 허용하고 또한 엑슨 포함의 구조를 가능하게 하는 수정된 U1 snRNAs의 발달에 사용될 수 있는 기자 기지를 둔 세포 접면 분석서를 기술합니다. 또한 프라이머 확장 및 RT-PCR에 의해 접합된 리포터 성적증명서를 모니터링하고, 프라이머 확장 및 RT-qPCR에 의해 수정된 U1 snRNAs의 발현을 결정하기 위한 프로토콜을 제공합니다.
Access restricted. Please log in or start a trial to view this content.
프로토콜
1. 시약 및 버퍼
참고: 진공 필터를 사용한 모든 멸균은 생물 안전 캐비닛에 0.2 μm polyethersulfone(PES) 멤브레인으로 수행해야 합니다.
- 1.0mL의 디틸피로카보네이트(DEPC)를 1.0L의 디에이온화된 물에 첨가하고, 실온(RT)에서 최소 1시간 이상 섞은 다음, 사용하기 전에 RT로 식힙니다.
- DMEM 분말 1패킷(13.4g), 중탄산나트륨 3.7g, 태아소 혈청(FBS), 페니실린 100mL, 멸균 데리온 화물 800mL를 혼합하여 덜벡코의 수정이이글 배지(DMEM)를 준비한다. DMEM의 페니실린 및 연쇄 절제술의 최종 농도는 각각 50 U/mL 및 50 μg/mL이어야 합니다. pH를 7.4로 조정한 다음 멸균 분수로 부피를 1.0L로 구성합니다. 여과에 의해 살균하고 4 °C에 보관하십시오.
- 25.6 g의 디나트륨 수소 이질산염(Na2HPO4·10x PBS)을 추가하여 10배 인산완충식식(10배 PBS)을 준비하세요. 7H2O), 이수소 인산염 2g(KH2PO4), 염화칼륨 2g(KCl), 염화나트륨 80g~800mL의 탈이온화수. 혼합하여 부피를 1.0 L. 여과에 의해 살균하여 4°C에 보관합니다.
- 0.5 M 에틸렌 디아민 테트라 아세트산(EDTA)을 Na2•EDTA•2H2O186.1g을 용해하여 ~800mL의 탈온화된 물로 준비한다. pH를 8.0으로 조정한 다음 멸균 된 분수로 부피를 1.0 L로 구성합니다. 여과에 의해 살균하고 4 °C에 보관하십시오.
- 10x 트립신(2.5%), 0.5m EDTA의 2mL 100mL를 혼합하여 1배 트립신-EDTA 솔루션을 준비하고, 여과및 알리쿼트에 의해 최대 1.0L. 멸균을 50mL 원추형 튜브에 첨가한다. 1-2 주 동안 4 °C에 저장하거나 장기 사용을 위해 -20 ° C에서 동결하십시오.
- 15mL의 최종 부피에 대해 14.4mL의 포르마이드 와 0.5 M EDTA의 0.6mL를 혼합하여 2배 포름아미드 DNA/RNA 로딩 염료를 준비한다. 브로모페놀 블루와 자일렌 시안올 파우더를 최종 농도0.02%에 넣고 4°C에 보관합니다.
참고: 포르마미드는 독성이 있고 부식성이 있습니다. 추가 안전 권장 사항에 대한 재료 안전 데이터 시트를 읽어보십시오. - 5배 트라이/붕산/EDTA(5배 TBE) 버퍼를 트리스 베이스 54.0g, 보릭산 27.5g, 0.5M EDTA 20mL를 ~800mL의 탈온화된 물에 혼합하여 준비한다. 혼합하여 용해하고 탈온화 된 물로 1.0 L로 볼륨을 구성합니다.
- 우레아 폴리아크라이글아미드 젤 전기포레시스(urea-PAGE) 용액을 5배 TBE 200mL, 40%의 250mL, 450mL 의 40%19:1 비스/아크릴아미드, 450.5g의 우레아를 준비한다. 그런 다음 성분이 완전히 녹을 때까지 최대 1.0 L. 혼합물을 추가한 다음 여과에 의해 살균한 다음 호박색 유리 병에 4°C에 보관하십시오.
참고 : 비스 / 아크릴아미드는 독성입니다. 추가 안전 절차를 위해 재료 안전 데이터 시트를 읽어보십시오. - 10mL의 탈수로 APS 1g을 용해하여 10% 암모늄 과삼산염(APS)을 준비하고 4°C에 보관하십시오.
2. 기자 및 U1 snRNA 플라스미드와 함께 HeLa 세포의 결합
참고: 헬라 세포의 트랜스포피는 생물학적 안전 캐비닛의 멸균 조건하에서 수행되어야 합니다. 모든 재료의 외부 표면은 생물학적 안전 캐비닛에 도입되기 전에 70 % 에탄올로 분사해야합니다.
- 세포가 약 80-90% 컨실루인 경우 2-3일마다 월지처리하여 5% CO2 를 가진 37°C 인큐베이터에서 DMEM에서 헬라 세포를 유지한다.
- HeLa 세포를 통과하기 위해, 소비된 배지를 흡인한 다음 3분 동안 37°C에서 1mM EDTA를 함유한 0.25%의 트립신으로 세포를 배양한다.
- 인큐베이션 후 신선한 DMEM 7mL를 추가합니다. 셀 서스펜션을 10mL 튜브로 옮기고 원심분리기를 1,000 x g 에서 5분 동안 전달합니다.
- 신선한 DMEM의 10 mL에서 세포 펠릿을 다시 중단한 다음 새로운 조직 배양 접시에 세포를 20 % 합류시 플레이트.
- 과도 과도 의 과도의 경우, 깨끗한 혈류계 슬라이드와 헬라 세포를 계산하고 2.5 x 105 세포 / mL의 밀도로 서스펜션을 준비합니다.
- 종자 1.0 mL 의 2.5 x 105 셀/mL 헬라 셀 현탁액은 12웰 플레이트의 각 웰에 넣고 37°C에서 하룻밤 동안 배양한다.
- 다음 날, 소비 된 매체를 흡인하고 세럼으로 신선한 DMEM0.8mL을 추가합니다.
- Dup51 또는 Dup51p 리포터 플라스미드의 0.2 μg, pcDNA 1.8 μg, pNS6U1 또는 pNS6U1-5a 플라스미드, 새로운 1.5mL 마이크로센트리푸지 튜브에 100 μL의 트랜스페션 배지를 추가하여 솔루션 I를 준비한다.
- 100μL의 형질과 시료당 4.0 μL의 트랜스페트 시약을 추가하여 모든 시료가 전해질 수 있도록 솔루션 II의 마스터 믹스를 준비합니다.
- 솔루션 I를 포함하는 각 미세 원심 분리기 튜브에 100 μL의 솔루션 II를 추가하여 전환 믹스를 준비합니다.
- 15s, 원심분리기의 원심분리기는 3,000 x g 에서 RT에서 10초동안 원심분리기를 혼합한 다음 RT에서 5분 동안 배양합니다.
- 12웰 HeLa 세포 판의 한 웰에 200 μL의 모든 200 μL을 추가하여 웰당 1.0mL의 최종 부피를 달성하고 48시간 동안 37°C에서 플레이트를 배양한다.
- 인큐베이션 후, 시판되는 구아니딘 티오야네이트 및 페놀 용액으로 전감염된 HeLa 세포로부터 RNA를 추출한다.
참고: 이 시약에는 페놀이 포함되어 있으며 이 단계는 연기 후드에서 수행해야 합니다. DEPC 처리된 물의 사용은 추출된 RNA의 재중단을 위해 권장됩니다.- 소비된 매체를 흡인하고 시약의 500 μL을 각 우물에 추가합니다. 5 분 동안 RT에서 인큐베이션.
- 위아래로 피펫팅하여 균질화합니다. 그런 다음 솔루션을 새로운 1.5 mL 마이크로 센심 분리기 튜브로 전송합니다.
- 15s에 클로로폼과 소용돌이 100 μL을 추가합니다.
- RT에서 15 분 동안 12,000 x g 의 원심 분리기.
- RNA를 함유하는 RNA의 200 μL을 새로운 1.5mL 마이크로센심심분리기 튜브로 이송한다.
- 각 RNA 샘플에 글리코겐 2μg과 이소프로판놀 200 μL을 추가합니다. 튜브를 반전시켜 섞는다.
- RNA 침전물을 4°C에서 10분 동안 12,000 x g 에서 원심분리하여 수집합니다.
- RNA 펠릿을 방해하지 않고 상체를 제거하고 폐기하십시오.
- 70% 에탄올의 1.0mL를 추가하고, 튜브를 반전시키고, 2.13.7단계에 설명된 바와 같이 원심분리를 추가하여 펠릿을 두 번 세척한다.
- 공기는 RT에서 ~ 10-20 분 동안 펠릿을 건조하고 RNase가없는 물의 10-20 μL에서 RNA를 다시 중단합니다.
- Desjardins 및 Conklin9에 의해 기술된 대로 260 nm에서 흡광도를 측정하여 RNA 농도를 결정합니다.
- -20°C에서 프라이머 확장 또는 저장 RNA 샘플을 진행합니다. 절연 RNA는 6-12 개월 동안 -20 °C에서 저장 될 수있다.
3. 올리고뉴클레오티드의 32P 라벨링
참고: 32P-ATP 및 32P 표지 된 올리고 뉴클레오티드의 사용과 관련된 단계는 공인 기관 기관의 승인을 받은 숙련 된 개인이 아크릴 방패 뒤에 수행해야합니다. 아래에 설명된 프로토콜은 올리고뉴클레오티드, Dup3r 및 U17-26-R, 및 요소-PAGE에 대한 마커의 라벨링에 사용될 수 있다. DEPC 처리된 물의 사용은 올리고뉴클레오티드 및 크기 배제 구슬의 재중단을 위해 권장됩니다.
- 1.5 mL 마이크로센심분리기 튜브에, 표 1에 설명된 바와 같이 올리고뉴클레오티드, T4 폴리뉴클레오티드 키나아제(T4 PNK), T4 PNK 완충제 및 32P-ATP를 추가한다. 혼합물에 마지막 32P-ATP를 추가; 이것은 중요합니다.
참고: 방사성 용액을 추가하기 위해 필터 팁을 사용하는 것이 좋습니다. - 37°C에서 30분 동안 수조에 배양합니다.
- 라벨링 반응이 인큐베이팅되는 동안, ~10s에 부드럽게 소용돌이를 통해 잘라낸 25 kDa 분자량으로 크기 배제 구슬을 다시 보냅니다.
참고: 크기 제외 구슬은 제조업체의 지시에 따라 준비되어야 하며 4°C에서 25% 에탄올에서 50% 서스펜션으로 보관해야 합니다. - 재일시 중단된 구슬의 600 μL을 1.5mL 수집 튜브에 배치한 일회용 미니 컬럼으로 전송하고 비드 스톡을 4°C로 반환하여 컬럼을 준비한다.
- RT에서 1 분 동안 2,000 x g 의 원심 분리기와 흐름을 폐기하십시오.
- 기둥에 RNase가 없는 물의 300 μL을 추가하여 구슬을 씻으시면 됩니다.
- 3.5 단계를 반복합니다. 및 3.6. 두 번 미니 컬럼을 새로운 1.5mL 원심분리기 튜브로 전송합니다.
- 크기 배제 비드 컬럼과 원심분리기는 RT에서 1분 동안 5000 x g 의 크기 배제 비드 컬럼과 원심분리기에 키나아제 반응 믹스를 추가합니다.
- 32P 표지 올리고뉴클레오티드가 있는 흐름을 수집하고 저장하고 모든 팁과 튜브를 아크릴 폐기물 상자에 버리십시오.
- RNase가 없는 물 20μL를 추가하여 32P 로표시된 올리고뉴클레오티드를 최종 농도인 2.5 μM에 희석시 합니다.
참고: 우레아 페이지 젤에 적재하는 데 필요에 따라 라벨이 부착된 마커를 희석시합니다. - -20°C의 아크릴 마이크로튜브 상자에 표지된 올리고뉴클레오티드를 저장하거나 프라이머 확장 분석을 진행한다.
4. 프라이머 확장에 의한 접합 기자 성적증명서 분석
참고: 사용하기 전에 RNase가 시약을 비활성화하여 표면과 장비를 청소하는 것이 좋습니다.
- 헬라 세포에서 추출한 RNA 2.0 μg를 별도의 200μL 마이크로센심분리기 튜브에 추가하고 RNase 가 없는 물을 추가하여 6.55 μL의 부피를 구성합니다.
- 표 2에 도시된 대로 희석된 32P-Dup3r 및 dNTP로 마스터 믹스 I를 준비하고 RNA 샘플을 포함하는 각 PCR 튜브에 믹스의 0.9 μL을 추가합니다.
- 튜브를 먼저 65°C에서 5분 동안 배양한 다음 얼음에서 1분 동안 배양합니다.
- 표 2에 도시된 바와 같이 5배 퍼스트 스트랜드 버퍼, 디티오스리톨(DTT), RNase 억제제 및 역전사로 마스터 믹스 II를 준비한다.
- RNA및 마스터 믹스 1을 포함하는 각 튜브에 혼합의 2.55 μL을 추가; 반응의 총 부피는 10 μL이어야 합니다. 10 분 동안 RT에서 튜브를 유지하십시오.
- 튜브를 마른 목욕이나 열 사이클러로 옮기고 인큐베이션을 60분 동안 50°C에서 한 다음 70°C에서 15분 동안 배양합니다.
- 인큐베이션 후, 각 샘플에 2x 포름아미드 RNA 로딩 염료10을 추가하고 -20°C의 아크릴 상자에 저장하거나 14cm 길이의 겔을 사용하여 우레아 페이지로 조각의 분리를 진행하며 8단계에서 설명된 바와 같이 겔 이미지의 시각화를 진행한다.
- 이미지 분석 소프트웨어로 젤 이미지의 밀도 스캔을 수행하고 아래와 같이 엑슨 2 포함의 백분율을 계산하기 위해 포함 및 건너뛴 제품의 대역 강도를 사용합니다.

5. 형광 RT-PCR에 의한 접합 기자 성적 증명서 분석
참고: 아래에 설명된 RT-PCR 분석은 cDNA 합성을 위한 무작위 hexamers및 접합제품의 PCR 증폭을 위한 레이블이 없는 Dup8f 및 Cy5 표지된 Dup3r 올리고뉴클레오티드의 조합을 사용합니다.
- cDNA 합성의 경우, 트랜스페드 헬라 세포로부터 추출된 RNA 2.0 μg를 별도의 200μL 마이크로센심분리기 튜브에 추가하고 RNase 가 없는 물을 추가하여 부피를 11.0 μL로 구성합니다.
- 표 3에 표시된 대로 임의의 hexamers 및 dNTP를 포함하는 마스터 믹스 I를 준비하고 각 샘플에 믹스의 2.0 μL을 추가합니다. 인큐베이션, 먼저 65 °C에서 5 분 동안 얼음에 1 분 동안.
- 표 3에 도시된 바와 같이 첫 스트랜드 버퍼, RNase 억제제, DTT 및 역전사를 포함하는 마스터 믹스 II를 준비하고 RNA 및 마스터 믹스 I를 포함하는 각 튜브에 믹스의 7.0 μL을 추가합니다.
- 튜브를 10분 동안 RT로 유지한 다음 50°C에서 60분, 70°C에서 15분 동안 배양합니다.
참고: 완성된 cDNA 반응은 -20°C에 저장될 수 있다. - PCR의 경우 각 cDNA 샘플의 1.0 μL(100 ng/μL)을 새로운 PCR 튜브로 전송합니다.
- 표 4에 설명된 바와 같이 Dup8f, Cy5-Dup3r, dNTP, Taq 버퍼, Taq 폴리머라제 및 물로 구성된 마스터 믹스를 준비하고 cDNA를 포함하는 각 튜브에 11.5 μL을 첨가한다.
- 3분 동안 94°C에서 초기 내포화 단계를 사용하여 열 사이클러를 사용하여 PCR을 수행; 그 다음으로 20사이클의 데니션(94°C 30s), 아닐링(30s용 65°C), 연장(15s용 72°C), 5분 동안 72°C의 종단 단계를 거쳤다.
- 각 튜브에 2배 포름아미드 DNA 하중 염료의 12.5 μL을 추가하고 5분 동안 95°C에서 가열합니다.
- PCR 반응을 -20°C에 저장하거나 8.1-8.4단계에서 아래에 설명된 바와 같이 우레아-PAGE를 진행한다.
- 전기포고후, 전기전도 장치에서 유리 판을 제거하고 형광 이미저를 사용하여 스캔하여 겔을 시각화한다.
- 젤 이미지의 밀도 측정 스캐닝을 수행하고 포함 된 및 건너 뛴 제품의 대역 강도를 사용하여 4.8 단계에 설명된 바와 같이 엑슨 2 포함의 백분율을 계산합니다.
6. 프라이머 확장에 의한 변이체 U1 snRNA 발현 분석
- 헬라 세포에서 추출한 RNA의 2.0 μg를 별도의 200 μL 마이크로센심분리기 튜브에 추가하고 RNase 가 없는 물을 추가하여 부피를 4.325 μL로 구성한 다음 표 5에 표시된 대로 dATP를 추가합니다.
- 각 튜브에 32P-U17-26-R 올리고뉴클레오티드의 10,000 CPM을 추가합니다.
참고: 32P-U17-26-R(3단계에서)의 10,000 cpm/μL 용액을 준비하려면, 라벨이 부착된 올리고뉴클레오티드(1:20 희석)를 희석시키고, 신클렌화 카운터를 사용하여 1.0 μL에서 cpm을 결정합니다. 또한 탈이온화된 물로 희석하여 새로운 1.5mL 마이크로센트심리분리기 튜브에서 10,000 cpm/μL의 용액을 준비합니다. - 65°C에서 5분 동안 배양한 다음 얼음위에 1분 동안 배양합니다.
- 표 5에 표시된 대로 5x 퍼스트 스트랜드 버퍼, RNase 억제제, DTT 및 역전사로 마스터 믹스를 준비하고 각 샘플에 믹스의 1.8 μL을 추가합니다.
- 인큐베이션, 먼저 RT에서 10분 동안, 그리고 42°C에서 10분 동안 배양합니다.
- 인큐베이션 후, 각 샘플에 2x 포름아미드 RNA 로딩 염료10μL을 넣고 -20°C의 아크릴 상자에 보관하거나 38cm 길이의 겔을 사용하여 우레아 페이지로 조각의 분리를 진행한다(8단계 참조).
7. RT-qPCR에 의한 변종 U1 snRNA 발현 분석
- 전술한 바와 같이 제조된 cDNA 스톡을 5.1-5.4단계에서 0.2 ng/μL의 농도로 희석한다.
- 파이펫 5.0 μL 희석 된 cDNA의 개별 우물로 96 웰 qPCR 플레이트의 트리플 리케이트. 템플릿 없음 제어(NTC)에 cDNA 대신 탈이온화된 물을 추가합니다.
- U1 및 U2 snRNAs에 대한 전방 및 역 프라이머로 구성된 두 개의 별도의 프라이머 믹스와 표 6에 표시된 대로 물을 준비합니다.
참고: U1 및 U2 snRNA 특이적 프라이머에 대한 서열은 표 7에 제공됩니다. - 샘플 및 NTC 웰에 U1 및 U2 snRNA 프라이머 믹스의 5.0 μL을 추가합니다.
- 각 웰에 실시간 PCR 믹스의 10.0 μL을 추가합니다.
- 광학 필름으로 플레이트를 밀봉한 다음 RT에서 2분 동안 원심분리기를 1,000xg로 밀봉하여 우물 바닥에 대한 반응을 수집합니다.
- 대상 앰플의 임계 정량화 주기(Cq) 값을 수집하는 동안 10분 동안 95°C에서 초기 내수 단계로 qPCR을 수행하고, 2단계 프로토콜의 40사이클을 선행하여 내포화(95°C for 15s) 및 아닐링/확장(62°C)으로 구성된다.
- U1 및 U2 snRNA 반응에 대한 해리 곡선에서 단일 피크를 확인하여 qPCR 반응을 완료합니다.
- Cq 값에서 pcDNA 제어와 비교하여 U1 및 U2 snRNAs에 대한 델타 Cq(ΔCq)를 계산합니다.
- 모든 샘플에 대해 아래와 같이 ΔΔCq 값을 사용하여 U2와 비교하여 변형 U1 snRNA 발현을 U1의 상대 수량(RQ)으로 결정합니다.

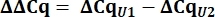
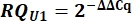
8. 우레아 페이지 젤의 설정 및 실행
참고: 유리 판의 조립 및 젤 실행 장치는 제조업체의 지시에 따라 수행되어야합니다. 10% 우레아-PAGE 젤의 주조는 Summer et al.10에 의해 이전에 설명된 프로토콜에 따라 수행될 수 있다. 마커 및 샘플의 제조와 관련된 단계, 및 젤의 실행 및 시각화는 아래에 설명되어 있습니다. 선택적으로, 젤이 유리 판에 달라지는 것을 방지하기 위해, 내부 표면은 표면에 용액의 1mL을 추가하고 조직으로 전체 표면에 고르게 퍼지면서 실리콘 용액으로 코팅될 수 있다. 일단 건조되면, 접시는 탈이온 물로 세척하고 다시 건조해야합니다.
주의: 중합되지 않은 아크릴아미드는 신경독성이며 재료 안전 데이터 시트에 권장되는 보호 기능으로 처리해야 합니다.
- 프라이머 확장 샘플 및 마커를 95°C에서 5분 동안 가열한 다음 RT에서 5s에 대해 3,000 x g 의 탁상 미세 원심 분리기에서 원심분리기를 준비합니다.
- 마커와 샘플을 적재하기 전에 1x TBE 버퍼로 우물을 내세워 정착된 우레아를 제거합니다.
- 10 μL/샘플/웰을 로드하고 젤을 300-500V에서 2-3시간 동안 또는 자일렌 시아놀이 바닥에 도달할 때까지 실행합니다.
참고: 32P 표지 마커의 약 1,000 cpm을 로드할 수 있습니다. - 전기 전구 후, 전기 전광 장치에서 유리 판을 제거합니다.
- 두 판을 조심스럽게 분리하여 젤이 유리 표면에 평평하게 놓여 있고 젤을 필터 용지에 옮기고 플라스틱 랩으로 덮습니다.
- 젤 드라이어를 사용하여 30 분 동안 80 °C에서 필터 용지에 젤을 진공 건조하십시오.
- 말린 젤을 인광 화상 진찰 카세트에 놓고 하룻밤 RT에 보관하십시오.
참고: 인광화면은 사용하기 전에 라이트 박스를 사용하여 지워야 합니다. - 젤 이미지를 시각화하려면 화면을 제거하고 인광 선저를 사용하여 스캔합니다.
Access restricted. Please log in or start a trial to view this content.
결과
접합 기자 Dup51, 3 개의 엑손-2 인트론 미니진은 인간 β-글로빈 유전자로부터 유래되었으며 이전에 설명되었다(그림 1A)11,12. 우리는 돌연변이 기자, Dup51p, 프로토 카데린 의 엑슨 3에서 발생하는 Usher 증후군 과 관련된 5'splice 사이트 돌연변이를 도입하여 15 (PCDH15) gene13. 엑손 2-인트론 2 접합부에서의 5'splice 사...
Access restricted. Please log in or start a trial to view this content.
토론
분석은 HeLa 이외의 세포주에서 접합 분석을 위해 적응될 수 있지만, 세포 합류 및 DNA의 양과 같은 형질 응력에 영향을 미치는 요인은 최적화될 필요가 있다. 리포터에서 U1 구문비는 다른 세포 유형에서 관찰된 발현 수준에 따라 결정되어야 할 수 있는 또 다른 중요한 매개 변수이다. 추출된 RNA의 품질은 접합 분석에 중요합니다. 따라서 RNase 비활성화 제의 로 RNase 가없는 물 및 표면의 오염 제거를 ?...
Access restricted. Please log in or start a trial to view this content.
공개
저자는 공개 할 것이 없습니다.
감사의 말
이 작품은 국립 보건원 (R21CA170786 및 R01GM127464)과 미국 암 학회 (기관 연구 보조금 74-001-34-IRG)와 밸리 연구 파트너십 프로그램 (P1-4009 및 VRP7)의 S.S. 및 W.M에 대한 자금으로 지원되었습니다. 이 내용은 전적으로 저자의 책임이며 반드시 국립 보건원의 공식 견해를 나타내는 것은 아닙니다.
Access restricted. Please log in or start a trial to view this content.
자료
| Name | Company | Catalog Number | Comments |
| Reagent Grade Deionized Water | ThermoFisher Scientific | 23-751628 | |
| Diethyl pyrocarbonate (DEPC) | Sigma-Aldrich | D5758-25ML | |
| Dulbecco's Modified Eagle Medium (DMEM) powder packet | Gibco | 12100-046 | |
| Sodium Bicarbonate | ThermoFisher Scientific | S233-500 | |
| Fetal Bovine Serum (FBS), Australian Source, Heat Inactivated | Omega Scientific | FB-22 | |
| Penicillin-Streptomycin (P/S) | Sigma-Aldrich | P4458-100ML | |
| Sodium Hydroxide, Standard Solution 1.0N | Sigma-Aldrich | S2567-16A | |
| Hydrochloric Acid, Certified ACS Plus, 36.5 to 38.0% | ThermoFisher Scientific | A144-500 | |
| Disposable PES Bottle Top Filters | ThermoFisher Scientific | FB12566510 | |
| EDTA Disodium Salt Dihydrate | Amresco | 0105-2.5KG | |
| 2.5% Trypsin (10x), no phenol red | ThermoFisher Scientific | 15090046 | |
| Sodium Chloride | Fisher Bioreagent | BP358-212 | |
| Potassium Chloride | Fisher Bioreagent | BP366-1 | |
| Disodium Hydrogen Phosphate Heptahydrate | Fisher Bioreagent | BP332-1 | |
| Potassium Dihydrogen Phosphate | Fisher Bioreagent | BP362-1 | |
| Transfection medium - Opti-MEM™ I Reduced Serum Medium, no phenol red | ThermoFisher Scientific | 11058021 | |
| Transfection Reagent - Lipofectamine™ 2000 | ThermoFisher Scientific | 13778150 | |
| TRIzol™ Reagent | ThermoFisher Scientific | 15596018 | |
| Chloroform (Approx. 0.75% Ethanol as Preservative/Molecular Biology) | ThermoFisher Scientific | BP1145-1 | |
| Ethanol, Absolute (200 Proof), Molecular Biology Grade, Fisher BioReagents | ThermoFisher Scientific | BP2818-4 | |
| Isopropanol, Molecular Biology Grade, Fisher BioReagents | ThermoFisher Scientific | BP2618-212 | |
| Glycogen (5 mg/ml) | ThermoFisher Scientific | AM9510 | |
| Direct-zol RNA Miniprep Kit | Zymo Research | R2052 | |
| ATP, [γ-32P]- 6000Ci/mmol 150mCi/ml Lead, 1 mCi | PerkinElmer | NEG035C001MC | |
| T4 Polynucleotide Kinase | New England Biolabs | M0201L | |
| Size exclusion beands - Sephadex® G-25 | Sigma-Aldrich | G2580-10G | |
| Size exclusion mini columns | USA Scientific | 1415-0600 | |
| pBR322 DNA-MspI Digest | New England Biolabs | N3032S | |
| Low Molecular Weight Marker, 10-100 nt | Affymetrix | 76410 100 UL | |
| Rnase inactivating reagents - RNaseZAP™ | Sigma-Aldrich | R2020-250ML | |
| dNTP Mix (10 mM ea) | ThermoFisher Scientific | 18427013 | |
| RNaseOUT™ Recombinant Ribonuclease Inhibitor | ThermoFisher Scientific | 10777019 | |
| Reverse Transcriptase - M-MLV Reverse Transcriptase | ThermoFisher Scientific | 28025013 | used for primer extension |
| Taq DNA Polymerase | ThermoFisher Scientific | 10342020 | |
| Random Hexamers (50 µM) | ThermoFisher Scientific | N8080127 | |
| Real time PCR mix - SYBR™ Select Master Mix | ThermoFisher Scientific | 4472903 | |
| SuperScript™ III Reverse Transcriptase | ThermoFisher Scientific | 18080093 | used for cDNA preparation |
| Dithiothreitol (DTT) | ThermoFisher Scientific | 18080093 | |
| 5X First-Strand Buffer | ThermoFisher Scientific | 18080093 | |
| Formamide (≥99.5%) | ThermoFisher Scientific | BP228-100 | Review Material Safety Data Sheets |
| Bromophenol Blue sodium salt | Sigma-Aldrich | 114405-5G | |
| Xylene Cyanol FF | Sigma-Aldrich | 2650-17-1 | |
| Tris Base (White Crystals or Crystalline Powder/Molecular Biology) | ThermoFisher Scientific | BP152-5 | |
| Boric Acid (Crystalline/Electrophoresis) | ThermoFisher Scientific | BP168-500 | |
| Acrylamide: Bis-Acrylamide 19:1 (40% Solution/Electrophoresis) | ThermoFisher Scientific | BP1406-1 | Review Material Safety Data Sheets |
| Urea (Colorless-to-White Crystals or Crystalline Powder/Mol. Biol.) | ThermoFisher Scientific | BP169-212 | |
| Ammonium peroxodisulphate (APS) ≥98%, Pro-Pure, Proteomics Grade | VWR | M133-25G | |
| Sigmacote | Sigma-Aldrich | SL2-100ML | |
| N,N,N',N'-Tetramethylethylenediamine (TEMED) ≥99%, Ultrapure | VWR | 0761-25ML | Review Material Safety Data Sheets |
| Adjustable Slab Gel Systems, Expedeon | VWR | ASG-400 | |
| Vertical Gel Wrap™ Glass Plate Sets, 16.5 x 14.5cm | VWR | NGP-125NR | |
| Vertical Gel Wrap™ Glass Plate Sets, 16.5 x 22.0cm | VWR | NGP-200NR | |
| Vertical Gel Wrap™ Glass Plate Sets, 16.5 x 38.7cm | VWR | NGP-400NR | |
| GE Storage Phosphor Screens | Sigma-Aldrich | GE28-9564 | |
| Typhoon™ FLA 7000 Biomolecular Imager | GE Healthcare | 28-9610-73 AB | |
| Beckman Coulter LS6500 Liquid Scintillation Counter | GMI | 8043-30-1194 | |
| C1000 Touch Thermal Cycler | ThermoFisher Scientific | ||
| QuantStudio 6 Flex Real-Time PCR Systems | ThermoFisher Scientific |
참고문헌
- Zhuang, Y., Weiner, A. M. A compensatory base change in U1 snRNA suppresses a 5' splice site mutation. Cell. 46 (6), 827-835 (1986).
- Scotti, M. M., Swanson, M. S. RNA mis-splicing in disease. Nature Review Genetics. 17 (1), 19-32 (2016).
- Ward, A. J., Cooper, T. A. The pathobiology of splicing. Journal of Pathology. 220 (2), 152-163 (2010).
- Scalet, D., et al. Disease-causing variants of the conserved +2T of 5' splice sites can be rescued by engineered U1snRNAs. Human Mutatation. 40 (1), 48-52 (2019).
- Yamazaki, N., et al. Use of modified U1 small nuclear RNA for rescue from exon 7 skipping caused by 5'-splice site mutation of human cathepsin A gene. Gene. 677, 41-48 (2018).
- Yanaizu, M., Sakai, K., Tosaki, Y., Kino, Y., Satoh, J. I. Small nuclear RNA-mediated modulation of splicing reveals a therapeutic strategy for a TREM2 mutation and its post-transcriptional regulation. Science Reports. 8 (1), 6937(2018).
- Balestra, D., et al. Splicing mutations impairing CDKL5 expression and activity can be efficiently rescued by U1snRNA-based therapy. International Journal of Molecular Sciences. 20 (17), 20174130(2019).
- Donadon, I., et al. Exon-specific U1 snRNAs improve ELP1 exon 20 definition and rescue ELP1 protein expression in a familial dysautonomia mouse model. Human Molecular Genetics. 27 (14), 2466-2476 (2018).
- Desjardins, P., Conklin, D. NanoDrop microvolume quantitation of nucleic acids. Journal of Visualized Experiments. (45), e2565(2010).
- Summer, H., Gramer, R., Droge, P. Denaturing urea polyacrylamide gel electrophoresis (Urea PAGE). Journal of Visualized Experiments. (32), e1485(2009).
- Dominski, Z., Kole, R. Selection of splice sites in pre-mRNAs with short internal exons. Molecular Cell Biology. 11 (12), 6075-6083 (1991).
- Amir-Ahmady, B., Boutz, P. L., Markovtsov, V., Phillips, M. L., Black, D. L. Exon repression by polypyrimidine tract binding protein. RNA. 11 (5), 699-716 (2005).
- Le Guedard-Mereuze, S., et al. Sequence contexts that determine the pathogenicity of base substitutions at position +3 of donor splice-sites. Human Mutation. 30 (9), 1329-1339 (2009).
- Sharma, S., Wongpalee, S. P., Vashisht, A., Wohlschlegel, J. A., Black, D. L. Stem-loop 4 of U1 snRNA is essential for splicing and interacts with the U2 snRNP-specific SF3A1 protein during spliceosome assembly. Genes and Development. 28 (22), 2518-2531 (2014).
- Steitz, J. A., et al. Functions of the abundant U-snRNPs. Structure and function of major and minor small nuclear ribonucleoprotein particles. , Springer Berlin Heidelberg. Berlin, Heidelberg. 115-154 (1988).
- Fortes, P., et al. Inhibiting expression of specific genes in mammalian cells with 5' end-mutated U1 small nuclear RNAs targeted to terminal exons of pre-mRNA. Proceedings of the National Academy of Sciences U.S.A. 100 (14), 8264-8269 (2003).
- Roca, X., et al. Widespread recognition of 5' splice sites by noncanonical base-pairing to U1 snRNA involving bulged nucleotides. Genes and Development. 26 (10), 1098-1109 (2012).
- Roca, X., Krainer, A. R. Recognition of atypical 5' splice sites by shifted base-pairing to U1 snRNA. Nature Structural Molecular Biology. 16 (2), 176-182 (2009).
- Taladriz-Sender, A., Campbell, E., Burley, G. A. Splice-switching small molecules: A new therapeutic approach to modulate gene expression. Methods. 167, 134-142 (2019).
- Hamid, F. M., Makeyev, E. V. A mechanism underlying position-specific regulation of alternative splicing. Nucleic Acids Research. 45 (21), 12455-12468 (2017).
- Martelly, W., et al. Synergistic roles for human U1 snRNA stem-loops in pre-mRNA splicing. RNA Biology. , 1-18 (2021).
Access restricted. Please log in or start a trial to view this content.
재인쇄 및 허가
JoVE'article의 텍스트 или 그림을 다시 사용하시려면 허가 살펴보기
허가 살펴보기This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. 판권 소유